Чем обусловлен аллергический синдром при стрептококковом тонзиллите

С.Я. КОСЯКОВ, д.м.н., профессор, И.Б. АНГОТОЕВА, к.м.н., А.А. МУЛДАШЕВА, Кафедра оториноларингологии Российской медицинской академии последипломного образования Минздрава России
Проблема хронического тонзиллита (ХТ) остается нерешенной. Отечественные классификации ХТ не идеальны и имеют ряд существенных недостатков. Отсутствуют объективные критерии диагностики XT. Простая форма хронического тонзиллита базируется на субъективных признаках не поддающихся цифровой оценке, что приводит к ошибочным диагнозам и соответственно неэффективности проводимого лечения. Открытым остается и вопрос о целесообразности удаления небных миндалин.
Актуальность проблемы ОТФ обусловлена его широким распространением, в основном стрептококковый тонзиллит выявляется у детей в возрасте 5--15 лет. Дети до двух лет чаще страдают ОТФ вирусной этиологии. В исследовании, проведенном в европейских странах, указывается, что средняя распространенность носительства Streptococcus pyogenes среди школьников составила 15,9% [1, 2]. Однако, по данным А.С. Лопатина, отсутствует точная информация о распространенности ОТФ, в том числе в России [3].
ОТФ опасен возникновением осложнений [4], которые могут привести не только к инвалидности пациента, но и к летальному исходу. Самым частым осложнением является паратонзиллярный абсцесс (ПТА). Заболеваемость ПТА увеличивается в детстве, достигая максимума у подростков, а затем постепенно снижается с возрастом [5].
По мнению зарубежных экспертов, острый тонзиллофарингит определяется, как воспаление небных миндалин и слизистой оболочки глотки [6]. Однако американские эксперты настаивают на том, что каждый эпизод ОТФ должен быть фиксирован врачом, т. к. затем определяются показания для тонзиллоэктомии. Сообщения со слов пациента о рецидивирующей инфекции в ротоглотке могут быть ненадежными. Американская классификация по J. Byron (2001) [7] звучит следующим образом:
- острый тонзиллофарингит;
- рецидивирующий тонзиллит -- от 4 до 7 эпизодов острого тонзиллита в год;
- хронический тонзиллит;
- обструктивная гиперплазия небных миндалин.
В этой классификации использованы критерии Centor R.M. [8] для определения эпизода ОТФ бактериальной этиологии, т. к. клинически очень трудно различить ОТФ вирусной природы и бактериальной природы. Главный симптом -- боль в горле -- будет присутствовать в обоих случаях. К критериям Centor R.M. относятся:
- фебрильная лихорадка;
- налет или экссудат в нёбных миндалинах;
- болезненность передних шейных лимфатических узлов;
- отсутствие насморка и кашля.
Насморк и кашель косвенно является признаком ОТФ вирусной природы. Если у пациента врач регистрирует 2 и более из вышеперечисленных признаков, то, вероятнее всего, он имеет дело с бактериальным ОТФ. На наш взгляд, этой классификацией удобно пользоваться в ежедневной практике лор-врача.
Причинами острого тонзиллофарингита в 90% случаев являются разного рода вирусы: Adenoviridae, Coxsackievirus, Human respiratory syncytial virus, Epstein-Barr virus [6, 9]. Среди бактерий, как причины ОТФ, на первом месте находится S. pyogenes, или ß-гемолитический стрептококк (БГСА) [6, 10]. Микробиология рецидивирующего тонзиллита у детей и взрослых разная. У взрослых выявляют представителей видов Prevotella, Porphyromonas и Вacteroides fragilis, а также бактерии, которые продуцируют бета-лактамазы [11]. У детей при рецидивирующем ОТФ чаще высевается Streptococcus pyogenes. Описаны случаи носительства S. pyogenes, когда микроорганизм персистирует в организме человека, но клиники ОТФ не вызывает. У носителей Streptococcus pyogenes повышены показатели антистрептолизина О (АСЛО), поэтому его повышение не является показателем ОТФ.
Кроме оценки клинических данных для диагностики ОТФ, зарубежные авторы предлагают широко использовать стрептатест для быстрого определения наличия Streptococcus pyogenes в ротовой полости. Чувствительность метода составляет 95--100%, а специфичность разные авторы указывают от 60 до 95% [13]. Проведение стрептатеста не входит в национальные российские стандарты диагностики ОТФ [14].
Для достоверной диагностики бактериального ОТФ используется бактериальный посев с нёбных миндалин. Чувствительность этого метода достигает 90%, специфичность 95--99%, однако минусом исследования является длительность получения результатов (около 7--10 дней) [13]. Проведение стрептатеста не исключает бактериального исследования мазка с нёбных миндалин.
Европейские и американские эксперты не рекомендуют опираться на результаты, полученные при проведении общего анализа крови из-за неспецифичности показателей. Однако при этом простом исследовании возможно заподозрить инфекционный мононуклеоз. Стоит отметить, что исследование крови на наличие иммуноглобулинов к Epstein-Barr virus при ОТФ имеет значение только для Ig M, который является маркером острой фазы инфекционного мононуклеоза [15].
Зарубежные эксперты отмечают неспецифичность таких показателей крови, как антистрептолизин О, ревматоидный фактор и С-реактивный белок (ревматоидные пробы), которые используются в России. Их неспецифичность обусловлена повышенными результатами у большой группы населения, являющейся носителями Streptococcus pyogenes, т. е. в их организме этот микроорганизм персистирует, но не вызывает клиники ОТФ [16]. Повышение показателей ревматоидного фактора и С-реактивного белка возможно при наличии системных заболеваний, таких как ревматоидный артрит и др. Однако их использование может быть обоснованным при наличии у пациента клинических критериев Centor G.M.
Для назначения системных антибиотиков при ОТФ необходимо, чтобы у пациента отмечалось наличие двух или трех критериев Centor R.M. В Канаде при назначении системной антибиотикотерапии пользуются шкалой MacIsaac W.J. [17], которая помимо критериев Centor R.M. предлагает учитывать возраст пациента, т. к. стрептококковый ОТФ чаще поражает группу пациентов до 15 лет [18].
- три эпизода ежегодно в течение трех лет; пять эпизодов ежегодно в течение двух лет; семь эпизодов ОТФ в год. Каждый эпизод тонзиллофарингита должен быть четко задокументирован врачом с указанием критериев Centor R. M.;
- первый эпизод паратонзиллярного абсцесса (ПТА) с предшествующими ему тремя эпизодами острого тонзиллита в предыдущем году, значительная обструкция верхних дыхательных путей при лечении первого эпизода ПТА, повторный ПТА;
- обструкция дыхательных путей в связи с острой инфекцией из-за увеличенных нёбных миндалин.
По поводу ХТ в российских и зарубежных классификациях также существуют разногласия. Б.С. Преображенский дал следующее определение хронического тонзиллита -- это стойкое хроническое воспаление нёбных миндалин, характеризующееся у подавляющего большинства больных рецидивирующими обострениями в виде ангин и общей токсико-аллергической реакции [12]. Но что имел в виду Б.С. Преображенский в этом определении ХТ под понятием стойкое воспаление нёбных миндалин? Если имелась в виду ангина, то к ангине трудно применить понятие стойкое воспаление. Ангина, как правило, разрешается за 1 неделю. Возможно, Б.С. Преображенский понимал под ХТ повторяющиеся ангины и возникающие за ними последствия для организма. В.Т. Пальчун указывает, что при ХТ нёбные миндалины являются очагом инфекции, а организм человека, в свою очередь, начинает воспринимать процесс, происходящий в нёбных миндалинах, как чужеродный, и запускает аутоиммунные процессы [20]. Однако показатели системного иммунитета, как правило, изменяются не существенно и носят транзиторный характер. [15,21]. Специфичных показателей для доказательств аутоиммунного характера воспаления при ХТ пока не выявлено, а значит, не доказана полностью теория аутоиммунного воспаления.
Европейское общество оториноларингологов определяет хронический тонзиллит как наличие инфекции (именно инфекции) и/или воспаления в ротоглотке или в миндалинах не меньше трех месяцев. Причем европейские эксперты настаивают на том, что диагноз ХТ устанавливается только на клинических данных. Косвенным признаком наличия ХТ может служить то, что боли в горле проходят во время приема системных антибиотиков, но после их отмены симптомы возвращаются [19].
Данные по распространенности ХТ в России резко отличаются в зависимости от времени проведения исследования, а также от региона исследования. Большинство авторов чаще цитируют других, либо приводят статистические данные только одного лечебного учреждения за 1--3 года работы [22, 23]. Таким образом, мы не располагаем достоверными данными по распространенности хронического тонзиллита у детей и взрослых в России.
Актуальность проблемы ХТ обоснована противоречивостью мнений по поводу диагностики и тактики лечения данных заболеваний. Достаточно вспомнить, что длительное время в России параллельно существуют две классификации тонзиллярной проблемы (Б.С. Преображенского -- В.Т. Пальчуна (1965 г.) и И.Б. Солдатова (1975 г.)), сформулированные несколько десятков лет назад. Устоявшиеся клинические критерии диагностики создавались в период описательной медицины, а с приходом доказательной медицины не изменились. Например, признаки, на которых основывается диагноз простой формы ХТ, являются субъективными и зависят в большой степени от индивидуального восприятия врача.
Классификация Б.С. Преображенского и В.Т. Пальчуна более популярна. По Б.С. Преображенскому, ХТ имеет две клинические формы -- простую и токсико-аллергическую (ТАФ), в которой различают две степени выраженности интоксикации. Однако включение термина аллергический представляется не совсем обоснованным [12], т. к. аллергическое воспаление -- это повышенная чувствительность человеческого организма, вызванное воздействием антигенов, проявляющееся IgE -- опосредованным воспалением. Каждая форма ХТ, по Б.С. Преображенскому, имеет свои характеристики и определяет лечебную тактику, но критерии, по которым врачу необходимо определить форму ХТ, очень субъективны. Например, автор классификации не определяет, какое количество ангин за 1 год можно считать за понятие частые ангины, и не указывает, что эпизод ангины должен фиксироваться врачом. Токсико-аллергическая форма разделена на 1-е и 2-е степени (ТАФ 1 и ТАФ 2). При описании критериев, характерных для ТАФ 1, авторы не указали, какие именно функциональные нарушения со стороны сердечно-сосудистой системы и какие именно лабораторные показания носят транзиторный характер (т. е. критерии субъективны). Также не установлены временные рамки транзиторности этих нарушений. По большому счету разработчики классификации считают, что эпизоды ангины являются причинами изменений нёбных миндалин, что ведет к развитию ХТ. Однако существует большая группа пациентов с диагнозом простая форма ХТ, у которых в анамнезе не было установлено ни одной ангины.
Американские оториноларингологи выделяют ХТ по следующим клиническим признакам: постоянная боль в горле, неприятный запах изо рта, пробки, перитонзиллярная эритема, шейный лимфаденит [7].
В последнем американском руководстве по ХТ указываются следующие причины хронического воспаления миндалин [19]:
- вирусы (например, Epstein-Barr virus);
- бактерии;
- гастроэзофагеальная рефлюксная болезнь;
- аллергия;
- астма.
По данным зарубежных авторов, в нёбных миндалинах при ХТ у взрослого населения выявляется полимикробный бактериальный состав с Streptococcus haemolyticus alfa- и beta, Staphylococcus aureus, Haemophilus influenzae, Вacteroides. Haemophilus influenzae выявляется чаще всего при гипертрофии нёбных миндалин и аденоидов [5]. В 2007 г. A. Swidsinski и соавт. установили, что у пациентов с аденотонзиллярной патологией могут выявляться множественные признаки очаговой гнойной инфекции в аденоидной ткани или в ткани нёбных миндалин в виде микроабсцессов, нарушение целостности поверхности миндалин в виде микротрещин. В гнойном очаге могут определяться как патогенные и условно-патогенные, так и комменсальные микроорганизмы, которые могут быть защищены либо воспалительными инфильтратами или лимфатической тканью, окружающей их, или бактерии могут быть включены в макрофаги и, таким образом, не доступны для стандартного микробиологического изучения. Авторы предполагают, что хронический аденотонзиллит может быть скорее следствием инфекций, вызванных участием нескольких патогенных, условно-патогенных и комменсальных микроорганизмов [25].
Зарубежные публикации подчеркивают, что в нёбных миндалинах находится нормальная микрофлора, представленная альфа-гемолитическими стрептококками, гамма-гемолитическими стрептококками, анаэробными микроорганизмами, которые не требуют лечения и не вызывают клиники ни ХТ, ни ОТФ [26]. В настоящее время рассматривается вопрос о влиянии биопленок на течение хронического инфекционного процесса в аденотонзиллярной ткани. Так, в 2007 году в Италии J. Galli и соавт. обнаружили в образцах аденоидной ткани и в образцах тканей нёбных миндалин у детей с хронической аднотонзиллярной патологией прикрепленные к поверхности ткани кокки, организованные в биопленки. Авторы исследования предполагают, что обнаруженные бактериальные биопленки на поверхности небных миндалинах и аденоидной ткани, могут помочь объяснить трудности эрадикации бактерий, принимающих участие в этих хронических инфекционных процессах [27]. Доказано, что при рецидивирующем и хроническом тонзиллите бактериальные возбудители заболевания могут располагаться внутри клеток, что делает консервативное лечение не всегда эффективным. Для обнаружения и идентификации внутриклеточно расположенных микроорганизмов могут применяться полимеразная цепная реакция (ПЦР), гибридизация in situ (FISH-метод). Так, доказано внутриклеточное расположение Staphylococcus aureus [28], Streptococcus pneumonia, Haemophilus influenzae и Moraxella catarrhalis [29], Streptococcus pyogenes [30]. В настоящее время не существует доступного и достоверного метода исследования присутствия микроорганизмов в тканях нёбных миндалин. Во всех проведенных исследованиях не удалось выявить один патогенный микроорганизм, который бы вызывал клинику ХТ. Возможно, что клинику ХТ может вызвать любой микроорганизм, в том числе и условно-патогенный, находящийся в ротоглотке при определенных условиях, которые способствуют воспалению в ткани нёбных миндалин. Одним из этих условий может оказаться ларингофарингеальный рефлюкс.
За рубежом и в России диагноз ХТ устанавливается только клинически. Но в США при вышеперечисленных клинических признаках проводят исследования для исключения астмы, гастроэзофагеальной рефлюксной болезни, аллергии. Ревмопробы и исследования иммунологического статуса не проводятся.
В России принято консервативное и хирургическое лечение ХТ. К консервативному лечению ХТ относят промывания лакун миндалин, системную антибиотикотерапию, введение системных антибиотиков и пробиотиков в строму небных миндалин, физиотерапевтическое лечение, которые не имеют доказательных данных по эффективности их применения, полученных в результате рандомизированных плацебо-контролируемых исследований.
Существуют доказательства о неэффективности системной антибиотикотерапии при ХТ. В исследовании, которое было основано на изучении бактериологического состава с поверхности небных миндалин у 30 детей, перенесших их удаление, выявили, что антибиотики, предписанные за 6 месяцев до операции, не изменяют бактериологию миндалин к моменту тонзиллэктомии [31].
Иностранные публикации в основном содержат информацию по хирургическому лечению ХТ, которое проводится только строго по показаниям [19]:
- подозрение на злокачественный процесс небных миндалин;
- случаи синдрома обструктивного апноэ сна;
- очень редко проводят тонзиллэктомию при упорном неприятном запахе изо рта из-за пробок в лакунах миндалин.
Не является показанием для удаления небных миндалин носительство Streptococcus pyogenes, которое наблюдается при повышенных показателях АСЛО, но без клиники ОТФ [20].
В России большинство врачей ориентируются на показания, описанные у В.Т. Пальчуна. К ним относятся:
• простая форма ХТ и токсико-аллергическая форма ХТ 1-й степени при отсутствии эффекта от 2 курсов консервативного (медикаментозного и физиотерапевтического) лечения;
• ХТ токсико-аллергическая форма 2-й степени;
• ХТ с осложнениями, тонзиллогенный сепсис [32].
Эффективность тонзиллэктомии многие годы обсуждается в отечественной и зарубежной литературе, сравниваются методы удаления нёбных миндалин, и этому посвящено несколько обзоров Кохрейна, установившие отсутствие точных данных о преимуществе какой-либо из методов тонзиллэктомии [33].
По данным последних нескольких лет, количество тонзиллоэктомий у взрослых в США снизилось [20]. Снижение показателей тонзиллэктомии, возможно, связано с полученными новыми данными о роли нёбных миндалин в организме. При удалении небных миндалин нарушается выработка секреторного иммуноглобулина А, необходимого для иммунологической защиты верхних дыхательных путей [20]. Кроме того, при изучении последствий тонзиллэктомий было обнаружено, что женщины, перенесшие двухстороннюю тонзиллэктомию в детстве, чаще страдают раком молочной железы в постменопаузальном периоде, чем те женщины, которым удалось сохранить нёбные миндалины [34].
В связи с полученной новой информацией назрела необходимость пересмотра отечественных классификаций, показаний для тонзиллэктомии, а также, возможно, пересмотра определения хронического тонзиллита.
-Источник: Медицинский совет, № 3, 2015
Тябут Тамара Дмитриевна, профессор кафедры кардиологии и ревматологии Бел МАПО, доктор медицинских наук
Год здоровья. Прочитай и передай другому
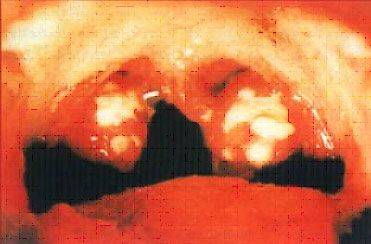
Тонзиллит, вызванный бета-гемолитическим стрептококком.
При наличии хронического тонзиллита в лакунах скапливается большое количество гноя, состоящего из погибших микробов, белых кровяных телец - лейкоцитов, других клеток (гнойно-казеозные пробки). В гнойном содержимом лакун размножаются болезнетворные микробы. Продукты жизнедеятельности микробов из миндалин попадают в кровь и приводят к развитию тонзиллогенной интоксикация, проявляющейся утомляемостью, болями в мышцах и суставах, головными болями, снижением настроения, субфебрилитетом. Миндалины превращаются в хранилище инфекционных агентов, откуда они могут распространяться по организму и быть причиной воспалительных процессов. Частые болезни еще более ослабляют иммунитет, что приводит к дальнейшему развитию тонзиллита. Так формируется порочный круг заболевания.
Хронический тонзиллит опасен осложнениями, связанными с распространением инфекции по организму. К ним относятся паратонзиллярные абсцессы, ·поражение сердца (тонзилогенная миокардиодистрофия, острая ревматическая лихорадка), сосудов, почек.
Тонзиллогенная миокардиодистрофия относится к часто развивающимся, но гораздо реже диагностируемым поражениям сердечной мышцы при хроническим тонзиллите. Она вызывается токсинами бактерий, находящихся в миндалинах, и продуктами местного воспаления и распада тканей.
Клинические признаки тонзиллогенной дистрофии миокарда обусловлены нарушением деятельности вегетативной нервной системы (вегетативной дисфункцией) и нарушением различных видов обмена в сердечной мышце (электролитного, белкового), следствием которых является нарушение образования энергии в сердечной мышце. На ранних этапах развития тонзилогенная миокардиодистрофия проявляется высокой частотой сердечных сокращений - тахикардией, перебоями в работе сердца - экстрасистолией, одышкой при интенсивных физических нагрузках, нарушением общего самочувствия больных. При поздней диагностике появляются признаки сердечной недостаточности, уменьшается объем нагрузки, вызывающей одышку, появляются более тяжелые нарушения ритма и проводимости. При своевременной диагностике и лечении внесердечного фактора - хронического тонзиллита, вызвавшего перечисленные изменения в сердечной мышце, они обратимы и постепенно структура и функции сердечной мышцы
восстанавливаются.
Наибольшую опасность для прогноза и качества жизни пациентов представляет поражение сердца при острой ревматической лихорадке.
Острая ревматическая лихорадка (ОРЛ) - постинфекционное осложнение тонзиллита (ангины) или фарингита, вызванных бета - гемолитическим стрептококком группы А, в виде системного воспалительного заболевания соединительной ткани с преимущественной локализацией патологического процесса в сердечно-сосудистой системе (кардит), суставах (мигрирующий полиартрит), мозге (хорея) и коже (кольцевидная эритема, ревматические узелки), развивающегося у предрасположенных лиц, главным образом молодого возраста (7-15 лет). В Российской Федерации и в РБ заболеваемость ревматической лихорадкой составляет от 0,2 до 0,6 случаев на 1000 детского населения. Первичная заболеваемость ОРЛ в России в начале ХХI века составила 0,027 случая на 1000 населения. Частота впервые выявленной хронической ревматической болезни сердца (ХРБС), которая включает пороки сердца и специфические изменения клапанов (краевой фиброз), выявляемые при ультразвуковом исследовании сердца - 0,097случаев на 1000 населения, в том числе ревматических пороков сердца - 0,076 случаев на 1000 взрослого населения. Имеющиеся статистические различия между частотой первичной заболеваемости острой ревматической лихорадкой и хронической ревматической болезнью сердца свидетельствует о наличии большого количества не диагностированных острых форм болезни.
Временной интервал между перенесенным острым стрептококковым тонзиллитом, фарингитом, обострением хронического тонзиллита и возникновением проявлений острой ревматической лихорадки составляет 3-4 недели. При острой ревматической лихорадке могут поражаться все структуры сердца - эндокард, миокард, перикард. Поражение миокарда (мышцы сердца) встречается всегда. Проявлениями поражения сердца могут быть сердцебиение, одышка, связанная с физической нагрузкой или в покое, боли в области сердца ноющего характера, которые в отличие о стенокардии не имеют четкой связи с физической нагрузкой и могут сохраняться длительный период времени, сердцебиение, перебои в работе сердца, приступообразные нарушения ритма - мерцательная аритмия, трепетание предсердий. Обычно поражение сердца сочетается с суставным синдромом по типу артралгий - болей в крупных суставах (коленных, плечевых, голеностопных, локтевых) или артрита (воспаления) этих же суставов. Для воспаления суставов характерны боль, изменения формы сустава, вызванные отеком, покраснение кожи в области пораженного сустава, местное повышение температуры и нарушение функции сустава в виде ограничения объема движений. Мелкие суставы поражаются гораздо реже. Воспалительный процесс в суставах носит мигрирующий характер и быстро проходит на фоне правильного лечения. Поражение сердца и суставов обычно сопровождается повышением температуры тела, слабостью потливостью, нарушением трудоспособности. У части пациентов встречаются поражения нервной системы, кожные сыпи по типу кольцевидной эритемы и подкожные ревматические узелки.
Для постановки диагноза острой ревматической лихорадки существуют диагностические критерии, которые включают клинические, лабораторные и инструментальные данные, а также информацию о перенесенной инфекции, вызванной бета-гемолитическим стрептококком группы А, его ревматогенными штаммами. Своевременно поставленный диагноз позволяет добиться выздоровления больного при проведении терапии антибиотиками, глюкокортикоидными гормонами, нестероидным противовоспалительными препаратами. Однако, при поздно начатом лечении, несоблюдении пациентами двигательного режима, наличии генетической предрасположенности, не санированной очаговой инфекции (декомпенсированный тонзиллит, кариес) исходом острой ревматической лихорадки может быть хроническая ревматическая болезнь сердца с пороком сердца или без него. Порок сердца возникает как исход воспалительного поражения клапанов сердца. Наличие порока сердца ревматической этиологии требует отнесения пациента к группе высокого риска развития инфекционного эндокардита, наиболее тяжелой формы поражения сердца, связанного с инфекционными агентами.
Острая ревматическая лихорадка относится к заболевания, при которых профилактика имеет важное значение для снижения как первичной заболеваемости, так и повторных эпизодов болезни (повторная острая ревматическая лихорадка).
Первичная профилактика имеет своей целью снижение первичной заболеваемости и включает комплекс медико-санитарных и гигиенических мероприятий, а так же адекватное лечение инфекций, вызванных бета-гемолитическим стрептококком группы А. Первое направление включает мероприятия по закаливанию, знакомство с гигиеническими навыками, санацию хронических очагов инфекции, в первую очередь - хронического тонзиллита и кариеса. Миндалины тщательно санируют повторными полосканиями и промываниями растворами антибактериальных средств, вакуум-аспирацией патологического содержимого лакун. Если это не дает желаемого результата обсуждается вопрос хирургического лечения - удаления миндалин. В каждом конкретном случае выбор тактики лечения определяет врач отоларинголог и терапевт, кардиолог или ревматолог.
Адекватное лечение ангины и фарингита направлено на подавление роста и размножения стрептококка в организме при развитии стрептококкового фарингита, ангины, тонзиллита. Основу лечения составляет антибиотикотерапия в сочетании с противовоспалительными средствами, которые должны проводиться не менее 10 дней с обязательным контролем общего анализа крови, мочи, а по показаниям биохимического анализа крови при возникновении признаков болезни, при окончании лечения и через месяц от появления первых признаков болезни. Лабораторное исследование, проведенное в эти сроки, позволяет правильно поставить диагноз, определить эффективность лечения, и что самое главное, не пропустить начало развития осложнения в виде острой ревматической лихорадки.
Вторичная профилактика имеет своей целью предупреждение развития повторной острой ревматической лихорадки и прогрессирования заболевания у лиц, перенесших ОРЛ. Она проводится у пациентов, не имеющих аллергии к препаратам пенициллинового ряда. Лекарственным средством, используемым для профилактики у взрослых является бензатинбензилпенициллин (экстенциллин, ретарпен) в дозе 2 400 000 ЕД 1 раз в 3 недели внутримышечно. Профилактические режимы зависят от возраста пациента и исхода острой ревматической лихорадки. В соответствии с рекомендациями Ассоциации ревматологов России вторичная профилактика включает следующие режимы:
Наиболее тяжелым и прогностически неблагоприятным заболеванием сердца, связанным с инфекцией считается инфекционный эндокардит - заболевание, характеризующееся развитием воспалительного процесса на клапанном или пристеночном эндокарде, включающее поражение крупных внутригрудных сосудов, отходящих от сердца, возникающее вследствие воздействия микробной инфекции. Наиболее часто это различные бактерии- стрептококки, стафилококки, энтерококки, кишечная палочка, синегнойная палочка и многие другие. Описано 119 различных возбудителей, приводящих к развитию заболевания.
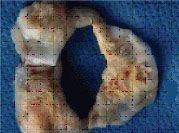
Аортальный клапан
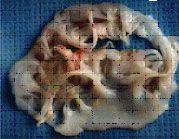
Митральный клапан
Так выглядят клапаны сердца при развитии инфекционного эндокардита.
Наложения из микробов, клеток крови нарушают их функцию,
разрушают клапан и зачастую требуют экстренного хирургического лечения.
Распространенность инфекционного эндокардита в начале 21 века составляла 2- 4 случая на 100 000 населения в год. Отмечается повсеместный рост заболеваемости, наиболее выраженный в старших возрастных группах и составляющий 14, 5 случая на 100 000 населения в возрасте 70-80 лет. Диагностика заболевания сложна. При первом обращении к врачу диагноз ставится только у 19 - 34,2% больных. Средний срок от первичного обращения до постановки диагноза составляет не менее 1,5 - 2 месяцев.
Выделяют группу больных с высоким риском развития инфекционного эндокардита, в которую входят:
- пациенты с ранее перенесенным инфекционным эндокардитом,
- пациенты с протезированными клапанами сердца,
- пациенты с синими врожденными пороками,
- пациенты после хирургических операций на аорте, легочных сосудах
- пациенты с приобретенными пороками сердца, в первую очередь ревматической этиологии (ХРБС).
Кроме этого выделена группа умеренного (промежуточного) риска, объединяющая пациентов со следующими заболеваниями:
- Пролапс митрального клапана, обусловленный миксоматозной дегенерацией или другими причинами с регургитацией 2-3 степени или пролапсы нескольких клапанов
- Нецианотичные врожденные пороки сердца (исключая вторичный ДМПП)
- Бикуспидальный (двухстворчатый)аортальный клапан
- Гипертрофическая кардиомиопатия (идиопатический гипертрофический субаортальный стеноз).
Установлено, что для развития инфекционного эндокардита необходимо попадание возбудителя в кровь. Наиболее частой причиной этого могут быть стоматологические манипуляции, сопровождающиеся повреждением десны и кровоточивостью. При наличии кариеса или заболеваний десен, бактериемия (наличие возбудителя в крови) может возникать достаточно часто.
Воспаление слизистой оболочки глотки, нередко также миндалин (тонзиллит), вызванное инфекцией или раздражением.
1. Этиологический фактор: в зависимости от возраста — у взрослых чаще всего вирусы (90–95 %; ОРВИ →разд. 18.1.2), реже бактерии (5–10 %). В большинстве случаев у детей встречается бактериальное воспаление, вызванное Streptococcus pyogenes (β-гемолитический стрептококк группы А — БГСА), у взрослых часто также Eusobacterium necrophorum ; реже стрептококки группы С и G.
2. Резервуар и пути заражения: резервуаром и источником инфекции БГСА (и большинства других этиологических факторов) является больной человек (редко бессимптомный носитель), заражение происходит воздушно-капельным путем или при непосредственном контакте (в том числе с выделениями верхних дыхательных путей). Часто встречается бессимптомное носительство БГСА.
3. Эпидемиология: наибольшая заболеваемость поздней осенью, зимой и ранней весной. Факторы риска (в зависимости от этиологии):
1) контакт с больным инфекционным фарингитом или с бессимптомным носителем (в том числе, родители детей школьного возраста или лица, контактирующие с такими детьми) — БГСА;
2) возраст — 5–15 лет — БГСА, дети и молодежь — инфекционный мононуклеоз (вирус Эпштейна-Барр); взрослые — F. necrophorum ;
3) оральный секс — N. gonorrhoeae ;
4) ослабленный иммунитет.
4. Инкубационный и заразный период:
1) вирусное воспаление — инкубационный период 1–6 дней; заразный период 1–2 дня перед возникновением симптомов до 3 недель после (в зависимости от этиологии). Заражение возникает у ≈2/3 лиц, находящихся в бытовом контакте с больным.
2) стрептококковое воспаление (БГСА) — инкубационный период от 12 ч до 4 дней; заразный период — 24 ч от момента начала эффективной антибиотикотерапии или ≈7 дней после исчезновения симптомов, если антибиотик не был использован. Риск передачи инфекции домочадцам ≈25 %.
3) воспаление, вызванное F. necrophorum — инкубационный период неизвестен.
В зависимости от этиологического фактора. наверх
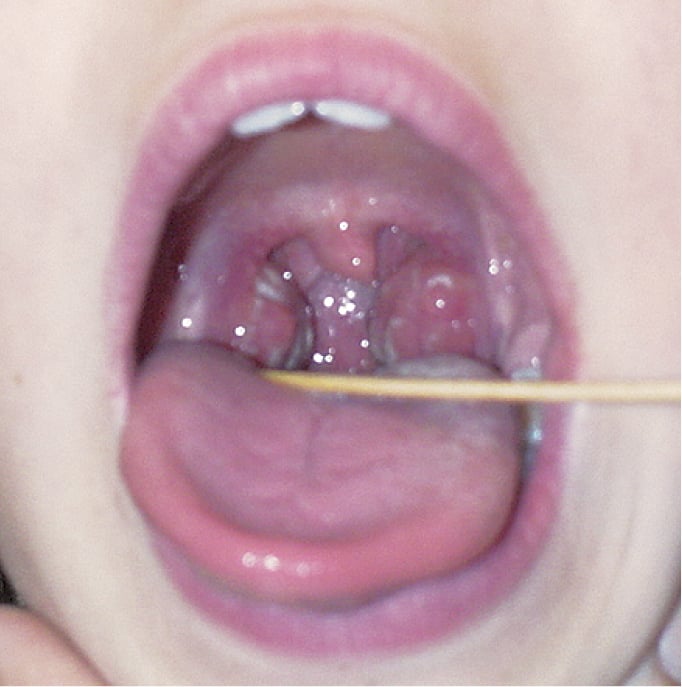
Рисунок 3.3-1. Стрептококковая ангина
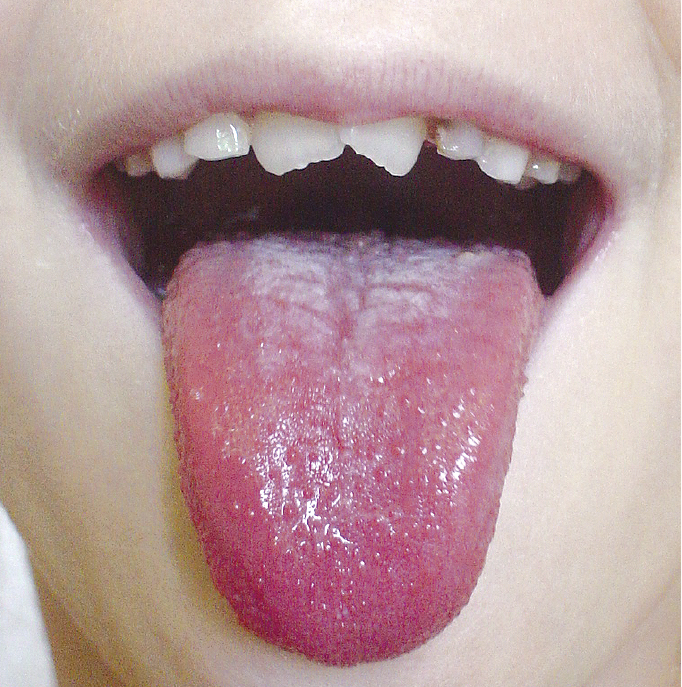
Рисунок 3.3-2. Малиновый язык
2. Воспаления, вызванные другими бактериями:
1) Arcanobacterium haemolyticum — у подростков и в молодом возрасте, следует учитывать при неэффективности ß-лактамных антибиотиков; симптомы схожи с таковыми при инфицировании БГСА. Часто имеет место скарлатиноподобная экзантема, после которой отсутствует шелушение эпидермиса.
2) F. necrophorum — чаще всего острый фарингит, часто длительный и рецидивирующий; симптомы, сходные с таковыми при инфекции БГСА. Особым видом является так наз. ангина Симановского-Плаута-Винсана (сопутствующее инфицирование спирохетами) — обычно односторонние налеты на верхнем полюсе миндалины, под налетами расположена язва; интенсивная односторонняя боль в горле.
3. Вирусное воспаление: боль в горле (обычно не очень сильная), головная боль, мышечные и суставные боли; субфебрильная лихорадка или нормальная температура тела, фарингит, конъюнктивит (аденовирус), ринит, кашель, охриплость; иногда отмечается выраженное изъязвление слизистой оболочки полости рта (энтеровирусы, ВПГ-1) или диарея; генерализованная лимфаденопатия и спленомегалия могут указывать на инфекционный мононуклеоз →разд. 18.1.9. При воспалении, вызванном ВПГ-1, — болезненное увеличение лимфатических узлов переднего треугольника шеи.
4. Естественное течение: большинство фарингитов (в том числе бактериальных) проходит самостоятельно — вирусное воспаление в течение 3–7 дней, вызванное БГСА в течение 3–4 дней (даже без антибиотика). При отсутствии лечения, инфекция БГСА имеет несколько более высокий риск гнойных осложнений и (очень редко у взрослых) ревматической лихорадки.
Дополнительные методы исследования наверх
1. Экспресс-тесты на наличие антигенов БГСА: материал — мазок из зева (→ниже); умеренная чувствительность, высокая специфичность, положительный результат подтверждает инфекцию, отрицательный — исключает инфекцию у взрослого пациента (у ребенка требует подтверждения посевом мазка из зева). наверх
2. Посев мазка из зева и миндалин: при подозрении на заражение БГСА (если нет возможности выполнить экспресс-тест) или при другой бактериальной инфекции ( N. gonorrhoeae, C. diphtheriae [дифтерия]). При помощи стандартного мазка невозможно выявить F. necrophorum и A. haemolyticum . Мазок берут с обеих миндалин и задней стенки глотки (не дотрагиваясь языка и щек — слюна содержит факторы, тормозящие рост БГСА) тампоном из готового комплекта с транспортной средой (агарозный гель) или обычным смоченным 0,9 % NaCl тампоном; после забора поместить его в стерильную пробирку с пробкой. Материал хранить при комнатной температуре и как можно быстрее доставить в микробиологическую лабораторию (без транспортной среды в течение 4 часов).
Выставить точный диагноз или исключить заражение БГСА на основании клинической картины невозможно. Клинические и эпидемиологические критерии полезны в выявлении пациентов, у которых вероятность наличия БГСА велика (показано сделать посев мазка из зева или экспресс-тест на наличие антигенов БГСА) или мала (нет необходимости в бактериологических исследованиях). Основное значение имеет принятие решения о необходимости лечения антибиотиком (заражение БГСА):
1) на основании клинических и эпидемиологических критериев (шкала Центора) оцените вероятность заражения БГСА и примените соответствующие меры →табл. 3.3-1. Если бактериологические исследования не доступны, а симптомы ярко выражены → назначьте антибиотик, активный в отношении БГСА. Ангина при скарлатине в 100 % обусловлена БГСА.
2) результат экспресс-теста на антигены:
а) отрицательный → примените симптоматическое лечение;
б) положительный → примените антибиотик, активный в отношении БГСА.
3) если назначен посев мазка из зева, а симптомы ангины ярко выражены → рассмотрите вопрос о назначении антибиотика до получения результата. Следует прекратить антибиотикотерапию, если результат посева отрицательный. Не следует определять чувствительности БГСА к антибиотикам (чувствительны к пенициллинам), если нет необходимости использовать макролиды (часто устойчивость).
Читайте также:


