Как определить очаг инфекции



Что такое сепсис?
Наиболее частые возбудители, которые приводят к заражению, это бактерии стафилококки, стрептококки, кишечная палочка, а также различные грибы.
Причины сепсиса у взрослых
Наиболее частая причина сепсиса – это попадание в кровь вредных микроорганизмов – бактерий, грибков и вирусов. И чем сильнее заражается организм, тем тяжелее протекает заболевание. Особенно это касается тех случаев, когда инфицирование происходит сразу несколькими видами возбудителей.
Сепсис часто может развиваться на фоне ослабленной иммунной системы. Это происходит при онкологических заболеваний, при ВИЧ, при приеме препаратов, ослабляющих иммунную систему, при лучевой терапии и других факторах.
В ряде случаев сепсис может развиваться при распространении бактерий, которые полезны для организма. Например, кишечных бактерий, которые помогают переваривать пищу. При ослабленном иммунитете эти бактерии становятся опасными. При их попадании в кровь развивается интоксикация.
Виды сепсиса у взрослых
Сепсис может развиваться на фоне различных инфекционных заболеваний. Например:
- Тяжелая ангина;
- Пневмония;
- Онкологические заболевания;
- СПИД;
- Перитонит;
- Воспаление среднего уха (отит);
- Другие тяжелые раны и инфекции.
Различают три фазы развития сепсиса:
-
Токсемия – начальная фаза заболевания, при которой возбудитель выходит из первичного очага инфекции. Сопровождается активизацией иммунной системы в ответ инфицирование;
-
Септицемия – ухудшение общего состояния пациента, в результате проникновения в кровь микроорганизмов или их токсинов;
Септикопиемия – при этой форме сепсиса вместе с общей интоксикацией в организме образуются метастатические абсцессы (гнойные очаги). Они могут находится в различных тканях и органах.
- Молниеносный сепсис с быстрым развитием септического шока и летальным исходом через 1-2 дня;
- Острый сепсис с острой воспалительной реакцией в течение 5-28 суток;
- Подострый – заболевание длится около 3-4 месяцев;
- Хронический – может продолжаться до нескольких лет.
Симптомы сепсиса у взрослых
Симптомы заболевания могут различаться в зависимости от расположения первичного очага инфекции. Однако имеются и общие симптомы, которые встречаются у всех типов заболевания. Обычно это резкое повышение температуры, жар может периодически сменяться ознобом.
Когда заболевание начинает прогрессировать, меняется внешний вид пациента, заостряются черты и меняется цвет лица, на коже появляются высыпания (гнойники). Если заболевание протекает остро у больного может развиться истощение, обезвоживание организма и пролежни. К другим симптомам сепсиса относят:
- Вялость, заторможенность сознания;
- Слабый пульс, аритмию;
- Дыхательную недостаточность;
- Чередующиеся запоры и понос;
- Нарушение мочеиспускания из-за развития токсического нефрита;
- Мутные выделения из ран.
Диагностика сепсиса у взрослых
Лечение сепсиса у взрослых
Возможен ли благополучный исход такой грозного заболевания как сепсис? Согласно статистике, около 50% случаев сепсиса заканчиваются летальным исходом. Однако вылечить заболевание все же можно, если вовремя поставить диагноз и начать лечение.
Обычно таких больных помещают в палату интенсивной терапии, где под контролем специалистов проводят антибактериальную, дезинтоксикационную, симптоматическую терапию. При необходимости поддерживают работу важных органов, назначают иммуностимулирующие средства.
Удалить очаг инфекции можно только хирургическим способом, полностью удалив гнойник. В наиболее тяжелых случаях приходится удалять целиком орган.
Для того, чтобы уничтожить возбудителя инфекции внутривенно вводят антибиотики, к которым наиболее чувствительны микроорганизмы, вызвавшие заболевание.
Длительность лечения сепсиса составляет около 2 недель. Больного можно считать выздоровевшим после полной нормализации температуры и отсутствии возбудителей в двух посевах крови.
СМОТРЕТЬ ДРУГИЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
Год утверждения 2015 год
Профессиональные ассоциации:
Союз педиатров России
Оглавление
1. Краткая информация
Лихорадка без очага инфекции (ЛБОИ) – высокая лихорадка у ребёнка до 3-х лет без катаральных явлений и симптомов, указывающих на локализацию процесса или этиологию заболевания.
Не включает больных в тяжелом состоянии с нарушениями сознания, нежеланием принимать жидкость, периферическим цианозом, гипо- или гипервентиляцией.
До 3-х лет максимальный риск скрытой бактериемии, приводящей к тяжелой бактериальной инфекции (ТБИ):
- бактериальный менингит,
- септический артрит,
- остеомиелит,
- целлюлит,
- тяжелая пневмония,
- инфекции мочевых путей.
Температурные критерии ЛБОИ:
>39˚С у детей с 3 до 36 месяцев;
>38˚С у детей до 3 месяцев при отсутствии других признаков заболевания.
Наиболее частые возбудители бактериемии:
- Streptococcus pneumoniae,
- influenzae типа b,
- meningitides,
- Salmonella spp.,
- typhi и paratyphi.
Наиболее частые вирусные инфекции:
- герпес-вирусные 1, 2, 6, 7 типов,
- энтеровирусные (ECHO),
- парвовирусные b 19,
- грипп.
До 2-х месяцев жизни частые причины ЛБОИ:
- coli,
- Klebsiella pneumoniae,
- Streptococcus haemolyticus,
- энтеробактерии,
- энтерококки.
Этиология около 20% ЛБОИ остается невыясненной.
ЛБОИ встречается в 20% случаев фебрильной лихорадки.
У вакцинированных против гемофильной палочки и пневмококка частота бактериемии и ТБИ при ЛБОИ значительно ниже.
ТБИ составляет 3,2 - 29,2% случаев ЛБОИ, в среднем 18%.
Частота бактериальных инфекций при ЛБОИ:
22% случаев у всех лихорадящих детей до 3-х месяцев,
3-8% случаев от 3 месяцев до 3 лет
Менингит при гемофильной бактериемии развивается в 12 раз чаще, чем при пневмококковой.
В структуре ЛБОИ на инфекции мочевых путей (ИМП) приходится 1/3 случаев.
У 1/3 лихорадка самопроизвольно разрешается.
А49.9 – Бактериальная инфекция неуточненная
A49.8 – Другие бактериальные инфекции неуточненной локализации
R50.0 – Лихорадка с ознобом
R50.1 – Устойчивая лихорадка
- Лихорадка без очага инфекции.
Если удается найти очаг инфекции или подтвердить вирусную этиологию лихорадки, диагноз дополняется:
- Инфекция мочевых путей
- Правосторонняя верхнедолевая пневмония
- Острая энтеровирусная инфекция и т.д.
Общепринятой классификации ЛБОИ не существует.
2. Диагностика
Опасность ЛБОИ - в отсутствии симптомов, позволяющих выявить очаг инфекции и определить этиологию для подбора терапии.
Признаки вероятной бактериемии при ЛБОИ:
- вялость,
- слабость,
- отказ от еды и жидкости,
- плаксивость и раздражительность,
- необычная бледность или гиперемия кожи,
- заостренность черт лица,
- сложность в установлении зрительного контакта с ребенком,
- выше обычного тревожность матери.
Критерии высокого риска ТБИ:
- Дети до 3 месяцев с температурой >38˚С;
- Дети 3-6 месяцев с неполной иммунизацией;
- Дети 3-6 месяцев с нарушением общего самочувствия.
Нацелено на выявление очага бактериальной инфекции или катаральных явлений.
При осмотре оценивается состояние, самочувствие, налаживается зрительный контакт с ребенком.
- Осмотр слизистой оболочки носа, глаз, полости рта для выявления катарального синдрома.
- Оценка цвета кожи и состояния тургора для выявления эксикоза, экзантемы.
- Орофарингоскопия для исключения абсцессов, тонзиллита, афтозного стоматита, гингивита.
- Отоскопия для исключения отита.
- Измерение роста и массы тела.
- Измерение температуры тела.
- Оценка состояния костно-суставной системы.
- Выявление геморрагического синдрома, гепатоспленомегалии, лимфаденопатии.
- Аускультация сердца и легких.
- Ребенок спокоен или громко плачет
- Довольный, улыбается, бодрствует, адекватно реагирует на внешние раздражители, возможно установить зрительный контакт
- Дыхание нормальное
- Нормальный цвет губ, языка и кожи
- Кожа, конъюнктивы нормальной влажности
- Влажные слизистые оболочки
- Нормальный диурез
Состояние средней степени тяжести:
- Ответ на внешние раздражители, активность
- Участие крыльев носа в дыхании
- Бледность, по мнению родителей
- Сухость слизистых оболочек
- Снижение диуреза
- Снижение аппетита
- Сонный, вялый, улыбается слабо, неактивно отвечает на обращение к нему, раздражителен
- Долго не может проснуться при попытке его разбудить или не может сам встать
- Слабый, плач на высоком тоне или продолжительный плач, или стон
- Пульсирующий большой родничок
- Практически отсутствует возможность установить зрительный контакт
- Втяжение межреберных промежутков ЧД >60/минуту
- Шумное дыхание
- Бледность, мраморность цианотичный, пепельный оттенок кожи, тахикардия,
- Наполнение капилляров ногтевого ложа >2 секунд
- Снижение тургора кожи
- Рвота желчью
- Тяжелое состояние, по мнению квалифицированного врача
- Возникновение лихорадки на фоне полного здоровья
- Нетяжелое общее состояние
- Отсутствие очага инфекции
- Неотягощенный неонатальный анамнез
- Общий анализ крови: лейкоциты 5-15 х 10 9 /л; палочкоядерные нейтрофилы 9 /л
- Общий анализ мочи: лейкоциты ≤10 в поле зрения
- Микроскопия кала (при диарее): лейкоциты
В 5% случаев ТБИ протекает с вирусной ко-инфекцией.
Выделение вируса при ПЦР не исключает наличия бактериальной инфекции.
Чем младше ребенок, тем выше риск бактериемии и ТБИ.
В 70% случаев ЛБОИ при ПЦР выделяется один и более вирусов, что не определяет их роли в развитии заболевания.
Клинический анализ крови с оценкой лейкоцитов, абс. числа нейтрофилов и палочкоядерных нейтрофилов для дифференциальной диагностики вирусной и бактериальной инфекции.
Сомнительные предикторы бактериальной инфекции, встречающиеся у 15-20% детей:
- нейтрофильный лейкоцитоз выше 15 х 10 9 /л;
- лейкоциты менее 15 х 10 9 /л + нейтрофилы больше 10 х 10 9 /л;
- палочкоядерные формы >1,5 х 10 9 /л.
Для детей до 2 лет норма лейкоцитов 15-17 х 10 9 /л.
Определение маркеров бактериальной инфекции:
- СРБ повышаться через 12 часов от начала заболевания, достигая максимума через 48-72 часа;
- Прокальцитонин (ПКТ) повышается в первые 2-6 часов от начала заболевания, достигая максимума через 24 часа, поэтому используется для мониторинга заболевания.
Обязательное бактериологическое исследование крови.
Общий анализ мочи для исключения патологии мочевыводящих путей.
Бактериологическое исследование мочи при лейкоцитурии и/или бактериурии и/или нитритов в моче.
ТБИ более вероятна при:
- лейкоцитурии >10 в поле зрения
- и/или лейкоцитоз >15 х 10 9 /л
- и/или СРБ >70 мг/л
- и/или ПКТ >2 нг/мл (наиболее надежный показатель).
Люмбальная пункция при наличии мозговых симптомов.
При диспноэ, тахипноэ, стонущем дыхании для исключения пневмонии.
Малоинформативна при отсутствии респираторных симптомов и маркеров бактериальной инфекции.
Обязательна у детей младше 3 месяцев при наличии одного или более признаков:
3. Лечение
Антибактериальная терапия при бактериальных или предположительно бактериальных формах ЛБОИ, продолжение 5-7 дней после нормализации температуры:
- при симптомах токсикоза;
- без токсикоза с лейкоцитами >15 х 10 9 /л; СРБ >70 мг/л; СРБ 2 нг/мл;
- при ухудшении состояния на фоне симптоматической терапии;
Тактика в зависимости от новых симптомов: стоматит, гингивит – введение ацикловира, сыпь – вероятна энтеровирусная инфекция.
Препараты первого выбора, парентерально:
- амоксициллин/клавуланат 90 мг/кг/сут по амоксициллину
- цефтриаксон 50-100 мг/кг/сут
Назначение пероральных антибиотиков не снижает частоту менингита.
При ЛБОИ у детей до 2-х месяцев цефалоспорины комбинируют с ампициллином в связи с высоким риском инфицирования листериями и энтерококком.
Детям в тяжелом состоянии с признаками токсикоза экстренно начинается:
Клинический эффект при бактериемии – в течение 12-24 часов от начала терапии.
При сохранении лихорадки более 48 часов от начала лечения повторно оценивается совокупность клинических симптомов и лабораторных данных для определения целесообразности продолжения антибактериального лечения или смены/добавления антибиотика.
При вирусной ЛБОИ назначается симптоматическая терапия с адекватным питьевым режимом.
Роза Исмаиловна Ягудина, д. фарм. н., проф., зав. кафедрой организации лекарственного обеспечения и фармакоэкономики и зав. лабораторией фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Евгения Евгеньевна Аринина, к. м. н., ведущий научный сотрудник лаборатории фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
С наступившим летом тема нашей статьи приобрела особую актуальность. Кишечные инфекции — это целая группа инфекционных заболеваний, поражающих в основном желудочно-кишечный тракт. Острые кишечные инфекции по своей распространенности уступают только острым респираторным заболеваниям. Пик заболеваемости обычно приходится на лето, но и в холодное время года часто встречаются кишечные инфекции, вызываемые преимущественно вирусами. Однако наиболее частая причина возникновения этих заболеваний — попадание возбудителей инфекции с загрязненными продуктами и водой в желудочно-кишечный тракт.
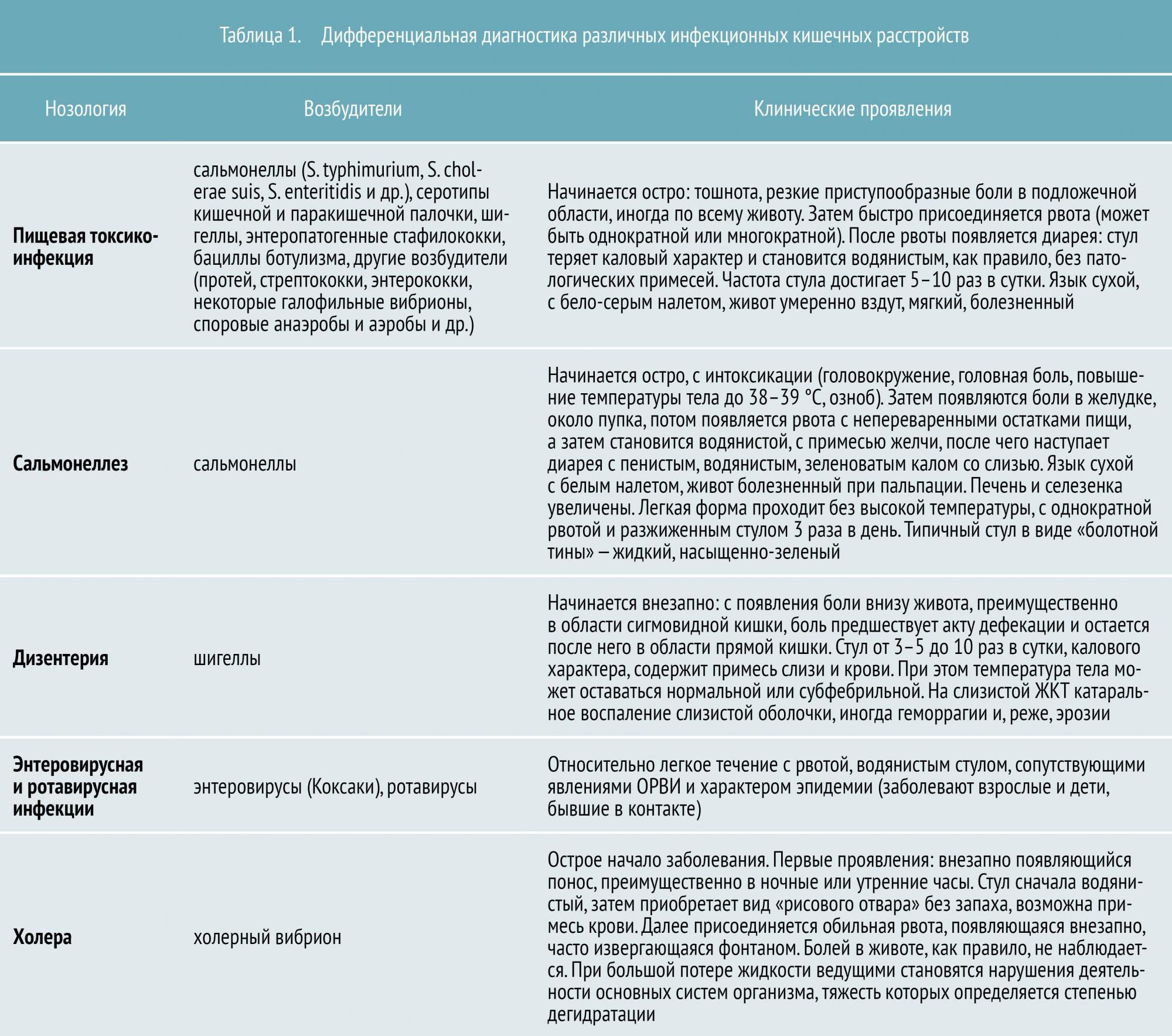
Всего в настоящее время известно около 30 инфекционных кишечных заболеваний. К наиболее распространенным относятся:
- пищевая токсикоинфекция (в основном стафилококковой этиологии)
- сальмонеллез
- дизентерия
- энтеровирусная и ротавирусная инфекция
- холера
Осложнения кишечных инфекций:
- бактериальные инфекции органов дыхания и среднего уха
- дисбактериоз кишечника
- кишечное кровотечение
- перфорация стенки кишки
- инвагинация кишечника
- бактериально-токсический шок
Возбудители кишечной инфекции
Помимо инфекционных агентов из естественной среды источником заражения может стать уже заболевший человек. Выделяя большое количество патогенных микроорганизмов (микробы выделяются с испражнениями, рвотными массами, иногда с мочой), больной заражает предметы, находящиеся вокруг, и, если не соблюдать меры предосторожности, может возникнуть цепная реакция в распространении инфекции.
Практически все возбудители кишечных инфекций чрезвычайно живучи. Они способы подолгу существовать в почве, воде и на различных предметах (ложках, тарелках, дверных ручках и мебели). Инфекционные микроорганизмы во внешней среде не только не погибают, но и сохраняют способность к размножению, а размножаются они наиболее активно в теплых и влажных условиях. Однако самая благоприятная среда для развития бактерий — это кисломолочные и мясные продукты.
Установлена связь отдельных форм острых кишечных инфекций с видами пищи. Так, дизентерия чаще возникает при употреблении молока и молочных продуктов, а кишечные инфекции, вызванные стафилококком, — при употреблении молочных продуктов и кондитерских изделий с кремом. Иерсиниозы обычно развиваются при употреблении сырых овощей, салатов и другой растительной пищи.
Возбудителями кишечных инфекций могут быть как бактерии (сальмонеллы, шигеллы, иерсинии, энтеропатогенные кишечные палочки, стафилококки), так и их токсины (пищевые токсикоинфекции). Вирусы (ротавирусы, энтеровирусы, астровирусы, парвовирусы) пока на втором месте по частоте встречаемости, однако в последнее время вирусные инфекции получают всё более широкое распространение. И на последнем месте — простейшие (лямблии, амебы, бластоцисты).
После попадания патогенов в организм человека, как правило, проходит бессимптомный инкубационный период, который продолжается от 6 до 48 часов — от попадания микроорганизмов в ротовую полость до момента поступления их в кишечник, где происходит их бурное размножение. После того как патогенные микроорганизмы размножились, начинается стадия клинических проявлений.
Наступает острый период — от 1 до 14 дней, в это время клинические проявления со стороны ЖКТ выражены максимально. Как правило, период заканчивается, когда нормализуется температура и прекращается ведущий симптом (понос или рвота).
Период реконвалесценции — не менее 2 недель, а в некоторых случаях при отсутствии лечения до нескольких лет. В этот период функция желудочно-кишечного тракта, как правило, восстанавливается не полностью — может быть неустойчивый стул.
В основном все кишечные инфекции протекают с достаточно похожими симптомами. Они всегда начинаются внезапно. В самом начале заболевания появляется резкая слабость, вялость, снижение аппетита, головная боль, повышение температуры — неспецифические симптомы, которые могут напоминать симптомы респираторных вирусных инфекций. Однако вскоре возникают тошнота, рвота, схваткообразные боли в животе, понос с примесью слизи, гноя или крови (например, при дизентерии), также могут беспокоить жажда и озноб. Среди клинических проявлений со стороны желудочно-кишечного тракта, как правило, сильнее всего выражены симптомы, связанные с пораженным органом:
- тошнота, рвота и боли в эпигастральной области (при гастрите);
- понос (при энтерите);
- рвота и понос (при гастроэнтерите);
- кровь в стуле и его нарушения (при колите);
- поражения всего кишечника (при энтероколите).
Одно из самых неблагоприятных последствий кишечной инфекции — это дегидратация организма из‑за рвоты и/или поноса и, как следствие, нарушение водно-электролитного обмена. Результатом резкой дегидратации может стать даже шок.
Однако иногда кишечные инфекции могут не иметь видимых симптомов, но сопровождаются выделением возбудителей. В плане распространения инфекции такое носительство наиболее опасно: ничего не подозревающий человек становится постоянным источником инфекции, заражая окружающих.
Врачу важно провести дифференциальную диагностику между кишечной инфекцией и соматическими заболеваниями со сходными симптомами: диареей, связанной с приемом лекарственных препаратов, острым аппендицитом, инфарктом миокарда, пневмонией, внематочной беременностью и т. д.
Диагностика и лечение кишечной инфекции
- Выделение из крови возбудителя и его антигенов (токсинов)
- Бактериологическое исследование: выделение и типирование возбудителя в посевах кала, других биологических секретов и экскретов организма больного
- Вирусологическое исследование: выделение вируса из кала в посевах на культуре клеток или при электронной микроскопии
- Микроскопическое исследование: обнаружение паразитов в мазках нативного кала после обработки специальными красителями
- Выявление сывороточных антител к антигенам возбудителя и роста их титра: серологическое обследование с использованием специальных диагностикумов в реакциях (РПГА, РИГА, ИФА и т. п.); прирост титра в 4 раза.
Основные принципы терапии кишечных инфекций:
- борьба с возбудителем (антибактериальная терапия);
- борьба с обезвоживанием (как правило, для устранения недостатка жидкости пациентам назначают солевые растворы);
- устранение диареи (энтеросорбенты);
- соблюдение щадящей диеты (исключение свежих овощей и фруктов, молочных продуктов, сладкого).
Во время болезни необходимо соблюдать диету, помогающую замедлить перистальтику кишечника. Рекомендуются продукты с высоким содержанием танина (черника, черемуха, крепкий чай); вещества вязкой консистенции (слизистые супы, протертые каши, кисели); сухари; индифферентные вещества — паровые блюда из нежирного мяса и рыбы. Важный этап в лечении кишечных инфекций — исключение из рациона жареных и жирных блюд, сырых овощей и фруктов.
Главное направление лечебной тактики — нейтрализация экзотоксинов в кишечнике (энтеросорбенты) и регидратация — компенсация патологических потерь жидкости и электролитов специально разработанными глюкозо-солевыми растворами. Объем вводимых растворов зависит от степени обезвоживания и массы тела больного, а скорость введения составляет 1–1,5 л/ч. Дезинтоксикационная и регидратационная терапия в 85–95 % случаев может осуществляться перорально.
Антибиотики может назначить только инфекционист с учетом проведенных лабораторных тестов и выявленного возбудителя инфекции. Однако при выраженной диарее для ускоренной санации обоснованным является назначение антибактериальных ЛС, которые не всасываются или плохо всасываются из кишечника и обладают широким спектром действия (например, энтерофурил или ко-тримоксазол). Эффективными средствами альтернативной этиотропной терапии, в качестве препаратов от острой кишечной инфекции, являются энтеросорбенты и пробиотики. Этиотропное действие пробиотиков связано с выраженной антагонистической активностью в отношении всех возбудителей острых кишечных инфекций (ОКИ) бактериальной этиологии и опосредованным иммуномодулирующим действием на местное звено иммунитета.
Обзор лекарств для лечения кишечных инфекций
Нифуроксазид (энтерофурил)
Безрецептурное противомикробное средство широкого спектра действия, производное 5‑нитрофурана. Антимикробная активность нифуроксазида вызвана наличием в его составе NO2‑группы, которая угнетает активность дегидрогеназы и нарушает синтез белков в патогенных бактериях.
Нифуроксазид не оказывает действия на сапрофитную флору, не нарушает равновесия нормальной кишечной флоры. При острой бактериальной диарее восстанавливает эубиоз кишечника. При инфицировании энтеротропными вирусами препятствует развитию бактериальной суперинфекции. Этот препарат для лечения кишечной инфекции можно назначать беременным и кормящим женщинам, детям начиная с одного месяца. Терапия нифуроксазидом не должна превышать 7 дней, при этом запрещено употреблять алкоголь.
Кипферон
Безрецептурный препарат в форме вагинальных и ректальных суппозиториев. Обладает иммуномодулирующим, противовирусным, антихламидийным действием. Кипферон — комплексная лекарственная форма, содержащая человеческий рекомбинантный интерферон-α2 и комплексный иммуноглобулиновый препарат (КИП). Разрешен к применению у детей на первом году жизни.
Ко-тримоксазол (сульфаметоксазол + триметоприм)
Механизм действия ко-тримоксазол а обусловлен двойным блокированием метаболизма микроорганизмов. Триметоприм обратимо ингибирует дигидрофолатредуктазу микроорганизмов, нарушает образование из дигидрофолиевой кислоты тетрагидрофолиевой, продукцию нуклеиновых кислот, пиримидиновых и пуриновых оснований; подавляет размножение и рост бактерий. Сульфаметоксазол, который по строению схож с парааминобензойной кислотой, захватывается бактерией и препятствует включению парааминобензойной кислоты в дигидрофолиевую кислоту. В связи с тем что ко-тримоксазол угнетает жизнедеятельность кишечной палочки, снижается образование в кишечнике никотиновой кислоты, рибофлавина, тиамина и прочих витаминов B-комплекса. Это лекарство, помогающее от кишечной инфекции, отпускается по рецепту, применяется с 2‑месячного возраста.
Бактисубтил — споры бактерий Bacillus cereus IP. Рецептурный препарат от кишечной инфекции бактисубтил сохраняет и корригирует физиологическое равновесие кишечной флоры. Споры бактерий, содержащиеся в препарате, устойчивы к действию желудочного сока. Прорастание бактерий в вегетативные формы происходит в кишечнике, затем они высвобождают энзимы, которые расщепляют углеводы, жиры, белки. В результате образуется кислая среда, предотвращающая процессы гниения. Препарат препятствует нарушению синтеза витаминов группы В и Р в кишечнике, его нельзя запивать горячим, а также сочетать с алкоголем. Детям его назначают с семилетнего возраста. Бактисубтил резистентен к действию различных антибиотиков и сульфаниламидных препаратов, поэтому может быть назначен одновременно с ними.
Декстроза + калия хлорид + натрия хлорид + натрия цитрат (регидрон)
Регидратирующее средство для перорального приема восстанавливает водно-электролитное равновесие, нарушенное при обезвоживании организма; корректирует ацидоз. Содержимое одного пакетика растворяют в литре свежепрокипяченной охлажденной питьевой воды. Приготовленный раствор нужно хранить в холодильнике и использовать в течение 24 часов. В раствор нельзя добавлять никакие другие компоненты, чтобы не нарушить действие препарата. Отпускается без рецепта.
Смектит диоктаэдрический
Безрецептурное лекарственное средство природного происхождения, обладающее протективным действием в отношении слизистой оболочки кишечника и выраженными адсорбирующими свойствами. Являясь стабилизатором слизистого барьера, образует поливалентные связи с гликопротеинами слизи и увеличивает продолжительность ее жизни, образуя физический барьер, который защищает слизистую оболочку пищеварительного тракта от отрицательного действия ионов Н+, соляной кислоты, желчных солей, микроорганизмов, их токсинов и других раздражителей. Обладает селективными сорбционными свойствами, защищает слизистую оболочку пищеварительного тракта от отрицательного воздействия. В терапевтических дозах не влияет на моторику кишечника.
Профилактика кишечных инфекций, в том числе и острых
Для профилактики кишечных инфекций важно регулярно мыть руки и проводить влажную уборку в квартире. Лучше сразу же выкидывать продукты с истекшим сроком годности, не покупать их в местах с непонятными условиями хранения — как бы ни были привлекательны, скажем, грибочки у бабушки возле метро — а фрукты и овощи есть только тщательно вымытыми.
Избежать распространения болезни поможет ранняя диагностика и изоляция больного с кишечной инфекцией. В очаге инфекции нужно обработать поверхности дезинфицирующими растворами, прокипятить посуду. Выписку пациентов проводят только после отрицательного результата контрольного обследования кала. Всем, кто перенес кишечную инфекцию, в течение месяца необходимо регулярно проходить диспансерное наблюдение в поликлинике.
Простые меры профилактики кишечных инфекций:
- пить воду и молоко только в кипяченом виде
- мыть овощи и фрукты горячей водой с мылом
- соблюдать правила и сроки хранения пищевых продуктов
- мыть руки перед едой
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.
, MD, University of Rochester School of Medicine and Dentistry
Last full review/revision January 2018 by Geoffrey A. Weinberg, MD
Причины, обследование и тактика ведения возможной скрытой бактериемии варьирует в зависимости от возраста и прививочного статуса детей. См. также Лихорадка у детей грудного и младшего возраста (Fever in Infants and Children).
Дети в возрасте от 3 до 36 мес.
В период до конъюгированных вакцин, примерно от 3 до 5% детей в возрасте от 3 до 36 мес. с лихорадочным заболеванием (температура ≥ 39 ° C) и без локализации патологических изменений (то есть, лихорадка без источника) имели скрытую бактериемию. И наоборот, дети старше 36 мес. с бактериемией почти всегда выглядели больными и имели идентифицируемый (т. е. не скрытый) очаг инфекции. Большинство (80%) случаев скрытой бактериемии до начала плановой вакцинации конъюгатами, было вызвано Streptococcus pneumoniae. Меньший процент случаев (10%) был вызван Haemophilus influenzae типа b, и еще меньший процент (5%) – Neisseria meningitidis.
Скрытая бактериемия является проблемой, потому что у порядка 5-10% детей развиваются тяжелые бактериальные инфекции (ТБИ) — в большинстве случаев они определяются как сепсис, менингит, а также инфекции мочеполовых путей, но в том числе и септический артрит и остеомиелит. Такие инфекции могут быть сведены к минимуму путем раннего выявления и лечения бактериемии. Вероятность прогрессирования серьезного очагового заболевания зависит от причины: от 7 до 25% бактериемий вызваны H. influenzae типа b, и 4-6% – S. pneumoniae.
В настоящее время в США и Европе, плановая вакцинация младенцев полисахаридной конъюгированной вакциной против S. pneumoniae и H. influenzae типа b ликвидировала (> 99%) инфекции H. influenzae типа b и существенно снизила (≥ 70% совокупно и ≥90% по типу вакцины) инвазивные инфекции S. pneumoniae. Таким образом, в этой возрастной группе скрытая бактериемия стала редким исключением у детей не вакцинированных должным образом или вообще не привитых, а также у детей с иммунодефицитом.
Дети в возрасте до 3 мес.
И наоборот, лихорадящие младенцы в возрасте до 3 мес. по-прежнему имеют больший риск тяжелой бактериальной инфекции, чем груднички постарше, примерно от 8 до 10%. В прошлом ТБИ у маленьких детей до 3 мес. наиболее часто были вызваны бета-гемолитическим Streptococcus группы В, S. pneumoniae, а также H. influenzae типа b. Однако химиопрофилактика во время родов у беременных, колонизированных бета-гемолитическим Streptococcus группы В, снизила раннее начало (инфекции, возникающее в возрасте до 7 дней) стрептококковых заболевании группы В более, чем на 80%. Кроме того, плановая вакцинация конъюгатами уменьшила колонизацию среди старших братьев и сестер, привитых против S. pneumoniae и H. influenzae типа b, таким образом, что частота ТБИ, вызванных данными микроорганизмами, также снизилась (коллективный иммунитет).
Следует отметить, что на стрептококковую инфекцию группы В с поздним началом (инфицирование происходит в возрасте старше 7 дней) не влияет химиопрофилактика во время родов, а также другие тяжелые бактериальные болезни, такие как ИМВП (чаще всего вызвана Escherichia coli), и отдельные случаи бактериемии Salmonella продолжают оставаться основными причинами лихорадки без видимого источника при объективном обследовании у детей
Клинические проявления
Основным симптомом скрытой бактериемии является лихорадка — температура ≥ 39 °С ( ≥ 38°С для грудных детей до 3 мес.). По определению дети с явным локальным заболеванием (например, кашлем, одышкой и легочными хрипами, предполагающими пневмонию, эритемой кожи, указывающей на флегмону или септический артрит) исключаются (то есть, потому что их заболевание не является скрытыми). Токсические проявления (например, вялость и апатичность, заторможенность, признаки плохой перфузии, цианоз, выраженная гиповентиляция или гипервентиляция) предполагают наличие сепсиса или септического шока, бактериемия у таких детей не классифицируются как скрытая или как лихорадка без видимого очага инфекции. Однако ранние этапы сепсиса может быть трудно отличить от скрытой бактериемии.
Диагностика
Посев мочи и общий анализ мочи
Полный анализ крови и лейкоцитарная формула
Иногда другие диагностические исследования, в зависимости от возраста и клинического состояния
Для диагностики бактериемии требуется посев крови; в идеале, набирается два образца из разных мест, что позволяет свести к минимуму проблему ложноположительных результатов из-за контаминации кожи, с получением результатов в течение 24 ч.
Рекомендации по обследованию и выбору диагностических тестов варьируют в зависимости от возраста, температуры и клинических проявлений; цель состоит в том, чтобы минимизировать обследования, не пропустив при этом ТБИ. Дети, которые имеют признаки очаговой инфекции в анамнезе или при объективном обследовании, оцениваются на основе этих результатов.
Когда доступно, диагностические экспресс-тесты на энтеровирусы, респираторно-синцитиальный вирус и вирус гриппа целесообразны при обследовании детей с лихорадкой без видимого источника, потому что дети, с положительными результатами тестов на вышеуказанные вирусы, вероятно, лихорадят в результате этих возбудителей и требуют небольшого количества диагностических процедур, или вообще не нуждаются в дальнейшем обследовании на ТБИ. Существуют также экспресс-тесты для других вирусов, но они недостаточно изучены, чтобы обосновать использование их результатов для изменения обследования на ТБИ.
У младенцев с CБИ клинический анализ крови обычно показывает повышенное количество лейкоцитов, однако только у 10% детей с количеством лейкоцитов > 15 000/мкл присутствует бактериемия, поэтому специфичность этого метода низкая. Маркеры острой фазы воспаления (например, СОЭ, С-реактивный белок) используются некоторыми врачами, но дают мало информации; некоторые врачи считают, что повышенный уровень прокальцитонина может быть более специфичным для тяжелого заболевания. У детей 3 мес. число тромбоцитов > 1500/мкл и низкое ( 5000/мкл) или высокое ( > 15 000/мкл) число лейкоцитов могут указывать на бактериемию.
Важно отметить, что любой лихорадящий ребенок, независимо от прививочного анамнеза, который выглядит тяжелобольным или интоксицированным, требует комплексного клинического и лабораторного обследования (ОАК с лейкоцитарной формулой, бакпосев крови, бакпосев мочи, спинномозговая пункция, и, в большинстве случаев, госпитализация в больницу с эмпирической антимикробной терапией). Лихорадящие дети в этой возрастной группе, которые не привиты должным образом или вообще не привиты, а также с ослабленной иммунной системой, более восприимчивы к ТБИ, чем их сверстники, а также, как правило, нуждаются в вышеупомянутом полном клиническом и лабораторном обследовании на ТБИ и эмпирической антибактериальной терапии. Детям с одышкой или низкой сатурацией кислорода также необходимо провести рентген грудной клетки.
У ранее привитых лихорадящих детей в возрасте от 3 до 36 мес., которые выглядят хорошо (не имеют признаков интоксикации), риск бактериемии в настоящее время низкий и даже ниже, чем частота ложно-положительных культур крови из-за контаминации кожи, что заставляет многих специалистов отказаться от посева крови у этих детей. Тем не менее, обычно рекомендуется общий анализ мочи с микроскопией и посев мочи, но не дополнительное лабораторное обследование (например, ОАК, рентген грудной клетки). Несмотря на то, что подавляющее большинство этих детей имеют вирусную инфекцию, очень небольшое количество детей, выглядящих здоровыми, будут иметь начало ТБИ, поэтому ухаживающим лицам следует рекомендовать следить за симптомами ребенка, давать жаропонижающие и иметь обратную связь с врачом (путем посещения или в телефонном режиме, в зависимости от обстоятельств и надежности ухаживающих лиц) в течение 24 - 48 часов. Дети, которым становится хуже или продолжают лихорадить, должны пройти обследование (например, ОАК с лейкоцитарной формулой, бакпосев крови, при возможности, рентген грудной клетки или люмбальная пункция).
Младенцы, которые выглядят интоксицированными или тяжелобольными, требуют немедленного клинического обследования и забора крови, мочи, бакпосева ликвора, а также госпитализации для эмпирической антибактериальной терапии. В отличие от детей более старшего возраста, дети в возрасте до 3 мес., клиническое отсутствие признаков интоксикации обычно не позволяет отложить обследование.
Был разработан алгоритм для оказания помощи в проведении оценки младенцев в данной возрастной группе (для примера, Оценка состояния и ведение младенцев с лихорадкой в возрасте
ПЗМ = поле зрения микроскопа под большим увеличением.
Читайте также:


