Оборудование для диагностики туберкулеза

В 2004 году по инициативе д.м.н., профессора Михаила Александровича Владимирского, заведующего сектором молекулярной диагностики туберкулёза НИИ Фтизиопульмонологии Первого МГМУ им. И.М.Сеченова, мы начали разработки в области ПЦР-диагностики туберкулёза.
Выделение ДНК: использование оригинальных реагентов и магнитных частиц обеспечивает получение максимального количества чистой ДНК и позволяет автоматизировать процесс выделения ДНК.
ПЦР в реальном времени: одновременная детекция нескольких различных участков генома комплекса микобактерий туберкулёза (МБТ) увеличивает информативность и достоверность анализа.
I этап – Пробоподготовка, инактивация
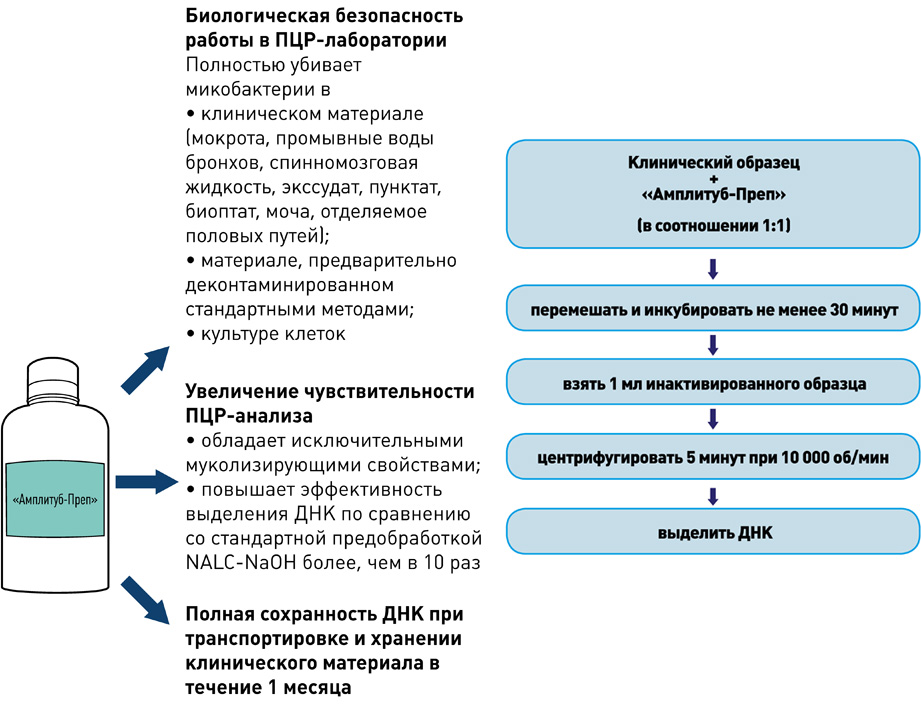
II этап – Выделение ДНК
набор реагентов для выделения ДНК (на магнитных частицах)
набор реагентов для выделения ДНК микобактерий из клинических образцов и культур клеток на автоматизированных станциях TECAN

- Снижение риска контаминации во время выделения ДНК практически до нуля.
- Значительное уменьшение трудоёмкости процесса выделения ДНК.
- Стандартизированное выделение ДНК из клинических образцов.
- Экономическая выгода: низкий расход пластика и реактивов.
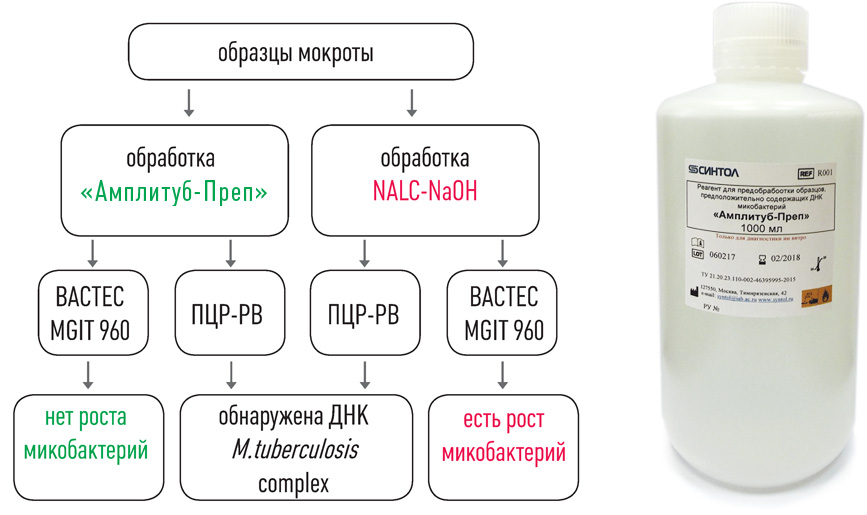
набор реагентов для ускоренной пробоподготовки и выделения ДНК микобактерий из образцов мокроты
III этап – ПЦР в реальном времени
Обнаружение и количественное определение комплекса МБТ
Набор реагентов АМПЛИТУБ-РВ — это:
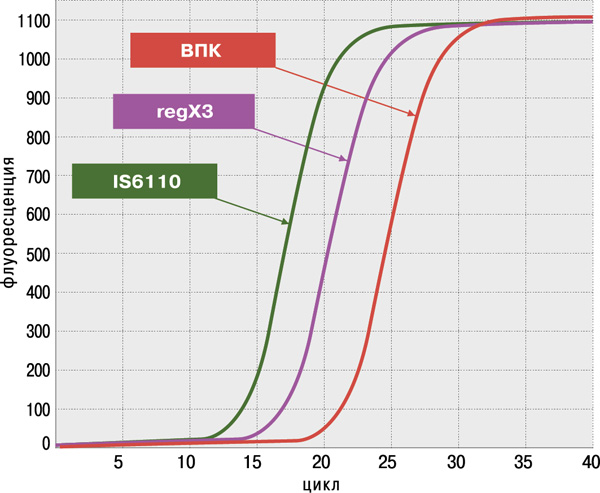
- высокая достоверность анализа благодаря одновременному обнаружению двух специфичных генов M.tuberculosis complex: IS6110 и regX3;
- оценка пригодности образца ДНК для определения антибиотикоустойчивости;
- высокая чувствительность (не более 100 КОЕ/мл мокроты или 1–10 копий фрагментов ДНК в реакции) и 100%‑ая специфичность, подтверждённые на панели QCMD (Quality Control for Molecular Diagnostics) Mtb EQA (UK).
Определение антибиотикоустойчивости МБТ к препаратам I и II ряда
Наборы реагентов АМПЛИТУБ-МЛУ-РВ, АМПЛИТУБ-FQ-РВ — это:
- диагностика форм туберкулеза с лекарственной устойчивостью, в том числе множественной лекарственной устойчивостью (МЛУ) и широкой лекарственной устойчивостью (ШЛУ);
- быстрая детекция мутаций M.tuberculosis, ассоциирующихся с устойчивостью к антибиотикам первого и второго ряда (рифампицину, изониазиду, этамбутолу, фторхинолонам);
- достоверность результатов, ежегодно подтверждаемая при проведении Федеральной службой внешней оценки качества (ФСВОК) Росздравнадзора испытаний шифрованных тест-культур и образцов.
Наборы АМПЛИТУБ-МЛУ-РВ и АМПЛИТУБ-FQ-РВ основаны на использовании оригинальной мультиконкурентной аллель-специфичной методики ПЦР в реальном времени, позволяющей выявлять мутации в генах микобактерий туберкулеза, ответственных за устойчивость к конкретным антибиотикам.

Принцип мультиконкурентной аллель-специфичной методики ПЦР в реальном времени
- В формате одной пробирки используются 5’-флуоресцентно-меченые аллель-специфичные праймеры с общим комплементарным им 3’-меченым олигонуклеотидом-гасителем и контрольный флуоресцентный зонд, комплементарный участку ДНК без мутаций.
- При отсутствии мутаций в ДНК нарастание флуоресценции в ходе ПЦР-РВ наблюдается только по флуорофору зонда.
- При наличии мутаций в ДНК нарастание флуоресценции в ходе ПЦР-РВ наблюдается как по флуорофору зонда, так и по флуорофору 5’-флуоресцентно-меченого аллель-специфичного праймера. Данный метод позволяет определить не только точку мутации, но и процент устойчивого мутантного штамма МБТ на фоне дикого.
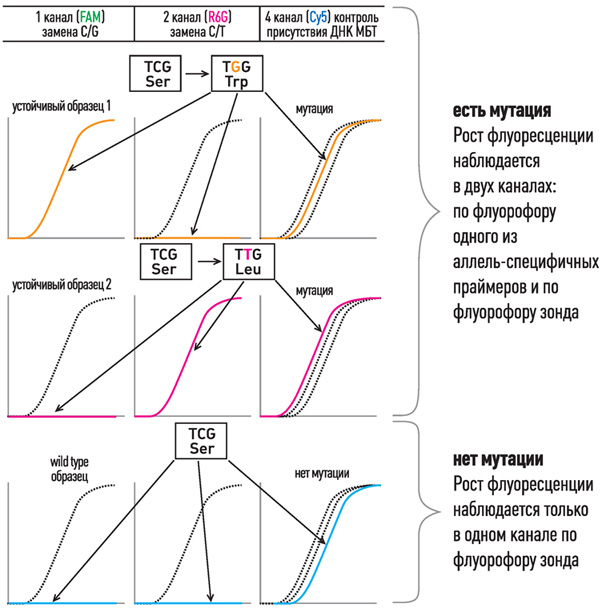
Интерпретация результатов выявления мутаций на примере
531 кодона rpoB гена M.tuberculosis
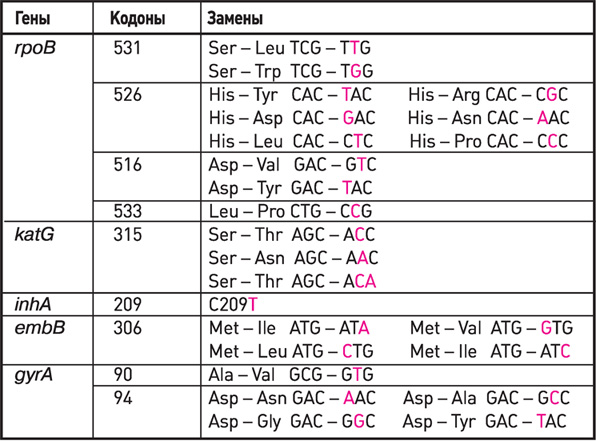
Гены, кодоны, замены, используемые в наборах реагентов
АМПЛИТУБ-МЛУ-РВ при определении антибиотикоустойчивости
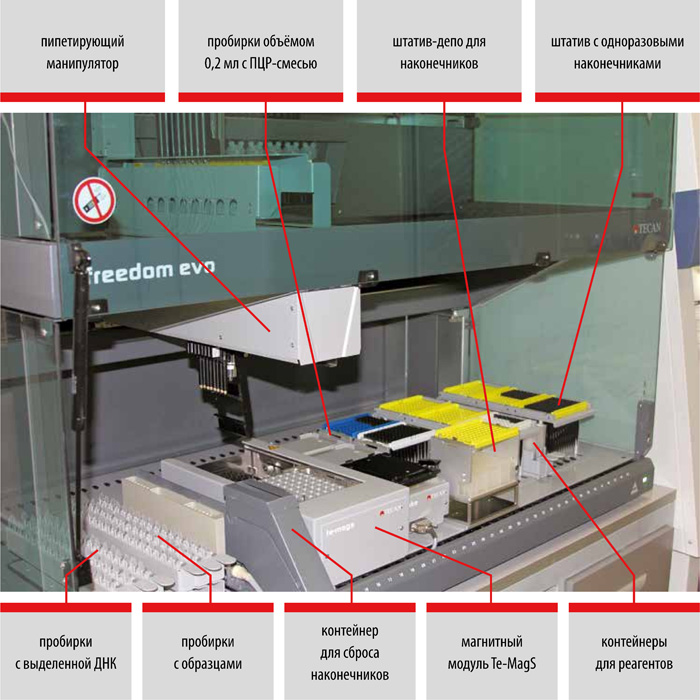
Использование автоматизированных станций Freedom EVO (TECAN, Швейцария) для молекулярно-генетической диагностики туберкулёза
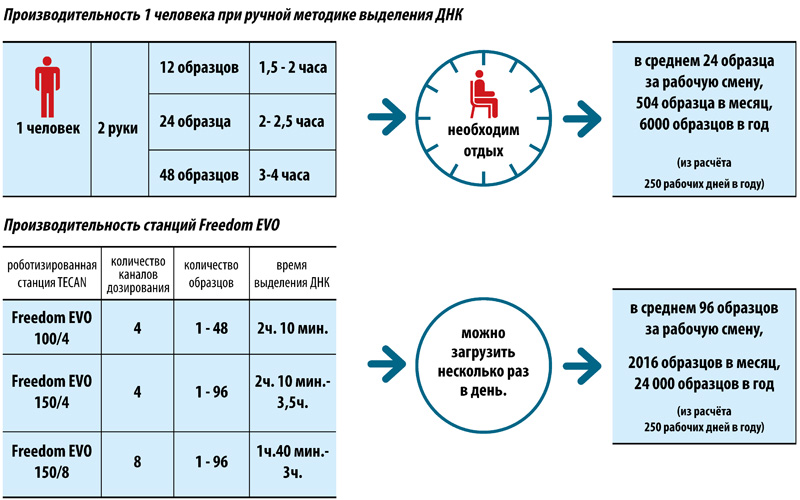

Трудозатраты — 1 час
Продолжительность выделения ДНК — не более 2 часов
Подготовка к амплификации и ПЦР-РВ — 1,5 часа
ИТОГО: результаты анализа будут готовы через 3,5 часа
Оператор затратит 1 час своего рабочего времени.
Туберкулез - хроническая инфекция с длительным периодом выделения возбудителя, многообразием клинических проявлений, поражением различных органов и систем - представляет непростую задачу для лабораторной диагностики. Молекулярно-биологические методы (ПЦР) используются для выявления, видовой дифференциации и определении лекарственной устойчивости микобактерий туберкулезного комплекса.
Ввиду биологических особенностей возбудителя и иммунного ответа человека диагностика туберкулеза не может ограничиваться каким-либо одним методом и должна проводиться комплексно.
Возбудители туберкулеза могут быть обнаружены в различных биоматериалах, природа которых определяет выбор наборов реагентов для экстракции ДНК. Ключевой принцип выбора биоматериала для диагностики туберкулеза методом ПЦР: необходимо выбирать биоматериал, соответствующий клинической форме туберкулезной инфекции.
Например, для диагностики туберкулеза мочеполовой системы нужно исследовать мочу или менструальную кровь, рекомендуется также исследовать биоптаты из подозрительного очага. Для диагностики туберкулеза легких используется мокрота, бронхо-альвеолярный лаваж.
Реагенты и оборудование для предобработки биоматериалов и экстракции ДНК
| Наборы реагентов для экстракции ДНК из мокроты, бронхо-альвеолярного лаважа, мочи, синовиальной жидкости и смывов с объектов окружающей среды | АмплиПрайм ДНК-сорб-В и АмплиПрайм РИБО-преп |
| Реагент для разжижения мокроты и синовиальной жидкости | Муколизин |
| Набор для экстракции ДНК, используемый при исследовании биоптатов (легкие, лимфатические узлы, почки, печень, мозг, селезенка) | ДНК-сорб-С |
| Оборудование для гомогенизации биоптатов | TissueLyser LT или TissueLyser II |
| Парафиновые блоки нарезают на микротоме или вырезают фрагмент ткани одноразовым скальпелем, а затем проводят экстракцию ДНК, например, с помощью набора реагентов QIAamp DNA FFPE Tissue Kit (50) | QIAamp DNA FFPE Tissue Kit (50) |
Наборы реагентов для ПЦР-диагностики туберкулеза
Применение молекулярно-биологических методов (в частности, выявление ДНК методом ПЦР) в диагностике туберкулеза регламентировано Приказом Минздрава РФ от 21.03.2003 № 109 "О совершенствовании противотуберкулезных мероприятий в Российской Федерации" (ред. от 29.10.2009).
Выявление микобактерий туберкулезного комплекса
Набор реагентов АмплиСенс® МТС-FL предназначен для обнаружения ДНК микобактерий туберкулеза – Mycobacterium tuberculosis complex (MTC), включающий в себя виды микобактерий разной степени вирулентности, вызывающих туберкулез у человека (M.tuberculosis, M.bovis, M.africanum, M.microti, M.canetti, М.pinipedii).
Микобактерии туберкулеза выявляются без видовой дифференциации; микобактерии, не относящиеся к MTC (например, M.avium и M.paratuberculosis) - не выявляются. Данный набор реагентов используется в топической диагностике туберкулеза и позволяет быстро (за несколько часов) с высокой чувствительностью и специфичностью (близким к 100%) определять наличие микобактерий туберкулеза в образце биоматериала.
Благодаря высокой скорости и информативности в диагностике туберкулеза, методы амплификации нуклеиновых кислот (в том числе ПЦР) в 2010 году были предложены CDC США для подтверждения диагноза туберкулеза наряду с культуральным методом.
Видовая дифференциация микобактерий туберкулеза методом ПЦР
Не менее важно дифференцирование до вида внутри группы MTC. Это связано с необходимостью определения источника заболевания, определения тактики противотуберкулезной терапии, а также для подтверждения случаев поствакцинальных осложнений.
С этой задачей позволяет справиться набор реагентов АмплиСенс® МТС-diff-FL, предназначенный для дифференцирования видов микобактерий туберкулеза внутри MTC: человеческого (M.tuberculosis), бычьего (M.bovis) и вакцинного штамма (M.bovis BCG) – в клиническом материале и культурах микроорганизмов.
Актуальность видовой дифференциации определяется, например, тем, что разные виды микобактерий отличаются профилем лекарственной устойчивости. Например, M.bovis и её вакцинный штамм M.bovis BCG отличаются природной резистентностью к одному из основных противотуберкулезных препаратов - пиразинамиду. Поэтому при туберкулезе, вызванной M.bovis, и БЦЖите пиразинамид не назначается.
Приказом Минздрава РФ от 21.03.2003 № 109 "О совершенствовании противотуберкулезных мероприятий в Российской Федерации" (ред. от 29.10.2009) регламентировано применение наборов реагентов, дифференцирующих M.bovis от ее вакцинного штамма M.bovis BCG, для диагностики БЦЖита.
Определение лекарственной устойчивости туберкулеза
Распространение штаммов туберкулеза с лекарственной устойчивостью, в том числе с множественной лекарственной устойчивостью (МЛУ, или MDR) составляет одну из серьезнейших проблем современного здравоохранения. Определение лекарственной устойчивости туберкулеза с помощью молекулярно-биологических методов всё шире применяется ввиду высокой скорости получения результатов (1-2 дня), что становится возможным благодаря использованию не только первичной культуры, но и непосредственно клинического материала.
Важно понимать, что наборы реагентов, основанные на разных молекулярно-биологических методах, характеризуются разными показателями диагностической чувствительности и специфичности.
| Наименование набора реагентов | АмплиСенс® MTC-Rif-Seq | АмплиСенс® MTC-PZA-Seq |
| Исследуемый ген | rpo B | pnc A |
| Препараты, к которым определяется устойчивость | рифампицин | пиразинамид |
| Кол-во выявляемых мутаций | более 200 | более 500 |
Наборы включают реагенты для амплификации фрагментов ДНК микобактерий туберкулеза, очистки продуктов амплификации (сорбентным методом), определения концентрации очищенного продукта амплификации и праймеры для секвенирования. Наборы для экстракции ДНК (АмплиПрайм РИБО-преп или ДНК-сорб-С ) и реагенты для проведения реакции секвенирования приобретаются отдельно.

Нормативные документы, публикации, информационные материалы >>
В соответствии с современными программами ВОЗ, основой выявления туберкулёза за рубежом считают проведение микроскопии мазков мокроты, полученной от кашляющих больных, обратившихся к врачам общей практики; мазки окрашивают по Цилю-Нильсену. Эта методика входит в отечественный поликлинический и клинический минимум обследования пациента, выделяющего мокроту. В 1995 г. Минздравмедпром России в приказе № 8 "О развитии и совершенствовании деятельности лабораторной клинической микробиологии (бактериологии) лечебно-профилактических учреждений" подтвердил эту обязанность клинико-диагностических лабораторий. Обязательное бактериологическое исследование мокроты на М. tuberculosis должно быть организовано для нетранспортабельных больных, больных хроническими заболеваниями органов дыхания и мочевыводящей системы, а также для работников неблагополучных по туберкулёзу животноводческих хозяйств. Этот старейший метод полностью сохраняет свое значение вследствие доступности для практических клинико-диагностических лабораторий, низкой стоимости и быстроты выполнения.
При бактериоскопии мазка, окрашенного по Цилю-Нильсену, микобактерии туберкулеза могут быть обнаружены при наличии не менее 100 000 - 1 000 000 бактериальных клеток в 1 мл патологического материала (мокроты). Такое большое количество микобактерий встречается у больных с далеко зашедшими прогрессирующими формами заболевания (диссеминированными и фиброзно-кавернозными). У значительно большего числа больных количество выделяемых ими микобактерий ниже предела метода бактериоскопии, что и является большим минусом этого метода. Только при идеальном выполнении всех требуемых условий, указанных в Приказе № 109 МЗ РФ,-исследование не менее трех проб диагностического материала, правильный сбор мокроты, наличие современного бинокулярного микроскопа и высококачественных реактивов, просмотр до 300 полей зрения - возможно повышение чувствительности до 10000 микробных клеток.
Микобактерии туберкулёза имеют вид тонких, слегка изогнутых палочек различной длины с утолщениями на концах или посередине, располагаются группами и поодиночке (рисунок 1,а) Окрашенные по Цилю-Нильсену мазки микроскопируют с иммерсионной системой не менее 10 мин.
Люминесцентная микроскопия
Метод основан на проникновении в микробную клетку карболового производного флюоресцентного красителя (аурамина, родамина). При окраске флюоресцентным красителем аурамином-родамином микобактерии можно видеть при неиммерсионном 100-кратном увеличении. Более точен результат при окраске по Цилю-Нильсену карболфуксином и иммерсионной микроскопии при 1000-кратном увеличении. Именно окраска мазка по Цилю-Нильсену рекомендована при применении технологий DOTS. Микобактерии в этом случае выглядят светящимися желтыми палочками (рисунок 1, б). Метод имеет неоспоримые преимущества, так как позволяет при меньшем увеличении микроскопа просмотреть фактически весь мазок, так же этот метод экономически более эффективен, так как уменьшается время, затрачиваемое на просмотр мазков.
К недостаткам метода ЛМ следует отнести значительно более высокую стоимость люминесцентного микроскопа, при процедуре окрашивания- соблюдение и коррекция pH мазка, а также освобождение микобактерий в диагностическом материале (особенно в мокроте) от окружающей их слизи, которая препятствует проникновению флуоресцентного красителя в микробную клетку. Поэтому нецелесообразно использование ЛМ для нативной мокроты, но применять этот метод рекомендуется при исследовании мазков, приготовленных после центрифугирования из осадка материала, обработанного для культурального исследования и нейтрализованного после деконтаминации. Поэтому метод ЛМ следует применять в бактериологических лабораториях, где культуральное и микроскопическое исследование может быть произведено из одной и той же порции диагностического материала.
При гистологическом или цитологическом исследовании иногда можно обнаружить характерные для туберкулёза клетки, являющиеся результатом защитной реакции организма на внедрение туберкулёзной палочки. Наличие в цитограмме гигантских клеток Лангханса с несомненностью решает диагноз туберкулёза. Эти клетки имеют очень большие размеры (80 - 90 мкм и более в диаметре). Цитоплазма окрашена в серо-голубой цвет. По её периферии расположено в ряд большое количество ядер (до 20), расположенных в форме кольца (рисунок 1, в).
Другим признаком туберкулёза является присутствие в препарате так называемых эпителиоидных клеток, из которых и развиваются клетки Лангханса. Это происходит при увеличении количества ядер без разделения цитоплазмы, которая только увеличивается в размерах (рисунок 1, г).
Микроскопия позволяет быстро получить результат, но обладает низкой чувствительностью и специфичностью, невозможностью дифференциации кислотоустойчивых микобактерий.
Рисунок 1
Микобактерии туберкулеза
а - метод окраски по Цилю-Нельсену
б - метод люминисцентной микроскопии
в - клетки Лангхаса
г - эпителиоидные клетки
Наиболее распространенным методом выявления микобактерий туберкулеза в нашей стране является культуральный метод. Это "золотой стандарт" бактериологической диагностики туберкулеза, так как чувствительность метода существенно выше микроскопического и дает возможность получить чистую культуру микобактерий для её последующей идентификации и исследования лекарственной устойчивости. Этот метод дает положительные результаты при наличии в исследуемом материале от 20 до 100 жизнеспособных микробных клеток в 1 мл. Однако он трудоемок и длителен в связи с тем, что микобактерии туберкулеза растут очень медленно и их обнаружение может быть зарегистрировано только через 3 недели культивирования.
Исторически сложилось, что питательные среды на яичной основе (Левенштейна-Йенсена, Финна-2, Огавы, Аникина, "Новая", Попеску) получили наибольшее распространение среди плотных питательных сред, применяемых для выделения МБТ. Посев материала на среду Левенштайна-Йенсена проводят в бактериологической лаборатории. Рост первых колоний на классических средах отмечают через 4 - 8 недель. Однако появившиеся в последние годы агаровые среды Миддлбрука (7Н10, 7Н11) позволяют быстрее обнаружить рост микобактерий (от двух до четырех недель) и обеспечивают лучшие возможности для изучения морфологии колоний, чем на яичных средах. Недостатком агаризованных питательных сред является необходимость инкубации посевного материала в термостате с углекислым газом, поэтому агаризованные среды в России практически не применяются.
Следует отметить, что в связи с высокой избирательностью различных штаммов микобактерий и потребностью в полноценных белках до сих пор нет универсальной питательной среды, способной заменить все остальные. В Приказе № 109МЗ РФ для посева диагностического материала на МБТ рекомендуется использовать по одной пробирке международной питательной среды Левенштейна-Йенсена и Финна-2. Однако практика показывает, что кроме указанных сред целесообразно использовать и какую-либо из дополнительных, а посев на три пробирки питательной среды также повышает эффективность культуральной диагностики.
Для полноценной культуральной диагностики туберкулеза необходимо иметь соответствующие помещения и оборудование. Особенно важно наличие центрифуги и антиаэрозольной защитой и способностью обеспечить ускорение 3000g. А также шкафов биологической безопасности для предотвращения внутрилабораторного инфицирования.
Основным недостатком культуральной диагностики туберкулеза является длительность исследования - от трех недель до трех месяцев. Поэтому остаются актуальными дальнейшие исследования по разработке методов ускорения роста микобактерий.
Культуральная диагностика туберкулеза переживает в настоящее время принципиальные изменения, связанные с внедрением в практику полностью автоматизированных систем культивирования МБТ. Главное отличие этих методов - применение жидких питательных сред для культивирования с последующей радиометрической (BACTEC 460), колорометрической (Mb-Bact, Вас- tALERT) и люминесцентной детекцией роста (BACTEC MGIT 960). Рост МБТ на жидкой питательной среде в этих системах удается обнаружить уже через 1 - 2 недели в зависимости от их исходного количества в диагностическом материале. Частота выявления микобактерий так же несколько выше, чем на плотных питательных средах. Автоматизированные системы BACTEC с использованием соответствующих флаконов, содержащих различные противотуберкулезные препараты, позволяют сократить время исследования лекарственной устойчивости микобактерий до 10 - 14 суток.
Из перечисленных автоматизированных систем наиболее эффективна в настоящее время система BACTEC MGIT 960BD. Флаконы MGIT с жидкой питательной средой 7Н9 содержат в придонной части под силиконом флуоресцентный индикатор, "погашенный" высокими концентрациями кислорода. При наличии роста микобактерий в процессе поглощения кислорода индикатор начинает светиться, регистрация флуоресценции в сисиеме BACTEC MGIT производится автоматически. Использование флаконов MGIT возможно и "вручную", тогда регистрацию свечения производят с помощью трансиллюминатора на флаконах MGIT составляет 11 суток.
Основным недостатком BACTEC MGIT, как и других систем BACTEC, является высокая стоимость оборудования (до 100000 долларов США) и флаконов с питательной средой - посев одной пробы диагностического материала стоит до 400 рублей.
Так называемые дефектные по клеточной стенке L-формы микобактерий и других инфекционных патогенов являются результатом изменчивости и основным видом персистирования, то есть переживания в неблагоприятных условиях. Посев на L-формы особенно эффективен при внелегочном туберкулезе, поскольку вегетация МБТ в очагах ВЛТ при повышенном ацидозе и анаэробиозе приводит к снижению их жизнеспособности и ферментативной активности.
Диагноз не может быть поставлен только на основании выявления L-форм микобактерий, но их обнаружение, особенно при верификации методом ПЦР, является весомым аргументом в пользу туберкулезной природы заболевания. В очагах внелегочного туберкулеза наблюдается ранняя L-трансформация микобактерий, поэтому их обнаружение позволяет поставить диагноз на начальных стадиях заболевания.
Новый диагностический тест на туберкулез, включая его самую распространенную устойчивую форму, рекордными темпами вводится в использование, а его основным потребителем является Южная Африка. Теперь необходимо обеспечить лечение для новых случаев заболевания. Репортаж Клэр Китон (Claire Keeton).
Молекулярная технология, первоначально разработанная для выявления возбудителя сибирской язвы в почтовых отправлениях в Соединенных Штатах Америки, приводит к радикальным изменениям в области диагностики туберкулеза, особенно в странах, где туберкулез является одной из основных причин смерти среди ВИЧ-инфицированных людей. Xpert MTB/RIF — это полностью автоматизированный экспресс-тест на основе амплификации нуклеиновых кислот, ставший первым крупным прорывом в области диагностики туберкулеза после того, как более 100 лет назад была разработана микроскопия мазка мокроты.
Но в отличие от микроскопии мазка мокроты, для которой характерна низкая чувствительность в отношении ВИЧ-позитивных людей, или от посева мокроты, при проведении которого на получение основных результатов уходит от трех до шести недель, а на получение результатов тестов на лекарственную чувствительность еще больше времени, новый тест позволяет выявлять Mycobacterium tuberculosis и устойчивость к рифампицину, широко используемому противотуберкулезному препарату, менее чем за два часа.
Новый тест начинает применяться в 77 странах, но ни в одной из этих стран его внедрение не осуществляется с таким энтузиазмом, как в Южной Африке. На сегодняшний день эта страна, расположенная к югу от Сахары, приобрела 288 аппаратов Xpert и более одного миллиона картриджей для проведения тестов на туберкулез, что составляет 59% глобальных поставок.

Для проведения нового теста пациенты сдают образцы мокроты (жидкости, выделяемой из легких), как и в случае таких диагностических методик, как микроскопия и посев. Образец смешивается с реагентом, и смесь вводится в картридж, который вставляется в модуль аппарата. Результаты выводятся на экран компьютера.

С тех пор как в Южной Африке был введен новый тест, показатели диагностирования туберкулеза среди людей с симптомами в центрах первичной медико-санитарной помощи почти что удвоились — с 9 до примерно 16%. Примерно в 7% всех подтвержденных случаях заболевания туберкулез является устойчивым к рифампицину.
Лекарственно-устойчивый туберкулез представляет большую проблему, в частности, потому что пациентам необходимо лечение дорогими препаратами второй линии, которые приводят к более тяжелым побочным эффектам, чем препараты первой линии, а на эффективное лечение уходит до 24 месяцев. А если эти пациенты имеют ВИЧ-инфекцию, шансов выжить у них немного.
И хотя на сегодняшний день новый туберкулезный тест наиболее широко применяется в Южной Африке, последние данные мониторинга ВОЗ за его глобальным внедрением свидетельствуют о том, что Индия, Китай, Российская Федерация и Филиппины, на которые, по оценкам, приходится 60% случаев заболевания туберкулезом с лекарственной устойчивостью в мире, заказали аппараты Xpert, имеющие, в общей сложности, 404 модуля, и 131 820 картриджей MTB/RIF.
В то время как ВОЗ играет ключевую роль во внедрении этой технологии с точки зрения разработки политики и руководящих принципов, Фонд для инновационных и новых диагностических средств (ФИНД), некоммерческая структура, базирующаяся в Женеве и работающая над улучшением диагностики в бедных странах, первым признал потенциальные возможности этой технологии в борьбе с туберкулезом.
Система Xpert была разработана в 2002 году компанией Cepheid Inc., базирующейся в Саннивейле, США, для тестирования на сибирскую язву после серии терактов, произошедших в почтовых службах в 2001 году.
ФИНД обратился к Cepheid Inc. и заключил с ней соглашение о совместной разработке. Впоследствии эта компания адаптировала эту технологию для диагностики туберкулеза в партнерстве с Университетом медицины и стоматологии Нью-Джерси и при финансировании, предоставляемом Национальными институтами здоровья США и Фондом Билла и Мелинды Гейтс.
На переговорах, посредником на которых был ФИНД, Cepheid Inc. согласилась поставлять аппараты Xpert MTB/RIF в государственный сектор 145 стран по льготным ценам. Первоначально была достигнута договоренность о снижении цены на аппараты и картриджи на 75%. Таким образом, стоимость одного картриджа составляла около 18 долларов США, значительно меньше, чем в частном секторе (60-80 долларов США).
Но даже при такой уступке тест все равно был вне досягаемости для бедных стран, поэтому к решению этой проблемы присоединились Правительство США (ЮСЭЙД и ПЕПФАР), Фонд Билла и Мелинды Гейтс и финансовая организация в области здравоохранения ЮНИТЭЙД. Это привело к соглашению с Cepheid Inc. в августе 2012 года о снижении цены на картридж до 9,98 доллара США для 145 стран.

В противотуберкулезном диспансере появилось новое оборудование, помогающее на ранних стадиях диагностировать болезнь легких, проводить сверхточные биохимические анализы. Новые методики позволяют сократить срок лечения пациентов и облегчить с последствия туберкулеза, сообщает РИА SakhalinMedia.
В противотуберкулезном диспансере появилось новое оборудование, помогающее на ранних стадиях диагностировать болезнь легких. Исследования на туберкулезную палочку проводятся в бактериологической лаборатории диспансера. Пациенты сдают биологические материалы: мокроту, плевральную жидкость. С помощью современного аппарата "BACTEC", приобретенного в прошлом году, проводится быстрая диагностика образцов и выявляется даже незначительное содержание вредоносных бактерий. Достаточно наличия двух-трех туберкулезных палочек в миллилитре мокроты, чтобы ее обнаружить. Заведующая бактериологической лабораторией Олеся Соболюк рассказала, что обычно диагностика занимает около трех месяцев, с применением "BACTEC" - всего месяц. Пробы обрабатывают специальными реактивами. Фотодетекторы прибора измеряют уровень флуоресценции, на основе чего происходит идентификация туберкулезных палочек. Главный нюанс – прибор определяет наличие в мокроте только живых ДНК туберкулеза. Однако "BACTEC" рекомендуется применять для впервые выявленных больных. Хроники на этих препаратах не обследуются, поскольку специфическая микрофлора, которая развилась после предыдущего лечения, может дать ложные сигналы.

Аппарат "BACTEC", применяющийся для диагностики туберкулеза. Автор фото: биохимический анализатор
Следующей новинкой, приобретенной диспансером в начале текущего года, является микроскоп для люминесцентной микроскопии. Разрешение прибора очень высокое - чтобы увидеть туберкулезную палочку под простым микроскопом, их должно быть около 100 тысяч в одном миллилитре, здесь достаточно 10-ти тысяч. Это помогает обнаружить болезнь еще на ранних стадиях развития. Кроме этого, микроскоп универсален, он позволяет проводить исследования сразу двум показателям - по Цилю-Нильсену и люминесцентной микроскопии.

Микроскоп для люминесцентной микроскопии. Автор фото: Влада Шипилова
Если туберкулезная палочка обнаружена, необходимо как можно скорее приступить к лечению болезни.
О новом методе лечения с использованием аппарата для плазмафереза "Гемонетик" рассказал врач анестизиолог-реаниматолог противотуберкулезного диспансера Александр Русин. У пациента происходит забор крови разделение ее на плазму и эритроциты. В эритроцитарную массу вводятся протекторы и иммуномодуляторы, затем клетки крови возвращаются обратно пациенту. Используется также ультрафиолетовое облучение крови. Кровь из вены больного пропускается через аппарат с ультрафиолетовым облучателем. Проходя через лучевое воздействие, кровь возвращается обратно пациенту. Таким образом происходит обработка эритроцитов, достигается иммуностимулирующий, противовоспалительный эффект. В результате сроки лечения больных туберкулезом сокращаются на 15-20%, прекращается выделение бактерий и происходит закрытие полостей в легких после туберкулезного процесса.

Аппарат для плазмафереза "Гемонетик". Автор фото: Влада Шипилова

На примере пациентки Александр Русин рассказывает о новой методике лечения. Автор фото: Влада Шипилова
Регулярно определять изменения, которые происходят в результате болезни, помогает биохимический анализатор - новый аппарат, работающий по методу сухой химии. По словам . заведующего лабораторией Владимира Матюхина, главная особенность его заключается в том, что все процессы происходят полностью автоматически, абсолютно исключено влияние человека. Поскольку у больного необходимо регулярно брать биохимические пробы крови, вручную это занимает полтора-два часа, для других биохимических анализаторов требуется 20 минут. Аппарат "VITROS" выдает первые результаты уже через 5-7 минут. В анализатор вставляются готовые образцы с кровью, мочой или спинномозговой жидкостью. Далее аппарат сам отделяет нужные фракции и проводит анализы. Результаты сразу распечатываются на бумаге. Поскольку полностью отсутствует человеческий фактор, точность анализов очень высока. С начала года с помощью биохимического анализатора было проведено около тысячи исследований.

Биохимический анализатор. Автор фото: Влада Шипилова
Благодаря современному оборудованию и новым методикам лечения Сахалинская область является одной из самых благополучных в Дальневосточном федеральном округе по ситуации с туберкулезом.
Читайте также:


