Новейшие исследования в туберкулезе

Светлана Тoмасова, лабораторный специалист ТБ проекта ПРООН, финансируемым Глобальным Фондом
ПРООН: Что такое ежегодная конференция Международного союза по борьбе с туберкулезом и болезнями легких?
Г-жа Томасова: Ежегодная конференция Международного союза по борьбе с туберкулезом и болезнями легких, является крупнейшим в мире собранием врачей, руководителей программ здравоохранения, исследователей и активистов, работающих над тем, чтобы положить конец страданиям, вызванным заболеваниями легких, прежде всего туберкулеза. Первая международная конференция по туберкулезу была проведена в Париже в 1920 году.
ПРООН: Как проходила конференция в 2017 году?
Г-жа Томасова: В этом году конференция прошла с 11 по 14 октября 2017 г. в городе Гваделахара, Мексика. Всемирная конференция Союза привлекла делегатов из более чем 125 стран. На конференции обсуждались вопросы биобезопасности, новые схемы и режимы лечения, поддержка пациентов, внедрение новых лабораторных методов диагностики туберкулеза и многое другое.
Хотелось бы отметить, что на конференции в 2017 году Всемирный Лекарственный Фонд (Global Drug Facility), который поставляет лекарства для лечения туберкулеза, наградил Туркменистан за лидерство в планировании закупок противотуберкулезных препаратов. Об этом ПРООН готовит отдельный пресс-релиз.
ПРООН: Какие новшества в диагностике туберкулеза были представлены?
Г-жа Томасова: Что касается диагностики туберкулеза, то я остановлюсь на трех новшествах, представленных на конференции.
Были представлены новые картриджи для аппаратов молекулярной диагностики – Дженэксперт. Такие аппараты есть в Туркменистане в Дирекции Центров Инфекционных болезней и всех велаятских противотуберкулезных лабораториях. Это самое современное, точное и быстрое средство диагностики туберкулеза. Новые картриджи Ultra сократят время постановки диагноза со 110 мин до 80 мин. Если для обнаружения бактерии туберкулеза с обычными картриджами Дженэксперт необходимо 114 микобактерий в одном миллилитре мокроты, то с картриджами Ultra достаточно всего 16 микобактерий. Из-за повышенной чувствительности Ultra, анализ позволит выявить туберкулез у пациентов с трудно-выявляемыми формами, а также у детей.
Также в настоящее время проходит испытание система Дженэксперт Omni, которая позволяет использовать специальные мобильные аппараты Дженэксперт через подключение блютуз, то есть можно делать анализы в полевых условиях, например, в самых отдаленных местах. Преимуществами является небольшой размер, портативность, низкое энергопотребление, встроенная батарея. Результаты тестирования загружаются в безопасную базу данных с мобильного устройства и могут быть доступны через другое устройство.
Третье новшество, представленное на конференции, касается улучшения транспортировки мокроты. Во всех странах есть проблемы с доставкой мокроты пациентов в лабораторию. В странах с жарким климатом, как у нас, при этом необходимо обеспечить холодовой режим во время доставки мокроты, иначе бактерии туберкулеза погибают, и может быть ошибка в диагнозе. Все наши поликлиники обеспечены сумками-холодильниками. Однако сейчас появляются инновации и в этой области. Например, созданы реагенты, которые добавляются в мокроту и консервируют ее. На конференции был представлен один из таких реактивов - OMNIgene®. Он значительно упрощает сбор и транспортировку мокроты, и позволяет сохранить выживаемость бактерий до 8 дней при температурах окружающей среды даже 40 градусов.
Все эти новшества, представленные на конференции, пока проходят испытания, и говорить об их широком применении в практике рано.
ПРООН: Какие новые методы исследования внедряются в диагностику заболевания в Туркменистане?
Г-жа Томасова: В настоящее время, благодаря усилиям нашего Правительства, в Туркменистане проводятся самые современные методы лабораторной диагностики, рекомендованные Всемирной организацией здравоохранения. Все эти методы доступны не только в Ашхабаде, но и в велаятах. Помимо методики Дженэксперт, четыре лаборатории выполняют молекулярно-генетическое тестирование методом HAIN, а также автоматизированные исследования на аппаратах BACTEC MGIT 960, которые позволяют определить чувствительность к противотуберкулезным препаратам первого и второго ряда. Диагноз туберкулеза ставится в течение одного дня. Централизованная лаборатория Центров инфекционных болезней в Ашхабаде проходит ежегодный контроль качества от Супра-национальной лаборатории, которая находится в Германии.
40 лет назад считалось, что до полной победы над туберкулезом осталось совсем немного. Масштабная вакцинация и широкое применение таких эффективных антибиотиков, как изониазид и рифампицин, вселяли надежду. Однако уже в начале 1990-х появились штаммы туберкулеза, устойчивые к имеющимся лекарствам, и эта болезнь снова стала глобальной угрозой. Сегодня она, согласно докладу ВОЗ за 2018 год, в списке десяти главных причин смерти людей в мире.
В зоне высокого риска
Если же проанализировать статистику по смертности от одного определенного возбудителя инфекции, то туберкулез и вовсе лидер. Он уносит больше жизней, чем ВИЧ/СПИД. В 2017 году он него умерли 1,3 млн человек, тогда как от ВИЧ/СПИД — 300 тыс. больных.
Согласно данным ВОЗ, около 10 млн людей в 2017 году поставили диагноз "туберкулез". И эти цифры могут вырасти, ведь, согласно оценкам ВОЗ, около 1,7 млрд человек или 23% населения планеты живут с латентной туберкулезной инфекцией. А значит, почти у каждого четвертого человека в определенный момент может развиться активная форма заболевания.
"В зоне высокого риска Россия, Индия и Китай. В 2018 году именно в этих странах была зарегистрирована почти половина случаев первичного заражения штаммами туберкулеза, устойчивыми к изониазиду и рифампицину. Лекарственно резистентный туберкулез отличается быстрым прогрессом и тяжелым течением болезни, часто приводит к патологическим процессам, поэтому ВОЗ уделяет особое внимание его распространению. А в Сибири и на Дальнем Востоке ситуация хуже, чем в остальных регионах России. И заболеваемость туберкулезом, и распространенность резистентных форм здесь в два раза выше, чем в среднем по стране", — поясняет Елена Уфимцева, кандидат биологических наук, старший научный сотрудник лаборатории медицинской биотехнологии НИИ биохимии Федерального исследовательского центра фундаментальной и трансляционной медицины (ФИЦ ФТМ).

Угроза настолько серьезна, что ее нельзя игнорировать. Выступая в ноябре 2017 года на Первой глобальной министерской конференции ВОЗ "Ликвидировать туберкулез", президент России призвал делегатов объединить усилия и вместе разработать эффективные средства диагностики и лечения.
Результаты совместной работы сотрудников НИИ биохимии ФИЦ ФТМ в Новосибирске и Уральского НИИ фтизиопульмонологии уже доказали, что этот подход плодотворен. Впервые получив живые клетки с возбудителями туберкулеза из тканей легкого человека, они разработали методики, которые перевернули традиционные представления о диагностике и лечении смертельно опасной болезни.
Пленных — брать
Чтобы понять, как работают новые методики, нужно разобраться в механизме возникновения заболевания. Туберкулез вызывает патогенный микроорганизм Mycobacterium tuberculosis, который далекие от медицины люди знают под названием "палочка Коха". В человека она попадет воздушно-капельным путем.
В легких человека ее встречают особые клетки — альвеолярные макрофаги, чья главная задача — защищать органы дыхания от микробов и всех других чужеродных агентов, способных нанести им вред. Это первый защитный барьер на пути любой инфекции. Однако палочки Коха макрофагам удается победить далеко не всегда.
"Заболеет человек туберкулезом или нет, зависит от того, справятся ли макрофаги в его легких с возбудителями туберкулеза. Каждый раз ход дальнейшего развития инфекции зависит именно от этого. Если макрофаги сумеют захватить и уничтожить микобактерии, человеку ничто не угрожает. Однако в процессе долгой эволюции, которую возбудители туберкулеза прошли вместе с человеком, они выработали механизмы, помогающие им подавлять бактерицидную функцию макрофагов", — поясняет Наталья Еремеева, кандидат биологических наук, старший научный сотрудник Уральского НИИ фтизиопульмонологии Минздрава РФ.
Если инфекция преодолеет первый защитный барьер, микобактерии проникают внутрь макрофагов и колонизируют их. При этом палочки Коха могут годами и даже десятилетиями жить внутри клеток-хозяев и не размножаться.
Это и есть латентная туберкулезная инфекция, которая, по оценкам ВОЗ, есть у четверти населения земного шара. А потом микобактерии могут внезапно активизироваться, и человек заболевает. Поэтому так важно оценить содержание палочки Коха в макрофагах и их функциональное состояние в легких конкретного человека.

"К сожалению, пока об этом известно мало. Исследования взаимоотношений микобактерий туберкулеза с клетками-хозяевами проводятся в основном при инфицировании лабораторными штаммами микобактерий клеток постоянных, то есть трансформированных раковых, клеточных линий, или клеток, полученных из организмов мыши и человека, — как правило, из крови. Однако понятно, что нельзя считать полученные данные реальной картиной патогенеза туберкулезной инфекции в легких того или иного человека. Необходимы новые подходы к изучению механизма заболевания", — убеждена Елена Уфимцева.
Захватить врага живьем
В клинике Уральского НИИ фтизиопульмонологии каждый день проводят несколько операций по удалению у больных туберкулезом фрагментов легких, наиболее пораженных инфекцией. Елена Уфимцева предложила использовать часть удаленных тканей для выделения альвеолярных макрофагов, зараженных возбудителями заболевания. Технологию получения и культивирования живых инфицированных клеток из воспалительных образований Уфимцева уже отработала в НИИ биохимии на лабораторных мышах.
Однако развитие инфекционного процесса при туберкулезе легких у человека и мыши существенно отличается. Поэтому Уфимцева и Еремеева разработали новую методику, позволившую впервые выделить живые мишени инфекции — макрофаги, пораженные микобактериями, из легких пациентов, которых пришлось прооперировать, поскольку лекарственная терапия не дала результатов.
"Мы начали совместную работу в августе 2014 года, а в июле 2016 года получили первый патент Российской Федерации на изобретение "Способ получения ex vivo культур альвеолярных макрофагов из операционного материала больных туберкулезом легких и способ оценки вирулентности (вирулентность — способность заражать организм человека — прим. ТАСС) Mycobacterium tuberculosis с использованием полученных ex vivo культур альвеолярных макрофагов", — рассказывает Елена Уфимцева.
Если не вдаваться в детали, запатентованная технология выглядит так: когда в операционной удаляют фрагменты легких, пораженных туберкулезом, часть тканей тут же направляется в микробиологическую лабораторию. Там их обрабатывают в стерильных условиях, выделяя иммунные клетки, которые помещают в лунки планшета с питательной средой.

"Менее чем за сутки макрофаги прикрепляются ко дну лунки, образуя одинарный слой клеток, — продолжает рассказ Елена Уфимцева. — Через 16–18 часов, когда прооперированный пациент еще лежит в реанимации, мы уже получаем клеточные культуры, которые можно исследовать под микроскопом. Мы имеем возможность оценить, в какой степени макрофаги инфицированы микобактериями, каково функциональное состояние возбудителя заболевания и самих клеток-хозяев, а также насколько вирулентны бактерии в легких пациента, больного туберкулезом, на момент проведения операции".
Чем более вирулентны микобактерии, тем опаснее они не только для самого больного, но и для окружающих. "Оценка вирулентности важна не только для продолжения лечения пациента, но и для врачей. Они должны знать, какие пациенты инфицированы высоковирулентыми микобактериями, чтобы не заразиться самим, предотвратить распространение возбудителя болезни и не допустить эпидемии", — подчеркивает Елена Уфимцева.
Игра на опережение
Ни один из методов диагностики, использующихся сейчас в клинических лабораториях противотуберкулезной системы Минздрава РФ, не способен дать подобные результаты за столь короткий срок. Согласно принятой медицинской практике, после плановых операций часть удаленных у пациента тканей направляется для проведения анализов — гистологического, бактериологического и ПЦР.
Их задача — оценить, есть ли в тканях ДНК микобактерий и произошли ли в них мутации, вызывающие устойчивость к противотуберкулезным препаратам. А чтобы определить вирулентность возбудителя туберкулеза, патогенами, полученными из организма больного, заражают морских свинок.
"Многие из этих методов очень трудоемки, а главное, результата обычно приходится ждать очень долго — от одного до трех месяцев, — говорит Елена Уфимцева. — А разработанная нами методика позволяет оценить зараженность микобактериями в первый же день после операции".
В клинике Уральского НИИ фтизиопульмонологии также проводятся все анализы, предусмотренные протоколом, утвержденным Минздравом РФ. Елена Уфимцева и Наталья Еремеева уже исследовали ткани из легких 30 пациентов. Одновременно проводились стандартные исследования этих же фрагментов. И каждый раз авторы новой методики получали результаты намного быстрее, чем позволяют обычные методы.

Новая методика превосходит традиционные методы не только по скорости, но и по результативности. У одного из прооперированных пациентов исследовали на микобактерии ткани легкого, удаленные от основных очагов туберкулезной инфекции — каверн и туберкулем.
Гистологический анализ, на который ушла неделя, вообще не выявил микобактерий в макрофагах в этих участках. Бактериологический анализ через два месяца показал, что возбудитель заболевания не растет и не образует колонии в лабораторных условиях.
А исследовательницы из Сибири и Урала всего за 18 часов определили, что в этих тканях легкого заражены более 3% клеток-защитников и почти в половине этих клеток микобактерии уже образовали колонии. Были и другие случаи, когда методика Еремеевой-Уфимцевой позволяла найти пораженные клетки там, где их не находили традиционные исследования.

"Так мы убедились: методы, использующиеся сейчас в клинических лабораториях, не позволяют точно оценить ни зараженность клеток легких возбудителем заболевания, ни функциональное состояние микобактерий и самих клеток-хозяев в прооперированных легких пациентов," — резюмирует Елена Уфимцева.
Убить, но не навредить
Скорость и результативность — далеко не основные преимущества новой методики. Ее главное достоинство в том, что она позволяет получить из легких пациентов, больных туберкулезом, живые клетки, инфицированные микобактериями.
Взаимодействие возбудителя заболевания и клетки-хозяина исследуют в искусственной среде в сроки, наиболее приближенные к их нахождению в организме больного. Поэтому результаты изучения поведения клеток-защитников и заражающих их микобактерий настолько же достоверны, как если бы они продолжали оставаться в легких пациентов.
"А значит, можно провести персонифицированную оценку ситуации, что не позволяет сделать ни один из использующихся сейчас методов диагностики, — поясняет Наталья Еремеева. — Если через два-три дня культивирования вне организма пациента количество микобактерий внутри макрофагов начинает увеличиваться, можно сделать вывод: туберкулезный процесс может прогрессировать".
Когда проведенное ранее лечение не помогло уничтожить возбудителя заболевания, крайне необходимо корректировать лекарственную терапию. Ведь, если не подобрать эффективный препарат, риск рецидива после операции резко повысится.
"Внутри макрофагов бактерии надежно защищены от внешнего воздействия, поэтому далеко не каждый антибиотик способен их уничтожить. А теперь мы имеем возможность прямо в лаборатории протестировать различные препараты и оценить, способны ли они справиться именно с теми штаммами микобактерий, которые стали причиной туберкулеза у прооперированного пациента", — подчеркивает Наталья Еремеева.
"Методы тестирования противотуберкулезных препаратов, которые используются обычно, занимают много месяцев. Но главное, чтобы их провести, нужно обязательно получить чистые изоляты микобактерий из тканей легких пациентов в лабораторных условиях. Однако существует так называемый "феномен некультурабельности микобактерий туберкулеза": изоляты удается получить лишь из легких единичных пациентов. Поэтому традиционные методы применимы только для ограниченного круга больных. В нашей методике подобных ограничений нет", — добавляет Елена Уфимцева.
Найти подходящий именно для данного больного антибиотик — половина дела. Не менее важно подобрать дозу, которая сможет уничтожить палочки Коха, но при этом нанесет минимум вреда ослабленному после операции организму пациента.
Новая технология позволяет за пару дней сделать и это — найти оптимальное соотношение эффективности противотуберкулезного препарата и его токсичности. Авторы методики уже получили патент РФ на изобретение "Способ оценки антимикобактериального действия противотуберкулезных препаратов с использованием биологического материала пациентов, больных туберкулезом легких".
Методики есть, а политической воли нет
Разрабатывая описанную выше методику, Елена Уфимцева и Надежда Еремеева сделали еще одно открытие.
"Исследуя ткани из легких различных пациентов, мы обнаружили, что микобактерии внутри макрофагов периодически образуют так называемые корды: выстраиваются вдоль своих длинных осей, заплетаясь в косы, — поясняет Елена Уфимцева. — Мы первыми в мире обнаружили корд-колонии микобактерий в альвеолярных макрофагах из легких пациентов, больных туберкулезом. Раньше такой рост в кордах иногда фиксировали, но лишь в лабораторных условиях при размножении штаммов микобактерий на плотных питательных средах. Феномен объясняли повышенной вирулентностью патогена. Мы связали появление корд-колоний в макрофагах с повышенной вирулентностью микобактерий, инфицирующих легкие больного туберкулезом".
Новая методика позволяет обнаружить корд-колонии тоже всего за 16–18 часов. Сразу же можно сделать вывод: микобактерии в легких больного отличаются повышенной вирулентностью. А как уже говорилось, чем раньше удастся это установить, тем легче предотвратить распространение возбудителя туберкулеза и избежать эпидемии.
"Потому так важно, что мы можем выявить корды уже на следующий день после операции. Напомню, что для анализа вирулентности на морских свинках понадобится три месяца", — подчеркивает Елена Уфимцева.
Корды из палочек Коха — это аналог бактериальных биопленок, которые наиболее устойчивы к действию антибиотиков. Даже если использовать повышенную концентрацию препарата, справиться с бактериями в таких случаях крайне сложно. Поэтому, если вовремя обнаружить корд-колонии, это позволит разработать индивидуальную стратегию лечения пациента после операции. А не допустить обострения и рецидива болезни поможет еще одна разработка сибирских и уральских исследователей.

"Проанализировав поведение микобактерий в исследованных нами тканях легких, мы разработали способ оценки рисков реактивации туберкулезного процесса после операции на легких. Мы уже получили патент на изобретение "Способ определения способности микобактерий туберкулеза к размножению в альвеолярных макрофагах пациентов, прошедших курс противотуберкулезной терапии", — рассказывает Елена Уфимцева.
Авторы инновационных разработок убеждены, что их можно быстро внедрить в медицинскую практику клиник, в которых проводят операции по удалению из легких пациентов тканей с очагами туберкулезной инфекции.
"Еще раз подчеркну, что наши методики просты в исполнении, информативны, наглядны и всего за пару дней позволяют получить результаты, которых не дают стандартные методы, которые сейчас используются в российских клиниках и финансируются государством. Необходимое оборудование для культивирования клеток, световые и флуоресцентные микроскопы во многих клинических лабораториях уже есть. А расходные материалы для выделения клеток из тканей легких стоят копейки. Даже если учитывать, что в России в год проводится примерно 10 тысяч операций по удалению пораженных туберкулезом тканей легких пациентов, сумма все равно получится не слишком большой", — говорит Уфимцева.
В наше время туберкулез — основная причина смертности прежде всего в развивающихся странах. От него умирает больше людей, чем от других инфекций, включая СПИД и заболевания, сопровождающие ВИЧ.

Пока имеются на земле трущобы, куда не проникает луч солнца, чахотка и дальше будет существовать. Солнечные лучи — смерть для бацилл туберкулеза. Я предпринял свои исследования в интересах людей. Ради этого я трудился. Надеюсь, что мои труды помогут врачам провести планомерную борьбу с этим страшным бичом человечества.

В медицине выделяют открытую и закрытую формы туберкулеза: БК+ и БК–. Открытая форма заразна, пациенты с этим диагнозом остаются в стационаре до момента исключения риска заражения здоровых людей. При открытой форме или в случаях бактериовыделения в мокроте больного обнаруживаются палочки Коха, наблюдаются некротические изменения и казеоз — туберкулезный гной.
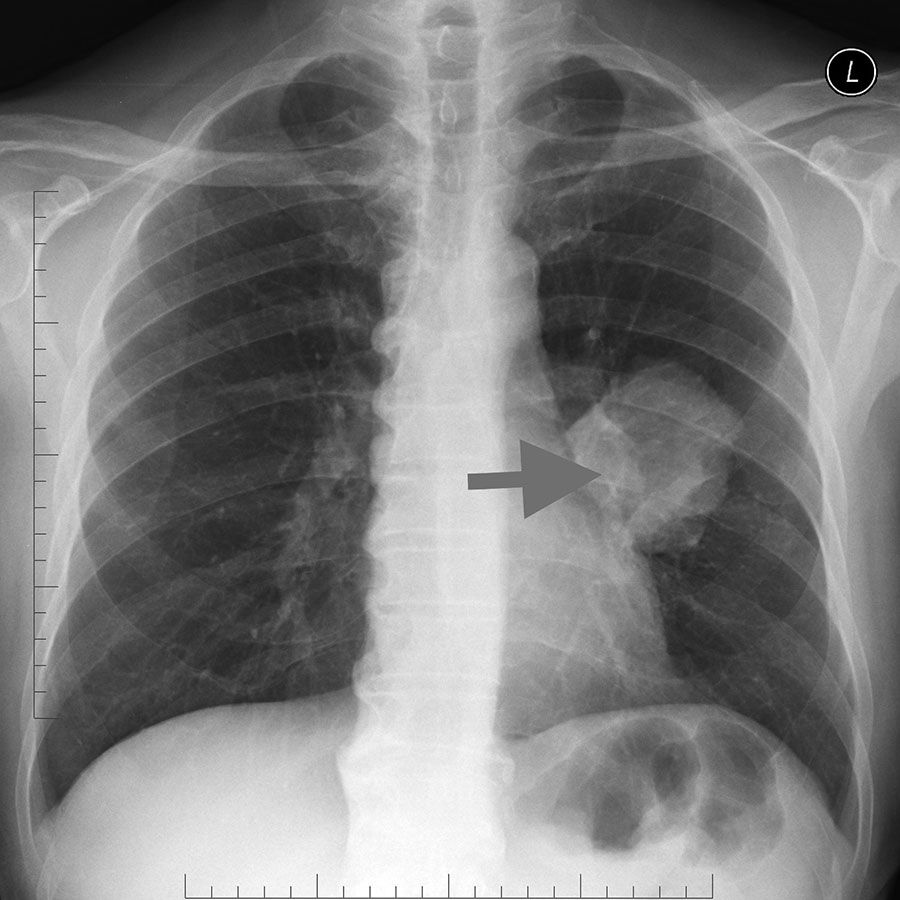
Закрытый туберкулез определить непросто, поэтому он требует специфической диагностики. Эта форма не опасна для окружающих и хорошо поддается лечению при своевременном обнаружении. При открытой форме люди всегда жалуются на кашель, повышение температуры, слабость и потливость. Возможно кровохарканье. Открытая форма туберкулеза может быть вылечена при строгом соблюдении рекомендаций врача и своевременном начале лечения.
Благодаря Коху туберкулез из смертоносной чахотки превратился в хроническую болезнь, с которой, даже заразившись, при применении терапии и мониторинге заболевания с помощью флюорографии грудной клетки можно прожить долго. Изначально спектр диагностики туберкулеза включал в себя поиск непосредственно самого возбудителя микроскопией мазка мокроты и определением специфических противотуберкулезных антител в крови. Сегодня существуют различные современные, высокотехнологичные методы. Например, метод генетической идентификации микобактерий туберкулеза.
Секвенирование в основном используется в научных исследованиях, так как для практического применения в клинических лабораториях эта технология сложна. Кроме того, стоит такая методика дорого, а результаты могут быть ложными.
Разнообразие форм устойчивости и наличие штаммов, резистентных одновременно к нескольким препаратам, требуют развития технологий мультианализа микобактерий туберкулеза на биочипах для ускоренного обнаружения возбудителя и определения его устойчивости к антибиотикам как первого, так и второго ряда в одном анализе. Мультиплексный анализ на биочипах выявляет десятки, сотни и даже тысячи видоспецифичных генетических последовательностей, а также генетических вариаций, определяющих резистентность микобактерий к антибактериальной терапии.
Туберкулез поражает преимущественно взрослых людей в их самые продуктивные годы. Однако риску подвергаются все возрастные группы. Более 95% случаев заболевания и смерти приходится на развивающиеся страны.
У людей, инфицированных ВИЧ, вероятность развития активной формы туберкулеза возрастает в 20–30 раз. Более высокому риску развития активного туберкулеза также подвергаются люди, страдающие от других нарушений здоровья, ослабляющих иммунную систему.
В 2017 году 1 млн детей (0–14 лет) заболели туберкулезом, 230 тыс. детей (включая детей с ВИЧ-ассоциированным туберкулезом) умерли от этой болезни.
Употребление табака тоже значительно повышает риск заболевания и летального исхода. 7,9% случаев инфицирования связаны именно с курением.
В 2017 году наибольшее число новых заболевших туберкулезом пришлось на регионы Юго-Восточной Азии и западной части Тихого океана — 62%. Далее следует Африканский регион, где было зарегистрировано 25% новых случаев. 87% заболевших проживают в 30 странах с тяжелым бременем туберкулеза. На долю восьми стран — Индии, Китая, Индонезии, Филиппин, Пакистана, Нигерии, Бангладеш и Южной Африки — пришлось две трети новых случаев заболевания туберкулезом.
Сегодня на рассмотрении в российском правительстве находится проект Государственной стратегии ликвидации туберкулеза к 2030 году. Никто не надеется, что к этому времени вообще не будет больных, речь идет о том, чтобы проблема перестала быть глобальной, объясняют специалисты. Особенно в свете проблем, с которыми столкнулись фтизиатры — множественной лекарственной устойчивостью микобактерий туберкулеза (МЛУ) и его сочетанием с ВИЧ-инфекцией.
Рост МЛУ — общемировая проблема. Если в 2009 году среди российских пациентов, выделяющих микробактерии туберкулеза, МЛУ-формы встречались в 10,5% случаев, то в 2017-м — уже в 54%. Среди инфицированных детей встречается в 40% случаев. Если у взрослых устойчивость развивается при нарушении назначенного режима и дозы препаратов или прерывании лечения, то дети сразу инфицируются уже резистентной к лекарствам бактерией. И если не остановить распространение МЛУ-туберкулеза от взрослых к детям, то инфицированные дети через 10–20 лет могут заболеть этой формой.
Сегодня улучшается молекулярно-генетическая диагностика заболевания, появляются быстрые (1,5–2 дня) тесты на лекарственную устойчивость возбудителя. В проекте Стратегии ставится цель охватить такими тестами до начала лечения 97% пациентов.Вторая основная проблема современной фтизиатрии связана с тем, что сегодня 21% больных, впервые попадающих на учет по туберкулезу, ВИЧ-инфицированы. И их доля продолжит расти, констатируют специалисты: у людей с вирусом иммунодефицита риск заражения туберкулезом повышен в 30–40 раз. Кроме того, медики недостаточно следят за детьми, которые родились без ВИЧ от инфицированных матерей.
Усугубляют ситуацию и антипрививочные настроения в обществе: большое число здоровых женщин, родивших здоровых детей, отказываются от их вакцинации. На сегодняшний день выписываются из роддомов с прививками лишь 80% новорожденных (необходимо 95%). В итоге среди детей до года, заболевших туберкулезом, около 41% не имели прививки БЦЖ. Всего же в прошлом году в России диагноз туберкулез был поставлен 300 детям до трех лет, 22% из них не были привиты.
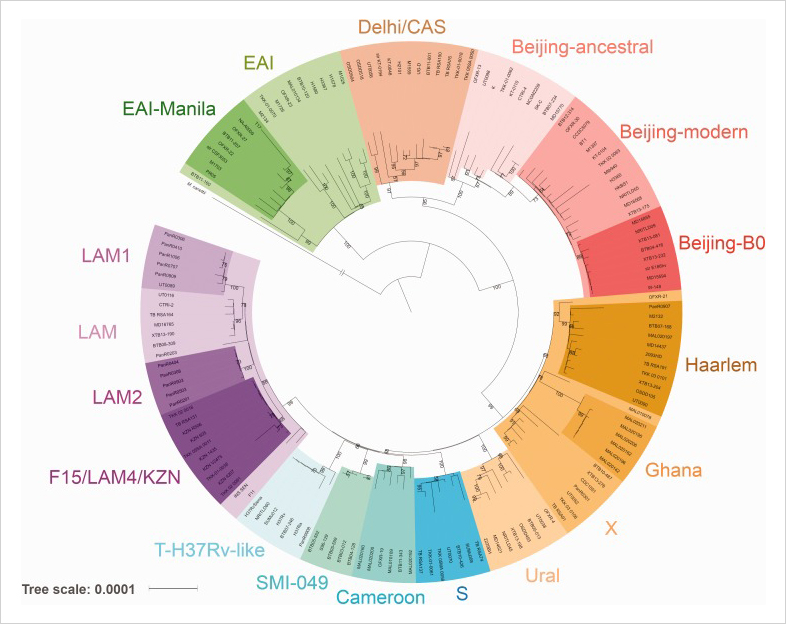
Ученые из Института общей генетики имени Н. И. Вавилова РАН и МФТИ создали каталог мутационных изменений в 319 генах вирулентности микобактерий, вызывающих туберкулез. Эти гены кодируют белки, ответственные за преодоление иммунного ответа у человека. Последующий анализ выявил набор из трех мутаций, они могут позволить микобактериям быстро развиваться в организме людей с пониженным иммунитетом. Появление новых штаммов требует иных подходов к лечению и предполагает разработку новых генно-инженерных вакцин, эффективных с точки зрения иммунного состояния конкретного пациента и особенностей вирулентности патогена.
Тест-системы позволят проводить комплексную диагностику в три этапа. Первый этап предполагает быстрый анализ мокроты для обнаружения микобактерии в течение нескольких минут с использованием специфических антител, меченных наночастицами золота. Для подтверждения положительных результатов будет разработана тест-система на основе биочип-картриджа, сочетающего мультианализ на биочипе и флюидные технологии. В качестве специфических реагентов для определения специфического паттерна антител пациента будут использованы белковые маркеры-антигены. Для третьего этапа диагностики разработают молекулярно-генетические методы обнаружения генетических маркеров лекарственной устойчивости микобактерий на основе мультианализа на биочипах.
Борьба с туберкулезом продолжается уже несколько веков. Пока он не побежден. Самым важным шагом на пути к окончательной капитуляции палочки является всеобщая вакцинация. Но, учитывая вышеупомянутые мутации вируса, каждому здоровому человеку следует проходить рентгенологическое исследование грудной клетки один раз в два года. Флюорография в системе профилактики позволяет начать лечение на ранних этапах заболевания, что является важным условием успешности борьбы с туберкулезом.
Читайте также:


