Влияние хламидийной инфекции на плод

Урогенитальная хламидийная инфекция – одна из наиболее распространенных форм инфекций, передаваемых половым путем, которая вызывается первичным патогеном человека – Chlamydia trachomatis. Заболевание привлекает внимание не только дерматовенерологов, но и акушеров-гинекологов. Объясняется это тем, что хламидии относятся к одной из самых частых причин уретритов и эндоцервицитов у женщин, восходящих воспалительных процессов мочеполовых органов, перигепатитов, поражения прямой кишки и других патологических состояний.
По данным литературы, частота обнаружения C. trachomatis среди женщин репродуктивного возраста в среднем составляет 2-11% [1; 2]. В Европе на сегодняшний день она является самой частой бактериальной инфекцией, передающейся половым путем [3]. По данным ВОЗ, частота обнаружения C. trachomatis у беременных колеблется в пределах от 2% до 37%, в среднем составляя 7%, и достигает 70% у пациенток с хроническими воспалительными заболеваниями органов малого таза [1; 2; 4].
Последние исследования, включающие скрининг экстрагенитальных участков беременных, являются новой практикой во многих странах [4; 5]. Подобная практика, подчеркивая распространенность хламидийной инфекции в ротоглотке и прямой кишке женщин, позволяет судить о гораздо большем количестве беременных, зараженных данной инфекцией. При этом у беременных женщин, которые занимаются оральным и анальным сексом, ротоглотка и прямая кишка служат скрытыми резервуарами для передачи инфекции [5].
Данные о влиянии Chlamydia trachomatis на течение и исход беременности противоречивы. Результаты некоторых рандомизированных контролируемых исследований (РКИ) указывают на то, что наличие урогенитальной хламидийной инфекции половых путей у матери может приводить к повышению частоты случаев невынашивания беременности, мертворождений, неонатальной пневмонии, преждевременных родов, преждевременного разрыва плодных оболочек, к развитию эндометрита и сальпингита в послеродовом периоде, а также к рождению детей с низкой массой тела [1; 2]. В других исследованиях связь хламидийной инфекции с неблагоприятными исходами беременности не была доказана [3].
Учитывая высокую частоту инфицирования C. trachomatis у беременных и значение данного патогена в развитии возможных осложнений у матери и плода, целесообразность антибактериальной терапии хламидийной инфекции в период беременности в настоящее время не вызывает сомнений.
Лечение беременных, больных урогенитальной хламидийной инфекцией, осуществляется акушерами-гинекологами (или дерматовенерологами при участии акушеров-гинекологов) на любом сроке беременности антибактериальными препаратами с учетом их влияния на плод. Однако вопросы, связанные со сложным выбором препаратов в терапии данного контингента больных, продолжают привлекать внимание научных исследователей, оставаясь важной медико-социальной проблемой [6; 7].
Европейское агентство по оценке лекарственных средств (англ. European Medicines Agency (EMEA)) в настоящее время наметило конкретные требования к критериям отбора лекарственных средств, для которых необходим активный эпидемиологический надзор во время беременности, руководство по мониторингу случайного или предполагаемого воздействия лекарственных препаратов во время беременности и конкретные требования к отчетности и представлению данных о неблагоприятных исходах их воздействия во время беременности [8].
В России подобных требований нет, напротив, различные стандарты лечения и клинические рекомендации порой противоречат не только зарубежным руководствам, но и друг другу. Так, например, в последних отечественных клинических рекомендациях дерматовенерологов (2015) есть ряд нарушений в разделе лечения хламидийной инфекции, которые не соответствуют мировым стандартам [9].
В связи с вышеизложенным считаем важным выяснить, какой из препаратов по факту сегодня чаще всего назначают в лечении хламидийной инфекции беременных практикующие акушеры-гинекологи, каких рекомендаций придерживаются и оправдан ли их выбор.
Проанализировать обоснованность выбора акушерами-гинекологами отдельных антибактериальных препаратов в терапии урогенитальной хламидийной инфекции у беременных женщин.
Материалы и методы исследования
Нами был проведен ретроспективный анализ 210 историй болезней (родов) беременных женщин с сопутствующим диагнозом: урогенитальная хламидийная инфекция. Все женщины в течение последних трёх лет находились на стационарном лечении в отделениях патологии беременности краевого клинического перинатального центра и различных других государственных медицинских учреждений г. Ставрополя.
Большинство женщин относилось к возрастной группе от 22 до 35 лет.
Во всех случаях (согласно медицинской документации) диагноз хламидийной инфекции был установлен женщинам на основании лабораторной диагностики. При этиологическом обследовании использовались ПЦР, ПЦР Real Time. Проводились и культуральные исследования для определения Tr. vaginalis и N. gonorrhoeae.
Контрольная ПЦР-диагностика проводилась спустя месяц после окончания терапии.
Статистическую обработку результатов проводили на персональном компьютере с помощью пакета прикладных программ StatSoft Statistica v10 Russian Portable 10.0.1011.0x86.
Результаты и обсуждение
Согласно проведённому анализу медицинской документации у 83 беременных (39,5%) отмечалось отсутствие субъективных симптомов заболевания, в то время как в остальных 127 случаях (60,5%) пациентки предъявляли жалобы на выделения из влагалища, зуд, жжение и дискомфорт в области наружных половых органов.
Из 127 женщин с жалобами на выделения хламидийный цервицит был описан у 103 (81,1%), при этом его клиническая картина чаще была представлена в виде незначительных выделений слизистого характера из канала шейки матки, иногда слизисто-гнойных, сопровождаемых умеренными выделениями из влагалища. Шейка матки у всех была гиперемирована, отечна. У 78 (61,4%) беременных цервицит сочетался с уретритом, поражением парауретральных желез или дизурией. У части женщин наблюдалось обострение процесса: повышалась температура тела до 38-39 °С, наступал озноб.
Во всех случаях терапия, направленная на лечение урогенитальной хламидийной инфекции, была проведена женщинам на сроках беременности больше 12 недель. Международные наименования оригинальных антибактериальных препаратов в зависимости от частоты их назначаемости акушерами-гинекологами отражены на рисунке 1.
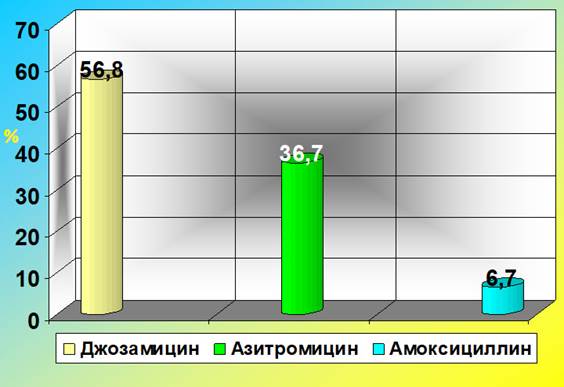
Рис. 1. Выбор акушерами-гинекологами препаратов для лечения хламидийной инфекции у беременных (2015-2017 гг.)
Как видно из рисунка, в 119 из 210 случаев (56,8%) терапия урогенитальной хламидийной инфекции у беременных проводилась джозамицином. Его назначали в дозировке 500 мг 3 раза в день в течение 10 дней. В 77 случаях (36,7%) препаратом выбора стал азитромицин в дозировке 1 г на однократный приём. В остальных 14 случаях (6,7%) терапия проводилась амоксициллином в дозировке 500 мг 3 раза в день 10 дней (при непереносимости макролидов).
Таким образом, по факту назначения беременным, больным урогенитальной хламидийной инфекцией, в отделениях патологии беременности на первое место вышел джозамицин. Однако оправдан ли такой выбор врачей и есть ли доказательная база данного препарата в лечении беременных с данной патологией? Мы считаем, что нет.
При назначении препарата важно учитывать силу рекомендаций (A-D) (рис. 2). Кроме того, следует помнить, что в лечении беременных рейтинг препаратов должен снижаться на одну ступень.
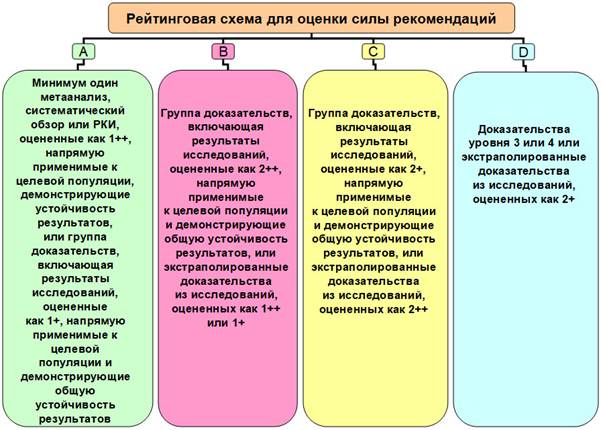
Рис. 2. Рейтинговая схема для оценки силы рекомендаций (A-D)
Согласно Европейским рекомендациям по диагностике и лечению инфекций, вызываемых Chlamydia trachomatis (2013), однократное назначение азитромицина и семидневный курс доксициклина обладают одинаковой эффективностью (класс рекомендаций А, уровень обоснованности I). Метаанализ, в который вошли 587 беременных, показал, что азитромицин, эритромицин и амоксициллин обладают одинаковой эффективностью [10]. Однако в группе, получавшей азитромицин, побочные эффекты встречались гораздо реже [10]. Следовательно, препаратом выбора при лечении урогенитальной хламидийной инфекции у беременных является азитромицин, допустимо назначение амоксициллина. Эритромицин для лечения беременных не рекомендуется. А что касается джозамицина, то он не был включен в Европейские рекомендации (2013) ни в схему выбора, ни даже в альтернативную схему лечения беременных.
Подтверждает это и Европейское руководство по борьбе с хламидийной инфекцией (2015), где азитромицин указан препаратом выбора, в то время как джозамицин также отсутствует в схемах лечения беременных [11].
Согласно руководству по лечению заболеваний, передаваемых половым путем (2015), центров по контролю и профилактике заболеваний США (Centers for Disease Control and Prevention, CDC) единственным препаратом выбора при лечении урогенитальной хламидийной инфекции у беременных является азитромицин, который считается наиболее безопасным и эффективным средством. Доксициклин не включен в схему лечения, так как, по данным этого же руководства, он противопоказан во втором и третьем триместрах беременности. К альтернативным препаратам отнесен амоксициллин, а джозамицин в США вообще не зарегистрирован [12].
1. Наиболее часто акушеры-гинекологи при лечении беременных, больных урогенитальной хламидийной инфекцией, назначают джозамицин (56,8%), на второе место по частоте назначения ими выходит азитромицин (36,7%), на третье – амоксициллин (6,7%). Вероятнее всего, это связано с тем, что у большинства практикующих врачей отсутствует осведомленность о рейтинговой схеме для оценки силы рекомендаций: А, В, С, Д, а также представление о стандартах лечения хламидийной инфекции у беременных в развитых странах.
2. Назначения препаратов акушерами-гинекологами больше всего соответствуют отечественным клиническим рекомендациям дерматовенерологов (2015). И хотя клинические рекомендации не обладают юридической силой, оставаясь лишь рекомендациями, практикующие врачи часто доверяют им, забывая, что любые возможные неблагоприятные исходы назначения тех или иных лекарственных средств будут возлагаться именно на назначающих их врачей.
- КЛЮЧЕВЫЕ СЛОВА: хламидийная инфекция, скрининг, Chlamydia trachomatis, chlamydial infection, screening, prophylaxis and treatment of chlamydiosis, antibacterial therapy
Хламидии представляют собой грамотрицательные облигатные внутриклеточные микроорганизмы, относящиеся к порядку Chlamydiales, семейству Chlamydiaceae, роду Chlamydia. Всего Chlamydia trachomatis имеет 18 сероваров, инфицирование которыми приводит к различным заболеваниям: серовары А, В, Ва, С – возбудители трахомы; D-K – урогенитального хламидиоза; L1, L2, L3 – венерической лимфогранулемы [2].
Развитие и течение хламидийной инфекции обусловлены состоянием организма, его иммунной системы, системы гомеостаза, а также свойствами возбудителя, который способен к длительной персистенции в организме хозяина.
Патофизиологические механизмы развития хламидийной инфекции на сегодняшний день изучены недостаточно. Chlamydia поражает клетки цилиндрического эпителия, причем девушки-подростки подвергаются особому риску инфицирования из-за присутствия переходной зоны между цилиндрическим и многослойным плоским эпителием на влагалищной части шейки матки.
Хламидии имеют уникальный двухфазный жизненный цикл, который адаптируется как к внутриклеточной, так и к внеклеточной среде. Формы существования хламидий включают в себя так называемые элементарные и ретикулярные (инициальные) тельца. Элементарные тельца – метаболически неактивные инфекционные частицы, функционально схожие со структурами типа спор [3]. Оказавшись внутри восприимчивой клетки-хозяина, элементарные тельца претерпевают ряд изменений: в них увеличивается количество рибосом и полирибосом, четко обнаруживается бактериальный нуклеоид, они увеличиваются в размере, появляются формы бинарного деления. Элементарные тельца, проходя стадию промежуточных телец через шесть – восемь часов после инфицирования клетки-хозяина, реорганизуются в метаболически активные неинфекционные внутриклеточные формы – ретикулярные тельца, обеспечивающие репродукцию микроба. Они делятся бинарно внутри образующейся эндосомы, которая представляет собой микроколонию и выявляется при использовании метода прямой иммунофлюоресценции как хламидийное включение. После периода роста и деления ретикулярные тельца подвергаются обратной трансформации через стадию промежуточных в элементарные тельца. Цикл развития считается завершенным после выхода из клетки инфекционных элементарных телец в результате лизиса клетки-хозяина, что позволяет элементарным тельцам вступать в новый жизненный цикл, распространяя инфекцию в еще не инфицированные клетки. При высвобождении хламидий из инфицированной клетки через узкий ободок цитоплазмы клетка может сохранять жизнеспособность. Этим можно объяснить бессимптомный характер течения инфекции [4].
Хламидии поглощаются моноцитами и распространяются в организме. Моноциты мигрируют в различные ткани (суставы, сосуды, область сердца) и становятся тканевыми макрофагами. Тканевые макрофаги могут сохранять жизнеспособность в течение нескольких месяцев, обеспечивая при этом мощную антигенную стимуляцию иммунной системы, приводящую к образованию фиброзных гранулем в здоровой ткани. Хламидии или их фрагменты вызывают образование специфических антител независимо от того, определяется ли хламидийный антиген в воротах инфекции.
Таким образом, Chlamydia trachomatis обладает способностью к персистенции, что подразумевает длительное существование хламидий без выраженного роста и размножения в состоянии равновесия с клеткой-хозяином. Доказано, что у хламидий в стадии персистенции наблюдается изменение в синтезе ключевых хламидийных антигенов: отмечается уменьшение продукции всех основных структурных компонентов, придающих особую прочность клеточной стенке [4]. На этом фоне идет непрерывный синтез белка теплового шока, который запускает вторичный иммунный ответ, что является важным моментом в иммунопатогенезе персистирующей инфекции и поддержании постоянной воспалительной реакции. Для лучшего понимания этих клеточно-опосредованных иммунных реакций необходимо проведение дальнейших исследований [5].
Взаимодействие хламидий-инфицированных клеток с системой цитокинов также играет важную роль в патогенезе инфекций, вызванных представителями Chlamydiales [6–9]. Хламидии стимулируют синтез цитокинов эпителиальными клетками организма и взаимодействия с иммунной системой [10]. Инфекция клеточных линий эпителия шейки матки и толстого кишечника индуцирует продукцию провоспалительных цитокинов: интерлейкина 8, ростозависимого онкогена альфа, фактора, стимулирующего образование колоний гранулоцитами и макрофагами, интерлейкина 6 [11].
При хламидийной инфекции цитокиновый ответ эпителия имеет отсроченный (через 20–24 часа после инфицирования) и более продолжительный (длится в течение всего жизненного цикла хламидий) характер [12].
К факторам риска инфицирования Chlamydia trachomatis относятся молодой возраст, промискуитет, воспалительные заболевания органов малого таза (ВЗОМТ) в анамнезе, пренебрежение барьерными методами контрацепции, наличие других инфекций, передаваемых половым путем, сочетание различных факторов [13, 15].
Пациенты с инфекциями, передаваемыми половым путем, находятся в группе повышенного риска по заражению еще одной инфекцией. Наиболее распространенным является сочетание хламидиоза и гонореи (у 40% женщин и 20% мужчин) [3].
Многие будущие мамы недоумевают, когда им назначают анализы на инфекции, передающиеся половым путем, среди которых значится и хламидиоз: зачем их сдавать, если ничего не беспокоит?
Однако, несмотря на отсутствие проявлений, хламидиоз может отрицательно повлиять на течение беременности, здоровье малыша и роды.

Хламидиоз – это инфекционное заболевание, вызываемое хламидиями. Это совсем обычные микроорганизмы, живущие внутри клеток. Долгое время из-за очень маленького размера их считали вирусами, затем нашли сходство с бактериями, а в настоящее время и вовсе отнесли к одноклеточным паразитам. Хламидии внедряются в клетки орга- низма человека и разрушают их. Попав однажды в организм, они способны жить в нем долгие годы, зачастую не вызывая никаких проявлений, но, тем не менее, подрывая изнутри работу легких, кишечника, суставов, мозга, глаз и других органов.
Они вызывают воспалительные реакции, ведущие к спаечным процессам и истощению иммунной системы. Примерно в половине случаев хламидиоз про- текает бессимптомно, но довольно часто он дает о себе знать болями внизу живота и воспалением канала шейки матки.
Нередко при хламидиозе ак- тивизируются другие болезнетворные микроорга- низмы: золотистый стафилококк, энтеробактерии, грибковая флора, что вызывает различные, часто гноевидные выделения из половых органов.
• полимеразная цепная реакция (ПЦР) является наиболее чув- ствительным методом диагностики заболевания – взятый на анализ материал сканируется на наличие ДНК хламидии. При этом возможно исследование целого семейства хламидий, а не одного вида. Поэтому перед анализом важно узнать, покажет ли исследование тех хламидий, которые вызывают орнитоз и другие болезни, передающиеся от птиц и животных;
• иммуноферментный метод (определение антител в крови);
• иммунофлюоресцентный метод (исследование соскоба под флуо- ресцентным микроскопом с обнаружением антигена хламидий);
• посев на культуре клеток (взятый материал размещают в особой среде и через несколько дней смотрят, есть ли хламидии) и не- которые другие методы.
На этот счет у специалистов единого мнения нет. Одни считают, что последствия этой инфекции ми- нимальны за счет работы фетоплацентарного ба- рьера, защищающего малыша от болезнетворных агентов, другие – что возможны очень серьезные нарушения. Например, развитие плацентарной не- достаточности, когда плацента не справляется со своей работой и плод не получает достаточного количества кислорода и питательных веществ. Помимо этого, хламидиоз может привести к преждевременному излитию околоплодных вод и слабости родовой деятельности.
Во время беременности обследование на хламидиоз не является обязательным, но будущим ма- мам с воспалительными заболеваниями половых органов, особенно в сочетании с проблемами в мочеполовой системе, его рекомендуется прой- ти. Также необходимо оно женщинам с невына- шиванием (предшествующими выкидышами), у которых были внематочные беременности и пре- ждевременные роды.
Если у будущей мамы найден хламидиоз, то требует- ся обязательное его лечение. Хронический хламиди- оз (в крови обнаружены антитела типа G) лечат в 20 и 30 недель беременности. Если же процесс острый (в крови обнаружены антитела типа М), лечение на- значают после 12 недель беременности.
Для борьбы с хламидиями используют антибиотики, разре- шенные для беременных женщин. Также врач может назначить препараты для поддержания иммунитета.
Мало кто знает, что хламидиоз передается не только половым путем. Существует множество видов хламидий, поражающих практически всех животных, птиц, рыб, амфибий, рептилий, мол- люсков и даже насекомых, и многие из этих воз- будителей передаются человеку, вызывая пнев- монии, бронхиты, болезни желудочно-кишечного тракта, глаз, рождение ослабленных деток и даже прерывание беременности. И неважно, под ка- ким названием скрывается хламидиоз: псит- такоз, орнитоз, попугайная болезнь или что-то иное.
Птицы, в част- ности, городские голуби, разносят заболевание буквально по всему свету. В организм человека инфекция проникает через дыхательные пути или рот. Очень часто хламидии ютятся на частичках пыли, с которыми и путешествуют по миру, ища но- вых хозяев.
Очень быстро хламидии проникают в кровь, вызывая симптомы общей интоксикации и поражение различных органов – легких, печени, селезенки, нервной системы и матки. При воз- никновении заболевания у беременной женщи- ны внутриутробного заражения малыша не про- исходит и пороков развития у него не возникает.
Однако болезнь может осложнить течение бере- менности. Тяжелые формы орнитоза, особенно в первые месяцы беременности, могут привести к ее самопроизвольному прерыванию. Кроме того, влияние на плод могут оказать антибиотики, на- значаемые для лечения, которое, кстати, прово- дят в инфекционном отделении стационара. Так что если в вашей семье есть домашний пи- томец, его диагностика на хламидиоз является важной частью спокойного протекания беремен- ности.
Для диагностики хламидиоза у животных применяются те же методы, что и для человека. А основой профилактики будет ограничение кон- тактов с домашними животными и соблюдение правил личной гигиены после общения с ними. Также надо следить, чтобы ваши питомцы не кон- тактировали с дикими и бродячими особями, не позволяйте им ловить птиц и лягушек.
Все права защищены и охраняются законом. Товарный знак №395740 от 2008 г. ООО "ШАНС БИО"
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
ММА имени И.М. Сеченова
П о данным ВОЗ, частота обнаружения Chlamydia trachomatis у беременных колеблется в очень широких пределах (от 2 до 37%), в среднем составляя 6-8% [11]. С. trachomatis передается преимущественно половым путем и обладает выраженным тропизмом к цилиндрическому эпителию. Поэтому наиболее частыми клиническими проявлениями являются уретрит и слизисто-гнойный цервицит. При распространении инфекционного процесса могут наблюдаться бартолинит, эндометрит, сальпингит, иногда проктит и некоторые другие более редкие формы заболевания [19]. Однако у 60% женщин хламидиоз протекает абсолютно бессимптомно [20].
Данные о возможном влиянии хламидийной инфекции на течение и исход беременности чрезвычайно противоречивы. Одни авторы указывают на увеличение частоты невынашивания беременности и мертворождаемости, другие категорически отрицают это [1,3,9,16]. Что не подлежит сомнению, так это тот факт, что урогенитальный хламидиоз беременных является существенным фактором риска развития хламидийной инфекции у новорожденных. Заражение происходит в 60-70% случаев, преимущественно интранатально при прохождении плода через инфицированные родовые пути. При этом у 20-50% детей, рожденных женщинами с хламидиозом, в первые две недели жизни развивается конъюнктивит, а у 10-20% на 1-3 месяц жизни хламидийная пневмония [17, 25].
В результате, учитывая высокую распространенность урогенитального хламидиоза беременных и его значительную роль в развитии осложнений у матери и плода, целесообразность антибактериальной терапии хламидийной инфекции в настоящее время не вызывает сомнений. Однако выбор препаратов для лечения инфекции, вызванной Chlamydia trachomatis, у беременных значительно ограничен, так как многие из них могут вызывать тератогенный эффект или оказывать эмбрио- и фетотоксическое действие [19].
Поскольку известны противопоказания к применению во время беременности высокоэффективных в отношении Chlamydia trachomatis антибиотиков тетрациклинового ряда и хинолонов, чаще всего для лечения беременных используется эритромицин [24]. Эффективность эритромицина достаточно высока - 83-95% [8,13]. Однако, по данным различных авторов, побочные эффекты со стороны желудочно-кишечного тракта наблюдаются у 38-58% пациенток, что нередко приводит к отказу от приема этого препарата. Кроме того, высокая курсовая доза и необходимость многократного приема значительно ограничивают применение эритромицина [5, 23].
Американский центр по профилактике и контролю за заболеваниями (CDC) рекомендует проводить начальный курс терапии эритромицином, а в качестве препарата второй линии, в случае неэффективности проведенного лечения, использовать амоксициллин [8]. Этот препарат показал себя безопасным во время беременности и эффективным для лечения хламидийной инфекции - в нескольких исследованиях он продемонстрировал эффективность 85-99% в сочетании со снижением частоты побочных эффектов (1,5-12,8% в сравнении с таковой при приеме эритромицина 23,1-31,6%) [6, 12].
Антибактериальная терапия хламидиоза у беременных
CDC, Sexually transmitted diseases, 2002
Эритромицин 500 мг х 4 раза в сутки - 7 дней перорально или амоксициллин 500 мг х 3 раза в сутки - 7 дней перорально.
Эритромицин 250 мг х 4 раза в сутки - 14 дней перорально или азитромицин 1 г однократно перорально.
Однако следует отметить, что in vitro пенициллины оказывают неполный ингибирующий эффект по отношению к Chlamydia trachomatis, в связи с чем возникает необходимость в повторном культуральном исследовании с целью установления излеченности через 3-4 недели после окончания терапии амоксициллином [22]. Кроме того, пенициллины воздействуют на жизненный цикл хламидий в фазу превращения метаболически активных ретикулярных телец в элементарные тельца, вызывая при этом образование аномальных включений с последующей продукцией белков теплового шока (HSP60). Данные вещества, в свою очередь, активируют дендритные клетки и запускают иммунологический ответ. Лечение больных пенициллинами, таким образом, не только недостаточно эффективно, но и чаще приводит к развитию синдрома Рейтера [14].
W.J. Hueston и соавт. [10], проводившие анализ по выбору антибактериальной терапии хламидийной инфекции во время беременности, считают рекомендуемую схему экономически невыгодной и приводящей к наиболее низкому уровню эффективности лечения (13,6 случаев безуспешной терапии на 1000 пролеченных пациенток). При оценке лекарственных средств с этой точки зрения авторами учитывалась общая стоимость лечения, включая затраты на культуральное исследование до и после проведения терапии, на курсовые дозы антибиотиков, а также процент случаев неудач.
Наиболее эффективной и экономичной признана следующая стратегия терапии: начальный курс амоксициллина по 500 мг три раза в сутки в течение семи дней с последующим однократным приемом азитромицина в дозе 1 г для пациенток с персистирующей хламидийной инфекцией. Уровень неизлеченности при применении данной схемы составляет 4,8 на 1000 пациенток.
Использование азитромицина представляется сейчас наиболее перспективным направлением в терапии урогенитального хламидиоза беременных. Этот антибиотик группы макролидов обладает уникальными характеристиками: высоким уровнем всасывания и устойчивостью в кислой среде, высокой концентрацией в тканях, продолжительным периодом полувыведения, возможностью проникновения внутрь клетки, где локализуется возбудитель хламидиоза, и способностью блокировать фазу превращения элементарных телец хламидий в метаболически активные ретикулярные тельца [14].
Ряд сравнительных рандомизированных исследований подтверждают высокую эффективность азитромицина при однократном пероральном приеме в дозе 1 г (97-100%), значительное снижение частоты побочных эффектов со стороны желудочно-кишечного тракта (7,4% в сравнении с таковой при использовании эритромицина 38,8%), отсутствие неблагоприятного влияния на плод [5, 23]. В многоцентровом исследовании, включавшем 347 пациенток, микробиологическая излеченность при применении азитромицина была достигнута в 97% случаев, а клиническая излеченность в 86% случаев. В то же время, по данным Stamm и соавт. [21], у 3 беременных через 5 недель после окончания терапии вновь была выделена Chlamydia trachomatis. Однако в данном случае нельзя однозначно говорить о рецидиве инфекций, так как невозможно достоверно исключить факт реинфецирования. Тем не менее, максимальная (из имеющихся в наличии в настоящее время лекарственных средств) терапевтическая и экономическая эффективность в сочетании с хорошей переносимостью, удобством применения и безопасностью позволяют рассматривать азитромицин, как препарат выбора в лечении урогенитального хламидиоза беременных.
Из макролидов, помимо эритромицина и азитромицина, для лечения хламидийной инфекции во время беременности G. Rigway [18] предлагает использовать джозамицин по 500 мг 2 раза в сутки в течение 7 дней. Данные российских ученых (Ю.К. Скрипкин и соавт. [4], Н.С. Потекаев и соавт. [2]) демонстрируют клиническую эффективность препарата от 97,2% до 100%, которая гарантируется высокой концентрацией джозамицина в тканях, а также его безопасность для беременных женщин и детей. Однако представленные исследования не являются плацебо-контролируемыми, что снижает их достоверность, а главное - малочисленность групп беременных женщин не позволяет оценить реальную безопасность этого препарата. Клинический же опыт применения джозамицина для лечения хламидиоза во время беременности весьма ограничен, поэтому немногочисленные неблагоприятные перинатальные исходы могут остаться незамеченными.
Опубликованные в последнее время отдельные сообщения об использовании в терапии урогенитальной хламидийной инфекции у беременных рокситромицина по 300 мг в сутки и кларитромицина по 250 мг 2 раза в сутки в течение 7 дней также требуют подтверждения крупномасштабными рандомизированными исследованиями с использованием значимых критериев эффективности и безопасности [18].
Ряд работ посвящен опыту применения клиндамицина для терапии урогенитального хламидиоза во время беременности. По эффективности и безопасности этот препарат сопоставим с амоксициллином. Использование клиндамицина для курса инициальной терапии с приемом азитромицина, как препарата резерва, продемонстрировало низкий уровень неизлеченности (4,2 случая на 1000 пациенток), но данная стратегия оказалась значительно более дорогой в сравнении с остальными комбинациями и потому менее целесообразной [10, 15].
Обобщенные данные по проблеме терапии хламидийной инфекции у беременных представлены в систематическом Кокрановском обзоре, включающем 11 рандомизированных контролируемых исследований по анализу сравнительной эффективности применения эритромицина, амоксициллина и азитромицина у пациенток с хламидиозом во время беременности. Показатель микробиологической излеченности, свидетельствующий о ликвидации возбудителя и об отсутствии риска заболевания новорожденного или матери, составляет около 90% для всех исследованных антибиотиков (при применении плацебо - 12%).
Препаратом первого выбора назван эритромицин. Амоксициллин и азитромицин весьма перспективны, демонстрируют большую клиническую эффективность и меньшую частоту побочных реакций в сравнении с эритромицином, однако отсутствие долгосрочных крупномасштабных рандомизированных исследований эффективности и безопасности применения этих препаратов во время беременности ограничивает их широкое внедрение в рутинную клиническую практику [7].
Приоритетным направлением фармакотерапии урогенитального хламидиоза в настоящее время является определение соответствия воздействия антибиотиков характеристикам внутриклеточного жизненного цикла хламидий. Примечательно, что Chlamydia trachomatis завершает свой цикл развития, находясь в составе вакуоли инфицированной эпителиальной клетки и оставаясь, по-видимому, недоступной для воздействия большинства клеточных и гуморальных механизмов защиты. Неизвестно, способны ли антибиотики, проникающие внутрь клеток, уничтожать хламидий в вакуолях или их бактерицидная активность направлена на элементарные тельца, высвобождающиеся при естественной гибели инфицированных клеток. В частности, нет сомнений в том, что азитромицин и рокситромицин проникают в клетки, в особенности в макрофаги, и накапливаются здесь в высоких концентрациях. Однако до сих пор не имеется убедительных доказательств того, что эти препараты обладают более выраженной внутриклеточной активностью по отношению к хламидиям, чем другие антибиотики или факторы иммунной защиты. Фармакокинетические исследования в данном направлении особенно актуальны для решения вопроса о латентной хламидийной инфекции, имеющей место примерно у 4-11% беременных и требующей более интенсивного и длительного лечения [14].
1. Евсюкова И.И., Кошелева Н.Г., Башмакова М.А., Савичева А.М. и соавт. Хламидийная инфекция в акушерстве и перинатологии (диагностика, профилактика, лечение). // СПб. -1995. С. 9.
2. Потекаев Н.С., Пашинян М.Г., Пашинян А.Г., Потекаев Н.Н. Джозамицин(вильпрафен) в терапии урогенитального хламидиоза. // Вести. Дерматол. Венерол. -2000. №1 С.48-50.
3. Савичева А.М., Башмакова М.А. Урогенитальный хламидиоз у женщин и его последствия. // Медицинская книга. Москва - 1998, С.65-87.
4. Скрипкин Ю.К., Пашинян М.Г. Лечение джозамицином больных урогенитальным хламидиозом. // Вести. Дерматол. Венерол. -2000 №2 С.49-50.
5. Adair C.D., Gunter M., Stovall T.G. et al. Chlamydia in pregnancy: a randomized trial of azithromycin and erythromycin. // Obstet.Gynecol. -1998, Feb.; 91(2): 165-168.
6. Alary M., Loey J.R., Moutquih J.M. et al. Randomized prospective study comparing erythromycin and amoxycillin in the treatment of genital chlamydial infection in pregnancy//Lancet -1994.344: 1461-1465.
7. Brocklehurst P. Update on the treatment of sexually transmitted infections in pregnancy. //Int.J.STD AIDS 1999. 10:571-580.
8. Centers for Disease Control and Prevention Guidelines for treatment of sexually transmitted diseases // MMWR -2002, v-51, N-RR-6, P.34.
9. Fiest A., Sydler Т., Gebbers S.S. et al. No association of Clamydia with abortion. //J.Soc.Med. -1999, 92(5);237-238.
10. Hueston W.J., Lenhart J.G., A decision analysis to guide antibiotic- selection for Chlamydia infection during pregnancy. // Arch.Fam.Med -1997, 6(6): 551-555.
11. Kovacs L., Nagy E., Berbik I. Et al. The frequency and the role of Chlamydia trachomatis infection in premature labor. // Int/J/Gynaecol.Obstet. 1998. 62:47-54.
12. Magat A.H., Alger L.S., Nagey D.A., Hatch C., Lavchik J.C. Double-blinded randomized study comparing amoxicillin and erythromycin for treatment of Chlamydia trachomatis in pregnancy. // Obstet.Gynecol. -1993, 81: 745-749.
13. Miller J.M., Martin D.H. Treatment of Chlamydia trachomatis infections in pregnant women. // Drugs -2000. 60(3): 597-605.
14. Morton R.S., Kinghorn G.R. Genitourinary Chlamydial infection: a reappraisal and hypothesis. // Int/J/STD AIDS 1999. 10:765-775.
15. Nuovo J., Melnikow J., Paliescheskey M., King J., Mowers R. Cost-effectiveness analysis of five different antibiotic regimens for treatment of uncomplicated Chlamydia trachomatis cervicitis. // J. Am. board. Fam.Pract. -1995,8:7-16.
16. Rastogi S., Kapur S., Salhan S. et al. Chlamydia trachomatis infection in pregnancy: Risk factor for an adverce outcome. // Brit.J.Biomed.Scien. 1999. 56:94-98.
17. Ratelle S., Keno D., Hardwood M. et al. Neonatal chlamydial infections in Massachusetts, 1992-1993//Am. J.Prev.Med. 1997. 13: 221-224.
18. Rigway G. Treatment of Chlamydia trachomatis Infections. // Abstracts of Proceeding of the 4th Meeting jf the European Society for Chlamydia research. August 2000. Helsinki, Finland. 28-32.
Читайте также:


