Спид вторичный иммунодефицит инфекционной этиологии
О ВИЧ/СПИДе. Этиология ВИЧ-инфекции. Введение.
ВИЧ-инфекция - это заболевание, вызываемое вирусом иммунодефицита человека, длительное время персистирующим в лимфоцитах, макрофагах, клетках нервной ткани, в результате чего развивается медленно прогрессирующее поражение иммунной и нервной системы, проявляющееся вторичными инфекциями, опухолями, подострым энцефалитом и другими патологическими изменениями, приводящими к гибели больного.
ВИЧ-инфекция - это смена стадий, последнюю из них обозначают термином СПИД - синдром приобретенного иммунодефицита человека, являющуюся заключительной, терминальной стадией процесса.
Возбудитель и эпидемиология ВИЧ-инфекции
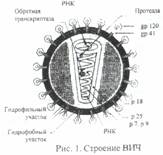
Возбудитель ВИЧ-инфекции - вирус иммунодефицита человека, принадлежит к подсемейству лентивирусов, семейства ретровирусов. Выделяют два типа вируса -ВИЧ-1 и ВИЧ-2. Вирусная частица представляет собой форму, близкую к сферической, со средним диаметром 100-120 нм, состоящую из ядра, окруженное оболочкой. Ядро содержит РНК и ферменты - обратную транскриптазу (ревертазу), интегразу, протеазу. Наличие обратной транскриптазы обеспечивает обратную направленность потока генетической информации: не от ДНК к РНК, а наоборот, от РНК к ДНК.
В составе вириона имеется оболочка и нуклеоид. Наружная оболочка пронизана вирусными белками: трансмембранным и внешним глико-протеидами. Белки выполняют функцию детерминанты и участвуют в прикреплении к мембране клетки-хозяина, С внутренней стороны оболочки расположен каркас, образованный белком р 17, окружающий внутреннюю структуру вириона - нуклеоид (сердцевина). Собственно оболочка сердцевины образована белком р 24. Внутри нуклеоида располагается геном вируса, состоящих из 2 цепочек РНК, окруженных белками р 7 и р 9 .
Жизненный цикл ВИЧ включает в себя процессы специфической сорбции вируса на CD 4(+) - лимфоцитах за счет процессов диффузии мембран, синтез ДНК копии генома и дальнейшей ее интеграции в хромосому клетки-хозяина.
При попадании ВИЧ в клетку под действием фермента обратной транскриптазы происходит образование ДНК ВИЧ, встраивающейся в ДНК клетки-хозяина, которая в дальнейшем продуцирует вирусные частицы.
ВИЧ не стоек в окружающей среде. Полностью инактивируется нагреванием при температуре 56°С в течение 30 мин, быстро погибает при кипячении (1-3 мин), а также под воздействием дезинфицирующих средств н концентрациях, обычно используемых в практике. ВИЧ в то же время устойчив к ультрафиолетовым лучам и ионизирующей радиации.
Источником заражения является человек, инфицированный ВИЧ как в стадии бессимптомного носителъства, так и развернутых клинических проявлений болезни. Вирус обнаруживается в крови, сперме, спинномозговой жидкости, грудном молоке, менструальной крови, влагалищном секрете, которые являются факторами передачи ВИЧ-инфекции. В слюне, слезной жидкости, моче ВИЧ находится в небольшом количестве, недостаточном для заражения.
Пути передачи ВИЧ-инфекции - половой (гетеро- и гомосексуальный), парентеральный и вертикальный.
Вертикальный путь передачи может быть от инфицированной матери ребенку во время беременности и родов, а также во время грудного вскармливания, возможно также заражение матери от ВИЧ-инфецированного ребенка при его вскармливании.
Патогенез ВИЧ-инфекции.
При попадании ВИЧ в клетку, РНК под воздействием ревертазы превращается в ДНК, которая встраивается в ДНК клетки-хозяина, продуцируя новые вирусные частицы - копии РНК вируса, оставаясь в клетке пожизненно. Ядро окружено оболочкой, в составе которой имеется белок g р 120, обуславливающий прикрепление вируса к клеткам организма человека, имеющим рецептор - белок CD 4 .
ВИЧ адсорбируется на клетках, в состав мембраны которых входит белок CD 4. Это Т-лимфоциты с фенотипом CD 4(+) , макрофаги, В-лимфоциты, клетки нейроглии (вследствие этого происходит поражение центральной нервной системы), клеток слизистой оболочки кишечника, дендритных клеток. Прежде всего поражаются С D 4(+)-лимфоциты, являющиеся центральной фигурой иммунного ответа. Причиной снижения Т-хелперов является не только прямое цитопатическое действие вируса, но и слияние неинфицированных клеток с инфицированными и образование синтиция.
Одновременно происходит нарушение функции В-лимфоцитов. повышается количество иммуноглобулинов, циркулирующих иммунных комплексов, что ведет к большему снижению С D 4(+) - лимфоцитов. Все перечисленные механизмы и формируют различные клинические проявления заболевания. В результате поражения центральных звеньев иммунной системы человек, инфицированный ВИЧ, становится беззащитным перед возбудителями различных инфекций, в первую очередь, условно-патогенными (оппортунистическими) микроорганизмами, которые не представляют угрозы для практически здорового человека.
В связи с прогрессированием вторичного иммунодефицитного состояния формируются опухолевые и аутоиммунные процессы, в патологический процесс всегда вовлекается ЦНС, куда проникает вирус вместе с инфицированными моноцитами. Поражение клеток нейроглии приводит к трофическим повреждениям нейронов, ткани мозга, нарушению мозговой деятельности, и в конечном итоге развитию СПИД-деменции (слабоумию).
Российская классификация ВИЧ-инфекции, 2006 год (В.В. Покровский)
Продолжительность клинических проявлений во второй стадии может варьировать от нескольких дней до нескольких месяцев, однако обычно они регистрируется в течение двух-трех недель.
В целом продолжительность стадии первичных проявлений ВИЧ-инфекции составляет один год с момента появления симптомов острой инфекции или сероконверсии.
Длительность субклинической стадии составляет от двух-трех до 20-ти и более лет, но в среднем она продолжается 6-7 лет. Скорость снижения уровня С04-лимфоцитов в этот период в среднем составляет 50-70x106/л в год.
В зависимости от тяжести вторичных заболеваний выделяют стадии 4А, 4Б, 4В.
4А обычно развивается через 6-10 лет от момента заражения. Для нее характерны бактериальные, грибковые и вирусные поражения слизистых и кожных покровов, воспалительные заболевания верхних дыхательных путей. Обычно стадия 4А развивается у пациентов с уровнем С04-лимфоцитов 500-350x106/л (у здоровых лиц число С04-лимфоцитов колеблется в пределах 600-1900x106/л).
4Б чаще возникает через 7-10 лет от момента заражения. Кожные поражения в этот период носят более глубокий характер и склонны к затяжному течению. Начинают развиваться поражения внутренних органов. Могут отмечаться потеря веса, лихорадка, локализованная саркома Капоши, поражение периферической нервной системы. Обычно стадия 4Б развивается у пациентов с уровнем С04-лимфоцитов 350-200x106/л.
4В преимущественно выявляется через 10-12 лет от момента заражения. Она характеризуется развитием тяжелых, угрожающих жизни вторичных заболеваний, их генерализованным характером, поражением ЦНС. Обычно стадия 4В имеет место при уровне С04- лимфоцитов менее 200x106/л.
Несмотря на то, что переход ВИЧ-инфекции в стадию вторичных заболеваний является проявлением истощения защитных резервов организма зараженного человека, этот процесс имеет обратимый характер (по крайней мере, на какое-то время). Спонтанно или вследствие проводимой терапии клинические проявления вторичных заболеваний могут исчезать. Поэтому в стадии вторичных заболеваний выделяют фазы прогрессирования (при отсутствии противоретровирусной терапии или на фоне противоретровирусной терапии) и ремиссии (спонтанной, после ранее проводимой противоретровирусной терапии или на фоне противоретровирусной терапии).
Т.В. Латышева, Н.Х. Сетдикова, К.С. Манько
Настоящее сообщение посвящено вторичным иммунодефицитным состояниям, анализу эффективности, безопасности и воздействия на формирования иммунного ответа отечественного иммуномодулятора галавита у больных различными заболеваниями, но имеющими либо спонтанную, либо индуцированную форму вторичной иммунной недостаточности, которая клинически проявляется хроническими, рецидивирующими инфекционно-воспалительными процессами бронхолегочного аппарата, придаточных пазух носа, урогенитального тракта, глаз, кожи, мягких тканей, вызванными оппортунистическими и условно-патогенными микроорганизмами, резистентными к этиопатогенетической терапии.
Начало развития иммунологии относится к концу XVIII в. и связано с именем Э. Дженнера, впервые применившего на основании лишь практических наблюдений метод (впоследствии обоснованный теоретически) вакцинации против натуральной оспы.
Открытый Э. Дженнером факт лег в основу дальнейших экспериментов Л. Пастера, завершившихся формулировкой принципа профилактики от инфекционных заболеваний - принцип иммунизации ослабленными или убитыми возбудителями. Многочисленные попытки выяснения механизмов, обусловливающих устойчивость организма против возбудителя, увенчались созданием двух теорий иммунитета - фагоцитарной, сформулированной в 1887 г. И.И. Мечниковым, и гуморальной, выдвинутой в 1901 г. П. Эрлихом.
Ухудшение экологической ситуации, влияние на организм неблагоприятных факторов окружающей среды привели к росту заболеваемости населения. Изменилось и клиническое течение различных заболеваний человека, увеличился процент атипичных и стертых форм инфекционных заболеваний, чаще отмечается хронизация и резистентность к общепринятым методам терапии, нередко условно-патогенные микробы становятся патогенными для человека. Одновременно с этим, по мере развития иммунологии, становится ясно, что практически все заболевания, процессы в организме в той или иной степени связаны с включением различных звеньев иммунного ответа, которые обеспечивают биологическую индивидуальность и направлены на ее сохранение. Иммунная система находится в состоянии готовности к защите внутренней среды организма от вторжения чужеродных агентов или сформировавшихся внутри организма измененных макромолекул (например, опухолевых клеток и их продуктов). Степень готовности зависит от генетической основы и особенно состояния организма на момент агрессии. Реализация защиты осуществляется через специфические и неспецифические факторы защиты, которые взаимодействуют между собой. Главной особенностью неспецифической составляющей иммунных процессов является то, что ее формирование не зависит от агрессии и является частью естественного развития организма. Неспецифический иммунный ответ включается практически немедленно после появления в организме чужеродного тела, в отличие от специфического ответа, для которого требуется определенное время.
Важную роль в неспецифическом иммунном ответе играют нейтрофилы, моноциты, макрофаги, а затем уже подключаются и лимфоциты. Активация этих клеток приводит к высвобождению медиаторов воспаления и активации ряда гуморальных систем защиты. Все это приводит к включению адаптивной реакции лимфоцитов. Антиген-специфические и неспецифические факторы действуют в тесной взаимосвязи, и их значение в формировании иммунного ответа бывает трудно разграничить [24, 25, 30].
В последнее время большое значение придается роли иммунных нарушений как системного, так и местного характера в патогенезе воспалительного процесса различной этиологии, что часто является причиной хронизации процесса и развития резистентности к общепринятой базисной терапии. Известно, что вторичный иммунодефицит (ВИД) отличается значительной гетерогенностью своего происхождения, вариабельностью нарушений показателей иммунного статуса, полиморфизмом клинических проявлений.
Основными клиническими проявлениями ВИД является развитие хронических, рецидивирующих инфекционно-воспалительных процессов бронхолегочного аппарата, придаточных пазух носа, урогенитального тракта, глаз, кожи, мягких тканей, вызванных оппортунистическими, условно-патогенными микроорганизмами и резистентными к этиопатогенетической терапии.
Результаты исследований позволяют утверждать, что иммунологическая система - важное звено в сложном механизме адаптации человеческого организма, а ее действие направленно, в первую очередь, на сохранение антигенного гомеостаза, нарушение которого может быть обусловлено проникновением в организм чужеродных антигенов (инфекция, трансплантация) или спонтанной мутацией.
Иммунодефициты - это снижение функциональной активности основных компонентов иммунной системы, ведущее к нарушению защиты организма от микробов и проявляющееся в повышенной инфекционной заболеваемости.
К первичным иммунодефицитам (ПИД) относятся врожденные нарушения иммунной системы, связанные с генетическими дефектами одного или нескольких ее компонентов, а именно - комплемента, фагоцитоза, гуморального и клеточного иммунитета.
К вторичным иммунодефицитам (ВИД) относятся нарушения иммунной системы, которые развиваются в позднем постнатальном периоде или у взрослых, и которые (как принято считать) не являются результатом какого-либо генетического дефекта.
Среди ВИД выделяют 3 формы: приобретенную (СПИД), индуцированную (имеется конкретная причина, вызвавшая их появление) и спонтанную (отсутствует явная причина, вызвавшая нарушение иммунологической реактивности).
Наиболее ярким примером приобретенной формы ВИД является синдром приобретенного иммунодефицита человека (СПИД), развивающийся в результате поражения лимфоидной ткани человека вирусом.
Индуцированная форма ВИД возникает в результате конкретных причин, вызвавших ее появление: рентгеновского излучения, цитостатической терапии, применения кортикостероидов, травм и хирургических вмешательств, а также нарушений иммунитета, развивающихся вторично по отношению к основному заболеванию (диабет, заболевание печени, почек, злокачественные новообразования). Спонтанная форма ВИД характеризуется отсутствием явной причины, вызвавшей нарушение иммунной реактивности. Клинически она проявляется в виде хронических, часто рецидивирующих инфекционно-воспалительных процессов бронхолегочного аппарата, придаточных пазух носа, урогенитального и желудочно-кишечного тракта, глаз, кожи, мягких тканей, вызванных оппортунистическими или условно-патогенными микроорганизмами.
В количественном отношении спонтанная форма является доминирующей формой ВИД.
При ВИД нарушается функция различных звеньев иммунной системы: фагоцитарного, клеточного, гуморального, системы комплемента и т. д.
В основе спонтанной формы ВИД может лежать первичная иммунологическая недостаточность какого-либо компонента иммунной системы, скомпенсированная за счет высокой активности других показателей этой системы.
По выявляемости лабораторными методами дефектов в иммунном статусе больных можно разделить на 3 группы:
1. Имеются клинические признаки нарушения иммунитета в сочетании с выявленными изменениями в параметрах иммунного статуса.
2. Имеются только клинические признаки иммунной недостаточности без конкретно выявленных изменений в параметрах иммунного статуса. Поэтому хронические, часто рецидивирующие, вялотекущие, трудно поддающиеся лечению традиционными средствами инфекционно-воспалительные процессы любой локализации у взрослых рассматриваются как ВИД состояния.
3. Имеются только изменения показателей иммунного статуса без клинических признаков иммунной недостаточности.
Исходя из данного деления пациентов на группы, можно сказать, что в первом и втором случаях необходимо введение в комплекс терапевтических мероприятий иммунотропных препаратов, в третьем же случае требуется лишь динамическое наблюдение за пациентом для возможно более раннего введения иммунотропных препаратов при появлении клинических признаков иммунодефицитного состояния.
Таким образом, иммунотерапию вообще можно разделить на активную иммунизацию (вакцинация), заместительную терапию и терапию иммунотропными препаратами. Одним из перспективных направлений является использование иммунотропных препаратов и разработка адекватных методов направленной иммунокоррекции в комплексной терапии.
Настоящее сообщение посвящено анализу эффективности, безопасности и воздействию на формирования иммунного ответа отечественного иммуномодулятора галавита у больных различными заболеваниями, но имеющими либо спонтанную, либо индуцированную форму иммунной недостаточности.
Состояние иммунной системы, как и любого другого органа (сердца, печени, легких), характеризуется комплексом морфологических, функциональных и клинических показателей, присущих иммунной системе в норме. Они-то и определяют иммунный статус. Изменение какого-либо одного или нескольких из этих показателей свидетельствует о нарушении иммунного статуса, то есть отклонении его от нормы, и трактуется как иммунодефицит. Следовательно, иммунодефицит — это изменение иммунного статуса, обусловленное дефектами одного или нескольких механизмов иммунных реакций.
Различают первичные (врожденные) и вторичные (приобретенные) иммунодефициты, а также состояния, когда сама иммунная система становится мишенью для инфекционного агента (СПИД, Т-клеточный лейкоз). Вторичные ИД встречаются гораздо чаще, чем первичные и формируются у лиц с исходно нормальной функцией иммунной системы. При вторичной иммунологической недостаточности могут поражаться Т-, В- системы иммунитета, а также факторы естественной резистентности (фагоцитоз, комплемент, интерфероны и др.), возможно сочетанное их поражение, что приводит к снижению защитных функций иммунной системы, нарушению регуляторных взаимоотношений между системами иммунитета.
Причиной развития вторичных (приобретенных) форм ИД могут быть различные факторы, наиболее часто эти формы ИД связаны:
• с вирусными инфекциями (ВИЧ-инфекция, грипп, эпидемический паротит, ветряная оспа, корь, краснуха, гепатиты острые и хронические, и др.;
• с бактериальными инфекциями (стафилококковые, стрептококковые, менингококковые, пневмококковые, сифилис, туберкулез и др.);
• с глистными и протозойными болезнями: (лейшманиоз, малярия, трихинеллез, токсоплазмоз и др.);
злокачественным новообразованиям;
• с хроническими, длительно текущими заболеваниями инфекционной и неинфекционной природы (хронические заболевания легких, мочевыводящей системы, сердечно-сосудистой системы, желудочно-кишечного тракта, системные заболевания соединительной ткани, дисбактериозы и др.);
• нарушениями питания (истощение, ожирение, микроэлементная и белковая недостаточность, авитаминозы, гиповитаминозы, нарушения всасывания и расщепления питательных веществ, длительное соблюдение строгих диет, несбалансированность питания по количественным и качественным составляющим и др.);
• влиянием химиопрепаратов, средств, оказывающих иммунодепрессивное воздействие (цитотстатики, стероидные гормоны, антибиотики, нитрофураны и т.д.);
• действием ионизирующей радиации и иммунотоксинов (в том числе ксенобиотиков); — с продолжительными стрессорными воздействиями, переутомлением;
• с патологией обмена веществ (сахарный диабет, дефицит микроэлементов, гипербилирубинемия, недостаточность карбоксилазы и др.);
• с эндокринными нарушениями (заболевания щитовидной железы, надпочечников, заболевания, связанные с нарушением центральных механизмов регуляции эндокринных функций и др.);
• травмами, операциями, ожогами и др.;
• возрастом (дети раннего возраста в связи с незрелостью иммунной системы; пожилые люди в связи с угнетением клеточных иммунных реакций, падением активности антител и др.).
Таким образом, ВИД могут возникать при действии на организм огромного числа социальных, экологических, медицинских, профессиональных и других факторов. В результате этого число ВИД среди популяции людей выражается значительными цифрами, достигающими в отдельных коллективах 80-90%.
Иммунные нарушения и клинические проявления при вторичных иммунодефицитах
По своей форме ВИД могут быть:
• Компенсипрованными. Для этой формы ВИД характерна повышенная восприимчивость к возбудителям инфекций, что выражается в виде частых ОРВИ, пневмоний, пиодермий и т.д.
• Субкомпенсированными. Для этой формы характерна склонность к хронизации инфекционных процессов, что клинически выражается в развитии хронических бронхитов, пневмоний, пиелонефритов, дуоденитов, панкреатитов, холециститов и др.
• Декомпенсированными, проявляющимися в виде развития генерализованных инфекций, этиологическим фактором развития которых является условно-патогенная микрофлора, злокачественных новообразований. Ярким примером декомпенсированной формы ВИД является СПИД.
Клинические проявления ВИД чрезвычайно разнообразны и проявляются четырьмя основными синдромами: инфекционным, аллергическим, аутоиммунным и иммунопролиферативным. Инфекционный синдром проявляется рецидивирующим характером течения острых и хронических инфекционно-воспалительных заболеваний различной этиологии и локализации, гнойно-воспалительными инфекциями, вызываемыми условно-патогенными микробами.
Аллергический синдром — аллергическими реакциями и заболеваниями.
Аутоиммунный синдром — самостоятельными аутоиммунными нозологическими формами, либо аутоиммунным компонентом на фоне длительного течения патологического процесса (поражение внутренних органов и систем организма). Иммунопролиферативный синдром — развитием опухолевого процесса, то есть злокачественных опухолей в различных органах и системах.
Учитывая многообразие и широкую распространенность факторов, которые потенциально могут привести к развитию вторичной иммунологической недостаточности, логично предположить, что каждый человек в течение своей жизни подвергается длительному воздействию тех или иных факторов или их сочетаний и подвергается реальному риску развития вторичного иммунодефицита. В связи с этим особенно в последние годы возникла реальная необходимость в рациональном иммунотропном воздействии с целью предотвращения развития и коррекции уже возникших иммунодефицитных состояний. Перечень иммуномодуляторов, зарегистрированных за рубежом и в нашей стране и применяемых в клинической практике, в настоящее время достаточно широк и составляет более 400 наименований.
Основными требованиями, предъявляемыми к иммунотропным препаратам являются:
• иммуномодулирующие свойства;
• высокая эффективность;
• естественное происхождение;
• безопасность, безвредность;
• отсутствие противопоказаний;
• отсутствие привыкания;
• отсутствие побочных эффектов;
• отсутствие канцерогенных эффектов;
• отсутствие индукции иммунопатологические реакций;
• не вызывать чрезмерной сенсибилизации и не потенцировать ее у других медикаментов;
• легко метаболизироваться и выводиться из организма;
• не вступать во взаимодействие с другими препаратами и обладать высокой совместимостью с ними;
• непарентеральные пути введения
В настоящее время выработаны и утверждены основные принципы иммунотерапии:
• Обязательное определение иммунного статуса до начала проведения иммунотерапии;
• Определение уровня и степени поражение иммунной системы;
• Определение уровня и степени поражения иммунной системы является одним из важнейших этапов в подборе препарата для иммуномодулирующей терапии.
Точка приложения действия препарата должна соответствовать уровню нарушения деятельности определенного звена иммунной системы с целью обеспечения максимальной эффективности проводимой терапии.
• Контроль динамики иммунного статуса в процессе иммунотерапии;
• Применение иммуномодуляторов только при наличии характерных клинических признаков и изменений показателей иммунного статуса;
• Назначение иммуномодуляторов в профилактических целях для поддержания иммунного статуса (онкология, оперативные вмешательства, стресс, экологические, профессиональные и др. воздействия).
Однако не все применяемые иммуномодуляторы соответствуют требованиям и принципам рациональной иммунотерапии и иммунопрофилактики. Разработанная академиком РАМН А.А. Воробьевым классификация иммуномодуляторов по вектору и характеру действия на иммунную систему, по природе и происхождению, по механизму действия с учетом причин и механизмов развития первичных и вторичных иммунодефицитов, позволяет в каждом конкретном случае выбрать наиболее эффективный модулятор (МЖЭИ, 2002, №4). Существующее множество иммуномодуляторов неравноценно по своей эффективности и по ряду других свойств, определяющих их безвредность, удобства применения, экономичность и прочее. Наиболее приемлемы и адекватны организму человека природные, естественные, так называемые, эндогенные иммуномодуляторы, основу которых составляют вещества, принимающие участие в регуляции иммунных процессов в организме человека и животных. К эндогенным иммуномодуляторам, как известно, относятся интерлейкины, интерфероны, препараты из пептидов тимуса, костного мозга и иммунокомпетентных клеток.
Среди иммунокорректоров этого класса в настоящее время существенный интерес представляет новый препарат "Трансфер фактор плюс" фирмы "4Life Research. LC", США.
Щербина Анна Юрьевна, заместитель директора Института гематологии, иммунологии и клеточных технологий, д.м.н., заведующая отделением иммунологии НМИЦ ДГОИ им. Дмитрия Рогачева, врач-педиатр, иммунолог-аллерголог, профессор кафедры гематологии факультета усовершенствования врачей Российского национального исследовательского медицинского университета им. Н.И. Пирогова.
Образование: 2-й Московский ордена Ленина государственный медицинский институт имени Н.И. Пирогова (сейчас — Российский национальный исследовательский медицинский университет им. Н.И. Пирогова), ординатура по педиатрии НИИ детской гематологии.
Регалии и звания: доктор медицинских наук, профессор, автор более 100 публикаций, член Российской ассоциации аллергологов и клинических иммунологов, Европейского общества иммунодефицитов.
Про виды иммунодефицитов
Иммунодефицит — это состояние, сопровождающееся значительными и долговременными изменениями в иммунной системе и серьезными симптомами. Есть иммунодефициты вторичные, а есть первичные (ПИД). Первичные обусловлены генетически. Как правило, симптомы возникают в раннем возрасте, однако иногда могут возникнуть и у взрослых. Но в любом случае проявления будут очень тяжелыми. С первичными иммунодефицитами встречаются крайне редко. Подтвердить многие такие заболевания можно, обнаружив дефект гена. Но пока, правда, найдены мутации не при всех ПИД, поиск продолжается.
Вторичные иммунодефициты — это те, которые возникли в течение жизни под воздействием каких-то факторов, приведших к стойким изменениям иммунитета, возможно пожизненным, но не всегда. Вторичный иммунодефицит может пройти без лечения: если, например, ушел воздействующий фактор. ПИД же обязательно нужно лечить.
Про СПИД и другие вторичные иммунодефициты
По международной классификации вторичными иммунодефицитами считаются серьезные изменения в иммунитете, возникшие под воздействием химиотерапии, облучения, после трансплантации органов и тканей (что сопровождается иммуносупрессивной терапией), при потере белка (основного инструмента, которым оперирует иммунная система). Последний вариант может возникнуть, когда у человека какое-то почечное заболевание и белок уходит с мочой. Или когда у пациента тяжелое заболевание кишечника, нередко врожденное, при котором возникает длительный понос, что также вызывает потерю белка.
СПИД тоже относится к вторичным иммунодефицитам, но он стоит несколько особняком. И во всем мире, и в России обычно этим синдромом занимаются отдельные люди. Но, естественно, у нас с ними есть какое-то взаимодействие, потому что к нам, например, может прийти человек с симптомами как при первичном иммунодефиците, но окажется, что у него СПИД. Таких детей я видела немало.
Про ложные диагнозы
Есть критерии, по которым можно заподозрить наличие иммунодефицита. Основное его проявление — наличие инфекций, часто и тяжело протекающих. Нормально, если взрослый человек четыре–шесть раз в год болеет легкими инфекционными заболеваниями, от которых быстро вылечивается, хотя у него и может иногда быть бронхит или пневмония, требующие применения антибиотиков. Но если он использует антибиотики, а выздороветь никак не получается, это уже подозрительно.
Про настоящие причины инфекционных заболеваний
Если у человека хроническая инфекция, от которой он не может избавиться никакими антибиотиками, то причину нужно устанавливать сугубо индивидуально. Нередко хроническая инфекция возникает из-за какого-то врожденного порока, дефекта строения, который мешает нормально функционировать органу. Причиной может быть нарушение pH-среды, кровоснабжения, как при диабете, и т.п. Иммунодефициты довольно редко служат причиной хронических инфекций одного органа.
Иммуномодуляторы я практически не назначаю, хотя многие это делают. Вероятно, когда-нибудь я поменяю свое мнение, но пока меня никто не убедил, что иммуномодуляторы кому-то помогают. Я подозреваю, что среди этих препаратов есть такие, которые несут реальную пользу. Но у нас существуют определенные российские особенности: например, очень плохо проводятся клинические испытания препаратов, в том числе и иммуномодуляторов. К любому зарубежному препарату довольно жесткие требования в этом смысле. У нас какие-то исследования могут пройти формально — то, что там участвовало пятнадцать алкоголиков и три ребенка, никого не волнует.
Про пользу инфекционных заболеваний
Если ко мне придет пациент и скажет, что ему назначил другой доктор иммуномодулятор, я не буду ничего отменять, а просто выскажу свое мнение об этой проблеме. Продолжать ли прием иммуномодулятора — личное дело пациента. Просто чем старше я становлюсь, тем меньше во мне категоричности. Иммуномодуляторы, которые основаны на использовании белков стенок бактерий и являются зарубежными, то есть прошли серьезные клинические исследования, имеют небольшую эффективность, но она есть. В редких случаях я назначаю какие-то препараты из этой группы. Такое бывает, когда пациент, даже выслушав все доводы, очень хочет чем-то полечиться. Но я предупреждаю — не ожидайте чуда, это не лекарство от всех болезней: может быть, вместо пяти раз заболеете четыре. Здоровый образ жизни, мытье рук, хорошее питание — это все уменьшает заболеваемость различными инфекциями, но люди не могут ими не болеть совсем. Чтобы так было, у нас должен иметься специфический иммунитет ко всем инфекциям. Он появляется у человека, когда тот хоть раз встречался с этой инфекцией.
Препараты вроде эхинацеи усиливают лишь местный иммунитет. Они могут чуть укоротить период знакомства с инфекцией, ускорить выздоровление. Вакцины покрывают лишь малое количество инфекций. Поэтому дети должны болеть. Более того, у детей, которые ограничены в контактах с потенциальными патогенами (единственный ребенок — к нему никого не подпускают, все стерильно), чаще всего развиваются аллергические заболевания, потому что здесь есть условные весы. Когда мы рождаемся, у нас так устроен иммунитет, что мы больше предрасположены к аллергии. Когда мы сталкиваемся с инфекциями, эти весы выравниваются. Если дети не болеют, у них гораздо дольше, а может быть и навсегда, остается предрасположенность к аллергии.
Аутоиммунные заболевания возникают, когда иммунитет, грубо говоря, заблудился. В нормальном состоянии он должен распознавать свои и чужие клетки. Поэтому так сложно осуществить трансплантацию сердца, почки или любого другого органа: организм тут же понимает, что это не его, и пытается от такого объекта избавиться. Но изначально эта система была придумана природой в основном для борьбы с инфекциями. При аутоиммунных заболеваниях механизм распознавания нарушается, организм воспринимает свое как чужое и атакует. Борьба может начаться с разными клетками или с клетками какого-то одного вида.
Мы занимаемся аутоиммунными заболеваниями, но по большому счету не очень много. Исторически так сложилось, что эти патологии чаще относят к кардиологии, ревматологии и гематологии. Однако и у наших больных с иммунодефицитами встречаются аутоиммунные заболевания — и, к слову, намного чаще, чем у обычных людей.
Про будущее иммунологии
Иммунология — довольно сложная область, и наши пациенты не так часто выздоравливают. Поэтому иммунологов не очень много: всем ведь хочется видеть результат своего труда, и сложно жить с мыслью, что большинство твоих больных уже умерло. Конечно, сейчас ситуация лучше, чем раньше: появились новые разработки, методы лечения. Я выбрала эту область, потому что она сложная, по большому счету мало кем изучается и оттого интересная.
Иммунология — не только клиническая наука, но и теория, которая постоянно меняется. Через 20 лет, возможно, мы будем смеяться над теми знаниями, которые имеем теперь. Не исключено, что тогда понимание всей этой проблемы будет другим. Например, в последнее время мы стали выявлять случаи, когда иммунограмма — анализ, показывающий состояние иммунной системы, — нормальная, но с помощью разных хитрых методов выясняется, что у человека иммунодефицит.
Стали обнаруживаться такие дефекты, при которых повышена чувствительность только к определенным группам микробов, а не, как обычно бывает при иммунодефицитах, ко всему сразу: микробам, грибковым инфекциям, вирусам. Недавно, например, выяснилось, что герпетический энцефалит (поражение головного мозга вирусом герпеса) — это тоже иммунодефицит, конкретный маленький дефект, который вызывает подобное состояние. Остальные инфекции такие больные переносят нормально.
Еще обнаружилась группа иммунодефицитов, которые проявляются повышенной чувствительностью к туберкулезу, микобактериям разного рода и небольшому количеству других инфекций, например сальмонеллам. Практически всем людям делают прививки БЦЖ, а это не что иное, как микобактерия. Она ослаблена, но это так с точки зрения обычного иммунитета. При той патологии, о которой мы говорим, микобактерия может вызывать соответствующие заболевания.
Относительно недавно к нам обратилась девочка, у которой основными проблемами были увеличенные шейные лимфоузлы, постоянная температура и периодически появляющиеся сыпи. Девочка также перенесла сальмонеллез, но, насколько я понимаю, после лечения ей не сделали два необходимых посева, которые должны были дать отрицательный результат. В целом картина складывалась довольно странная: сложно предположить, что у человека сразу несколько заболеваний, поэтому в таких случаях всегда хочется найти одну, общую причину проблем.
В процессе обследования выяснилось, что у девочки сальмонеллы высеваются отовсюду: из кишечника, слизистых носа, крови. У пациентки была активная воспалительная реакция, организм пытался избавиться от всех этих микробов. Оттого и увеличенные лимфоузлы, температура, сыпь. При этом стандартные иммунологические тесты не помогли с диагнозом. С помощью зарубежных коллег нам удалось подтвердить недавно описанный и очень редкий генетический дефект, который вызывает повышенную чувствительность к сальмонеллам, а также микобактериям. С помощью более интенсивных и длительных курсов антибиотиков нам удалось взять ситуацию под контроль.
Со знаниями в области иммунологии у рядовых врачей все очень плохо. Это, конечно, сложная наука, но ее можно упростить. Однако, к сожалению, есть не так много вузов, в которых иммунологию преподают в хорошем объеме. А нужно всего-то, чтобы врачи знали, что могут просто, как стрелочники, направлять таких и таких больных к нам.
Оборотной стороной медали отсутствия знаний в иммунологии становится то, что довольно часто к нам направляют пациентов без иммунодефицитов. Но пусть уж нам лучше пришлют 10 тысяч детей без этого заболевания, чем мы пропустим одного больного с ПИД. Теоретически в России около 15 тысяч таких пациентов, а найдена всего, может быть, тысяча. И необходимо обнаружить остальных, пока они не умерли.
Читайте также:


