Рентген новорожденным при инфекции
Мозг – важнейший орган человека, который защищает черепная коробка. При нарушениях ее функций важно выяснить степень поражения, чтобы принять меры исправлению ситуации. Для визуализации костей черепа используют рентгенографию – проводят рентген головы. Это недорогой и доступный метод исследования, не имеющий альтернативы. В ряде случаев это единственная возможность выявить патологию на ранней стадии и провести эффективное лечение.
Метод основан на разной способности лучей проникать сквозь ткани различной плотности. Аппарат фиксирует излучение после прохождения органов на светочувствительной пленке. Изображение костей и плотных структур получаются белыми, мягкие ткани с хорошей проникающей способностью – темными.
Показания для рентгена головы
Основанием для назначения исследования являются:
- Травмы, головные боли;
- Потемнение в глазах;
- Дрожь в руках;
- Носовые кровотечения;
- Головокружения;
- Боли при жевании;
- Снижение зрения и слуха;
- Асимметрия костей лица;
- Подозрение на рак мозга;
- Обмороки;
- Эндокринные нарушения.
Направление на диагностику может выписать врач-травматолог, невролог, эндокринолог, хирург. Процедуру не назначают беременным и кормящим женщинам. Это единственное противопоказание.
Что показывает рентген головы
Рентгенография покажет наличие:
- Признаков разрушения костных тканей;
- Кисты;
- Грыжи и опухоли мозга;
- Гематомы;
- Опухоли мозга;
- Деформации черепа;
- Перелома;
- Обызвествления костей.
Как делают рентген головы и шеи
Подготовка к диагностированию не предполагает каких-либо ограничений в пище и приеме лекарственных препаратов. На проходящем исследование пациенте не должно быть:
- Очков;
- Металлических украшений;
- Съемных зубных протезов.
Тело исследуемого покрывают фартуком для защиты от излучения. Важна неподвижность головы.
При необходимости делают несколько снимков в разных проекциях.
Получение результата
- Дает оценку форме, размерам и толщине черепных костей;
- Анализирует состояние черепных швов и носовых пазух;
- Обращает внимание на сосуды;
- Указывает интенсивность патологических изменений.
Насколько вреден рентген
Получаемая взрослым пациентом доза облучения составляет небольшую часть от годовой нормы (порядка 4%). Эта величина сравнима с часовым пребыванием на пляже. Врачи обращают внимание на то, что такой подход некорректен. Ведь в ряде случаев исследование проводится по жизненным показаниям, с целью обнаружения смертельного заболевания. Поэтому количество проводимых исследований должно быть подчинено главной цели – спасению жизни человека. Бывает так, что диагностику проводят и беременным, тщательно закрывая живот фартуком.
Рентген головы ребенку
К исследованию черепа детей используется другой подход:
- Ребенок более подвержен получить большую дозу облучения;
- Воздействие радиации может отрицательно сказаться на детском организме.
По этим причинам рентген головы грудничку назначают только в крайнем случае, если другие методы диагностики не информативны, а жизнь малыша находится под угрозой. Подобрать альтернативный метод трудно, так как кости черепа имеют сложную структуру, а ультразвук распознает не все патологии.
Основная причина назначения рентгена ребенку до года – травмы. Облучение малышей – нежелательный момент, но часто только таким образом можно выявить родовые травмы, угрожающие жизни ребенка. В случае проведения рентгена головы новорожденному все остальные органы максимально защищают.
Особенности проведения диагностики малышам
Процесс рентгена для ребенка слишком сложен – малыш не может лежать неподвижно. Здесь поможет родной человек, который придержит и успокоит. Новорожденным назначают успокоительное или снотворное.
Снимок головы при беременности
Рентгенография костей головы может потребоваться беременной женщине:
- Для оказания стоматологической помощи;
- При вывихах;
- При переломах для определения расположения костных отломков.
Принимая решение о необходимости проведения диагностики следует сопоставить риск и пользу от проведения процедуры. Состояния, при которых решается этот вопрос, уже представляют опасность здоровья матери. Отказ от проведения рентгена может повлечь серьёзные последствия – отсутствие медицинской помощи повлечет развитие опасных заболеваний. Тогда о нормальных родах не может быть и речи. К тому же меры предосторожности эффективно отражают излучение.
По данным научных исследований особенно неблагоприятно влияние рентгеновского излучения на ранних этапах беременности. Результатом может стать прерывание беременности или патология развития плода.
Где сделать рентген головы
, MD, University of Rochester School of Medicine and Dentistry
Last full review/revision July 2018 by Brenda L. Tesini, MD
(См. также Обзор пневмонии [Overview of Pneumonia] у взрослых и Обзор неонатальных инфекций [Overview of Neonatal Infections]).
Пневмония является наиболее распространенной инвазивной бактериальной инфекцией после первичного сепсиса. Рано развивающаяся пневмония является частью генерализованного сепсиса, и первые проявления возникают при рождении или в течение нескольких часов после ( Неонатальный сепсис). При позднем начале пневмония обычно развивается в возрасте старше 7 дней, наиболее часто в отделениях интенсивной терапии новорожденных среди детей, которым требуется длительная интубация трахеи из-за заболевания легких (называется ИВЛ-ассоциированная пневмония).
Этиология
Контакт с возбудителями происходит трансплацентарно или как следствие внутрибольничной инфекции. Эти организмы включают грамположительные кокки (например, стрептококки группы А и В, метициллин-чувствительные и метициллин-резистентные штаммы Staphylococcus aureus) и грамотрицательные бациллы (например, Escherichia coli, Klebsiella, Proteus). У детей, получивших антибиотики широкого спектра действия, могут быть обнаружены многие другие возбудители, в том числе Pseudomonas, Citrobacter, Bacillus, и Serratia. Некоторые случаи пневмонии вызваны вирусной и грибковой инфекцией.
Клинические проявления
При позднем начале внутрибольничная пневмония проявляется необъяснимым ухудшением дыхательного статуса пациента и повышением количества и изменением качества выделений из дыхательных путей (например, густые и коричневые). У младенцев может развиться острое заболевание с нестабильной температурой и нейтропенией.
Диагностика
Рентгенография грудной клетки
Обследование включает рентгенографию грудной клетки, пульсоксиметрию, культуральное исследование крови и окрашивание по Граму и культуральное исследование аспирата из трахеи.
Новые стойкие инфильтраты должны визуализироваться при рентгенографии грудной клетки, однако их бывает трудно распознать, если ребенок имеет тяжелую бронхолегочную дисплазию.
Если окрашивание по Граму демонстрирует значительное количество полиморфноядерных лейкоцитов и единственного возбудителя, который соответствует тому, что растет из культуры аспирата из трахеи, то повышается вероятность, что этот возбудитель является причиной пневмонии. Поскольку бактериальная пневмония у новорожденных может диссеминировать, нужно провести полную оценку на наличие сепсиса, включая ЛП. Тем не менее, посевы крови являются положительными только в 2–5% случаев внутрибольничой пневмонии.
Лечение
Обычно применяют ванкомицин и бета-лактамные антибиотики широкого спектра
Антимикробная терапия пневмонии с ранним началом такая же, как и при неонатальном сепсисе. В большинстве случаев внутрибольничной пневмонии начальной терапией выбора являются ванкомицин (см. Таблица дозирования ванкомицина для новорожденных [Table Vancomycin Dosage for Neonates]) и широкого спектра действия бета-лактамы, такие как меропенем, пиперациллин/тазобактам, или цефепим ( Рекомендованные дозировки некоторых парентеральных антибиотиков для новорожденных). Этот режим эффективен в лечение сепсиса, а также пневмонии, вызванной типичными внутрибольничными возбудителями, включая P. aeruginosa. При эмпирическом выборе антимикробных средств всегда необходимо учитывать эндемичные виды инфекции и бактериальную резистентность. Более специфичные антибиотики назначают после получения результатов антибиотикочувствительности. Общее лечение такое же, как и при неонатальном сепсисе.
Хламидийная пневмония
Воздействие хламидий во время родов может привести к развитию хламидийной пневмонии через 2–18 нед. У младенцев развивается тахипноэ, но обычно не до критической стадии, в анамнезе могут быть конъюнктивиты, вызванные этим возбудителем. Может присутствовать эозинофилия, а при рентгенографии выявляются двусторонние интерстициальные инфильтраты с гиперинфляцией.
Эритромицин или азитромицин
Пневмония обычно лечится приемом эритромицина 12,5 мг/кг перорально каждые 6 часов в течение 14 дней или азитромицином 20 мг/кг перорально в/в один раз в день в течение 3 дней. Иногда, однако, может быть необходим второй курс ( Рекомендованные дозировки некокторых пероральных антибиотиков для новорожденных *). Вследствие того, что эритромицины у новорожденных могут вызватьгипертрофический пилорический стеноз (ГПС), всех новорожденных, получавших эритромицин или азитромицин, необходимо проверить на наличие симптомов и признаков ГПС, а также их родители должны быть проконсультированы относительно потенциальных рисков.
Диагноз пневмонии, вызванной Chlamydia trachomatis, должен натолкнуть на обследование матери и ее партнера, потому что нелеченная материнская хламидийная инфекция может иметь такие осложнения, как воспаление тазовых органов и бесплодие.
Синдром аспирации мекония у новорожденных
- Российская ассоциация специалистов перинатальной медицины (РАСПМ)
Оглавление
Ключевые слова
синдром мекониальной аспирации
синдром аспирации мекония
персистирующая легочная гипертензия
Список сокращений
ИВЛ – искусственная вентиляция легких
МАР – среднее давление в дыхательных путях
РКИ — рандомизированные контролируемые исследования
САМ – синдром аспирации мекония
СДР, РДС — синдром дыхательных расстройств
СРАР – continuous positive airway pressure / метод респираторной терапии – постоянное давление в дыхательных путях
УЗИ — ультразвуковое исследование
ЧСС - частота сердечных сокращений
ЭТТ – эндотрахеальная трубка
f — частота аппаратных вдохов, в минуту
fO2 — содержание кислорода в воздушной смеси
Peep – пиковое давление в конце выдоха
Pip – пиковое давление на вдохе
SpO2 - сатурация, насыщение крови кислородом, измеряемое методом пульсоксиметрии
Ti — время вдоха
раСO2 - концентрация углекислого газа в крови
раО2 – концентрация кислорода в крови
Термины и определения
Синдром аспирации мекония – тяжелое расстройство дыхания у новорожденных детей, вызванное попаданием мекония в нижние дыхательные пути.
Сурфактант (в переводе с английского – поверхностно-активное вещество) – смесь поверхностно-активных веществ, выстилающая альвеолы изнутри.
Персистирующая легочная гипертензия – состояние, характеризующееся снижением кровотока в легких новорожденного и появление при этом право-левого сброса крови в результате возврата к констрикции артериол легких или персистирования.
Тахипноэ — учащённое поверхностное дыхание.
1. Краткая информация
1.1 Определение
Синдром аспирации мекония (САМ) – тяжелое расстройство дыхания у новорожденных детей, вызванное попаданием мекония в нижние дыхательные пути.
Синонимы САМ: синдром мекониальной аспирации новорожденных, неонатальная аспирация.
1.2 Этиология и патогенез
САМ чаще наблюдается у переношенных или доношенных новорожденных, которые подверглись внутриутробной антенатальной и/или интранатальной гипоксии и родились в асфиксии, приведшей к спазму сосудов брыжейки, усилению перистальтики кишечника, расслаблению анального сфинктера и пассажу мекония — выходу его в околоплодные воды. Обвитие пуповины вокруг шеи, сдавление ее стимулирует вагусную реакцию и пассаж мекония даже при отсутствии асфиксии.
1.3 Эпидемиология
1.4 Кодирование по МКБ 10
P24.0 – Неонатальная аспирация мекония
1.5 Классификация
Классификация САМ по вариантам течения
Первый вариант — с рождения имеется тяжелая дыхательная недостаточность, приступы вторичной асфиксии, одышки, притупления легочного тона, повышение ригидности грудной клетки, обильные разнокалиберные влажные хрипы в легких.
Классификация САМ по степени тяжести
В зависимости от количества, консистенции аспирированной жидкости, а также от сроков аспирации различают:
Легкая степень – отмечается тахипноэ, проходящее через 42-72 часа. Уровень рСО2 в артериальной крови в пределах нормы, рН крови без изменений. Редко отмечается незначительная гипоксимия, корригируемая ингаляцией кислорода.
Средняя степень – клиника схожа с легкой степенью, но нарастание дыхательной недостаточности происходит быстрее и пик приходится на 24 часа. В артериальной крови отмечается гипоксимия степень, которой не соответствует тяжести легочной патологии (сопоставление с Rg-граммой грудной клетки). Это может говорить о стойкой легочной гипертензии с шунтированием крови справа налево как на уровне открытого артериального протока так и на уровне предсердий (что подтверждается УЗИ сердца с Доплер-эффектом).
Тяжелая степень – дыхательная недостаточность отмечается сразу после рождения или в первые 24 часа жизни. В данном случае отмечается сочетание дыхательного и метаболического ацидоза, которые требуют немедленной коррекции.
При тяжелой степени достаточно часто развитие таких осложнений как напряженный пневмоторакс и практически всегда развитие стойкой легочной гипертензии. Стойкость легочной гипертензии связанна в первую очередь с утолщением стенок сосудов легочных артерий вследствие их чрезмерной гипертрофии и гиперплазии. Впервые о гипертрофии сообщили Siassi и соавт. в 1971 году. В частности, в их исследовании доказывалось, что хроническая гипоксия может вызывать утолщение стенок мелких легочных артерий вследствие гипертрофии гладкой мускулатуры, что в свою очередь приводит к стойкому сужению просвета сосуда. Помимо всего выше перечисленного сейчас установлено, что острая гипоксемия плода вызывает дальнейшее сужение легочных артерий, что в итоге приводит к стойкой легочной гипертензии.
2. Диагностика
2.1 Жалобы и анамнез
Анамнез заключается в выявлении факторов риска, таких как переношенность ребенка, эклампсия беременной, гипертензия беременной, сахарный диабет беременной.
2.2 Физикальное обследование
Рекомендовано на этапе постановки диагноза начать с оценки симптомов дыхательной недостаточности у новорожденного по шкале Даунса (Приложение Г) [1].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2b)
Комментарии: Раннее (в течение 2 ч) наблюдается появление симптомов дыхательной недостаточности: тахипноэ, раздувание крыльев носа, втяжения уступчивых мест грудной клетки, цианоз. Увеличение передне-заднего размера грудной клетки.
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2b)
Комментарии: При перкуссии выявляют участки притупления, чередующиеся с коробочным звуком. Выслушивается ослабленное или жёсткое дыхание с большим количеством проводных и крепитирующих хрипов. Удлинённый выдох. Тоны сердца приглушены, можно выслушать систолический шум. Из-за нарушения периферического кровотока кожные покровы приобретают мраморный цвет, могут появиться отёки.
2.3 Лабораторная диагностика
-
Рекомендовано на этапе постановки диагноза провести анализ кислотно-основного состояния и газов крови [1]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 3)
Комментарии: При САМ выявляют резко выраженную гипоксемию и смешанный ацидоз.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 3)
Комментарии: Поскольку меконий может усилить рост бактерий и САМ трудно отличить от бактериальной пневмонии.
2.4 Инструментальная диагностика
-
Рекомендуется на этапе постановки диагноза провести рентгенографию органов грудной клетки для подтверждения факта аспирации [1]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1a)
2.5 Дифференциальная диагностика
Дифференциальную диагностику проводят с РДС, персистирующей лёгочной гипертензией, вызванной тяжёлой асфиксией и сепсисом, врожденной пневмонией, при состоянии средней тяжести - с преходящим тахипноэ новорождённых.
При диагностике РДС характерными признаками на рентгеновском снимке являются: диффузное снижение прозрачности легочных полей, ретикулогранулярный рисунок и полоски просветлений в области корня легкого (воздушная бронхограмма).
Диагностика транзиторного тахипноэ новорожденных. Заболевание может встречаться при любом гестационном возрасте новорожденных, но более характерно для доношенных, особенно после родоразрешения путем кесарева сечения. Заболевание характеризуется отрицательными маркерами воспаления и быстрым регрессом дыхательных нарушений. Нередко требуется проведение назального СРАР - метод создания постоянного давления в дыхательных путях. Характерно быстрое снижение потребности в дополнительной оксигенации на фоне проведения СРАР. Крайне редко требуется проведение инвазивной ИВЛ. Отсутствуют показания для введения экзогенного сурфактанта.
Диагностика раннего неонатального сепсиса, врожденной пневмонии. Характерны положительные маркеры воспаления, определяемые в динамике в первые 72 часа жизни. Рентгенологически при однородном процессе в легких ранний неонатальный сепсис/пневмония неотличимы от САМ. Однако, если процесс в легких очаговый (инфильтративные тени), то это признак характерен для инфекционного процесса и не характерен для САМ. При САМ на рентгенограмме органов грудной клетки инфильтративные тени перемежаются эмфизематозными изменениями, ателектазами, (возможны пневмомедиастинум и пневмоторакс).
Диагностика персистирующей легочной гипертензии новорожденных. На рентгеновском снимке органов грудной клетки отсутствуют характерные для САМ изменения. При эхокардиографическом исследовании выявляется право-левый сброс и признаки легочной гипертензии.
3. Лечение
3.1 Консервативное лечение
Сурфактантная терапия
При подтверждении САМ рекомендуется применение сурфактантной терапии [3].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 3)
Комментарии: Способ сурфактант-терапии состоит в проведении лаважа трахеобронхиального дерева разведенным препаратом Порактант альфа**. Для этого препарат (75 мг во флаконе) разводят в 2,5 мл физиологического раствора, согласно инструкции фирмы производителя. Из этой эмульсии берут 0,5 мл и дополнительно разводят физиологическим раствором до 5,0 мл (осторожно перемешивая и не встряхивая) и проводят лаваж трахеобронхиального дерева дробно двумя-тремя порциями. Оставшиеся 2,0 мл (60 мг) эмульсии вводят попеременно по 1,0 мл в левый и в правый бронх болюсно через санационный катетер. Второй флакон препарата вводят микроструйно, так что общая доза составляла 50 мг / кг. Лечение синдрома аспирации мекония тяжелой степени путем проведения сурфактант-терапии в виде лаважа трахеобронхиального дерева разведенным Порактантом альфа** с последующим введением небольшой дозы препарата позволяет достоверно уменьшить время достижения нетоксической концентрации кислорода в подаваемой газовой смеси, время нахождения детей на искусственной вентиляции легких и в отделении реанимации и интенсивной терапии новорожденных. Известно, что меконий эффективно связывается с легочным сурфактантом за счет химических и физических механизмов взаимодействия и инактивирует его. При этом критерием инактивации является потеря сурфактантом свойства эффективно снижать поверхностное натяжение на границе раздела фаз воздух — вода. Меконий, сорбированный на частицах экзогенно введенного сурфактанта, удаляется при лаваже, а следующее за ним введение терапевтической дозы Порактанта альфа** 50 мг/кг выполняет роль заместительной терапии, приводя к повышению растяжимости легких, устранению ателектазов и улучшению вентиляционно-перфузионного отношения. Эффект терапии проявлялся улучшением аускультативной картины в легких и положительной динамикой на рентгенограммах грудной клетки.
Седация и миорелаксация
-
Для уменьшения потребления кислорода и исключения работы дыхания в отделении интенсивной терапии рекомендуется глубокая седация и миорелаксация [1].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2a)
Комментарии:тримеперидин** - доза насыщения - 0,5 мг/кг, поддерживающая - 20-80 мкг/(кгхч); фентанил** - доза насыщения 5-8 мкг/кг, поддерживающая доза - 1-5 мкг/(кгхч) ); пипекурония бромид # ** - 0,1 мг/кг.
Антибактериальная терапия
- Рекомендуется назначить стартовую антибактериальную терапию до получения результатов посевов [1].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2b)
Комментарии: Антибактериальная терапия показана при аспирации мекония, так как он способствует росту бактерий. Начинают с цефалоспоринов и аминогликозидов. По результатам посевов из трахеи проводят смену антибактериальной терапии.
Респираторная терапия новорожденных с САМ
Помощь новорожденному с САМ в родильном зале
- Рекомендуется оказание помощи в родильном зале всем новорожденным с САМ [2].
Уровень убедительности рекомендаций В (уровень достоверности доказательств–2b)
Комментарии: Широкое использование в предыдущие годы санации носо- и ротоглотки плода до рождения плечиков с профилактической целью не подтвердило своей эффективности, поэтому в настоящее время эта манипуляция не рекомендована для рутинного применения. Санация носо- и ротоглотки ребенка должна быть проведена после перемещения ребенка на реанимационный столик. При этом, несмотря на то, что околоплодные воды содержат меконий, если у ребенка сразу после рождения отмечается хороший мышечный тонус, активное самостоятельное дыхание или громкий крик, то санация трахеи не показана.
Если околоплодные воды содержат меконий и у ребенка отмечается сниженный мышечный тонус, неэффективное или ослабленное самостоятельное дыхание, сразу после рождения необходимо провести интубацию трахеи с последующей санацией через эндотрахеальную трубку. Следует обратить особое внимание на то, что санация проводится путем подключения шланга аспиратора через Т-образный коннектор или мекониальный аспиратор непосредственно к эндотрахеальной трубке. Санация производится до полной аспирации содержимого трахеи. Если эндотрахеальная трубка блокирована меконием, следует удалить эту трубку, повторно интубировать трахею ребенка и продолжить санацию. Использование с этой целью аспирационных катетеров, диаметр которых всегда меньше, чем диаметр эндотрахеальной трубки, не допускается. Если на фоне санации отмечается нарастание брадикардии менее 80уд/мин, санацию следует прекратить и начать искусственную вентиляцию легких (ИВЛ) до повышения частоты сердечных сокращений (ЧСС) более 100 уд/мин. Вопрос о необходимости повторной санации трахеи решается после восстановления сердечной деятельности ребенка в индивидуальном порядке.
Использование ИВЛ в условиях родильного зала
Рекомендуется начать ИВЛ сразу после извлечения ребенка из матери [2].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2a)
Комментарии: Использование саморасправляющегося мешка у новорожденных:
Следует использовать саморасправляющийся мешок объемом не более 240 мл. Такой размер более чем достаточен для проведения вентиляции легких у новорожденных. После сжатия мешок расправляется самостоятельно за счет своих эластических свойств, независимо от источника газовой смеси, что делает использование этого устройства удобным и простым. Однако, для проведения ИВЛ воздушно-кислородной смесью, необходимо подключить мешок к источнику кислорода и установить скорость потока 8 л/мин. Такая скорость позволяет добиться концентрации в дыхательной смеси около 40%. Для создания более высокой концентрации кислорода (80-90%) к саморасправляющемуся мешку требуется подключить дополнительно кислородный резервуар. Следует помнить, что при проведении ИВЛ с помощью саморасправляющегося мешка трудно поддерживать одинаковое пиковое давление от вдоха к вдоху. Поэтому целесообразно использовать манометр, подключенный к мешку. Максимальное пиковое давление ограничено клапаном сброса избыточного давления, который срабатывает при превышении около 40 смН2O. Для создания большего давления на вдохе следует заблокировать пальцем клапан сброса давления. Иногда это может потребоваться при неэффективности первых принудительных вдохов в процессе масочной ИВЛ у крупных доношенных новорожденных. При использовании саморасправляющегося мешка невозможно создать положительное давление в конце выдоха, не подключив дополнительно клапан, создающий давление в конце выдоха. Использование саморасправляющегося мешка не позволяет обеспечить раздувание легких длительностью более одной секунды.
Использование аппарата ИВЛ с Т-коннектором:
В аппаратах ИВЛ с Т-коннектором газовая смесь поступает в маску или интубационную трубку через контур, подключенный к смесителю сжатого воздуха и кислорода и к манометру. Вентиляция обеспечивается благодаря окклюзии пальцем выходной трубки Т-коннектора, осуществляемой с определенной периодичностью. Аппарат позволяет создавать и регулировать необходимое давление, как на вдохе, так и при помощи изменения диаметра отверстия выходной трубки на выдохе (СРАР, PEEP). Время вдоха регулируется путем изменения длительности окклюзии пальцем выходной трубки Т-коннектора. Для функционирования устройства требуется подключение его к источнику газовой смеси. Скорость потока устанавливается 8 л/мин. По сравнению с саморасправляющимся и поточнорасправляющимся мешками устройства с Т-коннектором являются наиболее удобными для проведения ИВЛ у новорожденных детей в родильном зале.
ИВЛ как метод респираторной терапии новорожденных с САМ
- При выраженных признаках дыхательной недостаточности, подтвержденной на рентгенограмме САМ, рекомендуется начать ИВЛ [4].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1b)
Комментарии: Умеренную гипоксемию можно корригировать ингаляцией увлажненного кислорода через кислородную палатку. Эффект от применения СРАР у новорождённых с САМ непредсказуем и поэтому его не рекомендуют для рутинного использования.
Показания к ИВЛ: 1) рефрактерная гипоксемия - ра02 0,9; 2) респираторный ацидоз - раС02 >60, рН
Пневмония
Пневмония у новорожденных младенцев достаточно обычное явление и может возникать из-за вирусных, бактериальных или других агентов. Младенец может заразиться пневмонией in utero , и она может проявиться при рождении (конгениальная), или новорожденный может приобрести ее после рождения (внутрибольничная). Конгенитальная пневмония может быть обусловлена восходящей инфекцией при длительном разрыве плодного пузыря или, менее часто, трансплацентарной инфекцией (см. след. публикации). Предположение данного диагноза строится, исходя из истории болезни матери, клинического обследования и радиографии грудной клетки, и подтверждается бактериологическими культурами крови и содержимого трахеи.
Этиология
Пневмония у новорожденных обычно имеет бактериальную природу и наиболее часто бактериальными патогенами, обуславливающими конгенитальную или приобретенную пневмонии, являются Грам-отрицательные бациллы ( Eschrichia coli , Klebsiella, Pseudomonas, Serratia sp.), β-гемолитические стрептококки группы В и Staphilococcus sp .
Более редкая бактериальная инфекция включает Listeria monocytogenes и анаэробные бациллы. Иногда пневмония обуславливается Chlamidia trachomatis , Mycoplasma pnemoniae или оппортунистическими патогенами, такими как Candida albicans и Pnemocystis carini . Случаи вирусной пневмонии редки, но все же встречаются и вызываются цитомегаловирусом (СМВ), вирусом Coxsackie , респираторным хориовирусом и рубеллой.
Клинические признаки
Ранние клинические признаки и симптомы часто неспецифичны и могут включать летаргию, апноэ, брадикардию, нестабильность температуры и непереносимость кормления. При рождении может быть трудно отличить пневмонию от других форм легочных заболеваний. В других случаях типичные признаки респираторного дистресса могут иметь место от рождения. История матери и ребенка может выявить факторы, предрасполагающие к неонатальной инфекции.
Аускультация грудной клетки может показать сниженное поступление воздуха вокруг областей консолидации и выпота. При вдохе могут быть слышны добавочные дыхательные звуки.
Радиология
Картина является неспецифичной, и пневмония может быть трудно отличима радиологически от аспирационного синдрома и даже ТТН. На протяжении всех легких могут наблюдаться очаговые затемнения или более сливающиеся области радиологической плотности. Долевая пневмония редко видна у новорожденных.
Лечение
- Антибиотики. Широкого спектра после взятия поверхностных и глубоких культур.
- Физиотерапия . Изменение положения для постурального дренажа и активная физиотерапия грудной клетки для областей консолидации.
- Респираторная поддержка (см. след. публикации).
Синдром утечки воздуха
Это состояние обычно наблюдается у новорожденных младенцев и имеет несколько типов:
- Пневмоторакс – воздух в плевральной полости (рис.10.4).
- Пневмомедиастинум – воздух в клетчатке средостения (рис.10.5).
- Пневмоперикардиум – воздух в перикардиальном пространстве.
- Легочная интерстициальная эмфизема (ЛИЭ) – воздух в интерстициальном пространстве легких (рис.10.6).
- Пневмоперитонеум – воздух в области брюшины.
- Воздушная эмболия – проникновение воздуха в легочные вены и распространение по кровотоку.
Рис.10.4. Ретнген грудной клетки, показывающий
левосторонний напряженный пневмоторакс. 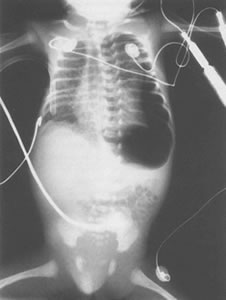
Рис.10.5. Рентген грудной клетки, показывающий пневмомедиастинум.
Контуры сердца и тимуса выделяются на фоне газа. 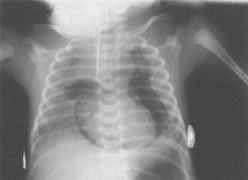
Рис.10.6. Рентген грудной клетки, показывающий обширную ЛИЭ.
Заметьте перераздутие грудной клетки и уплощение диафрагмы. 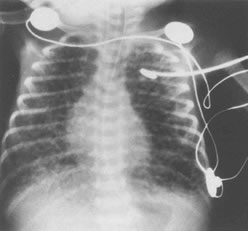
Патофизиология этих состояний одинакова в том, что альвеолы, становясь перераздутыми, лопаются. Воздух затем выходит в интерстициальное пространство легких (ЛИЭ) и продвигается вдоль периваскулярных пространств в средостение (пневмомедиастинум) через висцеральную плевру (пневмоторакс) или реже в перикардиум (пневмоперикардиум).
Спонтанный пневмоторакс возникает приблизительно в 1% случаев влагалищных родов и в 1.5% кесаревых сечений. Многие из них имеют только малые (слабые) симптомы и обнаруживаются неожиданно на рентгене грудной клетки.
Реанимация с вентиляцией положительным давлением делает возникновение пневмоторакса намного более вероятной. Терапия сурфактантом значительно снижает частоту синдрома утечки газа у вентилируемых младенцев.
Пневмоторакс обычно возникает в следующих условиях:
Клинические признаки
У младенцев с пневмотораксом напряжения очевидны признаки тяжелого респираторного дистресса. Часто синдром утечки воздуха возникает у ребенка, который уже имеет респираторный дистресс и может наблюдаться внезапное ухудшение с цианозом, недостаточной периферической перфузией и брадикардией. Специфическими признаками пневмоторакса напряжения являются сдвиг средостения к противоположной стороне, ассиметричное расширение грудной клетки, ассиметричный вход воздуха и слабый периферический пульс. Выступающая грудина позволяет предположить пневмомедиастинум.
Иногда развивается односторонняя ЛИЭ, как результат клапанного эффекта в главных бронхах. Легкое, пораженное эмфиземой, может обусловить компрессию более здорового легкого, следовательно, еще сильнее затрудняя вентиляцию (рис. 10.7)
Рис.10.7. Рентген грудной клетки, показывающий левовтроннюю ЛИЭ.
Средостение и правое легкое компрессированы перераздутым левым легким 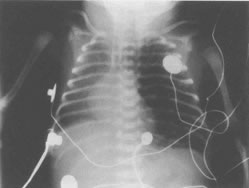
Диагноз
Постановка определенного диагноза осуществляется с помощью передне-задней проекции на рентгене. Чтобы обнаружить небольшой пневмоторакс потребуется вертикальная пленка, тогда как латеральная пленка будет необходима для диагностики наличия воздуха в переднем средостении. Когда имеет место пневмомедиастенум, на рентгене грудной клетки виден морской знак или спиннакер. У младенцев, находящихся в критическом состоянии и имеющих пневмоторакс напряжения, с целью подтверждения диагноза может быть предпринята диафоноскопия (трансиллюминация) грудной клетки. Иногда введение иглы-бабочки калибра 21G с лабораторной бюреткой и шприцем может спасти жизнь при подозрении на пневмоторакс напряжения. Эта срочная процедура диагностики и терапии проводится у критически больных младенцев в тех случаях, когда может быть задержка в получении результатов рентгеновского исследования. Слепое прокалывание иглой грудной клетки может обусловить пневмоторакс и должно предприниматься исключительно в срочных случаях.
Лечение
Для облегчения пневмоторакса напряжения можно ввести межреберный катетер во второе межреберное пространство по среднеключичной линии и соединить его с затвором подводного дренажа или клапаном однопроходного вибратора Хеймлиха . Иногда эвакуация из пневмоторакса будет неполной с помощью этого катетера, и тогда катетер необходимо поместить более назад в шестое межреберное пространство по среднеподмышечной линии. Для ненапряженного пневмоторакса у доношенных младенцев дыхание 100% кислородом в течение до 12 часов может ускорить реабсорбцию пневмоторакса. Изредка наличие большого плеврального или лимфатического выпота может потребовать торакосемтез.
ЛИЭ лучше всего лечить вентиляцией с быстрой частотой (см. след. публикации) или высокочастотной осциляторной вентиляцией. Тяжелую ЛИЭ с компрессией другого легкого можно лечить путем селективной интубации более здорового легкого, таким образом, позволяя легкому, пораженному эмфиземой, находиться в состоянии коллапса. (Brooks et al., 1977). Спустя 24-48 часа при условии, что наступило улучшение, подтвержденное радиологически, трубка должна быть удалена.
Синдром аспирации мекония
Синдром аспирации мекония является серьезной причиной респираторного дистресса у новорожденных, которую потенциально можно предотвратить. Меконий, подкрашенный амниотической жидкостью, почти всегда встречается у доношенных или переношенных младенцев и наблюдается приблизительно в 13% родов. Пассаж мекония часто указывает на дистресс плода, но при тазовом предлежании плода может быть нормальным явлением. Является ли это признаком дистресса плода или нет, возможность его аспирации в легкие должна быть серьезно принята во внимание. Аспирация мекония может возникнуть во время родов или при начале дыхания новорожденного. Ответом младенца на аспирацию во время родов является затрудненное дыхание, а если меконий попал в дыхательные пути, он будет аспирирован глубоко в бронхи. Как только начинается дыхание, возникает дистальная миграция мекония в малые (нижние) дыхательные пути.
Клинические признаки
Имеется широкий спектр проявлений этого состояния от тяжелой асфиксии, требующей активной реанимации, через раннее наступление респираторного дистресса до обычного состояния энергичного ребенка, не имеющего больших проблем. Типичным признаком этого состояния является то, что младенец рождается, покрытый ликвором, подкрашенным меконием, и имеет меконий, осажденный на пуповине, коже и ногтях. Грудная клетка перераздута, а грудина может резко выступать. Респираторный дистресс может сначала быть легким, быстро становясь более и более тяжелым спустя нескольких часов. У ребенка также могут появиться признаки церебральной раздражимости (чувствительности).
Патогенез и этиология
Меконий обуславливает закупорку дыхательных путей с последующим ателектазом. Он также приводит к обструкции по клапанному эффекту, сопровождающейся перераздутием легких и высоким риском синдрома утечки воздуха. Меконий раздражает дыхательные пути, обуславливая химическую пневмонию, иногда возникает вторичная бактериальная инфекция. У младенцев с тяжелым аспирационным синдромом развивается заметная вентиляционно-перфузионная неравномерность, приводящая к шунту справа налево и легочной гипертензии.
Радиология
На рентгене грудной клетки видно перераздутие (плоские диафрагмы, расширение реберных пространств) с диффузными затемнениями по всем полям обоих легких (рис.10.8). Может быть также виден пневмоторакс или пневмомедиастинум.
Рис.10.8. Рентген грудной клетки, показывающий синдром аспирации мекония.
Наблюдается обширное дискретное затенение через оба легочных поля. 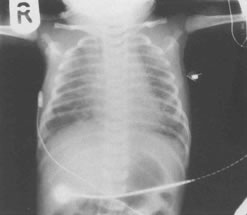
Профилактическое ведение
Заболеваемость и смертность от синдрома аспирации мекония может быть предотвращена или минимизирована оптимальным перинатальным ведением. Ведется дискуссия о том, должен ли неонатальный педиатр посещать все роды, при которых имеет место меконий, окрашивающий ликвор. Очень важно, однако, чтобы опытный неонатолог присутствовал при родах, если наблюдается толстый меконий. В этих условиях должно быть предпринято следующее:
- как только показалась голова и до появления плечей, акушерка должна быстро очистить (отсосать) ротоглотку младенца. Пуповина должна быть дважды пережата для анализа артериальных газов;
- после родов ребенок должен быть перемещен в реанимационную тележку, где реаниматолог аспирационным катетером отсасывает содержимое из ротоглотки под прямым ларингоскопическим контролем (обзором);
- если ребенок угнетен и если меконий виден в задней глотке, на или за голосовыми связками, ребенка необходимо интубировать эндотрахеальной трубкой с широким отверстием (просветом) и чисто отсосать трахею. Отсасывание облегчается использованием аспиратора для мекония. Отсасывание ртом из эндотрахеальной трубки не должно практиковаться. Дальнейшее отсасывание применяется непосредственно через эндотрахеальную трубку, до тех пор, пока ее не удалят. Если после экстубации в эндотрахеальной трубке находится большое количество мекония, ребенок должен быть реинтубирован и должно быть проведено дальнейшее трахеальное отсасывание. Желудок должен быть аспирирован вслед за интубацией и если там находится умеренное или большое количество мекония, желудочный зонд должен быть оставлен in situ для промывания, которое должно быть проведено позже;
- если ребенок энергичен и находится в хорошем состоянии, и только тонкий меконий отсасывается из задней глотки, нет необходимости проводить трахеальную интубацию;
- все дети, родившиеся с толстым меконием в ликворе, должны быть внимательно осмотрены, и у них должен проводиться регулярный мониторинг с тем, чтобы своевременно выявить признаки синдрома аспирации мекония.
Лечение подтвержденного синдрома аспирации мекония
Лечение будет таким же, как и при респираторном дистрессе (см. след. публикации). Особенные акценты должны быть сделаны на следующем:
- увлажнение вдыхаемого воздуха
- постуральный дренаж путем изменения положения, отсасывание из дыхательных путей и перкуссия грудной клетки
- антибиотики: обычно даются, хотя их эффективность не была установлена
Читайте также:


