Превотелла интермедиа что это такое
 |
| Prevotella melaninogenica |
Prevotella spp. входит в состав нормальной микрофлоры ротовой полости, верхнего респираторного тракта, влагалища и ряда других органов человека. Превотеллы обнаруживаются в желудке здоровых людей, неинфицированных и инфицированных Helicobacter pylori. Также обнаруживается при биопсии пищевода (Engstrand L., 2012).
Prevotella spp. могут быть причиной ряда болезней человека. Они были выделены при анаэробных инфекциях дыхательных путей, включая аспирационную пневмонию, абсцесс лёгкого, лёгочная эмпиему и хронические отит среднего уха, ринит и синусит. Превотеллы были выделены из абсцессов и ожогов в непосредственной близости ото рта, мест укусов, паронихии, инфекций мочевыводящих путей, абсцессов головного мозга, остеомиелита, бактериемии связанные с инфекциями верхних дыхательных путей. Prevotella spp. играет значительную роль в патогенезе парадонтоза, гингивита.
У курильщиков в популяции кишечных бактерий выявлено увеличение представителей рода Prevotella, которые связаны с повышенным риском развития колита и злокачественных новообразований кишечника*.
По современной классификации род Prevotella входит в семейство Prevotellaceae, порядок Bacteroidales, класс Bacteroidia, тип Bacteroidetes, Bacteroidetes/Chlorobi group, Fibrobactere-Chlorobi-Bacteroidetes superphylum, царство Бактерии.
В состав рода Prevotella входят следующие виды: P. albensis, P. amnii, P. aurantiaca, P. baroniae, P. bergensis, P. bivia, P. brevis, P. bryantii, P. buccae, P. buccalis, P. colorans, P. conceptionensis, P. copri, P. corporis, P. dentalis, P. dentasini, P. denticola, P. disiens, P. enoeca, P. falsenii, P. fusca, P. histicola, P. ihumii, P. intermedia, P. jejuni, P. loescheii, P. maculosa, P. marshii, P. massiliensis, P. melaninogenica, P. micans, P. multiformis, P. multisaccharivorax, P. nanceiensis, P. nigrescens, P. oralis, P. oris, P. oryzae, P. oulorum, P. pallens, P. paludivivens, P. phocaeensis, P. pleuritidis, P. ruminicola, P. saccharolytica, P. salivae, P. scopos, P. shahii, P. stercorea, P. timonensis, P. veroralis.
Ранее многие виды превотелл классифицировались как виды или подвиды бактерий рода Bacteroides, в частности:
- Prevotella albensis (новое наименование) — Bacteroides ruminicola subsp. ruminicola biovar 7 (старое наименование)
- Prevotella bivia — Bacteroides bivius
- Prevotella brevis — Bacteroides ruminicola subsp. brevis
- Prevotella bryantii — Bacteroides ruminicola subsp. brevis biovar 3
- Prevotella buccae — Bacteroides pentosaceus, Bacteroides capillus и Bacteroides buccae
- Prevotella corporis — Bacteroides corporis
- Prevotella denticola — Bacteroides denticola
- Prevotella disiens — Bacteroides disiens
- Prevotella intermedia — Bacteroides melaninogenicus subsp. intermedius
- Prevotella loescheii — Bacteroides loescheii
- Prevotella melaninogenica — Bacteroides melaninogenicus subsp. melaninogenicus
- Prevotella oralis — Bacteroides oralis
- Prevotella oris — Bacteroides oris
- Prevotella oulorum — Bacteroides oulorum
- Prevotella ruminicola — Bacteroides ruminicola
- Prevotella veroralis — Bacteroides veroralis
Активны в отношении видов превотелл следующие антимикробные средства из описанных в данном справочнике:
- метронидазол активен в отношении P. bivia, P. buccae, P. disiens
- кларитромицин — в отношении P. melaninogenica
- азитромицин — в отношении P. bivia
- тинидазол — в отношении P. melaninogenica
- клиндамицин — в отношении P. melaninogenica
Превотеллы умеренно чувствительны к левофлоксацину и резистентны к ванкомицину.
P. bivia и P. disiens устойчивы к b-лактамным антибиотикам, включая пенициллины, аминопенициллины, цефалоспорины.
Проблемы с зубами есть практически у каждого человека на Земле. По данным ВОЗ, у 80 - 98% населения, в зависимости от страны, есть кариес, чуть меньше людей испытывают проблемы с пародонтом - тканями, которые окружают зуб.
С пародонтитом, опасным воспалением полости рта, по тем же данным, в разное время жизни сталкивается практически каждый. А периимплантит, отторжение имплантата, - настоящая беда для тех, кто пытается вернуть себе здоровую и красивую улыбку. Оказалось, вся вина за эти опасные заболевания лежит на пяти бактериях.





В полости рта человека на самом деле живет множество микроорганизмов - 500 - 700 разных видов, при этом успешно сосуществуя и особо никому не мешая. Но оказалось, что не все из них безобидны.
И здесь возникает вопрос: а с кем конкретно нужно бороться? Бактерий сотни видов, и широкий спектр антибиотиков может и не помочь.
- Самых опасных бактерий в полости рта всего пять видов. Они виновники всех проблем. Чтобы с ними правильно бороться - нужно их определить, - говорит ученый. - Для этого мы разработали специальный тест. Он быстрый, эффективный и недорогой.



Специалистам необходимо всего несколько часов, чтобы определить, какой именно микроорганизм стал источником всех проблем. Фото: Даба ДАБАЕВ
Лечение будет более точным
- Наше исследование началось примерно год назад и проходило в кооперации с кафедрой терапевтической стоматологии Новосибирского медицинского университета и стоматологической поликлиникой Дорожной клинической больницы. Мы стали применять наш тест, и в итоге лечение пациентов проходило быстрее и эффективнее. С помощью теста выбирались правильные препараты, нацеленные именно на те микроорганизмы, которые явились причиной заболевания, - добавляет Сергей Коваленко.
Заведующий лабораторией генодиагностики Демид Бредихин объясняет принцип теста:
- Стоматолог берет образец и направляет его в нашу лабораторию. Мы выделяем из образца ДНК и проводим ПЦР-анализ, по результатам которого точно можем сказать, есть ли наиболее опасные бактерии в образце и как их много. Способ более быстрый и точный, чем стандартное исследование - высев на среды.
Специалистам необходимо всего несколько часов, чтобы определить, какой именно микроорганизм стал источником всех проблем.

Современный интерьер медицинского центра. Фото: Даба ДАБАЕВ
Разработчики уверяют: стоимость такого теста невелика, а польза вполне ощутима, в том числе и для кошелька. Он сможет сохранить десятки тысяч рублей, которые без него будут потрачены на перебирание антибиотиков, а затем на восстановление организма после массированного удара препаратами.
- Конечно, предложить сделать анализ - это работа стоматолога. Но и сам пациент должен не зевать и заботиться о своем здоровье, - рассуждает Демид Бредихин. - В идеале тест нужно проводить до стоматологических вмешательств и имплантации. Но все мы понимаем, что живем в реальном мире. Так что сделайте анализ хотя бы при появлении проблем.
Подобный тест - новинка для Новосибирска . Данный анализ широко распространен за границей, но в России только набирает свои обороты. Он станет доступен сибирякам с конца февраля здесь.

Конкретно
Пять самых опасных бактерий полости рта
• Porphyromonas Gingivalis - порфиромонас гингивалис
• Tannerella Forsythia - таннерелла форсайтиа (ранее Bacteroides Forsythus)
• Treponema Denticola - трепонема дентикола
• Aggregatibacter Actinomycetemcomitans - аггрегатибактер актиномицетемкомитанс
• Prevotella Intermedia - превотелла интермедиа
Известно, что в полости рта выявляют порядка 1200 филотипов, подавляющее большинство которых представляют собой резидентную флору, оказывающую стабилизирующее воздействие для существования общей биопленки полости рта. Ряд видов, будучи также резидентной флорой, стабилизирующими являются только до определенного предела, при превышении которого они проявляют агрессивность и могут принимать участие в воспалительных процессах.
К пародонтопатогенам на сегодняшний день относят около 20 видов бактерий, относящихся по степени вирулентности к двум подгруппам. К пародонтопатогенам 1-го порядка относятся бактерии, для которых выявлены строгие ассоциации с прогрессированием заболевания, к пародонтопатогенам 2-го порядка — бактерии, играющие второстепенную роль в развитии заболевания пародонта.
К первой подгруппе относят три вида. Это Porphyromonas gingivalis, Aggregatibacter actinomycetemcomitans и Tanerella forsythia. Все эти бактерии являются грамотрицательными анаэробами, облигатными или факультативными. Все имеют выраженную тенденцию к внутриклеточному паразитированию в десневом эпителии и тканях пародонта. Для всех трех бактерий доказана возможность распространения в человеческой популяции по типу экзогенного инфекционного агента.
Наиболее агрессивным пародонтопатогеном является Porphyromonas gingivalis, облигатно анаэробная, пигментообразующая бактерия, экспрессирующая три сильных фактора вирулентности (фимбрии, гингипаины и липополисахарид), непосредственно участвующих в деструкции тканей пародонта.
Ненамного уступает ему в вирулентности Aggregatibacter actinomycetemcomitans, грамотрицательная неподвижная факультативно анаэробная коккобацилла. Эта бактерия вырабатывает сильный лейкотоксин, разрушающий лейкоциты, моноциты и нейтрофилы, таким образом, атакуя факторы врожденного иммунного ответа. Лейкотоксин вызывает образование пор в клеточных мембранах и в высоких концентрациях вызывает лизис клеток, в том числе и опухолевых.
Факторы вирулентности Tanerella forsythia наименее изучены. Известно, что она продуцирует протео- и гликолитические ферменты, активность которых коррелирует с клиническими признаками пародонтита. Наиболее интригующей ее особенностью является способность индуцировать клеточный апоптоз. При добавлении экстракта T. forsythia к HL60 и другим клеточным линиям наступает ряд явлений, характерных для апоптозных процессов (активация каспазы3, образование пор в мембранах митохондрий и др.).
Также внимание исследователей привлекают две бактерии группы пародонтопатогенов второго порядка, Treponema denticola и Prevotella intermedia. По вирулентности они значительно уступают тройке лидеров, однако имеют свои интересные особенности, позволяющие им играть немаловажную роль в развитии пародонтита.
Treponema denticola — это изогнутая спирохета, обладающая самостоятельной подвижностью. Ее особенностью является способность к образованию ассоциаций с другими бактериями, способствуя тем самым распространению воспалительного процесса. Наиболее часто этот вид образует ассоциации с такими пародонтопатогенами, как P. gingivalis и T. forsythia. Присутствие у пациента, помимо других пародонтопатогенов, T.denticola — сигнал того, что процесс из локального может перейти к генерализации.
Prevotella intermedia — неподвижная палочковидная бактерия, обладающая несколькими факторами вирулентности, гораздо более слабыми, чем у пародонтопатогенов первой группы. Однако эта бактерия обладает мощными адгезивными свойствами, позволяющими ей быстро колонизировать участки тканей. Эти микробы первыми колонизируют ротовую полость вначале инфекционного процесса. Если
P. intermedia обнаруживается у пациента как моноинфекция, как правило, это означает самое начало заболевания. Если она обнаруживается с другими пародонтопатогенами, это указывает на прогрессирование заболевания, в то время как при стабилизации процесса она, как правило, отсутствует.
По всей видимости, роль пародонтопатогенных бактерий значительно шире, чем это представлялось ранее. В многочисленных работах последних лет появились сведения о том, что пародонтопатогены могут принимать участие в развитии многих заболеваний различных органов. Попадают они в кровоток через любые ранки или изъязвления во рту, в том числе при стоматологических манипуляциях. Наиболее часто обнаруживают в различных органах (легких, желудочнокишечном тракте, сердце, мозге) при воспалительных процессах A. actinomycetemcomitans. Показана роль P. gingivalis в развитии атеросклероза. Клетки P. gingivalis обладают способностью связывать эритроциты, и при попадании бактерии в кровоток ее буквально со всех сторон облепляют эритроциты. Бактерия передвигается по сосудам под прикрытием эритроцитов, избегая, таким образом, фагоцитоза. При наличии в сосудах какого-либо препятствия или изгиба бактерия останавливается, эритроциты распадаются и P. gingivalis колонизирует окружающие ткани, участвуя в формировании атеросклеротической бляшки. Помимо P. gingivalis в атеросклеротических бляшках обнаруживают также T. forsythia и P. intermedia. Также появились сообщения об обнаружении P. gingivalis в синовиальной жидкости и синовиальных тканях больных ревматоидным артритом.
Все это позволяет говорить об очень значимой роли пародонтопатогенов в развитии самых различных заболеваний. Таким образом, резко возрастает значимость диагностики пародонтопатогенов и эффективного их лечения.
Основными видами диагностики пародонтопатогенов являются микроскопический, бактериологический или культуральный и молекулярногенетический (в основном это полимеразная цепная реакция, ПЦР). На практике до появления ПЦР применялись микроскопический и культуральный методы. Но микроскопический метод не позволяет определять бактерии до вида, скорее, дает общую характеристику микрофлоры.
До вида же бактерии можно определить культуральным методом. Однако многие пародонтопатогены не культивируются вообще, а там, где культивирование возможно, оно является долгим (от 5 дней до трех недель) и не всегда успешным процессом.
Данная диагностика позволяет не только быстро идентифицировать пародонтопатогенные бактерии (время анализа — 1 день), но и назначать адекватный курс антибиотикотерапии в зависимости от видов выявленных в анализе микроорганизмов.
Медики из США и Израиля обнаружили, что бактерии, обитающие на зубах и деснах человека, могут стать невероятно опасными. О своем открытии они сообщили в научном журнале Cell Host & Microbe.
В число смертельно опасных микроорганизмов исследователи включили фузобактерии, которых можно найти чуть ли не в каждом рту - они входят в состав обычной микрофлоры. Эти бактерии считались безобидными тихонями. Но как выяснилось, в ослабленном организме они начинают наглеть - активно размножаются, мигрируют в пищеварительную систему, оседают на тканях толстого кишечника, где провоцируют развитие злокачественных новообразований благодаря особым белкам, входящим в оболочку бактерий.

Из полости рта бактерий разносит по сосудам и внутренним органам кровоток.
Ничем не лучше стрептококки и стафилококки. На них и на прочую гадость вроде Porphyromonas gingivalis, Actinobacillus actinomycetemcomitans, Prevotella intermedia, Treponema denticola, живущую во рту, ученые ныне возлагают ответственность и за другие недуги - казалось бы, никак не связанные с состоянием зубов и десен.
В первую очередь следует опасаться сердечно-сосудистых заболеваний. Механизм их развития таков: сначала расплодившиеся сверх меры микроорганизмы вызывают воспаления десен - пародонтит, а потом перекидываются на ткани сердца и сосудов. А могут и диабет вызвать, и воспаление легких. У женщин - преждевременные роды.
- У людей, страдающих пародонтитом, шанс появления каких-либо хронических заболеваний возрастает на 40 процентов, - заявили ученые из Бостонского университета (США) на недавней интерактивной конференции, которую организовало научно-исследовательское подразделение компании Colgate-Palmolive.
А если верить исследованиям, которые провели в Льежском университете ( Бельгия ), воспаление полости рта обнаруживают у 90 процентов больных ишемической болезнью.
Чем спасаться? Лечением, конечно же. И антибактериальной профилактикой. Банальный совет чистить зубы утром и вечером обретает новый смысл. Не худо, как советуют специалисты, еще и регулярно полоскать рот противовоспалительными отварами. Для верности. Ведь они многократно повышают эффективность чистки зубов и десен. Можно воспользоваться и уже готовыми препаратами, которые сейчас в изобилии производят фирмы, создающие зубные пасты.

У правильных девушек всякая гадость во рту не задерживается.
КСТАТИ
Поборемся зубной щеткой с ожирением
Чаще мыть руки, умываться, чистить зубы и полоскать рот медики советуют и тем, кому хотелось бы избавиться от лишнего веса. И не толстеть впредь.
- Почти одновременное увеличение числа тучных людей в большинстве стран сложно объяснить лишь неправильным питанием и малоподвижным образом жизни, - говорит доктор Лея Уигхем из университета Висконсина (США). - Ожирение распространяется стремительно. Словно эпидемия.
Ученая уверяет, что оно - ожирение - передается от человека к человеку. Чем? Так называемыми аденовирусами - возбудителями простуды. Как было установлено, они заставляют жировые клетки активнее расти и размножаться. Неизвестно, правда, пока, зачем. Известно другое: более 20 процентов американцев хронически заражены аденовирусами. И, как правило, это толстяки.

Ожирение заразно, передается, в том числе, и орально.
Одолеть вирусы сложно. Но можно. Иной раз они отступают под натиском препаратов, стимулирующих иммунитет. Им в помощь опять же потребна профилактика в виде гигиенических процедур, которые воспрепятствуют попаданию аденовирусов в организм, просто очищая от них кожу и полость рта.
Полость рта, ее слизистая оболочка и лимфоидный аппарат играют уникальную роль во взаимодействии организма с окружающим его миром микробов, между которыми сформировались в процессе эволюции сложные и противоречивые отношения. Поэтому роль микроорганизмов далеко не однозначна: с одной стороны, они участвуют в переваривании пищи, оказывают большое позитивное влияние на иммунную систему, являясь мощными антагонистами патогенной флоры; с другой стороны, они являются возбудителями и главными виновниками основных стоматологических заболеваний.
В полости рта находится больше различных видов бактерий, чем в остальных отделах желудочно-кишечного тракта (от 160 до 300 видов). Одни бактерии попадают в полость рта с воздухом, водой, пищей - так называемые транзитные микроорганизмы, время пребывания которых ограничено. Другие (почти 30 микробных видов) составляют резидентную (постоянную) микрофлору, образующую довольно сложную и стабильную экосистему ротовой полости.
В нормальных условиях (не используются антисептические пасты, антибиотики и др.) изменения в сложившейся экосистеме происходят в зависимости от времени суток, года и т.д., и лишь в одном направлении, т.е. изменяется только количество представителей разных микроорганизмов. Однако видовое представительство остается у конкретного индивидуума постоянным практически в течение всей жизни. Состав микрофлоры зависит от слюноотделения, консистенции и характера пищи, а также от гигиенического содержания полости рта, состояния тканей и органов полости рта и наличия соматических заболеваний. Расстройства слюноотделения, жевания и глотания всегда приводят к нарастанию количества микроорганизмов в полости рта. Различные аномалии и дефекты, затрудняющие вымывание микроорганизмов током слюны (кариозные поражения, некачественные зубные протезы и др.), способствуют увеличению их количества в полости рта.
Микробные сообщества в полости рта образуют аутохтонные и аллохтонные микроорганизмы. К аутохтонной флоре полости рта относят резидентные (постоянно обитающие) и транзиторные (временно присутствующие) микробы, включающие условно-патогенные и патогенные виды. Они проникают в полость рта из окружающей среды; не вегетируют в полости рта и быстро удаляются из неё. Аллохтонные микробы попадают в полость рта из других микробных биотопов (например, из кишечника или носоглотки).
Микрофлора полости рта крайне разнообразна и включает бактерии (спирохеты, риккетсии, кокки и др.), грибы (в том числе актиномицеты), простейшие, вирусы. При этом значительную часть микроорганизмов полости рта взрослых людей составляют анаэробные виды. По данным разных авторов, содержание бактерий в ротовой жидкости колеблется от 43 млн до 5,5 млрд в 1 мл. Микробная же концентрация в зубных бляшках и десневой бороздке в 100 раз выше - примерно 200 млрд микробных клеток в 1 г пробы (в которой около 80% воды). Самую большую группу постоянно обитающих в полости рта бактерий составляют кокки - 85 - 90% от всех видов. Они обладают значительной биохимической активностью, разлагают углеводы, расщепляют белки с образованием сероводорода.
Стрептококки являются основными обитателями полости рта. В 1 мл слюны содержится до 109 стрептококков. Большинство стрептококков являются факультативными (нестрогими) анаэробами, но встречаются и облигатные (строгие) анаэробы - пептококки. Стрептококки сбраживают углеводы по типу молочнокислого брожения с образованием значительного количества молочной кислоты и других органических кислот. Кислоты, образующиеся в результате жизнедеятельности стрептококков, подавляют рост некоторых гнилостных микроорганизмов, стафилококков, кишечной палочки, брюшнотифозных и дизентерийных палочек, попадающих в полость рта из внешней среды.
В зубном налете и на деснах здоровых людей присутствуют также стафилококки - Staph. epidermidis, однако у некоторых людей могут обнаруживаться и Staph. aureus.
Палочковидные лактобактерии в определенном количестве постоянно живут в здоровой полости рта. Подобно стрептококкам они производят молочную кислоту, подавляющую рост гнилостных и некоторых других микроорганизмов (стафилококков, E. colli, брюшнотифозных и дизентерийных палочек). Количество лактобактерий в полости рта при кариесе зубов значительно возрастает. Для оценки "активности" кариозного процесса предложен "лактобациллентест" (определение количества лактобактерий).
Лептотрихии - строгие анаэробы также относятся к семейству молочнокислых бактерий и являются возбудителями гомоферментативного молочнокислого брожения.
Актиномицеты (или лучистые грибы) почти всегда присутствуют в полости рта здорового человека. Внешне сходны с нитевидными грибами: состоят из тонких, ветвящихся нитей - гифов, которые, переплетаясь, образуют видимый глазом мицелий.
В полости рта здоровых людей в 40 - 50% случаев встречаются дрожжеподобные грибы рода Candida (C. albicans, C. tropicalis, C. crusei). Патогенные свойства наиболее выражены у C.albicans. Дрожжеподобные грибы, интенсивно размножаясь, могут вызывать в организме дисбактериоз, кандидоз или местное поражение полости рта (молочницу). Эти заболевания возникают как результат бесконтрольного самолечения антибиотиками широкого спектра действия или сильными антисептиками, когда подавляются антагонисты грибов из представителей нормальной микрофлоры и усиливается рост устойчивых к большинству антибиотиков дрожжеподобных грибов (антагонисты - это одни представители микрофлоры, подавляющие рост других представителей).
Спирохеты заселяют полость рта с момента прорезывания молочных зубов у ребенка и с того времени становятся постоянными обитателями полости рта. Спирохеты вызывают патологические процессы в ассоциации с фузобактериями и вибрионами (язвенный стоматит, ангина Венсана). Много спирохет обнаруживается в пародонтальных карманах при пародонтите, в кариозных полостях и погибшей пульпе.
У половины здоровых людей в полости рта могут обитать простейшие, а именно Entamoeba gingivalis и Trihomonas. Наибольшее их количество встречается в зубном налете, гнойном содержимом пародонтальных карманов при пародонтите, при гингивите и др. Они усиленно размножаются при негигиеничном содержании полости рта.
Нормальная микрофлора полости рта достаточно устойчива к действию антибактериальных факторов ротовой жидкости. Вместе с тем она сама участвует в защите нашего организма от микроорганизмов, поступающих извне (своя нормальная микрофлора подавляет рост и размножение болезнетворных "чужаков"). Антибактериальная активность слюны и количество обитающих в полости рта микроорганизмов находятся в состоянии динамического равновесия. Основная функция антибактериальной системы слюны заключается не в полном подавлении микрофлоры в полости рта, а в контроле количественного и качественного ее состава.
Стафилококки, лактобациллы, бактероиды, нейссерии, грибы, простейшие находятся в полости рта в гораздо меньшем количестве, чем стрептококки, вейллонеллы и
дифтероиды. Поэтому, различают главных и второстепенных представителей резидентной флоры. В норме некоторые из видов, составляющих определенную часть оральной флоры (бактероиды, лактобациллы, извитые формы, спирохеты), представлены в таких небольших количествах, что обычно теряются среди стрептококков, вейллонелл и дифтероидов, с которыми они обычно ассоциированы. Между этими постоянными представителями существуют антагонистические или синергические отношения. Считается, что стрептококки (S.salivarius, S.sanguis, S.mitis), вейллонеллы и дифтероиды являются стабилизирующей частью микрофлоры полости рта, а стрептококки (S.mutans), лактобациллы, бактероиды, актиномицеты — агрессивной.
При выделении микроорганизмов из разных зон ротовой полости взрослых отмечено преобладание определенных видов на различных участках. Если разделить полость рта на несколько биотопов, то предстанет следующая картина. Первый биотоп - слизистая оболочка ввиду своей обширности имеет самый вариабельный состав микрофлоры: на поверхности преимущественно выделяется грамотрицательная анаэробная флора и стрептококки. В подъязычных складках и криптах слизистой преобладают облигатные анаэробы. На слизистой твердого и мягкого неба встречаются стрептококки и коринебактерии.
В качестве второго биотопа выделяют десневую бороздку (желобок) и находящуюся в нем жидкость. Здесь присутствуют бактероиды (B. melaninogenicus), порфиромонады (Porphyromonas gingivalis), превотелла интермедиа (Prevotella intermedia),а также актинобациллюс актиномицетемкомитанс (Actinibacillus actinomicitemcomitans), дрожжеподобные грибы и микоплазмы, а также нейссерии и др.
Третьим биотопом является зубная бляшка - это самое массивное и разнообразное бактериальное скопление. Количество микроорганизмов составляет от 100 до 300 млн в 1 мг. Видовой состав представлен практически всеми микроорганизмами с преобладанием стрептококков.
Ротовую жидкость следует назвать в качестве четвертого биотопа. Посредством ее осуществляется взаимосвязь между всеми остальными биотопами и организмом в целом. В значительных количествах в ротовой жидкости содержатся вейлонеллы, стрептококки (Str. salivarius, Str. mutans, Str. mitis), актиномицеты, бактероиды, нитевидные бактерии.
Кариес и пародонтит - самые распространенные заболевания. Для развития кариеса обязательным моментом является присутствие микроорганизмов. Повышенной способностью образовывать зубной налет и вызывать поражение зубов обладает Streptococcus mutans, колонии которого составляют до 70% всех микроорганизмов зубного налета.
Для развития воспалительных заболеваний пародонта главным условием также является наличие ассоциации микроорганизмов, таких, как Actinibacillus actinomicitemcomitans, Porphyromonaas gingivalis, Prevotella intermedia, а также стрептококков, бактероидов и др. Причем возникновение и интенсивность патологических процессов напрямую зависит от качественного и количественного состава микрофлоры зубного налета и бляшки:
Главные виды бактерий, ассоциированные с этими заболеваниями
Как известно, каждый человек — это суперорганизм, сообщество, состоящее из самого этого человека и множества живущих в нем и на нем бактерий. Количество бактериальных клеток на несколько порядков превосходит количество клеток самого человека, а их суммарный вес составляет два-три килограмма.
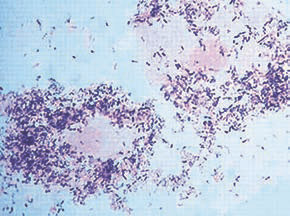
Gardnerella vaginalis — колонии в мазке (dic.academic.ru)
Большинство бактерий живет в кишечнике, но не только. Анализ бактериальных сообществ, живущих на коже человека, показал существование трех существенно различных типов микрофлоры: на влажной коже (например, подмышками или в пупке), на сухой коже (например, на плече или на локте) и на жирной коже (лоб между бровями, крылья носа, канал уха и т.п.) [1]. Области с жирной кожей характеризуются наименьшим разнообразием видов, в основном Propionibacteria и стафилококков. Впрочем, в другом исследовании было показано, что использование косметики, в частности пудры, существенно увеличивает разнообразие бактерий на лбу [2]. Следует отметить, что эти исследования имеют не только косметическое значение: так, агрессивный штамм лекарственно-устойчивого Staphylococcus aureus приобрел гены, дающие ему возможность жить на коже, горизонтальным переносом от обычного компонента нормальной микрофлоры S. epidermidis [3].
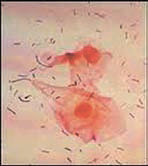
Gardnerella vaginalis и две клетки эпителия (medicus.ru)
Еще больший медицинский интерес представляет микрофлора слизистых оболочек, в частности, половых путей. В вагине здоровых женщин живут различные виды лактококков, причем доля женщин с преобладанием тех или иных видов лактококков зависит от этнической группы (белые, азиатки, афроамериканки и латиноамериканки); кроме того, у двух последних групп часто встречаются сообщества, в основном состоящие не из лактококков, а из строгих анаеробов (превотелл, гарднерелл и т.п.), впрочем, также производящих молочную кислоту [4]. В зависимости от преобладающего типа вагинальных сообществ различалась и кислотность: у латиноамериканок (pH 5.0 ± 0.59) и афроамериканок (pH 4.7 ± 1.04) она была значимо выше, чем у азиаток (pH 4.4 ± 0.59) и белых (pH 4.2 ± 0.3). Наблюдаемые различия могут быть связаны как с генетическими особенностями хозяев (иммунный статус, состав лигандов на поверхности эпителия и т.д.), так и с особенностями стиля жизни: диеты, гигиенических привычек, способов контрацепции, полового поведения и т.п. Одним из практических выводов из этой работы является то, что следует пересмотреть клинические (микробиологические) критерии нормальности вагинальной микрофлоры: они должны учитывать этническую принадлежность пациенток, поскольку при существующих критериях абсурдно большой доле афроамериканок и латиноамериканок должен быть диагностирован дисбактериоз при полном отсутствии клинических симптомов.
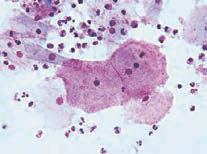
Gardnerella vaginalis на фоне эпителиальных клеток
Бактериальный вагиноз является фактором риска при опасности заражения ВИЧ. Анализ вагинальной микрофлоры 132 ВИЧ-положительных женщин из Танзании показал, что гарднереллы и лактобациллы присутствуют во всех сообществах, причем лактобациллы являются признаком нормальной микрофлоры,а вагиноз ассоциирован с превотеллами и Lachnospiraceae [5]. При этом, видимо, превотеллы являются фактором риска не потому, что они сами являются потенциальными патогенами, а поскольку они производят метаболиты (аммоний, аминокислоты), потребляемые патогенами Gardnerella vaginalis и Peptostreptococcus anaerobius 7. В похожем исследовании, проведенном в Китае, сравнивали 50 здоровых женщин и 50 женщин, больных вагинозом [8]. В то время, как единого маркера для здоровых сообществ обнаружено не было, три типа (Bacteroidetes, Actinobacteria, Fusobacteria) и восемь родов, в том числе и уже упоминавшихся (Gardnerella, Atopobium, Megasphaera, Eggerthella, Aerococcus, Leptotrichia/Sneathia, Prevotella, Papillibacter), значимо чаще наблюдались у больных вагинозом по сравнению со здоровыми контролями.
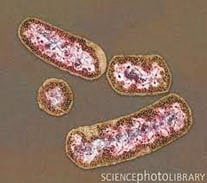
Prevotella melaninogenica — кишечная бактерия (SciencePhotoLibrary) 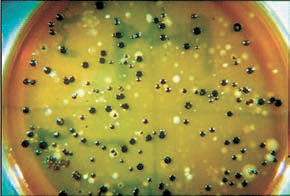
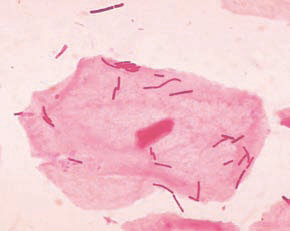
Колонии Prevotella intermedia, обитателя полости рта (GZFA)
Впрочем, исследователи изучают не только вагинальную микрофлору самок человека. Было показано, что, несмотря на анатомическое и физиологическое сходство репродуктивных органов человека и бабуина, их микрофлора существенно различна: хотя у самок бабуинов, как и у человека, преобладают Грам-положительные бактерии (Firmicutes), но это не лактобациллы; некоторые группы Грам-отрицательных бактерий встречаются у бабуинов, но не у человека [9]. С другой стороны, анализ микрофлоры уретры мужчин показал, что некультивируемые бактерии, ассоциированные с вагинальными патологиями, часто встречаются у асимптоматических носителей, не имеющих признаков воспаления уретры [10]. При этом асимптоматическое носительство возбудителей заболеваний, передающихся половым путем (хламидии и гонококки), коррелировало с наличием уже знакомых маркеров вагиноза: Sneathia, Gemella, Aerococcus, Anaerococcus, Prevotella, Veillonella.
Lactobacillus_sp_01 около клетки вагинального эпителия (Википедия) 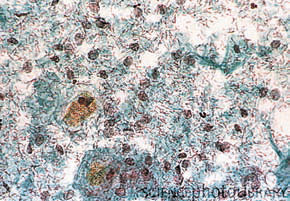
Lactobacillus на вагинальном мазке (SciencePhotoLibrary)
1. Grice EA et al. Topographical and temporal diversity of the human skin microbiome. Science 324: 1190 (2009).
2. Staudinger T et al. Molecular analysis of the prevalent microbiota of human male and female forehead skin compared to forearm skin and the influence of make-up. J. Appl. Microbiol. 110: 1381 (2011).
3. Diep BA et al. Complete genome sequence of USA300, an epidemic clone of community-acquired meticillin-resistant Staphylococcus aureus. Lancet 367: 731 (2006).
4. Ravel J et al. Vaginal microbiome of reproductive-age women. Proc. Natl. Acad. Sci. USA 108: 4680 (2011).
5. Hummelen R. Deep sequencing of the vaginal microbiota of women with HIV. PLoS One 5: e12078 (2010).
6. Pybus V, Onderdonk AB. Evidence for a commensal, symbiotic relationship between Gardnerella vaginalis and Prevotella bivia involving ammonia: Potential significance for bacterial vaginosis. J. Infect. Dis. 175: 406 (1997).
7. Pybus V, Onderdonk AB. A commensal symbiosis between Prevotella bivia and Peptostreptococcus anaerobius involves amino acids: Potential significance to the pathogenesis of bacterial vaginosis. FEMS Immunol. Med. Microbiol. 22:317 (1998).
8. Ling Z et al. Molecular analysis of the diversity of vaginal microbiota associated with bacterial vaginosis. BMC Genomics 11: 488 (2010).
9. Rivera AJ et al. Differences between the normal vaginal bacterial community of baboons and that of humans. Am. J. Primatol. 73: 119 (2011).
10. Nelson DE et al. Characteristic male urine microbiomes associate with asymptomatic sexually transmitted infection. PLoS ONE 5: e14116 (2010).
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Читайте также:


