Цитомегаловирусная инфекция у недоношенных детей
Скрытая угроза: цитомегаловирус
Цитомегаловирус — скрытый бич нашего времени, поражающий новорожденных гораздо чаще нашумевшего вируса Зика. Хотя у здоровых людей заражение часто протекает бессимптомно, вирус вызывает тяжелые осложнения у людей с ослабленным иммунитетом. К сожалению, вылечивать и тем более предотвращать инфицирование современная медицина еще не умеет.
Цитомегаловирус — крупный вирус размером в 150–200 нм, что делает его одним из самых больших по размеру вирусов, известных современной науке. Его геном представлен двухцепочечной ДНК, содержащей информацию для производства более 230 белков.
После заражения вирусные белки начинают синтезироваться в клетке хозяина с вирусной ДНК — ЦМВ так распространяется и поддерживает свою жизнедеятельность.
Один из таких белков (ДНК-полимераза, необходимая для прохождения жизненного цикла вируса) играет роль мишени для использующихся сейчас противовирусных препаратов.
Встречаемость вируса высока везде. Однако этот показатель колеблется в зависимости от возраста, места проживания и социально-экономического статуса: зараженность выше в развивающихся странах и неблагополучных группах населения. Согласно результатам обследований, в среднем в США половина населения от 6 до 49 лет инфицирована ЦМВ. Среди 75–80-летних американцев носителями являются уже девять человек из десяти. В развивающихся же странах среди детей от одного года до пяти лет инфицирован примерно каждый пятый, а у пожилых людей этот показатель может достигать 90–100%.
Поскольку вирус может вызывать врожденные дефекты у детей, эти цифры заставляют специалистов бить тревогу.
Судя по статистике, в группу риска заражения попадает практически любой. Однако серьезные осложнения от вируса грозят в основном людям с пониженной функцией иммунитета: например, пациентам с трансплантированными органами, со СПИДом или новорожденным. Особенно восприимчивы к инфицированию недоношенные дети с низким весом, поскольку их иммунные системы еще не до конца сформированы. Более того, ученые выяснили, что уязвимость для вируса могут повысить некоторые генетические мутации.
Вирус может передаться через выделения из организма инфицированных больных: через слюну, слезы, мочу, фекалии, грудное молоко, сперму и т.д.
Также заразиться можно при переливании крови либо трансплантации органов. Кроме того, на некоторых поверхностях ЦМВ остается жизнеспособным до шести часов, и поэтому изредка можно заразиться и через контакт с предметами.
У здоровых людей симптомов заражения часто нет, и вирус не дает о себе знать. Однако вирус может реактивироваться, и тогда болезнь может проявлять себя в осложнениях различной степени тяжести, от неспецифической фебрильной лихорадки до даже смертельного исхода.
Более того, некоторые ученые считают, что на самом деле вирус сильно недооценен и связан с гораздо большим количеством осложнений, чем можно найти в стандартном описании для врачей.
Клиническую диагностику ЦМВ можно за короткие сроки провести в лаборатории, причем методов обнаружения вируса множество. Диагностика вируса улучшилась и у беременных женщин, хотя, согласно самым последним исследованиям, стандартный тест выявляет отнюдь не все случаи заражения. Одобренного лечения для будущих матерей сейчас нет. Новорожденным с умеренным проявлением симптомов заражения обычно прописывают валганцикловир. Здоровые люди, зараженные ЦМВ, чаще всего не нуждаются в лечении. Лечение обычно назначают пациентам с ослабленной иммунной системой.
Главную угрозу ЦМВ представляет для детей в утробе. Хотя он и уступает по известности вирусу Зика, на самом деле именно цитомегаловирус — самая частая вирусная причина инвалидности и врожденных дефектов у детей в США. Внутриутробное заражение проявляется во многих формах, включая недоношенность, задержку внутриутробного развития, микроцефалию и потерю слуха. Бремя болезни у детей с пожизненной инвалидностью из-за врожденного вируса оценивается в $1,86 млрд в год.
Как отмечает Эми Армстронг-Хеймсот из Университета Северной Аризоны, лишь 13% женщин слышали об этом вирусе. Про то, что его передача от матери ребенку может обернуться трагедией, исследовательница узнала от коллеги с недиагностированным ЦМВ.
Особое внимание направлено на женщин и с ВИЧ, и с ЦМВ, поскольку при таком двойном вирусном заражении риск инфицирования младенца вырастает в разы. Согласно исследованиями, ВИЧ-инфицированные женщины с ЦМВ в моче при родах в пять раз чаще передают ВИЧ младенцам, чем женщины с ВИЧ, но без ЦМВ. Также они в 30 раз чаще заражают новорожденных ЦМВ.
Лучшим методом борьбы с вирусом в перспективе специалисты называют вовсе не лекарства, а вакцины. Они помогут контролировать вирус на уровне популяции — с помощью всеобщей иммунизации. В первую очередь такая стратегия была бы направлена на женщин детородного возраста для предотвращения заражения плода. Однако, конечно, они необходимы и для пациентов с трансплантированными органами и гематопоэтическими стволовыми клетками.
Хотя вакцины пока нет, у исследователей, по-видимому, уже есть достаточное количество фундаментальных знаний для ее создания.
Разработок с различными стратегиями сейчас много — занимаются ими даже такие гиганты фармбизнеса, как Merck и GSK.
Удивительно, как борьба с цитомегаловирусом еще не стала одним из приоритетов международных здравоохранительных учреждений. Разработки вакцин можно было бы ускорить привлечением общественного внимания к этой проблеме и обращением к политическим и экономическим организациям за помощью. Остается надеяться, что многочисленные разработки ученых по созданию эффективной и безопасной вакцины уже близки к успеху — ведь они избавят многие семьи от бремени последствий заражения вирусом и спасут множество жизней.

Цитомегаловирусная инфекция – широко распространенная вирусная инфекция, характеризующаяся многообразием проявлений от бессимптомного течения вплоть до тяжелейших генерализованных форм с поражением внутренних органов и центральной нервной системы. Во время трансплацентарной передачи инфекции возможно поражение плода.
Уровень инфицирования цитомегаловирусной инфекцией и степень зараженности организма зависит от социально-экономических условий, этнической принадлежности, практики медицинского обслуживания новорожденных и детей младшего возраста, времени вступления в половые отношения.
Доля носителей ЦМВ в России составляет около 90%.
Попадая в клетки человеческого организма, цитомегаловирус способен оставаться в нем пожизненно.
Возбудитель (Cytomegalovirus hominis) относится к вирусам герпеса (семейство Herpesviridae)
Резервуаром и источником инфекции является только человек. Вирус может находиться в слюне, молоке, моче, испражнениях, семенной жидкости, в секрете шейки матки.
У 20-30% здоровых беременных женщин ЦМВ присутствует в слюне, 3-10 % - в моче, 5-20% - в цервикальном канале или вагинальном секрете.
Кровь около 1% доноров содержит цитомегаловирус.
Хотя, вирусные частицы могут быть обнаружены по всему телу, цитомегаловирус, чаще всего, ассоциирован со слюнными железами.
Cпособы передачи инфекции
Цитомегаловирусная инфекция распространяется не только через слюну при близких контактах, но и во время полового контакта, через кровь, от беременной матери плоду, а также контактно-бытовым путем.
Наибольшую опасность для плода представляет первичная инфекция на ранних сроках беременности. Возбудитель, проникший в плод через кровь в ранние сроки беременности, вызывает формирование врожденных пороков развития.
При наличии инфекции в канале шейки матки у беременной, заражение плода может происходить в родах, во время прохождения плода по родовым путям.
Основной путь заражения ребенка до года – передача вируса через грудное молоко.
Источником заражения детей до 5-6 лет являются матери, выделяющие вирус со слюной или мочой.
Дети, находящиеся в организованных коллективах заражаются чаще контактно-бытовым путем.
Заражение в возрасте 16-30 лет происходит, как правило, при близком контакте через поцелуи и половым путем.
Переливание крови и другие манипуляции с кровью также могут приводить к заражению цитомегаловирусом.
Симптомы цитомегаловирусной инфекции
В здоровом организме вирус никак себя не проявляет, но может быть смертельно опасен для людей с иммунодефицитами: для ВИЧ-инфицированных, больных, после трансплантации органов, а также ожидающих трансплантацию, новорождённых.
При врожденной цитомегаловирусной инфекции характер поражения плода зависит от срока его заражения. Особенно опасно острое инфицирование матери в первые 20 недель беременности.
К чему может привести заражение в ранние сроки беременности?
Внутриутробная гибель плода;
Грубые врожденные пороки (анэнцефалия, микроцефалия, гидроцефалия, нарушение строения легких, бронхиального дерева, аномалии строения почек и др.).
Врожденные пороки в большинстве случаев несовместимы с жизнью.
При заражении ЦМВ в более поздние сроки беременности формирования пороков развития не происходит.
К чему приводит заражение ребенка цитомегаловирусом во время родов?
Клинические признаки, как правило, появляются через 1-2 месяца после родов.
Поражение легких (пневмония);
Увеличение печени, селезенки;
Поражение желудочно-кишечного тракта;
Заболевание может носить длительный рецидивирующий характер.
Максимальная летальность от цитомегаловирусной инфекции приходится на 2-4 месяц.
Профилактика цитомегаловирусной инфекции
Во время консультирования беременных женщин, или планирующих беременность необходимо информировать о главных источниках и путях инфицирования (половые контакты с инфицированными ЦМВ партнерами, физический контакт при ежедневном уходе за ребенком дома или профессиональный контакт с детьми младшего возраста в стационарах, домах ребенка, дошкольных учреждениях).
Для снижения риска первичного заражения ЦМВ беременным женщинам, использовать барьерные контрацептивы при половых контактах, соблюдать правила личной гигиены (мыть руки после прикосновения к дверным ручкам, прикосновения к игрушкам, испачканными слюной , мочой ребенка), не рекомендуется доедать или допивать за детьми, использовать совместную посуду, нельзя облизывать соску. Необходимо избегать поцелуев в губы детей грудного возраста, которые могут выделять вирус со слюной.
При планировании переливания крови недоношенному ребенку или взрослому человеку с ослабленной иммунной системой, необходимо осуществлять проверку крови и ее компонентов на наличие ДНК ЦМВ.
480 руб. | 150 грн. | 7,5 долл. ', MOUSEOFF, FGCOLOR, '#FFFFCC',BGCOLOR, '#393939');" onMouseOut="return nd();"> Диссертация, - 480 руб., доставка 1-3 часа, с 10-19 (Московское время), кроме воскресенья
Автореферат - бесплатно , доставка 10 минут , круглосуточно, без выходных и праздников
Павлова Мария Владимировна. Диагностика цитомегаловирусной инфекции у недоношенных новорожденных детей и оценка анти-ЦМВ активности новых мембраноактивных полианионных соединений in vitro : диссертация . кандидата биологических наук : 03.00.06 / Павлова Мария Владимировна; [Место защиты: Науч.-исслед. ин-т вирусологии им. Д.И. Ивановского РАМН].- Москва, 2008.- 155 с.: ил. РГБ ОД, 61 08-3/766
Введение к работе
. Актуальность проблемы.
Цитомегаловирусная инфекция (ЦМВИ) является одной из самых распространенных причин врожденных вирусных инфекций и может вызывать тяжелые патологии, вплоть до гибели ребенка (Орехов и др., 2004; Alford et al., 1990; Gaytant et al., 2002) По данным отечественных и зарубежных специалистов от 0,5 до 5% детей появляются на свет с врожденной ЦМВИ, из них около 90% детей являются бессимптомными носителями (Kenneson et al., 2007; Gaytant et al., 2002) Вместе с тем, субклиническая форма ЦМВИ не означает гарантии благополучия в дальнейшем у 5-15% таких детей в ближайшие 1-2 года и в более поздние сроки регистрируются нарушения ЦНС, органов слуха, зрения, отмечается детский церебральный паралич, отставание в умственном развитии, плохая успеваемость в школе (Michaels, 2007; Suresh et al, 1999)
Диагностика ЦМВИ у новорожденных детей часто представляет сложную задачу в связи с отсутствием типичных симптомов и признаков ЦМВИ, а также из-за особенностей иммунной системы новорожденных Недоношенные новорожденные представляют группу высокого риска по развитию ЦМВИ, так как известно, что заболеваемость у таких детей повышена по сравнению с доношенными новорожденными (Yamamoto et al., 2001) Несмотря на многочисленные исследования, посвященные этой проблеме, разработка четких и общепринятых рекомендаций по лабораторному обследованию недоношенных новорожденных с сочетанной перинатальной патологией с подозрением на ЦМВИ в России остается нерешенной задачей. Важность решения проблемы своевременного выявления врожденной и перинатальной ЦМВИ объясняется также тем, что именно ЦМВИ часто служит причиной гибели детей во втором полугодии жизни (Долгих и др, 1999).
Не менее важной проблемой является выбор адекватной терапевтической тактики лечения новорожденных с ЦМВИ. Существующие в настоящее время единичные патентованные препараты, обладающие противовирусной активностью в отношении ЦМВ, не применяются у новорожденных и детей раннего возраста вследствие их высокой токсичности Кроме того, эффективность лечения имеющимися препаратами снижена из-за развития лекарственной устойчивости, часто возникающей при длительном применении (Biron et al, 2006, Chou et al., 1999). Поэтому поиск эффективных и нетоксичных анти-ЦМВ агентов, перспективных в качестве химиотерапевтических средств при ЦМВИ, остается важной и актуальной проблемой
Цель и задачи исследования.
Цель настоящего исследования заключалась в изучении маркеров ЦМВИ у недоношенных новорожденных детей и детей раннего возраста с сочетанной перинатальной
патологией в течение первого года жизни, а также в исследовании антивирусной активности новых поликарбоксилатных соединений, модифицированных мембранотропными и аминосульфокислотными фармакофорами на модели экспериментальной ЦМВИ in vitro.
Для достижения поставленной цели ставились следующие задачи:
Выявить прямые маркеры ЦМВ (ДНК и инфекционную активность) у недоношенных новорожденных и детей раннего возраста с сочетанной перинатальной патологией
Установит присутствие противовирусных антител классов IgM и IgG и индекс авидности антител IgG у недоношенных новорожденных детей с клиническими признаками внутриутробного инфицирования.
Изучить динамику маркеров ЦМВИ у недоношенных новорожденных детей в течение первого года жизни.
4 Определить цитотоксичность и антивирусную активность новых поликарбоксилатных соединений, модифицированных мембранотропными и аминосульфокислотными фармакофорами, на модели экспериментальной ЦМВИ in vitro в лечебной, профилактической, вирулицидной и микробицидной схемах воздействия.
5. Выяснить возможный механизм анти-ЦМВ активности новых поликарбоксилатных соединений.
Научная новизна и практическая значимость.
1. Установлено, что для достоверной диагностики ЦМВИ у недоношенных новорожденных и детей раннего возраста необходим комплекс методов, включающих выявление противовирусных антител и их авидности, а также обнаружение прямых маркеров ЦМВ.
Изучение динамики маркеров ЦМВ у недоношенных новорожденных детей в течение первого года жизни показало необходимость проведения неоднократного вирусологического обследования данной группы риска по развитию ЦМВИ минимум до 1 года.
Впервые установлено, что новые поликарбоксилатные соединения, модифицированные мембранотропными и аминосульфокислотными фармакофорами, обладают низкой цитотоксичностью и высокой антивирусной анти-ЦМВ активностью
4. Впервые показано, что мембраноактивные полианионные соединения обладают
двунаправленным действием на ЦМВ предотвращают его проникновение в чувствительные
клетки и обладают внутриклеточным противовирусным действием.
Основные положения, выносимые на защиту.
1 Показана высокая частота выявления ЦМВИ у недоношенных маловесных новорожденных детей с сочетанной перинатальной патологией по сравнению с доношенными новорожденными детьми
2. Установлена необходимость проведения неоднократного (по крайней мере, трехкратного) вирусологического обследования детей из этой группы риска по развитию ЦМВИ в течение первого года жизни
3 Среди новых мембраноактивных полианионных соединений выявлены соединения, обладающие низкой циготоксичностью и высокой антивирусной анти-ЦМВ активностью Максимальный эффект противовирусного действия установлен для AS-688, химиотерапевтический индекс для которого в вирулицидной, микробицидной и лечебной схемах воздействия составляет не менее 3000.
4. Показано, что мембраноактивные полианионные соединения эффективно подавляют проникновение ЦМВ в чувствительные клетки, а также ингибируют накопление вирусной ДНК и экспрессию поздних структурных белков ЦМВ в зараженных клетках.
Апробация работы.
Структура и объем диссертации.

Дата публикации: 19.05.2015 2015-05-19
Статья просмотрена: 782 раза
Проанализированы истории болезней 100 детей, находившихся на стационарном лечении в 2012–2013 году в ДГКИБ г. Алматы, из них 52 больных с цитомегаловирусной инфекцией (ЦМВИ) в активной фазе. Диагноз ЦМВИ у обследованных детей верифицированы методами иммуноферментного анализа. Последующее наблюдение за ними осуществлялось до марта 2014года. Изучены особенности анамнестических данных, клинического течения и дальнейшего развития ребенка.
Перинатальными факторами риска развития ЦМВИ являются: отягощенный акушерский анамнез (35 %), осложненное угрозой прерывания (19 %), преждевременные роды (19 %).
Ключевые слова: внутриутробная инфекция, цитомегаловирусная инфекция, поражения центральной нервной системы, врожденные пороки развития, задержка психомоторного развития.
Analyzed 100 medical records of children who were on hospital treatment in 2012–2013 СНID in Almaty, 52 of them were with the active phase of cytomegalovirus infection (CMVI).
Diagnosis of CMVI of examined children were verified by enzyme immunoassay. Next observation carried out until March 2014. Also studied features of anamnesis, clinical course and further development of the child. Perinatal risk factors for CMV infection were: burdened obstetrical history (35 %), threat of termination of pregnancy (19 %), miscarriage (19 %).
Keywords:intrauterine infection, cytomegalovirus infection, central nervous system, congenital malformations, jaundice, deafness, delayed psychomotorical development.
В последние годы участились случаи внутриутробных инфекций (ВУИ) у новорожденных, в частности цитомегаловирусной инфекций (ЦМВИ). В республике Казахстан, среди причин смертности в раннем неонатальном периоде, ВУИ составляют 6–8 %, среди них ЦМВИ является причиной многих тяжелых заболеваний, которые могут привести к серьезным последствиям, а нередко и к летальному исходу. ЦМВИ вызывается цитомегаловирусом человека, который относится к семейству Herpesviridae и является типичным представителем рода Cytomegalovirus.
По данным экспертов ВОЗ:
- 1,5 % новорожденных инфицированы ЦМВ;
- 0,3 % вирусом простого герпеса.
В период беременности вероятность первичного инфицирования повышается и составляет около 54 %. Почти 41 % новорожденных от таких матерей страдают ЦМВИ.
Среди всех новорожденных приблизительно 1–2 % инфицированы ЦМВ в период внутриутробного развития. 6–60 % детей заражаются в первые 6 месяцев жизни при прохождении через родовые пути и через грудное молоко.
Высокая распространенность цитомегаловирусной инфекции (ЦМВИ), рост ее удельного веса среди этиологических факторов перинатальной патологии [7], а также сложности диагностики, сходство клинических проявлений различных внутриутробных инфекций и малодоступность современных методов диагностики [3] определяет актуальность проблемы ЦМВИ.
Целью нашей работы является оценка состояния здоровья детей перенесших цитомегаловирусную инфекцию.
1. Изучить клинические особенности ЦМВИ
2. Катамнестическое наблюдение в 6–12–24 месяцев.
Материалы и методы:
Мы проанализировали 100 истории болезни детей, находившихся на стационарном лечении в 2012–2013 году в ДГКИБ г. Алматы, из них 52 больных с ЦМВИ в активной фазе.
Последующее наблюдение за ними осуществлялось до марта 2014 года.
Точки исследования: Т0 — при рождении (по истории болезни); Т1- 6 месяцев; Т2–1 год; Т3- 2 года.
Диагноз у всех 52 больных ЦМВИ подтвержден серологическим методом (ИФА): Anti — CMV — IgM+++ у 76 % (40), Anti — CMV — IgG+++92,3 % (44), ИФА матери Anti — CMV — IgG+++81 % (42) и полимеразной цепной реакцией (ПЦР):Моча, слюна +++ 61,5 % (32).
Результаты исследования:
В возрастном аспекте и по полу обследованные дети распредилялись следующим образом:
По возрасту: с 26 недель до 1,5 месяцев — 20, до 3 месяцев — 12, с 3 до 10 месяцев — 20 пациентов.
По полу: мальчики — 32, девочки — 20.
Среди этих детей недоношенных было 6, с весом от 1800 до 3400г, с гестационным сроком 32–34 (2) недель.
Обследование матерей в период нахождения их с больными ЦМВИ детьми, дало положительный результат на цитомегаловирус у всех женщин, что свидетельствует о внутриутробном инфицировании их детей.
У 29 % женщин было физиологическое течение беременности, у 35 % отягощенный акушерский анамнез, у 21 % патологическое течение беременности и родов, так же у 15 % женщин были выявлены экстрагенитальные заболевания.
В активный период ЦМВИ у значительной части больных отмечалось тяжелое состояние (33,8 %) и полисистемность поражения (66,2 %):
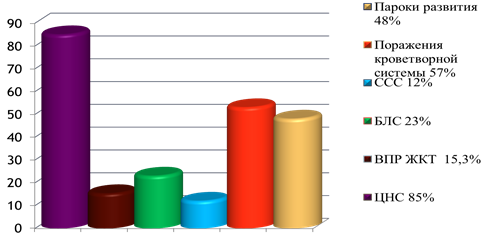
В раннем неонатальном периоде у инфицированных детей на первый план выступали выраженные нарушения со стороны ЦНС. Ведущими признаками являлись: гипертензионно-гидроцефальный синдром (14 %), судорожный синдром (24 %), синдром угнетения (16 %), синдром высокой нервно рефлекторной возбудимости (20 %), синдром двигательных нарушении (10 %), ГИП ЦНС (16 %).
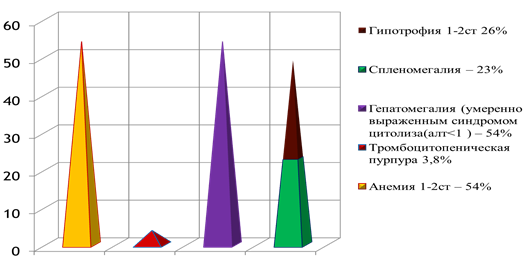
Из других клинических проявлений наиболее часто встречались:
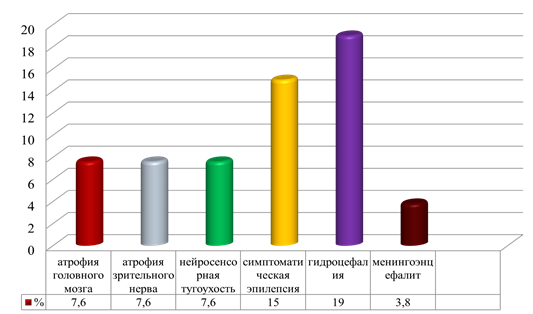
В позднем неонатальном периоде у детей были выявлены тяжелые органические поражения ЦНС в виде врожденных пороков развития головного мозга: атрофия головного мозга, атрофия зрительного нерва, нейросенсорная тугоухость, симптоматическая эпилепсия, гидроцефалия, менингоэнцефалит.
Кроме этого, у инфицированных детей на первом месяце жизни диагностировались: длительная желтуха (12 %), гипотрофия 1–2 степени (32 %), дисбактериоз (11,5 %), ИМВП (15,3 %).
Отмечалась гипербилирубинемия у 46,1 % детей. За счет прямого билирубина у 30,7 % больных (44,8+-100мкмоль/л). За счет непрямого билирубина у 15 % (30+-96мкмоль/л).
Наблюдение в катамнезе показало, что в 6-месячном возрасте у большинства больных (76,9 %) ЦМВИ была в неактивном периоде. Это сопровождалось обратным развитием клинических симптомов, отсутствием специфических анти-ЦМВ Ig. Лишь у 12 (23 %) сохранялись клинические симптомы активного периода при отсутствии IgМ анти-ЦМВ.
В возрасте 1 года у четверых детей наблюдался рецидив ЦМВИ с положительным подтверждением на ИФА IgМ анти-ЦМВ. В клинической картине у одного ребенка был двусторонний гнойный отит, у второго ребенка отмечалась слабость, повышение температуры до 38,5, снижение аппетита, явления атопического дерматита.
Через 1 год установлено значительное отставание в физическом развитии у 16 детей (31 %).
В годовалом возрасте у детей с ЦМВИ были достоверно ниже показателей нормы масса тела и рост.
- КЛЮЧЕВЫЕ СЛОВА: инфекция, легкие, печень, почки, мертворожденные дети, цитомегалия, иммуноглобулин, Виферон
Клетки, пораженные цитомегаловирусом (ЦМВ) и впервые описанные в 1882 г. немецким патологоанатомом Н. Ribbert, были выявлены в эпителии околоушных слюнных желез и мочевых канальцев, имели гигантские размеры и своеобразные внутриядерные включения. Впоследствии такие клетки были обнаружены в легких, печени, почках и других органах мертворожденных детей с цитомегаловирусной инфекцией (ЦМВИ).
В 1921 г. E. Goodpasture и F. Talbot предложили назвать болезнь детской цитомегалией, подчеркнув специфичность гигантоклеточного метаморфоза пораженных клеток. Вирус был выделен в 1956 г. М. Smith.
Цитомегаловирусная инфекция – общее инфекционное заболевание, вызываемое герпесвирусом человека 5-го типа (семейство Herpesviridae, подсемейство Beta-herpesviridae) и характеризующееся многообразием форм – от бессимптомных до генерализованных. Морфологически проявляется образованием в слюнных железах, висцеральных органах и центральной нервной системе цитомегалов – гигантских клеток с типичными внутриядерными и цитоплазматическими включениями. Возбудитель (Cytomegalovirus hominis) относится к медленно размножающимся цитолитическим вирусам, вызывающим цитомегалию клеток и латентную инфекцию в слюнных железах и почках. Вирион содержит дезоксирибонуклеиновую кислоту (ДНК), имеет размер 150–300 нм. Вирус состоит из капсида, вирусной оболочки и слабо характеризованной области под названием tegument.
Вирусный геном представлен двойной молекулой ДНК и несет генетическую информацию о синтезе 100 вирусных протеинов. Капсид, окружающий вирусный геном, состоит из 162 капсомеров – нефосфорилированных протеинов. Область между вирусным геномом и оболочкой (tegument) представлена 20 белками, многие из которых фосфорилированы. Главный фосфорилированный белок pp UL83 (pp65) составляет 95% tegument и вместе с главным структурным белком pp UL32 (pp150) имеет значение в диагностике ЦМВИ.
Вирус цитомегалии обладает строгой видовой специфичностью, термолабилен, инактивируется при температуре 56 °С, но сохраняется при комнатной температуре, быстро теряет инфекционность при замораживании. Оптимальные условия его жизнедеятельности в биологических объектах – рН 7,2–8,0, температура 4 °С. Вирус характеризуется слабым интерфероногенным действием, нечувствителен к антибиотикам.
На сегодняшний день известно шесть штаммов ЦМВИ (Davis, AD 169, Kerr, C-87, Esp, Towne). Не исключена возможность возникновения суперинфекции. Как и все остальные герпесвирусы, ЦМВ после внедрения в организм способен переходить в латентное состояние, которое периодически сменяется реактивацией с возможностью выделения вируса из организма с любыми биологическими жидкостями. Пребывание в детских учреждениях, школах способствует распространению ЦМВИ среди детей разного возраста. При этом инкубационный период при заражении ЦМВ составляет от 15 дней до трех месяцев.
По эпидемиологическим данным, ЦМВИ заболевают на всех континентах, во всех социально-экономических группах. В США процент инфицированных варьируется в пределах 50–80% взрослого населения. Доля сероположительных лиц зависит от возраста: в возрасте от шести лет инфицировано 58,9% индивидов, старше 80 лет – 90,8% 1 .
Основными группами риска по ЦМВИ являются беременные, новорожденные, особенно недоношенные, дети с иммунодефицитными состояниями, ВИЧ-инфицированные, внутривенные наркопотребители, реципиенты гемотрансфузий и трансплантатов, лица пожилого возраста, пациенты, принимающие лекарственные препараты (антибиотики, химиопрепараты, гормоны, рентгенотерапию и др.). Кроме того, к группе риска относится медицинский персонал родильных домов, отделений интенсивной терапии, перинатальных центров.
ЦМВ обнаруживается в различных биологических жидкостях инфицированного человека: грудном молоке, слезной жидкости, носоглоточной слизи, крови, слюне, моче, ликворе, сперме, цервикальном и вагинальном секрете, фекалиях.
Известно несколько путей заражения ЦМВИ: трансплацентарный, интранатальный, контактный, воздушно-капельный, фекально-оральный, контаминационный и половой.
Цитомегалия относится к персистирующим инфекциям, что дает основание рассматривать ее как одну из форм взаимодействия микро- и макроорганизма на клеточном уровне, позволяющих вирусу длительное время находиться в организме человека. Персистенцию рассматривают как разновидность облигатного внутриклеточного паразитизма вирусов в лейкоцитах, системе мононуклеарных фагоцитов, эндотелии сосудов, лимфоидных и других органах.
Основными путями внутриутробного инфицирования ЦМВИ являются гематогенный (трансплацентарный), восходящий и нисходящий. При внутриутробном инфицировании плода, как правило, имеет место трансплацентарный путь передачи ЦМВИ. Находящийся в материнской крови вирус проникает через плаценту к плоду по пупочной вене. Инфицирование возможно и при повреждении плаценты. Плод может инфицироваться от матери с латентной или острой формой ЦМВИ. Для трансплацентарной передачи ЦМВИ решающую роль играют длительная и выраженная вирусемия и синдром плацентарной недостаточности. Вероятность инфицирования плода при латентном течении процесса практически отсутствует, при реактивации и хроническом персистирующем течении она составляет 0,5–0,7%, при первичном инфицировании – 40–50%.
При восходящем (трансцервикальном) пути заражение происходит при наличии вируса в цервикальном и вагинальном секретах, а также через инфицированные околоплодные воды, которые заглатывает плод. Нисходящий (трансовариальный) путь внутриутробного заражения ЦМВИ характеризуется проникновением вируса из брюшной полости по маточным трубам. Нисходящий путь развития внутриутробной инфекции возможен только у женщин с очагами хронического воспаления в яичниках и маточных трубах.
ЦМВИ отличается от большинства внутриутробных инфекций тем, что плод чувствителен к ней на всех этапах развития. В зависимости от срока гестации, на котором произошло инфицирование ЦМВ, различают инфекционные бластопатии, эмбрио- и фетопатии.
Интранатально заражается до 5–7% новорожденных как путем непосредственного контакта с инфицированными тканями родового канала, так и при аспирации околоплодных вод, содержащих ЦМВ.
В постнатальном периоде новорожденный заражается в 30% случаев от выделений матери, содержащих вирус: слюны, мочи, выделений из гениталий, грудного молока, крови. Риск инфицирования новорожденного возникает во время родов или сразу после рождения от медицинского персонала в случае вирусоносительства, а также при переливании компонентов крови 2 .
Характер поражения плода и новорожденного зависит от сроков инфицирования и отличается многообразием проявлений – от серьезных дефектов развития, генерализованных форм до бессимптомного течения.
Врожденная ЦМВИ манифестирует в течение первых двух-трех недель жизни ребенка. При появлении симптомов болезни после третьей недели жизни можно говорить о постнатальном инфицировании.
ЦМВИ относится к группе TORCH-инфекций и чревата серьезными последствиями у новорожденных. Клиническая картина острой формы врожденной ЦМВИ характеризуется наиболее тяжелым течением с признаками гипотрофии второй-третьей степени, длительной желтухой, пневмонией, сиалоаденитом, панкреатитом, поражением почек, микроцефалией, хориоретинитом, петехиями. Нередко наблюдаются тромбоцитопения, прогрессирующая анемия.
У детей, перенесших острую форму заболевания, отмечается волнообразное течение хронической формы ЦМВИ. Часто формируются кальцификаты в головном мозге, имеют место микро- или гидроцефалия, нейросенсорная глухота, церебральный паралич, задержка психомоторного и речевого развития, поражение глаз (атрофия зрительного нерва, катаракта), хронический гепатит, панкреатит, пневмофиброз.
Лабораторная диагностика ЦМВИ основана на выявлении в исследуемых пробах клеток, пораженных цитомегаловирусом, самого вируса и его ДНК, антигенов, а также специфических антител к вирусу.
В настоящее время основными методами лабораторной диагностики ЦМВИ являются цитологический, вирусологический, молекулярно-генетический (полимеразная цепная реакция – ПЦР), иммуноферментный анализ, реакция иммунофлуоресценции.
Характерный патоморфологический признак ЦМВИ – цитомегалические клетки, выявляемые в тканях, слюне, мокроте, осадке мочи и цереброспинальной жидкости. При исследовании в световом микроскопе клетки в слюнных железах имеют вид совиного глаза. В ядре цитомегалических клеток формируется плотное внутриядерное включение, отделенное от оболочки ядра светлой оптически пустой зоной. Эти клетки настолько специфичны, что при их обнаружении не требуется вирусологического подтверждения диагноза ЦМВИ.
Диагностическими критериями острой врожденной ЦМВИ служат клинические проявления, развившиеся в первые три месяца жизни ребенка, обнаружение антигена вируса в моче, крови, наличие иммуноглобулинов М и G в крови, низкоавидных антител (индекс авидности до 30%) и определение ДНК или антигена вируса в лейкоцитах крови.
Цели лечения при ЦМВИ – устранение симптомов острой формы заболевания и удержание вируса в пассивном, неактивном состоянии. В остром периоде ЦМВИ применяют этиотропную и посиндромную терапию. Этиотропная терапия предполагает применение противовирусных препаратов (виростатиков), специфического гипериммунного антицитомегаловирусного иммуноглобулина (Цитотект/Неоцитотект) и интерферонов.
К этиотропной терапии прибегают только в фазе репликации вируса, при наличии клинических симптомов и выявлении специфических низкоавидных иммуноглобулинов G и/или иммуноглобулинов М.
При тяжелой генерализованной форме ЦМВИ используют виростатические препараты – ганцикловир, фоскарнет. Применение ганцикловира имеет возрастные ограничения: детям препарат назначают, если польза от лечения превышает существенный риск.
Особое место в лечении детей с ЦМВИ занимают интерфероны. Противовирусный эффект – одно из основных свойств интерферонов. В невысоких терапевтических дозах они являются модуляторами иммунитета, что позволяет отнести их к семейству регуляторных цитокинов.
Введение экзогенного интерферона обеспечивает элиминацию инфекционного агента задолго до того, как собственные клетки начинают синтезировать интерферон в необходимом количестве. Поступление интерферона помогает разгрузить пораженные клетки и компенсировать недостаток в продукции собственного интерферона в достаточном количестве. При лечении внутриутробной ЦМВИ экзогенный интерферон жизненно необходим в связи с возрастными различиями свойств интерферона у новорожденных, который не обладает противовирусным эффектом и направлен в первую очередь на пролиферацию, а не на борьбу с вирусами. Это показано в фундаментальных работах по изучению системы интерферона в России и за рубежом 3 . Ускоренная элиминация инфекционного агента при введении экзогенного интерферона сокращает сроки инфекционного процесса.
Научными сотрудниками Ярославской государственной медицинской академии в 2016 г. был запатентован способ лечения генерализованной ЦМВИ у детей раннего возраста. Предложена комбинированная схема противовирусного лечения. При вирусной нагрузке 10 5 коп/мл и более применяется ганцикловир (Цимевен) в дозе 5–7,5 мл/кг в течение 14–21 дня. Препарат отменяют при достижении положительной динамики и снижении вирусной нагрузки в крови до 10 4 –10 3 коп/мл. Далее лечение продолжают препаратом ВИФЕРОН® (150 000 МЕ) по схеме: один суппозиторий два раза в сутки в течение десяти дней, затем – по одному суппозиторию три раза в неделю (понедельник, среда, пятница).
Данную схему применяли в клиническом исследовании: 48 детей с ЦМВИ получали ганцикловир (Цимевен) под контролем количества вируса в сыворотке крови на 14-й и 21-й дни от начала лечения. Далее в течение 3–6 месяцев ежемесячно контролировали вирусную нагрузку методом ПЦР. Группа из 22 детей перешла на Виферон®. При достижении полной элиминации вируса из крови (отрицательной ПЦР) лечение препаратом Виферон® завершали. Результаты наблюдения показали, что рецидив ЦМВИ не зафиксирован ни у одного ребенка, получавшего комбинированную терапию. В группе из 26 детей, не принимавших Виферон®, вирусная нагрузка оставалась на прежнем уровне (11 пациентов) или увеличивалась на 10 1–2 коп/мл (15 пациентов), что свидетельствовало о репликации вируса и продолжении инфекционного процесса. Исследователи сделали вывод, что внедрение новой схемы терапии ЦМВИ у детей может приводить к успешной эрадикации инфекции.
Таким образом, ЦМВИ остается актуальной проблемой в педиатрической практике. Эффективный подход к противовирусной терапии ЦМВИ должен включать комбинацию препаратов различных групп разнонаправленного действия.
Читайте также:


