Большими диагностическими duke критериями инфекционного эндокардита являются
Справочник болезней

Инфекционного эндокардита
• Ревматическая болезнь сердца.
• Врожденные (цианотичные) пороки сердца.
• Искусственные клапаны сердца.
• Гемодиализ.
• Венозные катетеры.
• Внутривенное введение препаратов.
• Иммунодепрессанты.
• Пожилой и старческий возраст.
Тромбоэмболий
• Вегетации >10 мм (Mohananey D, et al, 2018).
• Флотирующие вегетации.
• Поражение митрального клапана.
• Инфекция Staph. aureus.
БОЛЬШИЕ КРИТЕРИИ
1. Положительная культура крови
1.1. Типичные микробы в 2 пробах крови:
• Str. viridans, Str. gallolyticus (bovis), Staph. aureus, HACEK группа.
• Внебольничные Enterococci без первичного очага.
1.2. Повторные культуры крови, характерные для ИЭ:
• ≥2 культур крови с интервалом >12 ч.
• Все 3 культуры крови или большинство из ≥4 проб.
1.3. Культура Coxiella burnetti или IgG в титре >1:800.
2. Визуальные признаки
2.1. Эхокардиографические признаки:
• Вегетация,
• Абсцесс, псевдоаневризма, интракардиальная фистула.
• Перфорация или аневризма клапана.
• Новое частичное раскрытие искусственного клапана.
2.2. Аномальная активность возле искусственного клапана по 18Ф-ФДГ ПЭТ/КТ (имплантация >3 мес) или СПЕКТ/КТ сцинтиграфии с меченными лейкоцитами.
2.3. Паравальвулярное повреждение по КТ сердца.
МАЛЫЕ КРИТЕРИИ
1. Предрасполагающие заболевания сердца, инъекции.
2. Лихорадка >38°С.
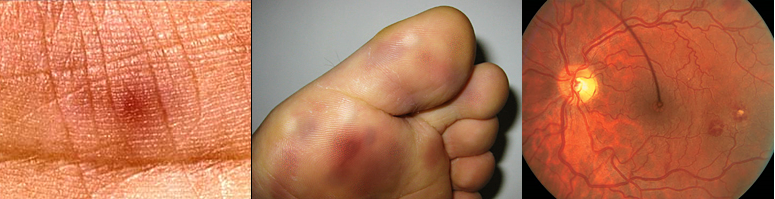
3. Сосудистые феномены: эмболии крупных артерий, септические инфаркты легких, микотические аневризмы, внутричерепные кровоизлияния, кровоизлияния в конъюнктиву, повреждения Джейуэя.
4. Иммунные нарушения: гломерулонефрит, узелки Ослера, пятна Рота, ревматоидный фактор.
5. Культура крови, не соответствующая большим критериям, или серологические признаки активной инфекции микробом, способным вызвать ИЭ.
Определенный ИЭ = 2 больших, или 1 большой + 3 малых, или 5 малых.
Вероятный ИЭ = 1 большой + 1 малый или 3 малых.
Лечение острого ИЭ до выявления микроба
• Ампициллин + Оксациллин по 12 г/сут в 4 приема в/в + Гентамицин 3 мг/кг однократно в/в, в/м.
• Ванкомицин 30 мг/кг/сут в 2 приема в/в + Гентамицин 3 мг/кг однократно в/в, в/м.
• Ванкомицин 30 мг/кг/сут в 2 приема в/в + Гентамицин 3 мг/кг однократно в/в, в/м + Рифампин 900–1200 мг в 2 приема в/в, per os при нозокомиальном или раннем эндокардите искусственного клапана.
Стрептококк, чувствительный к пенициллину
• Цефтриаксон 2 г однократно или Амоксициллин 100–200 мг/кг/сут в 4 приема в/в [4 нед].
• Цефтриаксон 2 г однократно или Амоксициллин 100–200 мг/кг/сут в 4 приема в/в + Гентамицин 3 мг/кг однократно в/в, в/м [2 нед].
• Ванкомицин 30 мг/кг/сут в 2 приема в/в [4 нед].
Стрептококк, относительно нечувствительный к пенициллину
• Цефтриаксон 2 г однократно или Амоксициллин 200 мг/кг/сут в 4 приема в/в [4 нед] + Гентамицин 3 мг/кг однократно в/в, в/м [2 нед].
• Ванкомицин 30 мг/кг/сут в 2 приема в/в [4 нед] + Гентамицин 3 мг/кг однократно в/в, в/м [2 нед].
• Терапия 6 вместо 4 нед при эндокардите искусственного клапана.
Стафилококк, чувствительный к метициллину
• Оксациллин 12 г/сут в 4 приема в/в [4–6 нед].
• Оксациллин 12 г/сут в 4 приема в/в + Рифампин 900–1200 мг в 2 приема в/в, per os [≥6 нед] + Гентамицин 3 мг/кг однократно в/в, в/м [2 нед] при искусственном клапане.
Стафилококк, нечувствительный к метициллину
• Ванкомицин 30–60 мг/кг/сут в 2 приема в/в [4–6 нед].
• Даптомицин 10 мг/кг однократно в/в [4–6 нед].
• Ванкомицин 30–60 мг/кг/сут в 2 приема в/в + Рифампин 900–1200 мг в 2 приема в/в, per os [≥6 нед] + Гентамицин 3 мг/кг однократно в/в, в/м [2 нед] при искусственном клапане.
Сердечная недостаточность
• Выраженная регургитация или обструкция с симптомами СН или эхокардиографическими признаками нарушенной гемодинамики.
• Отек легких или кардиогенный шок.
Неконтролируемая инфекция
• Локальная: абсцесс, ложная аневризма, фистула, растущие вегетации.
• Инфекция грибами или мультирезистентными микроорганизмами.
• Персистирующая позитивная культура крови, несмотря на адекватную антибиотикотерапию и контроль септических метастатических очагов.
• Эндокардит искусственных клапанов, вызванный стафилококками или не-HACEK грамотрицательными бактериями.
Профилактика эмболий
• Эндокардит аортального или митрального клапанов с персистирующими вегетациями >10 мм после ≥1 эмболического эпизода, несмотря на адекватную антибиотикотерапию.
• Эндокардит аортального или митрального клапанов с изолированными вегетациями >30 мм.


Автореферат диссертации по медицине на тему Сравнительная оценка диагностических критериев инфекционного эндокардита
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ЗДРАВООХРАНЕНИЮ И
СОЦИАЛЬНОМУ РАЗВИТИЮ НОВОСИБИРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
На правах рукописи
ЗАРБУЕВА Юлия Александровна
СРАВНИТЕЛЬНАЯ ОЦЕНКА ДИАГНОСТИЧЕСКИХ КРИТЕРИЕВ ИНФЕКЦИОННОГО ЭНДОКАРДИТА
14 00 05 - внутренние болезни 14 00 06 - кардиология
Автореферат диссертации на соискание ученой степени кандидата медицинских наук
доктор медицинских наук,
профессор Демин Александр Аристархович
доктор медицинских наук,
профессор Дробышева Вера Петровна
доктор медицинских наук,
профессор Поспелова Татьяна Ивановна
доктор медицинских наук,
профессор Гафаров Валерий Васильевич
диссертационного совета /л, ¿ио ио^ уи. при Новосибирском государственном медицинском университете (630091, г Новосибирск, Красный проспект, 52)
С диссертацией можно ознакомиться в медицинской библиотеке Новосибирского государственного медицинского университета
Ученый секретарь Диссертационного совета доктор медицинских наук, профессор
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. В развитых странах частота инфекционного эндокардита (ИЭ) снижалась в течение всего XX века вследствие уменьшения постревматических клапанных поражений сердца и положительного влияния антимикробной терапии и профилактики Тем не менее, последние исследования показали, что в России отмечается рост этого опасного заболевания [Барт Б Я , 2005, Демин А А, 2003, 2006, Тюрин В П , 2001], а в Европе и США нет тенденции к уменьшению частоты [Ноеп В et al, 2002]. Диагностика ИЭ улучшилась, в основном, в результате усовершенствования эхокардиографического и микробиологического подходов Несмотря на определенные достижения, ИЭ остается тяжелым заболеванием с высокой летальностью, вопросы диагностики заболевания постоянно привлекают внимание специалистов [Гогин Е Е, Демин А А, 2006, Дробышева В П, 2003, Комаров В Т, 2005, Тюрин В П, 2001]
Д ля верификации ИЭ в настоящее время общеприняты и показали свою высокую эффективность диагностические критерии, предложенные Durack D Т et al (1994), а также DUKE-критерии модифицированные Li J et al (2000) Однако по данным В П Тюрина (2001), В П Дробышевой (2003), С Lamas, S Eykyn (2003) сохраняется низкий уровень выявления типичной для ИЭ гемокультуры, в связи с чем, из DUKE-критериев выпадает один большой диагностический критерий и их эффективность значительно снижается. Разработка диагностических критериев, направленных на более радикальное выявление достоверного и отвергнутого ИЭ, при отсутствии типичной для ИЭ гемокультуры, является актуальной
До настоящего времени своевременная диагностика ИЭ - трудная клиническая задача Первые клинические признаки ИЭ могут быть неспецифичны, и болезнь остается нераспознанной в течение недель или даже месяцев Вместе с тем переоценка таких важных признаков, как повышение температуры тела, вегетации на клапанах сердца, обнаруженные при ультразвуковом исследовании, ведет к гипердиагностике ИЭ, то есть первоначально ошибочному диагнозу [Белов Б С, 2003, Дробышева В П, 2003, Колесников С А, Симоненко ВБ, 1998, Комаров ВТ, 2005, Ребров А П и соавт, 2000] Клиническая ценность распространенных Duke критериев (1994) диагноза инфекционного эндокардита (ИЭ) снижается из-за низкой чувствительности при негативных гемокультурах, ограниченных данных о специфичности и неизвестной роли категории "возможного инфекционного эндокардита"
Последующие модификации Duke критериев ИЭ, в основном, преследовали цель улучшить чувствительность, а специфичность ни в оригинальной работе (Durack et al, 1994), ни в последующих работах сотрудников(1994-2000) не была посчитана Вместе с тем, соответствие новых и прежних диагностических критериев необходимо для сравнения современных и архивных баз данных инфекционного эндокардита
Цель исследования. Провести сравнительную оценку новых и прежних диагностических критериев инфекционного эндокардита
1 Изучить причины гипер- и гиподиагностики инфекционного эндокардита
2 Разработать собственную модификацию диагностических Duke-критериев и провести ее сравнительную оценку с известными диагностическими критериями инфекционного эндокардита
3 Изучить и провести сравнительную оценку чувствительности и специфичности диагностических критериев инфекционного эндокардита
Уровень гипер- и гиподиагностики инфекционного эндокардита сохраняется высоким, что обусловлено полиморфностью симптоматики, недооценкой важных диагностических признаков или неполнотой клинической картины.
Практическая значимость. Анализ ошибок диагностики указывает на возможность нахождения больных в любом лечебном учреждении, что требует знания современной клинической картины и диагностических критериев ИЭ терапевтами, кардиологами, ревматологами, нефрологами, пульмонологами, инфекционистами, наркологами, геронтологами и другими специалистами Предлагаемые нами модифицированные диагностические DUKE-критерии будут способствовать своевременной диагностике ИЭ Ранее разработанные А А Деминым и Ал А Деминым (1978) диагностические критерии менее зависимы от результатов исследования гемокультуры, не зависят от технического оснащения (ультразвуковой диагностики) Это важно для раннего выявления ИЭ и допускает возможность их применения в практике врача интерниста
Основные положения, выносимые на защиту:
2 Равновысокая степень соответствия новых (Duke-критерии) и прежних диагностических критериев (Р>0,5) делает правомочным сравнение современных и архивных баз данных инфекционного эндокардита
3 Уровень гипер- и гиподиагностики инфекционного эндокардита при первом контакте с врачом сохраняется высоким, что обусловлено полиморфностью симптоматики, недооценкой важных диагностических признаков или неполнотой клинической картины.
Внедрение. Диагностические Duke-критерии в модификации А А Демина и соавт, 2006 внедрены в практику работы МУЗ МКБСМП №2 г Новосибирска Материалы диссертации получили отражение в учебном процессе кафедры госпитальной терапии и клинической фармакологии лечебного факультета НГМУ
Апробация работы Апробация диссертации состоялась на заседании экспертного Совета при диссертационном Совете Д 208 06 02 Новосибирского государственного медицинского университета 05 10 07 г
Публикации. По теме диссертации опубликовано 7 работ, из них 1 в журнале, рекомендованном ВАК
Структура и объем диссертации. Работа изложена на 177 страницах печатного текста, состоит из введения, обзора литературы, четырех глав полученных результатов и их обсуждения, заключения, выводов и практических рекомендаций, содержит 43 таблицы и 25 рисунков Библиография включает 108 отечественных и 65 иностранных авторов Весь представленный материал получен, обработан и проанализирован лично автором
Материал и методы исследования.
Работа выполнена на кафедре госпитальной терапии и клинической фармакологии НГМУ
Всего обследовано 260 больных Из них 150 больных ИЭ (у 70 больных диагноз ИЭ установлен на догоспитальном этапе, у 80 больных ИЭ
верифицирован в клинике) и 110 пациентов, у которых ИЭ диагностирован ошибочно Дизайн исследования представлен на рис 1
Рис 1 Когортное проспективное исследование (дизайн)
4 Лихорадка 31 (28,2%) 110(73,3%) 0,5) для диагностики ИЭ, в связи с чем мы исключили его из предложенной модификации Duke - критериев
Известно, сто спленомегалия является признаком системной реакции лимфоидной ткани на генерализованную инфекцию По данным Тюрина В П (2001) спленомегалия при ИЭ выявлена в 76,2% случаев на аутопсии По данным А А Демина и В П Дробышевой (2002) спленомегалия была выявлена в 80% случаев верифицированного ИЭ Анализируя результаты настоящего исследования выявлено, что спленомегалия (67 - 44,6% больных) весьма значима (р 0,5). Весьма значимо (р 0,5) результаты применения ОЦКЕ-критериев (О.Т. Оигаск и соавт., 1994) и ОЦКЕ-критериев в модификации ]. 1л и соавт. (2000): диагноз ИЭ отвергнут у 77 (70,0%) и у 78 (71,1%) больных, соответственно. Согласно предложенной модификации ОЦКЕ-критериев (Демин А.А. и соавт., 2006) диагноз ИЭ отвергнут у 90 (82,0%) больных, что весьма значимо выше (р 0,5 Рн 0,5 Р3-4 4
Таким образом, причины гипердиагностики ИЭ можно разделить на 2 группы 1-я группа - гиперболизация отдельных диагностических признаков при неполной клинической картине заболевания, 2-я группа обусловлена полиморфностью симптоматики ИЭ
Причины гиподиагностики ИЭ при первом обращении к врачу изучали анализируя истории болезни 150 больных с верифицированным ИЭ Из них у 70 (46,7%) больных диагноз ИЭ заподозрен на догоспитальном этапе и верифицирован в нашей клинике. Восемьдесят больных (53,3%) поступили в клинику с другими диагнозами и составили группу гиподиагностики ИЭ (табл 6, 7)
Общая характеристика 80 больных с недиагностированным ИЭ
Признак число больных %
Средний возраст, лет (пределы колебаний) 47(15-79)
ИНФЕКЦИОННЫЙ ЭНДОКАРДИТ
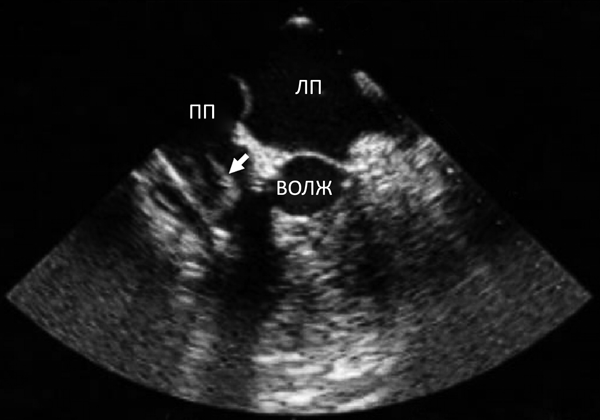
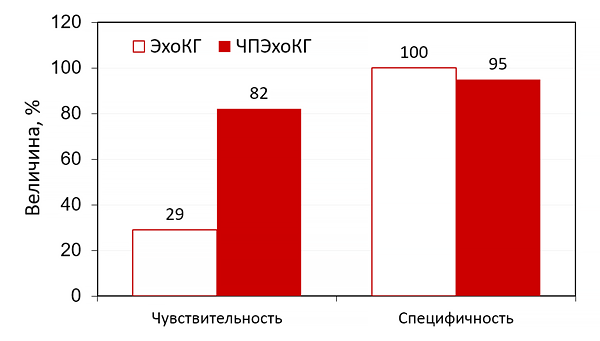
Ведущим критерием диагностики ИЭ является визуализация бактериальных вегетаций. Чувствительность одномерной ЭхоКГ в выявлении бактериальных вегетаций составляет от 13 до 48 %.
Характерным признаком вегетаций является обнаружение грубых, нерегулярных эхо-сигналов на створках клапанов (их называют лохматые,"shaggy"). Этот признак отличается от дрожания створок, обусловленного регургитантным потоком, возникновением в различные фазы систолы и диастолы. Эхо-сигнал от створок значительно усилен, кинетика клапана нарушается в зависимости от особенностей его поражения (стеноз или недостаточность). Следует отметить, что лохматость и утолщенность створок не является высокоспецифичным проявлением для ИЭ. Такие изменения могут наблюдаться при миксоматозном поражении створок (например, пролапс митрального клапана, синдром хлопающего клапана). Значительные трудности в определении признаков ИЭ при одномерной эхокардиографии возникают у больных с кальцификацией и фиброзированием створок. Такие клапаны выглядят толстыми, с нерегулярными вибрациями и лохматыми створками. Диагностические проблемы имеют место у больных с эластофиброзом эндокарда, вследствие врожденных и приобретенных пороков сердца, а также при определении вегетаций на искусственном клапане, особенно в аортальной позиции (возникает выраженный эффект реверберации).
Одномерная эхокардиография позволяет обнаружить только вегетации, превышающие 0,5 см в диаметре. Вновь образующиеся бактериальные вегетации выявляются значительно труднее, чем кальцифицированные.
Чувствительность двухмерной эхокардиографии в выявлении бактериальных вегетаций намного превышает одномерную методику и составляет от 81 до 100%. Наименьший размер клапанных вегетаций, обнаруживаемых с помощью двухмерной эхокардиографии, составляет 2-3 мм. Бактериальные вегетации имеют различную форму, чаще сферическую, плотно фиксированы на клапанных структурах, однако могут быть и подвижные. В последнем случае они перемещаются по направлению потока крови; клинически подтверждаются меняющейся аускультативной симптоматикой, чаще осложняются тромбоэмболическим синдромом. Вегетации могут быть представлены в виде единичного узла, или множественными, в виде гроздьев винограда. Последние отличаются по эхогенности от клапанных структур или поверхности эндокарда, выглядят плотными, имеют эффект реверберации.
Как и при одномерном исследовании эхокардиографические проявления бактериальных вегетаций при секторном сканировании могут имитировать следующие состояния:
- Миксоматозная дегенерация при пролапсе митрального клапана;
- Фиброз или кальцификация вторичные к ревматизму;
- Спонтанный отрыв хорд;
- Узелки на створках при сосудистых коллагеновых заболеваниях.
Ложноотрицательные случаи диагностики наблюдаются при:
- Вегетации менее 2 мм в диаметре;
- Вегетации локализуются на глубине более 7 мм от датчика,
- Эхокардиографическое обследование проведено в первые 2 недели от начала заболевания.
Чреспищеводная эхокардиография в отличии от стандартной методики позволяет выявлять:
- Вегетации при стенозе митрального клапана;
- Вегетации при миксоматозной дегенерации створок;
- Отрыв хорд с вегетациями и без вегетаций;
- Микотические аневризмы с образованием фистул;
- Вегетации на двухстворчатом аортальном клапане;
- Перфорацию створок.
Эхокардиография оказывает существенную помощь в оценке тяжести и прогноза заболевания. Так, установлено, что больные с ИЭ, у которых при обследовании выявляются бактериальные вегетации на митральном клапане чаще имеют проявления декомпенсации кровообращения. При ИЭ аортального клапана, такая взаимосвязь менее выражена, даже при отсутствии вегетаций на клапане заболевание имеет торпидное течение и осложняется рефрактерной сердечной недостаточностью.
Большое значение имеет оценка размера и локализации бактериальных вегетаций. При больших размерах вегетаций прогноз заболевания хуже. Крупные бактериальные вегетации (более 10 мм) чаще обуславливают эмболию. Последняя встречается чаще и при подвижных вегетациях.
Инфекционный эндокардит аортального клапана
ЭхоКГ критерии
Одномерная ЭхоКГ:
- Необычная форма утолщения аортальных створок.
- Нормальная величина открытия аортальных створок.
- Множественные эхосигналы линейного или хаотического характера в просвете аорты в различные фазы сердечного цикла (зависит от положения датчика), реже они могут присутствовать во всех фазах сердечного цикла.
- Нерегулярные, хаотические вибрационные эхосигналы, пролабирующие в левожелудочковый выходной тракт во время диастолы.
- ЭхоКГ-паттерн аортальной недостаточности.
Двухмерная ЭхоКГ:
Инфекционный
эндокардит
аортального клапана,
крупные подвижные
бактериальные
вегетации на
некоронарной створке
в разные фазы
сердечного цикла.
- Непосредственная визуализация клапанных вегетаций на створках с определением их размера, формы и подвижности (чаще поражается правая коронарная створка) (рис. 141 - 142).
- ЭхоКГ-паттерн недостаточности аортального клапана.
Инфекционный
эндокардит
аортального клапана,
вегетации на клапане,
трепетание передней
митральной створки.
Допплер-ЭхоКГ:
Оценка степени недостаточности аортального клапана.
Инфекционный эндокардит митрального клапана
ЭхоКГ критерии
Одномерная ЭхоКГ:
- "Лохматые" эхосигналы от створок митрального клапана, лучше видны во время диастолы ("shaggy").
- ЭхоКГ-паттерн отрыва сухожильных нитей митрального клапана.
- ЭхоКГ-паттерн митральной недостаточности.
Двухмерная ЭхоКГ:
- Дополнительные эхопозитивные массы отходящие от структур митрального клапана более 2 мм.
- Наличие эхопозитивных структур, связанных с митральным клапаном и пролабирующих в левое предсердие (такие подвижные бактериальные вегетации трудно дифференцировать от объемных образований в левом предсердии).
- Наличие эхопозитивных структур на передней створке со стороны левого желудочка в выходном тракте во время систолы (определяются при осложненном течении аортальной недостаточности).
Допплер-ЭхоКГ:
Оценка степени недостаточности митрального клапана.
Дифференциальная диагностика:
- Ревматический вальвулит.
- Наследственные заболевания соединительной ткани.
- Необходимо бактериальные вегетации отличать от альбиниевых узелков (мышечные утолщения свободного края створок, расположены между местами прикрепления к створкам сухожильных хорд - вариант нормального строения клапана), последние обычно не превышают 2 мм в диаметре.
Инфекционный эндокардит трикуспидального клапана
ЭхоКГ критерии
Одномерная ЭхоКГ:
- "Лохматые" (shaggy) эхосигналы от створок трикуспидального клапана.
- ЭхоКГ-паттерн недостаточности трикуспидального клапана.
Двухмерная ЭхоКГ:
- Прямая визуализация эхопозитивных структур, отходящих от клапана (рис.143).
- ЭхоКГ-паттерн недостаточности трикуспидального клапана.
Бактериальный
эндокардит
трикуспидального
клапана: вегетации,
отчодящие от створок
клапана.
Допплер-ЭхоКГ:
Оценка степени трикуспидальной недостаточности.
Введение
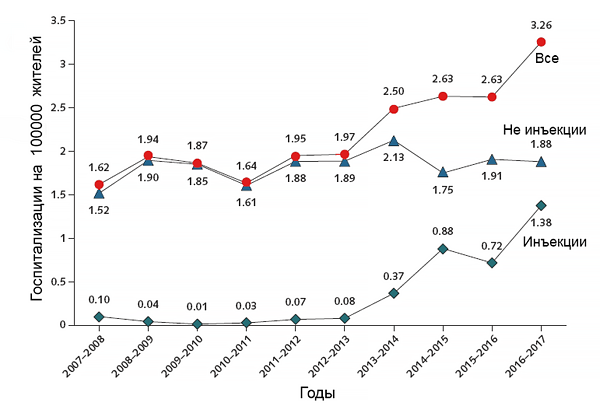
Инфекционный эндокардит (ИЭ) – заболевание сердечно-сосудистой системы, при котором инфекционный агент, циркулирующий в крови, поражает клапанные структуры сердца, пристеночный эндокард и вызывает общие инфекционно-токсические проявления, тромбоэмболические осложнения и системные поражения внутренних органов вследствие иммунопатологических реакций. В последние десятилетия отмечается рост заболеваемости ИЭ во всем мире. Это объясняется ростом операций на сердце, инвазивных методов диагностики и лечения, что привело к увеличению ситуаций, когда в кровоток из внешней среды попадает нозокомиальная флора. По данным проспективного исследования Международного сотрудничества по инфекционному эндокардиту, у 36% больных заболевание прямо связано с медицинским вмешательством. Несмотря на достижения современной антибактериальной терапии, до настоящего времени ИЭ относится к числу тяжелых заболеваний с большим числом осложнений и высоким уровнем летальности, которая при отсутствии лечения достигает 100% [1]. Диагностика ИЭ является актуальной проблемой клинической медицины. Частые неудачи в диагностике и, как следствие этого, высокая смертность обусловлены слабым знанием особенностей современного течения и дифференциальной диагностики, несовершенством и низкой чувствительностью бактериологического исследования, недостаточным оснащением лечебных учреждений современной эхокардиографической аппаратурой, нерациональным назначением антибиотиков, способствующих атипичному течению болезни, появлением ранее не встречавшихся, особых форм заболевания. В последние годы стал чаще встречаться ИЭ с поражением клапанов правого сердца, что связано с широким применением различных инвазивных процедур, а также внутривенной наркоманией. В связи с этим научная разработка и повышение эффективности диагностики ИЭ приобретают чрезвычайно важное значение 4.
Цель настоящего исследования – изучить особенности современного клинического течения ИЭ среди жителей северных урбанизированных территорий на примере г. Сургута – крупнейшего промышленно-административного центра Ханты-Мансийского автономного округа – Югры.
Материал и методы
Изучено 74 случая ИЭ, выявленного за период 2006-2013 гг. Диагноз считали достоверным согласно диагностическим критериям Duke; у всех больных имели место два больших критерия: 1) наличие клапанных вегетаций и 2) положительный бактериологический посев крови. Возраст больных составил в среднем 30-49 лет, из них 52 мужчины и 22 женщины (70 и 30% соответственно). Всем больным проводилось необходимое диагностическое обследование: клиническое, биохимическое и бактериологическое исследование крови, эхокардиография, рентгенография органов грудной клетки. Также всем больным проводилось исследование крови на наличие вирусного гепатита и ВИЧ-инфицирование.
Результаты и обсуждение
Предварительный анализ показал, что среди обследованных больных только у 12 пациентов (16,2%) был диагностирован ИЭ левых камер сердца. Основную массу составили пациенты с ИЭ трикуспидального клапана (83,8%). Исходя из этого все пациенты были распределены на 3 клинические группы. В I группу вошли 12 пациентов с левосторонним ИЭ. II группу составили 33 пациента с правосторонним ИЭ и сопутствующим вирусным гепатитом С. В III группу вошли 29 больных с правосторонним ИЭ, сопутствующим вирусным гепатитом С и ВИЧ- инфицированных. Все больные II и III групп были внутривенными наркоманами.
Сравнительный анализ по группам показал следующее.
Больные II-III групп были моложе больных I группы в среднем на 10 лет (30-39 против 40-49 дет).
Если в I группе существенных гендерных различий не установлено (мужчины – 41,6%, женщины – 58,3%), то среди больных II-III групп явно преобладали лица мужского пола (83,8%).
Все больные с ИЭ правых камер сердца оказались инъекционными наркоманами, в подавляющем большинстве случаев являлись носителями вируса гепатита С и ВИЧ-инфекции. Среди больных I группы не выявлено ни одного подобного случая.
У всех больных с левосторонним ИЭ имело место поражение измененного клапана (хроническая ревматическая болезнь сердца, протезированный клапан, врожденный порок сердца и др.). Среди больных с правосторонним ИЭ отмечено поражение нативного трикуспидального клапана.
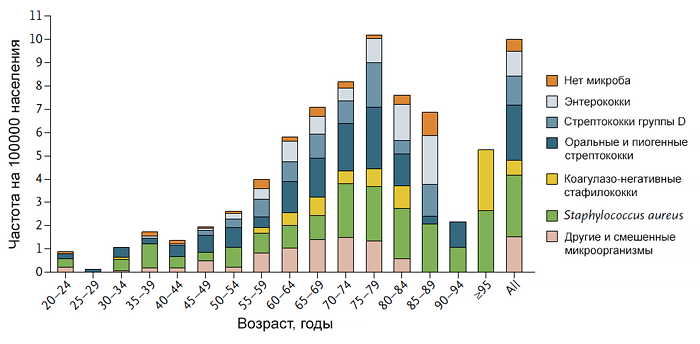
Если среди больных I группы в крови были обнаружены различные возбудители без существенного превалирования, то среди больных с правосторонним ИЭ явно преобладал Staphylococcus aureus: во II группе в 75,8% случаев, в III группе – в 69,0%, что соответствует данным других исследований.
Ни в одном случае не выявлено поздней диагностики ИЭ: диагноз выставлялся при первом обращении спустя 3-4 дня после появления первых признаков болезни.
Интересно отметить существенную разницу в проявлении лихорадочного синдрома у изучаемых больных. Если в I группе среднее значение температуры тела составило 37,8±1,1 о С, т.е. имел место субфебрилитет, то у больных II-III групп была более характерна фебрильная температура тела (39,6±0,5 о С). Не исключено, что здесь имело место сопутствующее инфицирование, а также снижение резистентности организма у наркозависимых лиц. В то же время высокая лихорадка способствовала раннему обращению больных за медицинской помощью.
Необходимо отметить, что у больных правосторонним ИЭ наиболее частым осложнением была пневмония (в 72,6% случаев), причем наиболее часто она встречалась и была наиболее тяжелой у ВИЧ-инфицированных лиц – 86,2%, причем у 55,2% больных отмечена ее двусторонняя локализация.
Выводы
- ИЭ на урбанизированном Севере характеризуется молодым возрастом больных, преимущественно 30-39 лет.
- Явно превалирует поражение правых камер сердца.
- Современный ИЭ северных урбанизированных территорий является проблемой инъекционных наркоманов, причем они поголовно заражены вирусом гепатита С и в половине случаев ВИЧ-инфицированы.
- Появление выраженного лихорадочного синдрома, а также поражения легких у лиц, страдающих внутривенной наркоманией, является прямым показанием для диагностики ИЭ.
- Всех больных, стадающих ИЭ правых камер сердца, необходимо обследовать на наркозависимость, а также носительство вирусного гепатита и ВИЧ-инфекции.
- Проблема профилактики современного ИЭ напрямую связана с эффективностью борьбы с внутривенной наркоманией.
- Характерные клинико-диагностические особенности ИЭ правых камер сердца дают основание для выделения его в отдельную клиническую форму.
Список литературы

Профилактика, диагностика и лечение инфекционного эндокардита
может оставаться отрицательной на протяжении нескольких недель.
При отрицательных результатах первичных посевов проводят 2-3 дополнительных посева в течение 48 часов. Многократные посевы крови существенно повышают вероятность выделения гемокультуры и позволяют дифференцировать истинные патогены (при повторном выявлении микроорганизмов того же вида) от случайных контаминантов, наблюдаемых в 41,5% случаев. При этом среди гемокультур коагулазонегативных стафилококков удельный вес контаминантов достигает 81,9%, а среди изолятов зеленящих стрептококков – 49,3%, что связано с применением внутрисосудистых катетеров и других инвазивных вмешательств, а также
с использованием высококачественных питательных сред для выделения гемокультур, обеспечивающих рост контаминантов кожи даже после тщательной ее дезинфекции перед венопункцией.
В случаях повторных отрицательных результатов посевов крови может возникнуть необходимость в использовании специальных питательных сред для выделения труднорастущих микроорганизмов (стрептококков
с повышенной питательной потребностью, L-форм бактерий, микроорганизмов группы НАСЕК) либо применении серологических методов и ПЦРдиагностики (полимеразных цепных реакций) для индикации других возбудителей (Brucellа spp., Neisseria spp., Legionella spp., Mycobacterium spp., Nocardia spp., Coxiella burnetii., Rickettsia spp., Bartonella spp., Chlamydia spp., Mycoplasma spp.).
Через несколько дней после начала адекватной антибактериальной терапии температура снижается, а бактериемия обычно исчезает (при стрептококковых ИЭ в течение 48-72 часов, при стафилококковой этиологии ИЭ лихорадка и бактериемия могут сохраняться до 10 дней), поэтому необходимость в дополнительных посевах крови не возникает. Однако отсутствие или недостаточная положительная динамика заболевания в ожидаемые сроки требуют дополнительного посева крови (материал берут перед очередной инфузией антибиотика, когда его концентрация в крови минимальна) и, возможно, замены антибактериальных препаратов до получения результатов посева, если имеется подозрение на суперинфекцию или развитие антибиотикорезистентности при первоначально выделенной гемокультуре.
После завершения курса антимикробной терапии и исчезновения симптомов ИЭ посев крови не проводят. Однако в случае рецидива заболевания, который чаще возникает на 2-4-й неделе после лечения и характеризуется появлением признаков инфекции, вновь требуется проведение многократных посевов крови.
Для повышения чувствительности бактериологического исследования

крови и увеличения частоты выявления возбудителя ИЭ необходимо соблюдать определенные правила.
Правила взятия крови для микробиологического исследования:
1. Кровь для исследования необходимо забирать до назначения антибиотиков. При отсутствии возможности отмены антибиотиков взятие крови следует выполнять непосредственно перед очередным введением препарата.
2. Необходимым минимумом являются 3 пробы из вен разных конечностей с интервалом 30 мин. Объем каждого образца крови должен быть не менее 15-20 мл (для взрослого).
3. Если пациент получал короткий курс антибиотикотерапии, взятие крови следует выполнять не ранее, чем через 3 дня после прекращения лечения, при предшествующем длительном курсе антибиотикотерапии – через 6-7 дней после отмены препарата.
4. В случае отрицательного результата первого исследования на гемокультуру и подозрения на ИЭ рекомендуется проведение 2-х или более дополнительных исследований через 48 ч.
5. Посев крови производить одновременно в два флакона для посева на аэробные и анаэробные среды.
Клиническая значимость регистрации бактериемии:
1. Подтверждение диагноза и определение этиологии инфекционного процесса.
2. Доказательство механизма развития инфекционного процесса (например, катетер-связанная инфекция).
3. Для некоторых ситуаций – аргументация тяжести ИЭ (стафилококковый, синегнойный, клебсиелезный).
4. Обоснование выбора или смены антибактериальной химиотерапии.
5. Оценка эффективности лечения.
Другие лабораторные методы исследования не являются специфическими, они позволяют определить степень активности воспалительного процесса, оценить степень нарушения функций органов.
Для ИЭ характерны:
лейкоцитоз со сдвигом влево;
ускорение СОЭ более 40-50 мм/час;
возможно развитие гипохромной анемии;
увеличение концентрации иммуноглобулинов;
повышение уровня мочевины и креатинина в крови;
Читайте также:


