Антибиотики при очаге хронической инфекции

Лечение инфекции костей и суставов является одной из сложных проблем в травматологии и ортопедии. Имплант-ассоциированная инфекция костей и суставов приводит к неэффективности антибактериальной терапии в связи с наличием биопленок [8]. С целью купирования воспаления проводятся неоднократные хирургические вмешательства с использованием материалов, способных доставлять и создавать локальную концентрацию антибиотика непосредственно в очаге инфекции [9].
В современной клинической медицине достигнуты значительные успехи в лечении периимплантной костной и суставной инфекции с применением различных материалов [4,6,7].
Остается много вопросов, которые необходимо решить при лечении данной патологии: как доставить антибиотик к месту назначения в необходимой концентрации для купирования воспаления; какой группы антибиотик использовать; какова его фармакокинетика; есть ли возможность использовать антибиотик совместно со средствами, усиливающими остеообразование и/или ослабляющими остеолиз; как удалить местную форму препарата из тканей, если это будет необходимо [5].
Все системы транспорта антибиотика к очагу инфекции можно разделить на нерассасывающиеся и рассасывающиеся (биодеградируемые)[10].
Цель исследования: улучшение результатов хирургического лечения периимплантной инфекции костей и суставов.
Материалы и методы исследования: в ОТО МОНИКИ с 2004 г. – по сентябрь 2015 г., при сочетании инфицирования с дестабилизацией компонентов эндопротеза у пациентов с перипротезным воспалением тазобедренного сустава в 34 случаях и с глубоким перипротезным нагноением коленного сустава в 8 случаях использован нерассасывающийся метод. Применяются временные спейсеры, импрегнированные антибиотиками с целью заполнения остаточной полости, воздействия на микрофлору очага воспаления и создание благоприятных условий для выполнения повторного тотального эндопротезирования на фоне стойкого купирования воспалительного процесса. Мужчин среди них – 24, женщин – 18, в возрасте от 31 до 75 лет.
При лечении имплант-ассоциированной костной инфекции с наличием костной деструкции в ОТО МОНИКИ с января 2015 г. – по сентябрь 2015 г. применен рассасывающий метод с использованием аутотрансплантата без фиксации и с фиксацией его биодеградируемым винтом с антибиотиком у 7-и пациентов, в возрасте от 36 до 60 лет. Мужчин – 6, женщин – 1.
Результаты и обсуждение:
Критерии для проведения двухэтапного эндопротезирования:
- Наличие местных проявлений перипротезного инфицирования;
- Стабильные компоненты эндопротеза при наличии положительной полирезистентной микрофлоры;
- Хроническое продуктивное воспаление с преобладанием сегментоядерных нейтрофилов [3].
- Гистопатологическое исследование: отсутствие при цитологическом исследовании остеокластов, наличие более 5 нейтрофилов в поле зрения при гистологическом исследовании свежезамороженных параартикулярных тканях;
- Неэффективность проведенных ранее хирургических санаций;
- Возможность проведения супрессивной антибиотикотерапии;
- Согласие больного на проведение двухэтапного метода лечения;
- Отсутствие тяжелых соматических заболеваний;
- Отсутствие критической потери костной ткани;
Первым этапом осуществляется хирургическая санация с широкой ревизией возможных путей распространения инфекции и удалением вертлужного, бедренного компонентов эндопротеза и фиксирующих материалов.
После завершения санации проводится интраоперационное формирование цементного спейсера в соответствии с формой и размерами вертлужной впадины с последующим укреплением его к проксимальному отделу бедренной кости (рис. 1)
а)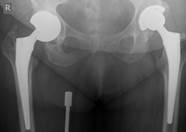
б)
в) 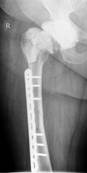
Рис. 1. Рентгенограмма таза больной К-ой, 1951 г.р., и/б 21813/18278
Нестабильность вертлужного компонента эндопротеза справа с комбинированным дефектом тазовой кости и повреждением бедренного компонента. а) – при поступлении в клинику; б) – удаленные компоненты эндопротеза с повреждением бедренного компонента; в) – рентгенограмма после первого этапа хирургического лечения – удаление компонентов эндопротеза справа, установка цементного спейсера, остеосинтез бедренной кости.
Фиксированный к бедренной кости цементный спейсер погружается в вертлужную впадину, заполняя пространство для последующего установления вертлужного компонента ревизионного эндопротеза (2-й этап).
Для изготовления цементного спейсера используется рентгеноконтрастный цементоподобный материал, обеспечивающий установку и крепление протезов к костям. Варианты антибиотиков, которые добавляют в спейсер: аминогликозиды (тобрамицин, гентамицин); Цефалоспорины 1-ого поколения (цефазолин), 2-ого поколения (цефуроксим), 3-его поколения (цефтазидим), 4-ого поколения (цефотаксим), 5-ого поколения (цефтаролин); фторхинолоны (ципрофлоксацин); гликопептиды (ванкомицин); оксазолидиноны (линезолид); противогрипковые (вориконазол).
Для формирования цементного спейсера достаточно полутора – двух доз, хотя требуемое количество зависит от характера хирургического вмешательства и применяемого метода. После окончания полимеризации приготовленный спейсер фиксируется к проксимальному отделу бедренной кости с помощью дополнительной дозы цемента. Перед установкой спейсера следует обеспечить тщательную санацию и высушивание проксимальной части костномозгового канала бедренной кости непосредственно перед погружением временного имплантата.
В случаях, когда нестабильность обоих компонентов эндопротеза сочетается с глубокой перипротезной инфекцией возможно применение преформированных (фабричных) спейсеров.
После тщательной хирургической санации очага воспаления выполняется удаление обоих компонентов эндопротеза тазобедренного сустава и фиксирующего материала. В канал бедренной кости устанавливается артикулирующий преформированный спейсер, импрегнированный антибиотиками (гентамицин, ванкомицин), а затем вправляются в вертлужную впадину, рана дренируется в течение двух дней (рис. 2).
а)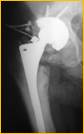
б)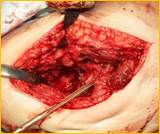
в) 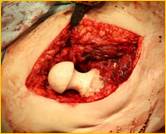
г)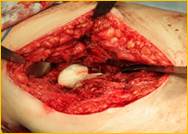
д) 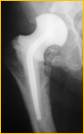
е) 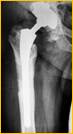
Рис. 2. Рентгенограмма правого тазобедренного сустава больного Г-на, 1963 г.р., и/б 16697/8454
Глубокое перипротезное инфицирование правого тазобедренного сустава. Комбинированный дефект правой вертлужной впадины и проксимального отдела бедренной кости. а) – при поступлении в клинику фистулограмма правого тазобедренного сустава; б) – внешний вид мягких тканей после удаления компонентов эндопротеза; в) – первый этап – санирующая операция на правом тазобедренном суставе с установкой спейсера в канал бедренной кости; г) – вправление спейсера; д) – рентгенограмма правого тазобедренного сустава после установки спейсера; е) – рентгенограмма правого тазобедренного сустава после второго этапа – удаление спейсера, повторное тотальное эндопротезирование правого тазобедренного сустава с установкой ревизионной конструкции и костной аутопластикой дефекта бедренной кости.
Среди 34 пациентов с перипротезным инфицированием тазобедренного сустава рецидив воспаления отмечен у 2 пациентов, что составило – 5,8%, которым выполнено удаление спейсера, формированием опорного неоартроза тазобедренного сустава. Три пациента отказываются от реэндопротезирования, что составляет – 8,8%. Купирование воспаления достигнуто в 94,2% случаев.
Среди 8 пациентов с глубоким нагноением эндопротеза коленного сустава рецидивов воспаления не отмечено. Двум пациентам планируется выполнить повторное эндопротезирование коленного сустава.
Необходимость проводить повторную операцию по замене спейсера на ревизионный эндопротез остается главным недостатком нерассасывающихся материалов [1].
С целью профилактики рецидивов перипротезного инфицирования суставов применен рассасывающийся биополимерный биодеградируемый материал на основе коллагеновой губки, содержащий антибиотик гентамицин. При имплантации 1 губки в полостях и тканях создается высокая локальная концентрация (666,66 мг/мл) гентамицина. Перед применением коллагеновой губки с гентамицином необходимо максимально просушить область аппликации.
а) 
б) 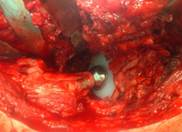
Рис. 3. а) – биополимерный биодеградируемый материал на основе коллагеной губки с гентамицином (collatampEG); б) – коллагеновая губка с гентамицином покрывает металлические участки эндопротеза тазобедренного сустава
Преимущества биополимерного биодеградируемого материала на основе коллагеновой губки с антибиотиком: создает высокую концентрацию антибиотика в областях с низкой перфузией крови в тканях; профилактики ранних и поздних инфекционных осложнений у пациентов из группы риска благодаря высокой концентрации антибиотика; обладает местным гемостатическим действием; является биодеградируемым материалом (не требует дальнейших манипуляций по удалению).
Критерии для лечения имплант-ассоциированной инфекции рассасывающимся методом с использованием аутотрансплантата без фиксации и с фиксацией его биодеградируемым винтом с антибиотиком.
- Наличие местных проявлений перииплантной костной и суставной инфекции;
- Возможность использовать аутотрансплантат для замещения костных дефектов;
- Отсутствие аллергической реакции на компоненты биодеградируемого винта;
- Чувствительность микрофлоры к антибиотику[2].
У 4-х пациентов с наличием дестрекции костей и суставов проводилась тщательная хирургическая санация очага воспаления, секвестрэктомия, замещение костного дефекта аутотрансплантатом из гребня подвздошной кости, дренирование послеоперационной раны (рис.4)
а) 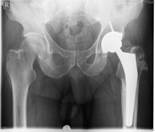
б)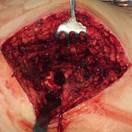
в) 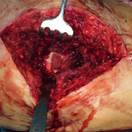
г) 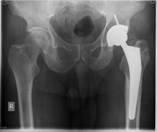
Рис. 4. Пациент К-н, 1957 г.р., и/б 14426
Глубокое перипротезное инфицирование левого тазобедренного сустава с наличием дефекта большого вертела, без дестабилизации комопнентовэндопротеза. а) – рентгенограмма левого тазобедренного сустава при поступлении в клинику; б) – внешний вид костного дефекта большого вертела после хирургической санации; в) – замещение костного дефекта трансплантатом из гребня подвздошной кости; г) – рентгенограмма левого тазобедренного сустава после оперативного лечения.
У одного пациента через четыре месяца после операции замещения костного дефекта большеберцовой кости по данным рентгенограмм отмечено рассасывания аутотрансплантата. У одного пациента после костной пластики костей стопы рецидив воспаления с формированием свищевого хода.
Трем пациентам с длительным вялотекущим процессом с наличием костной деструкции костей и суставов проведена хирургическая санация с замещением костного дефекта аутотрансплантатом и фиксация его биодеградируемым винтом с антибиотиком.
а)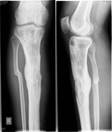
б)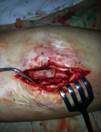
в) 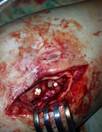
г) 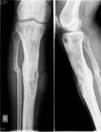
Рис. 5. Пациент Г., и/б 2485. Хронический остеомиелит большеберцовой кости справа с наличием секвестра, состояние после удаления погружного металлофиксатора большеберцовой кости, свищевая форма. а) – рентгенограмма правой голени с наличием очага деструкции большеберцовой кости, размером 9х2 см, б) – аутотрансплантат из гребня подвздошной кости, в) – фиксация аутотрансплантата винтами с антибиотиком,
г) – рентгенограмма правой голени после оперативного лечения
Послеоперационное ведение проводилось в соответствии со стандартным ведением пациентов с высоким риском инфекции.
У одного пациента в послеоперационном периоде отмечено длительное заживление послеоперационной раны. На контрольных рентгенограммах – рассасывания трансплантата ни в одном случае не произошло. Рецидива воспаления не отмечено ни в одном случае.
Заключение: использование спейсера с антибиотиком является золотым стандартом при лечении перипротезной инфекции крупных суставов и позволяет добиться стойкого купирования воспалительного процесса в 95,3% случаях. С целью профилактики перипротезного инфицирования у пациентов с высоким риском послеоперационного нагноения рекомендовано использовать биополимерный биодеградируемый материал на основе коллагеновой губки, содержащий антибиотик гентамицин.
При лечении имплант-ассоциированной костной инфекции с наличием костной деструкции использование биодеградируемого винта с антибиотиком позволяет воздействовать на микрофлору непосредственной в очаге инфекции, фиксация аутотрансплантата способствует его остеоинтеграции, повторной операции для удаления винта не требуется.
Рецензенты:
Оноприенко Г.А., д.м.н., профессор, ГБУЗ МО МОНИКИ им. М.Ф. Владимирского, г. Москва;
Дорожко И.Г., д.м.н., профессор, ГБУЗ МО МОНИКИ им. М.Ф. Владимирского, г. Москва.
Юдина Людмила Владимировна — доцент кафедры фтизиатрии и пульмонологии Национальной медицинской академии последипломного образования имени П.Л. Шупика, Киев
В большинстве случаев первопричиной заболеваний дыхательных путей является острая респираторно-вирусная инфекция, которая определяет клиническую картину заболевания и оказывает влияние на местные защитные механизмы слизистой оболочки верхних дыхательных путей: нарушается мукоцилиарный клиренс, снижается иммунитет слизистой оболочки. Все это предрасполагает к задержке, колонизации и размножению патогенной бактериальной флоры на поверхности слизистой оболочки верхних дыхательных путей.
Из множества видов микроорганизмов, колонизующих верхние дыхательные пути, лишь некоторые, обладающие повышенной вирулентностью, способны при проникновении в нижние дыхательные пути вызывать воспалительную реакцию даже при минимальных нарушениях защитных механизмов. Такими типичными бактериальными возбудителями негоспитальных инфекций нижних отделов дыхательных путей (пневмонии и бронхита) являются Streptococcus pneumoniae (Str. pneumoniae), Haemophilus influenzae, реже Staphylococcus aureus (S. aureus), Klebsiella pneumoniae. Определенную этиологическую роль играют атипичные возбудители — Mycoplasma pneumoniae, Chlamydophila pneumoniae, Legionella pneumophila (Яковлев С.В. и соавт., 2002). Условно-патогенная кокковая флора (Str. pneumoniae, S. aureus, Haemophilus influenzae) чаще вызывает острый фарингит, бронхит, а атипичные возбудители (Legionella pneumophila, Mycoplasma pneumoniae, Chlamydophila pneumoniae) — назофарингит, острый тонзиллит, бронхит.
Острые респираторные инфекции опасны своими осложнениями (острый бронхит, острый синусит, острый средний отит, пневмония, внутричерепные осложнения, поражение сердца).
Острый синусит (острое воспаление слизистой оболочки околоносовых пазух) в большинстве случаев развивается на фоне банального насморка при нарушении вентиляции пазух. При острых респираторных вирусных инфекциях организм ослаблен и в большей степени подвержен другим видам инфекции, в том числе бактериальной. Острый синусит обычно развивается как осложнение вирусной инфекции верхних дыхательных путей, при этом воспаление слизистой оболочки околоносовых пазух сохраняется >3 мес и завершается спонтанно или в результате лечения. Заподозрить синусит можно по затяжному течению банального насморка (в том случае, когда симптомы заболевания не проходят в течение 7–10 дней), асимметрии в проявлениях (затруднение носового дыхания, более выраженное в одной половине носа, обильные односторонние выделения из носа). Может отмечаться заложенность носа, ощущение тяжести в голове, характерна боль в области лба или проекции пазухи, возможно с иррадиацией в зубы, повышенная температура тела (до 37,5 °С). При отсутствии лечения острый синусит легко переходит в хроническую форму, терапия при которой значительно сложнее.
Выделяют острый катаральный (который может иметь вирусное происхождение или являться начальной стадией бактериальной инфекции) и острый гнойный синусит, однозначно требующий применения системной антибиотикотерапии.
Основная цель системной антибиотикотерапии при остром риносинусите — эрадикация инфекции и восстановление стерильности синуса. Выбор препарата при остром процессе в большинстве случаев проводят эмпирически на основе данных о преобладании тех или иных возбудителей в регионе, их резистентности и с учетом тяжести состояния больного.
Нижеприведенное клиническое наблюдение демонстрирует случай развития осложнения после перенесенной острой респираторной вирусной инфекции.
Пациентка П., 38 лет, заболела остро 2 нед назад, отмечала высокую температуру тела (до 39,5 ˚С), резкую слабость, светобоязнь. Лечилась амбулаторно, на 5-е сутки приступила к работе, однако спустя 1 нед появились жалобы на кашель с выделением слизисто-гнойной мокроты, повышение температуры тела до 37,6 ˚С, головную боль, слабость, затруднение носового дыхания, слизисто-гнойные выделения из носа, ощущение заполненности, тяжести, давления в проекции околоносовых пазух. По заключению оториноларинголога у пациентки выявлен правосторонний гайморит. Было назначено лечение азитромицином в стандартной дозе в течение 3 дней, которое не оказало эффекта.
При обследовании пульмонологом состояние удовлетворительное, температура тела — 37,5 ˚С, пульс ритмичный с частотой 96 уд./мин, число дыхательных движений — 24 в 1 мин, артериальное давление — 118/60 мм рт. ст.
Результаты дополнительных методов обследования: лейкоцитоз 10,2 • 10 9 /л (палочкоядерный сдвиг лейкоцитарной формулы влево до 16%), скорость оседания эритроцитов — 36 мм/ч. Креатинин, мочевина, билирубин, альбумин крови, общий анализ мочи — в пределах нормы. При рентгенологическом обследовании органов грудной клетки выявлены изменения, характерные для негоспитальной пневмонии верхней доли правого легкого (рис. 1, 2).


Таким образом, у пациентки помимо правостороннего гайморита выявлена негоспитальная пневмония верхней доли правого легкого, что требовало антибактериальной терапии, поскольку абсолютным показанием к назначению системных антибиотиков при инфекциях дыхательных путей являются: предположение или установленный диагноз пневмонии, эпиглоттит, гнойный синусит, острый стрептококковый тонзиллит (фарингит), паратонзиллярный абсцесс.
Важной задачей при негоспитальной инфекции является рациональный выбор антибиотиков, так как это ведет к снижению частоты назначения антибактериальных препаратов, более полному клиническому и бактериологическому излечению больного, и в конечном итоге — ограничению роста антибиотикорезистентности в популяции (Яковлев С.В. и соавт., 2002).
При выборе эмпирической терапии следует учитывать превалирующую микробную флору. Str. pneumoniae — наиболее частый возбудитель как негоспитальной пневмонии, так и синусита у лиц всех возрастных групп. Более 50% случаев острого синусита, рецидивирующего острого синусита и обострений хронического синусита вызваны Str. pneumoniae и Haemophilus influenzae, реже — Moraxella catarrhalis, Str. pyogenes, S. aureus, анаэробами. Поскольку большинство больных острым синуситом лечат амбулаторно, выбор препарата проводят эмпирически, на основании данных о преобладании и устойчивости возбудителей в регионе.
Основные принципы выбора антибиотика при остром синусите следующие:
- активность против Str. pneumoniae и Haemophilus influenzae;
- способность преодолевать резистентность возбудителей к антибиотику;
- хорошее проникновение в слизистую оболочку синусов с достижением концентрации выше минимальной подавляющей концентрации (МПК) для данного возбудителя;
- сохранение концентрации в плазме крови выше МПК в течение 40–50% времени между приемами препарата (Яковлев С.В. и соавт., 2002).
В настоящее время в качестве основных средств стартовой терапии негоспитальных респираторных инфекций в амбулаторной практике применяют аминопенициллины (ампициллин, амоксициллин), защищенные аминопенициллины (амоксициллин/клавулановая кислота), перорально цефалоспорины II поколения (цефуроксим аксетил), макролиды (Страчунский Л.С. и соавт. (ред.), 2002; Яковлев С.В. и соавт., 2002).
При выборе антибиотика при синусите необходимо учитывать тяжесть состояния пациента. При легком и среднетяжелом течении [а именно такова степень тяжести заболевания в представленном клиническом случае] антибиотики назначают перорально, препаратами выбора являются амоксициллин или амоксициллин/клавулановая кислота, альтернативой — применение цефалоспоринов II поколения (цефуроксим аксетил), макролидов (азитромицин, кларитромицин) или доксициклина (Страчунский Л.С. и соавт. (ред.), 2002).
Аминопенициллины (амоксициллин, ампициллин) характеризуются высокой активностью в отношении Str. pneumoniae (амоксициллин более высокой, нежели ампициллин). Имеются данные о том, что амоксициллин в стандартных дозах сохраняет высокую активность в отношении Str. pneumoniae. Высокодозные формы применяют для воздействия на резистентные штаммы. К недостаткам амоксициллина можно отнести его способность разрушаться β-лактамазами, которые могут продуцировать Haemophilus influenzae и Moraxella catarrhalis. Поэтому альтернативой его применению, особенно при неэффективности терапии или рецидивирующем процессе, является применение амоксициллина/клавулановой кислоты или цефуроксима аксетила. Амоксициллин/клавулановая кислота и цефуроксим аксетил включены в большинство международных и отечественных стандартов лечения при негоспитальной пневмонии ввиду высокой активности против Str. pneumoniae, Haemophilus influenzae, S. aureus (Niederman M.S. et al., 2001; Woodhead M. et al., 2005; Міністерство охорони здоров’я України, 2007; Mandell L.A. et al., 2007).
Основными возбудителями негоспитальной пневмонии являются Str. pneumoniaе, Mycoplasma pneumoniae, Haemophilus influenzae, S. aureus, Legionella spp., Chlamydophila pneumoniae, грамотрицательные энтеробактерии и вирусы. В приведенном клиническом случае лечение азитромицином оказалось неэффективным. Как известно, макролиды активны в отношении типичных и атипичных возбудителей инфекций дыхательных путей, однако отмечается тенденция к росту устойчивости Str. pneumoniaе к макролидам. Кроме того, слабым звеном препаратов этой группы является их низкая активность в отношении Haemophilus influenzae. Ввиду отсутствия эффекта от применения азитромицина и вероятной резистентности возбудителя к макролидам в рассматриваемом случае следует провести антибактериальную терапию антибактериальным препаратом другого класса.
Известно, что основу терапии преобладающего большинства случаев нетяжелой негоспитальной пневмонии составляют антибиотики, применяемые перорально, выбор которых определяется структурой потенциальных возбудителей. При негоспитальной пневмонии у взрослых в качестве приоритетных возбудителей выступает Str. pneumoniae, менее чем в 2% случаев рассматриваемый как устойчивый к пенициллину (МПК ≥2 мг/л). При выборе антибиотика при негоспитальной пневмонии (на догоспитальном этапе лечения и в стационаре) необходимо учитывать следующие критерии:
- активность препарата в отношении наиболее частых возбудителей негоспитальной пневмонии (Str. pneumoniaе, Mycoplasma pneumoniae, Haemophilus influenzae);
- способность создавать терапевтические концентрации в тканях и жидкостях органов дыхания;
- минимум противопоказаний;
- низкая токсичность;
- наличие форм для перорального и парентерального применения;
- удобство дозирования и хранения;
- минимальная индукция резистентности;
- возможность применения у детей и взрослых.
Этим критериям соответствуют такие группы препаратов, как аминопенициллины, защищенные аминопенициллины, цефалоспорины II поколения, которые являются приоритетными в лечении больных негоспитальной пневмонией, согласно национальным и международным рекомендациям (Niederman M.S. et al., 2001; Woodhead M. et al., 2005; Міністерство охорони здоров’я України, 2007; Mandell L.A. et al., 2007). Область клинического применения пероральных цефалоспоринов определяется исключительно спектром их антимикробной активности. Это связано с высоким уровнем накопления их в ткани легких и широким спектром бактерицидного действия в отношении наиболее распространенных возбудителей инфекций дыхательных путей.
Цефалоспорин II поколения цефуроксим аксетил (Зиннат™) в дозе 250 мг 2 раза в сутки более эффективен по сравнению с цефалоспоринами I поколения в отношении таких респираторных патогенов, как Haemophilus influenzae и Moraxella catarrhalis, которые становятся антибиотикорезистентными вследствие формирования плазмидных β-лактамаз; при этом препарат сохраняет высокую активность в отношении грамположительных микроорганизмов, таких как Str. pneumoniae, S. aureus и др. Цефуроксим аксетил в настоящее время рассматривают как один из основных препаратов для лечения при негоспитальных респираторных инфекциях (наряду с амоксициллином/клавулановой кислотой), а в частности при негоспитальной пневмонии во II клинической группе пациентов (нетяжелое течение, с наличием сопутствующей патологии и/или других модифицируемых факторов) он является препаратом выбора.
Цефуроксим аксетил является пролекарством и при приеме внутрь метаболизируется в стенке кишки до активного соединения — цефуроксима. Цефалоспорины относят к препаратам, для которых важна не столько концентрация, сколько длительность взаимодействия с микроорганизмом. Это означает, что концентрация цефуроксима, превышающая МПК в 2–4 раза, должна сохраняться около 50% времени между введениями, а повышение МПК, к примеру, до 20 раз не будет сопровождаться увеличением выраженности клинического эффекта. Из этого следует очень важный вывод: доза не является определяющей для клинического эффекта цефуроксима; более важна длительность взаимодействия антибиотика с микроорганизмом. Цефуроксим аксетил в форме таблеток после приема внутрь хорошо всасывается и быстро гидролизуется в слизистой оболочке кишечника и крови в цефуроксим (биодоступность цефуроксима аксетила повышается до 50% при приеме во время еды). Максимальная концентрация препарата создается через 2,5–3 ч после приема. В результате плавного повышения концентрации цефуроксима при применении цефуроксима аксетила увеличивается время экспозиции антибиотика с микроорганизмом, что позволяет применять режим дозирования препарата 250–500 мг 2 раза в сутки.
При проведении эмпирической антибиотикотерапии важно учитывать не только ее эффективность, но и безопасность. Особый практический интерес с этой точки зрения представляет Зиннат™ как антибиотик-пролекарство, который поступает в кишечник в неактивной форме (цефуроксим аксетил) и активизируется в слизистой оболочке тонкого кишечника в цефуроксим, всасывающийся в системный кровоток. В дальнейшем цефуроксим легко проникает в различные ткани и среды организма, включая легкие, пазухи носа и т.д. Фармакокинетика препарата Зиннат™ выгодно выделяет его среди других антибиотиков-пролекарств, например цефалоспоринов III поколения, — цефуроксим полностью выделяется почками, не метаболизируется в печени и не выводится через желудочно-кишечный тракт с желчью. Учитывая то, что в просвете кишечника находится только неактивное пролекарство, можно говорить о том, что препарат Зиннат™ оказывает незначительное воздействие на кишечную флору, тем самым минимизируется риск развития антибиотикассоциированной диареи. Фармакокинетический профиль препарата позволяет создавать необходимые терапевтические концентрации в очагах инфекции, что обеспечивает клиническую эффективность при инфекциях дыхательных и мочевыводящих путей, принимать препарат 2 раза в сутки, что обеспечивает хорошую приверженность пациентов терапии, и выводить активное вещество почками в неизмененном виде.
Наиболее частыми ошибками в амбулаторной практике являются недостаточная длительность антибиотикотерапии при инфекциях верхних дыхательных путей (например остром синусите) и чрезмерная длительность — при инфекциях нижних дыхательных путей (бронхите, пневмонии). В рассмотренном клиническом случае мы рекомендовали больной принимать Зиннат™ в дозе 250 мг 2 раза в сутки на протяжении 10 дней, поскольку длительность терапии синусита должна составлять не менее 10–14 сут. Выбранный антибиотик оказался эффективным: проявления гайморита исчезли, пневмония разрешилась (рис. 3). Инфильтрация в верхней доле правого легкого практически рассосалась. Дальнейшее применение антибиотиков в данном случае нецелесообразно. Клинически наблюдалось выздоровление.

Таким образом, выбор эмпирической терапии инфекций верхних и нижних дыхательных путей зависит от знания этиологической роли микроорганизмов, наиболее часто их обусловливающих (Str. pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, S. aureus, Str. pyogenes группы А). Все они высокочувствительны к цефуроксиму аксетилу, имеющему сбалансированный антибактериальный спектр, оптимальный для эмпирической терапии инфекций как нижних, так и верхних дыхательных путей. Правильный выбор антибактериального препарата позволяет своевременно устранить инфекционный процесс, снизить стоимость лечения и уменьшить вероятность развития антибиотикорезистентности микробной флоры.
Читайте также:


