Серологические признаки гепатита в
Серологические методы исследования
В основе всех серологических реакций лежит взаимодействие антигена и антитела.
Метод обнаружения с диагностической целью антител в сыворотке крови обследуемого .
В этом случае из двух компонентов реакции (антитело, антиген) неизвестным является сыворотка крови, так как постановка реакции проводится с заведомо известными антигенами. Положительный результат реакции свидетельствует о наличии в крови антител, соответствующих применяемому антигену; отрицательный результат указывает на отсутствие таковых.
С внедрением в практику лабораторий метода иммуноферментного анализа (ИФА) стало возможным определять в крови больных антитела, относящиеся к различным классам иммуноглобулинов (JgM и JgG), что существенным образом повысило информативность серологических методов диагностики.
При первичном иммунном ответе, когда иммунная система человека взаимодействует с инфекционным агентом в первый раз, синтезируются преимущественно антитела, относящиеся к иммуноглобулинам класса М ( JgM ) . Лишь позднее, на 8-12-й день после попадания антигена в организм, в крови начинают накапливаться антитела иммуноглобулинов класса G ( JgG ) . При иммунном ответе на инфекционные агенты вырабатываются также и антитела класса А ( JgA ), которые играют важную роль в защите от инфекционных агентов кожи и слизистых оболочек.
Метод полимеразной цепной реакции (ПЦР)
Полимеразная цепная реакция (ПЦР), являющаяся одним из методов ДНК-диагностики, позволяет увеличить число копий детектируемого участка генома (ДНК) бактерий или вирусов в миллионы раз с использованием фермента ДНК-полимеразы. Тестируемый специфический для данного генома отрезок нуклеиновой кислоты многократно умножается (амплифицируется), что позволяет его идентифицировать. Сначала молекула ДНК бактерий или вирусов нагреванием разделяется на 2 цепи, затем в присутствии синтезированных ДНК-праймеров (последовательность нуклеинов специфична для определяемого генома) происходит связывание их с комплементарными участками ДНК, синтезируется вторая цепь нуклеиновой кислоты вслед за каждым праймером в присутствии термостабильной ДНК-полимеразы. Получается две молекулы ДНК. Процесс многократно повторяется.
Для диагностики достаточно одной молекулы ДНК, т. е. одной бактерии или вирусной частицы. Введение в реакцию дополнительного этапа — синтеза ДНК на молекуле РНК при помощи фермента обратной транскриптазы — позволило тестировать РНК-вирусы, например вирус гепатита С.
ПЦР — это трехступенчатый процесс , повторяющийся циклично: денатурация, отжиг праймеров, синтез ДНК (полимеризация). Синтезированное количество ДНК идентифицируют методом иммуноферментного анализа или электрофореза.
-
Преимущество ПЦР в диагностике инфекционных заболеваний перед другими методами исследований заключается в следующем:
- возбудитель инфекции может быть обнаружен в любой биологической среде организма, в том числе и в материале, получаемом при биопсии;
- возможна диагностика инфекционных болезней на самых разных стадиях заболевания;
- возможность количественной оценки результатов исследований ( сколько вирусов или бактерий содержится в исследуемом материале);
- высокая чувствительность метода.
Исследования вирусов гепатита
В настоящее время выделяют следующие формы вирусных гепатитов: гепатит А, гепатит В, гепатит С, гепатит D, гепатит Е, гепатит G и гепатит ТТ. Для диагностики каждой из перечисленных форм вирусных гепатитов используется определенный перечень маркеров.
Вирусный гепатит А
Гепатит А — острая энтеровирусная инфекция. Возбудитель — вирус гепатита А (ВГА,HAV) — энтеровирус типа 72. Геном вируса представлен однонитчатой РНК. Вирус гепатита А содержит единственный антиген (HA-Ag). Удельный вес гепатита А в суммарной заболеваемости вирусными гепатитами составляет 70-80%. В структуре заболеваемости гепатитом А дети составляют до 80%, причем основная масса — дошкольники и школьники начальных классов.
Вирусный гепатит В
Гепатит В – вирусная антропонозная инфекция. Возбудитель вирус гепатита В (ВГВ, HBV) – относится к семейству гепаднавирусов, ДНК-содержащих вирусов, поражающих клетки печени. Вирионы ВГВ имеют наружную липопротеидную оболочку и нуклеокапсид, содержащий двунитчатую ДНК и ДНК-зависимую ДНК-полимеразу.
В диагностике вирусного гепатита В ведущее значение имеет определение комплекса маркеров гепатита. Свыше 5% населения планеты охвачено этой инфекцией, а частота безжелтушных форм ВГВ составляет, по данным разных авторов, от 60 до 82%.
Вирус гепатита С, генотипы
Гепатит С (ВГС) – вирусное заболевание, наиболее часто протекающее в виде посттрансфузионного гепатита с преобладанием безжелтушных и легких форм и склонное к хронизации процесса.
Возбудитель - вирус гепатита С – имеет сходство с флавовирусами, содержит РНК. На основе филогенетического анализа выделено 6 генотипов ВГС и более 80 субтипов.
Генотип 1 - наиболее распространенный генотип во всем мире (от 40 до 80%). Генотип 1а является доминирующим для США, а 1b преобладает в Западной Европе и Южной Азии.
Генотип 2 распространен во всем мире, однако встречается с меньшей частотой, чем генотип 1 (от 10 до 40%).
ВГС тип 3 характерен для Индии, Пакистана, Австралии и Шотландии. Генотип 4 распространен преимущественно в Средней Азии и Египте, генотип 5 – в Южной Африке, а генотип 6 – в Гонконге и Мокао.
Примерно 90% всех случаев посттрансфузионных гепатитов связано с ВГС. Среди доноров антитела к вирусу гепатита С (анти-ВГС) обнаруживают в 0,2-5% случаев.
У 40-75% пациентов регистрируется бессимптомная форма болезни, у 50-75% больных острым ВГС формируется хронический гепатит, у 20% из них развивается цирроз печени. Важная роль ВГС отводится и в этиологии гепатоклеточной карциномы.
Геном вируса гепатита С представлен одноцепочечной положительно заряженной РНК, которая кодирует 3 структурных и 5 неструктурных белков. К каждому из этих белков вырабатываются антитела, обнаруживаемые в крови больных гепатитом С.
Отличительной чертой ВГС является волнообразное течение заболевания, в котором разграничивают 3 фазы: острую, латентную и фазу реактивации.
Для острой фазы характерно повышение активности печеночных ферментов в сыворотке крови, уровня антител класса IgM и IgG к ВГС с нарастанием титров, а также РНК ВГС.
Латентная фаза характеризуется отсутствием клинических проявлений, наличием в крови антител класса IgG к ВГС в высоких титрах, отсутствием антител класса IgM и РНК ВГС либо их присутствием в низких концентрациях на фоне незначительного повышения активности печеночных ферментов в периоды обострения.
Для фазы реактивации характерно появление клинических признаков, повышение активности печеночных ферментов, наличие антител класса IgG (к нуклеокапсидному белку core и неструктурным белкам NS) в высоких титрах, присутствие РНК ВГС и нарастание титров антител класса IgM к ВГС в динамике.
Вирусный гепатит D
Гепатит D – вирусная инфекция, вследствие биологических особенностей вируса протекающая исключительно в виде ко- или суперифекции при гепатите В, характеризующаяся тяжелым течением,
часто неблагоприятным исходом.
Самостоятельно, без вируса В, вирус гепатита D не может попасть в организм человека
Возбудитель – вирус гепатита D (ВГD), по своим биологическим свойствам приближается к вироидам – обнаруженным молекулам нуклеиновых кислот. Печень человека – единственное место размножения (репликации) ВГD.
Известно существование двух вариантов инфекции: коинфекция (одновременное заражение ВГВ и ВГD) и суперинфекция (заражение HBsAg-позитивных пациентов). Сочетание ВГВ и ВГD сопровождается развитием более тяжелых форм патологического процесса, что определяется главным образом действием ВГD.
Летальность при суперинфекции достигает 15-20%. Инфицирование дельта-вирусом может вызывать острое заболевание, заканчивающееся выздоровлением, или формировать хроническое носительство ВГD.
При гепатите D могут отсутствовать в крови маркеры гепатита В – анти НВс и НВs-антиген – и наблюдается угнетение ДНК-полимеразной активности, так как ВГD ингибирует репликацию вируса гепатита В.
Гепатит и HBsAg
Итак, антиген HBsAg – один из компонентов оболочки вируса гепатита В (HBV). В контексте лабораторных исследований он является маркёром (индикатором) вируса.
Если говорить о составе капсида (внешняя оболочка вируса) гепатита В подробнее, то это сложная комбинация белков, гликопротеинов, липопротеидов и липидов клеточного происхождения. HBsAg в данном случае отвечает за процесс адсорбции вируса клеткой, то есть обеспечивает поглощение HBV гепатоцитами – клетками печени. Как и любой другой вирус, после внедрения в благоприятную среду, он начинает реплицировать (продуцировать) новые ДНК и протеины, необходимые для дальнейшего размножения (копирования) вируса. Фрагменты вируса, в нашем случае – HbsAg, поступают в кровоток, по которому распространяются дальше.
Возбудитель гепатита В относится к гепаднавирусам ( Hepadnaviridae ), само название которых указывает на их отношение к печени ( hepa ) и к ДНК ( DNA ). Таким образом, HBV – это гепатотропный вирус, при этом единственный среди всех вирусов гепатита, содержащий ДНК. Его активность (контагиозность и вирулентность) зависит от многих факторов:
- возраста (например, до 1 года – ≈90%, до 5 лет – ≈20–50%, старше 13 лет – ≈5%);
- индивидуальной восприимчивости;
- штамма вируса;
- инфицирующей дозы;
- гигиенических условий жизни и труда;
- эпидемиологической обстановки.
Но в целом контагиозность вируса гепатита B невысокая, ниже средней, если только полностью не пренебрегать всеми правилами безопасной половой жизни и гигиены.
Но как же передается вирус гепатита B? Процесс инфицирования происходит посредством крови и биологических жидкостей следующими путями:
- Парентеральным , то есть при попадании напрямую в кровь или слизистую оболочку, минуя защитные барьеры организма, такие как кожный покров или желудочно-кишечный тракт. Примерами такого инфицирования может служить нестерильный шприц или любой хирургический инструмент.
- Вертикальным – трансплацентарным, то есть внутриутробно от матери к ребенку, во время родов, после них.
- Половым (во всех его формах).
- Бытовым , то есть через предметы личной гигиены (бритвы, расчески, зубные щетки), при нанесении татуировок, пирсинге и др.
По окончании инкубационного периода наступает так называемая продромальная фаза заболевания, предшествующая острому периоду и предвещающая его. Тогда проявляются первые признаки болезни в виде общего недомогания, слабости, усталости, лихорадки с температурой на грани 37°C, понижения аппетита, тошноты, нарушений стула, суставно-мышечных болей, чувства сдавленности и тяжести в правом подреберье, раздражительности и апатии, кожных высыпаний в области суставов и зуда. Здесь следует отметить, что все эти симптомы могут быть выражены в разной степени у различных людей, вовсе отсутствовать или оставаться незамеченными. Продромальный, или преджелтушный, период может длиться от 1 до 30 дней. О его окончании свидетельствуют увеличенная печень и селезенка (30–50% случаев), повышенный уробилиноген в моче, обесцвечивание кала, а в сыворотки крови можно обнаружить рост концентраций АлАт и АсАт, пониженное содержание лейкоцитов, хотя в целом лейкоцитарная формула в норме.
Желтушность кожного покрова и иктеричность склер (желтая пигментация белковой оболочки глаз) знаменуют вступление в острую фазу , или в период разгара гепатита B. Повышение содержания общего и прямого билирубина в сыворотке крови нарастает первую неделю-две желтушного периода заболевания, достигая своего максимума, после чего происходит стагнация и постепенный спад в пигментации кожи вплоть до полного исчезновения желтой окраски, на что может уйти до 180 дней и даже более.
В пиковых точках болезни в большинстве случаев фиксируют брадикардию, пониженное артериальное давление, ослабление сердечных тонов. Кроме того, если гепатит протекает в тяжелой форме, обнаруживаются:
- угнетение центральной нервной системы;
- выраженные нарушения в работе ЖКТ;
- склонность к кровотечениям в слизистых оболочках (сильно понижен протромбиновый индекс);
- концентрация АлАт выше АсАт;
- пониженная сулемовая проба, реакция СОЭ – 2–4 мм/час, лейкопения;
- лимфоцитоз.
После острого периода (не путать с тяжелой формой!) болезнь развивается по одному из следующих сценариев (см. рис . 1 и 2):
- наступает период реконвалесценции (выздоровления) , с постепенным снижением (исчезновением) признаков гепатита B на клиническом, биохимическом и морфологическом уровнях;
- присоединяется суперинфекция в виде гепатита D и/или заболевание переходит в фульминантную форму, в так называемый молниеносный тяжелый гепатит (менее 1% случаев);
- болезнь переходит в активную хроническую форму :
- a. выздоровление;
- b. цирроз печени (20%), карцинома (1%);
- болезнь переходит в состояние устойчивой ремиссии ( стабильная хроническая форма ):
- a. излечение;
- b. внепеченочные патологии.

Рис. 1. Прогноз развития гепатита B
С точки зрения нагрузки на организм, врачи определяют три основных формы протекания острого гепатита B: легкая, средняя и тяжелая. С позиций выраженности симптомов заболевания, выделяют его желтушную (типичную), безжелтушную и субклиническую (атипичные) формы. В типичном варианте болезнь протекает в точности, как описано выше, однако это только 35% от всех случаев. Примерно 65% приходится на атипичные формы, когда не происходит пигментации кожных покровов и слизистой, а другие симптомы выражены слабо (безжелтушный вариант), или когда любые клинические проявления отсутствуют вовсе (субклиническая форма).
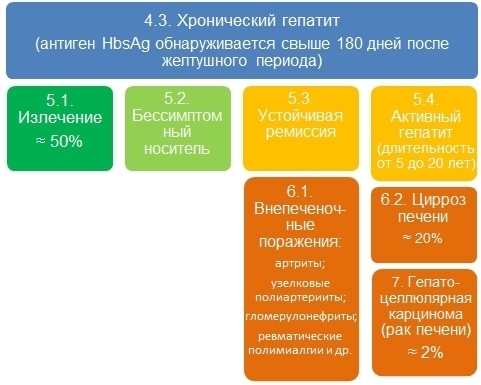
Рис. 2. Исход болезней при инфецировании HBV
Диагностические критерии бессимптомного носительства следующие:
- антиген HBsAg определяется в крови после 180 дней;
- маркёр HBeAg ( см. таблицу ) в сыворотке не обнаруживается;
- анти- HBe ( см. таблицу ) – присутствует;
- уровень HBV ДНК в сыворотке крови менее 105 копий/мл;
- концентрации АлАт/АсАт показывают норму при повторных анализах;
- при биопсии печени гистологический индекс активности (МГА) воспалительно-некротического процесса в печени обычно ниже 4.
Как можно увидеть, серологический маркер HBsAg является первым, основным, самым надежным, но далеко не единственным показателем инфекции гепатита B, кроме него требуют определения в сыворотке крови следующие антигены, антитела и молекулы ДНК вируса:
HBeAg
указывает на репликацию HBV в гепатоцитах, высокую активность вируса в крови и высокий риск перинатальной передачи вируса
HBcAg
маркирует репликацию HBV в гепатоцитах, обнаруживается только при морфологическом исследовании биоптатов печени и на аутопсии, в крови в свободном виде не выявляется
анти-НВс (total) (НВсАb)
суммарные антитела к HBcAg, выявляются через 7–14 дней после HBsAg
важный диагностический маркер, особенно при отрицательных результатах индикации HBsAg, используется для ретроспективной диагностики гепатита B и при неверифицированных гепатитах, определяют НВсАg без разделения на классы
IgM анти-НВс (НВсАb IgM)
антитела класса М к ядерному антигену , присутствуют в крови от 60 до 540 дней
один из наиболее ранних сывороточных маркеров гепатита В, наличие его в крови указывает на острую инфекцию (фазу болезни), при хроническом ГВ маркирует репликацию HBV и активность процесса в печени
анти-НВе (HBeAb)
может указывать на начало стадии реконвалесценции (исключение – мутантная форма HBV)
анти-HBs (HBsАb)
защитные антитела к поверхностному антигену HBV
указывают на перенесенную инфекцию или наличие поствакцинальных антител (их защитный титр от HBV-инфекции >10 МЕ/л); обнаружение же антител в первые недели гепатита В прогнозирует развитие гипериммунного варианта фульминантного гепатита В
HBV-DNA
ДНК вируса ГВ
маркер наличия и репликации HBV
Вышеуказанные маркёры появляются и исчезают в определенной последовательности в соответствии с этапами прохождения заболевания. Некоторые из них, такие как IgG анти-НВс, остаются на всю жизнь. Полную и достоверную диагностическую картину дает только весь набор маркёров. Кроме того, для острого, хронического, фульминантного и смешанного гепатитов существуют свои серологические профили (об этом ниже).
Нельзя не затронуть такое редкое, но чрезвычайно опасное явление, как параллельное инфицирование гепатитом D (HDV), оно может возникнуть в двух вариантах:
HDV – это своеобразный паразит вируса гепатита B, его сателлит, он не может реплицироваться в отсутствие HBV , поскольку синтез белков его внешней оболочки невозможен без наличия в гепатоцитах вируса гепатита B. Таким образом, переболеть гепатитом B можно и без дельта-инфекции, а вот наоборот не получится. Присоединение HDV вызывает в 30% случаев молниеносный (фульминантный) гепатит с развитием острой печеночной недостаточности и печеночной энцефалопатии, которые нарастают стремительно, в 60% случаев приводя к летальному исходу. Однако общий исход гепатита B в фульминантную форму находится в пределах 0,4–1% случаев. Поэтому при положительном результате на антиген HBsAg в обязательном порядке следует проводить диагностику дельта-инфекции. Для этого используются серологические маркеры:
IgM анти-HDV
антитела класса М к вирусу гепатита D
маркируют репликацию HDV в организме
IgG анти-HDV
антитела класса G к вирусу гепатита D
свидетельствуют о возможной инфицированности HDV или перенесенной инфекции
HDAg
антиген вируса гепатита D
маркер наличия HDV в организме
HDV-RNA
РНК вируса гепатита D
маркер наличия и репликации HDV
Анализ может быть сдан любым желающим, но есть определенные категории лиц, у которых подобное тестирование проводится обязательно:
- сотрудники медицинских учреждений, в особенности те, которые работают с кровью пациентов: медицинские сестры манипуляционных кабинетов, гинекологи, хирурги, фельдшеры, стоматологи;
- лица с повышенным уровнем ферментов АсАт и АлАт;
- больные, которым предстоит хирургическое вмешательство;
- потенциальные доноры крови;
- лица, являющиеся носителями вируса гепатита B, больные с хронической формой данного заболевания;
- беременные женщины.
Кроме того, исследование рекомендуется делать при наличии таких симптомов, как тошнота, рвота, потеря аппетита, изменение цвета мочи и кала, желтушность – то есть всех тех признаков гепатита B, которые были описаны в начале статьи. Но в целом каждый человек, если подходит к своему здоровью ответственно, должен делать серологическое исследование на HBsAg один раз в год.
Сегодня существует уже три поколения методов серологической диагностики HBsAg , и самые информативные и чувствительные из них, способные выявлять концентрации до 0,05 нг/мл, постепенно вытеснили своих предшественников.
I
Реакция преципитации в геле, РПГ (Gel precipitation test)
II
Встречный иммуноэлектрофорез, ВИЭФ (Counter immunoelectrophoresis),
Реакция связывания комплемента, РСК (Complement fixation test)
Реакция латекс-агглютинации, РЛА (Latex agglutination test)
Метод флюоресцирующих антител, МФА (Immunofluorescence)
Иммуноэлектронная микроскопия, ИЭМ (Immune electron microscopy)
III
Реакция обратной пассивной гемагглютинации, РНГА (Indirect hemagglutination test)
Радиоиммунный анализ, РИА (Radioimmunoassay)
Иммуноферментный анализ, ИФА (Enzyme immunoassay)
Почему ИФА и РИА более информативны в сравнении с предшественниками? Дело в том, что они способны выявлять IgM и IgG по отдельности, что позволяет делать определенные выводы о динамике инфекционного процесса или о состоянии реконвалесценции.
Качественные и количественные варианты ДНК-зондирования методом ПЦР имеют 100% точность и могут использоваться на самых ранних сроках после заражения. С помощью ПЦР выявляют персистирующие вирусы, которые находятся в клетке, продолжающей выполнять свои функции, а потому они с трудом обнаруживаются или не обнаруживаются другими методами.
Подобную диагностику можно проводить уже через 1–3 недели с момента предполагаемого заражения. Для такого тестирования используется венозная кровь (5–10 мл), которая берется натощак. Для получения ответа требуется один день.
НВsAg -качественный тест указывает лишь на наличие либо отсутствие заболевания. Очевидно, что отрицательный результат означает отсутствие заболевания, а положительный – наличие патологии. Последнее также может свидетельствовать о ранее перенесенном заболевании или носительстве. Любые сомнения подобного рода снимаются проведением количественного исследования на определение HBV-DNA методом ПЦР. Таблицы с трактовками маркеров острого и хронического гепатита B мы приводим ниже:
, MD, MPH, Harvard Medical School
Last full review/revision January 2019 by Anna E. Rutherford, MD, MPH
Вирус гепатита B (ВГВ) является наиболее полно охарактеризованным и сложным вирусом гепатита. Вирусная частица состоит из ядра и внешней оболочки. Ядро содержит циркулярную двухцепочечную ДНК и ДНК-полимеразу, вирус гепатита В реплицирует в ядре инфицированного гепатоцита. Оболочка вируса присутствует в цитоплазме и по неизвестным причинам производится в большом избытке.
HBV является второй наиболее распространенной причиной острого вирусного гепатита. Ранее нераспознанная инфекция достаточно распространена, но в настоящее время встречается гораздо реже, чем инфекция, вызванная вирусом гепатита А. В настоящее время в США ежегодно регистрируют примерно 3000 случаев острого вирусного гепатита В, что значительно меньше 25000 ежегодных случаев, регистрируемых до того, как появилась вакцина против гепатита В. Тем не менее, поскольку многие случаи не распознаются или о них не сообщается, ЦКЗ оценивает фактическое число новых заражений около 20 000 в год (см. Гепатит В: часто задаваемые вопросы [CDC Hepatitis B FAQs]).
HBV по неизвестным причинам иногда ассоциируется с экстрапеченочными расстройствами, включая нодозный полиартериит, другие заболевания соединительной ткани, мембранозный гломерулонефрит, эссенциальную смешанную криоглобулинемию. Патогенетическая роль ВГB при этих расстройствах неясна, предполагаются аутоиммунные механизмы.
Механизм передачи гепатита B
ВГB часто передается парентерально, обычно через инфицированную кровь или продукты крови. Рутинное обследование донорской крови на поверхностный антиген вируса гепатита В (HBsAg) привело практически к ликвидации ранее частой посттрансфузионной передачи, однако инфицирование через иглы, которыми пользуются внутривенно наркоманы, все еще остается актуальным. Риск инфицирования HBV остается высоким для пациентов на гемодиализе, в онкологических подразделениях и для персонала больниц, контактирующих с кровью.
Риск заражения младенцев гепатитом B, во время родов от инфицированных матерей, (см. неонатальный вирусный гепатит В) составляет 70- 90%, за исключением случаев, когда они получили иммуноглобулин против вируса гепатита B (HBIG) и были вакцинированы сразу же после родов. Более раннее трансплацентарное заражение возможно, но случается редко.
Вирус может передаваться через контакт слизистых оболочек с жидкостями организма (напр., между половыми партнерами, как гетеро-, так и гомосексуальными, в закрытых учреждениях, таких как психиатрические больницы и тюрьмы), но его инфективность намного ниже, чем у вируса гепатита A, более того, пути инфицирования часто остаются неизвестными.
Роль укусов насекомых в передаче не ясна. Многие случаи острого гепатита В возникают спорадически, без известного источника.
Хронические носители ВГB – резервуар инфекции повсеместно. Распространенность широко варьирует в зависимости от некоторых факторов, включая географическую зону (например, 0,5% в Северной Америке и Северной Европе, > 10% в некоторых регионах дальнего Востока и Африки).
Клинические проявления
Гепатит B вызывает широкий спектр болезней печени, от субклинического носительства до тяжелого гепатита или острой печеночной недостаточности (фульминантный гепатит), в частности у пожилых людей, у которых смертность достигает 10–15% случаев.
Большинство пациентов имеют типичные проявления вирусного гепатита, в том числе потерю аппетита, недомогание, лихорадку, тошноту и рвоту, с последующим развитием желтухи. Симптомы сохраняются от нескольких недель до 6 мес.
У 5–10% всех пациентов с ВГB развивается хронический гепатит или они становятся неактивными носителями. Чем меньше возраст при проявлении острого заражении, тем выше риск развития хронической инфекции:
Для детей в возрасте от 1 до 5 лет: 25-50%;
Взрослые: около 5%;
Если гепатит В переходит в хроническую форму, может развиваться цирроз печени, а в конечном счете также может развиваться гепатоцеллюлярная карцинома, даже без предшествующего цирроза.
Диагностика
Если подозревают острый вирусный гепатит, то проводят следующие тесты на выявление вирусов гепатита А, В и С:
Антитела к ВГA класса IgM (анти-HAV-IgM)
Поверхностный антиген гепатита В (HBsAg)
Антитела к сердцевинному антигену вируса гепатита В класса IgM (анти-НВс IgM)
Антитела к вирусу гепатита C (anti-HCV) и РНК-вирусу гепатита С (HCV-RNA)
Если какие-либо результаты тестов на гепатит В положительны, то необходимо провести дальнейшие серологические исследования для дифференцирования острой от ранее перенесенной или хронической инфекции (см. таблицу Серологический анализ на гепатит В [Hepatitis B Serology]). Если серология указывает на гепатит В, обычно проводится исследование на HВe-антиген (HBeAg) и антитела к HВe-антигену (анти-НВе), чтобы определить прогноз заболевания и назначить противовирусную терапию. Если серологически подтвержденная инфекция ВГB протекает в тяжелой форме, то исследуются антитела на вирус гепатита D (анти-ВГD).
Гепатит B имеет по крайней мере 3 системы антиген-антитело, которые могут быть исследованы :
Серцевинный антиген гепатита B (HBcAg);
Характерно появление HBsAg в инкубационный период, обычно в течение 1–6 нед до развития клинических или биохимических признаков болезни, что делает кровь такого индивидуума контагиозной. В период выздоровления он исчезает. Однако, он может иногда иметь транзиторный характер. Предполагаемые защитные антитела (анти-HBs) появляются через недели или месяцы после клинического выздоровления и обычно сохраняются на всю жизнь. Таким образом их обнаружение означает, что инфекция ВГB завершилась и иммунитет восстанавливается. В 5–10% случаев HBsAg сохраняется без выработки к нему антител. Такие пациенты становятся бессимптомными носителями или приобретают хроническую форму гепатита.
HBcAg – коровый (сердцевинный) антиген вируса. Определяется в инфицированных печеночных клетках, не определяется в сыворотке, если не применяются специальные технологии. Антитела к HBcAg (анти-HBc) обычно появляются с началом клинического заболевания, затем его титры постепенно снижаются, обычно с годами или в течение всей жизни. Их присутствие с анти-HBs указывает на выздоровление от ранее перенесенного инфекционного ВГB. Анти-HBc также присутствуют у хронических носителей HBsAg без сероконверсии в анти-HBs. При острой инфекции преимущественно определяются анти-HBc класса IgM, в то время как при хронической инфекции – анти-HBc класса IgG. Анти-HBc класса IgM – чувствительный маркер острой инфекции ВГB, иногда – единственный маркер недавно перенесенной инфекции, отражающий серологическое окно между исчезновением HBsAg и появлением анти-HBs.
HBeAg это белок, представляющий собой часть кор-протеина вируса (его не следует путать с вирусом гепатита Е). Присутствует только в HBsAg-позитивной сыворотке, наличие HBeAg предполагает активную репликацию вируса и высокую инфектогенность. По контрасту присутствие соответствующих антител (анти-НВе) предполагает меньшую инфектогенность. Маркеры е-антигена более помогают в определении прогноза заболевания, чем в его диагнозе. Хроническое течение чаще развивается среди пациентов с наличием HBeAg и менее часто – у пациентов с анти-НВе.
ДНК-ВГB может быть обнаружена в сыворотке пациентов с активным гепатитом.
Исследование проводится в целях первичного выявления вируса в организме и включает в себя определение в крови специфических маркеров инфицирования – суммарных антител ( IgG , IgM ) к вирусу гепатита С и вирусной РНК.
Какие тесты входят в данный комплекс:
- anti-HCV, антитела
- HCV , РНК [реал-тайм ПЦР]
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Исключить из рациона жирную пищу в течение 24 часов до исследования.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Вирус гепатита С (ВГС) – РНК-содержащий вирус из семейства Flaviviridae , который поражает клетки печени и вызывает гепатит. Он способен размножаться в клетках крови (нейтрофилах, моноцитах и макрофагах, В-лимфоцитах) и ассоциирован с развитием криоглобулинемии, болезни Шегрена и В-клеточных лимфопролиферативных заболеваний. Среди всех возбудителей вирусных гепатитов у ВГС наибольшее количество вариаций, а благодаря высокой мутационной активности он способен избегать защитных механизмов иммунной системы человека. Существует 6 генотипов ВГС, не исключена возможность инфицирования человека одновременно несколькими вирусами с различными генотипами. В 60-80 % случаев острая инфекция переходит в хроническую.
В лабораторной диагностике заболевания используют два основных подхода:
- серологические методы, основанные на обнаружении специфических антител к вирусу (anti-HCV);
- молекулярно-биологические методы, основанные на выявлении РНК вируса (реал-тайм ПЦР).
Антитела к вирусу гепатита С (anti-HCV) – специфические иммуноглобулины классов IgM и IgG к белкам вируса. Их появление в крови свидетельствует о возможной инфицированности или ранее перенесенной инфекции. Однако единственным достоверным критерием присутствия вируса в организме является определение вирусной РНК, так как она выявляется уже в первые 1-2 недели заболевания, в то время как антитела появляются в среднем через 8 недель. Определение вирусной РНК подходит и для обследования лиц, у которых антитела к вирусу не обнаружены, но в силу сопутствующих заболеваний или других причин (ВИЧ-инфекция, постоянный гемодиализ) снижена выработка антител.
Выявление РНК вируса считается "золотым стандартом" в диагностике гепатита С и подтверждает положительный результат обнаружения антител (anti-HCV) к белкам вируса и свидетельствует о наличии и репликации (размножении) вируса в крови.
Современные молекулярно-биологические методы диагностики обладают высокой чувствительностью (98-99 %) и в сочетании с серологическими исследованиями позволяют правильно оценить стадию заболевания, принять решение о тактике лечения, включая выбор препаратов и сроки медикаментозной терапии.
Для чего используется исследование?
- Для диагностики вирусного гепатита С;
- для дифференциальной диагностики гепатитов;
- для выявления ранее перенесенного вирусного гепатита С.
Когда назначается исследование?
- При обследовании людей из группы риска по заражению вирусным гепатитом С;
- при обнаружении антител к вирусу гепатита С для подтверждения диагноза;
- при симптомах вирусного гепатита и повышении уровня печеночных трансаминаз;
- если известно о перенесенном гепатите неуточненной этиологии;
- при скрининговых обследованиях;
- при сомнительных результатах серологического исследования;
- если ребенок родился от инфицированной матери;
- при гемодиализе;
- до начала лечения и в конце терапии вирусного гепатита C, затем через 6 и 24 месяца наблюдения.
Что означают результаты?
Для каждого показателя, входящего в состав комплекса:
1. Наличие антител (anti-HCV) не свидетельствует о продолжающейся репликации вируса, поскольку может являться признаком как текущей, так и перенесенной инфекции.
2. В ряде случаепри отсутствии антител не исключает инфекции - в ранний период острого гепатита C (ОГС) и при иммунодефицитах.
3. Необходимо учитывать, что у реципиентов, которым была перелита инфицированная кровь, могут обнаруживаться антитела (anti-HCV) донора; их наличие не обязательно свидетельствует о заражении HCV.
4. Одновременное обнаружение в крови РНК вируса и антител (anti-HCV) указывает на текущую острую инфекцию или обострение хронического гепатита С (ХГС). Дифференциальная диагностика острого гепатита С в большинстве таких случаев должна базироваться на наличии соответствующих данных эпидемиологического анамнеза за 1-4 месяца до момента обнаружения антител и увеличения печеночных ферментов.
5. Отсутствие РНК HCV при наличии антител (anti-HCV-позитивные образцы) в крови может являться признаком неустойчивой виремии, перенесенного острого гепатита, а также ложноположительного результата лабораторного исследования.
Интерпретация сочетаний серологических маркеров гепатита С
Читайте также:


