Гепатит дельта лечение 2020
Основные факты
- Вирус гепатита D (HDV) представляет собой вирус, для репликации которого необходим вирус гепатита B (HBV). Инфицирование HDV происходит только одновременно с HBV или в виде суперинфекции по отношению к HBV.
- Передача вируса чаще всего происходит перинатальным путем от матери ребенку, а также при контакте с кровью или другими биологическими жидкостями.
- Вертикальная передача от матери ребенку происходит редко.
- Не менее 5% всех людей с хронической инфекцией также инфицированы HDV. Другими словами, во всем мире число инфицированных HDV составляет 15-20 млн. человек. Тем не менее, это только приблизительная цифра, поскольку многие страны не ведут учета распространенности гепатита D.
- С 1980 г. наблюдается снижение общего числа случаев инфекции гепатита D в мире. Эта тенденция, главным образом, связана с успехами глобальной программы вакцинации против гепатита В.
- Коинфекция HDV-HBV считается самой тяжелой формой хронического вирусного гепатита ввиду более быстрого смертельного исхода от болезней печени и гепатоклеточной карциномы.
- В настоящее время показатели эффективности курсов лечения, в целом, невысоки.
- Инфекцию гепатита D можно предотвратить посредством иммунизации против гепатита В.
Гепатит D — это болезнь печени, протекающая как в острой, так и хронической форме, вызываемая вирусом гепатита D (HDV), для репликации которого необходим вирус HBV. Заражение вирусом гепатита D происходит только в присутствии вируса гепатита B. Коинфекция HDV-HBV считается наиболее тяжелой формой хронического вирусного гепатита гепатита ввиду более быстрого смертельного исхода от болезней печени и гепатоклеточной карциномы.
Единственным способом предотвращения инфекции HDV является вакцина против гепатита B.
Острый гепатит: одновременное инфицирование HBV и HDV может приводить к гепатиту в умеренной или тяжелой форме или даже к фульминантному гепатиту, но обычно за этим следует полное выздоровление, и хронический гепатит D развивается редко (менее чем в 5% случаев острого гепатита).
Суперинфекция: HDV может инфицировать человека, уже имеющего хроническую инфекцию HBV. Суперинфекция HDV при хроническом гепатите B ускоряет развитие более тяжелых форм болезни в любом возрасте у 70-90% людей. Суперинфекция HDV ускоряет развитие цирроза почти на 10 лет по сравнению с моноинфекцией HBV, несмотря на то, что HDV подавляет репликацию HBV. Механизм, ввиду которого HDV вызывает более тяжелый гепатит и ускоренное развитие фиброза по сравнению с моноинфекцией HBV остается неясным.
Риску инфицирования HDV подвержены хронические носители HBV.
Люди, у которых нет иммунитета к HBV (как естественного после болезни, так и в результате иммунизации вакциной против гепатита B), подвергаются риску инфицирования HBV, что сопряжено с риском инфицирования HDV.
Высокая распространенность гепатита D среди людей, употребляющих инъекционные наркотики, указывает на то, что употребление наркотиков является серьезным фактором риска коинфекции HDV.
Сексуальные контакты с высоким уровнем риска (например, у работников секс-индустрии) – также фактор повышенного риска инфекции HDV.
Миграция из стран с высокой распространенностью HDV в страны с низкой его распространенностью может оказывать влияние на эпидемиологическую ситуацию в принимающей стране.
Инфекция HDV диагностируется путем выявления высоких титров иммуноглобулина G (IgG) и иммуноглобулина M (IgM), антител к HDV, и подтверждается путем выявления РНК HDV в сыворотке.
Однако широкий доступ к диагностике HDV отсутствует, как и стандартизированный подход к анализу на наличие РНК HDV, который используется для мониторинга ответа на противовирусную терапию.
При отсутствии возможности количественного анализа РНК HDV целесообразным маркером для мониторинга реакции на лечение является HBsAg. Снижение титра HBsAg часто свидетельствует об исчезновении поверхностного антигена и клиренсе HDV, хотя исчезновение поверхностного антигена редко встречается при лечении.
В текущих руководствах обычно рекомендуется прием пегилированного интерферона альфа в течение как минимум 48 недель независимо от форм ответа на лечение. Общий уровень устойчивого вирусологического ответа низкий, однако это лечение является независимым фактором, ассоциированным с меньшей вероятностью прогрессирования заболевания.
Для пациентов с фульминантным гепатитом и болезнью печени на последних стадиях может рассматриваться возможность трансплантации печени. Необходимы новые терапевтические средства и стратегии. Новые препараты, такие как ингибитор пренилирования или ингибиторы входа HBV, дали предварительные положительные результаты.
ВОЗ не публиковала конкретных рекомендаций в отношении гепатита D. Тем не менее, рекомендованные меры по предотвращению передачи HBV, такие как иммунизация против гепатита B, безопасная практика инъекций, обеспечение безопасности крови и услуги по снижению вреда, заключающиеся в предоставлении стерильных игл и шприцев, эффективны для предотвращения передачи HDV.
В мае 2016 г. Всемирная ассамблея здравоохранения приняла первую “Глобальную стратегию сектора здравоохранения по вирусному гепатиту на 2016-2021 гг.”. В этой стратегии подчеркивается решающая роль всеобщего охвата услугами здравоохранения, а задачи стратегии находятся в соответствии с задачами в рамках Целей в области устойчивого развития. Главной целью стратегии является ликвидация вирусного гепатита в качестве проблемы общественного здравоохранения, и это отражено в глобальных задачах по сокращению числа новых случаев инфекции вирусного гепатита на 90% и сокращению смертности от вирусного гепатита на 65% к 2030 году. Действия, которые должны проводить страны и Секретариат ВОЗ для выполнения этих задач, изложены в стратегии.
Для оказания поддержки странам в ходе выполнения глобальных целей по гепатиту в рамках Повестки дня в области устойчивого развития на период до 2030 г. ВОЗ проводит работу по следующим направлениям:
- повышение осведомленности, укрепление партнерств и мобилизация ресурсов;
- разработка основанной на фактических данных политики и сбор данных для информационного обеспечения практических действий;
- предотвращение передачи инфекции;
- расширение услуг в области скрининга, ухода и лечения.
Кроме того, ежегодно 28 июля ВОЗ проводит Всемирный день борьбы с гепатитом для повышения осведомленности о вирусном гепатите и более глубокого осмысления связанных с ним проблем.
МОСКВА, 28 июл — РИА Новости, Альфия Еникеева. Ежегодно острые вирусные гепатиты уносят почти полтора миллиона жизней — больше, чем ВИЧ-инфекция, малярия и туберкулез. Во Всемирный день борьбы с гепатитом РИА Новости вместе с экспертами разбирается, чем опасна эта инфекция, и правда ли, что от нее теперь можно вылечиться.
Древняя болезнь

Их коллеги из Института изучения истории человечества Макса Планка в Йене полагают, что первое заражение человека произошло значительно позже — около семи тысяч лет назад. А британские ученые настаивают на еще более поздней датировке — от 4500 до 800 лет назад. При этом древнейшую вирусную ДНК гепатита В выделили из мумии XVI века, и она очень похожа на геном современного вируса, что само по себе странно. За пятьсот лет должны были произойти изменения.
Судя по многочисленным и противоречивым данным о происхождении вирусного гепатита, к согласию ученые придут не скоро. Пока ясно одно — несколько тысяч лет назад вирусный гепатит был столь же распространен, как и сегодня.
Как болеют россияне
"В России четыре-пять процентов взрослого населения болеют вирусным гепатитом В, два-пять процентов — гепатитом С. Это, конечно, не самые низкие показатели по миру, и в целом вирусный гепатит остается проблемой. Но что касается острого гепатита В, то мы тут на уровне передовых стран. И этого добились в последние 15-20 лет, когда появилась возможность привиться от этого заболевания", — рассказывает РИА Новости Галина Кожевникова, заведующая кафедрой инфекционных болезней медицинского института РУДН.
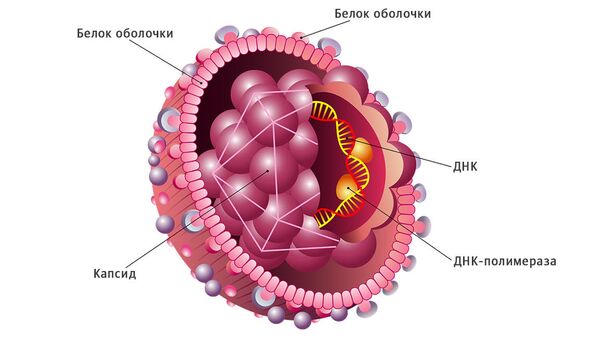
По словам Чавдара Павлова, профессора ПМГМУ имени И. М. Сеченова, в стране вирусный гепатит В уже стал управляемой инфекцией. Риск заражения при медицинских манипуляциях сведен к минимуму, вакцина, основанная на белке, а не на инфекционном материале, и хорошо переносимая людьми, внесена в Национальный календарь прививок и абсолютно бесплатна.
Два гепатита одним лекарством

Впрочем, по сообщениям Российского научного фонда, в ближайшие несколько лет на рынке могут появиться лекарства, способные полностью излечивать от вирусного гепатита В. Российские ученые первыми в мире разработали группу лекарственных препаратов, разрушающих вирус внутри клеток печени. Доклинические испытания на животных начнутся уже в следующем году.
Вероятно, это лекарство поможет и от гепатита дельта ( D ) — вируса-сателлита, которым заражаются инфицированные гепатитом В. Вирус-паразит кодирует всего один антиген (белок) и потому не может построить полноценную вирусную частичку — вирион. Для этого он использует белки оболочки вируса гепатита B.
Всего в мире около 15 миллионов человек инфицированы гепатитом дельта. Чавдар Павлов отмечает, что в России случаи коинфекции ( одновременного заражения вирусами гепатита В и дельта) и суперинфекции (инфицирования гепатитом D пациентов с хроническим гепатитом В) фиксируются в основном на Кавказе — в частности, в Дагестане.
Ласковый убийца обезврежен
Гепатит С — самый неприятный из всех вирусных гепатитов, так как острое течение болезни проходит практически бессимптомно. А при первых признаках недомогания — температура, тошнота, рвота, боли в мышцах — его можно спутать с обычным гриппом. Часто пациенты обращаются за медицинской помощью, когда болезнь уже запущена. Вирус гепатита С часто приводит к циррозу и раку печени, что в большинстве случаев заканчивается летальным исходом.

"Вакцины нет, ее сложно разработать. Вирус гепатита С ускользает от иммунологической защиты, внутри организма он меняет свои свойства. Те антитела, которые вырабатывала иммунная система три года назад, уже не действуют на новый, чуть измененный вирус. Но с гепатитом С очень хорошая история развития фармакологии. Сейчас мы совершенно точно можем говорить, что он излечим полностью. Разработаны и внедрены препараты так называемого прямого противовирусного действия. Они действуют на определенные структуры вируса, блокируют их и не позволяют ему размножаться", — резюмирует эксперт.
Специалисты предупреждают, что лучше свести риск заболевания этими опасными инфекциями к минимуму: вовремя вакцинироваться, предохраняться и с осторожностью относиться к пирсингу и татуировкам.
Среди примерно полумиллиарда лиц, инфицированных вирусом гепатита B, насчитывается около 25 млн инфицированных вирусом гепатита D. Дельта-вирус часто вызывает более тяжелые, быстро прогрессирующие поражения печени. Лечение дельта-вирусной инфекции остается нерешенной проблемой. Более 30 лет используются препараты интерферона. В настоящее время широкое распространение получил пегилированный интерферон альфа. Но применение препаратов интерферона не гарантирует излечения у большинства больных дельта-инфекцией, не обеспечивает стабильной элиминации вируса и дает множество побочных эффектов. Новые препараты с иным механизмом действия – аналоги нуклеотидов и препараты со специфическими механизмами действия мирклудекс B (myrcludex B), лонафарниб (lonafarnib), REP 2139 проходят клинические испытания. Перспективной представляется комбинированная терапия пегилированными интерферонами и аналогами нуклеотидов.
Среди примерно полумиллиарда лиц, инфицированных вирусом гепатита B, насчитывается около 25 млн инфицированных вирусом гепатита D. Дельта-вирус часто вызывает более тяжелые, быстро прогрессирующие поражения печени. Лечение дельта-вирусной инфекции остается нерешенной проблемой. Более 30 лет используются препараты интерферона. В настоящее время широкое распространение получил пегилированный интерферон альфа. Но применение препаратов интерферона не гарантирует излечения у большинства больных дельта-инфекцией, не обеспечивает стабильной элиминации вируса и дает множество побочных эффектов. Новые препараты с иным механизмом действия – аналоги нуклеотидов и препараты со специфическими механизмами действия мирклудекс B (myrcludex B), лонафарниб (lonafarnib), REP 2139 проходят клинические испытания. Перспективной представляется комбинированная терапия пегилированными интерферонами и аналогами нуклеотидов.
Лечение гепатита D
Согласно рекомендациям EASL 2017 г., терапией выбора у пациентов с коинфекцией HDV/HBV с хроническим гепатитом (ХГ) или компенсированным циррозом печени (ЦП) является пегилированный интерферон альфа (пегИФН-альфа) в течение 48 недель (уровень доказательности I, степень клинической рекомендации 1).
Больным с коинфекцией HDV/HBV с продолжающейся репликацией ДНК HBV необходимо назначать аналоги нуклеотидов (уровень доказательности II-2, степень клинической рекомендации 1).
При хорошей переносимости лечение пегИФН-альфа может быть продолжено до 48 недель независимо от ответа на него (уровень доказательности II-2, степень клинической рекомендации 2).
На сегодняшний день пегИФН-альфа – единственный доступный противовирусный препарат для лечения пациентов с хронической HDV-инфекцией с доказанной эффективностью. При использовании пегИФН-альфа вирусологический ответ на терапию достигается в 17–47% случаев [2].
По данным ряда исследований, у 25% пациентов концентрация РНК-HDV снижается на 24-й неделе применения пегИФН-альфа. Тем не менее поздние рецидивы после прекращения терапии отмечаются в 50% случаев, что позволяет подвергать сомнению возможность достижения устойчивого вирусологического ответа при коинфекции HDV/HBV. В связи с этим рекомендуется долгосрочное наблюдение за концентрацией РНК-HDV у всех получающих лечение пациентов – до тех пор, пока HBsAg определяется в сыворотке крови. Элиминация HBsAg возможна при длительном наблюдении примерно у 10% больных, находящихся на терапии пегИФН-альфа, что может служить маркером излечения HDV-инфекции [3, 4].
Были предприняты попытки повысить эффективность интерферонотерапии за счет увеличения ее длительности. Однако в настоящее время отсутствуют четкие доказательства, что подобная тактика подходит для большинства пациентов, хронически инфицированных HDV. При 96-недельной терапии пегИФН-альфа (монотерапия или в сочетании с тенофовиром) на 24-й неделе наблюдались рецидивы у 36,4% пациентов, ответивших на лечение [5].
Вероятность долгосрочного ответа на терапию пегИФН-альфа может быть оценена по уровням РНК-HDV и HBsAg на 12-й и 24-й неделе лечения. Преждевременное прекращение приема пегИФН-альфа не рекомендуется, если препарат переносится хорошо. Дело в том, что отрицательное прогностическое значение упомянутых маркеров невелико, а поздний ответ может возникнуть у больных с отсутствием раннего ответа на лечение. Предполагается, что терапия ИФН-альфа является фактором, приостанавливающим прогрессирование заболевания [6–9].
Ни аналоги нуклеотидов, ни рибавирин практически не влияют на уровень РНК-HDV у пациентов с HDV-инфекцией. Несмотря на то что HDV нередко доминирует, при естественном течении хронической HDV/HBV-инфекции можно наблюдать выраженные колебания концентрации обоих вирусов. Терапия аналогами нуклеотидов рекомендуется больным с уровнем ДНК-HBV выше 2000 МЕ/мл. Пациентам с декомпенсированным ЦП целесообразно назначать блокаторы репликации HBV, а не пегИФН-альфа. Такие больные должны пройти подготовку к трансплантации печени. Терапия аналогами нуклеотидов рекомендуется всем пациентам с декомпенсированным ЦП с определяемым уровнем ДНК-HBV [10, 11].
Современные рекомендации по применению интерферона альфа
Терапию ИФН-альфа могут получать только пациенты с компенсированным HDV-ассоциированным заболеванием печени. Единственным на сегодняшний день методом лечения декомпенсированного заболевания печени является трансплантация. ПегИФН-альфа – средство первого выбора при ХГ D. Годичный курс следует назначать всем больным, не получавшим ранее ИФН-альфа, а также тем, кто не ответил ранее на стандартную терапию ИФН-альфа. Сывороточные уровни РНК-HDV и HBsAg дают возможность клиницистам оценить ранний ответ, а также выявить больных с отсроченным вирусологическим ответом, которым может помочь длительная терапия [1, 2, 12].
Перспективы лечения хронического гепатита D
Эффективность терапии пегИФН-альфа как в монорежиме, так и в сочетании с аналогами нуклеотидов достаточно низкая, по окончании терапии часто возникают рецидивы. Поэтому крайне актуальна разработка новых видов терапии ХГ D.
В настоящее время клинические испытания проходят три класса новых лекарственных препаратов, влияющих на жизненный цикл HDV: ингибиторы его клеточного рецептора Na + -таурохолат ко-транспортного полипептида (NTCP), ингибиторы фарнезилтрансферазы (FTIs) и полимеры нуклеиновых кислот (NAPs).
Мирклудекс B: ингибитор проникновения вируса гепатита D в клетку
Впервые безопасность мирклудекса B для человека оценили A. Blank и соавт. В исследовании 36 здоровых добровольцев получали лекарственное средство либо внутривенно, либо подкожно в возрастающих дозах вплоть до 20 мг/сут. Использование препарата сопровождалось повышением уровня конъюгированных ЖК. Этот уровень на фоне длительного применения не достигал опасных для пациента значений. Концентрация мирклудекса B, необходимая для блокирования проникновения вирусов HBV/HDV через NTCP-рецептор, была приблизительно в 100 раз меньше, чем та, которая нарушала транспорт ЖК. Это указывало на возможность блокирования вирусов без избыточной нагрузки в отношении транспорта ЖК. Пациенты хорошо переносили лекарственное средство. Только в двух случаях отмечались серьезные побочные эффекты – повышение уровней липазы и амилазы. Данное исследование стало предварительным в отношении тестирования мирклудекса B у больных гепатитом B или D [17, 18].
Безопасность и эффективность мирклудекса B при ХГ D изучали в пилотном российском исследовании. 24 пациента были разделены на три группы поровну (рандомизация). Пациенты первой группы получали мирклудекс B 2 мг/сут в течение 24 недель после 48-недельной терапии пегИФН-альфа-2а, пациенты второй – мирклудекс B совместно с пегИФН-альфа-2а в течение 24 недель, затем монотерапию пегИФН-альфа-2a еще 24 недели. Пациентам третьей группы назначали только пегИФН-альфа-2a в течение 48 недель. Первой конечной точкой служил ответ HBsAg, определяемый как снижение сывороточной концентрации HBsAg не менее чем на 0,5 log IU/мл. Все пациенты были негативными по HBeAg, у троих имел место ЦП, девять больных ранее получали пегИФН-альфа-2a. Исходно средняя сывороточная концентрация РНК-HDV составила примерно 10 4 копий/мл, а средняя концентрация HBsAg около 10 4 IU/мл. Промежуточный анализ на 24-й неделе исследования у пациентов, получавших только мирклудекс B, показал нормализацию уровня аланинаминотрансферазы (АЛТ) в шести случаях и снижение уровня РНК-HDV более чем в 10 раз (1 log) – в четырех, с клиренсом 2. Однако уровень HBsAg оставался неизменным у всех больных. После прекращения лечения РНК-HDV вновь обнаруживалась у всех пациентов. У пятерых больных из тех, кто получал мирклудекс B вместе с пегИФН-альфа-2a, РНК-HDV стала негативной. ДНК-HBV также значимо снизилась только в этой группе. Побочными эффектами мирклудекса B были тромбоцитопения, лимфопения, эозинопения, нейтропения. Причем все изменения были незначительно выраженными, преходящими и не требовали изменения дозы препарата. Антитела к исследуемому препарату выявлены у шести пациентов, получавших комбинированное лечение с пегИФН-альфа-2a. Несмотря на то что это не влияло на эффективность лечения, ученые проанализировали значение данных антител. Во всех группах, в которых применяли мирклудекс B, уровень ЖК, конъюгированных с таурином и глицином, повышался [19].
Таким образом, мирклудекс B вызывает значительное снижение уровня РНК-HDV. Но этот эффект нестойкий, по окончании терапии не сохраняется. Результаты лечения были выше у больных, получавших одновременно мирклудекс B и пегИФН-альфа-2a. Монотерапия препаратом мирклудекс B при ХГ D малоэффективна. Уровни HBsAg не менялись при использовании мирклудекса B. Авторы предположили, что HBsAg может продуцироваться интегрированной в геном ДНК-HBV, отличной от cccDNA, и HBsAg снижается независимым от кинетики ДНК-HBV образом. Эффекты длительной монотерапии мирклудексом B или комбинированной терапии с пегИФН-альфа-2a и тенофовиром, а также использование более высоких доз должны быть изучены в дальнейших исследованиях [20].
Ингибитор сборки вируса лонафарниб и препарат REP 2139
Блокада процесса фарнезилирования с помощью FTI способствует накоплению промежуточных продуктов репликации HDV внутри гепатоцитов. Снижение концентрации сывороточной РНК-HDV происходит не за счет уменьшения количества инфицированных гепатоцитов, а в большей степени за счет снижения сборки частиц вируса HDV. Механизм, с помощью которого FTI уменьшает концентрацию сывороточной РНК-HDV, еще предстоит установить, а эффект внутриклеточного накопления частиц РНК остается малоизученным. Вопрос, может ли накопление репликативных интермедиатов HDV в печеночных клетках индуцировать цитотоксический эффект или усиливать иммуноопосредованное уничтожение клеток, остается нерешенным [23].
Лонафарниб, один из FTI, был изначально предложен как противораковое средство, поскольку фарнезилтрансфераза является важным клеточным ферментом, вовлеченным в некоторые клеточные функции, в том числе фарнезилирование ряда цитоплазматических белков семейства RAS, участвующих в росте, дифференцировке и выживании клеток, а также в Т-клеточной активации и выработке цитокинов [24, 25].
15 участников исследования LOWR HDV-1 (лонафарниб с добавлением ритонавира и без него для лечения HDV-инфекции) были разделены поровну на пять групп для определения оптимальной дозы препарата. Лонафарниб назначали в дозах 200 и 300 мг дважды в день или 100 мг трижды в день как в монорежиме, так и в сочетании с ритонавиром или пегИФН-альфа от восьми до 12 недель. Поскольку ритонавир является ингибитором цитохрома P450-3A4 – главного метаболизатора лонафарниба, предполагалось, что эта комбинация обеспечит максимальный внутрипеченочный уровень препарата. После четырех недель лечения HDV-виремия значительно уменьшилась независимо от схемы назначения лонафарниба – в монорежиме или в комбинации с другими препаратами. Это сочеталось со значительным снижением уровня АЛТ, однако отсутствовали изменения содержания HBsAg. Добавление ритонавира 100 мг к лонафарнибу 100 мг два раза в день вызывало более значительный антивирусный эффект и меньшее количество гастроинтестинальных побочных эффектов. Но в этой комбинации показатели HBsAg также не менялись. К концу лечения уровни сывороточных РНК-НDV и АЛТ возвращались к исходным параметрам у всех пациентов, за исключением двух. Пять пациентов, которые получали лонафарниб в дозах 200 и 300 мг дважды в день с пегИФН-альфа, прервали лечение в течение четырех недель из-за непереносимости [27].
Три других исследования под тем же акронимом (LOWR HDV-2, -3, -4) продолжаются, но предварительные результаты опубликованы в виде тезисов. В исследовании LOWR HDV-2, посвященном оценке наименьшей эффективной дозы лонафарниба в комбинированной терапии, 48 пациентов получали небольшие дозы препарата (75, 50 или 25 мг дважды в день) в комбинации с ритонавиром и пегИФН-альфа или без пегИФН-альфа. Тройной режим с лонафарнибом 25 или 50 мг, ритонавиром 100 мг дважды в день в комбинации с пегИФН-альфа 180 мкг показал лучший результат и переносимость [28].
В исследовании LOWR HDV-3 21 больной получал однократные ежедневные дозы лонафарниба (50, 75 или 100 мг) с ритонавиром 100 мг в течение 12 или 24 недель. Пациентам проводилась анти-HBV-терапия аналогами нуклеозидов до назначения лонафарниба. После 12 недель лечения средний log снижения концентрации РНК-HDV от исходного уровня колебался от 0,83 IU/мл (для лонафарниба 100 мг) до 1,6 IU/мл (для лонафарниба 50 мг). Комбинация ритонавира и лонафарниба у больных, получавших лечение в течение шести месяцев, была безопасной и эффективной в отношении снижения виремии HDV [29].
Увеличение дозы и достижение толерантности оценивали в исследовании LOWR HDV-4 с участием 15 пациентов. На старте терапии все больные получали лонафарниб в дозе 50 мг одновременно с ритонавиром 100 мг. Далее доза лонафарниба была увеличена до 75 мг, затем до 100 мг. Ритонавир назначали в дозе 100 мг дважды в день. В конце лечения снижение концентрации сывороточной РНК-HDV от исходного уровня составило 1,58 ± 1,38 log10 IU/мл. Уровни АЛТ нормализовались у 53% больных. Снижение РНК-HDV и нормализация уровня АЛТ не сохранялись после прекращения терапии. Кроме того, лонафарниб не оказывал существенного влияния на уровни HBsAg как до, так и после лечения. Возникновения резистентных мутаций не зафиксировано [30].
Значимость накопления рибонуклеопротеидного комплекса в гепатоцитах обусловливает перспективы длительного применения лонафарниба у больных ЦП. Более того, фарнезилтрансфераза является важным клеточным ферментом, что существенно для полного установления влияния его ингибирования на разнообразные внутриклеточные процессы.
REP 2139: полимер нуклеиновой кислоты
Фосфотионат фосфорилированных аналогов нуклеотидов (NAP) – это олигонуклеотиды с негативным зарядом и широкой ингибиторной активностью в отношении ряда вирусов (например, ВИЧ, вирус простого герпеса, вирус лимфоцитарного хориоменингита). Однако на модели НBV-инфекции на утках показано, что NAPs влияют как на проникновение вируса в клетку, так и на синтез и высвобождение HBsAg из гепатоцитов. Основываясь на этих результатах, безопасность и эффективность REP 2055 (Replicor) и REP 2139 (Replic) oценивали в первом, основанном на принципах доказательной медицины, исследовании у HBV-инфицированных HBeAg-позитивных больных. В обоих исследованиях на фоне монотерапии NAP наблюдалось уменьшение концентрации сывороточного HBsAg и ДНК-HBV с 2 до 7 и с 3 до 9 log соответственно, что сопровождалось появлением сывороточных анти-HBs (10–1712 мIU/мл). Из побочных эффектов лечения наблюдались лихорадка, головная боль и озноб [31–34].
Основываясь на значительном эффекте на сывороточный HBsAg, ученые изучили безопасность и эффективность REP 2139 в комбинации с пегИФН-альфа при ХГ D. В молдавском исследовании принимали участие 12 ранее не леченных больных в возрасте от 18 до 55 лет, позитивных по анти-HBeAg-антителам, а также по РНК-HDV с концентрацией сывороточного HBsAg свыше 1000 IU/мл и низким уровнем ДНК-HBV (от


До недавнего времени эффективного лечения "дельты" не существовало. Но вот сейчас - и об этом было сказано в "РГ" - оно, наконец-то, появилось. И именно на российском рынке. В Великобритании препарат получил статус "перспективной инновационной терапии", в США - статус "терапии прорыва". На встрече договорились отслеживать продвижение лекарства.
Гепатит не из разряда редких, неизвестных недугов. Напротив, он легко распространяется и может стать причиной эпидемии. Врачи мира признали его глобально опасной проблемой.
Еще в 80-е годы прошлого века Всемирная организация здравоохранения (ВОЗ) включила вирусные гепатиты в перечень наиболее опасных инфекционных заболеваний, для борьбы с которыми требуется объединение усилий служб здравоохранения всего мирового сообщества. Ведь при гепатитах прогноз не многим лучше, чем при СПИДе. По данным ВОЗ, гепатит вирусной модификации поразил уже 2 млрд. человек. То есть каждого третьего жителя Земли. Кто-то уже переболел им. Кто-то - носитель патологии. Да и сам факт, что 28 июля каждого года отмечается Всемирный день борьбы с гепатитами, свидетельствует о важности противостояния недугу.
Почему выбран именно этот день? Да потому что ВОЗ решила приурочить его к дню рождения великого исследователя Баруха Бламберга, который в 1976 году получил Нобелевскую премию за открытие вируса гепатита В и изучение его патологического воздействия на печень.
Почти полвека прошло. Для гепатита, выходит, не срок. А ведь меры противостояния известны. Соблюдение гигиены, внимательность при переливании крови, осторожность при выборе половых партнеров, вакцинация. Ничего особенного. Однако повсеместно не соблюдают, вакцинацию нередко игнорируют.


На круглом столе, что прошел в "РГ", руководитель отделения гепатологии МОНИКИ Павел Богомолов, главный специалист Минздрава РФ по инфекционным болезням профессор Елена Малинникова, председатель совета директоров биотехнологической компании "Гепатера" Дмитрий Попов обсуждали пути доступности профилактики и лечения этого грозного заболевания.
Участники "круглого стола" - и специалисты, и приглашенные гости - убеждены: надо более настойчиво и более доходчиво информировать о путях заболевания, о соблюдении правил гигиены и прохождении диспансеризации.
В нашей стране гепатит находится в списке социально опасных заболеваний. По примерным подсчетам, на территории России не менее 2,5% населения больны или инфицированы тяжелым заболеванием печени. Потому такое внимание к опыту Московской области, о котором рассказал Павел Богомолов. Область стала пионером в лечении пациентов с хроническим гепатитом С по полису ОМС.
Еще в 2014 году жители Подмосковья начали получать специальную терапию. С тех пор пролечено более 5500 пациентов. Опыт позволил расширить географию помощи: с 2017 года пролечено более 2000 пациентов с гепатитом С из более чем 15 регионов России. "Лечение вирусных гепатитов в рамках базовой программы ОМС, - отметил Павел Олегович, - означает, что любой гражданин РФ в любой точке страны может получить противовирусную терапию".
Согласитесь, информация, которая очень много значит и для страдающих тяжелейшими заболеваниями печени, и для их близких. Потому сразу последовали вопросы из зала. Вот человек живет не в Москве и не в Московской области. Он действительно может получить бесплатную медицинскую помощь, если ему поставлен диагноз гепатит С? Был приведен конкретный пример. Последовал четкий ответ Богомолова: "Не только может, но обязательно получит. Во многих субъектах начала действовать программа лечения гепатита С по ОМС".
Читайте также:


