Что такое модификация вирусов
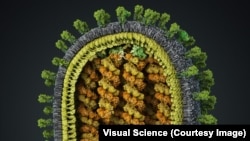
Исследователи создают в лабораториях опасные для человечества модификации вирусов. Научное сообщество задается вопросом, оправдан ли такой риск
Пожалуй, по-настоящему сильно наука стала пугать с момента создания атомного оружия: из бутылки был выпущен страшный джинн, и с тех пор едва ли не любые масштабные научные эксперименты и технологические прорывы вызывают опасения. Достаточно вспомнить разговоры о том, что запуск экспериментов на Большом адронном коллайдере может привести к возникновению микроскопических черных дыр, способных уничтожить планету, или сомнительную кампанию против использования ГМО в пищевой промышленности. Но у человечества появились возможности для куда более скорого самоубийства.
К двадцатому веку любопытное человечество достигло достаточного уровня развития, чтобы в результате своей деятельности цивилизация смогла уничтожить сама себя. Это медленное уничтожение происходит каждый день: через вызванные антропогенными факторами климатические изменения, через неосмотрительное использование ресурсов, через загрязнение окружающей среды. И все же самый распространенный сюжет научной паранойи в популярной культуре, в первую очередь в кино (можно вспомнить "12 обезьян" Терри Гиллиама, "28 дней спустя" Дэнни Бойла и многие другие), – пандемия, вызванная созданным в секретной лаборатории вирусом. И если опасности запуска БАКа большинство ученых не воспринимали всерьез, а дискуссия о вреде ГМО подогревается в первую очередь невежеством, то риски, связанные с проведением некоторых видов вирусологических исследований, широко обсуждаются в последние годы в научном сообществе и даже в некотором роде разделили биологов на два непримиримых лагеря.
В 2012 году голландский вирусолог Рон Фуше попал в список самых влиятельных людей года по версии журнала Time и в список самых ярких ученых года по версии журнала Nature. Этой чести он удостоился за то, что создал, возможно, самого страшного рукотворного монстра в истории человечества.
Фуше, исследователь из медицинского центра Эразмуса в Роттердаме, создал модификацию вируса птичьего гриппа H5N1, способную передаваться воздушно-капельным путем от хорька к хорьку. Известными природными модификациями птичьего гриппа млекопитающие, в том числе люди, могли заразиться (за исключением редких случаев) только при прямом контакте с больными птицами. Хотя птичьим гриппом переболело в общей сложности всего несколько сотен человек, официально признанная Всемирной организацией здравоохранения смертность составила от 25 до 50 процентов. Постепенно мутировав в естественных условиях, вирус птичьего гриппа может приобрести способность передаваться от животного животному и от человека человеку, а это грозит глобальной опустошительной пандемией, сравнимой с эпидемией испанского гриппа, от которой в 1918-1919 годах умерло несколько десятков миллионов человек. Именно для того, чтобы определить возможные направления естественной мутации вируса, в 2011 году Рон Фуше в лабораторных условиях создал свой искусственный штамм, в том же году независимо от Фуше аналогичный эксперимент произвела научная группа под руководством Йосихиро Каваоки из американского университета Висконсин-Мэдисон.
Сложно сказать, насколько созданные Фуше и Каваокой вирусы опасны для человека: об этом можно рассуждать только в теории. Впрочем, хорьки болеют тем же спектром вирусов гриппа, что и люди. По некоторым оценкам, вырвись мутировавший птичий грипп из лабораторий, он мог бы унести до 15 процентов населения Земли.
РИСК 1: ПУБЛИКАЦИИ
Сомнения в этичности и безопасности подобных исследований возникли немедленно: Научный совет по биобезопасности США рекомендовал научным журналам задержать публикацию работ Фуше и Каваоки, опасаясь, что, попав в публичное поле, описание метода создания вируса-убийцы может послужить инструкцией для потенциальных биотеррористов. Глава этого совета Поль Кейм, специалист по сибирской язве, сказал тогда в интервью изданию Science Insider об искусственном штамме птичьего гриппа: "Не могу вообразить более страшного патогенного организма. Сибирской язве до него очень далеко".
Впрочем, многие ученые уверены, что опасность публикации результатов подобных исследований преувеличена. “Да, при помощи этих данных теоретически можно получить патогенный вирус, например, включив в геном не очень патогенного птичьего вируса необходимые мутации, – считает Татьяна Цфасман, сотрудник лаборатории генетики РНК-содержащих вирусов НИИ вакцин и сывороток им. И.И.Мечникова. – Но это долгая работа, требующая высокой квалификации и некоторых специальных умений и знаний, а именно, нужен человек, который хорошо владеет методами обратной генетики вируса гриппа. Зачем террористам так мучиться?” С Цфасман согласен и Юрий Стефанов, сотрудник Института молекулярной биологии им. В. А. Энгельгардта РАН: “Это [создание вирусов в лаборатории] довольно хлопотно и затратно, а выхлоп представляется не очевидным и слабо предсказуемым”. Кроме того, научная статья – это все-таки не инструкция из IKEA по сборке вируса-убийцы. “В том же Nature методическая часть, например, довольно скупая. И очень часто бывает так, что по статье вроде бы идея экспериментов ясна, но конкретные детали не раскрыты или присутствуют ссылки на “стандартные методики”, – объясняет Стефанов.
В конечном итоге мораторий был снят и статьи опубликованы: работа Рона Фуше – в Science, а статья Каваоки – в Nature, но оба ученых и еще 38 ведущих мировых вирусологов взяли на себя добровольное обязательство в течение года не проводить опасных экспериментов типа gain-of-function (GOF, это можно перевести как "эксперименты приобретения свойств") – к этому типу как раз и относятся исследования, в процессе которых путем лабораторных манипуляций создаются новые штаммы опасных вирусов, крайне вирулентных и против которых у человека нет естественного иммунитета.
Дискуссия о том, перевешивает ли польза от создания искусственных вирусов возможные риски, с тех пор не утихала. В 2012 году Министерство здравоохранения и социальных служб США утвердило набор критериев, которым должно удовлетворять научное исследование вируса птичьего гриппа, чтобы претендовать на государственное финансирование. Вот главные из них: в процессе эксперимента не должен быть создан опасный штамм вируса, если только нет уверенности, что такая же его форма может развиться и в природе. Кроме того, оговаривается, что искусственное создание вирусов допускается, только если основной цели исследования нельзя добиться другими, менее рискованными методами. Позже в США были введены и другие правила, в частности, описания опасных экспериментов должны проходить дополнительную проверку перед публикацией. Все эти меры не отбили у вирусологов желание создавать искусственные формы смертоносных вирусов: дождавшись окончания добровольного годового моратория, Фуше и Каваока заявили, что планируют провести эксперименты над другим штаммом птичьего гриппа H7N9, несколько случаев заражения которым были зафиксированы в Китае весной 2013 года. Совсем недавно, в апреле этого года, были опубликованы результаты эксперимента уже другой научной группы из США по созданию передающейся от млекопитающего к млекопитающему версии еще одного штамма – H7N1. Стоит отметить, что статья прошла обязательную проверку перед публикацией, и мнения экспертов разделились: не все из них были согласны, что польза от проведенного эксперимента перевесила потенциальные риски.
Масла в огонь непрекращающихся споров о том, насколько оправданно создание в научных лабораториях монстров, способных уничтожить значительную часть человечества, подлила только что опубликованная в авторитетном медицинском журнале PLoS Medicine статья Марка Липситча из Гарварда и Элисон Гальвани из Йеля. Авторы обрушились на вирусологические исследования GOF (приобретения свойств), отмечая, что даже самые строгие меры безопасности не могут исключить случайное заражение лабораторного работника и дальнейшее стремительное распространение инфекции. Эксперименты такого рода в США проводятся с соблюдением высоких стандартов биобезопасности (в американской номенклатуре – уровня 3 или 3+), что предполагает не более двух инцидентов – в первую очередь, случайного заражения сотрудника лаборатории – за тысячу лет работы лаборатории. Липситч и Гальвани указывают на то, что даже такой, казалось бы, минимальный риск в действительности означает, что десять проводящих эксперименты GOF лабораторий дают 20-процентную вероятность трагического происшествия в течение одного десятилетия.
Авторы приводят несколько оценок вероятности того, что случайное лабораторное заражение приведет к значительному распространению инфекции. Ни одна из них не является достаточно обоснованной и состоятельной, да и разброс велик: Липситч и Гальвани делают вывод, что такой риск лежит в пределах от 5 до 60 процентов. “Как вы понимаете, – написал Марк Липситч в ответ на запрос Радио Свобода, – подобная оценка зависит от точных характеристик способов инфицирования агентом, уровня надзора над лабораторными сотрудниками и других факторов. Наш аргумент заключается в том, что, хотя мы и вряд ли когда-нибудь узнаем, где именно, в пределах 5 и 60 процентов, лежит истинная вероятность катастрофы, даже 5% процентов очень пугают, ведь мы говорим о вероятности распространения вирулентного и опасного вируса”. Комбинируя вероятности того, что за десятилетний промежуток в одной из 10 работающих лабораторий произойдет опасный инцидент (0,2), и того, что это происшествие приведет к полномасштабной эпидемии (0,05 – 0,6), получается, что реальный риск пандемии, вызванной искусственным вирусом, лежит в пределах 1–12%.
Липситч не смог точно сказать, сколько именно лабораторий в мире сейчас работают над экспериментами GOF: “Если судить по опубликованным в последние годы научным работам, такие лаборатории есть в США (минимум две), Нидерландах, Китае (не представляю, сколько именно), Японии (скорее всего, Каваока проводит свои исследования и там, и в США), Италии и Великобритании”. Итого получается как раз порядка 10 лабораторий, а значит, в течение десятилетия с небольшой, но заметной вероятностью в одной из них может произойти утечка сверхопасного искусственного патогена, которая приведет к пандемии.
Опрошенные Радио Свобода эксперты считают, что сделанные Липситчем и Гальвани пугающие оценки плохо обоснованы. “Хотелось бы подробностей и более серьезных источников в плане ссылок, – сказала Цфасман. – Из двух ссылок, которые авторы статьи дают к абзацу про оценку рисков, одну статью найти не удалось, а вторая – это нечто малонаучное, с какими-то расчетами, но без обоснования того, откуда они берут исходные цифры. Я работала в условиях BL3 – и в целом я считаю, что риск заражения персонала и распространения вируса из BL3 там сведен к минимуму. Не берусь оценивать риск в процентах, потому что эти проценты будут столь же взяты с потолка, как и в статье, на которую ссылаются авторы”.
Юрий Стефанов согласен: “Статья Липситча и Гальвани мне показалась несколько избыточно алармистской. В частности, описывая угрозы, исходящие от неаккуратного обращения с вирусами в лабораториях, авторы ссылаются на статью более чем двадцатилетней давности, в которой присутствует спекуляция на тему того, что одна из крупных эпидемий прошлого века могла быть косвенно связана с лабораторным вирусом. А могла и не быть связана. Мне, честно говоря, эта информация раньше не попадалась”.
Марк Липситч не настаивает, что сделанные в его статье оценки близки к реальности: “Мы как раз и предлагаем, чтобы была произведена независимая и точная оценка рисков. Сделать ее должны эксперты, не имеющие конфликта интересов, которые не будут заинтересованы в определенном результате экспертизы. Нужно иметь в виду, что хотя любые такие оценки не будут достаточно точными (как бывает всегда, когда речь идет об оценке маловероятных событий), но это не так уж важно: даже относительно невысокая вероятность большой катастрофы неприемлема”. Липситч привел такое сравнение: “Вероятность того, что именно сегодня ограбят именно этот банк, очень мала, но банк все же не откроется с утра, если на работу не выйдет охранник”.
НАУКА ИЛИ ЗДРАВООХРАНЕНИЕ
На одной чаше весов – возможность подробно разобраться в том, в каком направлении может пойти опасная мутация относительно безобидного для человека вируса, в том, как устроен монстр, с которым мы можем рано или поздно встретиться в природе. На другой – небольшая, но заметная вероятность, что этот монстр разорвет сковывающие его цепи и вырвется на свободу. Главный посыл статьи Липситча и Гальвани состоит в том, что, проводя рискованные исследования, нужно исходить не из научной любознательности, не из стремления к познанию, а из того, полезны ли эксперименты для здравоохранения, способны ли их результаты спасти жизни людей и можно ли добиться этих же результатов другими, безопасными методами.
“Из десятка очень многообещающих подходов к лучшему предупреждению и лечению гриппа есть только один, который угрожает миру пандемией, – считает Липситч. – И этот подход в то же время далеко не самый лучший в отношении научного потенциала, эффективности и способности в будущем спасти человеческие жизни. Ученым постоянно приходится делать нелегкий выбор, на что именно тратить ограниченные финансовые ресурсы. Мы считаем, что GOF-исследования не оправданы, если сравнить ту небольшую пользу, которую они способны принести, и связанный с ними огромный риск”.
К сожалению, единого мнения о том, насколько на самом деле необходимы для здравоохранения работы Фуше, Каваоки и других ученых, работающих над GOF, в научном сообществе нет. Действительно, для изучения мутаций вирусов существуют и другие способы, например, компьютерное моделирование или лабораторная работа с безопасными модификациями вирусов. Татьяна Цфасман объясняет, что подавляющее число ученых идут именно по этому пути: “Есть очень много данных, полученных исключительно методами биоинформатики, то есть только путем сравнения последовательностей вируса гриппа. Кроме того, большая часть лабораторий, которые что-то делают с вирусами птичьего гриппа, работают с безопасными реассортантами этих штаммов с лабораторными штаммами (вирусов, которые несут несколько генов от высокопатогенного штамма и остальные гены – от безопасного лабораторного штамма). Например, наша лаборатория в Институте Мечникова в Москве работала именно с таким безопасными реассортантами. Таких исследований большинство, хотя бы потому, что далеко не у всех лабораторий есть возможность работать в условиях 3-й степени биологической опасности, да и ни один разумный человек по доброй воле не захочет больше, чем надо, работать в этих условиях”.
Но достаточно ли этих безопасных и недорогих методов для того, чтобы предотвратить возможную пандемию? “Моделирование и сравнительная геномика – это инструменты, которые становятся все более и более сильными, – объясняет Юрий Стефанов. – Но все-таки обычно после моделирования и компьютерных расчетов ученые говорят: а теперь давайте посмотрим, как это работает в живой системе. Думаю, моделирование, при очевидной безопасности, даст все же менее надежные результаты, чем если изучаемые замены внедрить в настоящие белки и посмотреть, что будет”.
Цфасман согласна: “К сожалению, опыты на животных наиболее приближены к жизни, и только так можно проверить предположения, сделанные на основе других методов. Альтернатива – только наблюдение за естественным развитием событий (анализ высокопатогенных птичьих штаммов, вызвавших заболевание человека и птиц). Но этот второй метод существенно более медленный”.
Итак, одна партия утверждает, что только создание в лабораторных условиях искусственных опасных мутантов позволит нам предотвратить глобальные эпидемии и создать действенные вакцины. Но прямых подтверждений этой точке зрения пока нет и, видимо, не будет, пока природный птичий грипп не станет реальной угрозой человечеству. Оппоненты считают, что такие эксперименты слишком опасны, но точно оценить, насколько эта опасность велика, никто не берется, да это и вряд ли возможно. Первых можно обвинить в том, что они идут на неоправданный риск, кто-то, может быть, из тщеславия, а кто-то просто потому, что познание для ученого – высшая ценность. Вторых небезосновательно можно назвать алармистами. Ведь остановить научный прогресс вряд ли возможно, если только мы не хотим вернуться к охоте и собирательству. Нам пришлось привыкнуть жить в мире, в котором атомные установки вырабатывают энергию, коллайдеры сталкивают между собой частицы на околосветовых скоростях, а десятая часть мировых посевных площадей засеяна генетически модифицированными культурами. Мы научились создавать опасных монстров, и теперь все, что нам остается, – следить, чтобы сковывающие их цепи были надежны.
Иллюстрация любезно предоставлена студией Visual Science. Подробнее об изображении: Изображение Вируса гриппа A/H1N1. Visual Science 2014.

Семен Есилевский, биофизик, доктор физико-математических наук, ведущий научный сотрудник Института физики НАН и стипендиат программы им. Марии Кюри в Университете Бургундии Франш-Конте, Франция, рассказывает, почему не следует доверять разговорам о том, что коронавирус был создан искусственно.
Марго Гонтар: Мог ли, на ваш взгляд, этот коронавирус быть создан искусственно?
Семен Есилевский: Для того чтобы говорить о том, что он был создан, должны быть хотя бы какие-то доказательства. Голословно мы можем утверждать все что угодно, в том числе что Луна сделана из сыра, но без доказательств это ничего не стоит. На сегодняшний день доказательств именно научных, которые выдерживали бы хоть какую-то научную критику, нет. Это просто теория заговора в чистом виде.
М.Г. : Как вы думаете, почему сейчас она распространяется?
С.Е.: Теории заговора привлекают людей, потому что дают какую-то видимость контроля над ситуацией. Любому человеку некомфортно в ситуациях, которые он не контролирует. Есть люди, у которых этот дискомфорт выливается в то, что они пытаются найти какую-то внешнюю силу, которая всем управляет, чтобы снять с себя ответственность. Это людей психологически успокаивает. Появление этого в периоды потрясений, глобальных катаклизмов и стрессов усиливается, поэтому, естественно, усиливаются и теории заговора.
Вторая версия базируются на том, что одна из соавторов работы, которая создавала химерные вирусы в 2015-м, работала в Ухане в университете в том самом регионе, откуда пошел этот коронавирус. Но если вы исследуете вирусы летучих мышей – а это была работа о вирусе летучих мышей – то вполне логично основывать лабораторию там, где, во-первых, эти летучие мыши водятся, чтобы не через полмира, а, во-вторых, там, где от этих летучих мышей ожидаются какие-то проблемы. В Китае это все совпадает, потому что там летучие мыши плодятся в большом количестве, там их едят, продают на рынках, и уже были случаи передачи инфекции от летучих мышей людям. Где же еще основывать зоологического лабораторию по изучению вирусов летучих мышей, как не там? А эта версия все переворачивает с ног на голову. Мол, раз их изучали, значит это подтверждение того, что вирус из лаборатории.
М.Г.: Почему необходимо было создавать лабораторию по изучению вирусов летучих мышей именно там, где с ними проблема, в Ухане?
С.Е.: Дело в том, что летучих мышей в лабораторных условиях содержать достаточно непросто. Это не обычная мышь, не крыса и не хомячки. C ними много мороки. Некоторые виды летучих мышей содержать в лаборатории практически невозможно, их надо где-то отлавливать, и желательно находиться там, где их отлавливать легко и где их и так много. Этим все объясняется.
М.Г.: Возвращаясь к вопросу о биооружии, целесообразно ли вообще использование этого вируса?
С.Е.: Основная проблема биологического оружия состоит в том, что не понятно, как защитить того, кто его применяет. Это либо просто тотальный геноцид всего человечества, либо оно не будет нормально работать, тут третьего не дано. В фантастике можно найти множество вариантов решения этого вопроса, специалисты по биобезопасности тоже это обдумывали. Один из вариантов – создавать вирусы, которые, например, селективно поражают людей с определенным типом. Например, определенной расы, определенной национальности и так далее. Но эта идея не работает, хотя бы потому что расы от друг друга не настолько отличаются, чтобы вызывать селективность вируса. А, во-вторых, просто потому, что людей чистокровных, так сказать, практически нигде в мире нет. Все так или иначе перемешаны. Кроме того, нельзя найти ни одной инфекции в человеческой истории, которая селективно поражала бы одну расу. Все инфекции поражают всех.
М.Г.: Возможно ли создать защиту, с помощью которой мог себя обезопасить распространитель вируса? Вакцину, например.
С.Е.: Самое простое – закрыться в бункере и подождать, пока все умрут, а потом оттуда выйти. Из логических вариантов: впрыснуть себе антидот, который не даст заболеть, это из той же области научной фантастики. Надо понимать, что вирус мутирует. Тот вирус, который вы запустите, через некоторое время уже будет не совсем тем, который вы запустили: может произойти какая-то его гибридизация с каким-то очередным вирусом летучих мышей, и получится что-то третье. Никто не гарантирует, что ваш антидот, даже если мы его каким-то чудом создали, спасет вас от этого гибрида. Это как открыть ящик Пандоры и дальше играть в русскую рулетку.
М.Г.: Можем ли мы с уверенностью говорить, что этот штамм коронавируса появился в Ухане?
С.Е.: По данным, которые есть, создается впечатление, что действительно там он и появился. Не прослеживается ни одного случая заражения до того и не видно, откуда бы он мог быть завезен. Более того, когда анализировали геном вируса, то больше всего он похож на геном именно китайских летучих мышей, не каких-то других животных и не из другой страны. Из этого всего можно сделать вывод, что там он и появился.
М.Г.: Журнал Nature недавно опубликовал результаты исследования, согласно которому в коронавирусе не заметно следов модификации, что указывает на его естественное происхождение. Можно ли заметить подобные изменения?
С.Е.: Представьте, вы рассматриваете отфотошопленную картинку и пытаетесь доказать, что это фейк. Если смотреть попиксельно под микроскопом на эту картинку, то, если она сделана не очень хорошо, можно заметить вмешательство. Можно заметить ретушь, неправильно лежащие тени, смазанное и так далее. Примерно то же самое получается, когда есть генетические модификации. Сделать генетическую модификацию вируса так, чтобы не торчали уши того, что это искусственно сделано, достаточно сложно. Специалисты говорят, что это почти невозможно.
М.Г.: То есть если этот штамм был искусственно создан, то это было бы заметно, а раз нет доказательств этому и раз он так похож на вирус летучих мышей, значит он появился естественным образом. Правильно?
С.Е.: Да, с высокой вероятностью, это результат именно природного процесса. Есть такая максима: вы не можете доказать, что чего-то нет, не можете доказать, что это не сделано искусственно. Можно доказать только позитивное утверждение, а не негативное. Но, как я уже говорил, если это сделано искусственно, тому, кто это делал, – двойка, и вон из класса! Это сделано халтурно.
Компьютерный вирус — вредоносная программа, главной задачей которой может быть повреждение системы, на которой она установлена, перехват информации с компьютера и саморепликация — способность к размножению.
Классификация вирусов
Так как единой классификации вирусного ПО на данный момент не существует, их классифицируют условно по определенным критериям:
- Руткит (англ. rootkit) — вирус, предназначенный для сокрытия присутствия других вредоносных программ.
- Стелс-вирус (от англ. stealth virus — вирус-невидимка) — частично или полностью скрывающий свое присутствие в системе, таким образом затрудняя обнаружение антивирусной программой.
- Полиморфный вирус – вредоносная программа, с постоянно изменяющимся программным кодом.
- Microsoft Windows.
- Unix.
- Linux.
- DOS.
- Мобильные ОС.
- Загрузочный вирус — выполняет заражение Главной загрузочной записи (Master Boot Record, MBR) жесткого диска. Активируется вирус при загрузке (перезагрузке) операционной системы
- Скриптовый вирус — с помощью языков программирования добавляет себя к новым скриптам
- Файловый вирус — так называемый вирус-паразит, который при самокопировании изменяет содержимое исполняемых файлов
- Макровирус — вирус, использующий возможности макроязыков (чаще всего встраиваются в прикладные пакеты MS Word).
- Вирус, поражающий исходный код.
- Скриптовый язык.
- Ассемблер.
- Высокоуровневый язык.
- Другие языки программирования.
- Кейлоггер (от англ. key — клавиша и logger — регистрирующее устройство) — программа, выполняющая перехват и последующую отправку информации о набираемом на клавиатуре тексте.
- Шпион — вирус, собирающий данные о системе, активности программ на компьютере, посещенных сайтах и т.д.
- Бэкдор (от англ. back door — черный ход) — вирус, который после первичного доступа инсталлирует на компьютере взломщик для дальнейших подключений к системе.
- Ботнет (англ. botnet — от robot и network) — сеть компьютеров с запущенным автономным программным обеспечением — ботами. Задачей бота является подбор паролей, выполнение DDoS-атак и рассылка спама за счет ресурсов зараженного компьютера.
- Прочие разновидности.
Типы вирусов
В зависимости от способа заражения, функционала и целей, преследуемых злоумышленниками, вирусы можно разделить на следующие виды:
- Червь (Worm) — программа, которая самостоятельно создает копии самой себя, при этом не поражая другие приложения.
- Дроппер (Dropper) — исполняемый файл, который сам по себе вирусом не является, но устанавливает зловредное ПО в системе.
- Троян — вредоносная программа, проникающая в систему под видом безопасного приложения.
- Анти-антивирусный вирус (Anti-antivirus virus) — целью программы является нарушение работы антивирусного ПО, установленного на зараженном компьютере.
- Стелс-вирус (Stealth virus) — программа, частично или полностью маскирующаяся в системе с помощью специальных действий, например, перехвата обращений к ОС, направленных на получение информации о зараженных объектах.
- Модификация (modification) — измененный вариант одной и той же вирусной программы.
- Шифрованный вирус (Encrypted virus) — программа, которая самостоятельно шифрует свой исходный код, что затрудняет обнаружение в системе.
- Скрипт-вирус (Script virus) — программа, попадающая на компьютер под видом сообщения электронной почты, которое содержит в себе исполняемые файлы.
- Резидентный вирус — вирус, скрывающийся в оперативной памяти для заражения всех приложений и файлов, которые открываются либо копируются на компьютере.
Принцип работы
Механизм работы вирусной программы одинаков для всего ПО данного типа: при попадании в среду заражения, вирус внедряется в исполняемый код других программ. Чаще всего для проникновения могут использоваться уязвимости в популярных программах — почтовые клиенты, браузеры и т.д.
Среда обитания
Попасть в систему вирусное ПО может из различных источников:
Противодействие и профилактика
Основная статья: Антивирусная программа
На сегодняшний день самым действенным средством против вирусов являются антивирусные программы, позволяющие не только обнаружить и восстановить зараженные файлы, но и предотвратить их попадание на компьютер.
Полный текст:
Хронический гепатит В — тяжелое заболевание печени, связанное с персистенцией вируса гепатита В в гепатоцитах человека. Хронический гепатит В является одним из самых распространенных заболеваний в мире. По обновленной статистике, более 250 млн человек хронически инфицированы, и более 1 млн человек умирают ежегодно из-за последствий ХГВ, цирроза и гепатоцеллюлярной карциномы. Основная причина персистенции вируса гепатита В — особая суперспирализованная молекула кольцевой ковалентно замкнутой ДНК в ядре. Современные методы терапии подавляют вирусную инфекцию, но не действуют напрямую на матрицы кольцевой ковалентно замкнутой ДНК, поскольку она существует в ядре гепатоцитов в виде минихромосомы и является недоступной для действия противовирусных препаратов. Как правило, после прекращения курса терапии наступает реактивация инфекции, поэтому прием противовирусных препаратов может быть неопределенно долгим. Одной из современных технологий, способных действовать напрямую на кольцевую ковалентно замкнутую ДНК, является система сайт-специфических нуклеаз CRISPR/Cas9 организма Streptococcus pyogenes. SpCas9 белок можно привлекать к участку ккзДНК с помощью короткого РНК-проводника, в результате чего SpCas9 вносит двуцепочечные разрывы, разрушая или мутируя вирусный геном. Тем не менее на сегодняшний момент использование CRISPR/Cas9 для терапии хронического гепатита В сопряжено с рядом проблем, в том числе с такой, как внецелевое действие нуклеаз (разрезание генома клеток). В последние годы было заявлено о создании нескольких технологий, использование которых может усиливать нуклеолитическую активность CRISPR/Cas9 (модифицированные РНК-проводники) или увеличивать специфичность SpCas9 белка (eSpCas9, более безопасная форма классического белка Cas9). В этой работе было проведено сравнение противовирусного действия CRISPR/Cas9 с классической формой белка SpCas9 и белком eSpCas9 c модифицированными и немодифицированными РНК-проводниками на культуре клеток in vitro. Показано, что система SpCas9 подавляет транскрипцию и репликацию вируса гепатита В на 90%, а также снижает уровень ккзДНК на 94%, тогда как противовирусный эффект при использовании eSpCas9 оказывается существенно ниже. Несмотря на то что модифицированные РНК-проводники должны улучшать нуклеолитическую активность CRISPR/Cas9 систем, модификация РНК-проводников также значительно снижает противовирусное действие CRISPR/Cas9. Таким образом, CRISPR/Cas9 сама по себе обладает высокой эффективностью действия, почти полностью блокируя транскрипцию и репликацию вируса гепатита В. Использование описанных технологий по улучшению свойств CRISPR/Cas9 нерационально при создании методов терапии на основе CRISPR/Cas9, а для элиминации генома вируса следует сосредоточиться на поиске эффективных РНК-проводников.
Костюшева Анастасия Павловна, младший научный сотрудник лаборатории вирусных гепатитов
Адрес для переписки: Костюшева Анастасия Павловна, 111123, Россия, Москва, ул. Новогиреевская, 3А, ФБУН ЦНИИ эпидемиологии Роспотребнадзора. Тел.: 8 (925) 310-91-24.
1. Чуланов В.П., Зуева А.П., Костюшев Д.С., Брезгин С.А., Волчкова Е.В., Малеев В.В. Гепатит С стал излечим. Гепатит В следующий? //Терапевтический архив. 2017. Т. 89, № 11. С. 4–13. doi: 10.17116/terarkh201789114-13
2. Allweiss L., Dandri M. The role of cccDNA in HBV maintenance. Viruses, 2017, vol. 9, no. 2, p. 156. doi: 10.3390/v9060156
3. Chang T.T., Lai C.L., Kew Yoon S. Entecavir treatment for up to 5 years in patients with hepatitis B e antigen-positive chronic hepatitis B. Hepatology, 2010, vol. 51, no. 2, pp. 422–430. doi: 10.1002/hep.23327
4. Dang Y., Jia G., Choi J. Optimizing sgRNA structure to improve CRISPR-Cas9 knockout efficiency. Genome Biol., 2015, vol. 16, p. 280. doi: 10.1186/s13059-015-0846-3
5. Dong C., Qu L., Wang H., Wei L., Dong Y., Xiong S. Targeting hepatitis B virus cccDNA by CRISPR/Cas9 nuclease efficiently inhibits viral replication. Antiviral Res., 2015, vol. 118, pp. 110–117. doi: 10.1016/j.antiviral.2015.03.015
6. Fu Y., Sander J.D., Reyon D., Cascio V.M., Joung J.K. Improving CRISPR-Cas nuclease specificity using truncated guide RNAs. Nat. Biotechnol., 2014, vol. 32, no. 3, pp. 279–284. doi: 10.1038/nbt.2808
7. Ganem D., Prince A.M. Hepatitis B virus infection — natural history and clinical consequences. N. Engl. J. Med., 2004, vol. 350, no. 11, pp. 1118–1129. doi: 10.1056/NEJMra031087
8. Janssen H.L.A., Zonneveld M., Senturk H. Pegylated interferon alfa-2b alone or in combination with lamivudine for HBeAgpositive chronic hepatitis B: a randomised trial. Lancet, 2005, vol. 365, no. 9454, pp. 123–129. doi: 10.1016/S0140-6736(05)17701-0
9. Karimova M., Beschorner N., Dammermann W. CRISPR/Cas9 nickase-mediated disruption of hepatitis B virus open reading frame S and X. Sci. Rep., 2015, vol. 5, p. 13734. doi: 10.1038/srep13734
10. Lim S.G., Wai C.T., Rajnakova A., Kajiji T., Guan R. Fatal hepatitis B reactivation following discontinuation of nucleoside analogues for chronic hepatitis B. Gut, 2015, vol. 51, no. 4, pp. 597–599. doi:10.1136/gut.51.4.597
11. Lin S.R., Yang H.C., Kuo Y.T. The CRISPR/Cas9 system facilitates clearance of the intrahepatic HBV templates in vivo. Mol. Ther. Nucleic Acids, 2014, vol. 3: e186. doi: 10.1038/mtna.2014.38
12. Nassal M. HBV cccDNA: viral persistence reservoir and key obstacle for a cure of chronic hepatitis B. Gut, 2015, vol. 64, iss. 12, pp. 1972–1984. doi: 10.1136/gutjnl-2015-309809
13. Ramanan V., Shlomai A., Cox D.B.T. CRISPR/Cas9 cleavage of viral DNA efficiently suppresses hepatitis B virus. Sci. Rep., 2015, vol. 5, p. 10833. doi: 10.1038/srep10833
14. Seeger C., Mason W.S. Hepatitis B virus biology. Microbiol. Mol. Biol. Rev., 2000, vol. 64, no. 1, pp. 51–68. doi: 10.1128/MMBR.64.1.51-68.2000
15. Seeger C., Sohn J.A. Complete spectrum of CRISPR/Cas9-induced mutations on HBV cccDNA. Mol. Ther., 2016, vol. 24, no.7, pp. 1258–1266. doi: 10.1038/mt.2016.94
16. Seeger C., Sohn J.A. Targeting hepatitis B virus with CRISPR/Cas9. Mol. Ther. Nucleic Acids, 2014, vol. 3: e216. doi: 10.1038/mtna.2014.68
17. Slaymaker I.M., Gao L., Zetsche B., Scott D.A., Yan W.X., Zhang F. Rationally engineered Cas9 nucleases with improved specificity. Science, 2016, vol. 351, no. 6268, pp. 84–88. doi: 10.1126/science.aad5227
18. WHO. Global hepatitis report 2017. World Health Organization, 2017.
19. Yang H.C., Kao J.H. Persistence of hepatitis B virus covalently closed circular DNA in hepatocytes: molecular mechanisms and clinical significance. Emerg. Microbes Infect., 2014, vol. 3, no. 9: e64. doi: 10.1038/emi.2014.64
20. Yin H., Xue W., Chen S. Genome editing with Cas9 in adult mice corrects a disease mutation and phenotype. Nat. Biotechnol., 2014, vol. 32, no. 6, pp. 551–553. doi: 10.1038/nbt.2884
21. Zhang X.H., Tee L.Y., Wang X.G., Huang Q.S., Yang S.H. Off-target effects in CRISPR/Cas9-mediated genome engineering. Mol. Ther. Nucleic Acids, 2015, vol. 4: e264. doi: 10.1038/mtna.2015.37
22. Zhu W., Xie K., Xu Y. CRISPR/Cas9 produces anti-hepatitis B virus effect in hepatoma cells and transgenic mouse. Virus Res., 2016, vol. 217, pp. 125–132. doi: 10.1016/j.virusres.2016.04.003

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
Читайте также:


