Вильпрафен при кишечной палочке в моче
В прессе все чаще говорят о скором кошмарном будущем, где можно будет погибнуть от безобидного пореза: все лекарства окажутся бессильны против даже самой простой инфекции. Апокалиптические сценарии еще далеки от реальности, но проблема антибиотикорезистентности – устойчивости бактерий к лекарствам – с каждым годом становится все острее.
На прошедшей неделе в Давосе британский министр здравоохранения Мэтт Хэнкок призвал "предотвратить ужасное будущее", в котором люди окажутся беззащитны перед бактериями с множественной лекарственной устойчивостью (их иногда называют "супербактериями" или "супермикробами").
Представляя свой план борьбы, Хэнкок сравнил масштаб проблемы антибиотикорезистентности с войнами и изменением климата. Похожими формулировками оперирует Всемирная организация здравоохранения (ВОЗ) и специалисты по всему миру.
Настоящее Время разобралось для вас в антибиотиках и супербактериях.
Насколько все плохо?
Ситуация пока не критическая, но очень серьезная. Бактерии научились противостоять даже самым сильным и редко применяемым лекарствам ("антибиотикам резерва", таким, как колистин), при этом с 1980-х годов принципиально новых антибиотиков практически не появлялось. Исследования идут, но они слишком долгие и дорогие – а бактерии вырабатывают неуязвимость против антибиотиков куда быстрее. Дело осложняется и простотой путешествий: супербактерии получают возможность легко распространяться по всему миру.
Авторы британского исследования антибиотикорезистентности (2016 год) оценивали, что количество смертей от таких супербактерий в мире может вырасти примерно с 700 тысяч в год до 10 млн ежегодно к 2050 году – это больше, чем число жертв онкозаболеваний (на момент публикации). Потери ВВП при таком сценарии достигнут 100 триллионов долларов.
Пока не существует систем, позволяющих полноценно отслеживать мировую ситуацию с антибиотикорезистентностью в мировом масштабе. Проект ВОЗ под названием GLASS стартовал в 2015 году и по состоянию на конец 2018 года включал в себя лишь 71 страну. В последний отчет (опубликован в январе 2019 года) вошли данные об антибиотикорезистентности всего из 49 стран, при этом их качество пока не позволяет сравнивать между собой ситуацию в различных государствах и регионах.
В региональных отчетах также не много поводов для оптимизма. Страны Евросоюза за восемь лет (2007-2015) зафиксировали более чем двукратный рост числа погибших от инфекций, вызванных неуязвимыми для антибиотиков микробами, говорится в недавнем исследовании. По количеству потерянных лет здоровой жизни в пересчете на 100 тысяч населения (170) подобные инфекции практически сравнялись с суммарным эффектом ВИЧ, гриппа и туберкулеза (183). Более всего таким инфекциям в ЕС подвержены дети до года и люди старше 65 лет.
Хотя в еще одной свежей публикации крупный госпиталь Марселя показал, что за 15 лет (2001-2016) у них ситуация с резистентностью к антибиотикам не ухудшилась. К тому же, судя по мировой прессе, пока неуязвимые к абсолютно всем антибиотикам инфекции все же не носят массовый характер: громче всего обсуждали отчет двухлетней давности о 70-летней американке, погибшей от неуязвимой для всех антибиотиков бактерии (ее она скорее всего подхватила в Индии, где попала в больницу с переломом).
Какие именно организмы называют супербактериями?
Супербактерии (супермикробы) – это микроорганизмы, обладающие устойчивостью сразу к нескольким антибиотикам. Иногда – ко всем существующим.
В 2017 году ВОЗ опубликовала список из 12 бактерий, для борьбы с которыми срочно нужны новые антибиотики. Критически важны лекарства, способные справиться с устойчивыми к карбапенему энтеробактериями (например, кишечной палочкой E.Coli), синегнойной палочкой (Pseudomonas aeruginosa) и ацинетобактером (Acinetobacter baumannii). Чаще всего именно эти возбудители вызывают так называемые "внутрибольничные инфекции", с которыми врачам особенно сложно бороться из-за множественной устойчивости бактерий и ухудшенного состояния больных.
Также в список ВОЗ попали ванкомицин-резистентные энтерококки (Enterococcus faecium), невосприимчивый к метициллину и ванкомицину золотистый стафилококк (methicillin-resistant staphylococcus aureus, MRSA), цефалоспорин- и фторхинолон-резистентный гонококк, кларитромицин-резистентный хеликобактер и другие бактерии. Они вызывают серьезные болезни: заражение крови, менингит, пневмонию, инфекции мочевыводящих путей и гонорею.
Часто в материалах об антибиотиках фигурируют понятия “грамположительные бактерии” и “грамотрицательные бактерии”. Последние (например, кишечная палочка) обладают двумя клеточными мембранами: с ними сложнее бороться, и эффективных против них антибиотиков в мире меньше.
Как действуют антибиотики и появляется резистентность?
Антибиотики или "противомикробные препараты" – особые вещества, останавливающие рост клеток бактерий или уничтожающие их. Для этого существуют несколько механизмов: как правило антибиотики атакуют клеточную стенку, мешают синтезу белка или ДНК бактерий.
Резистентность к антибиотикам обнаружили вскоре после их появления. Первый в мире антибиотик – перевернувший медицину ХХ века пенициллин – Александр Флеминг открыл в 1928 году, но массово применять его начали лишь в 1942-м. Еще до этого, в 1940-м стало известно об устойчивой к пенициллину кишечной палочке.
Бактерии постоянно меняются, чтобы стать невосприимчивыми к действию антибиотиков: "выгодные" мутации передаются бактериями друг другу. Микробы приспосабливаются к антибиотикам даже в огромной концентрации крайне быстро. Посмотрите на видео, как всего за 11 дней кишечная палочка адаптируется к тысячекратной дозе (в центре) антибиотика:
Главными "инкубаторами" супербактерий оказываются больницы: там, где постоянно применяются мощные антибиотики, растут популяции невосприимчивых к ним микробов. Способствует развитию устойчивости бактерий и сельское хозяйство: там антибиотики широко применяют для профилактики болезней и ускорения роста животных.
Смертельна ли встреча с супербактерией?
Для здорового человека с нормальным иммунитетом – нет. Но чаще всего такие микробы встречаются в больницах, куда попадают люди, уже ослабленные той или иной болезнью. Для пациентов (например, находящихся на искусственной вентиляции легких) встреча с супербактериями может запросто стать фатальной.
Сейчас без антибиотиков невозможны сложные хирургические операции, трансплантации и борьба с раком посредством химиотерапии. Последняя обычно значительно подавляет иммунитет: для таких больных даже самая обычная инфекция может стать смертельной, не говоря уже о вызванной супермикробами.
При этом с инфекциями от мультирезистентных бактерий, пока на них действуют хоть какие-то антибиотики, можно жить, пусть даже это и будет сопряжено со страданиями.
Эмили Моррис рассказала, что супербактерию в ее мочевом пузыре обнаружили в подростковом возрасте и с тех пор ей пришлось перепробовать множество антибиотиков, в том числе "препараты резерва", вроде карбапенема.
Во время беременности она была вынуждена принимать антибиотик, не проверявшийся на беременных, ее новорожденному ребенку пришлось сразу пройти курс терапии антибиотиками. "Это было очень страшно", – рассказывала 24-летняя Моррис журналу New Scientist в 2017 году.
32-летняя Кэтрин Уильямс уже более 10 лет постоянно принимает антибиотики из-за болезни мочевыводящих путей, вызванной супербактериями.
"Каждый раз, когда заканчивается курс приема антибиотиков, болезнь возвращается, – говорила она в интервью BBC. – Боль просто приковывает тебя к постели до следующего курса приема антибиотиков. То, что мне придется принимать антибиотики всю жизнь, меня очень пугает".
Что в России и других постсоветских странах?
В России и других постсоветских странах – например, Украине, Казахстане, Беларуси – антибиотики долго продавались без рецепта. Это вело к злоупотреблениям и самолечению, а в итоге – способствовало развитию резистентности у бактерий.
В октябре 2017 года в России приняли "Стратегию предупреждения распространения антимикробной резистентности". Документ, подписанный главой правительства Дмитрием Медведевым, предусматривает два главных этапа:
- До 2020 года население будут информировать о правильном использовании антибиотиков, работать над лучшим выявлением резистентности и определении базовых показателей, как оценивать ее распространенность.
- На втором этапе (до 2030 года) планируется снизить число случаев болезней, связанных с супербактериями.
Почему так долго не появляются новые антибиотики?
За последние десятилетия арсенал медиков практически не пополнялся антибиотиками принципиально новых классов. Причин тому несколько.
Разработка таких лекарств – это сложное и затратное занятие, обходящееся в сотни миллионов или миллиарды долларов. Для фармакологических компаний оно не всегда интересно с коммерческой точки зрения: курсы антибиотиков обычно краткосрочны, в отличие от лекарств для хронических заболеваний (антиретровирусная терапия, например, людям с ВИЧ необходима всю жизнь). К тому же из-за быстрого возникновения резистентности растет риск обесценивания инвестиций в разработку новых препаратов.
Тем не менее, в последнее время вошли в обиход мощные антибиотики, полученные на базе старых открытий – в первую очередь, Линезолид (Зивокс). Да и представители существующих классов все время совершенствуются и нередко могут усиливать эффект при совместном использовании.
Что делать?
ВОЗ рекомендует использовать антибиотики только по назначению врача (а врачам – их разумно назначать) и всегда полностью проходить курс лечения, а не останавливать прием антибиотиков сразу после улучшения самочувствия.
Также рекомендуется не хранить, не использовать заново и не передавать другим оставшиеся дозы лекарства.
Важно не пытаться лечить вирусные заболевания антибиотиками, вакцинироваться, укреплять собственный иммунитет и тщательно соблюдать правила гигиены, рекомендует ВОЗ.
Также есть смысл по возможности избегать больниц в регионах, где санитарная ситуация далека от идеальной. В первую очередь – в Азии и Африке. По данным британского отчета, там к 2050 году будет больше всего погибших от инфекций супербактериями.
Если у вас или у близких есть подозрение на такую инфекцию, добейтесь консультации специалиста по инфекционным болезням. Недавнее исследование показало, что это может на 50% снизить смертность от инфекций, вызванных бактериями с множественной лекарственной устойчивостью.
Чего ждать в будущем?
Проблемой невосприимчивости к антибиотикам годами занимаются ученые и специалисты в области охраны общественного здоровья, и поводы для оптимизма есть.
ВОЗ в 2015 году одобрила глобальный план по борьбе с устойчивостью к противомикробным препаратам. Различные страны – в том числе США, Россия и совсем недавно Великобритания – принимают собственные комплексы мер по борьбе с устойчивостью бактерий к антибиотикам. Обычно они включают информирование пациентов и врачей о разумном использовании препаратов, ограничения на применение антибиотиков в сельском хозяйстве и содействие разработкам новых классов антибиотиков.
Несмотря на все сложности, такие разработки уже идут и появляются отдельные многообещающие результаты. Например, теиксобактин – принципиально новый антибиотик, открытый в 2015 году группой ученых из США, Германии и Великобритании.
В конце 2017 года его научились эффективно синтезировать, а в 2018-м действие синтетического теиксобактина успешно проверили на мышах. Но до появления лекарства для людей еще далеко: по оценкам ученых, 6-10 лет.
Оно может и вовсе не появиться: например, многообещающий платенсимицин, представленный в 2006 году, так и не добрался до полноценных клинических тестов из-за его неэффективности при введении стандартными методами. Однако исследования принципов работы платенсимицина позволяют надеяться на появление новых, более эффективных разработок.
В начале 2018 года ученые Рокфеллеровского университета в США представили еще один принципиально новый класс антибиотиков – малацидины, но до появления лекарств на их основе понадобится еще больше времени.
Рассматриваются и другие варианты терапии против супербактерий: целенаправленное усиление иммунитета, антимикробные пептиды, синтетические вещества, позаимствованные у вирусов, добавление особых элементов к уже существующим антибиотикам для повышения эффективности и другие способы. Однако все они пока находятся на разных стадиях готовности и для массового клинического использования не одобрены.
МОСКВА, 7 мая — РИА Новости, Альфия Еникеева. Супербактерии, устойчивые к антибиотикам, — одна из главных проблем современной медицины. Возбудители гонореи, стафилококка, пневмококка мутировали, и теперь непонятно, как с ними бороться. Согласно прогнозам, особо стойкие инфекции угрожают миллионам жизней, поэтому перед наукой поставлена задача — разработать более мощные средства борьбы, а также альтернативу антибиотикам.

Обычная бактерия кишечной палочки Escherichia coli всего за 11 дней приспособилась к тысячекратной дозе антибиотиков. Видео, снятое в ходе эксперимента учеными Гарвардской медицинской школы, показывает, как постепенное увеличение концентрации препарата превращает ее в супермикроб, неуязвимый для любых лекарств.
Вырабатывать антибиотики и уметь им сопротивляться — естественная стратегия выживания в мире бактерий. Но в природе стойкие к антибиотикам штаммы оказывались в проигрыше, поскольку размножались медленнее "диких" бактерий.
В начале XX века Александр Флеминг открыл антибактериальные свойства пенициллина, и с 1950-х годов антибиотики производятся в промышленных масштабах для медицины и животноводства. Так люди неожиданно помогли мутировавшим штаммам микробов победить в эволюционной борьбе и подставили себя под удар. В 2017 году Всемирная организация здравоохранения (ВОЗ) объявила о наступлении "постантибиотиковой эры" и обнародовала список особо стойких инфекций.
Откуда берутся супербактерии
Антибиотики действуют на наименее устойчивые бактерии, а вот мутировавшие держатся до последнего. И если с ними не бороться, они передают ген устойчивости при размножении. Кроме того, бактерии обмениваются мутациями.
Такой супермикроб вырабатывает ферменты, разлагающие антибиотик. Его клеточная мембрана, по которой раньше лекарства наносили сокрушительный удар, теперь неуязвима. Некоторые супербактерии умеют обманывать антибиотики, выстраивая вокруг себя слой белков, мимикрирующих под рибосомы — внутриклеточные белковые фабрики. Препарат их уничтожает, настоящие же рибосомы продолжают функционировать, а бактерия — жить.
Три смертельно опасных мутанта
Из-за быстрой приспособляемости к антибиотикам супербактерии опаснее для человечества, чем климатические изменения или загрязнение окружающей среды. Уже сегодня, по данным ВОЗ, в мире от заболеваний, вызванных этими микробами, умирает примерно 800 тысяч человек в год. А к 2050-му, по прогнозам специалистов, суперинфекции ежегодно будут уносить до десяти миллионов жизней.
Три супербактерии признаны ВОЗ критически опасными для человека — они показали резистентность практически ко всем антибиотикам, даже к так называемым препаратам последнего резерва, колистину и бета-лактамным антибиотикам широкого спектра. Это акинетобактерия Баумана, приводящая к пневмонии и инфекциям крови, синегнойная палочка, вызывающая кожную сыпь, ушные инфекции у здоровых людей, серьезные кровяные инфекции, пневмонии у пациентов в больницах, а также энтеробактерии, населяющие кишечник человека, в частности сальмонелла и кишечная палочка.
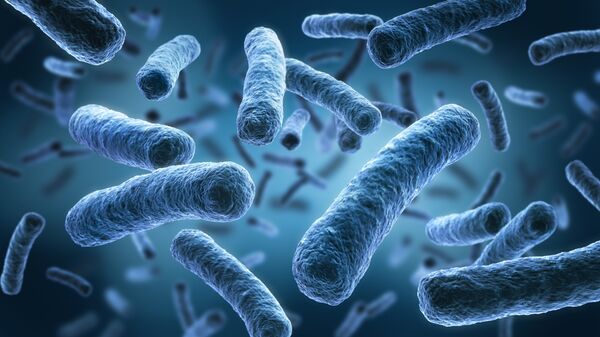
Сильно опасными ВОЗ считает более распространенные золотистый стафилококк (Staphylococcus aureus), пневмококк (Klebsiella pneumoniae) и гонококк (Neisseria gonorrhoeae), вызывающий гонорею. Кстати, первый случай супергонореи, от которой не помогают антибиотики, недавно зафиксировали в Великобритании. Пациент, чье имя не раскрывают, заразился инфекцией после полового контакта с жительницей Юго-Восточной Азии.
Ученые также опасаются супербактерии туберкулеза, поскольку почти половина штаммов этого патогена устойчива к изониазиду и другим средствам противотуберкулезной терапии. Шестнадцать процентов штаммов не поддаются воздействию ни одного из имеющихся антибиотиков. Такие суперустойчивые туберкулезные палочки выявлены в Индии и Ираке.
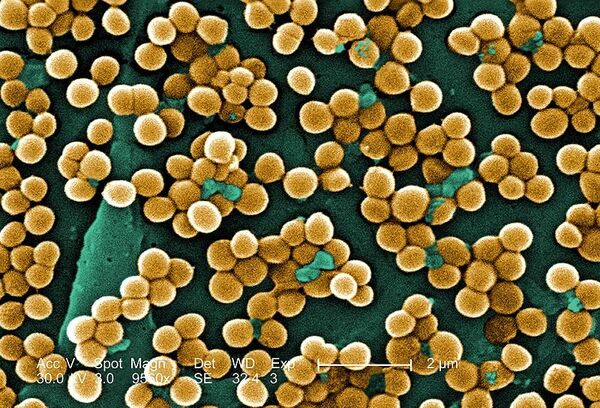
Суперантибиотики против супербактерий
Для борьбы с супербактериями ученые создают новые антибиотики либо модифицируют существующие под генетические изменения в конкретных микроорганизмах. Именно этот путь выбрали исследователи МГУ, разработавшие принципиально новый гибридный антибиотик — митохондриально направленный антиоксидант, воздействующий на мембранный потенциал, который обеспечивает бактериальные клетки энергией.
Другой перспективный препарат создан на основе теиксобактина — антибиотика, открытого в 2015 году в образцах почвы. Совсем недавно ученые успешно применили его синтетическую форму для лечения бактериальной инфекции у лабораторных мышей. Предполагается, что это лекарство поможет в борьбе с метициллин-резистентным стафилококком и энтерококком, устойчивым к ванкомицину.
Помимо антибиотиков, ученые разрабатывают и совершенно новые классы препаратов. Так, исследователи из российско-американской лаборатории биомедицинской химии ИХБФМ СО РАН создали аналоги нуклеиновых кислот — фосфорилгуанидины, умеющие проникать в клетку и вступать во взаимодействие с ДНК и РНК, уничтожая бактерию. Ученые отмечают, что в будущем такие вещества можно будет создавать под каждый конкретный патоген на основе анализа его генома.
Еще один точечный метод — бактериофаги, то есть вирусы, поражающие бактериальные клетки. Совсем недавно команда ученых из ИБХ РАН, ИТЭБ РАН и ИБФМ имени Г. К. Скрябина РАН научила фермент бактериофага Т5 разрушать клеточные стенки бактерии кишечной палочки даже с утолщенной из-за мутаций мембраной. Кроме того, исследователи выяснили, что фермент эффективнее уничтожает бактерии, когда ему помогает агент (например, хлоргексидин в очень низких концентрациях).
Эксперты все же считают, что с супербактериями лучше бороться с помощью антибиотиков. Но необходимо ограничивать их свободную продажу в аптеках и применение в сельском хозяйстве — иначе даже новые высокоэффективные препараты не помогут.
В январе 2019 года Колумбийский университет сообщил о том, что четыре пациента, находящиеся в его Медицинском центре Ирвинга (Irving Medical Center) в Нью-Йорке, страдают от необычного вида кишечной палочки (E. coli). Хотя эта новость в основном прошла незамеченной для средств массовой информации, она привлекла к себе внимание экспертов в области инфекционных заболеваний. Кишечная палочка — довольно распространенная бактерия и неопасная, если находится в желудке, где обычно и живет, однако может стать смертельно опасной в неправильных местах, — например, в салат-латуке, в говяжьем фарше или в нашей кровеносной системе. В том случае, когда антибиотики оказываются беспомощными в борьбе против кишечной палочки, половина пациентов умирают в течение двух недель.
Вот почему сообщение Колумбийского университета о кишечной палочке вызвало такую тревогу. Для некоторых зараженных пациентов последняя надежда связана с антибиотиком колистином (colistin), токсичной субстанцией, способной вызывать побочные эффекты и наносить ущерб почкам и головному мозгу. Та кишечная палочка, о которой сообщили сотрудники Колумбийского университета, имела мутацию в гене MCR-1, придающую ей ужасное свойство — невосприимчивость к колистину.
С того момента, когда в 1942 году чудесный экспериментальный препарат под названием пенициллин был в срочном порядке доставлен в Бостонскую больницу, где он спас жизни 13 пострадавшим в перестрелке в ночном клубе, ученые-медики обнаружили более 100 новых антибиотиков. Все они очень нам нужны, однако их уже недостаточно. И причина не только в кишечной палочке. Существуют также виды стафилококов (Staphylococcus), энтеробактерий (Enterobacteriaceae) и клостридиум диффициле (Clostridium difficile), которые успешно противодействуют антибиотикам. В одном исследовании говорится о том, что количество смертей, вызванных устойчивыми к применению антибиотиков заболеваниями, выросло в четыре раза в период с 2007 года по 2015 год. Недавно в больницах Нью-Йорка и Чикаго была обнаружена устойчивая, резистентная версия грибка Кандида аурис (Candida auris), который стал причиной смерти половины зараженных пациентов.
Эксперты в области медицины связывают надежды с совершенно новыми стратегиями лечения инфекционных заболеваний. Новые способы уничтожения бактерий они ищут в экзотических местах — в вирусах, рыбьей слизи и даже на других планетах. Они используют наработки в геномике, а также в других областях и предлагают новые технологии для ликвидации бактерий и ограничения их распространения. Кроме того, они подвергают дополнительному исследованию методы лечения в больницах, а также в других местах распространения бактерий, используют более целостные стратегии для борьбы с бактериями в наших телах, а также в наших больницах и кабинетах врачей.
Альтернативные варианты кажутся перспективными, однако до их реализации еще далеко. Пока не ясно, сможем ли мы изобрести какие-нибудь новые средства, прежде чем супербактерии, как армия зомби у ворот, уничтожат наши оборонительные укрепления.
Новые охотники за микробами

Управление бактериями
Хотя антибиотики, на самом деле, являются чудодейственным препаратами, наши нынешние проблемы частично возникли как раз из-за того, что медицина сделала на них слишком большую ставку. Врачи назначают их применение при ушной инфекции, при боли в горле, а также при заражении мочевого пути. Хирурги используют их для предотвращения постоперационных инфекций. Бактерии способны вырабатывать устойчивость, а применение антибиотиков имеет смысл как часть целостного подхода для контроля над процессом распространения бактерий и для лечения инфекций. Антибиотики постепенно начитают терять свою эффективность, и поэтому эксперты в области медицины подчеркивают необходимость использования комплексных стратегий для того, чтобы держать бактерии под контролем.
Больницы начинают менять практику. Многие теперь используют роботов в форме мусорных контейнеров для дезинфекции стен с помощью ультрафиолетового света (палаты в это время должны быть пустыми, поскольку подобный свет вреден и для человека). В Медицинском центре Риверсайд (At Riverside Medical Center), расположенном к югу от Чикаго, два робота, изготовленные компанией Xenex, дезинфицирует более 30 палат в день.
Селим и его коллеги пытаются найти способы настройки цвета лазера для воздействия на определенные резистентные бактерии. Если его работа увенчается успехом, то работники системы здравоохранения смогут использовать лазеры не крупнее обычного фонаря для безопасного уничтожения вредоносных бактерий на коже пациента, а также проводить дезинфекцию кабинетов врачей. Этим лучом можно будет также обрабатывать кожу и одежду самих работников системы здравоохранения для того, чтобы они не могли распространять инфекцию. Его коллеги в настоящее время готовятся к проведению клинических испытаний.
Замедлить развитие супербактерий
Хотя фармацевтическая промышленность почти отказалась от производства антибиотиков, исследователи еще надеются найти их новые виды. Революция в области антибиотиков началась в 1928 году, когда Александр Флеминг вернулся из отпуска в свою лондонскую лабораторию и обнаружил странного вида плесень, образовавшуюся в оставленной им у окна кювете. С тех пор исследователи пытаются обследовать каждый уголок природы в надежде найти новые бактерии-убийцы. Согласно последним данным, среди новых субстанций, которые могут оказаться смертельными для резистентных бактерий, — но и безопасными для человека, — можно назвать насекомых, водоросли, слизь молодых рыб, богатая мышьяком грязь в Ирландии и даже марсианская почва. Одна группа исследователей из Лейденского университета в Голландии пытается создать искусственную бактерию в надежде, что на ее основе можно будет получить новый антибиотик.
Кроме того, врачи пытаются максимально использовать уже имеющиеся антибиотики за счет замедления процесса появления новых резистентных видов. Для этого нужно сократить чрезмерное использование антибиотиков, в результате которого супербактерии получают стимулы для эволюционного развития. Подобные действия должны стать международными, поскольку резистентные бактерии из одной части мира часто перемещаются в другую.
Материалы ИноСМИ содержат оценки исключительно зарубежных СМИ и не отражают позицию редакции ИноСМИ.
Доступность: Есть в наличии
- Доставка Курьером
- Самовывоз
- Доставка Новой почтой
- Доставка УкрПочтой
- Оплата и доставка
- Киев
- Одесса
- Харьков
- Днепр
- Львов
- Ивано-Франковск
- Винница
- Запорожье
- Кременчуг
- Кривой Рог
- Тернополь


- Производитель: Astellas Pharma Europe (Нидерланды)
- Форма товара: Таблетки
- Температура хранения: не выше +25°С
- Регистрационное удостоверение: UA/4350/01/01
Выберите позиции для добавления в корзину покупок или выбрать все
Антибиотик широкого спектра действия Вильпрафен благодаря активному действующему веществу - джозамицину, справляется со многими штампами, которые выработали устойчивость к другим схожим препаратам. Простая лекарственная форма, доступность и цена на Вильпрафен сделали его популярным антибиотиком для лечения воспалительных инфекционных заболеваний.
Вильпрафен (Wilprafen) инструкция по применению
Антибиотик группы макролидов. Оказывает бактериостатическое действие, обусловленное ингибированием синтеза белка бактериями. При создании в очаге воспаления высоких концентраций оказывает бактерицидное действие.
Высокоактивен в отношении внутриклеточных микроорганизмов: Chlamydia trachomatis и Chlamydia pneumonuae, Mycoplasma pneumoniae, Mycoplasma hominis, Ureaplasma urealyticum, Legionella pneumophila; в отношении грамположительных аэробных бактерий: Staphylococcus aureus, Streptococcus pyogenes и Streptococcus pneumoniae (pneumococcus), Corynebacterium diphtheriae; грамотрицательных аэробных бактерий: Neisseria meningitidis, Neisseria gonorrhoeae, Haemophilus influenzae, Bordetella pertussis; в отношении некоторых анаэробных бактерий: Peptococcus, Peptostreptococcus, Clostridium perfringens.
Препарат также активен в отношении Treponema pallidum.
Фармакокинетика.
Всасывание:
После приема внутрь джозамицин быстро абсорбируется из ЖКТ. Сmax достигается через 1-2 ч после приема. Через 45 мин после приема дозы 1 г средняя концентрация джозамицина в плазме составляет 2.41 мг/л.
Распределение:
Связывание с белками плазмы не превышает 15%.
Прием препарата с интервалом в 12 ч обеспечивает сохранение эффективной концентрации джозамицина в тканях в течение суток. Равновесное состояние достигается через 2-4 дня регулярного приема.
Джозамицин хорошо проникает через биологические мембраны и накапливается в различных тканях: в легочной, лимфатической ткани небных миндалин, органов мочевыделительной системы, коже и мягких тканях. Особенно высокие концентрации определяются в легких, миндалинах, слюне, поте и слезной жидкости. Концентрация джозамицина в полиморфонуклеарных лейкоцитах человека, моноцитах и альвеолярных макрофагах приблизительно в 20 раз выше, чем в других клетках организма.
Метаболизм:
Джозамицин биотрансформируется в печени до менее активных метаболитов.
Выведение
Выводится главным образом с желчью, выведение с мочой составляет менее 20%.
Показания к применению:
Лечение инфекционно-воспалительных заболеваний, вызванных чувствительными к препарату микроорганизмами:
инфекции верхних отделов дыхательных путей и ЛОР-органов (в т.ч. фарингит, тонзиллит, паратонзиллит, средний отит, синусит, ларингит);
дифтерия (дополнительно к лечению дифтерийным антитоксином);
скарлатина (при повышенной чувствительности к пенициллину);
инфекции нижних отделов дыхательных путей (в т.ч. острый бронхит, бронхопневмония, пневмония, включая атипичную форму, коклюш, пситтакоз);
инфекции полости рта (в т.ч. гингивит и болезни пародонта);
инфекции кожи и мягких тканей (в т.ч. пиодермия, фурункулы, сибирская язва, рожистое воспаление /при повышенной чувствительности к пенициллину/, угри, лимфангит, лимфаденит);
инфекции мочевыводящих путей и половых органов (в т.ч. уретрит, простатит, гонорея; при повышенной чувствительности к пенициллину - сифилис, венерическая лимфогранулема);
хламидийные, микоплазменные (в том числе уреаплазменные) и смешанные инфекции мочевыводящих путей и половых органов.
Рекомендуемая доза для взрослых и подростков старше 14 лет составляет 1-2 г в 2-3 приема. Начальная рекомендуемая доза составляет 1 г.
Для лечения урогенитального хламидиоза - по 500 мг 2 раза/сут в течение 12-14 дней.
Для лечения розацеа - по 500 мг 2 раза/сут в течение 10-15 дней.
Для лечения пиодермии - по 500 мг 2 раза/сут в течение 10 дней.
Для лечения хронического пародонтита, при абсцедировании пародонтальной кости - по 500 мг 2 раза/сут в течение 12-14 дней.
При обыкновенных и шаровидных (конглобатных) угрях назначают по 500 мг 2 раза/сут в течение первых 2-4 недель, далее - 500 мг 1 раз/сут в качестве поддерживающей терапии в течение 8 недель.
Таблетки следует проглатывать, не разжевывая, с небольшим количеством жидкости, между приемами пищи.
Обычно продолжительность лечения определяет врач. В соответствии с рекомендациями ВОЗ по применению антибиотиков длительность лечения стрептококковых инфекций должна составлять не менее 10 дней.
Грудным детям и детям в возрасте до 14 лет предпочтительно назначать препарат в виде суспензии. Суточная доза составляет 30-50 мг/кг массы тела, разделенная на 3 приема. У новорожденных и детей в возрасте до 3 мес дозу следует подбирать в соответствии с точной массой тела ребенка.
Перед употреблением флакон с суспензией необходимо встряхивать.
Со стороны пищеварительной системы: редко - отсутствие аппетита, тошнота, изжога, рвота, дисбактериоз, диарея; в отдельных случаях - повышение активности печеночных трансаминаз, нарушение оттока желчи и желтуха.
Аллергические реакции: в единичных случаях - крапивница.
Со стороны органа слуха: редко - дозозависимые преходящие нарушения слуха.
Прочие: в отдельных случаях - кандидоз.
- Гиперчувствительность к антибиотикам макролидам.
- Тяжелые нарушения функции печени
Беременность и лактация:
Разрешено применение при беременности и в период грудного вскармливания после оценки соотношения риска и преимуществ лечения.
Вильпрафен с другими антибиотиками:
Так как бактериостатические антибиотики могут снижать бактерицидный эффект других антибиотиков, таких как пенициллины и цефалоспорины, следует избегать совместного назначения джозамицина с данными видами антибиотиков. Джозамицин не следует назначать совместно с линкомицином, так как возможно обоюдное снижение их эффективности.
Вильпрафен с ксантинами:
Некоторые представители антибиотиков макролидов замедляют элиминацию ксантинов (теофиллина), что может привести к возможной интоксикации. Клинико-экспериментальные исследования указывают на то, что джозамицин оказывает меньшее влияние на выделение теофиллина, чем другие антибиотики макролиды.
Вильпрафен с антигистаминными препаратами:
После совместного назначения джозамицина и антигистаминных препаратов, содержащих терфенадин или астемизол, может отмечаться замедление выведения терфенадина и астемизола, что в свою очередь может приводить к развитию угрожающих жизни сердечных аритмий.
Вильпрафен с алкалоидами спорыньи:
Имеются индивидуальные сообщения об усилении вазоконстрикции после совместного назначения алкалоидов спорыньи и антибиотиков макролидов. Отмечен один случай отсутствия у пациента толерантности к эрготамину при приеме джозамицина. Поэтому сопутствующее применение джозамицина и эрготамина должно сопровождаться соответствующим контролем больных.
Вильпрафен с циклоспорином:
Совместное назначение джозамицина и циклоспорина может вызывать повышение уровня циклоспорина в плазме крови и создание нефротоксической концентрации циклоспорина в крови. Следует регулярно контролировать концентрацию циклоспорина в плазме.
Вильпрафен с дигоксином:
При совместном назначении джозамицина и дигоксина возможно повышение уровня последнего в плазме крови.
Вильпрафен с гормональными контрацептивами:
В редких случаях противозачаточный эффект гормональных контрацептивов может быть недостаточным во время лечения макролидами. В этом случае рекомендуется дополнительно использовать негормональные средства контрацепции.
Передозировка.
До настоящего времени нет данных о специфических симптомах отравления. В случае передозировки следует предполагать возникновение симптомов, описанных в разделе "Побочные действия", особенно со стороны желудочно-кишечного тракта.
Таблетки, покрытые оболочкой: 10 шт. - упаковки ячейковые контурные (1) - пачки картонные.
Суспензия для приема внутрь: 100 мл - флаконы темного стекла (1) в комплекте с мерным стаканчиком - пачки картонные.
Список Б. Препарат следует хранить в защищенном от света, недоступном для детей месте при температуре не выше 25 C. Срок годности - 4 года.
Препарат отпускается по рецепту врача.
1 покрытая оболочкой таблетка содержит 500 мг джозамицина.
В 10 мл суспензии для приема внутрь содержится 300 мг джозамицина.
Прочие ингредиенты: метилцеллюлоза, микрокристаллическая целлюлоза, кремнезем коллоидный безводный, полисорбат 80, натрия карбоксиметилцеллюлоза, тальк, магния стеарат, макрогол 6000, титана диоксид (Е171), алюминия гидроксид, поли(этакрилатметилметакрилат)-30% дисперсия.
У больных с почечной недостаточностью лечение следует проводить с учетом результатов соответствующих лабораторных тестов.
Следует учитывать возможность перекрестной устойчивости к различным антибиотикам макролидам (например, микроорганизмы, устойчивые к лечению родственными по химической структуре антибиотиками, могут также быть резистентны к джозамицину).
Читайте также:


-vil-prafen-500-mg-tabletki-%E2%84%9610-13.jpg)
