Может ли папиллома у девственниц
ЖУРНАЛ "ПРАКТИКА ПЕДИАТРА"
С.М. Харит, руководитель отдела иммунопрофилактики ФГУ "НИИ детских инфекций" Росздрава, главный внештатный специалист по вакцинопрофилактике детей Комитета здравоохранения Санкт-Петербурга, профессор, д-р мед. наук
В начале XX века И.И. Мечников впервые предположил, что существует взаимосвязь некоторых соматических заболеваний, в том числе злокачественных опухолей, с микроорганизмами. На сегодняшний день известно, что вирусы гепатита В (в 73% случаев) и С (в 27%) ответственны за развитие рака печени, микроорганизм Helicobacter pylori в 55% - за злокачественные опухоли желудка, а вирус папилломы человека - за развитие рака половых органов.
В настоящее время насчитывают около 180 типов вирусов папилломы человека (ВПЧ), каждому из типов присвоен номер (например, ВПЧ 16). Каждый тип имеет специфическое сродство со строго определенной областью организма человека. Вирусы папилломы вызывают обыкновенные бородавки на руках, подошвенные бородавки на стопах, на гениталиях и вокруг ануса (остроконечные кондиломы), в гортани, а также злокачественные заболевания. По степени онкогенности выделяют вирусы низкой, средней и высокой степеней риска. ВПЧ низкой степени риска (неонкогенные) - 6, 11, 40, 42, 43, 44, 54, 60, 70, 72, 81, ВПЧ средней степени риска - 26, 31, 33, 35, 51, 52, ВПЧ высокой степени риска - 16, 18, 39, 45, 56, 59, 68, 73, 82. ВПЧ 16 (в 54%) и ВПЧ 18 (в 13%) ответственны за большинство случаев рака шейки матки (табл. 1).
Таблица 1. Клинические проявления инфекции и типы вирусов, их вызывающих
| Проявления | Генотипы вируса |
| Кожные бородавки (ладони, стопы) | 1-4, 7, 10, 26-28, 41, 48, 49, 57, 60, 63, 65 |
| Папилломы верхних дыхательных путей и глаз | HPV 2, 6, 11, 13, 16, 32 |
| Эрозии, слущивающаяся клеточная карцинома | HPV 5, 8, 9, 12, 14, 15, 17, 19, 20-25, 36, 38, 47, 50 |
| Аногенитальные кондиломы, опухоли | HPV 2, 6, 11, 16, 18, 30, 40-42, 44, 45, 54, 55, 61 |
| Аногенитальные карциномы, рак шейки матки, вульвы, пениса, анальной области, прямой кишки | HR HPV 16, 18, 26, 31, 33, 35, 39, 45, 51-53, 56, 58, 59, 66, 68, 73, 82 |
ПУТИ ИНФИЦИРОВАНИЯ
Заражение ВПЧ происходит различными путями: сексуальный контакт (при генитально-генитальном, мануально-генитальном и орально-генитальном контактах); у девственниц инфекция может быть следствием сексуального контакта без полового акта. Известно, что правильное применение презерватива может снизить риск инфицирования, но не защищает полностью. Применение оральных контрацептивов не защищает от инфицирования.
Другие пути передачи: от матери новорожденному (вертикальный путь); через предметы (нижнее белье, хирургические перчатки, инструменты для биопсии); но заражение ВПЧ через предметы пока достоверно не подтверждено.
Большинство инфицированных не знают о заражении. От момента инфицирования до момента появления клинических проявлений проходит от 3 недель до 2-10 лет, но весь "скрытый период" человек является источником инфекции.
КЛИНИКА ВПЧ у детей
Латентная инфекция (клинических проявлений нет). Кожные бородавки. Рецидивирующий папилломатоз гортани. Бородавки выявляются у 4-20% детей школьного возраста и составляют 71% всех кожных заболеваний этого возраста. Вирусы, вызывающие аногенитальные кондиломы у взрослых, могут инфицировать плод и новорожденного, что является причиной развития у детей тяжелого заболевания - папилломатоза гортани, вызывающего нарушение дыхания и требующего неоднократных оперативных вмешательств.
ВПЧ у мужчин
Латентная инфекция (клинических проявлений нет). Генитальные папилломы. Внутриклеточная злокачественная неоплазма анальной области и полового члена. Анальный рак. Рак полового члена. Рецидивирующий папилломатоз гортани.
ВПЧ у женщин
Латентная инфекция (клинических проявлений нет). Генитальные папилломы. Злокачественное перерождение клеток 2-й и 3-й степени, рак шейки матки, влагалища.
По данным литературы, в течение сексуально активной жизни ВПЧ инфицируется 30-50% женщин, причем чем больше партнеров, тем выше этот риск.
Остроконечные, аногенитальные кондиломы у мужчин и женщин наблюдаются в основном в возрасте 15-30 лет и старше. ВПЧ 6-го и 11-го типа более чем в 90% случаев ответственны за развитие всех аногенитальных кондилом, которые клинически проявляются у 1% сексуально активного взрослого населения. За последние годы число случаев увеличилось в 6 раз у мужчин и в 10 раз у женщин. Ожидаемый риск развития генитального кондиломатоза в течение жизни составляет 10%.
Причиной развития рака шейки матки в 80% случаев являются ВПЧ 16-го и 18-го типов. Это второе по частоте злокачественное заболевание у женщин в возрасте до 45 лет после рака молочной железы. В США была проведена оценка сокращения продолжительности жизни. Она составила 26,1 лет при раке шейки матки, при раке молочной железы - 19,0, при раке яичников - 17,6 лет жизни. Конечно, не у всех инфицированных ВПЧ развивается рак. Реализации этого способствуют факторы риска и в первую очередь наличие различных заболеваний, приводящих к снижению иммунитета.
ПРОФИЛАКТИКА
Специфического лечения заболеваний, вызываемых ВПЧ, нет. Но в мире разработано две вакцины для предупреждения инфицирования наиболее опасными вирусами. Одна из них, вакцина Гардасил, в настоящее время зарегистрирована более чем в 60 странах мира (в том числе и в России) и не только рекомендована для прививания в частном порядке, но и включена с 2007 года в календари прививок многих стран, например США, Австрии, Германии и Франции. Другой вакцинный препарат против ВПЧ проходит стадии регистрации.
Гардасил - четырехвалентная вакцина, в состав которой входят белки, похожие на белки, содержащиеся в ВПЧ 6-го, 11-го, 16-го, 18-го типов. Синтезированы эти белки питьевыми дрожжами, абсолютно безопасными для человека. Эта вакцина, как и вакцина против гепатита В, не содержит инфекционных частиц. В препарат включены ВПЧ 6-го и 11-го типа, так как они вызывают в 90% случаев кондиломы и ВПЧ 16-го, 18-го типов, которые вызывают до 80% случаев рака шейки матки, до 40% случаев рака влагалища, а у мужчин в 40% случаев рак полового члена, ануса. В последние годы показано, что иммунитет, создаваемый вакциной, защищает и от некоторых других онкогенных ВПЧ, за счет перекрестного реагирования. Вакцина является профилактической, а не лечебной, и если человек уже инфицирован, то вакцина не излечит. Но так как инфицирование сразу четырьмя типами ВПЧ может происходить редко, то если инфицированного одним типом вируса вакцинировать, это защитит его от других трех типов вирусов. Поэтому предварительное обследование на инфицирование ВПЧ перед прививкой не требуется.
Наиболее рационально проводить вакцинацию до того, как возникают условия инфицирования, то есть до начала сексуальной активности. Рекомендуемый для вакцинации возраст: для детей и подростков обоего пола - 9-17 лет, для молодых женщин - 18-26 лет. В настоящее время ведутся работы по вакцинации женщин старшего возраста.
Показания к вакцинации
Профилактика:
- рака шейки матки,
- рака вульвы, влагалища, а также наружных половых органов у мужчин,
- генитальных кондилом,
- предраковых состояний,
- папилломатоза гортани.
Схема вакцинации
Иммунизация проводится трехкратно. Основная схема: 0-2-6 месяцев. Ускоренная: 0-1-3 месяца. Нарушения интервала: если три прививки сделаны в течение года, вакцинация считается завершенной. Вакцина высокоэффективна, иммунитет вырабатывается у 95-100% привитых.
Реакции на вакцину
Данный вакцинный препарат малореактогенный. Общие обычные (нормальные) вакцинальные реакции развиваются у 0,1% привитых в первые 3 дня и проявляются кратковременным недомоганием и субфебрильной температурой (до 37,5 °С). У 3-5% вакцинированных возможно появление в первые 1-5 дней местных реакции в виде отека и красноты не более 8 см в диаметре. Поствакцинальных осложнений в настоящее время не зарегистрировано.
Противопоказания к вакцинации
Временные: острое и хроническое заболевание в стадии обострения. Прививки проводят после выздоровления.
Постоянные: тяжелые аллергические реакции на компоненты вакцины (дрожжи, алюминий) или предшествующую дозу.
Рекомендуется воздержаться от беременности во время курса прививок. Прием контрацептивов не является противопоказанием к прививкам.
В заключение хотелось бы отметить, что вакцинация против четырех типов ВПЧ практически на 90% защищает от развития кондилом и рака, но сохраняется риск инфицирования остальными типами вируса. Поэтому проведение вакцинации не означает, что человек не должен соблюдать другие меры предосторожности.
Плохая новость: почти у половины сексуально активных мужчин и женщин обнаруживают вирус папилломы человека (ВПЧ). А значит – вероятность заразиться им крайне высока. Хорошая новость – это не смертельно и поддается лечению.
ВПЧ – один, а типов много
Подошвенная бородавка, папилломы, небольшие или обширные кожные отростки в области половых органов или ануса (они же – остроконечные кондиломы) – все это проявления ВПЧ. Точнее, разных типов одного вируса. Сегодня их насчитывают свыше 130. Типы ВПЧ подразделяют на две большие категории: низкоонкогенные и высокоонкогенные. Вирусы с низкой онкогенностью вызывают кондиломы и доброкачественные поражения шейки матки, а высокоонкогенные могут спровоцировать злокачественные опухоли шейки и рак полового члена. Наиболее опасными с онкологической точки зрения признаны 16 и 18 типы вируса. Также в группу вирусов высокого риска входят 31, 33, 35, 39, 45, 51 и другие типы ВПЧ.
Как происходит заражение ВПЧ?
Ой, что это? Внешние проявления папилломавирусной инфекции
Вообще кондиломы генитальной области – больше косметическая проблема, чем реальная угроза здоровью. Гораздо опасней другое проявление ВПЧ – плоская кондилома шейки матки. Она образуется, когда вирусные частицы уже изменили клетки эпителия шейки. Обнаружить плоскую кондилому непросто. Для этого нужно провести несколько исследований: кольпоскопию (исследование шейки матки под микроскопом), гистологию (изучение кусочка ткани шейки на предмет раковых клеток), биопсию. Если вовремя не выявить плоскую кондилому, она в будущем может переродиться в злокачественную опухоль.
ВПЧ как угроза онкологических заболеваний
Во-первых, онкология развивается далеко не у всех носителей ВПЧ. Во-вторых, даже самые серьезные последствия, настигают человека не внезапно. К примеру, чтобы вызвать рак шейки матки вирусу требуется минимум – несколько лет, и максимум – несколько десятилетий. За это время можно избавиться от злосчастного ВПЧ и не дать ему совершить непоправимое с вашим здоровьем.
Лечение ВПЧ: сложно, но можно
Впрочем, до серьезного лечения доходит не всегда. Нередко вирус папилломы самоизлечивается. Большинство зараженных ВПЧ женщин избавляются от вируса (даже не зная о его наличии) с помощью собственных антител. Они вырабатываются в организме через 9-15 месяцев после заражения. Однако это не защищает женщину от рецидива папилломавирусной инфекции.
"Острый" вопрос. Лечение остроконечных кондилом
Лечение остроконечных кондилом сводится к деструкции, т.е. удалению новообразований. Наиболее эффективными и безболезненными способами деструкции считаются радиоволновая хирургия (быстрое удаление и возможность исследовать ткань кондиломы на наличие раковых клеток) и лазерная хирургия (позволяет удалять не только кондиломы наружных половых органов, но и плоскую кондилому шейки матки, не оставляет шрамов и рубцов). Для удаления кондилом на слизистой или внутри влагалища применяют химические коагулянты – препараты-смеси органических и неорганических кислот. В лечении кондилом у мужчин также применяется лазерная и радиоволновая хирургия.
Не стоит забывать: избавление от внешних проявлений вируса не лечит сам вирус. Если вы удалили кондилому, но оставили без внимания сам ВПЧ, новообразования могут появиться вновь. Поэтому папилломавирус рекомендуется лечить комплексно, а не ограничиваться деструкцией кондилом.
Как защититься от ВПЧ? Профилактика папилломавируса и его рецидивов.
Основной способ заражения ВПЧ – это половой контакт. А значит – нужно быть осмотрительнее в выборе сексуального партнера, использовать презерватив и помнить: чем больше связей,
тем выше риск заполучить ВПЧ. Но, увы, ни презерватив, ни постоянный партнер, ни воздержание и даже девственность в случае вируса папилломы – не панацея от заражения. Именно поэто
му практически каждый второй человек является носителем ВПЧ. Это не страшно само по себе, опасны лишь проявления вируса на шейке матки и головке полового члена.
Чтобы исключить риск серьезных последствий проконсультируйтесь с врачом-гинекологом, иммунологом или вирусологом. Вероятно, потребуется обследование: кольпоскопия, мазок с шейки матки на атипичные (раковые) клетки, гистология. Также врач может порекомендовать сделать скрининг ВПЧ. Этот анализ позволяет определить тип вирусов. Если у вас выявят высокоонкогенные типы – периодические обследования нужно будет проходить обязательно. Дабы потом не оказаться на приеме у онколога.
Не лишним для профилактики ВПЧ (и его рецидивов) будет укрепление иммунитета. Вот несложные рекомендации, которые помогут сделать ваш организм сильнее.
Остались вопросы? Задайте их доктору. Онлайн. Бесплатно.
Обзорная информация
Генитальные бородавки (кондиломы) передаются контактным путем (половым, бытовым и в родах) и являются клинически видимыми признаками присутствия в организме ВПЧ-инфекции. Новообразования встречаются с одинаковой частотой у лиц обоих полов, причиняют физический и психологический дискомфорт, выступают фактором риска раковых заболеваний. Кроме наружных половых органов, кондиломы у женщин могут развиваться там, где их сложно обнаружить - во влагалище, на шейке матки и прямой кишке.
Как девушка может заразиться?
Девственница может заразиться штаммом ВПЧ, который вызывает кондиломы, если кожа или слизистые оболочки ее половых органов, уретры или ануса имели контакт с инфицированным объектом (одушевленным или неодушевленным). Это включает в себя, например:
- молодого человека, прикасающегося к своему члену, а затем к девушке,
- соприкосновение или трение инфицированного пениса с внешней или внутренней поверхностью вульвы,
- использование секс-игрушек от инфицированного человека
- любые вещи, связанные контактом с половыми органами более, чем 1 человека прямо или косвенно.
Где чаще всего у девственниц вскакивают кондиломы?
Локализации данных образований могут быть самыми различными, но, как правило, место первичного очага роста - это точка внедрения вируса. У девушек virgo папилломы гинекологи находят здесь (по мере снижения частоты выявления в %):
- на девственной плеве,
- на анальном отверстии и внутри прямой кишки,
- на малых половых губах и клиторе,
- вокруг наружного отверстия уретры,
- в ротоглотке,
- сочетанные поражения.
Может ли мужчина заразиться, если он имел оральный секс от инфицированной девственницы?
Да, к сожалению, мужчина может получить генитальные бородавки, получив оральный акт от девственницы. Если девушка переносит ВПЧ-инфекцию в своей слюне, это может очень легко быть передано и на член. Как, впрочем, и обратное - мужчина-носитель, делая кунилингус девственной партнерше, может наградить ее интимными папилломами.
Мне 19, девственница, половых контактов не было никаких и никогда. Решила осмотреть свои половые органы с помощью зеркала и по всем признакам у меня остроконечные кондиломы, при том они разрослись на обширные участки губ и даже девственной плевы. По ощущениям (такая шерховатая текстура) это у меня весь подростковый возраст, но я была уверена что это норма. Год назад на медосмотре в школе гинеколог мне ничего не сказал. Думаю, только один вариант, как я могла самозаразиться - это мастурбация последние 3 года. Это реально?
Вирус папилломы человека способен проникать в организм через ссадины и царапины на коже, микротравмы на слизистой. Возможно самозаражение при бритье гениталий, эпиляции глубокого бикини, самоудовлетворении и т.п. случаях при условии, что руки или предмет, используемы для этих целей, был инфицирован ВПЧ. Попав в ткани через "входные ворота" (кожные покровы или слизистую аногенитальной области, он и вызывает у девушки появление кондилом на девственной плеве и в иных интимных местах.
Это страшно, если у молодой девушки - кондиломы?
ВПЧ есть у большинства взрослых людей, и большинство его типов не опасны и не вызывают последствий. Появление же папиллом на половых органов само себе выглядит неэстетично, к тому же они могут расти и распространяться. Но есть онкогенные типы ВПЧ - у женщин они в несколько раз повышают вероятность рака шейки матки и прямой кишки. Как избежать возможных последствий - девочки-подростки с 15-17 лет ежегодно могут посещать врача и сдавать анализы на скрытые инфекции, даже являясь фактическими девственницами. также хорошей идеей будет сделать прививку от онкотипов вируса.
В принципе, в желании следить за своим здоровьем в любом разумном возрасте нет ничего особенного, нужно просто найти время и заставить себя записаться к хорошему гинекологу. На приеме наш доктор выслушает ваши жалобы или подозрения и после этого проведет обследование. Деликатные специалисты, безболезненный осмотр, индивидуальный подход и лучшие условия на услуги по лечению гарантируются! Приходите вдвоем-втроем - скидки на услуги для учащихся и школьников!
В зависимости от ситуации и ваших пожеланий могут быть проведены:
- полный гинекологический осмотр
- осмотр кожных покровов
- вульвоскопия (по ситуации - кольпоскопия)
- аноскопия
- ректальное исследование
- пробы с уксусной к-той и проба Шилллера
- взятие анализа на ВПЧ (Дайджен-тест)
 | 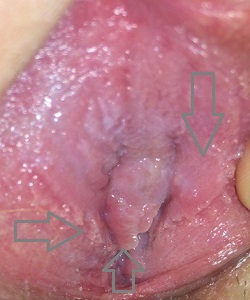 | 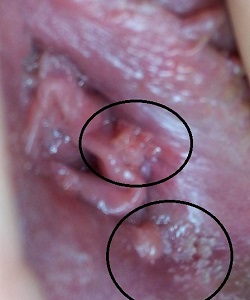 |  |
| фото 1 | фото 2 | фото 3 | фото 4 |
Какие еще можно себя проверить
Пантеева Я.И., Артамонов Р.П.
Резюме
Основным фактором развития рака шейки матки является инфициривание вирусом папилломы человека. В настоящее время изучены более 300 генотипов, 14 из которых приводят к развитию рака шейки матки. Вирус папилломы человека 16 и 18 типов вызыват развитие рака шейки матки в 75% случаев.
Ключевые слова
Статья
Пантеева Я.И., Артамонов Р.П.Научный руководитель: ассистент Макиенко А.А.
ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава РФ
Кафедра факультетской хирургии и онкологии им. С.Р. Миротворцева
Актуальность темы: Рак шейки матки - злокачественная эпителиальная опухоль, поражающая влагалищную часть шейки матки или шеечный канал в виде экзофитного или эндофитного образования. Рак шейки матки (РШМ) занимает 6‑е место в структуре онкозаболеваемости женского населения России (в мире – 2‑е место). В 2017 г. удельный вес РШМ составил 4,9% (17303 впервые выявленных больных). Наиболее часто РШМ выявляется в возрастной группе 25–49 лет и находится на 2-м месте после рака молочной железы. За десятилетний период (2007–2017 гг.) наблюдается рост показателя активного выявления РШМ на 12,8% (показатель 2017 г. составил 42,3%). В I-II стадии выявлено 65,7% случаев выявления РШМ. В III стадии – 23,1%, в IV стадии – 9,3%. В III-IV стадиях выявлено 32,5% случаев РШМ.
В Саратовской области увеличилось число выявленных случаев рака шейки матки при профилактических осмотрах с 26,6% в 2010 году до 41,6% в 2017 году. В 2017 г. удельный вес РШМ составил 4,3% (262 впервые выявленных больных). Чаще всего РШМ выявляется в возрасте 55-59 лет. В I-II стадии выявлено 82,8% случаев выявления РШМ, в III стадии – 9,2%, в IV стадии – 8,0%. В III-IV стадиях выявлено 17,2% случаев РШМ [1].
В этиологии РШМ выделяют инфицирование ВПЧ. Впервые папилломавирусная инфекция была описана в I веке до н. э. врачами древней Греции. По их мнению, генитальные бородавки передавались половым путем. В 60 – х годах XIX в. Melnick и А.Д.Тимофеевский выявили присутствие вирусоподобных частиц в паппиломах. В 1892 году исследователь Rigoni-Stern заметил, что причиной смерти у замужних женщин часто был рак шейки матки, но не встречался у девственниц. Исследователи Dunn и Ogilvie в 1968 году обнаружили в генитальных бородавках вирусные частицы.
8 октября 2008 г. Нобелевский комитет присудил премию Харальду цур Хаузену из Германского центра исследования рака в Гейдельерге, которую он разделил с французким вирусулогами Люком Монтанье и Франсуазой Барре-Синусси за открытие роли ВПЧ в генезе рака шейки матки и создание вакцины для его профилактики.
Основным этиологическим фактором патогенеза РШМ считается инфицирование вирусом папилломы человека (ВПЧ) высокой степени онкогенного риска. ВПЧ относится к высококонтагиозным инфекциям с инкубационным периодом от 3-4 недель до 8 месяцев. На сегодняшний день идентифицировано более 300 новых папилломавирусов. Четырнадцать хорошо изученных генотипов ВПЧ (ВПЧ 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66 и 68) считаются патогенными или генотипами "высокого риска" и вызывают развитие рака шейки матки. Хроническая персистенция ВПЧ 16 и 18 типов вызывает рак шейки матки в 70-75% наблюдений.
Нормальный клеточный цикл состоит из G1, S, G2 и M фаз. Эпителий шейки матки представляет собой динамическую ткань с постоянным клеточным обновлением. Киназа, которая обеспечивает прохождение клетки из G1 в S фазу клеточного цикла, — это E2F.В норме она неактивна, находится в связанном состоянии с белком супрессором Rb (продукт гена ретинобластомы). Белок р16 (INK4a) осуществляет контроль разобщения комплекса E2F-Rb, не допуская безудержной пролиферации клетки. Однако синтез р16 (INK4a) в норме по механизму обратной связи сдерживается. Таким образом, концентрация данного белка в нормальной клетке чрезвычайно мала, что проявляется негативной ИЦХ реакцией [6]. Белок Е7 вируса папилломы человека высокого онкогенного риска при своем взаимодействии с продуктом гена Rb приводит к разобщению комплекса E2F-Rb. E2F остается постоянно в активном состоянии, стимулируя безудержную пролиферацию клеток. Р16 (INK4a) пытается сдержать пролиферацию клетки, что приводит к бесконтрольному его синтезу. Однако р16 лишен своей мишени, что в условиях отсутствия обратной связи значительно повышает его концентрацию в клетке. ИЦХ при этом проявляется позитивной реакцией, что и является биомаркером инициации канцерогенеза в эпителии шейки матки [7]. Было достоверно показано, что экспрессия р16 связана с низкой, умеренной и тяжелой дисплазией (с внутриэпителиальными плоскоклеточными поражениями шейки матки как высокого, так и низкого Grade, LSIL и HSIL соответственно классификации ВОЗ), причем экспрессия р16 не встречалась в плоском эпителии без признаков дисплазии [8].
Процесс канцерогенеза при раке шейки матки включает в себя четыре стадии: ВПЧ инфицирования зоны трансформации шейки матки, персистенции инфекции, увеличения и трансформации ВПЧ инфицированных клеток до развития цервикальной интраэпителиальной неоплазии (CIN III) или аденокарциномы in situ (AIS), а также прогрессирование в инвазивный рак. Незначительные клеточные аномалии, такие как атипичные плоскоклеточные изменения неясного значения (ASCUS), плоскоклеточные интраэпителиальные поражения низкой степени (LSIL) или атипичные железистые изменения клеток неопределенного значения (AGUS) в цитологических мазках или цервикальное интраэпителиальное поражение низкой степени (CIN I) при гистологическом ответе может наблюдаться в течение нескольких месяцев после инфицирования ВПЧ ВР. При несвоевременном лечении CIN III и AIS в 40%-50% случаев может прогрессировать до рака шейки матки в течение 5-30 летнего периода [9].
В настоящее время существует первичная и вторичная профилактики рака шейки матки: первичная профилактика включает в себя вакцинацию для профилактики ВПЧ - инфекции девочек - подростков в возрасте от 9 до 18 - лет до начала половой жизни; вторичная профилактика, главной задачей которой является выявление предраковых поражений шейки матки, таких как CIN III и AIS путем скрининга – ВПЧ - тестирования у женщин в возрасте от 30 лет и старше. В настоящее время доступны две рекомбинантные вакцины против ВПЧ, содержащие вирусные частицы: четырехвалентная вакцина против ВПЧ 16, 18, 6, и 11 типов, а также двухвалентная вакцина, защищающая от ВПЧ 16 и 18 типов. Обе вакцины для профилактики рака шейки матки, проведённые женщинам в возрасте 15 -26 лет, показали высокую иммуногенность и существенную защиту от хронической инфекции ВПЧ, CIN III, а также показали защиту от интраэпителиальной неоплазии ануса. Обе вакцины в вакцинированной популяции имеют высокий потенциал защиты от 70% случаев рака шейки матки. Эффективность вакцин против персистирующей инфекции, исследуемых в III фазе клинических испытаний, превышала 99%. Исследования вакцин показали достаточно сильную иммуногенность и отличную безопасность в подростковом возрасте, хотя клинические испытания не включали девочек до 9 лет, являющиеся основной целевой группой национальных программы вакцинации. Фактические данные о безопасности и эффективности вакцин в клинических испытаниях, также руководства в области общественного здравоохранения рекомендуют внедрение вакцинации против ВПЧ в национальные программы иммунизации. [10]
Цель работы: Оценить состояние активного поиска РШМ на выделенном территориальном участке г. Саратова.
Материалы и методы. Ретроспективно исследованы амбулаторные карты пациенток с РШМ, прикрепленных к городской поликлинике с населением выше 75000 человек. Укомплектованность штатами составляет 55%. Женская консультация состоит из трех лечебно-диагностических отделений, расположенных на отдаленных участках района. В каждом отделении имеется штат гинекологов, акушерок под руководством заведующего отделением. Прием ведется в кабинете доврачебного осмотра и кабинетах гинекологов. На доврачебный осмотр попадают все женщины, впервые обратившиеся в поликлиническое учреждение в этом году.
За период 2012-1017гг. на территориальном участке г. Саратова было выявлено 47 больных (%) с РШМ. Средний возраст составил – 58 лет. В I стадии выявлено 21% (10 человек), во II стадии – 60% (28 человек), в III – 13% (6 человек), в IV – 6% (3 человека). При гистологическом исследовании у 80% больных был обнаружен плоскоклеточный рак, у 20% – аденокарцинома. Оперативное лечение проведено у 75% пациенток, из них у 13% выполнена конизация шейки матки с последующим выскабливанием, у 64% – расширенная экстирпация матки II типа, у 23% – расширенная экстирпация матки III типа. Радиологическое лечение проведено у 15% пациенток, симптоматическое у 10%. При ретроспективном анализе гинекологической патологии в этой группе больных установлено, что до постановки диагноза РШМ ВПЧ 16 и 18 типов был обнаружен у 57% больных. Из них лечились до установления диагноза 74%. Лечение проводилось противовирусным препаратом, курс лечения – 10 дней, количество курсов – 3 с перерывом в 10 дней.
Заключение: На основании результатов проведенной работы необходимо разработать мероприятия, которые позволят увеличить уровень выявления ВПЧ. Следует проводить мероприятия по информированию пациентов о важности посещения гинекологического кабинета не реже 1 раза в год, увеличить мотивацию к участию в мероприятиях по раннему выявлению злокачественных новообразований. Важным аспектом является необходимость информированности населения о важности вакцинации против ВПЧ.
Литература
4. Давыдов М. И. Ганцев Ш.Х. Онкология. - М.: ГЭОТАР-Медиа, 2013. - 920
5. IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. Human Papillomavirus // International Agency for Research on Cancer IARC, Lyon, France. – 2007. - No3. Vol. 90.– Р. 45 -48.
6. Дамиров М. М. Радиоволновая технология в лечении патологии шейки матки / М. М. Дамиров. – М., 2010. – С. 70.
7. Ю.Г. Паяниди, К.И. Жорданиа, М.В. Савостикова, А.Г. Маргарян. Рак шейки матки в России. Пути профилактики/ Вестник ФГБУ" РОНЦ им. Н.Н. Блохина", т. 26, №1, 2015

Австралийский врач, занимающийся проблемой менопаузы у подростков, высказывает серьезные опасения.
В апреле 2011 года в клинику доктора Дейрдры Литтл, в сельский район Нового Южного Уэльса, с проблемой преждевременной менопаузы обратилась 16-летняя Сюзан (имя изменено). При обследовании Сюзан не было найдено ни одной причины гормонального сбоя, что, в общем-то, обычная практика, поскольку в 90% случаев сложно назвать точную причину нарушения овуляции. Однако это был не рядовой случай, так как начало менопаузы без какой-либо причины у девочек-подростков происходит настолько редко, что нет даже какой-либо статистики.
Сюзан сделала три прививки: в феврале, мае и августе 2008 года, через год после начала менструального цикла. В течение полугода цикл стал нерегулярным, а два года спустя вообще прекратился. Ее лечащий врач, не анализируя симптомы, предложила ей таблетки для оральной контрацепции. Но Сюзан не вела половую жизнь. Она отказалась от таблеток и обратилась за консультацией к другим врачам.
Анализ показал, что ее яичники находятся в таком же состоянии, как уженщины в период постменопаузы: антимюллеровский гормон, показатель здоровья яичников, был на рекордно низком уровне. Это состояние известно как преждевременное нарушение овуляции (POF).
Больше беспокоит то, что в документах исследования препарата на безопасность доктор Литтл не обнаружила детального доклада о гистологическом исследовании состояния яичников вакцинированной крысы. Был только доклад о гистологическом состоянии семенников.
Вскоре еще две девушки 17 и 18 лет обратились в клинику с проблемой отсутствия цикла. Они тоже сделали прививку от HPV после начала менструального цикла. Всем трем девушкам ранее были прописаны контрацептивные таблетки, действие которых усложнило постановку диагноза.
Девушки рассматривали вариант заморозки яйцеклеток, и одна из них даже начала это делать через программу Криосохранения экстракорпорального оплодотворения, чтобы позднее, когда она захочет родить ребенка, воспользоваться этим биоматериалом.
Все три случая были тщательно задокументированы, описаны и опубликованы в специализированных журналах, выпущенных за последние три года, и также были взяты на заметку Администрацией терапевтических товаров (TGA), лицензионным органом в Австралии.
Информация из лаборатории клинических исследований у подростков позволяет сделать некоторые выводы и высказать связанные с ними опасения:
* Большинство молодых женщин при исследованиях безопасности использовали гормональные средства контрацепции, которые маскируют изменения в менструальном цикле.
По истечении длительного времени фиксировались только те изменения, которые требовали срочного медицинского вмешательства. По определению сюда не входят проблемы с менструальным циклом, поскольку они не угрожают здоровью и не грозят госпитализацией.
* Исследования препарата на безопасность принимали во внимание и основывались только на случаях, приведших к госпитализации. Эти исследования не могут заметить нарушение овуляции, утверждает доктор Литтл, отмечая, что она еще никогда не направляля девушку в стационар из-за отсутствия менструации.
* Количество девушек, прошедших все исследования до конца, было слишком мало, поскольку в целевой возрастной группе по вакцинации из нескольких сотен девушек-подростков более половины девочек затерялись год спустя, после чего осталось только 240 подростков. Также не было зафиксировано, какое количество девочек уже вступили в менструальный цикл на момент исследования, поскольку основной возраст был 11.9 лет.
* Не хватает данных по исследованийю среди мальчиков. Хотя мальчики тоже прививаются от HPV и являются его переносчиками, в исследовании участвовало только двести мальчиков, большая часть из которых также затерялась в течении года. В ходе исследования в группе мальчиков был зафиксирован один случай внезапной смерти. Поскольку после смерти ничего не обнаружилось, исследователи высказали уверенность, что смерть наступила не в результате вакцинации против вируса папилломы человека.
Вакцинация всегда включает в себя вычисление рисков и пользы. В этом случае риск масштабной вакцинации девочек в период полового созревания должен быть оценен в сравнении со случаями заболевания и смерти от рака шейки матки. Причем, это должно было быть сделано до того, как вакцина получила одобрение.
После внедрения национальной системы ранней диагностики рака шейки матки только в течение одного десятилетия эти цифры уменьшились более чем в два раза, а в 2000 году было диагностировано лишь 578 новых случаев заболевания. Чаще всего это происходило в отдаленных областях, где риск смерти от рака шейки матки для туземных женщин Австралии в шесть раз превышал уровень среди не-туземцев.
В 1989 году было установлено, что ранняя диагностика может предотвратить 90% злокачественных образований. К 2002 году в Австралии количество заболеваний раком шейки матки составляло 6.2 на 100 000 женщин, а уровень смертности – 1.7 на 100 000 женщин. В 2011году в Австралии было зафиксировано 229 случаев смерти от рака шейки матки.
В любом случае, вакцинация не избавляет от всех проблем: заболевания раком шейки матки все еще может случиться среди привитых лиц, поэтому анализ на мазок Папаниколау все еще необходим для сексуально активных женщин в возрасте до 70 лет.
В свете этих фактов лекарственные компании, производящие вакцину против вируса папилломы человека, и власти, которые это одобряют, должны обеспечить гарантии того, что в попытках большего снижения уровня заболевания раком шейки матки они не поставят здоровых девушек-подростков под угрозу нарушения овуляции. Если не власти, то сами женщины должны требовать всестороннего исследования лекарства в отношении его воздействия на яичники, которое может привести к их бесплодию.
Читайте также:



