Золотистый стафилококк в позвоночнике лечение
Инфекции позвоночника (спинальные инфекции)
Определенные группы людей находятся в большей группе риска заболеть спинальными инфекциями. Это люди злоупотребляющие курением, страдающие ожирением, недостаточностью питания, с ослабленным иммунитетом, либо с синдромом приобретенного иммунодефицита возникшим в результате лечения онкозаболеваний, страдающие артритом, после трансплантации органов, наркоманы, больные сахарным диабетом, или те, подвергся инвазивным процедурам на мочевых путях. Достаточно редко встречается как туберкулез, так и сифилитическое поражение позвоночника.
Симптомы варьируют в зависимости от конкретной инфекции, но в первую очередь заслуживают внимания постоянные боли в спине без наличия в анамнезе травмы. Нередко диагностика бывает запоздалой из-за не всегда выраженной симптоматики или трудности идентификации болевого синдрома, и отсутствие системных признаков, таких как повышение температуры. Лабораторное исследования также могут ввести в заблуждение так, как например может быть нормальное количество лейкоцитов, рентгенограммы часто не выявляют никаких отклонений на ранних стадиях заболевания, и даже более чувствительные диагностические методы, такие как сканирование костей (КТ) может быть вначале без патологических признаков в течение первой недели заболевания. На сегодняшний день при подозрении на спинальную инфекцию единственным достоверным методом диагностики является МРТ. Кроме того, скрининг-тестом является анализ крови на скорость оседания эритроцитов (СОЭ).
Дисцит или инфекция дискового пространства, это воспалительное поражение межпозвонкового диска, которое возникает чаще у детей, чем у взрослых. Причина дисцита до сих пор является предметом дискуссий,но большинство исследователей считают это заболевание инфекционным. Инфекция, вероятно, начинается в одной из концевых пластин, и диск заражается вторично. Сильная боль в спине, которая возникает неожиданно является характерным симптомом дисцита. И хотя большинство детей будет продолжать ходить, несмотря на боль, маленькие дети могут отказываться двигаться. Характерный признаком является также расширение позвоночника на рентгенографии и полный отказ ребенка сгибать позвоночник.У детей с дисцитом,как правило, нет системных заболеваний. У них редко повышенная температура и количество лейкоцитов в крови часто в норме. Тем не менее, скорость оседания эритроцитов(СОЭ), как правило, увеличена.
Боковые рентгенограммы позвоночника обычно визуализируют сужение дискового пространства с эрозией позвоночных концевых пластин смежных позвонков. КТ может быть полезным для локализации поражения, которые достаточно трудно диагностировать клинически. В некоторых случаях томография может быть ложно отрицательна, но это не является поводом исключения инфекции диска. Магнитно-резонансная томография (МРТ) может оказаться необходима для диагностики локализации инфекции диска. Лечебные мероприятия при дисцитах до сих пор являются темой для дискуссий. Большинство медиков рекомендуют иммобилизацию с помощью гипса и,как правило, во многих случаях такая тактика оправдана.Кроме того рекомендуется антибиотикотерапия из-за инфекционного генеза дисцита (в организме человека это чаще всего золотистый стафилококк). При лечении дисцита у детей, биопсия обычно не требуется. Биопсия может быть назначена подросткам или взрослым, особенно если есть подозрение на употребление наркотиков так,как в таких случаях будут другие микроорганизмы, а не золотистый стафилококк.
Остеомиелит позвоночника представляет собой инфицирование тела позвонка. Причиной остеомиелита могут быть как бактерии,так и грибки. Наиболее часто возникает бактериальный или пиогенный остеомиелит. Проявления остеомиелита отличаются от инфекции дискового пространства. Это могут быть инфекции из других частей тела, занесенные в позвоночник гематогенно. У этих пациентов присутствуют системные признаки такие,как повышение температуры, увеличение количества лейкоцитов и СОЭ. Среднее время от начала симптомов до постановки окончательного диагноза, как правило, колеблется от 8 недель до 3 месяцев. Начало заболевания, как правило, острое, и с боль в спине является наиболее частым симптомом. Боль локализуется вначале на уровне вовлеченной области с постепенным увеличением интенсивности. Боль в конце концов становится настолько интенсивной, что не проходит даже в положении лежа.
Обычно неврологических симптомов не бывает до тех пор, пока в ходе процесса не происходит разрушение и распад тела позвонка. Другие симптомы включают: периодические ознобы,снижение веса, расстройство мочеиспускания(дизурия), светобоязнь, и выделения из послеоперационной раны (если проводилось оперативное вмешательство). Возбудителем заболевания, как правило, является золотистый стафилококк. При остеомиелите требуется длительная антибиотикотерапия — как правило в течение шести недель антибиотики вводятся внутривенно и потом еще в течение шести недель прием антибиотиков перорально. Оперативное лечение может быть необходимо при хронических инфекциях таких, как туберкулез позвоночника. Чаще всего такие инфекции встречаются встречаются в слаборазвитых странах.
Эпидуральный абсцесс - это инфекция, которая возникает в пространстве вокруг твердой мозговой оболочки(дуральной оболочкой), которая окружает спинной мозг и нервные корешки. Эти очаги с содержанием гноя могут окружать спинной мозг и / или нервные корешки и оказывать компрессионное воздействие с нарушением функций нервных структур. Симптомы могут быть незначительными (парестезии — ощущение покалывания булавкой) или незначительная общая слабость.Необходим осмотр спины для оценки наличия асимметрии, паравертебрального отека и болезненности позвонков,а также изучение неврологического статуса. В диагностическом плане имеет значение СОЭ также, как и при других спинальных инфекциях. Количество лейкоцитов в крови и посев крови используются в качестве базовых параметров. Обычная рентгенограмма не информативна. Магнитно-резонансная томография (МРТ) является методом диагностики для выбора тактики лечения. МРТ исследование позволяет определить наличие компрессии спинного мозга и состояние спинного мозга, определить наличие и размер абсцесса, позволяет диагностировать сопутствующий остеомиелит, и исключить образование паравертебрального набора жидкости. Показаниями к хирургической декомпрессии спинного мозга являются увеличение неврологического дефицита, стойкие сильные боли, высокая температура и увеличение лейкоцитов.
Послеоперационные инфекции. Увеличение частоты послеоперационных раневых инфекций связано с увеличением использования фиксаторов. Преимущества жесткой фиксации позвоночника с помощью специальных (металлических) фиксаторов заключаются в возможности ускорить регенерацию и уменьшить внешнюю иммобилизацию в послеоперационном периоде, чтобы увеличить скорость слияния и снижения послеоперационной внешней иммобилизации -результаты этого очевидны. Но инфекция является одним из основных недостатков имплантации инородных тел в позвоночник. Профилактическое применения антибиотиков имеет определенный эффект, но небольшой процент осложнений избежать не удается. В основном риск инфекции зависит от исходного состояния организма. Недавно было определено, что, в частности, курильщики находятся в очень высокой группе риска послеоперационного заражения. Диагноз послеоперационной инфекции, как правило, выставляется на основе выделения из раны или неожиданного появления болей. Другими симптомами являются повышенная температура, формирование гематомы покраснение и отек в области раны, повышенная СОЭ и повышение количества лейкоцитов в крови. После того, как возникло подозрение на инфекцию необходимо оперативное исследование раны, которое выполняется в операционной и под наркозом. Это необходимо для активной хирургической санации всей раны. Диагностическая визуализация имеет ограниченное применение. Лечение инфицированных ран включает санацию, антибиотики широкого спектра, введение антибиотиков в рану,орошение раны или открытое лечение. Возможно можно потребоваться удаление омертвевших тканей. Если же такое лечение не дает результат может потребоваться удаление имплантатов. Наиболее распространенной инфекцией являются бактерии золотистого стафилококка. Продолжительность внутривенного введения антибиотиков зависит от инфекции. Лечение послеоперационных инфекций может быть длительным и дорогостоящим, но всегда оптимальным.
Использование материалов допускается при указании активной гиперссылки на постоянную страницу статьи.
Здравствуйте, хочу рассказать мою историю, возможно, кому-то будет интересно и полезно. Писать буду много. Мне 29 лет, веду активный образ жизни, не ем всякую дрянь, занимаюсь танцами, из вредных привычек-курение. Мое заболевание началось очень странно и до сих пор я не могу найти ответов на мои вопросы. Все началось с головных болей на работе(работя сидячая, за компом). Сначала я терпела, потом стала принимать препараты от головной боли, все вроде нормально, но тут вдруг после приема Цитрамона у меня отек глаз. Работала я тогда в Здании, где находится клиника, я тут же к врачу, она говорит, что это конъюнктивит, выписала капли, лучше не стало, так и ходила, пошла ещё к одному офтальмологу, потом к другому, потом на диагностику-ничего, с глазами все нормально, посоветовали обратиться к неврологу. Пришла-остеохондроз шейного отдела, назначили медикаментозное лечение-стало хуже. Обратилась в другую клинику, там назначили капельницы, массаж, иглоукалывание. После капельницы на следующий день стало совсем плохо. Резко закружилась голова, еле дошла до ближайшего магазина, хотела скорую вызвать, но тут посмотрелась в зеркало и стало страшно-все лицо плыло, я не могла сфокусировать зрение, нос как будто плавал по кругу. Я попыталась успокоиться, потом поняла, что у меня немеет язык и правая рука, вызываю такси, еду в клинику, к этому времени началась рвота и страшные головные боли. В больнице мне поставили уже другую капельницу и отправили на мрт. Мрт показало внутричерепную гипертензия по гидроцефальному типу, отек зрительных нервов. Мой врач оставила лечение это же-капельницы и иглоукалывание и массаж. Улучшения не было, по мимо этого дома я носила воротник, купила ортопедическую подушку, исключила компьютер и телефон(только по делу), с работы пришлось уволиться, тк я понимала, что с такой работой будут только ухудшения. Тк улучшений не было, я обратилась в больницу по месту жительства, там мне назначили медикаменты от внутричерепного давления, уколы, улучшений не было, мучили дикие головные боли, краснота в глазах и боль за глазницами, местный офтальмолог тоже сказала, что с глазами все норм. В то же время я не чувствовала себя пациентом невролога, что то тут не так, раз лечение не помогает. Сходила к аллергологу, тк после приёма противовоспалительных так и отекал глаз, сказал, что аллергия на нпвп, хотя раньше я их нормально всегда переносила, пролечилась от аллергии-не помогло, исключила нпвп.Так же у меня были увеличены лимфоузлы на шее и, раз уж я без работы, свободного времени полно, на всякий случай пошла к лору. Мне назначили бак посев из носа, носовые проходы были сужены-диагноз хронический ринит, по мрт носовые пазухи свободны. По анализу обнаружили золотистый стафилококк. Лечение-антибиотики, хлорофиллипт, антибиотик в нос. И тут началось! После первого дня приема антибиотиков внутрь остеохондроз дал о себе знать, ранее боли в позвоночнике меня не беспокоили, только головные и глазные боли, тут стал болеть весь позвоночник и все суставы, я не могла спать, в побочках это не указывалось, но! Аллилуя!-за все 7 дней приёма ни разу не болела голова! Это чудо! Соплей у меня не было, но во время лечения потекло, я не знаю откуда столько взялось и где помещалось такое количество))) После окончания приема антибиотиков внутрь, лечение носа продолжилось, головная боль вернулась, но я заметила одну вещь, боль всегда начиналась на уровне глаз и лба и потом охватывала всю голову, тк нпвп я исключила, то спасалась ношпой и я заметила, что после приема таблетки головная боль проходила, а боль в районе лба оставалась, я решила, что это болят лобные пазухи, но как? Мрт же показало, что лобные пазухи свободны. Но при массировании лба боль ощущалась именно в пазухах и отдавала в районе глаз. Что хочу сказать. мое лечение подходит к концу и я чувствую себя намного лучше-головные боли почти не беспокоят, глаза тоже, при чем краснота исчезла и мой остеохондроз куда то тоже! Я не врач и не знаю есть ли связь, много искала инфы в интернете, кое что там об этом есть, но все врачи опровергают связь стафилококков с остеохондроз от, но я знаю точно, что врачи сами НИ ХЕРА не знают, я могу сказать это со 100% уверенностью, тк все мои друзья врачи и за свою жизнь я немало побывала у врачей и в платных и в гос учреждениях. Ещё хочу сказать надейтесь только на себя, слушайте своё тело, ни один врач вам не поможет, кроме вас самих, не верьте диагнозам, доверяйте только своему телу.
Инфекции позвоночника одни из самых распространенных симптомов, возникновение которых происходит спонтанно или вторично от разных заболеваний в организме пациента. В успешных странах инфекция позвоночника очень редкое явление.

Безболезненная, уникальная методика доктора Бобыря
Дешевле, чем мануальная терапия
Получайте пропуск и приезжайте к нам!
Только с 10 по 20 апреля! Записывайтесь!
Инфекции позвоночника одни из самых распространенных симптомов, возникновение которых происходит спонтанно или вторично от разных заболеваний в организме пациента. В успешных странах инфекция позвоночника очень редкое явление.
В результате каждый год выявляется 0,037 промилле с инфекцией диска и только 0,037 бактериальный остеомиелит, что сопровождается эпидуральным абсцессом. Только 1% приходится на послеоперационные инфекции дискэктомии и до 6-8% это операция с использованием фиксаторов.
Опасность заболеть спинальными инфекциями очень велик у людей, злоупотребляющих курением, недостатком питания, со слабым иммунитетом, которые страдают ожирением, зачастую есть признаки приобретённого иммунодефицита в ходе лечения онкологических заболеваний у многих людей, при наличии артрита, после пересадки органа, наркоманы или подвергшиеся инвазийными процедурами в мочевыводящих путях. Иногда встречается у больных туберкулезом или сифилитическими изменениями в позвоночнике.
Наличие или присутствие болевых ощущений в спине без присутствия анамнеза травмы, характерных инфекций, но иногда диагностика случается запоздавшей и не всегда проявляется в этих симптомах, инфекции болевого синдрома, сопровождающиеся отсутствием увеличения температуры. Исследования в лабораторных условиях еще не настолько точные, при нормальном уровне лейкоцитов рентгенограммы не полностью показываются изменение на ранней стадии болезни, есть более точные способы, например, сканирование костной системы (КТ) на начальной стадии без патологий в первые дни болезни. В наше время самой точной диагностикой на выявление спинальной инфекции является диагностирование через МРТ, с помощью которого получение анализа крови на скорость оседания эритроцитов будет более точным.
Воспалительное поражение межпозвоночного диска называется дисцитом или инфекцией в дисковом пространстве, возникновение его наблюдается у ребенка чаще, чем у взрослого. Дисцит до сих пор у исследователей стал предметом обсуждения, но ряд ученых выделяют эту болезнь как инфекционную. Возможное инфекционное заболевание появляется на концевых пластинах, при этом диски заражены вторично. Дисцит сопровождается сильными болевыми ощущениями в спинном отделе позвоночника.
При этом большинство детей будут продолжать двигаться, несмотря на боли в позвоночнике, но слишком маленькие при этой боли не смогут передвигаться из-за боли в позвоночнике. Основным признаком считают расширение в позвоночнике на рентгенографии, сопровождается отказом ребенка сгибаться, в большей степени заболеваний дисцитом у детей системных нет. Уровень лейкоцитов нормальный, температура нормальная, что сопровождается увеличением СОЭ.
Визуально можно наблюдать сужение дисков пространства с эрозией позвонка в концевых пластинках соседних позвонков боковыми рентгенограммами позвонка. Очень сложно диагностировать локализацию поражения позвоночника, с применением КТ все локализации поражений будут выявлены и диагностированы в лучший результат. В результате несколько случаев томография возможна как отрицательной, что обосновывается отсутствием инфекции диска.
Наиболее распространенным способом выявления локализации инфекций является диагностирование с помощью магнитно-резонансной томографии, при этом диагностировании лечебные мероприятия дисцита еще пока являются темой множества обсуждений. Многие медики советуют и применяют в лечение больных иммобилизацию с применением гипса, что зачастую оправдывает свое применение на практике. Все эти мероприятия сопровождаются антибиотикотерапией, потому что в организме пациента присутствует золотистый стафилококк, поражающий инфекционный генезис диска дисцита. Обычно при лечении детей биопсия не нужна. В подозрение на употребление наркотиков у подростков или у взрослых будет назначена биопсия, потому что есть наличие на присутствие других микроорганизмов, и не выявляется золотистый стафилококк.
Остеомиелит позвоночника – зачастую является инфицированием тела позвоночника, сопровождая за собой появление бактерий и грибка в ряде частого возникновения бактериального или пиогенного остеомиелита. Это проявление остеомиелита не похоже на инфекцию в дисковом пространстве, сопровождающееся инфекцией частей тела и присутствующее в позвоночнике гематогенно. Больной зачастую чувствует увеличенную температуру, растут лейкоциты и СОЭ.
Окончательный диагноз проявления всех симптомов можно считать полностью готовым от восьми недель до трех месяцев. На начальной стадии у больного проявляется боль в спине, это самая распространённая симптоматика. На начальной стадии лечения присутствие боли уменьшается вовлеченной области с периодической интенсивностью, а в самом конце приобретает продолжительный характер с переходом пациента в лежачее состояние.
Невралгический симптом может быть до тех пор, пока нет разрушения тела позвоночника. Такое сопровождается: снижением массы тела, частым ознобом, расстройством мочеиспускания (дизурией), боязнью света, появлением выделений из раны пациента (с оперативным вмешательством), причиной которого служит золотистый стафилококк. Лечение остеомиелита сопровождается продолжительной терапией в течение 6 недель, лекарства вводят внутривенно, и продолжается повторение курса еще на 6 недель перорально. Лечение туберкулеза позвоночника с сопровождением хронической инфекции требует быстрого вмешательства со стороны медиков, и зачастую такое вмешательство распространено в менее развитых странах.
Инфекционное заболевание, возникающее в окружающем спинном мозге и нервных корешках пространства, вокруг твёрдой мозговой оболочки (дуральная оболочка). Очаги этой инфекции содержат гнойные выделения, они окружают спинной мозг и нервные окончания, при этом оказывают сдавливающее воздействие, которое приводит к нарушению функций в нервных структурах.
Признаки эпидурального абсцесса проявляются слабо в виде парестезии (ощущение лёгкого покалывания иголкой), или небольшой общей слабости всего организма. Для выявления и диагностирования заболевания необходимо проведение ряда процедур, включающих в себя: общий осмотр спины, позволяющий определить наличие асимметрии, паравертебрального отёка и болезненности позвонков; исследование общего неврологического статуса. Кроме того, большое значение в диагностике эпидурального абсцесса, как и при других инфекциях позвоночника, имеет исследование анализа крови, в частности, показатель СОЭ.
К сожалению, проведение рентгенологического исследования не даёт полной картины заболевания, ввиду малой информативности обычной рентгенограммы. К современным методам исследования, позволяющим более точно диагностировать заболевание и выбрать необходимую тактику лечения, является метод магнитно-резонансной томографии. Исследование с применением МРТ даёт возможность установить, как наличие сдавливания спинного мозга, а также его состояние, так и определить присутствие абсцесса.
Кроме этого, МРТ помогает выявить возможные сопутствующие заболевания, в частности, остеомиелит, а также даёт возможность исключить образование паравертебрального набора жидкости. Наличие у человека устойчивых болей в спине, высокой температуры тела, повышение уровня лейкоцитов в крови, а также повышение неврологического дефицита, могут быть показаниями к операционному вмешательству с целью декомпрессии спинного мозга.
В послеоперационный период необходимо уделять большое внимание профилактике возникновения послеоперационных инфекций. Любая операция несёт с собой значительные нагрузки на организм пациента, его иммунитет. В послеоперационных период возрастает риск возникновения и развития различных инфекций, связанных как с общим ослаблением организма, так и с применением различного рода имплантатов, вживляемых в организм пациента, а также использование разнообразных фиксаторов, применение которых направленного на скорейшее заживление и выздоровление.
Так, с одной стороны, очевидна польза жёсткой фиксации позвоночника в послеоперационных период при помощи специальных фиксаторов, изготовленных из различных металлов, применение которых даёт возможность ускорить процесс заживления, восстановления и уменьшает внешнюю иммобилизацию (фиксацию). С другой стороны, частота использования имплантат и особых металлизированных фиксаторов неизбежно приводит к росту числа послеоперационных инфекций, что является одной из важных проблем при проведении операций на позвоночнике. К симптомам послеоперационной инфекции относятся: высокую температуру, наличие отёчности вокруг раны, гематому, повышение СОЭ и количество лейкоцитов в крови, боль в области раны, а также выделения из раны.
При наличии данных симптомов проводятся дополнительные исследования, в том числе, повторное оперативное вмешательство с целью выявления и устранения очага инфекции. При проведении оперативного вмешательства для устранения причин инфекции проводится санация раны, в случае необходимости производится замена или удаление имплантат. В послеоперационный период применяются различные виды антибиотиков и иные лекарственные препараты. Проведение повторного хирургического вмешательства несёт с собой дополнительные затраты, а также связано с увеличением общего периода выздоровления, но даёт нужный положительный эффект.
Инфекции позвоночника или спинальные инфекции — это острое или хроническое инфицирование элементов опорно-двигательного аппарата. Могут развиваться как самостоятельное заболевание, так и стать осложнением уже перенесённой патологии в организме. Сегодня болезни встречаются крайне редко, но в любом случае проходят в тяжёлой стадии и требуют немедленного вмешательства специалистов. В группе риска находятся люди любого возраста, пола, образа жизни, но больше всего поражению подвержены пациенты с патологическими расстройствами, вредными привычками и слабым иммунитетом. Чтобы вылечить недуг, следует обращаться к врачу-неврологу, нейрохирургу, инфекционисту, генетику и прочим специалистам узкого профиля.
Симптомы инфекций позвоночника
Большинство инфекционных процессов в позвоночном столбе, спинном мозге и околопозвоночных тканях имеют симптомы, характерные одновременно для других заболеваний. Именно поэтому при появлении первых признаков необходимо сразу пройти обследования, чтобы не спровоцировать осложнения. На какие симптомы нужно обратить внимание:
- сильная боль в области спины без видимых причин, которая выражается в различных формах силы, периодичности и продолжительности;
- повышенная температура тела без наличия простуды или воспаления, при острых стадиях — повышение до 40 градусов;
- общая слабость, упадок сил, быстрая утомляемость, сонливость, вялое состояние;
- припухлость, покраснение, покалывание или онемение некоторых участков кожи на спине;
- в запущенных случаях — неконтролируемое мочеиспускание, судороги, параличи.
Причины
Источником спинальной инфекции могут стать различные причины:
- перенесённые хирургические операции и пункции в области позвоночника;
- последствия межпозвоночной грыжи, патологии позвонков и дисков;
- послеоперационные осложнения;
- травмирование с тяжёлыми последствиями;
- недостаточная реабилитация после травм и операций;
- стеноз позвоночного канала;
- нарушения обменных процессов, ожирение;
- расстройства эндокринной системы;
- недостаток или избыток питания;
- алкоголизм, наркомания, курение;
- артриты и ревматоидные болезни;
- трансплантация внутренних органов;
- онкология, ВИЧ-инфекции;
- радиационное облучение;
- заражение крови при переливании;
- урологические инвазивные процедуры;
- инфекционные заболевания в анамнезе;
- генетическая предрасположенность.
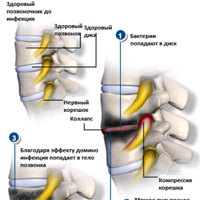
Стадии развития спинальных инфекций
Инфекционные поражения опорно-двигательного аппарата развиваются в определённой последовательности и проходят в 3 стадии:
- Первая. Попадание инфекционных бактерий в мягкие ткани позвоночника (например, диск). Происходит компрессия нервных корешков, дисковые ткани стираются, повреждаются фиброзное кольцо и пульпозное ядро.
- Вторая. Распространение инфекции в кости позвонка. При поражении фиброзное кольцо и мягкое ядро ослабевают, что вызывает проседание и инфицирование диска. Ослабленные твёрдые ткани начинают распадаться.
- Третья. Разрушение инфицированных костей. Происходят дегенеративно-дистрофические процессы, которые провоцируют полное разрушение костных тканей и сращение двух дисков (верхнего и нижнего).
Разновидности
Существует огромное количество видов инфекционных заболеваний позвоночника, которые отличаются по локации поражения, симптомам, причинам и способам лечения. Большинство патологий врачи разделяют на категории:
- гнойные;
- негнойные;
- спонтанные;
- послеоперационные;
- эпидуральный абсцесс.
Инфекционная патология межпозвонковых дисков, которая может сочетаться с воспалениями. Сопровождается сильным болевым синдромом и ограничением двигательных функций спины. Выявить нарушения можно на рентгене или МРТ. Наблюдается чаще у детей и подростков.
Происхождение патологии может быть бактериальным или грибковым, возбудитель инфекции поражает позвонковые кости. Развивается как самостоятельное или вторичное заболевания. От начальной до развитой стадии обычно проходит 4-8 месяцев. Проявляется спинальной болью мощной интенсивности, высокой температурой тела, увеличенным уровнем лейкоцитов в крови. В запущенных случаях наблюдаются неврологические отклонения.
Представляет собой гнойное воспаление костной спинномозговой оболочки. Скопления гноя постепенно увеличиваются и вызывают компрессию нервных корешков спинного мозга. Возможно разрушение не только нервных волокон, но и окружающих мягких тканей. Характеризуется отёчностью спины, покраснениями и припухлостью кожи в месте поражения.
Чаще возникают при установке металлических вспомогательных фиксаторов — инородное тело служит внутренним раздражителем и провоцирует формирование инфекций. Характерные признаки — острая боль после реабилитации, выделения жидкости разной консистенции из мест хирургических разрезов, развитие гематом, отёков и воспалений.
Бывают двух типов:
- Туберкулёзный. Возникает чаще в грудном отделе позвоночника, может распространяться на соседние сегменты (поясницу, шею). Сопровождается нестабильностью спины, смещением позвонков, инфицированием элементов связочного аппарата.
- Бруцеллёзный. Источник заражения — животные с острыми инфекциями. Первые 1-2 месяца протекают бессимптомно, после чего резко возникает лихорадка, высыпания на коже, гнойные процессы в мышцах, связках, костях и суставах.
Диагностика
- Лабораторные анализы крови на определение уровня лейкоцитов и скорости оседания эритроцитов, бактериальный посев для выявления возбудителя и изучения стафилококка.
- Рентгенография проводится для визуализации костей, хрящей и суставов, а также изучения их состояния, расположения и поиска повреждений (деструкции, эрозии, смещения).
- КТ и МРТ выполняют по-отдельности или комбинируют для получения максимально точных результатов.
Вы можете обследовать позвоночник на наличие спинальных инфекций в сети клиник ЦМРТ:
(1) Санкт-Перербургский НИИ фтизиопульмонологии; Северо-Западный государственный медицинский университет им. И.И.Мечникова
(2) Городская многопрофильная больница №2, Санкт-Петербург
Локальный мониторинг структуры возбудителей и их чувствительности к антибиотикам на уровне стационаров и его верификация при пункционной биопсии является основой для выбора рациональной эмпирической терапии в лечении неспецифического остеомиелита позвоночника (НОП). Анализ хирургического лечения 196 пациентов с НОП показал, что в посевах преобладала грамположительная микрофлора (75,2%), из которых в 57,3% (51 пациент) верифицированы различные штаммы стафилококков. У 11 пациентов выявлены штаммы MRSA. В 6 случаях входными воротами стафилококковой бактериемии являлся подключичный катетер. Госпитальные штаммы MRSA характеризовались полирезистентностью.
Ключевые слова: метициллин-резистентный стафилококк, спондилит, неспецифический остеомиелит позвоночника, антибиотикотерапия.
Сведения об авторе:
Вишневский А.А. – д.м.н., руководитель отдела фтизиовертебрологии, С.-Пб НИИ фтизоиопульмонологии
Nonspecific Osteomyelitis of the Spine Caused by Methicillin-resistant Staphylococcus: Rational Antibiotic Treatment
A.A. Vishnevsky (1), S.V. Babak (2)
(1) St-Petersburg SRC for Phthisiopneumology, and I.I.Mechnikov North-West State Medicine University, St.Petersburg
(2) City Multihospital №2, St.Petersburg
Monitoring of pathogens types and their antibiotics resistance at a hospital level, as well as pathogens verifying after needle biopsy is the basis for the treatment of non-specific osteomyelitis of the spine (NOS). Data gained from 196 surgical inpatients with NOP showed that Gram-positive pathogens (75,2% of all cases) prevailed in crops, among them there were 57.3% various strains of staphylococci (51 patients). In 11 patients (12,3% of all cases) MRSA strains revealed. In 6 cases a gateway for staphylococcal bacteremia was subclavian catheter. Nosocomial MRSA strains were characterized by polyresistance.
Keywords: methicillin-resistant staphylococcus, spondylitis, nonspecific osteomyelitis of the spine, antibiotic treatment.
Проблема выбора рациональной антибиотикотерапии (АБТ) при хирургических инфекциях, и в частности, при cпондилитах имеет не только медицинское, но и важное экономическое значение. Прежде всего, это определяется большими финансовыми затратами, обусловленными резистентными формами микроорганизмов. В бактериологических исследованиях послеоперационного материала при хирургическом лечении неспецифического остеомиелита позвоночника (НОП) в 70–80% случаев выявляют грамположительную микрофлору, которая более чем в половине случаев представлена различными штаммами золотистого стафилококка [1–3].
Рациональное применение антибиотиков имеет исключительное значение для хирургии, поскольку подразумевает не только получение хорошего результата при профилактике хирургической инфекции, но и при лечении уже развившейся нозокомиальной инфекции (НИ). На основании многочисленных исследований установлено, что в 40–60% случаев стартовая эмпирическая антибактериальная терапия НИ является неадекватной [4, 5]. В большинстве случаев это объясняется полирезистентностью микрофлоры [6, 7]. В частности, в 8,0–12,3% всех случаев НИ выявляются госпитальные штаммы золотистого стафилококка, которые характеризуются тем, что они нечувствительные ко всему классу бета-лактамов, включая карбапенемы [8–10].
В последние годы ВОЗ были разработаны специальные рекомендации, которым должны соответствовать препараты, применяемые для лечения инфекций: эффективность препарата не менее 95%, доступная цена, хорошая переносимость и малая токсичность, возможность однократного применения, пероральный прием, медленное развитие резистентности микроорганизмов к средствам терапии [1]. При этом подразумевается и снижение расходов на антибиотикотерапию, являющейся одной из самых затратных видов фармакотерапии в [12].
Таким образом, трудность терапии заболеваний, вызванных резистентными штаммами стафилококков, в первую очередь – MRSA, связана с ограничением выбора эффективных антибиотиков, а неадекватный эмпирический режим антибактериальной терапии существенно ухудшает прогноз, увеличивает длительность госпитализации и стоимость лечения.
Материал и методы
В период с 1995 по 2012 гг. в Санкт-Петербургском Центре хирургии позвоночника (Городская многопрофильная больница №2) и СПб НИИ фтизиопульмонологии было пролечено 196 больных НОП. Диагноз НОП у всех больных был верифицирован при гистологическом и бактериологическом исследованиях. Верификацию возбудителя проводили по методике культурологического типирования и определения чувствительности микроорганизма к антибиотику с применением дисков Научно-исследовательского центра фармакотерапии (С.-Петербург) и дисков фирмы Bristol Myers Squibb (Англия).
Результаты бактериологического исследования посевов крови позволили обнаружить микрофлору у 64 (32,6%) пациентов. При посевах крови и послеоперационного материала лишь у 89 (45,4%) больного верифицирована микрофлора. В посевах преобладала грамположительная флора – у 67 (75,2%) больного, у 22 (24,8%) пациентов выявлена грамотрицательная микрофлора (кишечная палочка, синегнойная палочка, протей, клебсиелла и т.д.). Среди грамположительных микроорганизмов у 51 (57,3%) пациентов верифицированы различные штаммы стафилококков. У 11 (12,3%) пациентов выявлены MRSA штаммы.
Проведенный анализ материала показал, что у штаммов Staphylococcus aureus отсутствует чувствительность к природным и полусинтетическим пенициллинам, а также к цефалоспориновым актибиотикам III–IV поколений (цефипим, цефатоксим). В то время, сохраняется умеренная чувствительность к цефлоспоринам I–II поколения (цефазолину, цефамандолу, цефуроксиму) и в 50–70% случаев сохраняется чувствительность к гликопептидам (ванкомицин) и карбапенемам (меронем, имепинем) (табл. 1.). Эти данные согласуются с результатами исследования С.В.Яковлева [9], который показал, что чувствительность госпитальных штаммов S.aureus к оксациллину составляет 67%, к линкомицину – 56%, к ципрофлоксацину – 50%.
При неизвестном возбудителе все пациенты в качестве стартовой терапии в течении 2-х недель получали стартовую антибикотикотерапию (цефалоспориновые антибиотики I–II поколения в сочетании с аминогликозидами) [9]. В дальнейшем, в соответствии с полученными результатами посевов крови и биопсии, пациенты были разбиты на 2 группы. В первую группу (I) вошли пациенты (n=40), у которых был были выявлены микроорганизмы с широкий спектром чувствительности к антибиотикам. В качестве этиотропной терапии были использованы оксациллин или цефалоспориновые антибиотики. При выявлении резистентных штаммов стафилококка у 11 пациентов (II группа) были использованы гликопептиды (ванкомицин, линезолид, тейкопланин), карбапенемы (имипенем, меронем) или рифампицин в сочтеании с ко-тримоксазолом. Курс антибиотикотерапии был не менее 6–8 недель, поскольку при коротких курсах (до 2–3х недель) рецидивы заболевания возникают в 19–25% случаев [13, 14].
Своевременное назначение антибиотикотерапии дает лучшие результаты и позволяет в начальной стадии затормозить развитие НОП и снижает риск развития септического шока. Клиническая эффективность действия антибиотика проявляется снижением температуры тела, уменьшением выраженности болевого синдрома, как правило, на 2–3 сутки после назначения. Однако ориентироваться только на клинические признаки не следует. Целесообразно оценивать выраженность системного воспалительного ответа, определять концентрацию антибиотика в крови пациента [1, 2].
Затраты на АБТ разделяли на прямые и непрямые. Прямые затраты подразделяли на медицинские и немедицинские. При расчете прямых медицинских затрат были учтены следующие расходы, связанные с оказанием медицинской помощи:
1. Стоимость основной антибактериальной терапии.
2. Стоимость дополнительной антибактериальной терапии, назначенной в связи с неэффективностью основной антибактериальной терапии.
3. Стоимость пребывания пациента в стационаре рассчитывалась как стоимость пребывания пациента в специализированном отделении, умноженная на среднее количество суток, в течение которых пациенты каждой подгруппы в нем находились.
Стоимость пребывания пациентов в отделении и в палате интенсивной терапии была взята из тарифов Спб НИИФ (соответственно 1000 и 9000 руб. в сутки). Средний срок пребывания пациентов в стационаре для I группы составил 37,2±2,4 дня, для II – 57,1± 5,6 дня, для III – 54,4±2,8 дня. В данном исследовании стоимость оперативного вмешательства не учитывалась. Анализ прямых немедицинских затрат не проводился, т.к. все включенные в исследование пациенты с документированным диагнозом спондилит находились в отделении по поводу основного заболевания и прямые немедицинские затраты (транспортирование пациента в ЛПУ, спецодежда, питание, лабораторные материалы и др.) были приняты как одинаковые для обеих групп. Анализ непрямых затрат не проводился, т.к. протокол клинического исследования не предполагал сбор информации о социальном статусе пациентов и не представлялось возможным оценить затраты на оплату больничных листов, стоимость производственных потерь и т.д. (табл. 2).
Результаты исследования и обсуждение
В настоящее время нет оптимального антибиотика для стартовой терапии НОП, но с учетом преобладания грамположительной флоры для выбора эмпирической антибиотикотерапии пациенты в течении 2-х недель получали антибиотики широкого спектра действия (комбинация оксациллина, цефалоспоринов 1-го поколения или ингибиторозащищенных пенициллинов в сочетании с аминогликозидами). Таким образом, средние затраты на антибиотикотерапию до выявления возбудителя (2-недельный курс) составили от 1220 руб. (при комбинации оксациллина и гентамицина) до 3880 руб. (при сочетании ципрофлоксацина и гентамицина).
При выявлении резистентных штаммов стафилококка (II группа) предпочтительно использовать гликопептиды (ванкомицин, линезолид, тейкопланин), карбапенемы (имипенем, меронем) или циклические липопептиды (даптомицин). Менее затратным было использование рифампицина (0,45–0,9 г в сутки) в сочетании с ко-тримоксазолом. Использовать рифампицин в качестве монотерапии нельзя в силу того, что к нему быстро развивается устойчивость. Месячный курс антибиотикотерапии во II группе составлял от 15600 до 168 000 руб. (табл. 3.).
С целью оптимизации антибиотикотерапии при лечении НОП необходимо придерживаться следующих принципов выбора препарата:
- определение спектра антимикробной активности препарата in vitro;
- доказанная эффективность в контролируемых клинических исследованиях;
- определение способа введения препарата и его кратности;
- безопасность и отсутствие токсичности препарата;
- фармакоэкономическая обоснованность применения препарата.
Таким образом, при выборе эмпирической антибиотикотерапии при НОП следует ориентироваться на спектр потенциального возбудителя, учитывать первичные данные микробиологического исследования (посевы крови и материала свищевого содержимого), уровень эндотоксемии, тяжесть состояния пациента (по шкалам SAPS, APACHE). Кроме того, при выборе той или иной схемы антибактериальной терапии необходимо учитывать не только механизм действия препаратов, их групповую характеристику, но и особенности взаимодействия лекарственных средств между собой, а также особенности чувствительности микрофлоры в конкретном стационаре.
Мы не проводим операции на позвоночнике по поводу спондилита на фоне генерализованного септического состояния или при выраженном системном воспалительном ответе. В течение 2-3 недель необходима подготовка к операции, включающая дезинтоксикационную терапию, экстракорпоральную детоксикацию, рациональную антибиотикотерапию и т.д. Эти мероприятия позволили исключить возможные осложнения и летальные исходы при операциях.
Читайте также:


