Эукариот или прокариот золотистый стафилококк
В мае этого года в работе "Mitochondria-targeted antioxidants as highly effective antibiotics", опубликованной в журнале Scientific Reports, коллектив авторов из МГУ впервые показал принципиально новый гибридный антибиотик: его действие направлено против мембранного потенциала бактерий, который обеспечивает болезнетворные клетки энергией.
Победа! — но только временная
В середине прошлого столетия человечество находилось в состоянии эйфории, связанной с невероятными успехами в лечении инфекционных заболеваний бактериальной природы. Многие бактериальные инфекции, вызывавшие ужасающие по количеству жертв эпидемии в средние века, превратились в карантинные инфекции, которые легко и эффективно вылечивались.
Этот успех стал возможен после открытия в 1920-х годах британским бактериологом Александром Флемингом первого антибиотика — пенициллина; он обнаружился в плесневых грибах Penicillium notatum . Спустя десятилетие британские ученые Говард Флори и Эрнст Чейн предложили способ промышленного производства чистого пенициллина. Все трое в 1945 году были удостоены Нобелевской премии в области физиологии и медицины.
Массовое производство пенициллина было налажено во время Второй мировой войны, что вызвало резкое уменьшение смертности среди солдат, обычно умиравших от раневых инфекций. Это позволило французским газетам накануне визита Флеминга в Париж писать, что для разгрома фашизма и освобождения Франции он сделал больше целых дивизий.
Углубление знаний о бактериях привело к появлению большого числа антибиотиков, разнообразных по механизму, широте спектра действия и химическим свойствам. Почти все бактериальные заболевания либо полностью вылечивались, либо серьезно подавлялись антибиотиками. Люди полагали, что человек победил бактериальные инфекции.
Мелкие очаги сопротивления — и поражение
Одновременно с успехами появились и первые признаки грядущей глобальной проблемы: случаи бактериального сопротивления антибиотикам. Прежде безропотно чувствительные к ним микроорганизмы вдруг становились индифферентны. Человечество ответило бурным развитием исследований и новыми антибиотиками, это привело лишь к увеличению числа препаратов и новой резистентности бактерий.
В мае 2015 года Всемирная организация здравоохранения признала кризисом бактериальное сопротивление антибиотикам и выдвинула Глобальный план борьбы с устойчивостью к противомикробным препаратам. Его следовало выполнить безотлагательно, свои действия должны были координировать многочисленные международные организации вроде защитников окружающей среды, и отрасли экономики — не только человеческая медицина, но и ветеринария, и промышленное животноводство, и финансовые институты, и общества защиты прав потребителей.
План, должно быть, так или иначе выполняется, но к несчастью, несмотря на это уже в сентябре 2016 года одна американская пациентка умерла от сепсиса. Такое бывает, и даже чаще, чем хотелось бы, но ее погубила так называемая супербактерия — Klebsiella pneumoniae , но не обычная, а устойчивая ко всем разрешенным в США 26 антибиотикам, в том числе к антибиотику "последнего резерва" колистину.
Итак, ученым стало очевидно, что бактериальные инфекции побеждают человечество, и современная медицина может быть отброшена во времена, предшествовавшие открытию антибиотиков. Одним из главных вопросов, поднятых на международной конференции ASM Microbe , проводившейся в Новом Орлеане в июне 2017 года Американским обществом микробиологов, был такой: "Может ли человечество выиграть войну с микробами?". На той же конференции, кстати, отдельного внимания удостоилось движение antimicrobial stewardship, или управление антибиотикотерапией, которое имеет своей целью максимально разумно и достаточно, в соответствии с рекомендациями доказательной медицины, назначать антибиотики. Пока что законом такое обращение с антибиотиками стало только в одном месте в мире — в штате Калифорния, США.
Стало очевидным, что бактериальные инфекции побеждают человечество, и современная медицина может быть отброшена на уровень, предшествующий открытию антибиотиков
Как работает помпа
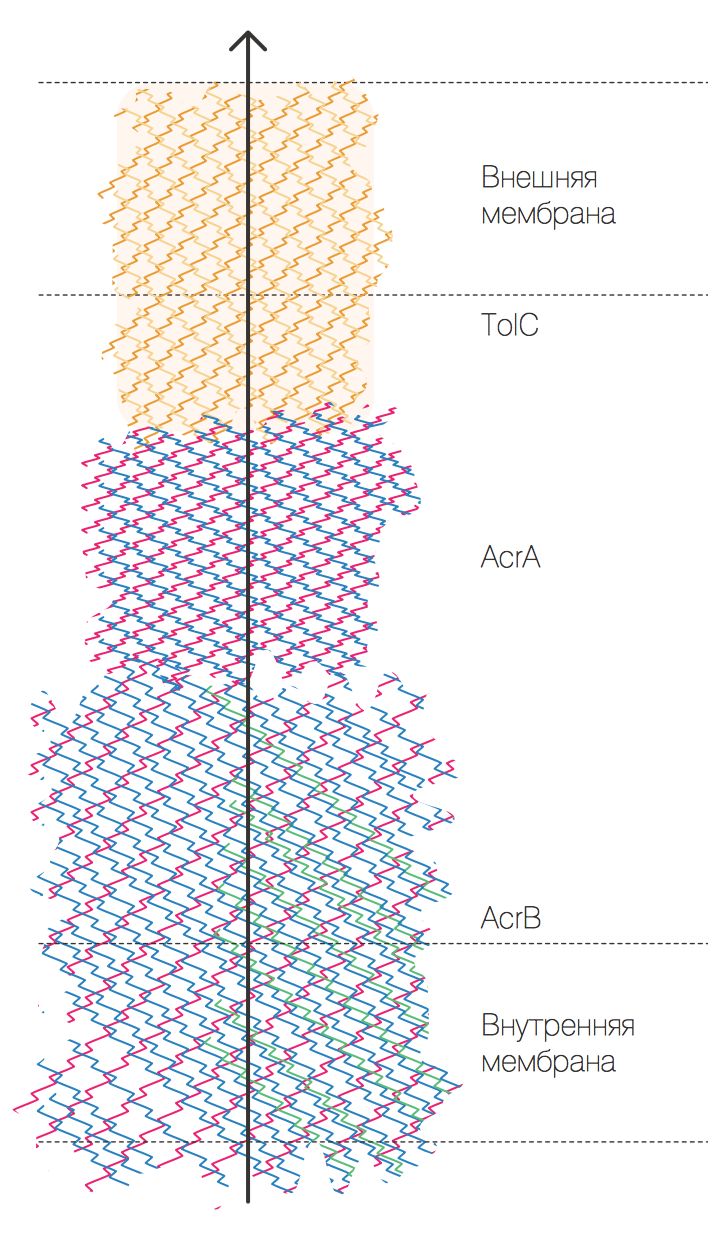
Действие помпы можно проиллюстрировать на примере основной помпы множественной лекарственной устойчивости кишечной палочки — AcrAB-TolC . Эта помпа состоит из трех основных компонентов: (1) белка внутренней клеточной мембраны AcrB , который за счет мембранного потенциала может перемещать вещества через внутреннюю мембрану (2) адаптерного белка AcrA , связывающего транспортер AcrB с (3) каналом на внешней мембране TolC . Точный механизм работы помпы остается недостаточно изученным, однако известно, что вещество, которое помпа должна выбросить за пределы клетки, попадает на внутреннюю мембрану, где его ждет транспортер AcrB , связывается с активным центром помпы и затем за счет энергии встречного движения протона выкачивается за пределы наружной мембраны бактерии.
Антиоксиданты направляются в митохондрию
Но решение, обходящее резистентность бактерий, можно считать, найдено — российскими учеными. В мае этого года в работе " Mitochondria-targeted antioxidants as highly effective antibiotics ", опубликованной в журнале Scientific Reports, коллектив авторов из МГУ впервые показал принципиально новый гибридный антибиотик широкого спектра действия — митохондриально направленный антиоксидант.
Митохондриально направленные антиоксиданты (МНА) получили широкое распространение не только как инструмент исследований роли митохондрий в разных физиологических процессах, но и как терапевтические средства. Это конъюгаты, то есть соединения, состоящие из какого-либо хорошо известного антиоксиданта (пластохинона, убихинона, витамина Е, ресвератрола) и проникающего, то есть способного преодолеть мембрану клетки или митохондрии, катиона (трифенилфосфония, родамина и др.).
Механизм действия МНА доподлинно не известен. Известно лишь, что в митохондрии они частично разобщают окислительное фосфорилирование, метаболический путь синтеза универсального клеточного горючего — аденозинтрифосфата, АТФ, что стимулирует клеточное дыхание и снижает мембранный потенциал и может приводить к защитному эффекту при окислительном стрессе.
Предположительно это выглядит так. МНА из-за своей липофильности (тяги к липидам или сродства с ними) связываются с мембраной митохондрии и постепенно мигрируют внутрь митохондрии, где, видимо, соединяются с отрицательно заряженным остатком жирной кислоты; составив комплекс, они теряют заряд и вновь оказываются снаружи мембраны митохондрии. Там остаток жирной кислоты захватывает протон, из-за чего комплекс распадается. Захватившая протон жирная кислота переносится в обратном направлении — и внутри митохондрии теряет протон, то есть, проще говоря, переносит его в митохондрию, отчего как раз и снижается мембранный потенциал.
Один из первых МНА был создан на основе трифенилфосфония в Оксфорде — английским биологом Майклом Мерфи; это был конъюгат с убихиноном (или коферментом Q , принимающим участие в окислительном фосфорилировании). Под названием MitoQ этот антиоксидант получил значительную известность как перспективный препарат для замедления старения кожи, а также как возможное средство защиты печени при гепатитах и жировом ее перерождении.
Позднее тем же путем пошла группа академика Владимира Скулачева из МГУ: на основе конъюгата трифенилфосфония с антиоксидантом пластохиноном (участвует в фотосинтезе) был создан эффективный SkQ1 .
В соответствии с симбиотической теорией происхождения митохондрий, выдвинутой членом-корреспондентом АН СССР Борисом Михайловичем Козо-Полянским в 1920-х годах и американским биологом Линн Маргулис в 1960-х годах, между митохондриями и бактериями — много общего, и можно ожидать, что МНА будут воздействовать на бактерии. Однако несмотря на очевидную схожесть бактерий и митохондрий и десятилетний опыт работы с МНА во всем мире никакие попытки обнаружить антимикробное действие МНА не приводили к положительным результатам.
Последний рубеж пал
Колистин считается антибиотиком последнего резерва — это старый препарат из класса полимиксинов, вышедший из употребления из-за своего токсического воздействия на почки. Когда обнаружились супербактерии, которые, кроме того что сами сопротивлялись известным антибиотикам, еще и обзавелись способностью передавать друг другу генную информацию, позволяющую сопротивляться антибиотикам, выяснилось, что во-первых, колистин губителен для всех этих бактерий, а во-вторых, бактерии не могут обмениваться генами резистентности к колистину, если вдруг таковая все-таки возникнет.
Увы, но в мае 2016 года в американское Хранилище мультирезистентных микроорганизмов, которое находится в структуре Исследовательского института имени Уолтера Рида (это структура армии США), поступила-таки бактерия, которая не просто была индифферентна к колистину, но еще и оказалась способна передавать генную информацию с этой резистентностью другим бактериям. Первый такой микроорганизм еще в 2015 году был зафиксирован в Китае, долгое время была надежда, что это единичный случай, но она не оправдалась. Особенно печально, что в США этим микроорганизмом оказалась всем хорошо знакомая кишечная палочка.
Загадка двух палочек
Прорыв случился в 2015 году: впервые антибактериальное действие МНА на примере SkQ1 было показано в работе "Разобщающее и токсическое действие алкил-трифенилфосфониевых катионов на митохондрии и бактерии Bacillus subtilis в зависимости от длины алкильного фрагмента" — ее опубликовал журнал "Биохимия" в декабре 2015 года. Но то было описанием феномена: эффект наблюдался при работе с сенной палочкой ( Bacillus subtilis ) и не наблюдался при работе с палочкой кишечной ( Escherichia coli ).
Но дальнейшие исследования, которые легли в основу новейшей работы, опубликованной в журнале Scientific Reports , показали, что МНА SkQ1 — высокоэффективный антибактериальный агент в отношении широкого спектра грамположительных бактерий. SkQ1 эффективно подавляет рост таких надоедливых бактерий, как золотистый стафилококк ( Staphylococcus aureus ) — один из четырех наиболее частых видов микроорганизмов, вызывающих внутрибольничные инфекции. Так же эффективно SkQ1 подавляет рост микобактерий, в том числе палочки Коха ( Mycobacterium tuberculosis ). Более того, МНА SkQ1 оказался высокоэффективным средством против грамотрицательных бактерий, таких как Photobacterium phosphoreum и Rhodobacter sphaeroides .
И только в отношении кишечной палочки он был крайне неэффективен, а ведь именно Escherichia coli — та бактерия, которую микробиологи используют как модельный организм, что и было, по-видимому, причиной неудачных попыток ранее обнаружить антимикробное действие МНА.
Естественно, исключительная резистентность кишечной палочки вызвала весьма сильный интерес исследователей. К счастью, современная микробиология сделала большой шаг вперед в методологическом аспекте, и у ученых созданы целые коллекции микроорганизмов с делециями (отсутствием) некоторых генов, не вызывающими их гибель. Одна из таких коллекций — делеционных мутантов кишечной палочки — находится в распоряжении МГУ.
Исследователи высказали предположение, что резистентность может быть обусловлена работой какой-либо из помп множественной лекарственной устойчивости, имеющихся у кишечной палочки. Любая помпа плоха для инфицированного человека тем, что просто выбрасывает из бактериальной клетки антибиотик, он на нее не успевает подействовать.
Генов, отвечающих за действие помп множественной лекарственной устойчивости, у кишечной палочки много, и было решено начать анализ с продуктов генов, входящих в состав сразу нескольких помп,— а именно белка TolC .
Белок TolC — канал на внешней мембране грамотрицательных бактерий, он служит внешней частью для нескольких помп множественной лекарственной устойчивости.
Анализ делеционного мутанта (то есть палочки без белка TolC ) показал, что его резистентность снизилась на два порядка и стала неотличима от резистентности грамположительных бактерий и нерезистентных грамотрицательных бактерий. Таким образом, можно было заключить, что выдающаяся резистентность кишечной палочки — результат работы одной из помп множественной лекарственной устойчивости, имеющих в составе белок TolC . А дальнейший анализ делеционных мутантов по белкам — компонентам помп множественной лекарственной устойчивости показал, что только помпа AcrAB-TolC участвует в откачке SkQ1 .
Резистентность, вызванная наличием помпы AcrAB-TolC, не выглядит непреодолимой преградой: антиоксидантный конъюгат SkQ1 — также уникальное для этой помпы вещество, очевидно, можно будет найти для нее ингибитор.
В мае 2015 года Всемирная организация здравоохранения (ВОЗ) выдвинула Глобальный план действий по борьбе с устойчивостью к противомикробным препаратам, признав бактериальное сопротивление антибиотикотерапии кризисом
Бессмертие Генриетты Лакс

Линия "бессмертных" клеток HeLa получила свое название по имени негритянки Генриетты Лакс (Henrietta Lacs). Клетки были получены из раковой опухоли ее шейки матки, без ее ведома и тем более согласия в феврале 1951 года Джорджем Гаем, врачом-исследователем питтсбургской университетской больницы имени Джона Хопкинса. Генриетта Лакс умерла в октябре того же года, а доктор Гай выделил одну конкретную клетку из эндотелия ее матки и начал с нее клеточную линию. Вскоре он обнаружил, что это уникально живучая культура, и начал делиться ею с исследователями по всему миру. Клетки, произошедшие от Генриетты Лакс, помогли человечеству при создании вакцины от полиомиелита, при определении числа хромосом в человеческой клетке (46), при первом клонировании человеческой клетки, наконец, при экспериментах с экстракорпоральным оплодотворением.
Надо сказать, что происхождение клеток Джордж Гай держал в тайне — оно стало известно только после его смерти.
Не только лечить, но и чинить
Но чтобы называться антибиотиком, SkQ1 необходимо соответствовать множеству критериев, таких как (1) способность подавлять жизненные процессы микроорганизмов в малых концентрациях и (2) мало повреждать или вовсе не повреждать клетки человека и животных. Сравнение SkQ1 c известными антибиотиками — канамицином, хлорамфениколом, ампициллином, ципрофлоксацином, ванкомицином и пр.— показало, что SkQ1 действует на бактерии в таких же, как они, или даже более низких концентрациях. Более того, при сравнительном исследовании действия SkQ1 на культуру клеток человека линии HeLa выяснилось, что в минимальной бактерицидной концентрации SkQ1 не оказывает практически никакого воздействия на клетки человека — а замечают клетки SkQ1 , когда концентрация антиоксидантного конъюгата становится более чем на порядок выше необходимой для бактерицидного действия.
Механизм действия SkQ1 на бактерии оказался подобен действию МНА на митохондрии, однако общее действие на прокариотическую и эукариотическую клетку различалось. Одна из главных причин — пространственное разделение процессов генерации энергии (исключая субстратное фосфорилирование) и процессов транспорта веществ внутрь клетки, что, по-видимому, представляет собой существенное эволюционное преимущество, которое часто обходят вниманием при рассмотрении выгод от сожительства протомитохондрии и протоэукариота. Так как у бактерий генерация энергии и транспорт локализованы на клеточной мембране, то падение потенциала вызывает, по-видимому, остановку сразу обоих процессов, что приводит к смерти микроорганизма. В эукариотической клетке процессы транспорта веществ внутрь клетки локализованы на клеточной мембране, а генерация энергии происходит в митохондриях, что позволяет эукариотической клетке выживать при летальных для бактерий концентрациях МНА. Кроме того, разность потенциала на мембране бактерии и эукариотической клетки различается в пользу бактерий — и это тот самый дополнительный фактор, аккумулирующий МНА на мембране бактерий.
Рассматривая механизм действия SkQ1 на бактерии, нельзя пройти мимо другого уникального свойства этого МНА — способности лечения поврежденных бактериями эукариотических клеток за счет антиоксидантных свойств. SkQ1 , действуя как антиоксидант, снижает уровень вредных активных форм кислорода, образующихся при воспалении, вызванном бактериальной инфекцией.
Таким образом, SkQ1 может быть признан уникальным гибридным антибиотиком широчайшего спектра действия. Дальнейшая разработка антибиотиков на его основе может позволить переломить ход войны человечества против все более совершенных микробов.
Павел Назаров, кандидат биологических наук, НИИ Физико-химической биологии им. А.Н. Белозерского МГУ
Бактерии, как и протисты (более сложно устроенные микроорганизмы), состоят из одной клетки и являются самостоятельными жизнеспособными организмами. Хотя для них свойственно образовывать скопления — колонии, которые, кстати, вполне могут быть видны невооруженным глазом.
На фото чашка Петри с разросшимися на ней бактериями, собранные мной на одной из станций Питерского метро.
Бактерии не имеют оформленного ядра и органелл, которые выполняли бы все функции (аналог наших органов, если можно так выразиться). Их еще называют прокариотами (доядерными организмами), а тех, кто имеет ядра — эукариотами (к которым относимся и мы).
Все, из чего состоит бактерия:
— протопласт — цитоплазма (все внутренне содержимое клетки) и покрывающая сверху мембрана
— клеточная стенка, вокруг которой может быть слизистый чехол и/или капсула
— могут быть жгутики для передвижения
Так вот, антибиотики — вещества, обладающие бактерицидной активностью. Как было сказано выше, от вирусов они не помогут, как и от простейших. Но это скорее исключение.
Теперь же давайте разбираться, почему они действуют именно на бактерии и как именно.
- Самый первый из изученных — воздействие на клеточную стенку.
По своему химическому составу клеточная стенка бактерий отличается от клеточной стенки эукариот. Основной компонент — муреин, который образует на поверхности муреиновую сеть.
Датский микробиолог Ганс Грам предложил способ окраски мазков бактерий, названный потом в его честь. Мазок окрашивался генцианвиолетом (краситель) и закрепляется раствором иода. Дальше уже бактерии ведут себя по-разному, из-за чего их разделили на две группы: те, у кого краситель удерживается в клетке при обработке спиртом или ацетоном (грамположительные), и те, кто обесцвечиваются (грамотрицательные).
Staphylococcus aureus — золотистый стафилококк (грамположительные кокки, темные) и Escherichia coli — кишечная палочка (грамотрицательные бациллы, розовые).
Утомлять всякими дополнительными особенностями строения стенки я не буду, это и так очевидно из картинки внизу.
Стенка выполняет барьерную функцию и устанавливает контакт бактерии с окружающей средой. Грамотрицательные бактерии — более высокая ступень эволюции, они более устойчивы в токсинам, в том числе и антибиотикам, чем грамположительные, хотя те и имеют более толстую (и в то же время более уязвимую) стенку.
Некоторые антибиотики (группа пенициллина и циклосерина) подавляют синтез клеточной стенки, что приводит к образованию протопластов (см. выше) и сферопластов (клеточная стенка разрушена, но не до конца). При прекращении приема антибиотиков они снова реверсируют (превращаются) в нормальные клетки или трансформируются в L-формы, но могут и погибнуть.
L-формы не имеют клеточной стенки, но могут развиваться, расти и делиться. Образование L-форм — одна из причин хронических рецидивирующих заболеваний. При неправильном приеме антибиотиков состояние больного может улучшиться, но после полной отмены происходит реверсия до полноценных форм исходного вида с восстановлением их патогенности. Кстати, может еще и появиться иммунитет к этим антибиотикам, что значит, что при рецидиве они не помогут.
Чтобы понять, почему прием антибиотиков имеет ту или иную дозировку, по стоит посмотреть на этот график:
концентрация вначале всегда выше оптимальной, но со временем выводится из организма, поэтому необходимо принимать таблетки снова. И поэтому важно подобрать антибиотики, в которых их эффективность была бы сильнее или хотя бы на уровне с возможными рисками и побочными эффектами.
Именно таким способом антибиотики влияют на представителей крупозной и очаговой пневмонии, менингита, инфекций мочевыводящих и желчных путей, сифилиса, гонореи, дифтерии, скарлатины, ангины, ЛОР-заболеваний и многих других.
-
Другой механизм воздействия — нарушение синтеза белка в клетке: ингибирование (подавление) функций рибосом и синтеза белка (стрептомицин). Лечат туберкулез легких и других органов, бруцеллез, чума.
Нарушение целостности мембран, т. е. нарушение ионных каналов, что может сделать клетку проницаемой для веществ, которые внутрь попадать не должны, или наоборот — заблокировать доступ важных веществ. (грамицидин, полимиксин). Используют при заболеваниях желудочно-кишечного тракта, сепсиса, и, как и пенициллин, при менингите и ЛОР-заболеваниях.
Нарушение синтеза ДНК и РНК, но за счет нарушения самих азотистых оснований — компонентов непосредственно самих нуклеиновых кислот (саркомицин). Подавляет рост культуры клеток рака Эрлиха.
Теперь стоит обсудить такую вещь как антибиотикорезистентность, т. е. устойчивость микроорганизма к действию антибиотика. Может возникать из-за мутаций и после воздействия антибиотика закрепляться у всей группы организмов.
-
блокирование входа в клетку — дополнительная мембрана у большинства грамотрицательных бактерий, что делает их невосприимчивыми к пенициллину.
уменьшение размера пор (антибиотик не проходит внутрь) или появляется белок, который сразу же выводит антибиотик из клетки.
некоторые бактерии научились инактивировать антибиотики. Например, у стафилококков (р. Staphylococcus) вырабатывается для этого вещество β-лактоназа, которое разрушает β-лактамовое кольцо у большинства пенициллинов. Для этого в них добавляют фолиевую кислоту, чтобы подавлять β-лактоназу.
Напоследок стоит упомянуть, что тот факт, что антибиотики не влияю на вирусы, не означает, что они безвредны для человека. Их нельзя принимать просто так, не убедившись в том, что возбудитель болезни именно бактерия, потому что антибиотики влияют на печень (именно она занимается детоксикацией организма), кишечник (микрофлора погибает, и на ее месте может прижиться первое, что попадет). Так же то, что при лечение данной группы лекарств нельзя пить, знают все. Алкоголь влияет на активность антибиотиков и их выведение из организма печенью. Некоторые антибиотики могут взаимодействовать с алкоголем и вызывать побочные эффекты, начиная с поноса и рвоты и заканчивая судорогами и даже смертью.
Данный урок по биологии проводится на 1 курсе для обучающихся по специальности "Технология продукции общественного питания". Он имеет ярко выраженную профессиональную направленность, т.к. формирует у обучающихся представления о значении бактерий сфере человеческой жизни, связанной с питанием. Один из основных методов обучения на этом уроке - учебный проект.
Скачать:
| Вложение | Размер |
|---|---|
| metod_razrabotka_uroka_bez_kartinok.doc | 568 КБ |
Предварительный просмотр:
Разработала и провела:
Сапожок 2010 Тема урока: Прокариоты
Тип урока: формирования новых знаний
Вид урока: комбинированный урок с использованием учебного проекта и элементов игры-соревнования
Методическая цель урока: активизация познавательной самостоятельности обучающихся в приобретении профессионально значимых знаний путем использования деятельностного подхода в обучении (метода учебного проекта)
- образовательная : сформировать представления обучающихся о двух уровнях клеточной организации живой природы, познакомить их с особенностями строения прокариот, показать многообразие бактерий и их роль в природе и жизни человека
- развивающая : развитие самостоятельности и активности в познании объектов и явлений органического мира, формирование навыков работы с различными источниками информации, умения выделять главное, сравнивать, анализировать
- воспитательная : формирование ответственности, аккуратности, а также социальной коммуникации.
Методы обучения: фронтальный опрос, объяснительно-иллюстративный рассказ, репродуктивный метод, самостоятельная работа, учебный проект
Х О Д У Р О К А
Приветствие. Проверка присутствующих. Настрой на рабочий лад.
2. Повторение ранее изученного с направленностью на новый материал.
Преп.: Ребята, на прошлых уроках мы изучали с вами строение растительной и животной клеток, говорили об органоидах клетки.
Сейчас я буду зачитывать вам описание или назначение органоида в клетке, а вы называйте его.
( Названия органоидов прикрепляются в столбик на доску)
- Отграничивает внутреннее содержимое клетки от внешней среды.
- Внутренняя полужидкая среда клетки
- Система полостей и трубочек, участвующая в транспорте различных веществ и синтезе белков
- Округлые органоиды, состоящие из двух субъединиц, осуществляющие синтез белков
- Органоид, состоящий из сложенных стопкой плоских полостей, участвующий в хранении и выведении веществ
- Органоиды, присущие только растительным клеткам, придающие им окраску и выполняющие важнейшие разнообразные функции
- Непостоянные структуры цитоплазмы, в которых содержаться запасные вещества
- Разнообразные выросты (жгутики, реснички), помогающие клетке передвигаться
- Важный центр клетки, в котором храниться вся наследственная информация клетки
- То, чем ядро отделено от клетки
- Длинные и тонкие нити ДНК, в которых в виде триплетов нуклеотидов записана информация о строении белков клетки
- Округлые тела, в которых синтезируются рибосомы
Молодцы. Вы показали хорошие знания
3. Изучение нового материала
Актуализация приобретаемых знаний
Преп .: Итак, ребята, мы вспомнили с вами строение клеток растений и животных.
Но наш сегодняшний урок посвящен другим, совершенно удивительным созданиям.
Вы, наверное, догадались, о каких организмах идет речь?
Обуч. : О бактериях
Объяснение преподавателем нового материала
Преп. : Совершенно верно. Ученые выделяют их в особую группу – прокариоты.
Дело в том, что по строению клетки все живые организмы делятся на ядерные организмы – эукариоты и доядерные – прокариоты, основными представителями которых являются бактерии, а также сине-зеленые водоросли.
На сегодняшнем уроке вы познакомитесь со строением прокариот, прежде всего бактерий, их многообразием и значением в жизни человека. Особенно в том, что связано с питанием человека. Сделаем мы это по следующему плану (записан на доске) :
- Строение прокариот
- Многообразие бактерий
- Значение бактерий в природе и жизни человека
Объяснение с демонстрацией плаката
А сейчас, пожалуйста, посмотрите на плакат. Я расскажу вам о строении прокариот на примере бактериальной клетки.
Снаружи бактериальная клетка окружена плотной оболочкой, а у некоторых видов еще и слизистой капсулой
Под оболочкой, состоящей из углеводов, находится плазматическая мембрана. Цитоплазма прокариот содержит несколько меньше растворенных веществ, чем эукариотическая. В ней располагаются органоиды- рибосомы, включения, а также многочисленные мембранные структуры, выполняющие различные функции (пигментсодержащие используются для фотосинтеза, аэросомы – газовые вакуоли, карбоксисомы, заполненные ферментами.
У многих бактерий имеются органоиды движения – жгутики, которые, быстро вращаясь, вызывают вращение клетки. Так она передвигается.
Как уже было сказано, у прокариот бактерий и сине-зеленых водорослей нет оформленного ядра. Генетический аппарат представлен нуклеоидом, состоящим из двухспиральной молекулы ДНК. Размножаются прокариоты делением пополам.
Похожи по строению и клетки сине-зеленых водорослей.
Итак, вы прослушали рассказ о прокариотической клетке.
Промежуточное обобщение и закрепление знаний
- Клеточная оболочка
- Ядерный сок
- Хромосомы (ДНК)
- ядрышки
Обучающиеся, отвечая по очереди о каждом органоиде, заполняют таблицу.
Преп.: Итак, какой же вывод мы можем сделать? У вас на листочках есть неполный текст. Давайте сформулируем вывод.
Обуч.: Прокариоты, это организмы , не имеющие оформленного ядра и многих органоидов (ЭПС, аппарата Гольджи, митохондрий, пластид) . Наследственная информация хранится в нуклеоиде - кольцевой молекуле ДНК.
Обучающиеся записывают вывод в тетрадь
Продолжение объяснения преподавателем нового материала
Преп.: Итак, мы выяснили общие черты строения прокариот в целом и бактерий в частности. Но на самом деле бактерии очень многообразны, отличаются друг от друга по многим параметрам и прежде всего по форме, способу питания и отношению к кислороду. У вас на столах находятся сведения о видах бактерий. Я прошу их вклеить в тетрадь, а дома внимательно изучить и запомнить.
Мир бактерий или – в широком смысле слова – прокариот, огромный, но до сих пор мало изученный, рядом с нами, вокруг нас, внутри нас, всегда с нами
Роль крохотных бактерий велика не только в жизни человека, но и всей планеты Земля:
- Многие бактерии принимают участие в геохимических процессах образования серы, фосфора, каменного угля, нефти
- Бактерии играют важнейшую роль в круговороте азота: нитрифицирующие и азотфиксирующие повышают плодородие почвы
- В результате деятельности гнилостных бактерий, земля очищается от погибших растений и животных
- Человек научился использовать бактерии для приготовления вакцин и сывороток, в производстве антибиотиков.
Поэтому изучить многообразие бактерий, познать их свойства, выяснить их значение в природе и для человека – первоочередные задачи, стоящие перед биологией и ее особой областью – микробиологией. Она с этими задачами довольно успешно справляется.
Изучение нового материала по подготовленным обучающимися творческим работам
И вот вы, ребята, заранее получили задание подготовить плакат – стенгазету, освещающую ту или иную сферу участия бактерий в нашей жизни. Я думаю, вы подготовились и сейчас познакомите нас с ними. Я попрошу всех внимательно слушать. Вам в дальнейшем предстоит не только использовать эти сведения, но и оценить своих товарищей.
Творческие проекты обучающихся
Преп.: Большое спасибо. Все работы были очень творческими и интересными. Все молодцы. А теперь каждую команду оценят две другие. Каждый из вас должен поставить оценки 0 – если сообщение оставило вас равнодушным, + если оно понравилось и ++ - если очень понравилось.
Обучающиеся оценивают своих товарищей
4. Творческое применение и закрепление полученных знаний
- Кишечная палочка
- Молочнокислый стрептококк
- Золотистый стафилококк
Обучающиеся готовятся, потом выступают с сообщениями.
5. Подведение итогов занятия
Подсчитываются результаты, объявляются победители.
Делается вывод: итак, на сегодняшнем уроке вы, ребята, узнали о существовании двух форм клеточной организации жизни на Земле – прокариотической и эукариотической. И если о эукариота мы говорили ранее, то сегодня очень подробно разобрали строение прокариот, а также их важнейших представителей – бактерий. Я думаю, вы поняли, что их значение в жизни человека, в его питании очень велико. Мы с вами еще будем изучать бактерии на уроках физиологии питания, а также целая дисциплина на 4 курсе – микробиология – будет посвящена этим маленьким, но таким значительным организмам. А сегодня мы с ними лишь немного соприкоснулись. Я, надеюсь. Что вы заинтересовались и в дальнейшем приложите усилия для их изучения.
6. Информация о домашнем задании, инструктаж по его выполнению
А сейчас запишите, пожалуйста, домашнее задание: (записано на доске)
- § 36 (до вирусов)
- записи в тетради, дополнительная информация о видах бактерий
- тестовое задание
Разъясняется выполнение теста.
Большое спасибо всем за урок, до свидания
Дидактические материалы урока:
Читайте также:


