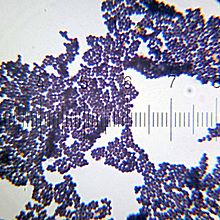
Что такое стафилококки 5 класс

В последние годы не угасает интерес к эпидемиологии стафилококков как этиологических агентов многих инфекционных заболеваний, поcкольку стафилококковое бактерионосительство служит причиной формирования серьезных осложнений в условиях госпитализации.
Особую актуальность этот вопрос приобретает в связи с широким распространением и циркуляцией как в природной популяции, так и госпитальной среде метициллинрезистентных штаммов золотистого стафилококка (MRSA). Принципиально важным для дифференциации таких штаммов является исследование генных комплексов, входящих в состав стафилококковых хромосомных кассет mec (staphylococcal chromosome cassette mec, SCCmec), а также определение генов, детерминирующих синтез энтеротоксинов A, B, C и др., токсина синдрома токсического шока (TSST).
Для большинства стафилококков естественной средой обитания является поверхность кожи человека, слизистые, где они персистируют, не причиняя вред организму хозяина. Однако, как показывают работы последних лет [1, 3], при хронических дерматозах происходят изменения микробиоценозов кожи, в частности, возрастает степень обсемененности кожи представителями рода Staphylococcus, особенно S.aureus. В этой связи встает вопрос об этиопатогенетической роли этих бактерий в развитии кожных патологий. Поскольку основными поражающими факторами воздействия стафилококков на эукариотические клетки и ткани являются секретируемые факторы вирулентности и патогенности (токсины), целью настоящей работы явилось исследование вариабельности геномных комплексов стафилококков, выделенных с кожи людей при хронических дерматозах.
Материал и методы исследования
Бактериальные штаммы. В работе были использованы 185 штаммов стафилококков, из них – 91 штамм S. aureus (49,1 %), полученные от лиц в возрасте от 18 до 80 лет, находящихся в стационаре областного кожно-венерологического диспансера г. Ульяновска с хроническими дерматозами: псориаз (57/144, 39,6 %), экзема (68/144, 47,2 %), атопический дерматит (19/144, 13,2 %).
Забор материала осуществляли с пораженных и интактных участков кожи ватным тампоном, смоченным 0,85 % раствором хлористого натрия. Смывы в количестве 0,1 мл засевали на селективные питательные среды, через 48 часов подсчитывали количество выросших колоний и пересчитывали на 1 см 2 кожи (Иванов, 1984). Результаты пересчитывали на КОЕ/см 2 . Первичную родовую и видовую идентификацию стафилококков осуществляли на основании морфологии колоний, окраски по Граму, данных каталазного и коагулазного тестов. Качественное и количественное исследование микробиоценозов кожи осуществляли на базе бактериологической лаборатории городской клинической больницы № 1 г. Ульяновска (зав. лабораторией – Волгина Т.И.). Полученные данные подвергали статистической обработке с использованием пакета прикладных программ Microsoft Еxcel 2003.
Видовая идентификация стафилококков прямым масс-спектрометрическим профилированием. Свежие бактериальные клетки (1–2 колонии) переносили в 300 мкл деионизированной воды, перемешивали и добавляли 900 мкл этанола. Осадок после центрифугирования (15 мин×14000 об/мин) растворяли в 20 мкл смеси 50 % ацетонитрила (АЦН), 35 % муравьиной кислоты. Полученный в результате последующего центрифугирования супернатант анализировали времяпролетной МАЛДИ масс-спектрометрией. Все использованные реактивы, включая воду, были аналитической чистоты или специальные для масс-спектрометрии.
В качестве матрицы применяли a-циано-4-гидроксикоричную кислоту ( a -cyano-4-hydroxycinnamic acid, a-CHCA, BrukerDaltonics, Германия) в виде насыщенного раствора в смеси 50 % АЦН, 2,5 % трифторуксусной кислоты (ТФУ). Для сокристаллизации матрицы и образца 1 мкл аналита наносили на ячейки стальной мишени для масс-спектрометрии (MSP 96 target ground steel, BrukerDaltonics, Германия), давали подсохнуть 1–2 минуты и сверху наслаивали 2 мкл насыщенного раствора матрицы. Кристаллы оставляли на воздухе в течение 5–10 мин до полного высыхания. Влажность и температуру при этом не контролировали.
Масс-спектрометрический анализ осуществляли с помощью времяпролетного МАЛДИ масс-спектрометра MicroflexTM (BrukerDaltonics, Германия), оснащенного азотным лазером 337 нм. Все измерения проводили в линейном режиме, детектируя положительные ионы. Для накопления масс-спектров мощность лазерного излучения устанавливали на уровне минимального порогового значения, достаточного для десорбции-ионизации образца. Параметры масс-спектрометра оптимизировали для диапазона m/z от 2000 до 20000. Внешнюю калибровку проводили с использованием точных значений масс известных белков E. coli.
Для записи, обработки и анализа масс-спектров использовали программное обеспечение компании Bruker Daltonics (Германия): flexControl 2.4 (Build 38) и flexAnalysis 2.4 (Build 11). Точность измерения масс составляла ± 2 Да. Видовую идентификацию бактерий проводили путем сопоставления получаемых масс-спектров с имеющимися базами данных с помощью программного пакета MALDI Biotyper 2.0 (Bruker Daltonics, Германия).
Генетическое тестирование стафилококков
Для установления наличия генов, детерминирующих синтез стафилококковых энтеротоксинов (гены sea – sed, sei – sej), токсина синдрома токсического шока (ген tsst) и лейкоцидина (гены lukS – lukF) применена традиционная ПЦР с использованием предложенных ранее праймеров [9, 10].
Амплификацию исследуемых фрагментов ДНК выполняли в реакционной смеси, содержащей 10 мМ Tris-HCl, pH 9,0; 50 мM KCl; 2 мM MgCl2, по 250 мкМ каждого дНТФ, 1 едTaq-полимеразы (Promega, USA) и по 10 пмоль каждого праймера в объеме 25 мкл. Реакцию амплификации проводили в программируемом термостате DNA EngineTetrad 2 (MJ Research, USA), используя следующий профиль амплификации: 94 ° С – 5 мин., 30 циклов: 94 ° С – 1 мин, 60 ° С – 1 мин, 72 ° С – 1 мин. Продукты реакции анализировали в 2 % агарозном геле.
Результаты исследования и их обсуждение
Согласно данным бактериологического и масс-спектрометрического тестирования установлен видовой состав стафилококков, выделяемых от пациентов с дерматитами. Среди проанализированных 185 штаммов, 91 штамм (49,1 %) принадлежал к виду S. aureus, 28 штаммов (15,1 %) – к S. epidermidis, 30 штаммов (16,2 %) составили S. hominis, 18 (9,7 %) штаммов – S. haemolyticus, S. capitis– 4 (2 %), на такие виды как S. saprophyticus, S. warneri, S. pattenkoferi приходилось по 0,5 %. Также результаты генетического типирования показали наличие среди выделенных штаммов Micrococcus luteus и Corynebacteriumaurim ucosum в 0,5 % случаев.
Исследуемые штаммы продемонстрировали наличие гена mecA в 15 случаях из 185 (8,1 %), причем данный признак был обнаружен только среди коагулазоотрицательных стафилококков: S. hominis – 7 штаммов из 30 (23,3 %); S. epidermidis – 4 штамма из 28 (14,3 %); S. haemolyticus – 4 штамма из 18 (22,2 %).
Наличие стафилококковой хромосомной кассеты SCCmec у коагулазоотрицательных стафилококков, по мнению некоторых авторов [4], свидетельствует о ее участии в функции горизонтального обмена генами. Считается, что первыми стафилококками, получившими SCCmec, были S. haemolyticus, и только в последующем произошла передача этого элемента другим коагулазоотрицательным стафилококкам и S. aureus [2].
Полученные результаты по отсутствию гена mecA среди изученных штаммов S. aureus согласуются с данными литературы. Cобранные нами штаммы относятся к внебольничной популяции стафилокококков, среди которых процент устойчивых к метициллину штаммов составляет не более 30 %, тогда как ген mecA, кодирующий устойчивость к метициллину, обнаруживается преимущественно среди госпитальных стафилококков – до 40 %.
Следующую группу молекулярных маркеров составили расположенные на МГЭ гены, детерминирующие синтез энтеротоксинов A, B, C и др., токсина синдрома токсического шока, т.е. те гены, продукты которых обладают суперантигенной активностью (PTSAgs) и могут оказать влияние на состояние иммунореактивности макроорганизма. Определение наличия генов PTSAgs позволяет выявить патогенный потенциал и охарактеризовать отдельные штаммы. Проведенные исследования показали наличие генов, детерминирующих токсинообразование стафилококков у 40,5 % изученных штаммов (75 клинических изолятов). Следует отметить, что частота встречаемости указанных генов у штаммов золотистого стафилококка составила 86,7 %, у коагулозоотрицательных штаммов – 13,3 % случаев.
Обнаружена значительная вариабельность в наборе генов, детерминирующих синтез этих токсинов у клинических изолятов стафилококков. Так, изученные штаммы имели от одного до четырех генов в различных сочетаниях. В геноме 35 изолятов обнаружен только один ген из sea – sei. У 20 штаммов преобладали по два гена и у 20 – от трех до четырех генов. При этом установлено, что коагулазоотрицательные штаммы, несущие mec A, не обладали ни одним из перечисленных генов. В целом из общего количества генетических детерминант токсинообразования преобладали гены seg – 26,8 %, seh – 17,1 % случаев.
Исходя из значительной видовой вариабельности грамположительной флоры в микробиоценозе кожи исследуемых больных, была проанализирована частота встречаемости генов, определяющих токсинообразование стафилококков в зависимости от видовой принадлежности штаммов.
Так, наибольшим разнообразием генов обладали штаммы золотистого стафилококка, среди которых преобладал ген seg. В связи с тем, что среди коагулазоотрицательных штаммов стафилококков наибольшую частоту встречаемости показали гемолитический и эпидермальный стафилококки, а доля остальных оказалась незначительна, то анализ генов, детерминирующих токсинообразование, осуществляли только у этих видов стафилококков, что показало у S. haemolyticus наличие только генов seb и sed, у эпидермального стафилококка только seh.
Значительный интерес представлял анализ полученных результатов в зависимости от участка кожи, с которого были выделены микроорганизмы. В соответствии с этим все полученные штаммы разделили на две группы: 1-я – штаммы, выделенные с чистых участков кожи, 2-я – штаммы, выделенные с пораженных участков кожи (рис. 1).
Таким образом, наиболее значимые различия по частоте встречаемости детерминант токсинообразования можно отметить для генов sea (14,7 % в 1-й группе и 7,3 % во 2-й) и sei (11,7 % в первой группе, 19,1 % – во второй). Причем ген sea достоверно чаще обнаруживался в стафилококках, изолированных на чистых участках кожи, тогда как ген sei – на пораженных. Частота встречаемости данного признака в указанных группах в зависимости от вида микроорганизмов показала различия только для S. aureus (рис. 2). Для остальных видов из рода Staphylococcus, наиболее часто обнаруживаемых на коже, результаты следующие: S. epidermidis показал ген энтеротоксина sei в одном случае с чистого участка кожи. А S. haemolyticus – наличие 1 случая из двух, наличие гена sed – в одном из четырех случаев.
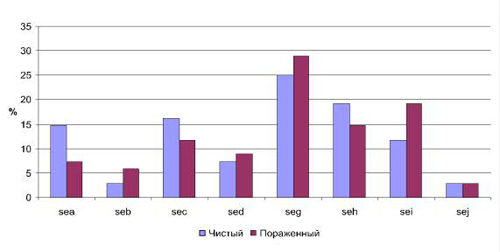
Рис. 1. Частота встречаемости энтеротоксинов a, b, c, d, g, h, I, j в зависимости от участка кожи
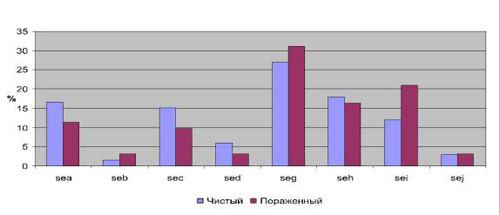
Рис. 2.Частота встречаемости детерминант токсинообразования у S. aureus, выделенных с чистого и пораженного участка кожи
Ген TSST обнаружен только в 10,8 % случаев от всего количества исследуемых штаммов, причем в двух случаях параллельно с наличием хромосомной кассеты mecA у S. epidermidis. При этом в 55 % случаев ген TSST обнаруживали у штаммов, выделенных с чистых участков кожи, в 45 % случаев – с пораженных участков.
Сравнительный анализ хромосомной ДНК стафилококков, выделенных при хронических кожных патологиях, показал, что изученные штаммы Staphylococcus spp. обнаруживают значительную вариабельность в наборе генетических детерминант, характеризующих их патогенный потенциал.
Кассета mecA, рассматриваемая как фактор устойчивости к метициллину, была обнаружена в 8,1 % случаев и только среди коагулазоотрицательных стафилококков.
Гены токсинообразования наиболее часто встречались среди коагулазоположительных стафилококков (S. aureus). Наиболее часто в проанализированной выборке встречались гены seg – 26,8 %, и seh – 17,1 % случаев.
Штаммы, изолированные с разных участков кожи, значимо отличались по частоте обнаружения маркеров генов энтеротоксинов A, С и I.
Таким образом, молекулярно-генетический анализ ДНК и генотипирование стафилококков может иметь теоретическое и практическое значение в целях обеспечения более качественной диагностики стафилококковой инфекции, эффективного мониторинга и лечения.
Нестеров А.С., д.м.н., профессор, зав. Циклом кожных и венерических болезней кафедры инфекционных и кожно-венерических болезней медицинского факультета Ульяновского государственного университета, г. Ульяновск;

Стафилококки (лат. Staphylococcus) — род повсеместно распространённых грамположительных бактерий-кокков.
Стафилококки встречаются в норме на всем протяжении желудочно-кишечного тракта человека, включая желудок (О.В. Добровольский, С.Ю. Сереброва), а также на коже, слизистой оболочке респираторных органов и в урогенитальном тракте.
Стафилококки представляют собой неподвижные шарообразные клетки диаметром от 0,5 до 1,5 мкм, располагающиеся одиночно, парами или гроздьями. Не образуют спор.
Стафилококки лучше других бактерий переносят воздействие высокой температуры, света, высушивания и химических агентов. Они выдерживают нагревание до 60°С в течение часа, а отдельные штаммы — до 80°С в течение получаса и 10 минут при нагревании до 150°С, солнечный свет в течение 10-12 часов, сухой жар — до 2-х часов. Стафилококки устойчивы к повышенному содержанию хлористого натрия (поэтому они хорошо сохраняются в консервированных продуктах), чистому этанолу и фенолу. Оптимальная температура для развития стафилококков 30–37 °С.
Частота выделения некоторых видов стафилококков от человека и ряда сельскохозяйственных и домашних животных (Широкова И.Ю.).
| Вид стафилококков | Вид хозяев (%) | ||||
| человек | ослы | овцы | козы | кошки | |
| S. aureus | 4,6 | 2,9 | 37,5 | 19,7 | 13,0 |
| S. epidermidis | 23,6 | 2,3 | 6,7 | 9,2 | 6,0 |
| S. hominis | 26,9 | 6,9 | — | — | — |
| S. capitis | 4,7 | 2,3 | — | — | 1,0 |
| S. haemolyticus | 11,8 | — | — | 18,5 | 2,0 |
| S. warneri | 4,6 | — | 2,5 | 13,0 | — |
| S. saprophyticus | 8,4 | 4,6 | 5,0 | 3,8 | — |
| S. cochnii | 4,2 | 2,3 | — | 1,7 | — |
| S. xylosus | 9,9 | 10,3 | 11,7 | 6,6 | 2,0 |
| S. simulans | 1,3 | — | 7,5 | — | 4,0 |
| S. intermedius | — | — | — | — | 10,0 |
| S. felis | — | — | — | — | 45,0 |
| S. sciuri | — | 25,1 | 17,5 | 5,8 | 6,0 |
Род стафилококки входит в семейство Staphylococcaceae, порядок Bacillales, класс Bacilli, тип Firmicutes, Terrabacteria group, царство Бактерии.
В род стафолококки входят следующие виды: S. agnetis, S. argensis, S. argenteus, S. arlettae, S. aureus (стафилококк золотистый), S. auricularis, S. capitis, S. caprae, S. carnosus, S. chromogenes, S. cohnii, S. condimenti, S. delphini, S. devriesei, S. epidermidis (стафилококк эпидермальный), S. equorum, S. faecalis, S. felis, S. fleurettii, S. gallinarum, S. haemolyticus, S. hominis, S. hyicus, S. intermedius, S. kloosii, S.leei, S. lentis, S. lugdunensis, S. lutrae, S. lyticans, S. massiliensis, S. microti, S. muscae, S. pasteuri, S. petrasii, S. pettenkoferi, S. piscifermentans, S. pseudintermedius, S. pseudolugdunensis, S. rostri, S. saccharolyticus, S. saprophyticus (стафилококк сапрофитный), S. schleiferi, S. schweitzeri, S. sciuri, S. simiae, S. simulans, S. stepanovicii, S. succinus, S. vitulus, S. warneri, S. xylosus.
У некоторых видов стафилококков выделены подвиды:
Ряд видов рода стафилококков, исходя из общности физиологических признаков и генетического родства, объединены в 4 группы:
- группа Staphylococcus epidermidis: S. epidermidis, S. capitis, S. warneri, S. haemolyticus, S. hominis и S. saccharolyticus
- группа Staphylococcus saprophiticus: S. saprophyticus, S. cohnii и S. xylosis
- группа Staphylococcus simulans: S. simulans и S. carnosus
- группа Staphylococcus sciuri: S. sciuri и S. lentus
В зависимости от способности продуцировать коагулазу, экстрацеллюлярный фермент, вызывающий свертывание плазмы крови, стафилококки подразделяются на коагулаза-положительные (коагулазопозитивные) и коагулаза-отрицательные (коагулазонегативные).
Коагулаза-положительными являются 5 видов стафилококков: Staphylococcus aureus (золотистый стафилококк), Staphylococcus delphini, Staphylococcus hyicus, Staphylococcus intermedius, staphylococcus lutrae, staphylococcus schleiferi subsp. coagulans, среди которых патогенный для человека только золотистый стафилококк. Кроме стафилококков коагулаза-положительной является бактерия Yersinia pestis — возбудитель чумы.
К коагулаза-отрицательным относятся эпидермальный и сапрофитный стафилококки, а также Staphylococcus caprae, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus lugdunensis, Staphylococcus pettenkoferi, Staphylococcus schleiferi, Staphylococcus warneri, Staphylococcus xylosus и другие виды. Коагулаза-отрицательные стафилококки менее патогенны, чем коагулазо-положительные.
Коагулаза-отрицательные стафилококки входят в состав нормальной микрофлоры кожи человека и обычно не вызывают серьёзных заболеваний. Staphylococcus lugdunensis более вирулентны, чем другие коагулаза-отрицательные стафилококки и, в случае имплантируемых медицинских изделий или катетеров, Staphylococcus lugdunensis могут быть причиной тяжело текущих инфекций костей и суставов, возникающих у пациентов, находящихся на лечении в стационаре.
При исследовании биологического материала человека при положительном тесте на коагулазу делается вывод о наличии золотистого стафилококка.
При микробиологическом анализе кала на дисбактериоз отдельно подсчитывают коагулаза-положительные (фактически золотистый стафилококк) и коагулаза-отрицательные (в основном это эпидермальный и сапрофитный) стафилококки. При этом в норме золотистый стафилококк должен отсутствовать, а количество коагулаза-отрицательных стафилококков не должно превышать 10 4 колониеобразующих единиц (КОЕ) на 1 г кала.
Коагулаза-отрицательные стафилококки обнаруживаются в кале у 15,0±3,0 % здоровых людей, причем среднее содержание в 1 г кала от 800 до 3200 КОЕ (М.Д.Ардатская, О.Н.Минушкин).
При избыточном росте стафилококка, как следствии дисбактериоза кишечника, кроме бактериофагов, при медикаментозной терапии применяются различные пробиотки (Бифидумбактерин, Бифиформ, Лактобактерин, Ацилакт, Линекс и др.) и/или адекватные конкретному штамму стафилококка и причине дисбактериоза антибиотики (у взрослых).
| стафилококк | |
|---|---|
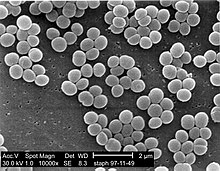 | |
| СЭМ микрофотография из золотистого стафилококка колоний: Обратите внимание на виноград, как кластеризацию , общий для Staphylococcus видов. | |
| Научная классификация | |
| Домен: | |
| Учебный класс: |
Staphylococcus является родом из гр-положительных бактерий в семье Staphylococcaceae в порядке Bacillales . Под микроскопом , они появляются сферические ( кокки ), ав форме винограда -подобных кластеров. Виды Staphylococcus являются факультативными анаэробными организмами (способные к росту и аэробный и анаэробный). Стафилококк включает в себя , по меньшей мере 40 видов. Из них девять есть два подвида , один имеет три подвида, и один имеет четыре подвида. Большинство из них безвредны и находятся обычно на коже и слизистых оболочек человека и других организмов . Staphylococcus было установлено, что нектар обитающего микроба. Найдено по всему миру, они являются небольшой частью почвы микробной флоры . содержаниетаксономияТаксономии основана на 16s рРНК последовательностей, и большинство видов стафилококка попадают в 11 кластеров:
12 - й группе - у С. caseolyticus - теперь удалены к новому роду, Macrococcus , виды которого в настоящее время является ближайшим известные родственники стафилококка . Два вида были описаны в 2015 году - стафилококк Argenteus и стафилококки schweitzeri - оба из которых были ранее рассмотрены варианты золотистого стафилококка . А новые коагулазонегативные негативные виды - Staphylococcus edaphicus - были выделены из Антарктиды . Этот вид, вероятно , является членом S. saprophyticus группы. Золотистый стафилококк подвид. стафилококка С. лишай подвид. лишай С. carnosus подвид. carnosus С. cohnii подвид. cohnii С. equorum подвид. equorum С. хоминис подвид. хоминис S petrasii подвид. croceilyticus S. saprophyticus подвид. BOVIS S. schleiferi подвид. coagulans S. sciuri подвид. carnaticus S. succinus подвид. Casei На основе анализа содержания ортологического гена, были предложены три групп (А, В и С). Группа А включает в себя S. стафилококк , S. Capitis , S. эпидермальный , S. haemolyticus , S. Hominis , S. lugdunensis , S. pettenkoferi , S. simiae и S. warneri . Группа B включает в себя S. arlettae , S. cohnii , S. equorum , S. saprophyticus и S. xylosus . Группа C включает в себя S. Delphini , S. Интермедиус и S. pseudintermedius . С. saprophyticus и S. sciuri группа обычно новобиоцин резистентного, как С. Hominis подвид. novobiosepticus . Члены из S. sciuri группы оксидазы -положительным из - за их хранение фермента цитохром с - оксидазы . Эта группа является единственной клады в стафилококков обладают этим геном. В S. sciuri группа , кажется, самые близкие отношения к роду Macrococcus . С. pulvereri было показано, является младшим синонимом S. vitulinus . В этих кладах, в S. haemolyticus и S. simulans группа , по всей видимости, связан, как это делает S. стафилококк и S. эпидермальных групп. С. lugdunensis по- видимому, связано с haemolyticus S. группы. С. petrasii может быть связано с S. haemolyticus , но это должно быть подтверждено. Систематическое положение S. lyticans , С. pettenkoferi , С. petrasii и С. pseudolugdunensis еще предстоит выяснить. Опубликованные описания этих видов , кажется , не были надлежащим образом опубликованы. Биохимическая идентификацияПрисвоение штамма к роду Staphylococcus требует, чтобы это было грамположительные кокки , который формирует кластеры, имеет соответствующую клеточной стенки структуры ( в том числе пептидогликана типа и наличием тейхоевой кислоты) и содержание G + C в ДНК в диапазоне 30-40 % мол. Staphylococcus видов можно отличить от других аэробных и факультативных анаэробных, грамположительных кокков несколько простых тестов. Staphylococcus виды являются факультативными анаэробами (способными к росту и аэробный и анаэробный). Все виды растут в присутствии солей желчных кислот . Все виды стафилококка были когда - то думали, что коагулазонегативное положительным, но с тех пор были опровергнуты. Рост также может иметь место в 6,5% растворе NaCl. На Baird среды Паркера , Staphylococcus виды растут ферментативно, за исключением S. saprophyticus , который растет окислительному. Staphylococcus виды устойчивы к бацитрацин (0.04 U диска: сопротивление = производство Коагулазо Одним из наиболее важных фенотипических признаков , используемых в классификации стафилококков являются их способностью производить коагулаз , фермент , который вызывает сгусток крови образования. Семь видов в настоящее время признано, что коагулазонегативные положительным: S. стафилококк , С. Delphini , С. hyicus , С. Интермедиус , С. lutrae , С. pseudintermedius и С. , schleiferi подвид. coagulans . Эти виды относятся к двум отдельным группам - на золотистом стафилококк ( золотистый стафилококк в покое) группу и hyicus-Интермедиусе S. группы (оставшиеся пять). Восьмой вид был также описан - Staphylococcus leei - у пациентов с гастритом . Золотистый стафилококк является коагулазонегативным положительным, то есть она производит коагулаз. Темменее,то время как большинство золотистого стафилококка штаммов коагулазонегативные положительно, некоторыемогут быть нетипичными в томчто они не производят коагулаз. Золотистый стафилококк является каталазо -положительным (означаетчто он может производить фермент каталаза) и способный превращать перекись водорода (H 2 O 2 ) в воду и кислород, что делает каталаз тест полезно отличать от стафилококков энтерококков и стрептококков . С. pseudintermedius населяет и иногда поражает кожу домашних собак и кошек. Этот организм также может нести генетический материалкоторый придает множественную устойчивость бактерий. Он редко участвует в инфекций вчеловека, как зоонозов . С. эпидермальный , коагулазонегативные виды, являются синантропными кожами, но может вызвать серьезные инфекции в ослабленном иммунитете больных и лицо с центральным венозным катетером . S. saprophyticus , еще коагулазонегативных видов, является частью нормальной флоры влагалища , преимущественно вовлечены в мочеполовых путей инфекции у сексуально активных молодых женщин. В последние годы ряд других Staphylococcus видов были вовлечены в человеческих инфекций,частности С. lugdunensis , С. schleiferi и С. caprae . Genomics и молекулярная биологияПервые золотистого стафилококка геномы секвенировать были те N315 и Mu50, в 2001 году многие более полных золотистого стафилококка геномов были представлены в общедоступных базах данных, что делает его одним из наиболее широко секвенированы бактерий. Использование геномных данных в настоящее время широко распространено и представляет собой ценный ресурс для исследователей , работающих с золотистым стафилококком . Целые технологии геном, такие как секвенирование проекты и микрочип , показали огромное разнообразие золотистого стафилококка штаммов. Каждый из них содержит различные сочетания поверхностных белков и различных токсинов . Относительно этой информации патогенного поведения является одним из основных направлений стафилококковых исследований. Разработка методов молекулярного типирования позволило отслеживания различных штаммов золотистого стафилококка . Это может привести к лучшему контролю штаммов вспышки. Более глубокое понимание того , как стафилококки развиваться, особенно в связи с приобретением мобильных генетических элементов , кодирующих гены устойчивости и вирулентности помогает идентифицировать новые штаммы вспышек и может даже предотвратить их появление. Широко распространена частота устойчивости к антибиотикам в различных штаммах золотистого стафилококка , или между различными видами Staphylococcus была приписана горизонтальным перенос генов генов , кодирующих устойчивость к антибиотикам / металла и вирулентность. Недавнее исследование показало степень горизонтального переноса генов среди Staphylococcus быть намного больше , чем ожидалось ранее, и включает в себя гены с функциями помимо устойчивости к антибиотикам и вирулентности, и за его пределами генов , находящихся в пределах мобильных генетических элементов . Различные штаммы Staphylococcus доступны из биологических исследовательских центров, таких как Национальная коллекция типовых культур . диапазон хоста
Представители рода Staphylococcus часто колонизирует кожу и верхние дыхательные пути млекопитающих и птиц. Некоторые виды Специфичность наблюдается в диапазоне хозяина, таким образом, что Staphylococcus виды , наблюдаемые на некоторых животных появляются реже на более отдаленное родственных видов хозяев. Некоторые из наблюдавшихся принимающей специфичности включает: С. arlattae - куры , козы клиническаяСтафилококк может вызывать широкий спектр заболеваний у людей и животных , либо через производство токсина или проникновение. Стафилококковые токсины являются частой причиной пищевого отравления, потому что они могут быть получены путем бактерий , растущих в неправильно хранящиеся продукты питания. Наиболее распространенный сиаладенит вызываются стафилококками, как бактериальные инфекции. Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу. Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции
|