Брюшной тиф это микробиология
Пензенский государственный университет
Кафедра "Микробиологии, эпидемиологии и инфекционных болезней"
Дисциплина: Инфекционные болезни
Тема лекции: Брюшной тиф, паратифы А и В
Брюшной тиф (typhoidfever — англ., Abdominaltyphus — нем., abdominale fievre — фр.) — острая инфекционная болезнь, обусловленная сальмонеллой (Salmonella typhi), характеризуется лихорадкой, симптомами общей интоксикации, бактериемией, увеличением печени и селезенки, энтеритом и своеобразными морфологическими изменениями лимфатического аппарата кишечника.
Возбудитель брюшного тифа (S. typhi) относится к семейству Enterobacteriaceae, роду Salmonella, виду Salmonella enterica, подвиду enterica, serovar typhi и морфологически не отличается от других сальмонелл. Это грамотрицательная подвижная палочка с перитрихиально расположенными жгутиками, спор и капсул не образует, хорошо растет на обычных питательных средах. Биохимически отличается от других сальмонелл ферментацией глюкозы без образования газа и замедленным выделением сероводорода. Антигенная структура S. typhi характеризуется наличием соматического О (9, 12, Vi) — комплекса и жгутикового антигена Н (d). В зависимости от количества и расположения Vi-антигена различают 3 варианта культур.
1) V-форма содержит Vi-антиген, покрывающий О-комплекс, колонии таких культур непрозрачны и не агглютинируются О-сывороткой;
2) W-форма не содержит Vi-антигена, колонии прозрачны, культура хорошо агглютинируется О-сывороткой;
3) VW-форма имеет гнездное расположение Vi-антигена и агглютинируется О- и Vi-сыворотками.
Возбудители брюшного тифа по чувствительности к типовым бактериофагам подразделяются на 78 стабильных фаговаров. Фаготипирование представляет удобную метку для установления эпидемиологической связи между заболеваниями и выявлением источника инфекции. Брюшнотифозные бактерии способны к L-трансформации, что, возможно, является результатом эволюционного приспособления возбудителя к выживанию в условиях иммунного организма. S. typhi умеренно устойчивы во внешней среде — в почве, воде могут сохраняться до 1-5 мес, в испражнениях — до 25 дней, на белье — до 2 нед, на пищевых продуктах — от нескольких дней до недель, особенно продолжительно — в молоке, мясном фарше, овощных салатах, где при температуре выше 18°С они способны размножаться. При нагревании быстро погибают. Дезинфицирующие средства (лизол, хлорамин, фенол, сулема) в обычных концентрациях убивают возбудителя в течение нескольких минут.
Брюшной тиф относится к кишечным антропонозам. Единственным источником и резервуаром инфекции является человек. Источником инфекции чаще всего являются хронические бактерионосители возбудителя брюшного тифа, которые, оставаясь практически здоровыми, выделяют сальмонеллы в течение продолжительного времени (годы и даже десятки лет). Представляют также опасность лица с легкими и атипичными формами болезни, так как они не всегда своевременно изолируются, посещают общественные места, продолжают выполнять служебные обязанности, в том числе на объектах питания и водоснабжения.
Механизм передачи возбудителей фекально-оральный, т.е. заражение людей происходит при употреблении инфицированной воды или пищи. Контактно-бытовой путь передачи S. typhi наблюдается редко, преимущественно среди детей. Водные вспышки возникают при загрязнении водоисточников сточными водами, технической неисправности водопроводной, канализационной систем и сооружений, а также вследствие нарушения режима очистки воды. Опасность пищевых заражений состоит в том, что в некоторых продуктах (молоко, холодные мясные закуски) сальмонеллы брюшного тифа могут сохраняться и даже размножаться. Риск возникновения заболевания в этих случаях увеличивается вследствие большой инфицирующей дозы возбудителя.
Восприимчивость людей к брюшному тифу различна, несмотря на то, что возбудитель обладает облигатной патогенностью и эволюционно приспособился к паразитированию в организме человека. Невосприимчивость обычно обусловлена наличием специфического иммунитета в результате перенесенного заболевания, бытовой иммунизации или вакцинации. При массовом заражении в эпидемических очагах может заболеть до 40-50% людей.
Заболевание встречается во всех климатических зонах и частях света. Однако в большей степени оно распространено в странах с жарким климатом и низким уровнем санитарно-коммунального обустройства населения.
Разработанная еще в 1924—1934 гг. Ш. Ашаром и В. Лаверне фазовая теория патогенеза брюшного тифа сохранилась в целом до настоящего времени. На ее основе выделяют следующие звенья патогенеза: внедрение возбудителя в организм, развитие лимфаденита, бактериемию, интоксикацию, паренхиматозную диффузию, выделение возбудителя из организма, формирование иммунитета и восстановление гомеостаза. Приведенная схема условна, поскольку экспериментально доказано, что, например, проникновение возбудителей в кровь происходит уже в пределах первых двух фаз. Следовательно, правильнее говорить о взаимообусловленных и часто совпадающих по времени звеньях патогенеза брюшного тифа.
Для возникновения заболевания необходимо попадание в желудочно-кишечный тракт определенной инфицирующей дозы микробов-возбудителей. В исследованиях на добровольцах американские авторы [Ноrnick R.В.] установили, что она составляет от 10 млн до 1 млрд микробных клеток. Внедрение возбудителя происходит в тонкой кишке, из просвета которой сальмонеллы проникают в солитарные фолликулы и пейеровы бляшки, вызывая лимфангит. Затем микробы попадают в мезентериальные лимфатические узлы, где они размножаются, и, прорвав лимфатический барьер, через грудной проток попадают в кровь. Возникает бактериемия, которая совпадает с первыми клиническими признаками брюшного тифа. В результате бактерицидного действия крови часть микробов гибнет с выделением эндотоксина. Такой же процесс происходит и в лимфатических узлах. Циркулирующий в крови эндотоксин вызывает интоксикацию организма различной интенсивности.
Эндотоксин оказывает выраженное нейротропное действие с токсическим поражением нервных центров и развитием в них процессов торможения. Клинически это характеризуется инфекционно-токсической энцефалопатией, которая проявляется в своеобразной заторможенности больных, затуманенности сознания. При тяжелом течении болезни она наиболее выражена и получила название тифозного состояния (status typhosus). Эндотоксин действует также на симпатические нервные окончания чревного нерва (в месте выделения) и на вегетативные ганглии, что приводит к трофическим и сосудистым нарушениям в слизистой оболочке и лимфатических образованиях тонкой кишки. В результате возникают кишечные язвы, появляются метеоризм, иногда понос. В пользу подобного механизма возникновения язвенных поражений тонкой кишки при брюшном тифе свидетельствуют факты образования сходных по морфологии язв у экспериментальных животных при введении брюшнотифозного эндотоксина в абдоминальные вегетативные узлы [Казанцев А.П., Матковский В.С., 1985]. Эндотоксин S. typhi поражает также костный мозг, что проявляется лейкопенией.
Одновременно с диссеминацией сальмонелл начинается очищение организма путем выведения возбудителя различными органами выделения (почки, пищеварительные железы кишечника, слюнные, потовые железы, печень).
Наиболее интенсивно бактерии выводятся через печень, где основная масса их погибает, а остальные выделяются с желчью в просвет кишечника. Часть их выводится с испражнениями во внешнюю среду, а часть снова внедряется в лимфоидные образования тонкой кишки. Связанная с этим фактом гипотеза об аллергическом генезе формирования язв тонкой кишки сейчас представляется маловероятной, поскольку брюшному тифу не свойственны выраженные аллергические реакции, а изменения кишечника можно объяснить токсическим действием эндотоксииа как на периферические вегетативные узлы и окончания, так и непосредственно на лимфатические образования кишечника.
Защитные реакции организма при брюшном тифе развиваются с начала возникновения инфекционного процесса. Уже на 4—5-й день болезни в крови можно обнаружить специфические антитела, относящиеся к IgM. Ко 2-3-й неделе заболевания специфический иммуногенез достигает наивысшего развития (преобладают О-антитела IgM). В это же время появляются IgG-антитела, титр которых в последующем нарастает, а антител IgM — снижается. Формирование клеточного иммунитета индуцируется антигенами сальмонелл тифа в меньшей степени, нежели гуморального, что является следствием глубокого дефицита общего пула Т-клеток и Т-хелперов, а также умеренного снижения Т-супрессоров.
Циклическое течение брюшного тифа может проявляться пятью периодами патогенетических изменений в тонкой кишке, иногда поражается и толстая кишка. Первый период (1-я неделя болезни) характеризуется значительным набуханием групповых лимфатических фолликулов; второй (2-я неделя) сопровождается некрозом этих образований. Во время третьего периода происходит отторжение некротических масс и формирование язв. Четвертый (3—4-я недели) называют периодом чистых язв. В пятом периоде (5—6-я недели) происходит заживление язв. При лечении антибиотиками патогенетические изменения кишечника могут развиваться уже на фоне нормализации температуры тела.
Постинфекционный иммунитет при брюшном тифе является строго специфичным и может длительно сохраняться (15—20 лет). Однако в настоящее время имеются наблюдения повторных заболеваний брюшным тифом через сравнительно короткие промежутки времени (1,5—2 года), что чаще всего связывают с нарушением иммуногенеза в результате анти-биотикотерапии.
Возбудители брюшного тифа, паратифов
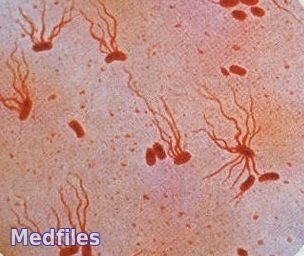
Возбудителя брюшного тифа (S. typhi) выявил впервые немецкий гистолог Эберт в 1880 г., увидевший его при микроскопии гистологических препаратов – срезов селезенки, периферических лимфоузлов и пейеровых бляшек, взятых у умерших от тифа больных. В 1884 г. Гаффки получил чистую культуру возбудителя. В этом же году А. Брион и Х. Кайзер описали возбудителя паратифа А (S. paratyphi A), а Г. Шоттмюллер – возбудителя паратифа В (S. paratyphi В). Этих сальмонелл выделили в чистой культуре и изучили Ашар и Бедсон в 1896 г.
Родовое название связано с именем американского ветеринарного врача Д. Сальмона, который в 1885 г. выделил возбудителя сальмонеллезов (S. choleraesuis) от больных свиней. В 1888 г. Гертнер выделил S. enteritidis из мяса и селезенки коров, погибших от острой пищевой инфекции. В 1890 г. Леффлер, 1893 г. С.С. Мережковский и 1900 г. Даниш обнаружили другого возбудителя S. typhimurium, вызвавшего аналогичные заболевания у человека и у мышей.
В 1934 г. Ф. Кауфман и П. Уайт разработали классификацию сальмонелл по антигенной структуре.
(вызывают заболевания у человека и животных)
S. typhi (палочка Эберта-Гаффки)
S. paratyphi A (палочка Бриона-Кайзера)
S. paratyphi В (палочка Шоттмюллера)
Однако в большинстве учебных пособий и справочников для удобства используется исторически сложившаяся таксономия, рассматривающая серовары, как виды (например, S . typhi , вместо S . enterica подвид enterica серовар Typhi )
Морфология и тинкториальные свойства.
Мелкие грамотрицательные палочки с закругленными концами размером 0,7-1,5?2-5 мкм, в мазках располагаются беспорядочно, подвижны (перетрихи), имеют пили I и II типов, S . typhi – микрокапсулу, спор не образуют.
Факультативные анаэробы, хемоорганогетеротрофы. Не требовательны к условиям культивирования: оптимальная температура роста 370С, значение рН 6,8-7,2, длительность культивирования – 24-48 часа. Хорошо растут на простых питательных средах (МПБ, МПА). В МПБ наблюдается рост в виде диффузного помутнения с последующим образованием осадка. На МПА образуют колонии в S - (средних размеров, гладкие, блестящие, полупрозрачные с голубоватым оттенком) и R -форме, S . paratyphi В и S . enteritidis по краю колоний формируют слизистый валик. В качестве накопительных сред используют желчный и селенитовый бульон. На дифференциально- диагностических средах Эндо, Левина и Плоскирева образуют бесцветные колонии (не ферментируют лактозу). На висмут-сульфитном агаре – колонии черного цвета с металлическим блеском, окруженные черным ободком прокрашенной среды.
Сальмонеллы обладают выраженной ферментативной активностью. Оксидазоотрицательны и каталазоположительны. Реакция Фогеса-Проскауэра отрицательная. Сахаролитическая активность: не расщепляют лактозу и сахарозу; глюкозу, маннит, мальтозу и другие сахара разлагают до кислоты и газа (исключение, S . typhi – до кислоты), по способности разлагать ксилозу и арабинозу различают 4 типа: К+А+; К-А-; К+А-; К-А+. Протеолитические свойства: не образуют индол, желатин не разжижают, образуют H 2 S (исключение, S . paratyphi A ).
Антигенная структура сальмонелл – сложная, имеются О-, Н-, Vi -, М-антигены.
* О – соматический антиген, липополисахарид клеточной стенки, термостабильный, (выдерживает кипячение в течение 2,5 часов, автоклавирование при 1200 С – 30 мин.), чувствительны к формальдегиду, но устойчив к спирту, групповой – согласно классификации Кауфмана-Уайта, семейство делится на 67 серогрупп (А, В, С, Д…). О-АГ состоит из R -ядра и боковой S -цепи, к которой присоединяются сахара – рецепторы (обозначаются цифрами). Общность конечного сахара (по химической природе является 3,6-дидезоксигексозой) является основанием для объединения в серогруппу. Некоторые группы имеют общие О-АГ, но каждая группа содержит один основной антиген: в группе А – 2, в группе В – 4, в группе С – 7, Д – 9…
* Н – жгутиковый антиген, белок флагеллин, термолабильный (разрушается при нагревании до 75-100С, а также под действием соляной кислоты, спирта, протеолитических ферментов), типовой (более 250 сероваров, расположены в алфавитном порядке в таблице Кауфмана-Уайта). У Н-АГ сальмонелл различают 2 фазы: I (специфическая) – различна у серотипов, входящих в одну группу, обозначается строчными латинскими буквами; II (неспецифическая) – содержат в своем составе общие для всей группы компоненты, обозначается арабскими цифрами. Если у серовара присутствуют обе фазы Н-АГ, то его называют двухфазным, если одна – монофазным.
* Vi -АГ – поверхностный полисахаридный антиген S . typhi , являющийся разновидностью К-АГ, термолабильный (разрушается при кипячении за 10 минут), чувствительный к соляной кислоте и спирту, встречается только у вирулентных сальмонелл, препятствует агглютинации О-антисыворотками, является рецептором для бактериофагов.
* М-АГ – слизистый, водонерастворимый, разрушается под действием кислот и спиртов.
* эндотоксин – липополисахарид клеточной стенки, высвобождается при массовой гибели возбудителей, играет основную роль в патогенезе брюшного тифа, оказывая пирогенное и токсическое действие;
* возбудители сальмонеллезов выделят экзотоксины – термолабильный белковый энтеротоксин, сходный с холерогеном и LT -токсином E . coli (увеличивают в клетках эпителия тонкого кишечника содержание цАМФ, что приводит к повышенному выходу воды из клеток и развитию диареи) + цитотоксическое действие, вызывая гибель энтероцитов.
2. Ферменты патогенности: гиалуронидаза, фибринолизин, лецитиназа, муциназа, протеаза, супероксиддисмутаза (инактивирует суперактивные радикалы О2, что придает устойчивость к фагоцитозу).
3. Структурные и химические компоненты клетки:
* пили I и II типов;
* микрокапсула у S . typhi ;
* белки наружной мембраны – инвазины (обеспечивающие инвазию слизистой и резистентность к фагоцитозу, позволяющую сальмонеллам сохраняться и размножаться внутри фагоцитов);
Резистентность у сальмонелл – достаточно высокая. Выдерживают рН в диапозоне 4-9, в водоемах, сточных водах, почве сохраняют жизнеспособность до 3 месяца, в комнатной пыли – от 80 до 550 дней. Хорошо переносят низкие температуры: во льду сохраняются более 60 дней, в замороженном мясе – 6-13 месяцев (в толще мяса могут сохраняться и после тепловой обработки), размножается в мясном фарше при +50С, в яйцах – до 13 месяцев (при хранении яиц в холодильнике могут проникать через неповрежденную скорлупу и размножаться в желтке), в колбасе – 2-4 месяца, в хлебе – до 3-х месяцев, на овощах и фруктах – 5-10 дней. Хуже выдерживают высокую температуру: при 560 С выдерживают 40-60 минут, при 700 С погибают через 10 минут, при 1000 С – моментально. Чувствительны к дезрастворам в рабочей концентрации (5% фенол, 3% хлорамин, 3% лизол вызывают гибель бактерий через 2-3 минуты) и антибиотикам.
Брюшной тиф (название болезни дал Гиппократ, происходит от греч. typos – туман, спутанное сознание) – острое антропонозное инфекционное заболевание, характеризующееся поражением лимфоидного аппарата тонкого кишечника, бактериемией, выраженной лихорадкой, интоксикацией и розеолезной сыпью. Паратифы А и В сходны по характеру и клиническим проявлениям с брюшным тифом, но протекают более легко.
Сальмонеллезы – группа полиэтиологичных острых зооантропонозных кишечных инфекций, протекающих по типу гастроэнтеритов у взрослых и токсико-септических инфекций у детей.
Источник инфекции: больные и бактерионосители.
Механизм передачи: фекально-оральный (пути: пищевой, водный, контактно-бытовой). Брюшной тиф и паратиф А распространяются чаще водным путем (употребление воды из неглубоких загрязненных водоемов, технических водопроводов, в случаях прорыва канализационных вод). При паратифе В преобладает пищевой путь (заражение чаще происходит через молоко, молочные продукты, кремы, овощные салаты). Бытовой путь реализуется, как правило, через бактерионосителей.
Патогенез и клинические особенности брюшного тифа и паратифов А и В .
1. Стадия внедрения возбудителя: сальмонеллы попадают в организм через рот и преодолев барьеры неспецифической защиты организма, проникают в тонкий кишечник, где происходит их адгезия к энтероцитам за счет пилей I типа.
2. Стадия поражения лимфоидной ткани: поражают пейеровы бляшки тонкого кишечника, в лимфатических фолликулах тонкой кишки сальмонеллы фагоцитируются макрофагами, с которыми проникают сначала в лимфоузлы, затем через грудной проток и в кровь.
3. Бактериемия (конец инкубационного периода): с током крови макрофаги вместе с поглощенными сальмонеллами циркулируют по организму (микроорганизмы могут даже в них размножаться).
4. Интоксикация: под воздействием бактерицидных факторов крови сальмонеллы погибают и при этом высвобождается эндотоксин, обусловливая лихорадку и сильнейшую интоксикацию, которая сохраняется на протяжение всего заболевания. (соответствует периоду выраженных клинических проявлений заболевания, температура тела достигает 39-400С и держится от 4 до 8 недель).
5. Стадия паренхиматозной диффузии: макрофаги с сальмонеллами циркулируют по организму и после гибели фагоцитов микробы могут попасть в различные органы: костный мозг, селезенку, печень, желчный пузырь, кожа и т.д. (воспаление, образование гранулем).
6. Выделительно-аллергическая стадия: вместе с желчью возбудители снова попадают в тонкий кишечник, при повторном контакте с сенсибилизированной лимфоидной тканью развивается гиперчувствительность немедленного типа (феномен Артюса), что приводит к некрозу пейеровых бляшек и образованию язв (кишечные кровотечения, прободение кишечника). По мере накопления антител организм постепенно освобождается от возбудителя – они выделяются со слюной, потом, испражнениями, желчью и мочой.
Инкубационный период – 10-14 дней. Клиника брюшного тифа, паратифов А и В характеризуется циклическим течением и проявляется лихорадкой (повышение температуры тела до 39-400С), интоксикацией, появлением розеолезной сыпи, гепатолиенальным синдромом,нарушениями со стороны нервной (бред, галлюцинации) и сердечно-сосудистой (падение АД, коллапс…) систем. Выздоровление не всегда совпадает с освобождением организма от возбудителей, этот процесс затягивается; 5 % переболевших становятся бактерионосителями.
Патогенез и клинические особенности сальмонеллезов .
Возбудители попадают в организм человека с обсемененными пищевыми продуктами. В желудке происходит частичная гибель сальмонелл. Воротами инфекции являются клетки слизистой тонкого кишечника. Здесь сальмонеллы внедряются между ворсинками, колонизируют и повреждают их. Это вызывает умеренное воспаление слизистой оболочки. Эндотоксин, выделяющийся при разрушении сальмонелл, обуславливает интоксикацию. Вырабатываемый сальмонеллами экзотоксин (энтеротоксин) вызывает диарею и рвоту, нарушение водно-солевого обмена и обезвоживание организма. Он обладает также цитотоксическим действием, вызывая гибель энтероцитов. Сальмонеллы проникают в подлежащие ткани слизистой оболочки, транспортируются через нее в макрофаги и могут поступать в лимфу и кровь, вызывая бактериемию и генерализацию инфекционного процесса.
Короткий инкубационный период – 12-24 часа. Начала заболевания – острое: озноб, повышение температуры до 390С, интоксикация (головная боль, слабость, тошнота), боли в животе, диспептические расстройства (рвота, понос), признаки обезвоживания организма, падение АД. Заболевание протекает обычно в течение 3-5 дней и заканчивается выздоровлением. При генерализованных формах сальмонеллез протекает более тяжело и длительно. Как субклиническую форму сальмонеллеза рассматривают бактерионосительство (острое – до 3 месяцев, хроническое – более 3 месяцев).
Постинфекционный иммунитет при брюшном тифе и паратифах – гуморальный, напряженный, длительный (не менее 15-20 лет, часто пожизненный). Образуются антитела к О-, Н-, Vi-антигенам:
* Первыми к концу 1-й недели заболевания появляются антитела к О-АГ, достигая максимума к периоду разгара (14-15 дней), а затем исчезают.
* Антитела к Н-АГ появляются к концу 2-й недели, достигая максимума в период реконвалесценции и длительно сохраняясь в организме после перенесенного заболевания.
* Антитела к Vi-АГ обнаруживаются у бактерионосителей брюшного тифа.
Постинфекционный иммунитет при сальмонеллезах – гуморальный и клеточный, типоспецифический, ненапряженный и недлительный, опосредован SIgA.
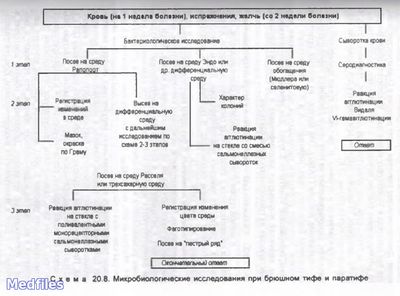
Микробиологические исследования при брюшном тифе и паратифе
Исследуемый материал: выбор материала для исследования при брюшном тифе и паратифах определяется стадией заболевания (инкубационный период – испражнения, продромальный период, 1-я неделя заболевания – кровь на посев, разгар заболевания и период реконвалесценции, с конца 2-ой недели – моча, испражнения, желчь, соскоб из розеол, костный мозг…, кровь на серодиагностику), при сальмонеллезах – испражнения, рвотные массы, промывные воды желудка, пищевые продукты, кровь.
1. Бактериоскопический метод.
2. Бактериологичекий метод (основной).
3. Серологический метод:
* Реакция Видаля (развернутая РА с О- и Н-антигенами);
* РНГА с эритроцитарными О-, Н-, Vi-диагностикумами;
4. Молекулярно-биологический метод (ПЦР, ДНК-зонды).
5. Аллергологический метод (кожно-аллергическая проба с эбертином).
Специфическая профилактика проводится по эпидпоказаниям:
- Вакцина ТАБТе – химическая сорбированная вакцина (содержит полные антигены брюшнотифозные, паратифозные А и В, столбнячный анатоксин);
- Брюшнотифозная спиртовая вакцина, обогащенная Vi- антигеном;
Неспецифическая профилактика : ранняя диагностика и изоляция больных, дезинфекция в очаге инфекции, выявление бактерионосителей, соблюдение санитарного режима в детских учреждениях, предприятиях питания, санитарно-бактериологический контроль за работой систем централизованного и нецентрализованного водоснабжения.
Лечение : ХТП и антибиотики; при сальмонеллезах применяется, в основном, патогенетическая терапия, направленная на нормализацию ВЭБ (антибиотики назначают только при генерализованных формах); спецефическое лечение – брюшнотифозные и сальмонеллезные бактериофаги.
Бактерии брюшного тифа и паратифов вызывают заболевания, сходные по патогенезу, клинике и эпидемиологии. Возбудитель брюшного тифа впервые описан Эбертом в 1880 г., паратифозные бактерии — Ашаром и Бансодом (1896), и дифференцированы Шоттмюллером на два вида: S. paratyphi А. и S. schottmulleri.
В современной систематике бактерии брюшного тифа, паратифов и возбудители пищевых токсикоинфекций на основании их антигенной структуры и других признаков объединены в один род Salmonella (в честь бактериолога Салмона).
Морфология. Палочки по величине и форме сходны с кишечными, имеют в среднем от 2 до 3 мк в длину и от 0,5 до 0,7 мк в толщину (см. рис. 78). Спор и капсул не образуют, хорошо подвижны, грамотрицательны.
Культуральные и биохимические свойства. Тифозные и паратифозные бактерии растут на простых питательных средах в аэробных условиях. Оптимум роста между 30 и 37°.

Рис. 79. Сальмонеллы паратифа Б. Колонии на мясо-пептонном агаре. Ув. 12
На чашках с агаром колонии палочки брюшного тифа и паратифов имеют вид умеренно выпуклых влажных прозрачных дисков, более мелких и нежных, чем колонии кишечной палочки (рис. 79). Колонии палочки паратифа В отличаются характерной особенностью строения, которая заключается в образовании по периферии колонии приподнятого слизистого валика, окружающего плоский центр колонии наподобие бортика пуговицы. Валик появляется при хранении посевов (после 24-часового стояния в термостате) в течение нескольких последующих дней при комнатной температуре.
Колонии тифозной и паратифозных палочек, выделенные в начале и в разгаре болезни, имеет гладкую форму (тип S), а полученные в стадии выздоровления часто растут в виде шероховатых форм (тип R), состоящих из маловирулентных бактерий.
При посеве штрихом на скошенном агаре получается сплошной по черте рост, сначала нежный с голубоватым отливом, затем грубый, но нежнее роста кишечной палочки. На бульоне появляется диффузный рост.
На молоке тифозные и паратифозные палочки обильно размножаются, причем молоко не створаживается. Лактозу они не сбраживают, а глюкозу, мальтозу и маннит разлагают брюшнотифозные бактерии только до кислоты, паратифозные до кислоты и газа. Ферментативные свойства паратифозных бактерий в общем сходны, но бактерии паратифа А менее активны, газообразование незначительно и появляется позже.
Биохимические свойства бактерий кишечно-тифозной группы
| Вид микроба |


