Некроз тазобедренного сустава вич

Актуальность исследования. Операция по замене тазобедренного суставапозволяет человеку вернуться к полноценной жизни и распрощаться с теми артрозными симптомами, которые мешали испытывать жизненные радости много лет подряд. Как показывают исследования, осложнения после эндопротезирования тазобедренного сустава развиваются у 1% молодых людей и у 2,5% пожилых пациентов [3, с.341; 6, с.70]. По данным Joseph T., King Jr. (Yale University School of Medicine) и его коллег в исследовании, посвященном послеоперационной летальности у ВИЧ-инфицированных пациентов при эндопротезировании тазобедренного сустава, смертность в тридцатидневный период после операций составила 3,4%, тогда как у людей без ВИЧ-инфекции – 1,6% (разница в 2,11 раза) [3, с.341; 4; 6, с.71]. Послеоперационная смертность у ВИЧ-инфицированных была выше, чем у людей без ВИЧ, при любом уровне CD4-клеток, однако, уровень CD4-клеток значимо влиял на таковые риски в пределах группы ВИЧ-инфицированных [3, с.142; 6, с.72].
После корректировки потенциально значимых факторов исследователи обнаружили, что по сравнению с ВИЧ-отрицательной группой ВИЧ-инфицированные, которые имели 500 или больше CD4-клеток, имели риски 30-дневной послеоперационной летальности в 1,92 выше, чем у ВИЧ-отрицательных; при иммунном статусе (ИС)от 200 до 499 CD4-лимфоцитов – в 1,89 раза выше; при ИС от 50 до 199 клеток – в 2,66 раза; и при уровне CD4 менее 50 клеток/мкл – в 6,21 [1; 2; 4, с.133; 5].
Цель исследования – изучить актуальные вопросы эндопротезирования тазобедренного сустава у ВИЧ-инфицированных пациентов по данным литературы и по клиническим случаям больниц города Пермь.
Задачи исследования. Одной из важных задач является выявление всевозможных причин развития постоперационных осложнений у ВИЧ-инфицированных пациентов при эндопротезировании. Провести выборку и рассмотреть истории болезни пациентов травматологических отделений с ВИЧ-статусом, перенесших эндопротезирование тазобедренного сустава. Провести анализ полученных данных.
Нами изучены доступные литературные источники по проблеме эндопротезирования тазобедренного сустава у ВИЧ-инфицированных пациентов, в которых найдены ответы на такие вопросы как показания к операции, особенности хода операций, нюансы постоперационного ведения ВИЧ-инфицированных пациентов, возможные постоперационные осложнения, тактика борьбы с ними, постоперационная смертность ВИЧ-положительных пациентов ввиду развития осложнений.
Показания для эндопротезирования: Вполне естественно, что к выполнению замены тазобедренного сустава искусственным протезом должны быть весомые показания. В их основе лежит такое разрушение компонентов сочленения, при котором человек либо испытывает мучительную боль, либо не в состоянии выполнять элементарные движения пораженной конечностью. Другими словами, сустав перестает соответствовать своему физиологическому предназначению и становится ненужной частью организма, так как резко ухудшает качество жизни. В таких случаях эндопротезирование является единственным выходом их ситуации. К таким ситуациям относится: двусторонний деформирующий артроз II-III степени; односторонний деформирующий артроз II-III степени; деформирующий коксартроз III степени и анкилоз одного из крупных суставов на этой же конечности; односторонний коксартроз II-III степени одного тазобедренного сустава и анкилоз конрлатерального; двусторонний фиброзный или костный анкилоз тазобедренных суставов (болезнь Бехтерева); посттравматический коксартроз III степени на почве тяжелых повреждений вертлужной впадины; перелом и ложный сустав шейки бедренной кости у больных старше 70 лет; опухолевые процессы в головке и шейке бедренной кости, требующие резекции патологического очага.
Неприятные патологические ситуации, связанные с имплантацией, возникают нечасто. Однако они фиксируются, о чем должен быть проинформирован пациент. Согласно проводимым рандомизированным контролируемым исследованиям, получены следующие данные о наиболее распространенных проблемах: вывих головки протеза развивается примерно в 1,9 % случаев; септический патогенез – в 1,37 %;тромбоэмболия– в 0,3 %; перипротезный перелом возникает в 0,2 % случаев [3, с.341].
Второе по частоте неблагоприятное явление, характеризующееся активизацией тяжелых гнойно-воспалительных процессов инфекционной природы происхождения в районе установленного имплантата. Инфекционные антигены заносятся интраоперационно через недостаточно стерильные хирургические инструменты (редко) или после вмешательства по кровеносному руслу перемещаются от любого проблемного органа, имеющего болезнетворно-микробную среду (часто). Плохая обработка раневой зоны или слабое заживление (при диабете) также способствует развитию и размножению бактерий.
Гнойный очаг пагубно воздействует на прочность фиксации эндопротеза, вызывая его расшатывание и нестабильность. Гноеродная микрофлора трудно поддается лечению и, как правило, предполагает снятие имплантата и проведение повторной установки спустя продолжительное время. Основный принцип лечения – тест на установление вида инфекции, долгая и дорогостоящая антибиотикотерапия, обильный лаваж раны антисептическими растворами.
Для ВИЧ-инфицированных пациентов необходимо рассмотреть такой вопрос, как действие наркозного пособия. Общая анестезия существенно влияет на иммунную систему, приводя к еще большему ее угнетению. Ряд препаратов (тиопентал, сукцинилхолин, изофлюран, дроперидол, фентанил, кетамин) вызывает угнетение системы комплемента, подавление фагоцитоза и антителозависимой цитотоксичности, снижая потенциал антибактериальной защиты. В результате воздействия этих анестетиков в крови больных увеличивается скорость синтеза фактора некроза опухоли, α- и β-интерферонов, что вызывает гиперактивацию лимфоцитов, а значит – усиливает проявления воспаления.
Наиболее прогностически значимым является уменьшение содержания NK-клеток – естественных киллеров, осуществляющих противоопухолевую и противовирусную защиту, поскольку именно они являются наиболее чувствительным звеном этого воздействия и считаются самыми информативными критериями реактивности организма после операции. Оперативные вмешательства, выполненные под общей анестезией, могут приводить к нарушениям клеточного и гуморального иммунитета, снижению фагоцитарной активности и естественных киллеров, угнетению противоопухолевой защиты.
Таким образом, пациенты с тяжелой сопутствующей патологией и неблагоприятным фоновым заболеванием в форме ВИЧ-инфекции относятся к категории пациентов с потенциально высоким риском гематогенной диссеминации как источника инфекции в области эндопротеза.
В группе выборки, состоящей из 11 ВИЧ-инфицированных пациентов, которым было проведено одностороннее эндопротезирование тазобедренного сустава, наблюдалось постоперационное осложнение в форме парапротезного остеомиелита. У 9 пациентов данный процесс развивался в большом вертеле бедренной кости, у 2 пациентов процесс распространялся так же на вертлужную впадину. У всех исследуемых заболевание в течение трех месяцев перешло в форму хронического остеомиелита. Рецидив в форме обострения остеомиелита также наблюдался у всех пациентов. В течение года 10 пациентов погибли, у 9 из которых был установлен диагноз диссеминированного молниеносного септического состояния, 1 пациент умер от передозировки наркотическими препаратами. У 11-го пациента заболевание рецидивирует в течение последних 6 лет. На сегодняшний день у него определяется полный лизис большого и малого вертела, нарушение костной структуры вертлужной впадины с ее переломом и вклинением в малый таз чаши эндопротеза и полным вывихом головки эндопротеза (рис. 1).
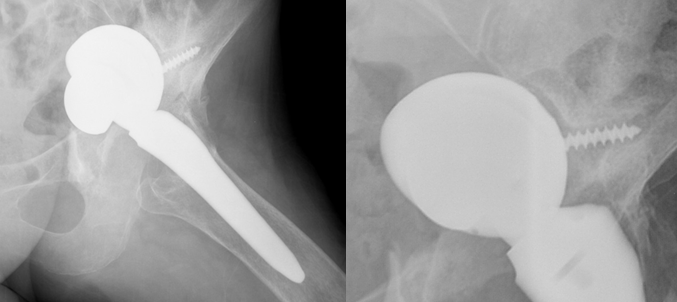
Рис. 1. Рентгенография левого тазобедренного сустава в 2-х проекциях
(На рентгенограмме левого тазобедренного сустава (вынужденное положение - пациент не может разогнуть левую нижнюю конечность в положение стандартной укладки), произведено рентгеноскопическое исследование с прицельным снимком левого тазобедренного сустава в прямой проекции: состояние после эндопротезирования левого тазобедренного сустава, неадекватное стояние протеза: чаша фиксирована одним шурупом, вывернута, пролябирует в полость малого таза, крыша вертлужной впадины четко не определяется, головка эндопротеза расположена вне чаши, стояние ножки и централизатора эндопротеза в проекции центральной оси диафиза бедра)

ВИЧ был обнаружен и зарегистрирован в 1983 году [1]. ВИЧ-инфекция разрушает иммунную систему и вызывает СПИД, что в свою очередь увеличивает риск развития катастрофических оппортунистических инфекций и онкологических заболеваний [2].
К наиболее пораженным субъектам Российской Федерации (по предварительным данным) относятся: Свердловская (зарегистрировано 1511,0 живущих с ВИЧ на 100 тыс. населения), Иркутская (1503,7), Кемеровская (1448,2), Самарская (1373,5), Оренбургская (1128,2), Ленинградская (1116,3) области, Ханты-Мансийский автономный округ (1094,9), Тюменская (1093,9), Челябинская (943,7) области, г. Санкт-Петербург (941,3) [3].
В Российской Федерации в 2015 г. среди ВИЧ-инфицированных по-прежнему преобладали мужчины (63,0%), большая часть из них заразились при употреблении наркотиков. К 1 ноября 2015 г. в России было зарегистрировано более 364 тысяч инфицированных ВИЧ женщин, которые преимущественно инфицировались при половых контактах с мужчинами.
Среди впервые выявленных в 2015 г. ВИЧ-позитивных с установленными факторами риска заражения 53,6% инфицировались при употреблении наркотиков нестерильным инструментарием, 42,8% – при гетеросексуальных контактах, 1,5% – при гомосексуальных контактах, 2,1% составляли дети, инфицированные от матерей во время беременности, родов и при грудном вскармливании [4, 5, 6].
В настоящее время для лечения ВИЧ-инфекции используются высокоэффективные антиретровирусные препараты (ВААР терапия), которые включают мощные ингибиторы протеазы или ингибиторы обратной транскриптазы. Использование данных препаратов привело к увеличению продолжительности жизни ВИЧ-инфицированных и снижению развития оппортунистических инфекций.
Исследование N. Lohse позволяет прогнозировать более чем 35-летнюю выживаемость молодых ВИЧ-инфицированных людей, получающих современную терапию [7].
Наряду с этим все большее внимание врачей привлекают заболевания, возникающие у ВИЧ-положительных пациентов. Одним из таких заболеваний является асептический некроз головки бедренной кости (АНГБК). Асептический некроз головки бедренной кости (АНГБК) — тяжелое хроническое заболевание, вызванное недостаточностью местного кровообращения, которое ведет к разрушению костной ткани в головке бедра.
На ранних стадиях заболевание, как правило, протекает бессимптомно, а уже при наличии болевого синдрома остается чаще всего только один вариант лечения – хирургический. Боль, связанная с аваскулярным некрозом бедра, может сосредоточиться в паховой области, бедрах или крестцово-подвздошном сочленении, маскируя проблему и вынуждая пациентов долгое время получать лечение у неврологов по поводу остеохондроза позвоночника.
Почему асептический некроз головки бедренной кости является проблемой у ВИЧ-инфицированных людей?
Некоторые эксперты считают, что это может быть результатом хронической ВИЧ-инфекции. Другие считают, что длительное применение препаратов, таких как ингибиторы протеазы или стероиды, может привести к повреждению кровеносных сосудов, питающих головку бедра. Третьи считают, что метаболические изменения в организме, которые являются общими у ВИЧ-положительных людей, могут иметь значение в развитии асептического некроза [8].
И ВИЧ-инфекция, и лечение ВААРТ являются факторами риска для остеонекроза головки бедренной кости [9]; риск в 100 раз выше для ВИЧ-инфицированных пациентов, чем для населения в целом.
Американские ученые обнаружили необычайно высокий процент асептического некроза головки бедренной кости при МРТ-исследовании у ВИЧ-инфицированных. Данное исследование проведено у 339 ВИЧ-инфицированных пациентов, и процент с асептическим некрозом головки бедренной кости составил 4,4% [10].
В настоящее время не существует лечения, которое останавливает или лечит асептический некроз. Наркотические и ненаркотические обезболивающие препараты можно использовать краткосрочно для снятия симптомов. Нестероидные противовоспалительные средства могут уменьшать отек и воспаление в области тазобедренного сустава и могут использоваться для купирования болевого синдрома, связанного с асептическим некрозом.
Существуют, конечно, хирургические методы лечения, которые направлены на улучшение притока крови к пораженной области, однако чаще всего требуется тотальное эндопротезирование тазобедренного сустава для восстановления функции нижней конечности.
Распространено мнение, что иммунодефицит у ВИЧ-инфицированных больных увеличивает частоту инфекционных осложнений тотального эндопротезирования тазобедренного сустава. Parvizi с соавторами при анализе 21 операции тотального эндопротезирования тазобедренного сустава у ВИЧ-позитивных пациентов отметили возникновение глубокой инфекции у 6 пациентов. Авторы связали частоту осложнений со снижением количества СD4-лимфоцитов до 239±112 мкл [11].
По данным Калифорнийского университета в США в период c 2002 по 2008 гг. в США выполнено 8229 операций эндопротезирования у ВИЧ-инфицированных больных, что составило 0,14% от общего количества операций эндопротезирования. При этом эндопротезирование тазобедренного сустава составило 6449 пациентов – 79%. Частота инфекционных осложнений у ВИЧ-инфицированных больных в 2 раза превысила количество данных осложнений у ВИЧ-негативных пациентов и составила 0,6% [12].
Haberman с коллегами сообщили о развитии инфекции после тотального эндопротезирования тазобедренного сустава в 12,7% случаев в группе из 41 ВИЧ-инфицированного пациента, при этом не отмечено снижения CD4-лимфоцитов [13].
При исследовании пациентов, имеющих в анамнезе наркоманию и перенесших тотальное эндопротезирование тазобедренного сустава, Wieser с соавторами отметили возникновение септических осложнений в 70% случаев за период в 10 лет наблюдений и не нашли связи септических осложнений с положительными серологическими реакциями на ВИЧ [14].
Hicks с соавторами в результате многоцентрового ретроспективного анализа показали, что существует повышенный риск развития септических осложнений после тотального эндопротезирования тазобедренного сустава у ВИЧ-положительных, больных гемофилией [15].
Наблюдения Lubega не обнаружили различий в послеоперационном периоде при краткосрочном наблюдении за 14 пациентами (перенесшими 18 ТЭП), которые были ВИЧ-положительными, и 28 пациентами, которые были ВИЧ-отрицательными [16].
Tornero E. в своем исследовании показывает, что исход эндопротезирования тазобедренного сустава у ВИЧ-положительных пациентов не хуже, чем у ВИЧ-отрицательных пациентов [17].
В Южно-Африканском университете им. Нельсона Манделы в период с 2000 по 2001 гг. выполнено 14 операций тотального эндопротезирования тазобедренного сустава у ВИЧ-инфицированных пациентов с использованием эндопротезов бесцементной фиксации. В период до 72 месяцев у троих пациентов отмечено снижение количества CD4-лимфоцитов ниже 200 клеток в 1 мм 3 , и эти пациенты получали антиретровирусную терапию, однако инфекционных осложнений зарегистрировано не было [18].
Ta-I Wang с соавторами сообщили о 6 ВИЧ-положительных пациентах, которым в общем выполнено 10 оперативных вмешательств с 2000 по 2009 гг. Из них 7 – эндопротезирование тазобедренного сустава, два – коленного сустава и одно – эндопротезирование плечевого сустава. За период наблюдения в 38,6 месяца инфекционных осложнений не выявлено [19].
Graham SM сообщил о краткосрочном наблюдении и функциональном результате после тотального эндопротезирования тазобедренного сустава в группе ВИЧ-инфицированных пациентов, которые не страдают гемофилией и не имеют в анамнезе внутривенного употребления наркотиков. В общей сложности 29 пациентов подверглись 43 операциям тотального эндопротезирования тазобедренного сустава со средним сроком наблюдения от 6 месяцев до 3 лет. В группе было 10 женщин и 19 мужчин, средний возраст которых составил 47 лет и 7 месяцев (от 21 года до 59 лет и 5 месяцев). В период наблюдения инфекционных осложнений не было. Средняя предоперационная оценка по шкале Харриса была 27 (от 6 до 56), средняя послеоперационная была 86 (от 73 до 91), давая среднее улучшение на 59 пунктов [20].
Таким образом, при анализе зарубежной литературы мы не выявили единого мнения на предмет увеличения частоты инфекционных осложнений у ВИЧ-инфицированных пациентов, подвергшихся плановой операции тотального эндопротезирования тазобедренного сустава и влияния уровня CD4-лимфоцитов.
Цель исследования. На собственном клиническом материале выяснить причинно-следственные связи между ВИЧ-инфекцией и АНГБК, а также сравнить пред- и послеоперационный период после тотального эндопротезирования тазобедренного сустава у здоровых и больных людей. Оценить риски развития осложнений.
Материалы и методы. За последние 5 лет в период с 01.01.2011 по 31.12.2015 гг. в ФБГУ РНИИТО им. Р.Р. Вредена были госпитализированы 166 ВИЧ-инфицированных пациентов. Из них экстренная госпитализация у 50 пациентов (30%), плановая – у 116 (70%). Средний возраст пациентов 29,9 лет, от 22 до 66 лет. Среди всех госпитализированных ВИЧ-инфицированных преобладали мужчины ¾ 115 (69,3%) человек, женщины составили 51 человека (30,7%). Жители Санкт-Петербурга составили 85 (51,2%), Ленинградской области ¾ 25 (15%).
С патологией тазобедренного сустава госпитализировались 43 пациента, что составило 25,9% от общего числа ВИЧ-госпитализированных больных и 37% от числа плановых госпитализаций ВИЧ-инфицированных пациентов.
В отделении № 11 в период с 2012 по 2016 гг. выполнено 15 оперативных вмешательств у 13 ВИЧ-инфицированных пациентов, из них 3 операции реэндопротезирования у пациентов с асептической нестабильностью, на момент первичного эндопротезирования у этих больных ВИЧ не диагностировался, одно реэндопротезирование после установки спейсера, который был установлен пациентке с септическим некрозом головки бедренной кости после металлоостеосинтеза перелома шейки бедра. У двух пациентов выполнено двустороннее эндопротезирование с периодом между операциями 6 месяцев. У всех прооперированных пациентов уровень CD4-лимфоцитов перед операцией был более 300 клеток в 1 мм 3 . У троих пациентов на основании анамнеза зафиксировано внутривенное употребление наркотических препаратов, однако последняя инъекция произведена более чем за 3 года до операции.
Результаты и обсуждение. За период наблюдения от 3 до 42 месяцев инфекционных осложнений в области оперированного сустава не зарегистрировано. Функциональная оценка по шкале Харриса до операции составила от 38 до 52 баллов, через 3 и более месяца после операции – от 89 до 95 баллов, то есть отмечены хорошие и отличные функциональные результаты и значительное купирование болевого синдрома.
Таким образом, подводя итоги обзора литературы и личного клинического опыта, можно сказать, что возраст людей, пораженных АНГБК, страдающих ВИЧ-инфекцией, ниже, чем у тех, кто обладает ВИЧ-отрицательным статусом.
Также можно сделать вывод, что наличие ВИЧ не является главной причиной возникновения асептического некроза. Более того, исследования показывают, что развитие осложнений происходит примерно с одинаковой вероятностью как у ВИЧ-отрицательных, так и у ВИЧ-положительных людей. Именно по этой причине эндопротезирование тазобедренного сустава может существенно улучшить качество жизни ВИЧ-инфицированных пациентов с заболеваниями тазобедренного сустава.
Однако предыдущие доклады по этой проблеме показали высокие показатели инфицирования ВИЧ-положительных пациентов, которым выполнялось тотальное эндопротезирование тазобедренного сустава [21, 22].
При глубоком и осмысленном анализе литературы всплывает еще одна патология, которая сопровождает ВИЧ-инфекцию, – гемофилия, представляющая собой патологию коагуляционной системы. И большинство негативных результатов с возникновением ранней перипротезной инфекции возникает у такой группы пациентов.
Так, в ретроспективном исследовании 102 случаев эндопротезирования тазобедренного сустава у ВИЧ-положительных пациентов из 8 центров гемофилии уровень инфицирования составил 18,7% при первичной артропластике и 36,3% при ревизии (средний срок наблюдения составил 5,7 лет) [15]. Кроме того, частота инфекционных осложнений у таких больных была значительно выше в группе с более низким предоперационным количеством CD4-лимфоцитов – в 49% случаев.
В другом исследовании из 27 артропластик коленного сустава и 7 – тазобедренного сустава у пациентов с ВИЧ-положительным статусом с гемофилией уровень ранних инфекционных осложнений составил 29,6% и 14,3% соответственно [21].
В исследовании, проведенном более 20 лет назад американскими коллегами, сообщалось, что 66 ВИЧ-положительных пациентов с предоперационным числом CD4 ≤ 200 клеток/мм 3 имели уровень инфицирования, достигающий 15,1% [22]. Авторы также сообщают об увеличении смертности у пациентов с ВИЧ-положительным статусом с числом лимфоцитов CD4 3 .
В настоящее время некоторые иностранные эксперты [20] предположили, что лучшее время для выполнения тотальной артропластики – когда количество CD4 составляет> 200 клеток/мм 3 , а другие > 400 клеток/мм 3 и не обнаруживается вирусная нагрузка [9].
К слову сказать, в немногих исследованиях упоминается вирусная нагрузка в качестве критерия повышения риска осложнений, в том числе инфекционных. В исследовании европейских коллег [23] 332 пациентов с ВИЧ-положительным статусом после ортопедических операций с вирусной нагрузкой из 30 000 к/мл имели высокий уровень осложнений, а другие исследователи сообщают об увеличении осложнений у ВИЧ-положительных пациентов с вирусной нагрузкой > 10 000 к. [24].
Таким образом, нет однозначного мнения и ясной картины о результатах и осложнениях после артропластики у ВИЧ-инфицированных пациентов.
В настоящий момент для решения вопроса о целесообразности эндопротезирования у данной группы пациентов, опираясь на опыт коллег из Европы, мы ориентируемся лишь на уровень CD4-лимфоцитов, а также на отсутствие терминальной стадии СПИД.
Исследования в этом направления будут продолжаться с целью разработки абсолютных противопоказаний для артропластики у ВИЧ-инфицированных пациентов или возможных корректирующих схем подготовки к этой плановой высокотехнологичной операции.
Коллективный опыт тотального эндопротезирования тазобедренного сустава в любом отечественном или западном медицинском учреждении небольшой и ограниченный, что требует дальнейшего изучения данной проблемы.
Здравствуйте!
Принимаю терапию с 2005 года. Сначала была схема комбивир+стокрин, затем видекс+эпивир+стокрин, затем комбивир+калетра и теперь абакавир+ламивудин+калетра.
В декабре 2014 заболели суставы, на данный момент развился двусторонний асептический некроз головки бедренной кости (АНГБК). В начале болезни я консультировалась с нашим инфекционистом местным, но он сказал, что терапия не может вызвать боли в суставах, ничего менять не нужно. Врач наш мягко говоря глуповат, но чтобы попасть в другой СПИД центр на консультацию, нужна прописка, мне ее негде взять. Мне оставалось только надеяться, что врач был прав и что терапия тут ни при чем. Сегодня же я с трудом двигаюсь на костылях, костные балки практически полностью разрушены, и я снова начала искать информацию на эту тему в сети . И появилось немного новой информации, которая доказывает, что все-таки именно терапия вызвала у меня этот некроз. И к тому же вот что я вычитала в инструкции к калетре , в побочных действиях:
"Со стороны опорно-двигательного аппарата
Часто: скелетно-мышечная боль, в том числе артралгия и боль в спине, миалгия, мышечная слабость, спазмы мышц; нечасто: рабдомиолиз, остеонекроз."
Примерно после выявления вич, у меня появились боли в суставах пальцев одной руки. В целом, тема влиянием вич на суставы понятна. Правильно ли я понял, что принимать статины можно в качестве профилактики целогл ряда проблемм, которые вызывает вич и терапия? Нужно ли получить назначение какого-то врача (какого?) или можно просто купить и принимать, как витамины? ))
Лучше с кардиологом согласовывать все же.
Добрый день. Пишу в эту ветку, т.к. первоначально ставили артроз левого тазобедренного сустава 1 степени.
На АРВТ с лета 2015. Сменили схему 14.03.2016 с калетры+дизаверокс на Невирапин+зидовудин+ламивудин (причиной стало отсутствие прогресса в цифрах-25.02.2016 ИС-213; ВН-н.о.). Далее всё пошло по плану: 14.04.2016 ИС-319; ВН-менее 50, 11.06.2016 УЗИ внутренних органов (печень, почки, поджелудочная)-норма, 21.07.2016 ИС-333; ВН-менее 500; ALT-196/40; AST-168/37; Гемоглобин 166; ОАК-норма.
22.08.2016 биохимия в МСК: Белок общ.77(66-87); Креатин 81(53-97); Билирубин общ. 16(5-21); AST-68(до 50); ALT-149(до 50); Глюкоза в сыв. 5.2(3.89-6.17); Холестерин 6.02(3.60-5.20); ЛПНП 3.65(1.61-5.44); С-реактивный белок 0.68(до 5). Проходил терапию печени (Гептор+Гепа Мерц+Эссенциале+аскорутин), потом забил, т.к. печень с повышенными печеночными показателями вела себя стабильно-жалоб не было.
Жалобы появились в ноябре 2016 после определенной нагрузки в спорт.зале-беговая дорожка 60 минут, после чего сильные тянущие боли в тазобедренном суставе, не мог нормально присесть и нагнуться. Дексаметазон мне в помощь был))) 25.01.17. сходил к хирургу в поликлинику по ДМС сделали рентген: R-признаки артроза 1ст., артрозоартрит лев.т/б сустава; УЗИ-признаки синовита левого т.б сустава, лигаментит. Назначили и выполнены курсы Arcocsia, Dona (Глюказамин), нимесил. Также выполнены физиопроцедуры-УВЧ, озокерит, фонофорез с гидрокортизоном. Физио помогли-боли из именно тазобедренного ушли, но по-прежнему не могу поднять ногу на 90 град. ни прямую, ни согнутую в колене, плохо встаю с постели, с раб.кресла (особенно если сразу на больную ногу).
Поехал в свой региональный СЦ (за 1000 км. от МСК) сдал анализы 09.03.2017.ИС-413; ВН-н.о. Тут вроде gut.
С хирургом и физио завязал. Пошел к неврологу. Осмотрела-критичного ничего нет, но назначила Об.моча, ОАК, УЗИ мягких тканей, рентген. 31.03.2017 УЗИ мягких тканей выявлен единичный лимфатический узел 12х5,5мм с четкой дифференцировкой эхоструктур, кровоток в области ворот в виде единичных сигналов. Заключение: признаки аденопатии бедренных лимфатических узлов слева. Результаты мочи, ОАК, рентгена будут 04.04.17 (сюда предоставлю, самому интересно)+встреча с неврологом 08.04.17 (расскажу, что услышу).
ВОПРОСЫ: 1.стоит ли делать МРТ хоть за свой счет? 2.МРТ только тазобедренной части делать или всего позвоночника? 3.Чего ожидать (т.к. по УЗИ я вычитал от аллергии и ЗППП, до онкологии)? 4.Надо полагать, что невролог от меня отпишется, направив к инфекционисту выявлять причины? 5.Брать выписку из поликлиники, где всё делали, и к своему инфекционисту? 6.Могут ли быть это побочки от действующей схемы или распространенная проблема у всех, требующая отдельной терапии как, например, с печенью при невирапине? 7.Что может/должен сделать мой инфекционист в моём случае?
Спасибо.
Итак, события продолжаю развиваться следующим образом. Невролог поликлиники и хирург-невролог, просмотрев меня всего и прокрутив на кушетке, проверив все симптомы и реакции, пришли к выводу, что боли в левом тазобедренном суставе всё же не от двух межпозвоночных грыж. Было назначено КТ, и оно от 16.10.2017 показало "КТ данные двухстороннего коксартроза 3 ст., на фоне асептического некроза головок бедренных костей. Левосторонний синовит".
В связи с постановкой данного диагноза у меня возникли вопросы:
1. связано ли это с текущей схемой - NVP 200 + ZDV 300 + ЗТС 150?
Инфекционист, увидев хромоту, и последнюю биохимию (ALT 124, AST 63, холестерин 6,8 и повыш щелочная фосфотаза), решила сменить схему на: ZDV 300 + ЗТС 150 + RTV 100 + DRV 600.
2. связано ли это решение с поставленным выше диагнозом (естественно, инфекционист и невролог не коммуницируют друг с другом, но, при этом, инфекционст запросила выписку по суставу).
1. маловероятно, но терапия очень не современная и очень напрашивается на модернизацию.
решила сменить схему на: ZDV 300 + ЗТС 150 + RTV 100 + DRV 600. Тенофовира нет? Зидовудин бы заменить на тенофовир и был бы однократный прием и вообще замечательно.
Спрошу. У врача буду в январе. Спасибо.
1,2,3 – план обследований и прогноз уточнять у специалиста. Я не эксперт тут.
4 – пока не проверите, не узнаете.
5 – вот не знаю.
6 – маловероятно.
7 – что может сделать кто-то… не знаю.
Скажите, пожалуйста, в чем разница между анализом СРБ и вчСРБ (который дороже)?
Как они кореллируют между собой?
Если представить для ясности, например, СРБ=1 мг/л, а вчСРБ - может ли при этом оказаться 2 или даже 5 мг/л? Или он просто добавит пару уточняющих цифр после запятой (типа 1,06 мг/л)?
вч — высокочувствительный, вся разница в аналитической чувствительности метода.
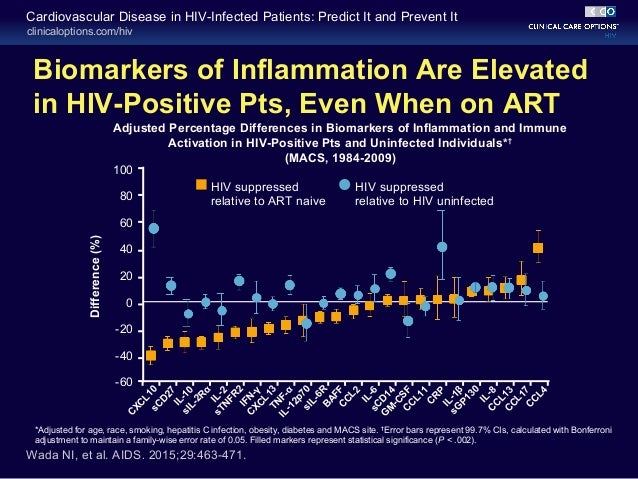
Вроде бы на слайде (выше) разброс показателей в графе AIDS меньше чем в целом по всей выборке (all cause death)--- т.е. для ВИЧ+ не обнаружено такой уж жесткой связи между смертностью и повышением уровня IL6?
Обнаружено. Для смерти от всех причин- связь достоверна, для смерти от причин, не связанных со СПИДОм- связь достоверна. О чем и рассказывается на указанной картинке. По отдельным нозологиям из разряда non-AIDS тоже всё довольно чётко :

RESULTS:
During approximately 24,000 person-years of follow-up (PYFU), 172 patients developed cancer (70 infection-related; 102 infection-unrelated). The risk of developing cancer was associated with higher levels (per doubling) of IL-6 (hazard ratio 1.38, P
Результаты. За период наблюдения 24000 человеко-лет онкологические заболевания развились у 172 пациентов ( 70 случаев были связаны с вич-инфекцией, 172 случая-нет ). Риск раковых заболеваний увеличивался при повышении ( вдвое) уровня ИЛ-6 (ОР 1.38, P по поводу других воспалительных IL
По поводу СРБ и D-димера понял для себя что надо мониторить, но пока все же не уяснил как часто. Раз в месяц, раз в квартал, чаще, реже?
В кардиологии по поводу СРБ и D-димера есть отдельные рекомендации и сложившаяся практика, в гайдах по ВИЧ-инфекции ничего такого нет. Но если посмотреть,что замеряется, например,в немецких клиниках или американских, нет, не в рамках КИ,это рядовые анализы,то там можно увидеть не только СРБ или ИЛ-6,а еще кучу всего.Вот, например, как вам образчик ?



Это обычные, рядовые анализы, ничего выдающегося.Видите, замеряют и СРБ и D-димер и маркеры иммунной активации и пр.
Читайте также:


