Какие клетки организма поражаются вич в первую очередь
Рецептором для ВИЧ является дифференцировочный антиген CD4, а также неспецифические, не зависящие от наличия CD4 компоненты. Фиксация вируса с мембранным рецептором CD4 клетки хозяина блокирует основную функцию этих иммунокомпетентных клеток -- восприятие сигналов от антигенпрезентирующих клеток. Последующая за рецепцией репликация вируса ведет к гибели клеток, выпадению выполняемой ими функции и развитию иммунодефицита.
В организме человека имеется целый ряд иммунокомпетентных, соматических и ряд других клеток, имеющих рецепторы для ВИЧ (CD4+ лимфоциты, CD8+ лимфоциты, дендритные клетки, моноциты, эозинофилы, мегакариоциты, нейроны, микроглия, сперматозоиды).
Помимо основного рецептора для ВИЧ-1 -- CD4, имеется еще ряд корецепторов, в частности, хемокиновые рецепторы, необходимые для проникновения ВИЧ в клетку.
Проникнув в CD4+ клетки, ВИЧ сразу же начинает репликацию. Все регуляторы, активирующие СD4+клетки, обеспечивают увеличение репликации вируса. К подобным регуляторам относятся фактор некроза опухолей (ФНО), фактор, стимулирующий колонии гранулоцитов/макрофагов, интерлейкин-6 (ИЛ-6). К негативным регуляторам, тормозящим репликацию вируса, относятся интерферон (ИФ) и трансформирующий фактор роста.
Выделено два типа СР4+клеток: Т-хелперы-1 (Th1) и Т-хелперы-2 (Th2). У больных ВИЧ-инфекцией идет угнетение Th1, чем обеспечиваются и вирусная патология, и онкогенез.
Жизненный цикл ВИЧ после проникновения в организм имеет последовательный характер: связывание вириона с поверхностью клетки, слияние мембран вириона иклетки, проникновение вируса внутрь клетки, высвобождение нуклеотида и геномной РНК вируса, интеграция генома вируса в геном инфицированной клетки, латентная фаза, фаза активации транскрипции с ДНК провируса и последующая транскрипция белков вируса, наработка всех компонентов вируса с формированием новых вирионов и их высвобождением из клетки, влекущим за собой гибель клетки-мишени.
В патологический процесс вовлекаются в первую очередь и в большей степени CD4+ лимфоциты, моноциты крови, макрофаги тканей, дендритные клетки крови, лимфатических узлов, селезенки, кожи, альвеолярных и интерстициальных макрофагов легких, микроглия и другие клетки нервной системы, имеющие CD4-рецепторы. Так же поражаются В- и О-лимфоциты, ретикулярные клетки, эпителиальные клетки кишечника, клетки Лангерганса, причем последние инфицируются даже легче, чем CD4+ лимфоциты. Именно клеткам Лангерганса придается большое значение в распространении ВИЧ по организму, ибо в них вирус сохраняется длительное время, иногда годы.
Наличие CD4 рецептора на многих и не только иммунокомпетентных клетках, возможность поражать и клетки, не имеющие этого рецептора, определяют политропность ВИЧ и полиморфизм клинической картины.
Если на CD4+ лимфоциты вирус оказывает цитопатическое действие с лизисом клетки или слиянием в синцитий, то в моноцитах/макрофагах ВИЧ реплицируется с умеренной интенсивностью и не оказывают цитонекротического действия. Изучение динамики сывороточных монокинов подтверждает активное участие в патогенезе ВИЧ-инфекции моноцитов/макрофагов, основных продуцентов фактора некроза опухолей и интерлейкина-1B. С гиперпродукцией ФНО-а, ИЛ-1b и ИЛ-6 связывают развитие при ВИЧ-инфекции лихорадки, анемии, диареи, кахексии, патологических изменений на коже и слизистых при саркоме Капоши, церебральных симптомов. В то же время было установлено, что ВИЧ ингибирует продукцию ИЛ-2 и g -ИФ, синтезируемым Т-хелперами первого типа, и не ингибирует функцию Т-хелперов второго типа. Следовательно, играя важную роль в регуляции синтеза цитокинов, ВИЧ за счет переключения иммунного ответа с Т-хелперов первого типа на Т-хелперы второго типа, стимулирует гуморальное звено иммунитета.
После инфицирования клетки вирусом происходит соединение вирусной оболочки с мембраной клетки. Помимо того, вирусный белок обеспечивает слияние мембран соседних клеток между собой с образованием одной многоядерной клетки -- синцития. При этом слияние может быть как зараженных клеток между собой, так и зараженных с незараженными.
С момента интеграции генома вируса в геном клетки начинается стадия латентной инфекции. В этот период вирус находится в клетке в виде интегрированного в геном ДНК -- провируса.
В расшифровке патогенеза ВИЧ-инфекции многие вопросы решены, установлены основные этапы развития процесса в клетке после инфицирования ее вирусом. Выявлен ряд факторов, активирующих экспрессию генов ВИЧ. К ним относятся факторы, активирующие Т-лимфоциты: специфические антигены (например, вирусы группы Herpes), неспецифические антигены (например, митогены типа фитогемаглютинина), цитокины (например, фактор некроза опухолей, некоторые интерлейкины, гамма-интерферон), бактериальные иммуномодуляторы. К активаторам экспрессии ВИЧ относятся глюкокортикостероидные гормоны, ультрафиолетовое облучение, перекись водорода, свободные кислородные радикалы. Активирует инфекционный процесс беременность.
Исключительно важный этап патогенеза болезни -- сборка вирусных частиц и выход нового потомства вируса из инфицированной клетки. Отличительной чертой ВИЧ является взрывной характер процессов активации транскрипции, синтеза белков-предшественников, сборки вирионов и их почкования: за 5 минут одна лимфоцитарная клетка может образовать до 5000 вирусных частиц.
Вирусная экспрессия определяет клинику ранней фазы болезни. Пик экспрессии вируса в клетках лимфоидной ткани предшествует накоплению его в плазме. Появление вирусспецифических цитотоксических Т-лимфоцитов совпадает со временем окончания экспрессии вируса в лимфатических узлах. Образование нейтрализующих антител обеспечивает переход острой фазы болезни в хроническую.
Иммунопатогенетически ВИЧ-инфекция проявляется дефицитом Т- и В-звеньев иммунной системы, дефицитом комплемента, фагоцитов, снижением функции неспецифических факторов защиты. В результате идет формирование анергии с проявлениями аллергического, аутоаллергического и иммунокомплексного патологического процесса. Уже во II стадии ВИЧ-инфекция характеризуется снижением абсолютного числа лейкоцитов, повышением уровня естественных киллеров (NK-клетки), нарастанием реакции торможения миграции лимфоцитов. Изменения гуморального звена иммунитета проявляются нарастанием IgG+ В- лимфоцитов и 4-5-кратным ростом уровня сывороточных IgE. Выявляется диспропорция уровней подклассов иммуноглобулинов: IgG1 и IgG3 у больных увеличивается, а концентрация IgG2 и IgG4 существенно уменьшается. Несмотря на гипергаммаглобулинемию, увеличение количества циркулирующих в крови В-лимфоцитов, их функциональная активность на митогены остаются относительно сниженными, что позволяет В-систему иммунитета у ВИЧ-больных расценивать как супрессированную. Количество В-клеток в периферической крови больных в стадии СПИДа может быть снижено в три и более раз.
Взаимодействие ВИЧ-1 с мембраной CD4+ лимфоцитов определяет не только отрицательные реакции инфицированных клеток, но и приводит к программированной клеточной гибели -- апоптозу зрелых CD4+ лимфоцитов или CD34+ гемопоэтических клеток-предшественников даже при отсутствии их инфицирования вирусом.
Л.Монтанье (1996) считает, что в патогенезе СПИДа основное место принадлежит аутоиммунному процессу. В пользу этого говорят исследования характера иммунных реакций у больных: наличие аутоантител и аллоантител к лимфоцитам, формирование аллергических реакций цитотоксического типа, накопление циркулирующих иммунных комплексов, наличие комплементопосредованной цитотоксичности, активация антителозависимой клеточной цитотоксичности. В пользу наличия аутоиммунных процессов в патогенезе ВИЧ-инфекции говорят и клинические проявления болезни, в частности, часто сопутствующие болезни такие типичные аутоаллергические варианты патологии, как спондилоартропатии, системные ревматоидные синдромы.
Формирование иммунодефицита при ВИЧ-инфекции не ограничивается только поражением лимфоцитов с CD4-фенотипом. Так, нарушение синтеза белков НLA I ведет к ингибированию функции лимфоцитов с CD8-фенотипа, т.е. Т-супрессоров. Белок вируса оказывает супрессивное действие на продукцию Т-клетками ИЛ-2 и g - интерферона. А с продукцией ИЛ-2 и других цитокинов тесно связана функция цитотоксических Т-лимфоцитов, ответственных за противовирусную и противоопухолевую защиту организма. Все это патогенетически определяет характерную для ВИЧ-инфекции ассоциированную вирусную, бактериальную, грибковую и онкопатологию.
Наряду с поражением иммунной системы в патологический процесс вовлекается и кроветворная ткань. Для заболевания характерны лейкопения, анемия, тромбоцитопения.
Таким образом, поражение иммунной системы при ВИЧ-инфекции носит системный характер, проявляясь глубокой супрессией Т- и В-звеньев клеточного иммунитета. В ходе развития ВИЧ-инфекции происходят закономерные изменения гиперчувствительности немедленного и замедленного типа, гуморального иммунитета и факторов неспецифической защиты, функциональной активности лимфоцитов и моноцитов/макрофагов. Нарастает уровень сывороточных иммуноглобулинов, циркулирующих иммунных комплексов. Наряду с дефицитом CD4+ лимфоцитов в динамике болезни нарастает функциональная недостаточность CD8+ лимфоцитов, NK-клеток, нейтрофилов. Нарушение иммунного статуса клинически проявляется инфекционным, аллергическим, аутоиммунным и лимфопролиферативным синдромами иммунологической недостаточности, синдромами, свойственными болезни иммунных комплексов. Все это определяет в целом клинику ВИЧ-инфекции.
Ни для кого уже давно не является секретом то, что представляет собой это страшное заболевание- ВИЧ-инфекции. Не будет лишним напомнить о том, что ВИЧ-инфекция - это, прежде всего, вирусное заболевание, которое возникает в результате воздействия на человеческий организм вируса иммунодефицита. В действительности, ВИЧ-инфекция - это смертельное заболевание, последней стадией которого принято считать СПИД.
ВИЧ заражает клетки, которые являются частью иммунной системы организма. По мере того как все большее число клеток заражается этим вирусом, иммунная система теряет свою способность бороться с заболеванием. Для того чтобы заразить клетку продуктивно, ВИЧ должен внедрить свой генетический материал внутрь клетки. Этот процесс начинается с присоединения и внедрения вируса, вскрытия вирусной оболочки и проникновения генов в ген человека. Клетка человека начинает использоваться для создания вирусных строительных блоков для множества копий, которые затем собираются вместе и в конечном итоге вырываются из инфицированной клетки в поисках других клеток, которые они заражают. Вирус убивает зараженные им клетки, а также убивает незараженные клетки, пассивно находящиеся рядом. В результате такого воздействия вируса клетка человека живет, пока не будет завершен процесс ее размножения.
Проникнув в организм человека вирус иммунодефицита человека, начинает в нем размножаться, при этом поражая огромное количество клеток. В первую очередь поражается клетки иммунной системы и как следствие люди со слабым иммунитетом не могут долго противостоять инфекции. Именно поэтому данный вирус очень быстро завладевает всем организмом, что в итоге приводит к гибели больного. Развитие ВИЧ-инфекции подразделяется на несколько периодов. Это инкубационный, продромальный, латентный периоды, а также ПреСПИД и терминальная стадия. В общей сложности люди с ВИЧ-инфекцией могут прожить около десяти - двадцати лет.
Эпидемия ВИЧ/СПИДа продолжает распространяться по миру тревожными темпами. В настоящее время число людей, инфицированных ВИЧ на Земле, насчитывает от 33,4 до 46 млн. чел., при этом число новых случаев инфицирования ежегодно превышает 4 млн. чел.
Россия сейчас относится к региону с максимальными темпами развития эпидемии. По официальным данным количество случаев ВИЧ-инфекции в стране превышает 408 тыс. чел. Реальное число в стране оценивается в пределах 0,8-1,2 млн. чел. ВИЧ уже широко распространился в определенных подгруппах населения.
По состоянию на 01.06.2011 г. на территории Ямало-Ненецкого автономного округа зарегистрировано 1823 случая Вич-инфекции, из общего числа выявленных случаев, в 243 случаях ВИЧ-инфекция выявлена среди жителей других регионов, что составляет 13.,3 %. За 5 месяцев текущего года впервые выявлено 66 случаев ВИЧ -инфекции, среди трудовых мигрантов 38 случаев, что составляет 57,5 % от всех выявленных случаев ВИЧ-инфекции. Среди лиц работающих вахтово-экспедиционным способом выявлено 14 случаев из 38, что составляет 37% от общего числа выявленных в 2011 году случаев. В результате контакта вахтовика из Чувашии, произошло заражение жительницы п. Ныда, что в конечном итоге привело к формированию активнодействующего очага с вовлечанием в эпидемический процесс 23 жителей Надымского района, в том числе 16 коренных жителей п. Ныда.
Наверняка все слышали уже ни раз, что любое заболевание намного легче предупредить, чем его же лечить. Особенно если речь идет о ВИЧ-инфекции.
Что вообще подразумевается под словом профилактика? Профилактика - это ряд мер, соблюдая которые человек может не только предупредить развитие заболевания, но еще и сохранить нормальное общее состояние в том случае, если заболевание уже имеется.
Одной из самых эффективных профилактических мер ВИЧ-инфекции является исключение незащищенных половых контактов. Не стоит иметь незащищенные половые контакты особенно с незнакомыми людьми. Для этого есть средства защиты. Во всем мире половой контакт является ведущим способом передачи ВИЧ. Вероятность передачи ВИЧ от мужчин женщинам намного выше, чем вероятность передачи от женщин мужчинам. Среди женщин самый высокий риск грозит девочкам-подросткам и молодым женщинам, поскольку их развивающаяся репродуктивная система делает их намного более уязвимыми к инфекции, если они соприкасаются с инфекциями, передающимися половым путем (ИПП), включая ВИЧ.
Еще одной мерой профилактики ВИЧ-инфекции является отказ от наркотиков, так как заражение данным заболеванием очень часто происходит при введении иголок от шприцов.
Хотелось бы напомнить, что возможна передача от ВИЧ-инфицированной матери ее ребенку, во время беременности, родов или в результате грудного вскармливания. В случае если женщина ВИЧ инфицирована, ей не стоит рожать детей. Именно поэтому нужно стараться предупреждать развитие беременности. Если же женщина все же забеременела, тогда врачам нужно провести все необходимые меры профилактики для предупреждения заражения малыша в утробе матери.
ВИЧ/СПИД - это заболевание, которое было изучено тщательнее всего за всю историю. Существует огромное число фактов, которые указывают на то, что вы не можете заразиться следующим путем: пожимая руки, обнимая или целуя других; при кашле или чихании; пользуясь общественным телефоном; посещая больницу , открывая дверь; через общую пищу, пользуясь общими приборами для приема пищи или питья; пользуясь фонтанчиками для воды;
пользуясь туалетами или душами; в результате укуса комара или насекомого; работая, общаясь или живя рядом с ВИЧ-инфицированными людьми
ВИЧ-инфекция пока еще не лечится. Однако на сегодняшний день существует очень много поддерживающих лекарственных препаратов, которые могут гарантировать больному нормальное общее состояние.
Профилактика - это основа всех мер, предпринимаемых в ответ на эпидемию ВИЧ/СПИДа.
(c) Управление Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека по Ямало-Ненецкому автономному округу, 2006-2020 г.
Адрес: 629000, г. Салехард, ул. Титова, д. 10
14 октября 2013
- 19593
- 15,7
- 2
- 3
Распространенность СПИДа в мире на 2009 год.

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Обратная транскрипция осуществляется вирусным белком обратной транскриптазой [31]. Обратная она потому, что обычно в клетке все наоборот — информация переносится с ДНК на РНК (а с РНК — в последовательность аминокислот белков). РНК по сравнению с ДНК очень нестабильна, и поэтому для ВИЧ характерна огромная скорость мутации — в десятки тысяч раз быстрее, чем для человека. Если скорость нейтральных мутаций для ДНК составляет у различных видов и для различных генов в среднем меньше 10 −9 замен на сайт в год, то скорость мутирования генетического материала РНК-вирусов — около 10 −3 замен на сайт в год (у гена env ВИЧ: 10 −2 –10 −3 замен на сайт в год [21]). Это одна из причин, почему иммунная система не может справиться с ВИЧ — он слишком быстро изменяется.
Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
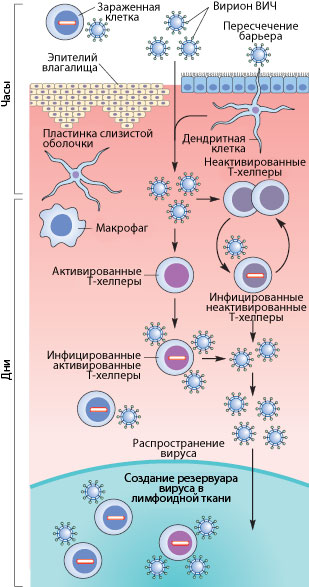
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
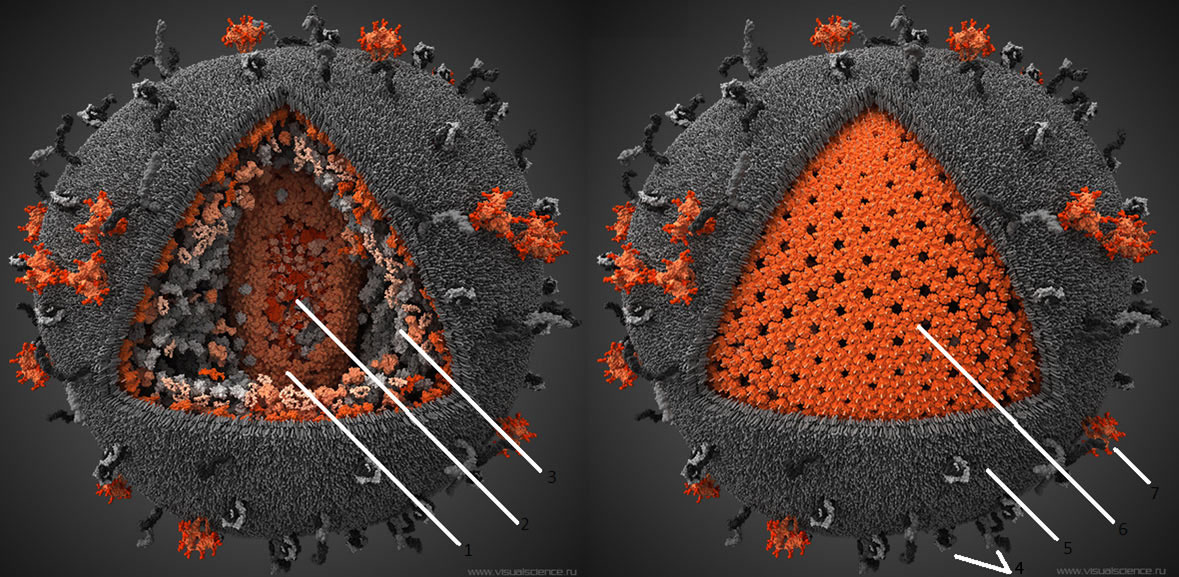
10000 нуклеотидов в каждой. Всего геном включает девять генов, которые в результате альтернативного сплайсинга кодируют 15 различных белков. 3 — Различные белки, захваченные вирусом из хозяйской клетки. 4 — Человеческие белки, обычно находящиеся на поверхности мембраны клеток. Захваченые в результате отпочковывания, они увеличивают вирулентность вируса. 5 — Внешняя оболочка ВИЧ, ведущая свое происхождение от цитоплазматической мембраны клетки, от которой когда-то отпочковался вирион. 6 — Матрикс, образованный тримерами белка р17. 7 — Тримерные комплексы белков gp120 и gp41, при помощи которых вирус проникает в клетку. На поверхности среднего вириона насчитывается около 20 таких тримеров. Чтобы увидеть рисунок в полном размере, нажмите на него.
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.
Вирус иммунодефицита человека (ВИЧ) отнесен к семейству ретровирусов (Retroviridae), подсемейству медленных вирусов (Lentivirus).
В настоящее время описаны 2 серотипа вируса: ВИЧ-1 и ВИЧ-2, различающиеся по структурным и антигенным характеристикам. Наибольшее эпидемиологическое значение имеет ВИЧ-1, который доминирует в современной пандемии и имеет наибольшее распространение на территории Российской Федерации. По данным электронной микроскопии, вирионы ВИЧ имеют округлую форму диаметром 100-120 нм. Наружная мембрана вируса построена из белков клетки хозяина и пронизана собственными белками вируса, которые обозначены как оболочечные белки.
Вирусная частица представляет собой ядро (cor), окруженное оболочкой. Ядро содержит двойную вирусную РНК, обратную транскриптазу (ревертазу), интегразу, протеазу. Различают два основных белка оболочки - трансмембранный гликопротеин с молекулярной массой 41 кД (gр41) и внешний гликопротеин - 120 кД (gр120) (табл. 1).
Таблица 1. Группы белков ВИЧ-1 и ВИЧ-2
| Группа белков | ВИЧ -1 | ВИЧ -2 |
| Белки оболочки вируса | gр160, 120, 41 кД | gp140, 105, 36 кД |
| Белки сердцевины | p55, 24, 17 кД | p56, 26, 18 кД |
| Ферменты вируса | p66, 51, 31 кД | p68 кД |
Примечание. Молекулярная масса белков выражена в килодальтонах - кД; gp - гликопротеины; р - протеины.
Нуклеоид вируса имеет округлую форму, но принимает продолговатую после отпочковывания вирусной частицы от клетки. Оболочка нуклеотида содержит протеин с молекулярной массой 24кд (р24). Между наружной оболочкой вириона и нуклеоидом существует каркас, состоящий из матриксного белка 17кд (р17).
В естественных условиях ВИЧ может сохраняться в высушенном биосубстрате в течение нескольких часов в жидкостях, содержащих большое количество вирусных частиц, таких как кровь и эякулят - в течение нескольких дней, а в замороженной сыворотке крови активность вируса сохраняется до нескольких лет.
Нагревание до температуры 56°С в течение 30 мин приводит к снижению инфекционного титра вируса в 100 раз, при 70°- 80°С вирус гибнет через 10 мин; через 1 мин инактивируется 70% этиловым спиртом, 0,5% раствором гипохлорита натрия, 1% глутаральдегидом, 6% перекисью водорода. ВИЧ относительно мало чувствителен к УФ-облучению, ионизирующей радиации.
| env | gp120 | Самый наружный белок обеспечивает связывание с клетками-мишенями. Лиганды - молекула CD4 + ; галактозилцерамиды; рецепторы для цитокинов |
| gp41 | Обеспечивает интернализацию вириона в клетку | |
| gag | р24 | Составляет оболочку ядра вируса (нуклеокапсида) |
| р17 | Составляет матриксное вещество вируса | |
| р9 | Связан с геномной РНК | |
| р7 | То же | |
| pol | р66 | Обратная транскриптаза (синтез ДНК на матрице РНК) |
| р31 | Интеграза (встраивает ДНК вируса в клеточный геном) | |
| р10 | Протеаза (расщепляет большие белковые трансляты на дифинитивные белки вируса) | |
| tat | p14 | Существенен для экспрессии белков оболочки (Env) |
| nef | p27 | Может усиливать и ингибировать репликацию ВИЧ |
| vif | p23 | Необходим для выхода новорожденных вирусов из клетки-мишени (вероятно, участвует в фолдинге белков Env) |
| vpu | p16 | Необязателен для жизненного цикла вируса; усиливает отпочковывание вируса из клетки-мишени |
Гликопротеин gр120 обусловливает присоединение ВИЧ к рецепторам СD4 клеток человека. При попадании ВИЧ в клетку под действием обратной транскриптазы синтезируется ДНК ВИЧ, встраиваемая в ДНК клетки-хозяина, которая в дальнейшем начинает продуцировать вирусные частицы.
Основа естественного иммунитета - это действие неспецифических механизмов, в большинстве своем реагирующих на повреждение тканей воспалительными реакциями. Некоторые клетки (макрофаги - МФ) и гуморальные факторы (комплемент, лизоцим) направлены на уничтожение бактерий. Другие клетки могут секретировать интерферон, действие которого в основном направлено против вирусов.
Адаптивный иммунитет основан на свойствах Т- и В-лимфоцитов избирательно отвечать на чужеродные вещества (антигены) с образованием специфической памяти и продукцией антител.
Попадая в организм человека, ВИЧ поражает различные органы и ткани, но, в первую очередь, клетки, несущие маркер СD4 + . В таблице 3 приведены основные типы клеток, поражаемых ВИЧ. В цитоплазме пораженных клеток освобождается вирусная РНК, и с помощью фермента обратной транскриптазы на основе вирусной РНК синтезируется ДНК - копия, которая встраивается в ДНК клетки хозяина (провирус). При каждом новом делении клетки все ее потомство содержит ретровирусную ДНК. В пораженной клетке начинают создаваться структурные элементы ВИЧ, из которых при помощи другого фермента - протеазы, собираются новые полноценные вирусы, в свою очередь поражающие новые клетки-мишени. С течением времени большинство зараженных клеток погибает.
Таблица 3. Типы клеток, поражаемых ВИЧ
| Тип клеток | Ткани и органы |
| Т-лимфоциты, макрофаги | Кровь |
| Клетки Лангерганса | Кожа |
| Фолликулярные дендритные клетки | Лимфоузлы |
| Альвеолярные макрофаги | Легкие |
| пителиальные клетки | Толстая кишка, почки |
| Клетки шейки матки | Шейка матки |
| Клетки олигодендроглии, астроциты | Мозг |
Уменьшение клеток, несущих рецептор СD4 + , приводит к ослаблению цитотоксической активности CD8+ Т-лимфоцитов, уничтожающих инфицированные вирусом клетки. В результате теряется контроль за проникающими в организм возбудителями бактериальных, вирусных, грибковых, протозойных и других инфекций (оппортунистических), а также за клетками злокачественных опухолей. Одновременно происходит нарушение функции В-лимфоцитов, поликлональная активация которых приводит, с одной стороны, к гипергаммаглобулинемии, а с другой - к ослаблению их способности продуцировать вируснейтрализующие антитела. Повышается количество циркулирующих иммунных комплексов, появляются антитела к лимфоцитам, что еще больше снижает число CD4 + Т-лимфоцитов. Возникают аутоиммунные процессы.
Оппортунистические инфекции, как правило, имеют эндогенное происхождение и возникают за счет активации собственной микрофлоры человека вследствие снижения напряженности иммунитета (например, эндогенная активация микобактерий туберкулеза из очагов Гона).
Цитопатическое действие ВИЧ приводит к поражению клеток крови, нервной, сердечно-сосудистой, костно-мышечной, эндокринной и других систем, что определяет развитие полиорганной недостаточности, характеризующейся разнообразием клинических проявлений и неуклонным прогрессированием ВИЧ-инфекции.
Читайте также:


