Септический эндокардит у ребенка
, MD, North Shore Hospital, Auckland
Last full review/revision September 2017 by Guy P. Armstrong, MD







Эндокардит обычно означает инфекцию эндокарда (то есть инфекционный эндокардит). Термин эндокардит также может включать неинфекционный эндокардит, при котором стерильные тромбоциты и фибриновые тромбы фиксируются на клапанах сердца и прилегающем эндокарде. Неинфекционный эндокардит иногда может приводить к инфекционному эндокардиту. Оба могут привести к эмболизации и нарушению функции сердца.
Диагноз инфекционного эндокардита обычно устанавливается с учетом совокупности всех клинических данных, а не результата одного исследования.
Инфекционный эндокардит может возникнуть в любом возрасте. Мужчины заболевают в два раза чаще, чем женщины. Лица, употребляющие внутривенные наркотики, пациенты с ослабленным иммунитетом и пациенты с искусственными клапанами сердца и другими внутрисердечными устройствами имеют наибольший риск.
Этиология
Здоровое сердце относительно устойчиво к инфекции. Бактерии и грибы не легко адгезируются к поверхности эндокарда, и постоянный ток крови помогает предотвратить их оседание на эндокард. Таким образом, для развития эндокардита требуются, как правило, 2 условия:
Предшествующая аномалия эндокарда
Присутствие микроорганизмов в кровотоке (бактериемия)
Реже, массивная бактериемия или особо вирулентные микроорганизмы поражают нормальные клапаны.
Эндокардит часто поражает клапаны сердца. Основными предрасполагающими факторами ИЭ являются врожденные пороки сердца, ревматическое поражение клапанов, бикуспидальный или кальцинированный аортальный клапан, пролапс митрального клапана, гипертрофическая кардиомиопатия и предшествующий эндокардит. Протезирование клапанов и других внутрисердечных устройств представляет особый риск. Иногда пристеночные тромбы, дефекты межжелудочковой перегородки и область открытого аортального протока подвергаются инфицированию. Ядром инфекции является стерильная фибринозно-тромбоцитарная вегетация, формирующаяся при высвобождении поврежденными эндотелиальными клетками тканевых факторов.
Инфекционный эндокардит чаще всего поражает левые отделы сердца (например, митральный или аортальный клапаны). Примерно в 10–20% случаев поражаются правые отделы (трикуспидальный или пульмональный клапаны). Внутривенные наркоманы имеют более высокий риск развития правостороннего эндокардита (около 30–70%).
Микроорганизмы, поражающие эндокард, могут попадать из отдаленных очагов инфекции (например, кожный абсцесс, воспаленные или инфицированные десны, инфекция мочевыводящих путей) или через очевидные входные ворота, такие как центральный венозный катетер или места инъекций препаратов. Практически любой чужеродный имплантированный материал (например, желудочковый или перитонеальный шунт, протез) подвергается риску бактериальной колонизации, тем самым становясь источником бактериемии и, следовательно, эндокардита. Эндокардит может быть результатом асимптомной бактериемии, которая, как правило, возникает во время инвазивных стоматологических, медицинских или хирургических вмешательств. Даже чистка зубов и жевание могут приводить к бактериемии (обычно зеленящим стрептококком) у пациентов с гингивитом.
Возбудители различаются в зависимости от места инфекции, источника бактериемии и факторов риска пациента (например, внутривенные наркоманы), но в 80–90% случаев стрептококки и Staphylococcus aureus являются причиной ИЭ. Энтерококки, грам-отрицательные бациллы, микроорганизмы группы HACEK (Haemophilus, гемофильные бактерии, Actinobacillus actinomycetemcomitans, Cardiobacterium hominis, Eikenella corrodens и Kingella kingae) и грибки являются причиной большинства других случаев.
Болезнь протекает в трех стадиях:
Бактериемия: микроорганизмы присутствуют в крови
Адгезия: микроорганизм присоединяется к аномальному или поврежденному эндотелию с помощью поверхностных адгезинов
Колонизация: пролиферация организма вместе с развитием воспаления, что приводит к образованию зрелых вегетаций
Многие из возбудителей образовывают полисахаридные биопленки, которые защищают их от иммунной защиты хозяина и препятствуют проникновению антибиотиков
Патофизиология
Эндокардит имеет локальные и системные осложнения.
Местные последствия инфекционного эндокардита включают:
Абсцессы миокарда с деструкцией тканей, а иногда и с нарушением проводимости (чаще при нижне-перегородочных абсцессах).
Внезапная, тяжелая клапанная регургитация может привести к сердечной недостаточности и смерти (чаще из-за поражения митрального или аортального клапана).
Аортит в связи с распространением инфекции из прилегающих структур.
Для больных с протезированными клапанами характерно развитие абсцессов клапанного кольца, обструктивных вегетаций, абсцессов миокарда и грибковых аневризм, что проявляется клапанной обструкцией, дисфункцией клапана и нарушением проводимости.
Системные осложнения в первую очередь обусловлены
Эмболизация инфицированным материалом из сердечного клапана
Иммуно-опосредованные явления (в основном при хронической инфекции)
Поражение правых камер сердца характеризуется развитием септических эмболий легочной артерии, которые могут привести к инфаркту легкого, пневмонии или эмпиеме. Поражение левых камер сердца может приводить к эмболиям любых органов, особенно часто почек, селезенки и центральной нервной системы. Микотические аневризмы могут формироваться в любых крупных сосудах. Часто развиваются эмболии кожи и сетчатки. Вследствие отложения иммунных комплексов развивается диффузный гломерулонефрит.
Классификация
Инфекционный эндокардит может иметь вялотекущее, подострое течение или более острое, молниеносное течение с высокой опасностью развития быстрой декомпенсации.
Подострый бактериальный эндокардит (ПБЭ), несмотря на агрессивность, обычно развивается незаметно и прогрессирует медленно (т.е от нескольких недель до месяцев). Источник инфекции или входные ворота часто не выявляются. Возбудителями ПСЭ чаще всего являются стрептококки (особенно зеленящий, микроаэрофильный, анаэробный, стрептококки группы D и энтерококки), реже причиной могут быть золотистый и эпидермальный стафилококки - S. aureus, Staphylococcus epidermidis, стрептококки Gemella morbillorum, Abiotrophia defectiva (ранее, Streptococcus defectivus), Granulicatella и требовательный к питательным средам Haemophilus. Стрептококковый подострый эндокардит часто развивается на пораженных клапанах после асимптомной бактериемии, вследствие инфекций периодонта, гастроинтестинальных и урогенитальных инфекций.
Острый бактериальный эндокардит (ОБЭ) обычно развивается внезапно и прогрессирует быстро (т.е. в течение дней). Источник инфекции или входные ворота часто легко выявляются. Когда инфекция высоко вирулентна или бактериальное воздействие массивно, острый бактериальных эндокардит может поражать нормальные клапаны сердца. Он обычно вызван золотистым стрептококком S. aureus, гемолитическим стрептококком группы А, пневмококком или гонококком.
Эндокардит протезированного клапана (ЭПК) развивается у 2–3% пациентов в течение первого года после протезирования клапана и в 0,5% в последующие годы. Чаще развивается после замены аортального клапана, нежели митрального и в одинаковой степени поражает как механические, так и биологические протезы. Раннее начало инфекции ( 2 мес. после хирургического лечения) вызвано главным образом инфицированием в ходе операции бактериями, резистентными к противомикробным препаратам (S. epidermidis, дифтероиды, колиформные бациллы, Candida, Aspergillus). Позднее начало инфекции происходит в основном в результате контаминации низко-вирулентными организмами во время оперативного вмешательства или при транзиторных бессимптомных бактериемиях, чаще всего благодаря попаданию стрептококка; S. epidermidis; дифтероидов; и требовательной к средам грамотрицательной палочки Haemophilus, Actinobacillus actinomycetemcomitans, и Cardiobacterium hominis.
Клинические проявления
Клиническая картина зависит от классификации, но она неспецифична.
Первоначально симптомы подострого бактериального эндокардита смазанные: субфебрильная лихорадка ( 39 ° С), ночные поты, утомляемость, недомогание и потеря веса. Возможны озноб и артралгии. Симптомы клапанной недостаточности могут быть первым признаком, ведущим к постановке диагноза. Первоначально менее чем ( ≤ ) у 15% пациентов наблюдается лихорадка или шумы в сердце, но со временем оба эти симптома развиваются практически у всех больных. Объективное исследование может выявлять бледность, лихорадку, изменение ранее существовавшего шума или появление шума новой регугитации и тахикардию.

Этот пациент с инфекционным эндокардитом имеет множественные узелки Ослера (болезненные, эритематозные узелки на пальцах ног).
У данного пациента с инфекционным эндокардитом на ладонях видны множественные язвочки Джейнвея (безболезненные эритематозные папулы). На пальцах пациента также наблюдаются своеобразные узлы Ослера (болезненные, эритематозные узелки на пальцах).
На изображении слева показан узелок Ослера (мягкий эритематозный узелок) на большом пальце. На изображении справа показаны язвочки Джейнвея (безболезненные эритематозные пятна на ладони).
Точечные кровоизлияния представляют собой небольшие линейные кровоизлияния под ногтевыми пластинами.

На данной фотографии показаны конъюнктивальные петехии у пациента с инфекционным перикардитом.
На данной фотографии показано конъюктивальное кровоизлияние у пациента с инфекционным перикардитом.
На изображении слева показаны множественные пятна Рота или ретинальные кровоизлияния. Изображение справа – увеличенный снимок пятен Рота с бледной зоной в центре.
Клиническая картина острого бактериального эндокардита и эндокардита искусственного клапана подобна картине подострого бактериального эндокардита, но течение более быстрое. Лихорадка почти всегда выявляется в начале заболевания, у пациентов имеются симптомы интоксикации; иногда развивается септический шок. Сердечные шумы выявляются первоначально примерно у 50–80% пациентов и со временем у > 90%. Редко развивается гнойный менингит.
Септическая эмболия легочной артерии может вызывать кашель, плевральные боли в грудной клетке и иногда кровохарканье. Характерно наличие шума трикуспидальной регургитации.
Диагностика
Эхокардиография, иногда – другие методы получения изображения
Так как клиническая картина неспецифична, вариабельна и может развиться незаметно, диагностика требует высокой настороженности. Эндокардит следует подозревать у пациентов с лихорадкой без явных причин инфекции, особенно если есть шум в сердце. Настороженность в плане ИЭ должна быть очень велика в том случае, если имеются положительные результаты посева крови у пациентов с патологией клапанов сердца, у пациентов, которым недавно выполнялись инвазивные процедуры или у внутривенных наркоманов. Пациенты с доказанной бактериемией должны быть тщательно и многократно обследованы на предмет новых клапанных шумов и признаков эмболии.
Кроме позитивных посевов крови, других специфических лабораторных изменений нет. Установленные инфекционные поражения эндокарда часто приводят к нормохромной нормоцитарной анемии, лейкоцитозу, повышению СОЭ, увеличению уровня иммуноглобулинов, появлению циркулирующих иммунных комплексов и положительному ревматоидному фактору, но эти изменения не помогают в постановке диагноза. В общем анализе мочи часто выявляется микрогематурия, иногда эритроцитарные цилиндры, пиурия или бактериурия.
Идентификация возбудителя и определение его чувствительности к антибиотикам жизненно необходимы для определения тактики лечения.
Если заподозрен эндокардит, должно быть выполнено 3 забора крови на посев (20 мл каждый) в течение 24 ч (если клиническая картина представлена острым бактериальным эндокардитом, то 2 забора крови с интервалом между 1-м и 2-м в 1 час). Каждый новый забор крови должен быть произведен путем отдельной венепункции (т.е. не из ранее установленных внутрисосудистых катетеров). Забор крови не должен производиться во время наличия у пациента лихорадки или озноба, поскольку у большинства пациентов бактериемия носит постоянный характер. При эндокардите и в отсутствие предшествовавшей антибиотикотерапии все 3 посева образцов крови положительны, поскольку бактериемия продолжается; по крайней мере, 1 посев крови положительный в 99% случаев. Необходимо избегать преждевременного использования эмпирической антибактериальной терапии у пациентов с приобретенными или врожденными пороками во избежание эндокардитов с негативными посевами крови. Если ранее проводили антибактериальную терапию, следует также получить результаты гемокультуры, однако они могут быть отрицательными.
Посевы крови требуют 3–4-недельной инкубации для определенных микроорганизмов; однако некоторые запатентованные автоматически мониторирующие культуральные системы могут идентифицировать позитивные культуры в течение недели. Другие микроорганизмы (например, Aspergillus sp) могут не выявляться при посевах крови. Некоторые микроорганизмы (например, Coxiella burnetii, Bartonella sp, Chlamydia psittaci, Brucella sp) требуют серологической диагностики; другие микроорганизмы (например, Legionella pneumophila) требуют специальную культуральную среду или ПЦР (например, Tropheryma whippelii). Негативные результаты посевов крови могут быть следствием первичной антибактериальной терапии, инфицированности микроорганизмами, которые не растут на стандартных питательных средах, или указывать на другой диагноз (например, неинфекционный эндокардит, миксома предсердия с эмболиями, васкулит).
На начальном этапе необходимо выполнение эхокардиаграфии, обычно трансторакальной (ТТЭ), а не трансэзофагеальной (ТЭЭ). ТЭЭ является более чувствительной (т.е. способна выявлять вегетации маленького размера, невидимые при ТТЭ),
Чреспищеводную эхокардиографию следует проводить при таких случаях:
Пациенты имеют искусственный клапан
Трансторакальная эхокардиография не является диагностической
Диагноз инфекционного эндокардита был установлен клинически (проводится для выявления перфораций, абсцессов и свищей)
Иногда используется КТ, если при ЧПЭ не возможно точно определить околоклапанные абсцессы, а также для обнаружения микотических аневризм. ПЭТ является новым инструментом для диагностики эндокардита, который возникает в простетических и внутрисердечных устройствах. В настоящее время патологии, выявленные при КТ и ПЭТ включены в Европейские рекомендации в качестве основных критериев.
Инфекционный эндокардит достоверно диагностируется, когда микроорганизмы выявляются гистологически (или культурально) в эндокардиальных вегетациях, полученных в ходе операции на сердце, эмболэктомии или аутопсии. Так как вегетации обычно недоступны для исследования, существуют разнообразные клинические критерии для установления диагноза. К ним относятся пересмотренные критерии Дюка (с чувствительностью и специфичностью > 90%— Диагностические требования к диагнозу инфекционного эндокардита в соответствии с пересмотренными критериями Дюка а также Пересмотренные клинические критерии Дюка для диагностики инфекционного эндокардита) и модифицированные критерии Европейского общества кардиологии (ESC) 2015 года (1).
Критерии ESC аналогичны модифицированным критериям Дюка, но в качестве основных критериев включают результаты расширенной визуализации как указано далее:
Вегетации, абсцесс, псевдоаневризма, внутрисердечная фистула, клапанная перфорация или аневризма или новое частичное раскрывание створок искуссвенного клапана, которые выявлены при эхокардиографии
Аномальная активность вокруг искусственного клапана (имплантированного > 3 мес раньше), обнаруженная при ПЭТ/КТ или ОФЭКТ/КТ с лейкоцитами, меченными радиоактивными изотопами
Околоклапанные поражения, выявленные при КТ сердца
Критерии ESC также отличаются от малых модифицированных критериев Дюка, детализируя, что только лишь выявление бессимптомных сосудистых явлений при визуализации является достаточным.
Инфекционный эндокардит
Инфекционный эндокардит – общее инфекционное заболевание с локализацией воспаления на клапанном и пристеночном эндокарде и возможным распространением патологического процесса на интиму магистральных сосудов.
Этиология. Инфекционные эндокардиты вызываются разнообразной флорой. Часто этиологическими факторами являются стрептококки и стафилококки. β-ремолитический стрептококк группы А способствует развитию ревматического эндокардита. Инфекционный эндокардит может возникнуть после перенесения ребенком скарлатины, пневмонии, сепсиса и др. Причиной эндокардитов могут быть и грамотрицательные микробы (клебиелла, протей), сальмонеллы, вирусы, грибы.
Наряду с инфекционным фактором в развитии эндокардита большое значение имеет изменение общей реактивности организма и местной – эндокарда, вызванное охлаждением, физическим и психическим перенапряжением, аллергией. Предрасполагающими факторами могут быть и нарушения внутрисердечной гемодинамики при врожденных и приобретенных пороках сердца, образование тромбов с последующим отложением в них микроорганизмов.
Клиника. Для острой формы инфекционного эндокардита характерно острое начало заболевания с появлением высокой температуры тела с размахами в течение суток в 1–1,5 °C, потливости, слабости, тахикардии. Кожа бледно-серого цвета, возможно возникновение желтухи. Геморагические сыпи на коже и слизистой оболочке ротовой полости, артралгии, увеличение печени и селезенки.
Клиническая картина изменений сердца зависит от локализации воспаления эндокарда и в начале заболевания может быть неманифестной, скудной. При пристеночном эндокардите шум в сердце может отсутствовать. При локализации воспалительного процесса на клапанах сердца появляются шумы, характерные для поражения данного клапана. Вначале они негромкие, локальные, затем их проводимость усиливается. Возможно острое формирование клапанного порока.
В клинической картине инфекционного эндокардита в начале заболевания преобладают общие септические симптомы, что затрудняет его диагностику.
При присоединении миокардита отмечаются расширение границ сердца, приглушение тонов, часто – появление аритмии.
В анализах крови – нейтрофильный лейкоцитоз с выраженным сдвигом формулы крови до юных и миэлоцитов, анемия, высокая СОЭ, увеличение α2– и γ-глобулинов, появление С-реактивного белка, положительная формоловая проба. В анализах мочи – микрогематурия, протеинурия, лейкоцитурия. Большое значение в диагностике имеет выделение гемокультуры, но брать кровь на исследование целесообразно в самом начале заболевания, до применения антибиотиков. При УЗИ сердца вегетации на клапанах, их деформацию удается обнаружить обычно спустя 1 месяц от начала заболевания.
У детей с врожденным пороком сердца инфекционный эндокардит развивается часто исподволь, клинические данные скудные, что затрудняет его раннюю диагностику, особенно у детей первого года жизни. Для постановки диагноза инфекционного эндокардита, развившегося на фоне порока сердца, необходимо учитывать следующие данные: появление лихорадки неясной этиологии, изменение шумов или тонов сердца, изменение окраски кожных покровов (появление бледности, бледно-серого цвета кожи), увеличение размеров сердца, тахикардия и одышка более выраженные, чем при данном пороке, невысокая эффективность лечения недостаточности кровообращения, увеличение селезенки, нарушения функции других органов, бактериемия, тромбоэмболические осложнения, данные УЗИ сердца.
Лечение. Назначают постельный режим до ликвидации недостаточности кровообращения или стабилизации гемодинамики при развитии инфекционного эндокардита на фоне порока сердца. В питании детей до 1 года большое значение имеет грудное материнское молоко, при его отсутствии – адаптированные смеси. Обязательна антибиотикотерапия. Препараты первоначального выбора – полусинтетические антибиотики пенициллинового ряда (ампициллин, амоксициллин и др.) в сочетании с гентамицином в дозе 2–5 мг/кг в сутки. Можно использовать и другие аминогликозиды: тобрамицин 3–5 мг/кг в сутки в/м; амикацин по 10–15 мг/кг в сутки в/в или в/м; сизомицин 3–5 мг/кг в сутки в/в или в/м. Применяются также цефалоспорины и другие антибиотики. Оптимально назначать антибиотики с учетом чувствительности к ним микрофлоры. Антибактериальную терапию проводят 6–8 недель непрерывно.
При развитии недостаточности кровообращения показаны сердечные гликозиды, диуретики, препараты, улучшающие сократительную функцию миокарда (рибоксин, милдронат, препараты калия, витамины). При острых стафилококковых инфекционных эндокардитах показано использование стафилококкового иммуноглобулина, при подострых – стафилококкового анатоксина. Глюкокортикоидную терапию используют при бактериальном шоке и в иммунологической фазе заболевания в небольших дозах (преднизолон 15–20 мг/сут). Для ликвидации нарушений микроциркуляции и для их предупреждения назначают гепарин, трентал.

Дата публикации: 19.05.2016 2016-05-19
Статья просмотрена: 326 раз
В современной клинической практике проблема инфекционного эндокардитастоит достаточно остро. Это обусловлено довольно высокой заболеваемостью, выраженным клиническим полиморфизмом, нарастанием числа атипичных форм, повышением удельного веса возбудителей, резистентных к антибактериальной терапии [2, 4].
По данным литературы заболеваемость ИЭ у взрослых составляет 1,7–6,5:100.000 населения в год [1], у подростков — более низкая, и составляет 3,0–4,3:1 млн. населения в год [3]. В то же время по данным, поступающим из крупных медицинских центров Европы и США, удельный вес ИЭ среди детей и подростков в специализированных стационарах постепенно нарастает, что связывают с увеличением числа операций на сердце при врожденных пороках, постоянным расширением спектра инвазивных диагностических и лечебных медицинских манипуляций, а также распространением внутривенной наркомании [4]. При этом мальчики заболевают эндокардитом в 2–3 раза чаще, чем девочки. Среди всех случаев эндокардита инфекционный генез составляет 25–40 % [3].
Недостаточная изученность патогенетических механизмов и клинических проявлений ИЭ у детей в зависимости от вариантов течения являются причиной поздней диагностики и заболевания [1].
Целью исследования явилось изучениеклинических, лабораторных и инструментальных методов исследования, инфекционного эндокардита у детей в современных условиях.
Материалы иметоды исследования.
Исследование проводилось при кафедре Госпитальной педиатрии № 2 на базе клиники ТашПМИ. В исследование были включены 8 детей с установленным диагнозом Инфекционный эндокардит, находившихся на лечении с 2013 по 2016гг, и проведён ретроспективный анализ 12 историй болезни детей с диагнозом Инфекционный эндокардит за период с 2010 по 2016гг. Всем детям проводился комплекс клинико-лабораторных исследований включающий в себя посев крови на стерильность, при анализе результатов которого определились нижеследующие результаты.
Результаты иих обсуждение. Наиболее опасным возбудителем ИЭ является S. Aureus. В последние годы его роль как лидирующего возбудителя ИЭ в отдельных регионах возрастает: этот микроорганизм является возбудителем ИЭ не менее чем в 40 % случаев. S. epidermidis встречается реже в 5 раз, чем S. Aureus (табл. 1).
Частота основных возбудителей больных детей ИЭ
Возбудители
Частота,%
S. faecalis (энтерококк)
S. pneumoniae (пневмококк)
B — гемолитические S. spp.
Другие или смешанные
Различные виды бета — гемолитических стрептококков идентифицированы как возбудители ИЭ, наиболее частым является зеленящий стрептококк. Факторы, способствующие его инвазии: манипуляции в полости рта, хирургические вмешательства, тонзиллиты, фарингиты, синуситы. При энтерококковом эндокардите очаги инфекции чаще всего локализуются в гастроинтестинальном, гинекоуринальном трактах, а также в полости рта — парадонтоз. ИЭ, вызываемый Strep. Bovis, развивается на фоне патологии кишечника, нередко осложняет опухолевые процессы в кишечнике. Анаэробные стрептококки чаще всего вызывают ИЭ, связанный с хирургическими операциями, в том числе и с протезированием клапанов.
Развитию грибковых эндокардитов могут предшествовать длительное лечение антибиотиками, глюкокортикоидами, сахарный диабет, внутривенное введение глюкозы, кардиохирургические вмешательства.
Из грамположительных микроорганизмов заслуживают внимания факультативные анаэробы — листерия, дифтероиды, лактобациллы, стрептобациллы, актинобациллы и др. эта группа вызывает эндокардиты протезов клапанов.
Таким образом,положительная гемокультура у больных с инфекционным эндокардитом выявлена в 40 %, из них: грам (+) флора в 69,6 %, грам (-) флора в 26,8 %, грибы рода Кандида в 3 %. Клинико-лабораторные септические и иммунокомплексные проявления при ИЭ, вызванные золотистым стафилококком и зеленящим стрептококком, предопределяют прогноз заболевания и ассоциируются с острым и подострым вариантами ИЭ. При ИЭ, вызванном грам (-) флорой, наблюдается высокий процент тромбоэмболических осложнений (33,3 %) и иммунокомплексных изменений (нефрит, полиартрит, геморрагический васкулит), которые ассоциируются с затяжным вариантом заболевания.
При анализе предрасполагающих факторов развития инфекционного эндокардита у детей определилось, что при ВПС риск развития ИЭ во многом зависит от характера анатомического дефекта сердца и максимален у пациентов с синими пороками Фалло, дефектом межжелудочковой перегородки, при атрио–вентрикулярной коммуникации, аортальном стенозе.
В нашем исследовании у 12 детей инфекционный эндокардит развился на фоне ВПС, при этом у 50 % отмечалисьпороками Фалло, ДМЖП у 25 %, аотральный стеноз отмечался у 8 % исследуемых. Наименьший риск ИЭ имеют пациенты с дефектом межпредсердной перегородки, открытым артериальным протоком.
Выявлены клинико-лабораторные особенности вторичного ИЭ: на фоне ВПС отмечался в 60 %, при врожденных пороках сердца: у половины больных ИЭ проявлялся гломерулонефритом, у трети — миокардитом, у четверти больных- суставным синдромом, на фоне ревматизма ИЭ определился в 33 % случаях и проявлялся наличием в 50 % постоянной формы фибрилляции предсердий, в 30 %- тромбоэмболических осложнений, в основном за счет ЗСН. При ИЭ на фоне дисплазии соединительной ткани при ПМК проявлялся в основном иммунокомплексными поражениями, а при двустворчатом аортальном клапане- умеренным септическим синдромом. Факторами риска неблагоприятного прогноза развития вторичного ИЭ являются: при ревматизме- митрально-аортальные пороки сердца, фибрилляция предсердий; врожденных пороках сердца- пороки сердца синего типа, возникновение ИЭ после перенесенных реконструктивных операций.
Клиническая симптоматика ИЭ появляется в основном через 2 недели с момента возникновения бактериемии. Наиболее ранний и частый симптом заболевания — лихорадка (в большинстве случаев — неправильного типа) с ознобом различной выраженности 100 % и последующим профузным потоотделением 80 % случаях. Характерны быстрая утомляемость, нарастающая слабость, анорексия и потеря веса в 60 %. Нередки распространенные артралгии и миалгии, головные боли, боли в сердце 50 %, носовые кровотечения 20 % (рис. 1).
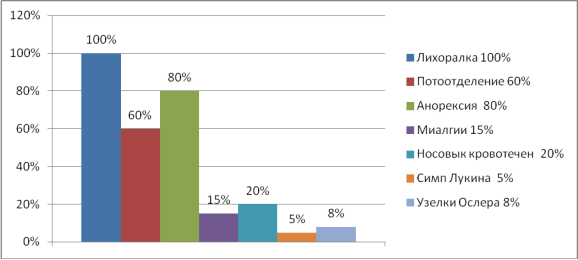
Рис.1. Клиническая симптоматика ИЭ
Основным клиническим синдромом заболевания является эндокардит с быстрым развитием клапанной регургитации (преимущественно — аортальной) при локализации процесса на нативных (естественных) клапанах. При современном ИЭ у детей и подростков наблюдается тенденция к учащению поражения митрального и трикуспидального клапанов, а также клапанов легочной артерии как в отдельности, так и в виде поливальвулярной патологии.
При клиническом исследовании особое внимание уделяется не только однократно фиксируемой аускультативной картине, но и ее динамике. В частности, в дебюте поражения первоначально не измененного аортального клапана может быть выслушан систолический шум по левому краю грудины, вероятно, обусловленный стенозированием устья аорты за счет вегетаций на полулунных клапанах. В дальнейшем появляется нежный протодиастолический шум в V точке с усилением при наклоне тела больного вперед; по мере усугубления клапанной деструкции интенсивность и продолжительность шума нарастает, отмечается ослабление II тона на аорте и снижение диастолического артериального давления.
Заключение. Таким образом,проведена углубленная оценка инфекционного эндокардита с клинико-лабораторных позиций на фоне ревматизма, врожденных пороков сердца, ИБС, дисплазии соединительной ткани сердца и выявлены факторы риска неблагоприятного прогноза. Оценены новые формы инфекционного эндокардита: нозокомиальные и правосердечные. Показана значимость иммунокомплексных и аутоиммунных реакций в развитии и прогрессировании инфекционного эндокардита. Определена прогностическая значимость вспомогательных лабораторных и инструментальных методов исследования в диагностике вариантов инфекционного эндокардита.
- Самсыгина Г. А., Щербакова М. Ю. Кардиология и ревматология детского возраста. М. 2004.
- Мелехов А. В., Гендлин Г. Е., Сторожаков Г. И. Эндокардит внутривенных наркоманов. // Росс. мед. журн. — 2007: выпуск: 42–45. 3.
- Соболева М. К., Белов Б. С. Инфекционный эндокардит у детей. РМЖ. 2006. — том 14. — № 8. — С. 630–636.
- Bitar F. F., Jawdi R. A., Dbaibo G. S. et al. Paediatric infective endocarditis: 19– years experience at a tertiare care hospital in a developing country // Acta Pediatr. — 2000.– V.89.– N.4.– P. 427–430.
Читайте также:


