Что такое септическое заболевание мягких тканей
- Лекция
- 23.04.2020
- конференц-зал Большой бульвар, 46, стр.1
- Другое событие
- 25.04.2020
- г. Москва, 4-й Добрынинский переулок, д. 1/9, корпус 1 А, 7 этаж.
Регистрация участников с 8.00 часов, открытие конференции в 9.00 часов.
ОСНОВНЫЕ ТЕМЫ КОНФЕРЕНЦИИ
Планируется обсуждение актуальных вопросов этиопатогенеза, клинико-лабораторной диагностики, лечения и профилактики внебольнпчных и госпитальных микробных инфекций у детей:
• Хирургические инфекции: кожи и мягких тканей, костей и суставов, интраабдоминальные, торакальные, инфекции мочевыводящих путей, сепсис
• Послеоперационные осложнения: бактериемия, раневая инфекция, ИВЛ-ассоциированная пневмония, катетер-ассоциированные инфекции
• Особенности течения инфекций у больных со сниженной иммунореактивностью
• Современные возможности антимикробной терапии и иммунокоррекции
• Новое в диагностике инфекции
• Интересные клинические случаи
ФОРМЫ ПРОВЕДЕНИЯ КОНФЕРЕНЦИИ
Первый день - 5 июня
• Лекции, научные доклады
• Круглый стол с экспертами
• Выставка современных лекарственных средств, клинического питания, изделий медицинского назначения, оборудования и реактивов
Второй день - 6 июня
• Лабораторная диагностика бактериемии
• Современные маркеры сепсиса
• Демонстрация лабораторных методов, обучение участников
• Интерпретация результатов исследований, клинические примеры
Для участия в конференции необходимо отправить в адрес оргкомитета заявку, в которой указать фамилию, имя, отчество, наименование организации и подразделения, почтовый адрес, телефон и E-mail для обратной связи, а также желаемую форму участия.
ОРГАНИЗАТОРЫ КОНФЕРЕНЦИИ
ОРГАНИЗАЦИОННЫЙ КОМИТЕТ
- Председатель: главный врач ДГКБ №13 им. Н.Ф. Филатова, докт. мед. наук В.В. Попов
- Председатель научного комитета: руководитель Кабинета рациональной антибиотикотерапии Департамента здравоохранения г. Москвы, докт. мед. наук, профессор Н.В. Белобородова
ЧЛЕНЫ ОРГАНИЗАЦИОННОГО КОМИТЕТА
- Академик РАМН Ю.Ф. Исаков Профессор М.А. Барская
- Профессор А.В. Гераськин К.м.н. О.С. Горбачев
- Профессор Л.М. Рошаль К.м.н. ДА. Попов
- Профессор А.Ф. Дронов К.м.н. О.Н. Хабиб
- Профессор А.Н. Смирнов К.м.н. А.В. Бирюков
- Профессор И.В. Бурков К.м.н. М.А. Голованев
- Профессор Е.Н. Падейская Зам. главного врача Т.В. Потапова
ОБЩАЯ ИНФОРМАЦИЯ
Дата проведения конференции - 5-6 июня 2008 года Участие в конференции для делегатов - бесплатное
Место проведения: Главная аудитория Детской городской клинической больницы им. Н.Ф.Филатова.
Адрес: г. Москва, ул. Садовая-Кудринская, д. 15, ДГКБ №13 им. Н.Ф. Филатова, корпус № 3, 3-й этаж, главная аудитория
Координаты организационного комитета:
Адрес: 121552, г. Москва, Рублевское шоссе, д. 135. НЦССХ
им. А.Н. Бакулева РАМН, лаборатория клинической микробиологии и
Телефоны: +7(495) 254-2917; +7(495) 414-7510; 8(919) 760-8929 (моб.)
Электронная почта: orgkomitet_popov@mail.ru
ФОРМЫ УЧАСТИЯ В КОНФЕРЕНЦИИ
• обучение на мастер-классе
• демонстрация клинического случая
• только публикация тезисов
ТРЕБОВАНИЯ К ТЕЗИСАМ
Тезисы объемом не более 2-х страниц машинописного текста (формат А4, шрифт Times New Roman размером 12 пт, через 1,5 интервала, поля по краям 2,5 см) принимаются в формате Word for Windows по электронной почте в виде вложенного файла. Файл с тезисами должен быть назван фамилией первого автора.
Тезисы необходимо оформить в следующем формате:
Фамилия, И.О. авторов
Учреждение, город, страна
Материалы и методы:
Почтовый адрес ответственного автора, телефон, факс, E-mail.
Заявку на участие в конференции и тезисы направлять по E-mail: orgkomitet_popov@mail.ru. В виде исключения допускается отправка по почте на адрес оргкомитета (в распечатанном виде с обязательным приложением диска или дискеты).
Присланные тезисы будут опубликованы в официальном сборнике конференции.
ВНИМАНИЕ! Направляемые материалы должны соответствовать основным темам конференции и должны быть получены оргкомитетом не позднее 30 мая 2008 г.
Принимайте участие в специальных проектах Департамента здравоохранения города Москвы.

Среди пациентов с гнойно-некротическими поражениями нижних конечностей отдельную клиническую группу представляют больные с постинъекционными осложнениями парентеральной наркомании. За последние годы число больных, страдающих наркотической зависимостью, возросло в 8–13 раз [6, 11] и на настоящий момент достигает 6 млн. [2].
С увеличением числа парентеральных наркоманов неуклонно растет и количество пациентов с гнойно-септическими постинъекционными осложнениями, которое за последние годы выросло с 0,8% до 9,3% от общего количества пролеченных пациентов [7]. Это связано с увеличением числа больных, применяющих кустарно изготовленные смеси из маковой соломки, эфедрина и других веществ с использованием высокоагрессивных растворителей, в частности, ацетона, уксусной кислоты, растворителя – 480 и других токсичных веществ [9]. Введение подобных препаратов приводит не только к склерозированию сосудистой стенки и острым тромбозам, но и к тяжелому поражению паравазальных тканей.
Растёт и количество смертей в результате употребления наркотиков, в последнее десятилетие оно увеличилось в 12 раз [3]. Частота летальных исходов составляет 5,2-26%, а при развитии тяжелого сепсиса в 9% наблюдений возрастает до 67%. Число случаев ампутации конечностей достигает 5,8-27,3% [1, 10, 13, 14].
Несмотря на определенные успехи в области изучения патогенеза, клиники и лечения гнойно-септических заболеваний у наркозависимых больных постинъекционные гнойно-воспалительные поражения нижних конечностей остаются малоизученными [5]. Их разнообразие и отсутствие общепринятой систематизации нередко создают значительные трудности при установлении диагноза и назначении рационального лечения [8]. До настоящего времени не до конца изучены особенности их клинического течения, нет четких критериев выбора оптимальных методов антибактериальной терапии, восстановления кровообращения и местного лечения в зависимости от локализации и распространенности гнойно-некротического процесса, вида и степени нарушения магистрального кровотока в конечности, уровня нарушения иммунитета и вида наркотической зависимости [2, 4, 12]. В связи с этим представляются актуальными дальнейшие исследования, посвященные выработке рациональной тактики лечения постинъекционных гнойно-септических поражений нижних конечностей у наркозависимых больных.
Цель: разработать адаптированную клиническую классификацию гнойно-септических постинъекционных осложнений у больных парентеральной наркоманией.
Материалы и методы
Результаты и обсуждение
При анализе эпидемиологических данных выявлен неуклонный рост числа больных с гнойно-септическими осложнениями парентеральной наркомании. Если в 2008 году доля этих пациентов среди всех пролеченных больных с гнойно-септическими поражениями мягких тканей составляла 1,3%, то к 2012 этот показатель возрос до 3,2%. При этом количество больных с поражениями нижних конечностей также имеет тенденцию к росту (рис. 1).
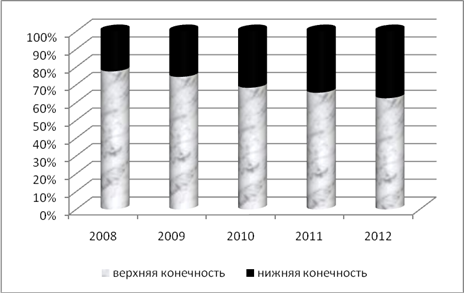
Рис. 1- Постинъекционные поражения верхних и нижних конечностей у больных парентеральной наркоманией
Среди препаратов, вызывающих постинъекционные осложнения у наркозависимых пациентов, наиболее часто встречался коаксил (31,5%) и другие кустарно изготовленные смеси из эфедрина или других веществ и героин – 18,5% (рис. 2).

Рис. 2 - Виды вводимых препаратов у больных с постинъекционными осложнениями парентеральной наркомании
В 13% случаев применялись смеси раствора димедрола с другими веществами, в 9,8% – привентина. В 19,6% наблюдений пациенты не знали точный состав вводимого препарата. Такая ситуация представляет значительные сложности при назначении медикаментозного лечения в связи с возможными побочными проявлениями или осложнениями неизвестных лекарственных средств.
Наиболее частым местом введения препаратов на нижних конечностях являлась область верхней трети бедра – 35 (38%) случаев как самая доступная для самостоятельных инъекций, а также паховая область в 27 (29,3%) наблюдениях (рис. 3).
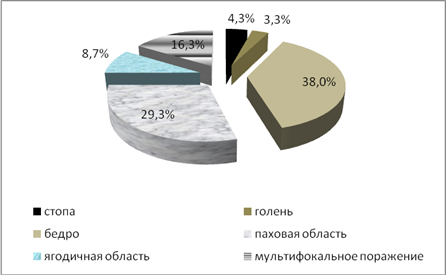
Рис. 3 - Локализация гнойно-септических очагов на нижней конечности у больных
Изолированные поражения стоп встретились у 4 (4,3%) больных, голеней у 3 (3,3%) пациентов. У 15 (16,3%) больных выявлен мультифокальный характер поражения, когда гнойно-некротические очаги локализовались в разных сегментах нижних конечностей. Обращает на себя внимание появление постинъекционных осложнений у наркоманов в ягодичной области (8,7%), что раньше встречалось крайне редко. Характерным признаком для данной локализации гнойно-некротического процесса является выраженное поражение венозной системы на всем протяжении нижней конечности, что практически исключало возможность внутрисосудистых инъекций, парентеральной наркоманией.
По данным бактериологических исследований, монокультура возбудителей гнойно-септического процесса была выделена у 67 (72,8%) пациентов, в 25 (27,2%) случаях выделены ассоциации 2 и более микроорганизмов. Обращает на себя внимание то, что в раневом отделяемом, полученном при хирургической обработке гнойного очага у 83 (90,2%) пациентов, обнаружено значительное увеличение концентрации жирных кислот. Уровень содержания уксусной кислоты в раневом отделяемом составил 18,7±4,7 мг/л, масляной – 0,88±0,2 мг/л, пропионовой – 7,3±2,4 мг/л. Это служит косвенным доказательством присутствия в составе возбудителей неклостридиальной анаэробной флоры в подавляющем большинстве случаев постинъекционных гнойно-септических осложнений у больных парентеральной наркоманией.
По результатам бактериологических исследований, монокультура выделена у 62 (67,4%) больных, ассоциации двух и более микроорганизмов – у 30 (33,6%) пациентов (рис. 4). Наиболее часто монокультура была представлена стафилококками – 37 (40,2%). Из них в 7 (18,9%) случаях получены коагулазотрицательные штаммы St. epidermidis, St. lentus, St. sciuri, St. capitis, St. intermedius (рис. 2). Грамотрицательные возбудители семейства энтеробактерий, выделены у 16 (17,4%) пациентов, псевдомонады – 6 (6,5%) . Среди энтеробактерий преобладали представители рода E. сoli – 7 (7,6%) штаммов, Klebsiella – 5 (5,4%) штаммов, Proteus – 3 (3,3%) штаммов и Enterobacter – 1 (1,1%) штамма. В 3 наблюдениях (3,3%) выделены штаммы Vibrio parahaemolyticus, Micrococcus lylae, Aerococcus viridans.
Ассоциации из двух микроорганизмов были представлены энтеробактериями в сочетании со стафилококком – 19 (20,7%) случаев, в том числе энтеробактерия + St. aureus – 15 (16,3%), энтеробактерия + коагулазотрицательный штамм стафилококка – 4 (4,3%). Ассоциация синегнойная палочка + золотистый стафилококк выявлена у 2 больных (2,2%). У 4 (4,3%) пациентов выделены ассоциации 3 микроорганизмов: стафилококк и 2 энтеробактерии у 2 (2,2%) больных, псевдомонада, энтеробактерия и стафилококк в 7 (12,1%) случаях, Proteus vulgaris + Vibrio + St. xylosus у 1 (1,1%) больного. Уровень микробной обсемененности на момент хирургической обработки составил в среднем 7,7±0,2×107 КОЕ/г ткани.
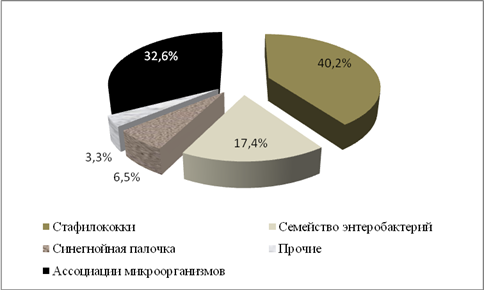
Рисунок 4 -Структура аэробных возбудителей у больных с гнойно-некротическими процессами нижних конечностей на фоне сахарного диабета
В структуре гнойно-септических осложнений у парентеральных наркоманов преобладали глубокие поражения мягких тканей нижних конечностей. Изолированные поверхностные гнойно-септические процессы в виде абсцессов кожи, поверхностных инфицированных колотых ран, трофических язв встретились лишь у 4 (4,3%) пациентов. Постинъекционные абсцессы и флегмоны подкожной жировой клетчатки диагностированы у 12 (13%) больных. Глубокие внутримышечные и межмышечные абсцессы и флегмоны нижних конечностей осложнили течение парентеральной наркомании в 19 (20,7%) случаях. В 57 (62%) наблюдениях постинъекционные осложнения были представлены паравазальными флегмонами, флегмонами глубоких клетчаточных пространств конечности и таза.
Локализация гнойно-некротического процесса во многом определяла и характер сосудистых повреждений. Нарушения магистрального кровотока и лимфообращения различной степени выраженности обнаружены у 89 (96,7%) больных. У 29 (31,5%) пациентов при обследовании выявлены изолированные нарушения венозного кровотока в нижних конечностях. Тромбозы и склеротические повреждения поверхностных и глубоких вен с проявлениями ХВН, соответствующим классам С1-С5 по классификации СЕАР, выявлены в 17 (18,5%) случаях, с проявлениями ХВН, соответствующим классу С6 по классификации СЕАР, – у 12 (13%) пациентов. Нарушения лимфатического дренажа нижних конечностей в виде поверхностного и глубокого лимфангоита, регионарной и отдаленной лимфаденопатии и лимфедемы отмечены у 14 (15,2%) пациентов. У 48 (52,2%) больных нарушения венозного и лимфатического оттока сочетались с поражением магистральных артерий, которые были представлены острыми тромбозами артерий, стенозами и окклюзиями магистральных артерий, ложными аневризмами артерий и артериовенозными фистулами. Ложная аневризма общей бедренной артерии диагностирована у 19 (20,79%) пациентов, ложная аневризма с артерио-венозной фистулой между общей бедренной артерией и веной — у 15 (16,3%), Ложная аневризма поверхностной артерии бедра с бедренной веной выявлена у 3 (3,3%) больных. Острые тромбозы общей бедренной артерии диагностированы в 7 (7,6%) случаях, критические стенозы и окклюзии в 4 (4,3%) наблюдениях.
У подавляющего числа пациентов с постинъекционными осложнениями парентеральной наркомании отмечалось наличие двух и более признаков системного воспалительного ответа при доказанном наличии гнойно-септического процесса, что позволяло классифицировать их как больных с ангиогенным сепсисом. Клинические проявления сепсиса без признаков органной дисфункции были выявлены у 58 больных. У 16 пациентов установлено наличие тяжелого сепсиса с признаками органной дисфункции. В 9 случаях больные поступали с явлениями септического шока. Только в 9 наблюдениях не обнаружено выраженной системной воспалительной реакции, что при наличии запущенного гнойно-септического процесса на фоне длительного употребления наркотиков может быть связано с иммунологическими нарушениями и снижением общей резистентности организма.
Тяжесть состояния пациентов с гнойно-некротическими постинъекционными поражениями нижних конечностей усугублялась наличием сопутствующих гемоконтактных инфекций. Гепатит В диагностирован у 12 (13%) больных, гепатит В и С – у 18 (19,6%), гепатит С – у 44 (47,8%). Наличие ВИЧ-инфекции в сочетании с гепатитом С выявлено в 5 (5,4%) случаях. Не выявлено сопутствующих гемоконтактных инфекций у 13 (14,1%) пациентов
На основании анализа данных обследования и полученного опыта лечения больных в клинике создана и применяется адаптированная классификация гнойно-септических постинъекционных осложнений у больных парентеральной наркоманией, учитывающая глубину гнойно-некротического процесса, характер и уровень поражения сосудов, наличие признаков ангиогенного сепсиса и сопутствующих гемоконтактных инфекций (AVLSH).
Адаптированная клиническая классификация постинъекционных гнойно-септических осложнений у больных с наркозависимостью
ПО ГЛУБИНЕ ПОРАЖЕНИЯ
I Поверхностные (абсцессы кожи, поверхностные инфицированные колотые раны, гранулемы, трофические язвы, стигмы, петехии и т.д.)
II Абсцессы и флегмоны подкожной жировой клетчатки
III Внутримышечные абсцессы и межмышечные флегмоны
IV Паравазальные флегмоны, флегмоны глубоких клетчаточных пространств конечности, таза
ПО ВИДУ СОСУДИСТОГО ПОРАЖЕНИЯ И СТЕПЕНИ НАРУШЕНИЯ МАГИСТРАЛЬНОГО КРОВОТОКА
А – нарушения артериального кровотока
А0 – нарушений магистрального артериального кровотока нет
А1 – гемодинамически незначимые стенозы и окклюзии артерий, аневризмы и артериовенозные свищи
А2 – гемодинамически значимые стенозы и окклюзии артерий, аневризмы и артериовенозные свищи без явлений критической ишемии конечности
А3 - стенозы и окклюзии артерий, аневризмы и артериовенозные свищи с явлениями критической ишемии конечности
V – нарушения венозного кровотока
V0 – нарушений венозного кровотока нет
V1 – тромбозы и склеротическое поражение поверхностных вен
V2 - тромбоз, склероз центральных вен с проявлениями ХВН, соответствующим классу C1-C5 по классификации СЕАР.
V3 – тромбоз, склероз центральных вен с проявлениями ХВН, соответствующим классу С6 по классификации СЕАР.
L- поражения лимфатической системы
L0 – нарушений лимфатического оттока нет
L1 – поверхностный лимфаденит, лимфангоит
L2 – лимфангоит с вовлечением магистральных лимфатических сосудов, выраженная регионарная и отдаленная лимфаденопатия
L3 – лимфостаз, лимфедема, синдром Абеля
ПО ПРИЗНАКАМ ХРОНИЧЕСКОГО АНГИОГЕННОГО СЕПСИСА
S0 – отсутствие клинических признаков ангиогенного хрониосепсиса
S1 – признаки сепсиса без органной дисфункции
S2 – клинические признаки тяжелого сепсиса с органной дисфункцией
S3 – септический шок
ПО НАЛИЧИЮ СОПУТСТВУЮЩИХ ГЕМОКОНТАКТНЫХ ИНФЕКЦИЙ
H0 – нет клинических признаков сопутствующих гемоконтактных инфекций (гепатит В, С, D, ВИЧ-инфекция).
H1 – имеются клинические признаки сопутствующих гемоконтактных инфекций (гепатит В, С, D, ВИЧ-инфекция).
Лечение парентеральных наркоманов с постинъекционными гнойно-септическими поражениями нижних конечностей представляет серьезную медицинскую и социальную проблему, сопряжено со значительными материальными затратами и большим количеством осложнений. Многообразие клинических проявлений, связанных с глубиной поражения, характером и уровнем нарушения магистрального кровообращения в конечности, наличием сопутствующих гемоконтактных инфекций и других факторов, определяет разницу в тактических подходах к лечению этой категории больных. Предложенная адаптированная клиническая классификация постинъекционных гнойно-септических поражений нижних конечностей у больных с наркозависимостью может помочь осуществить выбор рациональной тактики лечения в зависимости от локализации гнойно-септического процесса, вида сосудистого поражения, степени тяжести сепсиса.
Рецензенты:
Оноприев А.В., д.м.н., профессор, профессор кафедры ФПК и ППС № 1 ГБОУ ВПО КубГМУ Минздрава России, г. Краснодар.
Шапошников В.И., д.м.н., профессор, профессор кафедры госпитальной хирургии ГБОУ ВПО КубГМУ Минздрава России, г. Краснодар.

Дата публикации: 05.04.2019 2019-04-05
Статья просмотрена: 73 раза
Гнойные заболевания кожи и подкожно-жировой клетчатки — наиболее часто встречающиеся гнойные заболевания, составляют около 30 % среди этих болезней. По поводу гнойных заболеваний кожи и подкожной клетчатки проводится около 60 % всех амбулаторных хирургических вмешательств. По данным ВОЗ, гнойно-септические заболевания в настоящее время вызываются более чем 30 видами микроорганизмов. Удельный вес возбудителей, участвующих в развитии воспалительного процесса, постоянно меняется. Наиболее часто возбудителем этих заболеваний является стафилококковая флора (70–90 %) [1]. При определённых, благоприятных для развития микроорганизмов условиях воспалительный процесс может быть вызван условно-патогенными микробами, среди которых присутствуют представители нормальной микрофлоры кожи, такие как St. epidermidis, St. haemolyticus и другие.
В современном мире одним из факторов передачи возбудителей гнойно-воспалительных заболеваний может являться такая популярная косметическая процедура как пирсинг. Пирсинг — это своего рода микрооперация, связанная с перфорацией кожи, слизистой, мышц, хрящей, с последующим вживлением в них различных украшений из медицинской стали, титана, благородных и полимерных материалов [6].
Пирсинг является инвазивной процедурой, которой сопутствует определённый риск: возникновение аллергических реакций, занесение инфекции, появление рубцов и шрамов, непредвиденные реакции организма. Выполнение пирсинга без соблюдения надлежащих норм предосторожностей и санитарных мер, несоблюдение принципов асептики и антисептики может привести к передаче инфекционных заболеваний, таких, как гепатит В и С, и даже ВИЧ [4]. В процессе эксплуатации украшение выступает предметом высокой контаминации и размножения условно-патогенной и патогенной микрофлоры. В условиях сниженной резистентности организма возможны местные осложнения, спровоцированные пирсингом [5].
Пирсинг в полости рта является нарастающей тенденцией среди подростков и молодых людей. По данным литературы, пирсинг полости рта имеет множество неблагоприятных эффектов, к которым относятся местные проявления — рецессии десны, травматические дефекты эмали, перелом зуба, нарушение речи или системные осложнения — эндокардит, невралгия тройничного нерва, аллергические реакции, острые воспалительные процессы [2].
Процедура пирсинга должна иметь минимальный риск развития осложнений, которые возникают при несоблюдении определенных правил их проведения. Существование разнообразных источников и путей передачи возбудителей инфекций в условиях парикмахерских и косметических салонов обусловливает риск инфицирования гнойно-септическими инфекциями [3].
Целью настоящего исследования явилось изучение и оценка роли пирсинга в формировании гнойно-воспалительных заболеваний кожи и мягких тканей у человека.
Материалы иметоды. Было обследовано 31 доброволец без острых и хронических соматических заболеваний в возрасте 18–24 лет. В качестве исследуемого материала использовали смыв с пирсингового украшения с поверхности соприкосновения с местом прокалывания. Материал был взят с 77 украшений для пирсинга. Забор материала проводили с использованием стерильных ватных тампонов, фиксировали в транспортировочной среде и доставляли в лабораторию. Исследуемый материал засевали на кровяной агар, желточно-солевой агар и среду Сабуро. После 24–48 часов инкубации выделяли чистые культуры. Идентификация микроорганизмов производилась с использованием метода MALDI-TOF масс-спектрометрии. Также было проведено анкетирование с целью сбора дополнительной информации для исследования.
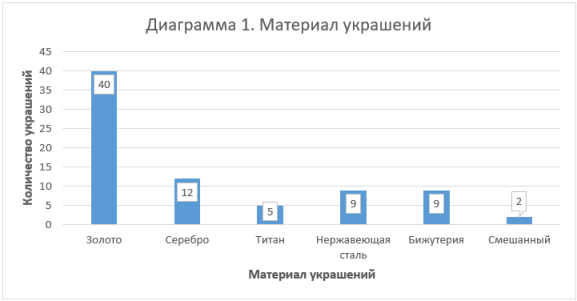
Путем анализа параллельно проведенного анкетирования было выяснено следующее: после процедуры пирсинга в 78,9 % случаев осложнений не было, в 11,8 % — наблюдалось долгое заживление, и лишь в 9,2 % случаев наблюдалось местное воспаление, связанное в свою очередь с ненадлежащим уходом за пирсингом.
В результате исследований были обнаружены бактерии рода Staphylococcus (на 69 обследуемых украшениях пирсинга — 89,6 %), рода Streptococcus (на 2–2,6 %), рода Klebsiella (на 1–1,3 %), рода Corynebacterium (на 1–1,3 %), рода Dermabacter (на 1–1,3 %). Причем на 2 (2,6 %) обследуемых украшениях пирсинга были выявлены одновременно бактерии нескольких родов.
В ходе анализа у добровольцев в микрофлоре украшений пирсинга выделены ассоциации микроорганизмов. Двухчленные ассоциации на 18 обследованных украшениях пирсинга (23,4 %), трехчленные — на 1 (1,3 %). Один вид микроорганизмов обнаружен на 53 обследованных украшениях пирсинга (68,8 %) и ни одного вида на 6 украшениях.
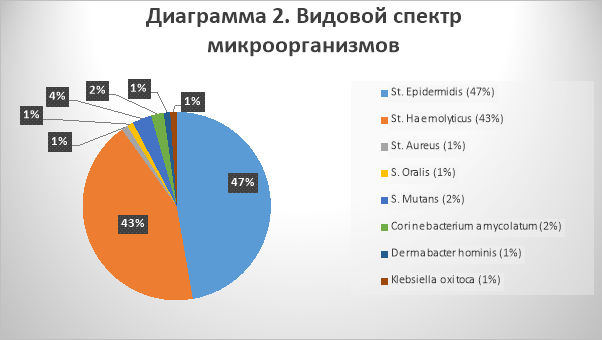
Кроме количественных показателей было охарактеризовано видовое разнообразие выявленных микроорганизмов. Род Staphylococcus: St. epidermidis, St. haemolyticus, St. aureus, род Streptococcus: S. oralis, S. mutans.
Наибольшее видовое разнообразие представлено у бактерий рода Staphylococcus. На диаграмме 2 показан видовой спектр выделенных микроорганизмов.
Выводы
1) Несмотря на то, что St. Epidermidis и St. haemolyticus являются представителями нормальной микрофлоры кожи, у части людей со скомпрометированной иммунной системой может вызывать инфекции, включая гнойно-воспалительные.
2) Наблюдается связь между материалом украшения и присутствующими на них микроорганизмами, на примере сравнения золота и серебра: на украшениях из золота в 2 раза чаще выделялись St. Epidermidis чем на украшениях из серебра.
3) Исходя из параллельно проведенного анкетирования при должном уходе за пирсингом можно избежать осложнений, которые могут привести к возникновению гнойно-воспалительных заболеваний.
Рекомендации. Учитывая достаточную популярность пирсинга, необходимо проводить профилактические мероприятия, направленные на минимизацию развития возможных осложнений. Профилактика должна состоять из социально-популяризируемых мероприятий, в которые входит информирование о возможных осложнениях, а также индивидуальных мероприятий, включающих рекомендации по уходу за пирсингом.
- Голованов В. Н., Пуликов А. С., Кин В. О., Толстоногова Н. И., Хохлов Е. В. Гнойно-воспалительные заболевания пупка у новорожденных // Вестник Хакасского государственного университета им. Н. Ф. Катанова. 2015. № 12. С. 30–31.
- Макеева И. М., Ерохин А. И., Воронкова В. В., Кузин А. В. Пирсинг в стоматологии: обзор литературы // Кафедра терапевтической стоматологии, Кафедра факультетской хирургической стоматологии ГОУ ВПО Первый МГМУ им. И. М. Сеченова, Москва, Пародонтология № 3 (64) 2012
- Тургенева И. А. Роль парикмахерских и косметических технологий в распространении контактных (гемоконтактных) инфекций // Казанский медицинский журнал, 2006 г, том 87, № 6.
- Рябоконь Е. Н., Стоян Е. Ю., Камина Т. В., Шатов П. А. Боди-арт челюстно-лицевой области. Обзор литературы. // Харьковский национальный медицинский университет, кафедра терапевтической стоматологии, кафедра стоматологии
- Ines Kapferer. Tongue Piercing: The Effect of Material on Microbiological Findings / Ines Kapferer, Ulrike S. Beier,Rutger G. Persson // Journal of Adolescent Health — 2011 –49(1). –С.76–83
- Струев И. В., Семенюк В. М., Наумкина Е. В., Одинокий А. И. Микрофлора раневого канала при пирсинге языка, верхней и нижней губы и ее чувствительность к антибактериальным препаратам // Институт стоматологии. 2008. -№ 1. — С.94.
Гнойно-септические заболевания новорожденных
Локализованные гнойно-воспалительные заболевания новорожденных
Заболевания этой группы – одни из наиболее частых у детей периода новорожденности (около 70–80 %). Это обусловлено незрелостью барьерных функций кожи и слизистых оболочек новорожденного ребенка, сниженной сопротивляемостью по отношению к бактериальной инфекции. В группу локальных гнойно-воспалительных очагов условно объединяют так называемые малые инфекции – гнойничковые сыпи, омфалит, дакриоцистит, а также серьезные заболевания – флегмону и пузырчатку новорожденных, остеомиелит. Причинами этих заболеваний чаще всего являются стафилококки и стрептококки, клебсиелла, кишечная палочка, псевдомонас и др.
Лечение местное – обработка водными и спиртовыми растворами антисептиков (фурацилин, хлорофиллипт, бриллиантовый зеленый, раствор калия перманганата), лизоцимом; применение гелий-неонового лазера, при значительной инфильтрации – мази Вишневского, при некротических изменениях – масла облепихового и масла шиповника.
С учетом чувствительности высеянной из пупочной ранки флоры и выраженности воспалительного процесса антибиотики можно применять как местно (орошения, мази), так и внутримышечно или внутривенно.
Свищ пупка – врожденная аномалия развития, является следствием незаращения желточного протока или мочевого хода, существующих в раннем эмбриональном периоде и в норме зарастающих к моменту рождения. Свищ бывает полным и неполным.
Клинические проявления. После отпадения пуповинного остатка обнаруживают свищевое отверстие, из которого выпячивается слизистая оболочка ярко-красного цвета и вытекает кишечное содержимое (полный свищ желчного протока). При полном свище мочевого хода на дне пупочной ямки нет шаровидного выпячивания слизистой оболочки, а имеется участок мокнущей поверхности со свищевым отверстием в центре. Из этого отверстия при натуживании струйкой выделяется моча.
Неполные свищи протекают с явлениями незначительного мокнутия пупка, кожа вокруг которого может быть раздраженной.
Подозрение на врожденный свищ пупка возникает во всех случаях длительного незаживления пупочной ранки, выделений из нее.
Часто неполный свищ трудно определить визуально. Для уточнения диагноза может быть показано рентгенографическое исследование.
Лечение. Полный свищ подлежит хирургическому лечению при установлении диагноза, неполный – в возрасте старше 1 года.
Везикулопустулез – поверхностное гнойное поражение кожи новорожденных. Процесс локализуется в устье потовых желез. Способствуют развитию заболевания иммунная недостаточность у искусственно вскармливаемых детей, перегревание, повышенная потливость.
Клинические проявления. Гнойнички размером с просяное зерно или горошину располагаются по всему кожному покрову, но чаще локализуются на спине, в складках, на коже шеи, груди, в области ягодиц и на волосистой части головы, сопровождаются незначительно повышенной температурой тела. Возможны осложнения в виде отита, бронхопневмонии, пиелонефрита.
Лечение. Умывать, купать детей в период заболевания не рекомендуется. Очаги поражения и видимо здоровую кожу обрабатывают антисептическими бактерицидными средствами: раствор фурацилина 1: 5000, 0,1 %-ный раствор риванола (этакридина лактат), 0,1–0,2 %-ный раствор перманганата калия, анилиновые красители. Непосредственно на очаги гнойничковых элементов наносят пасты с 1 % эритромицина, 1 % линкомицина; мази (эритромициновая, гелиомициновая, линкомициновая, линимент риванола, стрептоцида).
Эпидемическая пузырчатка новорожденных вызывается патогенным золотистым стафилококком, иногда стафилококком в ассоциации с другими микроорганизмами (стрептококками, диплококками). Заболевание представляет собой распространенное гнойное поражение у детей первых дней жизни с недостаточностью иммунных резервов, наличием очагов хронической инфекции у родителей.
Клинические проявления. Характерна множественная разнообразная сыпь: пузыри, гнойники, эрозии на месте вскрывшихся пузырей, наслоение серозно-гнойных корок. Преимущественная локализация – кожа туловища, конечностей, крупных складок. Процесс распространяется на слизистые оболочки рта, носа, глаз и гениталий, сопровождается повышением температуры, диареей, реактивными изменениями в крови и моче. Возможны тяжелые септические осложнения.
Эксфолиативный дерматит новорожденных (болезнь Риттера) – тяжелая форма эпидемической пузырчатки новорожденных.
Клинические проявления. Заболевание характеризуется покраснением кожи со множественными пузырями, обширными эрозивными поверхностями, напоминающими ожог.
В тяжелых случаях процесс протекает септически со снижением массы тела, токсикозом, желудочно-кишечными расстройствами, анемией.
Контагиозность заболевания достаточно велика. Инфицирование новорожденных возможно при наличии внутрибольничной инфекции, а также в результате внутриутробного инфицирования через плацентарное кровообращение.
Лечение. Обязательно внутривенное или внутримышечное введение пенициллинов (метициллина, оксациллина и др.). В качестве антибиотиков специфического антистафилококкового действия используют фузидин-натрий, линкомицина гидрохлорид и производные цефалоспоринов – цефалоридин (цепорин), цефалексин и цефазолин (кефзол). Сульфаниламидные препараты назначают редко вследствие их недостаточной эффективности и возможных токсико-аллергических осложнений. Одновременно с антибиотиками применяют гамма-глобулин, антистафилококковую плазму, антистафилококковый гамма-глобулин, стафилококковый анатоксин. С целью детоксикации вводят капельно внутривенно гемодез, альбумин, реополиглюкин, полиглюкин, плазму, 20 %-ный раствор глюкозы. При дисбактериозе кишечника назначают эубиотики (бифидумбактерин, бификол, бактисубтил, лактобактерин и др.). Показана витаминотерапия, особенно аскорбиновая кислота, пиридоксальфосфат, пантотенат или пангамат кальция, витамины А и Е.
Наружное лечение и уход за детьми имеют особое значение вследствие контагиозности процесса. Производят ежедневную смену белья. Рекомендуются ежедневные ванны с раствором калия перманганата (1: 10 000).
Профилактика. Тщательное соблюдение гигиенического режима. Обязательное кварцевание палат. По возможности детей, страдающих стафилодермиями, помещают в боксы. Сохраняется грудное вскармливание или при недостаточности молока у матери ребенка переводят на донорское грудное молоко.
Стафилококковая пиодермия. Различают поверхностные (остеофолликулит, фолликулит) и глубокие (гидраденит, фурункул, карбункул) формы.
Остеофолликулит – гнойное воспаление устья волосяного фолликула с образованием гнойничка, пронизанного в центре волосом. При распространении нагноения вглубь фолликула возникает фолликулит. Более глубокое гнойно-некротическое воспаление волосяного фолликула и окружающих тканей с образованием гнойного стержня называется фурункулом. Фурункул верхней части лица опасен вследствие возможного распространения инфекции в полость черепа.
Средний отит характеризуется наличием в среднем ухе серозного секрета. Причиной могут быть аллергические процессы в носоглотке, неправильное применение антибиотиков. Скопление серозного секрета в среднем ухе ограничивает подвижность слуховых косточек и барабанной перепонки, что приводит к развитию тугоухости.
Лечение. Санация носоглотки, восстановление проходимости слуховой трубы.
При отсутствии эффекта показаны пункция барабанной перепонки, удаление секрета и введение гормональных препаратов.
Остеомиелит представляет собой гнойное воспаление элементов кости. Возбудителем заболевания может быть любой гноеродный микроорганизм.
Клинические проявления. Заболевание начинается остро. Первым симптомом является резкая боль в конечности, от которой ребенок кричит и избегает всяких движений. Старшие дети строго локализуют боль, у детей младшего возраста она проявляется особым беспокойством, когда их берут на руки или перекладывают. Температура тела поднимается до 39–40 °C. Наблюдаются рвота, понос. Внешние признаки остеомиелита вначале могут отсутствовать. При пальпации место наибольшей болезненности удается установить только у старших детей. По мере развития процесса, когда он переходит на мягкие ткани, появляется припухлость, изменяется конфигурация конечности. Кожа становится отечной и покрасневшей. Близлежащий сустав деформирован.
Клиническое течение острого остеомиелита зависит от ряда причин: патогенности микроорганизма и реактивности организма ребенка, возраста больного и др. Различают 3 формы заболевания: токсическую, септикопиемическую, местную. Первая характеризуется бурным началом, преобладают явления сепсиса, и больной нередко умирает раньше, чем успели проявиться местные изменения.
Вторая форма наблюдается чаще других; четко выражены местные явления, сочетающиеся с общесептической реакцией; иногда поражаются сразу несколько костей, наблюдаются гнойные метастазы в другие участки тела.
Третья форма отличается легким течением с преимущественным выражением местных явлений.
Диагностику заболевания уточняет рентгенологическое исследование.
Дакриоцистит новорожденных – это воспаление слезного мешка. Причиной заболевания является неполное раскрытие носослезного протока к моменту рождения. Проявляется слезостоянием, слизисто-гнойным отделяемым у внутреннего угла глаза. При надавливании на область слезного мешка (у внутренних углов глаз) выделяется гнойное содержимое.
Лечение. Массаж области слезного мешка в направлении сверху вниз для разрыва пленки и восстановления проходимости носослезного протока. Если проходимость не восстанавливается в течение недели, ребенка необходимо направить к окулисту для зондирования и промывания слезных путей.
Парапроктит представляет собой воспаление клетчатки около прямой кишки. Внедрению инфекции способствуют раздражение кожи и опрелости.
Клинические проявления. На ограниченном участке кожи около заднего прохода появляются уплотнение и покраснение, сопровождающиеся болью во время акта дефекации. Ребенок становится беспокойным, иногда нарушается общее состояние, температура тела повышается до 38–39 °C. Больной избегает садиться или опирается только на одну половину ягодиц. Боли постепенно нарастают.
Характерно резкое усиление боли при надавливании. Иногда при этом выделяется гной из заднего прохода.
Лечение заключается в как можно более быстром вскрытии нагноения. Иногда происходит самопроизвольное вскрытие гнойника. При этом после стихания воспалительных явлений остается свищ с гнойным отделяемым. Временами свищ закрывается, но после очередного обострения вскрывается вновь, и так повторяется многократно. При наличии свища показано хирургическое лечение.
Флегмона новорожденных – это своеобразное воспаление подкожной клетчатки, наблюдаемое в первый месяц жизни. Возбудителем может быть любой гноеродный микроорганизм, чаще стафилококк.
Клинические проявления. Заболевание начинается остро. Ребенок беспокоен, теряет аппетит, температура тела поднимается до 39–40 °C. На коже появляется ограниченный участок покраснения и уплотнения, болезненный на ощупь. Наиболее частая локализация – крестцово-копчиковая область, грудь, шея. Воспалительный очаг быстро увеличивается по площади. Кожа над ним приобретает багровый, затем синюшный оттенок.
На 2—3-и сутки в центре поражения возникает участок размягчения. В этом месте кожа быстро расплавляется и образуется свищ, через который отторгаются омертвевшие ткани.
По краям происходит отслойка кожи, которая подвергается расплавлению, и образуется обширная рана с неровными краями. Нередко процесс распространяется вглубь и вширь, обнажаются кости.
Лечение. Новорожденному требуются экстренная помощь и лечение в условиях хирургического стационара.
Сепсис новорожденных детей
Сепсис – тяжело протекающая, приобретенная внутриутробно или сразу после рождения (в периоде новорожденности) общая бактериальная инфекция.
Предрасполагающими факторами со стороны матери являются: общее состояние здоровья, тяжелые заболевания внутренних органов, токсикозы беременных и инфекционные заболевания. Незадолго до родов или во время их у рожениц отмечают повышение температуры тела, сопровождающее обострение хронических инфекционных заболеваний.
Со стороны новорожденного исключительное значение для возникновения септического процесса имеет состояние реактивности его организма. Повышение содержания различных факторов защиты в определенной степени связано с началом грудного вскармливания.
Преобладающей флорой, высеваемой при сепсисе новорожденных, являются стафилококки, кишечная палочка, реже клебсиелла, энтеробактер и протей.
Частое развитие септического процесса у новорожденных связано с анатомо-физиологическими особенностями организма, незрелостью ряда систем и органов, в первую очередь ЦНС и системы иммунитета.
Помимо особенностей организма новорожденных, в развитии сепсиса большое значение имеют патогенность возбудителя и массивность инфицирования.
Инфицирование новорожденного может произойти внутриутробно, во время родов или после рождения. Дородовое инфицирование у доношенных новорожденных встречается редко и только при условии массивной и длительной циркуляции бактерий в крови матери во время беременности. Среди недоношенных детей с сепсисом 20 % инфицируется до начала родов, 40 % – в процессе родового акта, остальные – после рождения. Недоношенность, незрелость, пороки развития и наследственные заболевания являются благоприятным фоном для развития септического процесса.
Пупочная ранка у новорожденного является одним из мест для проникновения инфекции и локализации первичного очага с вовлечением в процесс пупочных сосудов.
Наряду с этим входными воротами инфекции могут быть кожные покровы, легкие, кишечник, мочевыводящая система и др.
При внутриутробном сепсисе симптомы заболевания можно отметить при рождении или в первые часы жизни. Развитие септического процесса при инфицировании после рождения чаще наблюдают на 2—3-й неделе жизни.
Клинические проявления. В начальном периоде сепсиса наряду с местными симптомами гнойного очага на месте входных ворот обращают на себя внимание признаки токсикоза – снижение аппетита или полное его отсутствие, плохая прибавка в массе тела, вялость или возбуждение, стойкий отечный синдром, повышение температуры тела, снижение рефлексов, неустойчивый стул, вздутие живота, одышка, учащение сердечных сокращений, приглушение тонов сердца, синюшность, бледность кожи, нередко с сероватым или желтушным оттенком.
Характерен внешний вид больного: беспокойство, адинамия, серо-бледный цвет кожи, вздутый живот с отечностью передней брюшной стенки и хорошо видимой венозной сетью, срыгивания, рвота, амимичное (лишенное мимики) лицо, увеличение печени и селезенки.
Молниеносный сепсис (септический шок) характеризуется сменой нескольких фаз. В первой фазе шока отмечаются снижение артериального давления, одышка, снижение мочевыделения, возбуждение, вздутие живота.
Во второй фазе шока при прогрессирующем ухудшении микроциркуляции крови развивается сердечно-сосудистая недостаточность – нарастание числа сокращений сердца и одышки, расширение границ сердца, синюшность, отеки; увеличение печени. Одновременно появляются вялость, заторможенность, снижение мышечного тонуса, могут быть судороги. Кожа приобретает мраморный рисунок. Появляются признаки внутрисосудистого свертывания крови: кишечные, легочные кровотечения, кровоточивость из мест инъекций, отсутствие образования и выделения мочи, желтуха. Особая тяжесть состояния отмечается при кровоизлиянии в надпочечники. Типичным для септического шока является появление участков омертвления кожи с последующим их отторжением в виде пузырей.
Острый сепсис клинически может выявляться как септицемия или септикопиемия.
Септикопиемия характеризуется высокой лихорадкой, резко выраженными явлениями интоксикации, наличием гнойных очагов, синдромом кровотечений, высыпаниями на коже, падением массы тела и пр.
Септицемия – клиническая форма сепсиса, при которой у больного резко выражены признаки нарастающего токсикоза при отсутствии очагов гнойного воспаления.
Для подострого течения сепсиса характерно преобладание вышеперечисленных признаков токсикоза при нерезко выраженной или стертой симптоматике на месте очага инфекции.
Для недоношенных детей типично подострое течение сепсиса, проявляющееся в первые дни и недели жизни как синдром дыхательных расстройств. Температура тела при этом может быть нормальной.
Для стафилококкового сепсиса типичны локальные гнойные поражения кожи, пупка, подкожной клетчатки, костей, признаки острого токсикоза.
Лечение. Вскармливание ребенка, больного сепсисом, должно быть естественным. Важнейшим звеном лечения в начале и в разгаре септического процесса является антибактериальная терапия. Обычно используют максимальные возрастные дозировки двух антибиотиков и назначают их разными путями (через рот, внутримышечно, внутривенно). Антибиотики в максимальных дозах применяют только на фоне инфузионной терапии. Дезинтоксикация обеспечивается назначением инфузионной терапии при нормальной функции почек. Иммунокорригирующая терапия в периоды начальный и разгара носит заместительный характер, т. е. осуществляется пассивная иммунизация путем переливания свежей крови, иммуноглобулинов. Местное лечение гнойных очагов осуществляется совместно с детским хирургом. Симптоматическая терапия включает сердечно-сосудистые средства, витамины.
Прогноз. Летальность от сепсиса варьируется от 10 до 80 %.
В зависимости от локализации септического процесса у выздоровевших детей могут наблюдаться различные состояния (задержка физического развития, частые инфекционные заболевания, анемия, увеличение печени и селезенки, поражение ЦНС и др.).
Диспансерное наблюдение. Все больные, перенесшие сепсис, наблюдаются в течение 12 месяцев. В возрасте до 1 года осмотры проводятся ежемесячно, старше 1 года – ежеквартально. Обращается внимание на общее состояние, мышечный и эмоциональный тонус, аппетит, динамику массы тела, режим дня и вскармливание. Показатели периферической крови контролируются через 1 месяц после выписки, затем 1 раз в 3 месяца. Медикаментозные назначения зависят от состояния ребенка. При полном благополучии дети снимаются с учета через 12 месяцев.
После сепсиса, развившегося с первых дней жизни, вакцинация БЦЖ и другие прививки проводятся строго индивидуально.
Профилактика. Профилактика сепсиса начинается задолго до рождения ребенка. Она включает в себя широкий комплекс мероприятий по оздоровлению девочекподростков, санитарно-гигиеническому просвещению населения (борьба с курением, употреблением алкоголя, гигиена половой жизни). Большое значение имеет работа женских консультаций по оздоровлению женщин, предупреждению абортов, санации беременных.
Сохраняет свое значение в профилактике сепсиса четкое соблюдение санитарно-гигиенического режима в роддоме, соблюдение правил обработки пуповины (вторичная обработка на 2—3-й день жизни), раннее прикладывание к груди, совместное пребывание матери и новорожденного.
Важная роль принадлежит ограничению применения антибиотиков в роддоме (особенно пенициллинового ряда) и профилактике дисбактериоза. Огромное значение в профилактике гнойно-септических заболеваний у новорожденных и грудных детей имеет естественное вскармливание, предупреждение маститов.
Данный текст является ознакомительным фрагментом.
Читайте также:


