Свечи при стрептококковой инфекции
К наиболее популярным бетта-гемолитическим стрептококкам относятся:
Серогруппа A (GAS): Streptococcus pyogenes (ранее — Streptococcus haemolyticus), Streptococcus agalactiae anginosus, S. dysgalactiae subsp. Еquisimilis. Эта группа стрептококков обычно способствует развитию большого количества болезней по всему организму — ангины, фарингита, пиодермии, скарлатины, вагинита, цистита, цервицита, эндометрита и других.
Серогруппа B (GBS): Streptococcus agalactiae. Эта группа стрептококков обычно оседает в кишечнике и мочеполовой системе. Способствуют развитие различных инфекционных заболеваний новорожденных детей и рожениц – эндометрита, менингита, сепсиса, неврологические расстройства и другие.
Серогруппа С (GCS): Streptococcus equi (мытный стрептококк), Streptococcus zooepidemicus. Являются патогенной микрофлорой, инфицирующей животных, и вызывающей заболевание именно у животных.
Серогруппа D (GDS): Streptococcus faecalis, Streptococcus faecies. Способствуют развитию септических процессов. Данные виды бактерий были переведены в другое семейство — энтерококки (лат. Enterococcus).
Анализ на стрептококк обычно берется из следующих материалов: мазки, взятые из ротоглотки (при заболеваниях верхних дыхательных путей), влагалища или уретры (при заболеваниях мочеполовой системы), мокрота из носа, соскобы поверхности кожи (при рожистых заболеваниях), а также крови и мочи.
Таким образом, выделяют следующие анализы и методы обследования организма при стрептококковой инфекции:
Кроме того, необходимо дифференциальная диагностика, чтобы отличить стрептококковую инфекцию от: дифтерии, инфекционного мононуклеоза, краснухи, кори, дерматитов, экземы и других видов инфекции – стафилококка, трихомонады, герднереллы, кандиды, хламидии, уреаплазмы, микоплазмы и т.д.

Как лечить стрептококк? Лечение стрептококка обычно состоит из нескольких пунктов:
1. Антибактериальная терапия;
2. Укрепление иммунной системы;
3. Восстановление нормальной микрофлоры кишечника, которая обычно нарушается при применении антибактериальных препаратов;
4. Детоксикация организма;
5. Антигистаминные препараты – назначаются детям, при аллергии на антибиотики;
6. Симптоматическая терапия;
7. При одновременном заболевании и другими болезнями, производится и их лечение.
Начало лечения – обязательное посещение врача, который с помощью диагностики выявит тип возбудителя и эффективное против него средство. Применение антибиотиков широко спектра действия может усугубить течение болезни.
Лечение стрептококковой инфекции может проводиться разными специалистами – в зависимости от формы инфекции – терапевт, педиатр, дерматолог, гинеколог, хирург, уролог, пульмонолог и др.
1. Антибактериальная терапия
Важно! Перед применением антибиотиков обязательно проконсультируйтесь с лечащим врачом.
Курс антибактериальной терапии назначается индивидуально, лечащим врачом. Обычно он составляет 5-10 дней.
Важно! Для лечения стрептококков широко применяют антибактериальные препараты пенициллинового ряда. Если на пенициллины появились аллергические реакции, применяют макролиды. Антибиотики тетрациклинового ряда против стрептококковой инфекции считаются малоэффективными.
2. Укрепление иммунной системы
Природным иммуностимулятором является аскорбиновая кислота (витамин С), большое количество которого присутствует в таких продуктах, как – шиповник, лимон и другие цитрусовые, киви, клюква, облепиха, смородина, петрушка, калина.
восстановление нормально микрофлоры кишечника
4. Детоксикация организма.
Как и писалось в статье, стрептококковая инфекция отравляет организм различными ядами и ферментами, которые являются продуктами их жизнедеятельности. Эти вещества усложняют течение болезни, а также вызывают немалое количество малоприятных симптомов.
Для выведения из организма продуктов жизнедеятельности бактерий необходимо пить много жидкости (около 3 литров в сутки) и полоскать носо- и ротоглотку (раствором фурациллина, слабо-соляным раствором).
5. Антигистаминные препараты
6. Симптоматическая терапия
Для облегчения симптоматики при инфекционных заболеваниях, назначают различные препараты.
Лечение стрептококка народными средствами
Важно!; Перед применением народных средств проконсультируйтесь с врачом.
Абрикос. Для лечения стрептококковой инфекции хорошо зарекомендовали себя абрикосы – абрикосовую мякоть нужно употреблять 2 раза в день, утром и вечером, натощак. При кожных поражениях, кожу также можно натирать абрикосовой мякотью.
Черная смородина. Ягоды черной смородины не только содержат высокую дозу витамина С, но и являются природным антибиотиков. Чтобы использовать данные ягоды в качестве лечебного средства, нужно после каждого приема пищи съедать их по 1 стакану.
Хлорофиллипт. В качестве спиртового и масляного раствора можно использовать для лечения заболеваний ЛОР-органов. Спиртовой раствор применяется в качестве полоскания носовой полости и горла, масляным раствором закапывают нос и смазывают миндалины. Курс лечения 4-10 дней.
Шиповник. Залейте жменьку шиповника 500 воды, доведите средство до кипения, прокипятите около 5 минут и отставьте на несколько часов для настаивания. Приготовленный отвар пейте по 150 мл, два раза в день. Замечено повышение эффективности при одновременном применении этого средства с употреблением абрикосового пюре.
Лук и чеснок. Данные продукты являются природными антибиотиками против различной инфекции. Для использования лука и чеснока в качестве лечебного средства, не нужно готовить что-нибудь особенного, их нужно просто употреблять вместе с другой пищей, хотя бы пару раз в день.
Череда. Тщательно измельчите и залейте 400 мл кипятка 20 г. сухой череды, накройте емкость и оставьте для настаивания. Когда средство остынет, хорошо его процедите и принимайте по 100 мл, 4 раза в день.

Профилактика стрептококка включает в себя следующие рекомендации:
— Соблюдайте правила личной гигиены – чаще мойте руки, чистите зубы, пищу кушайте только мытыми руками;
— Делайте в дома влажную уборку, не менее 2 раз в неделю;
— Старайтесь больше двигаться, займитесь спортом, закаляйтесь;
— Не оставляйте на самотек возможные очаги инфекции – воспаленные миндалины, кариес зубов, аденоиды, конъюнктивиты, фурункулы, воспалительные процессы в мочеполовой системе и т.д.;
— Чаще проветривайте помещение;
— Избегайте мест большого скопления людей, особенно в закрытых помещениях и в сезон респираторных заболеваний;
— Если дома есть больной, выделите ему для личного пользования столовые приборы, предметы личной гигиены, полотенце и постельное белье;
— Не используйте на работе одну посуду на нескольких человек, а также не пейте воду из горла, одновременно с несколькими людьми;
— Старайтесь питаться продуктами, богатыми витаминами и микроэлементами;
— Если в жилом помещении есть кондиционер, воздухоочиститель или пылесос, не забывайте чистить их фильтры, и кстати, листья некоторых цветов также являются природными воздухоочистителями, поэтому не забывайте их тоже ополаскивать водой;
— Старайтесь не посещать салоны красоты, солярии, татту-салоны, стоматологические и другие клиники сомнительного характера, где могут не придерживаться необходимых санитарных норм при своей деятельности.
К какому врачу обратится при стрептококковой инфекции?
, MD, FACP, Charles E. Schmidt College of Medicine, Florida Atlantic University;
, MD, Wellington Regional Medical Center, West Palm Beach
Last full review/revision September 2017 by Larry M. Bush, MD, FACP; Maria T. Perez, MD









Классификация стрептококков
Три различных типа стрептококков дифференцируют по характерным зонам гемолиза при выращивании на агаре овечьей крови:
Бета-гемолитические стрептококки образуют зоны прозрачного гемолиза вокруг каждой колонии.
Альфа-гемолитические стрептококки (обычно называемые стрептококки viridans) окружены зоной зеленоватой окраски, образующейся в результате частичного гемолиза.
Гамма-гемолитические стрептококки не являются гемолитическими.
Следующая классификация, базирующаяся на особенностях углеводов клеточной стенки, подразделяет стрептококки на группы согласно Лэнсфилду от А до H и от K до T ( Классификация стрептококков). Стрептококки группы вириданс формируют отдельную группу, которая трудно поддается классификации. В классификации Лэнсфилда энтерококки были первоначально включены в группу стрептококков D. Позже энтерококки были классифицированы как отдельный род.
Группа по Лэнсфилду
Streptococcus pyogenesStreptococcus pyogenes
Фарингит, тонзиллит, инфекции ран и кожи, септицемия, скарлатина, пневмония, ревматическая лихорадка, гломерулонефрит
Пенициллин, эритромицин, клиндамицин
Незамедлительный хирургический контроль
Бета-лактамы (обычно широкий спектр, если этиология не выявлена; если выявлены бета-гемолитические стрептококки группы А, можно назначить пенициллин или цефазолин) плюс клиндамицин
Сепсис, послеродовой или неонатальный сепсис, менингит, инфекции кожи, эндокардит, септический артрит, ИМП
Пенициллин или ампициллин, цефалоспорин, ванкомицин
Фарингит, пневмония, целлюлит, пиодермия, рожистое воспаление, импетиго, инфекции раны, послеродовой сепсис, неонатальный сепсис, эндокардит, септический артрит
Пенициллин, ванкомицин, цефалоспорины, макролиды (разной восприимчивости)
Энтерококковый: Enterococcus faecalis, E. faecium
Неэнтерококковый: S. bovis, S. equinus
Альфа или гамма
Эндокардит, инфекция мочевых путей, интраабдоминальная инфекция, целлюлит, инфекция раны, а также сопутствующая бактеремия
Пенициллин, ампициллин, ванкомицин (плюс аминогликозид при тяжёлой инфекции)
Ванкомицин-резистентные энтерококки: стрептограмины (хинупристин/дальфопристин), оксазолидононы (линезолид), липопептиды
S. gallolyticus (ранее S. bovis биотип I)
Кишечные аденомы или карциномы, эндокардиты
S. mutans, S. sanguis, S. salivarius, S. mitior, S. anginosus (ранее S milleri), S. constellatus, S. intermedius
Альфа или гамма
Эндокардит, бактериемия, менингит, локализованная инфекция, абсцессы (особенно S. anginosus)
Пенициллин, ампициллин, ванкомицин (плюс аминогликозид при тяжёлой инфекции), другие антибиотики, основываясь на in vitro чувствительности
Менингит, иногда синдром токсического шока
Целлюлит, инвазивные инфекции, обусловленные рыбой
*Нет соответствия специфической подгруппе.
GABHS = бета-гемолитические стрептококки группы А.
Факторы вирулентности
Многие стрептококки вырабатывают факторы вирулентности, включая стрептолизины, ДНКазы и гиалуронидазу, которые способствуют разрушению ткани и распространению инфекции. Отдельные штаммы продуцируют экзотоксины, которые активируют определенные Т-клетки, вызывая высвобождение цитокинов, включая фактор некроза опухоли-альфа, интерлeйкины и другие иммуномодуляторы. Эти цитокины активизируют комплемент, коагуляцию и фибринолитические системы, что ведет к шоку, полиорганной недостаточности и смерти.
Болезни, вызываемые стрептококками
Наиболее значимым патогеном из группы стрептококков является S. pyogenes, который является бета-гемолитическим и по классификации Лэнсфилда относящийся к группе А, поэтому его относят к бета-гемолитическим стрептококкам группы А (БГСА).
Самыми распространенными острыми заболеваниями, вызванными GABHS, являются:
Кроме того, отдаленные негнойные осложнения (ревматизм, острый гломерулонефрит) наблюдаются спустя ≥ 2 недели после инфекции.
Заболевания, вызываемые другими штаммами стрептококков, менее распространены и обычно включают инфекцию мягких тканей или эндокардит ( Классификация стрептококков). Некоторые инфекции, вызываемые не β-гемолитическими стрептококками группы А, развиваются у определенных групп населения (например, стрептококки группы B вызывают заболевания у новорожденных и рожениц).
Бета-гемолитический стрептококк группы А может распространяться через поражённые ткани и вдоль лимфатических каналов (вызывая лимфангиты) к региональным лимфоузлам (вызывая лимфадениты). БГСА могут также вызывать местные гнойные осложнения, такие как перитонзиллярный абсцесс, средний отит, синусит и бактериемию. Нагноение зависит от тяжести инфекции и восприимчивости ткани.
Другие тяжелые инфекции БГСГА включают септицемию, послеродовый сепсис, эндокардит, пневмонию и эмпиему.
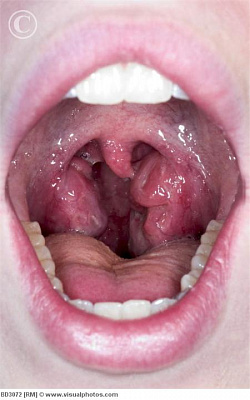
Стрептококковый фарингит обычно вызывается β-гемолитическими стрептококками группы А. Приблизительно у 20% пациентов наблюдается острый тонзиллит, лихорадка, покраснение ротоглотки и гнойный налет на миндалинах. У остальных – менее выраженные симптомы, первичный осмотр может выявить картину, похожую на вирусный фарингит. Шейные и подчелюстные узлы увеличены и болезненны. Стрептококковый фарингит может осложниться перитонзиллярным абсцессом. Кашель, ларингит и заложенность носа нехарактерны для стрептококковой фарингеальной инфекции; наличие таких симптомов предполагает другую причину (обычно вирусную или аллергическую).

Состояние бессимптомного носительства может наблюдаться примерно в 20% случаев.
Скарлатина в настоящее время - редкое заболевание, однако вспышки скарлатины все еще возникают. Передача усиливается в условиях тесного контакта между детьми (например, в школах или детских садах).
Скарлатина - преимущественно детская болезнь, как правило, поражает глотку; реже встречается поражение стрептококковой инфекцией других областей (например кожи). Скарлатина вызывается стрептококками группы А, которые продуцируют эритрогенный токсин, приводящий к диффузному покраснению кожи с розовато-красным оттенком, бледнеющим при надавливании.
Сыпь лучше всего видна на животе или боковой части грудной клетки в виде темно-красных полос в кожных складках (линии Пастиа), на фоне бледного носогубного треугольника. Сыпь состоит из характерных, многочисленных, небольших (1–2 мм) папулезных высыпаний, придающих коже вид наждачной бумаги. Когда лихорадка купируется, обычно начинается отшелушивание верхнего слоя кожи. Обычно, сыпь длится 2–5 дней.

Малиново-красный язык (воспалённые сосочки, проявляющиеся сквозь ярко-красную оболочку) также типичен, эти симптомы необходимо дифференцировать от изменений языка, характерных при синдроме токсического шока и болезни Кавасаки.

Другие симптомы похожи на стрептококковый фарингит, а течение и контроль скарлатины – те же, как и при других инфекциях группы А.
Кожные инфекции включают:
Импетиго – это поверхностная инфекция кожи, протекающая с образованием корок и пузырей.

Рожистое воспаление (рожа) – это вариант поверхностной флегмоны с поражением лимфатических сосудов дермы. У пациентов имеются блестящие, красные, выпуклые, уплотненные очаги поражения с четкими краями. Чаще всего поражение вызвано БГСА, но иногда и другими стрептококками и нестрептококковыми возбудителями.

Флегмона затрагивает глубокие слои кожи и может быстро распространяется из-за многочисленных литических ферментов и токсинов, продуцируемых преимущественно стрептококками группы А.

На фотографии продемонстрировано локальное покраснение и отек, которые обычно сопровождаются местным повышением температуры и болезненностью при надавливании, характеризующие очаговый целлюлит.
Некротизирующий фасциит, вызванный S. pyogenes, является тяжелой кожной (иногда и мышечной) инфекцией, которая распространяется по фасциальным каналам. Инокуляция возбудителя происходит в коже или кишечнике.

Некротирующий фасциит распространен среди наркоманов, злоупотребляющих внутривенными препаратами.
Прежде известный как стрептококковая гангрена, этот синдром может также быть полимикробным, с участием аэробной и анаэробной микрофлоры, включая Clostridium perfringens. Полимикробная этиология заболевания вероятна, когда источником инфекции является кишечник (например, после операции на кишечнике, перфорации кишечника, дивертикулита или аппендицита).
Некротический фасциит начинается остро с повышения температуры тела и резкой локализованной боли, несоразмерной наблюдаемой физической картине, боль быстро прогрессирует и часто бывает первым, а иногда и единственным, проявлением болезни. Может присутствовать диффузная или локальная эритема. Тромбоз микроциркуляторного русла вызывает ишемический некроз, что приводит к быстрому распространению и непропорционально тяжелой интоксикации. У 20–40% пациентов поражены соседние мышцы. Шок и дисфункция почек распространены. Характерна высокая летальность даже при адекватном лечении.
Стрептококковый синдром токсического шока, подобный СТШ, вызванному S. aureus, может развиваться в результате инфекции токсин-продуцирующими штаммами GABHS и иногда другими стрептококками. У здоровых детей и взрослых стрептококки этой группы вызывают обычно инфекции мягких тканей и кожи.
Механизм, при котором определенные штаммы β-гемолитических стрептококков группы А вызывают поздние осложнения, неясен, может проявиться как аутоиммунное заболевание.
Ревматическая лихорадка – это воспалительное заболевание, встречающееся приблизительно у 3% пациентов через несколько недель после недолеченного фаринита, вызванного GABHS. Она стала гораздо менее распространенной в развитых странах, но все еще обычна в развивающихся странах. Диагноз первого эпизода основан на сочетании симптомов артрита, кардита, хореита, специфических кожных проявлений и результатов лабораторных анализов (критерии Джонса— Измененные критерии Джонса и первый эпизод острой ревматической лихорадки (ОРЛ)*).
Одна из самых основных причин необходимости лечения фарингита, вызванного БГСА (стрептококкового воспаления горла), состоит в том, чтобы предотвратить ревматическую лихорадку.
Постстрептококковый острый гломерулонефрит – острый нефритический синдром, развивающийся как осложнение фарингита или инфекции кожи, вызванной ограниченными нефрогенными штаммами GABHS (например, М-протеин серотипов 12 и 49). После инфекции горла или кожи, вызванной одним из этих штаммов, приблизительно 10–15% пациентов заболевают острым гломерулонефритом. Состояние чаще распространено среди детей и развивается спустя 1–3 нед. после инфекции. Почти все дети и несколько меньшее число взрослых выздоравливают без хронического почечного нарушения. Лечение данной инфекции антибиотиками имеет небольшое влияние на последующее развитие гломерулонефрита.
Синдром PANDAS (детское аутоиммунное нейропсихическое нарушение, связанное со стрептококками группы А), относится к под-множеству обсессивных нарушений или тиковых расстройств у детей, которые, как считается, также связаны с инфекцией β-гемолитических стрептококков группы А.
Определенные формы псориаза (например, каплевидный) могут также быть связаны с бета-гемолитическими стрептококковыми инфекциями.
Диагностика
Иногда экспресс-диагностика на антиген или титры антител
Стрептококки быстро идентифицируются посевом в питательной среде с бараньей кровью.
Существуют тесты для быстрого выявления антигена, которые могут обнаружить β-гемолитические стрептококки группы А непосредственно по мазку из ротоглотки (например, для диагностики на месте). Многие анализы основаны на иммуноферментном анализе, но в последнее время стали применяться анализы с использованием оптического иммунологического исследования. Эти быстрые тесты имеют высокую специфичность ( > 95%), но варьируют в значительной степени по чувствительности (от 55 до 80–90% у более современных оптических иммунологических анализов). Таким образом, положительные результаты могут установить диагноз, но отрицательные результаты, по крайней мере у детей, должны быть подтверждены культуральным исследованием. Поскольку стрептококковый фарингит менее распространен среди взрослых и они вряд ли будут иметь постстрептококковые осложнения, многие врачи не подтверждают у взрослых отрицательный результат при культивировании, если только не рассматривается вопрос использования макролидов; в таких случаях следует проводить тестирование на чувствительность к макролидам.
Обнаружение антистрептококковых антител в сыворотке крови в период выздоровления дает лишь косвенные доказательства инфекции. Анализ на противострептококковые антитела не являются целесообразным при диагностике острой БГСА-инфекции, поскольку антитела впервые вырабатываются через несколько недель после начала болезни, а повышение одного титра антител, скорее всего, отражает длительную предшествующую инфекцию. Обнаружение антител является основным при диагностике постстрептококковых заболеваний, таких как ревматизм и гломерулонефрит.
Титры антистрептолизина O (АСЛ-О) и антидезоксирибонуклеазы В (анти-ДНКазы B) начинают расти примерно через 1 неделю после заражения БГСА и достигают максимума через 1-2 месяца после заражения. Оба титра могут оставаться повышенными в течение нескольких месяцев, даже после неосложненных инфекций. Титры измеряются в острой фазе и в фазе выздоровления, спустя 2-4 недели. Результат считают положительным при увеличении титра в 2 и больше раза. Повышение одного титра выше верхнего предела нормы, указывает на предшествующую стрептококковую инфекцию или высокую стрептококковую эндемичность в социальной среде. Титр АСO повышается только в 75–80% инфекций. Для окончательного подтверждения диагноза в трудных случаях может также использоваться любой из других анализов (антигиалуронидаза, антиникотинамид аденин динуклеотидаза, антистрептокиназа).
Пенициллин, который назначают в течение первых 5 дней при симптоматическом стрептококковом фарингите, может задержать появление и уменьшить интенсивность иммуного ответа на антистрептолизин.
Пациенты со стрептококковой пиодермией обычно не дают выраженного иммунного ответа на антистрептолизин, но могут дать реакцию на другие антигены (т.е. анти-ДНКаза, антигиалуронидаза).
Возбудителем инфекции является гемолитический стрептококк (Streptococcus haemolyticus). Он имеет овальную или шаровидную форму, его размер в пределах 0,6 — 1 мкм. Образующиеся под его действием в питательных средах цепочки вызывают гемолиз. Довольно устойчив в окружающей среде, в высохшей крови и гное сохраняется несколько месяцев. В благоприятных условиях размножается в некоторых пищевых продуктах, например, креме или мороженом. Дезинфицирующие средства и кипячение быстро убивают микробы.
Ядовитость возбудителя основана токсическими субстанциями, которые обладают свойствами экзотоксина (токсин Дика), а также рядом ферментов — стрептокиназой, гаалуронидазой, РНК-азой, ДНК-азой, фибринолизином, липопротеазой и эндотоксином.
Источником возбудителя инфекции может являться как больной человек, так и его носитель. Носительство отмечено среди всех возрастных категорий. Особое значение вызывает носительство гемолитического стрептококка роженицами и персоналом родильных домов, что довольно часто приводит к появлению инфекции у новорожденных.
Только стрептококк служит возбудителем рожи и скарлатины. Ангина в 80—90% случаев вызывается стрептококком. При диффузных заболеваниях соединительной ткани: ревматизме, остром гломерулонефрите - стрептококковая инфекция является пусковым механизмом патологического процесса. Также стрептококк может быть одним из вероятных возбудителей генерализованной и местной гнойных инфекций — карбункула, абсцесса, лимфаденита, синусита, отита, пиодермии, раневой инфекции, пневмонии, флегмона, менингита, остеомиелита, фурункула, септикопиемии, эндокардита; пищевых токсикоинфекций.
В последние годы стрептококковая инфекция стала частой причиной инфекций мочеполовых путей, как мужчин, так и женщин, причиной выкидышей у женщин и инфекций у плода. У 25% женщин стрептококк обнаруживается и во влагалище. В основном бактерия не обнаруживает своей враждебности. Но так происходит до тех пор, пока иммунная система справляется со своими задачами.
Симптомы стрептококковой инфекции
Стрептококковая инфекция мочеполовых путей у женщин выявляется при бактериологическом посеве из влагалища. Но заболевание не всегда протекает бессимптомно. При стрептококковом вагините (кольпите) вас должны насторожить следующие признаки:
Яркие симптомы наблюдаются при обострении кольпита. При хронической форме проявления заболевания совсем незаметны.
Причины стрептококковой инфекции
Причиной болезни может стать осложнение после скарлатины или ангины, несоблюдение правил личной гигиены, злоупотребление спринцеванием, раздражение от химических веществ и чужеродных объектов, прием медикаментов и общее ослабление организма и иммунитета.
Лечение стрептококковой инфекции
При наличии признаков болезни вам обязательно нужно обратиться к врачу! При стрептококковой инфекции мочеполовых путей доктор пропишет влагалищные свечи или палочки с антибиотиками пенициллинового ряда. Влагалищные ванночки с синтомицином. Состояние облегчит орошение влагалища настоем ромашки, разведенным кефиром или кислым молоком (содержащим молочную кислоту).
Положительный результат даст фитотерапия. Следует принимать природные иммуностимуляторы – эхинацею, женьшень, лимонник, солодку, элеутерококк, алоэ, зверобой. Останавливающее инфекцию действие имеют отвары репейника и хмеля. Положительный эффект даст употребление вишневого сока.
Профилактика стрептококковой инфекции
Профилактика стрептококковой инфекции направлена на источник ее возбудителя, возможные пути его передачи и восприимчивый организм. В отношении источника производят мероприятия, которые направлены на раннее обнаружение у больных некоторых форм инфекций (скарлатины, ангины, местной гнойной инфекцией) и немедленную изоляцию в инфекционном стационаре или в домашних условиях. Лица, которые имели контакт с больным, подлежат обязательному врачебному осмотру для выявления как выраженных, так и стертых форм болезни.
Также проводят дезинфекцию в помещении, где находится инфекционный больной. Лица, которые перенесли болезнь, получают допуск к работе в родильном доме, детском дошкольном учреждении, больнице, на пищеблоке после полного выздоровления, однако не ранее 22-го дня от начала заболевания.
Похожие акции:
Пока нет ни одной акции связанной с данной темой.
Акушерство, гинекология и репродукция. 2015; N2: c.19-23
Целью исследования явилось определение частоты встречаемости стрептококка группы В у рожениц и новорожденных. Материалы и методы. Проспективное исследование включило две группы наблюдения: 1-я группа пациенток (n=35) с доношенной беременностью и срочными родами, 2-я группа пациенток (n=22) с преждевременными родами в сроке от 34 до 37 нед. Всем пациенткам при поступлении и всем новорожденным был проведен экспресс-тест на стрептококк группы В. Результаты исследования. В 1-й группе тест был положительным у 25,7% женщин и у 8,6% новорожденных. Во 2-й группе тест был положительный у 18,2% женщин и у 22,7% новорожденных.
Статья поступила: 30.03.2015 г.; в доработанном виде: 08.04.2015 г.; принята к печати: 17.06.2015 г.
Конфликт интересов
Авторы заявляют об отсутствии необходимости раскрытия финансовой поддержки или конфликта интересов в отношении данной публикации.
Все авторы сделали эквивалентный вклад в подготовку публикации.
Для цитирования
Леваков С.А., Боровкова Е.И. Контаминация родовых путей у беременных стрептококком группы В: актуальность внедрения скрининговых программ. Акушерство, гинекология и репродукция. 2015; 2: 19-23.
Streptococcus Group B contamination of the birth canal in pregnant women: the relevance of the introduction of screening programs
Levakov S.A., Borovkova E.I.
First Moscow State Medical Sechenov University of the Ministry of Health Russian Federation
Summary
The aim of the study was to determine the frequency of occurrence of group B Streptococcus in women in labour and newborn babies. Materials and methods. prospective study included two groups: group 1 patients (n=35) with full-term pregnancy and term birth, group 2 patients (n=22) with preterm birth in the period from 34 to 37 weeks. All patients upon admission and all newborns was carried out rapid test for Streptococcus group B. Results. in the 1st group, the test was positive in 25.7% of women and 8.6% of newborns. In the 2nd group, the test was positive in 18.2% of women and 22.7% of newborns.a prospective study was conducted of contamination of the genital tract in pregnancy Streptococcus group B. We have formed 2 groups: group 1 patients (n=35) with full-term pregnancy and term birth, group 2 (n=22) patients with preterm birth in the period from 34 to 37 weeks. All patients upon admission and all newborns was conducted rapid test for Streptococcus group B. In the 1st group, the test was positive in 25.7% of women and 8.6% of newborns. In the 2nd group, the test was positive in 18.2% of women and 22.7% of newborns.
Key words
Pregnancy, group b Streptococcus, preterm birth, intrapartum infection of the fetus.
Received: 30.03.2015; in the revised form: 08.04.2015; accepted: 17.06.2015.
Conflict of interests
The authors declared that they do not have anything to disclosure regarding funding or conflict of interests with respect to this manuscript.
All authors contributed equally to this article.
For citation
Levakov S.A., Borovkova E.I. Streptococcus group B contamination of the birth canal in pregnant women: the relevance of the introduction of screening programs. Akusherstvo, ginekologiya i reproduktsiya / Obstetrics, gynecology and reproduction. 2015; 2: 19-23 (in Russian).
Ключевые слова: Беременность, стрептококк группы В, преждевременные роды, интранатальное инфицирование плода.
Концептуальной основой для решения этих задач является раннее выявление и предупреждение репродуктивных нарушений, охрана здоровья женщин, оптимизация организации и качества оказания акушерско-гинекологической помощи.
Стрептококк группы В (СГВ, Streptococcus agalactiae) – это грамположительный диплококк рода Streptococcus, семейства Streptococcaceae. Он относится к условно-патогенной флоре, обитающей в кишечнике человека, колонизирует слизистые влагалища и верхних дыхательных путей у детей и подростков. У беременных СГВ диагностируется в 15-40% случаев [1].
Во время беременности СГВ часто является причиной развития бессимптомной бактериурии, гестационного пиелонефрита, внутриутробного инфицирования плода и хореонамнионита. Восходящее инфицирование матки повышает риск спонтанных выкидышей ранних сроков и преждевременных родов. В послеродовом периоде СГВ является причиной развития послеродового эндометрита (8%), пневмонии и сепсиса новорожденных (2%), а также бактериемии без очага поражения (31%) [1,4].
Инфицирование плода происходит интранатально, кроме того, возможно антенатальное заражение при восходящем распространении возбудителя и внутриутробном инфицировании.
В патогенезе развития стрептококковой инфекции у плода и новорожденного имеет значение массивность колонизации Streptococcus agalactiae. При отсутствии проведения лечебных и профилактических мероприятий заболеваемость новорожденных достигает 2% [7].
Согласно рекомендациям Всемирной организации здравоохранения скрининг на наличие бета-гемолитического стрептококка проводится всем беременным в 36 нед. или (если не был выполнен ранее) в родах в случае развития преждевременных родов, лихорадки или длительности безводного промежутка более 12 ч [5].
Абсолютным и доказанным является риск интранатального инфицирования плода, которое происходит в 80-90% случаев. Выделяют две формы неонатальных и перинатальных инфекций: ранняя инфекция (развивается в первые 24-48 ч) и поздняя инфекция (проявляется через 8-10 дней после родов). Наиболее опасной является ранняя инфекция в связи с более острым характером ее течения. Поздняя форма заболевания может быть вызвана внутрибольничной инфекцией (при родах в медицинском учреждении) и очень редко связана с осложнениями при родовспоможении. Заражаемость стрептококками группы B составляет от 1 до 5% (для всех рождений живого плода), смертность от развивающейся инфекции колеблется от 22 до 80% [2,6].
В Российской федерации специфического обследования на бета-гемолитический стрептококк не проводится. Косвенно о контаминации организма можно судить по результатам культурального исследования мочи (проводится после 14 нед. беременности) и отделяемого влагалища.
Целью исследования явилось определение частоты встречаемости СГВ у рожениц и новорожденных.
Материалы и методы
Для достижения поставленной цели было проведено проспективное исследование, включившее 57 рожениц, на базе филиала №2 больницы им. А.К. Ерамишанцева.
При поступлении в родильный дом всем пациенткам проводилось стандартное клинико-лабораторное обследование, включающее УЗИ плода, допплерометрию, кардиотокографию, определение группы крови, резус-фактора, клинического анализа крови и показателей гемостаза.
Кроме того, всем пациенткам и новорожденным, включенным в исследование, проводилось исследование на контаминацию стрептококком группы В с помощью качественного иммунохроматографического экспресс-теста для определения антигена стрептококков группы В во влагалищных мазках.
Метод определения основан на использовании специфического комплекса конъюгированных с красителем мышиных моноклональных антител к стрептококку В и иммобилизованных в тестовой зоне кассеты поликлональных мышиных антител к стрептококку В для его избирательного определения в тестируемых пробах с высокой степенью чувствительности. При прохождении пробы через слой адсорбента меченый конъюгат антител с красителем связывается с присутствующим в пробе стрептококковым антигеном, образуя комплекс антиген-антитело. Этот комплекс связывается с иммобилизованными на мембране в тестовой зоне кассеты поликлональными антителами к антигену стрептококков группы B, образуя в нем пурпурно-розовую полосу, если в пробе присутствует стрептококковый антиген. Если же стрептококки группы B в пробе отсутствуют, окрашенной полосы в тестовой зоне не образуется. Несвязанный конъюгат, продолжая продвигаться по слою адсорбента, достигает контрольной зоны (C), где осаждается с образованием контрольной полосы, подтверждающей качественность применяемых в тесте реагентов.
Статистическая обработка полученных результатов проводилась по стандартным методам описательной и вариационной статистики с применением линейного регрессионного анализа.
Были сформированы две группы: 1-ю группу составили 35 рожениц с доношенной беременностью (37-41 нед.), 2-ю группу – 22 роженицы с преждевременным родами в сроках от 35 до 37 нед.
85% всех пациенток были в возрасте от 24 до 35 лет. В структуре экстрагенитальных заболеваний значимых различий в группах выявлено не было. НЦД по гипертоническому типу встречалось у 14,3 и 13,6% пациенток, варикозное расширение вен нижних конечностей – у 11,4 и 9%, хронический гастрит – у 22,8 и 22,7%, ЖКБ – у 8,6 и 4,5%, железодефицитная анемия – у 11,4 и 13,6% соответственно. В структуре заболеваний органов мочевыводящих путей хронический цистит (14,3 и 18,2%) и МКБ (8,6 и 9%) выявлялись с одинаковой частотой.
Средний возраст менархе в обеих группах составил 11,6 лет (от 10,5 до 14 лет). 89% женщин имели регулярный менструальный цикл. Среди гинекологических заболеваний наиболее распространенными были инфекции, передаваемые половым путем (37,1 и 36,4%), дисфункция яичников (7,7 и 4,5%), эктопия шейки матки (48,6 и 45,5%), миома матки (5,7% в 1-й группе) и полип эндометрия (2,9 и 9%).
Все пациентки были первородящими. 82% пациенток в 1-й группе и 72,7% во 2-й группе были первобеременными. Среди повторнобеременных предыдущие беременности закончились медикаментозным абортом (5,7 и 4,5%), самопроизвольным выкидышем в сроке до 12 нед. (8,6 и 13,6%) и артифициальным абортом (2,8 и 9,1%).
Течение первого триместра настоящей беременности осложнялось развитием раннего токсикоза легкого и среднетяжелого течения (77,1 и 86,4%) и угрозы прерывания беременности, диагностированной в 14,4 и 40,9% случаях соответственно группам. По поводу угрозы прерывания беременности пациентки получали спазмолитическую (дротаверин 120 мг в сут., препарат магния 300 мг в сут.) и гормональную терапию (дидрогестерон 20 мг в сут., натуральный микронизированный прогестерон 400 мг в сут.) до 16-20 нед.
Во II триместре у беременных выявлена железодефицитная анемия (14,3 и 13,6%), угроза прерывания беременности (8,6 и 36,4%), бессимптомная бактериурия (5,7 и 9%) и острый цистит (0 и 4,5%). По поводу развившихся осложнений пациентки получали антианемическую терапию (препараты железа в суточной дозе до 300 мг), спазмолитическую терапию (дротаверин, свечи с гиосцина бутилбромидом), антибактериальную терапию в течение 5-7 дней (защищенные пенициллины, цефалоспорины 2-3-го поколения).
В III триместре беременности умеренная преэклампсия диагностирована у 11,4% пациенток 1-й группы и у 9% 2-й группы, задержка роста плода по асимметричному типу выявлена у 5,7 и 4,5% женщин, угроза преждевременных родов – у 5,7% и 90,9% женщин, частота инфекций нижних отделов мочевыводящих путей составила 11,4 и 22,7% соответственно.
Пациентки, включенные в исследование, поступали в родильный дом с регулярной родовой деятельностью. Из них в 1-й группе с излитием околоплодных вод было 10 (28,5%) пациенток, во 2-й группе – 11 (50%) пациенток. Средняя продолжительность родов у пациенток 1-й группы составила 9±1,2 ч, безводного промежутка – 10,5±1,7 ч. Средняя продолжительность родов у пациенток 2-й группы составила 7,5±2,3 ч, безводного промежутка – 12,2±1,5 ч.
Все дети родились живыми, из них недоношенными 22 ребенка, незрелыми 27 детей. Средняя масса новорожденных в 1-й группе составила 3369±81 г, во 2-й группе – 2725±54 г.
С признаками морфофункциональной незрелости было рождено 27 детей, гипоксически-ишемическое поражение ЦНС выявлено у 8,6 и 9,1% детей, а острую асфиксию в родах перенесли 2,8 и 9,1% детей соответственно. Врожденная пневмония развилась в 2,8 и 18,2% случаев, а проведения интубации трахеи и искусственной вентиляции легких потребовалось в 2,8 и 22,7% случаев.
Всем роженицам при поступлении и их новорожденным был проведен экспресс-тест на наличие СГВ (см. табл. 1). Материалом для исследования у женщин были мазки из заднего свода влагалища и перианальной области, а у новорожденных – мазки из носоглотки и ротовой полости. При получении положительного результата, по данным экспресс-диагностики, пациенткам было проведено профилактическое введение цефазолина 2 г в/в однократно.
Таблица 1. Результаты экспресс-теста на стрептококк группы В.
 |
Из 35 пациенток 1-й группы у 9 (25,7%) был получен положительный результат теста. При этом пять пациенток ранее получали терапию во II и III триместрах в связи с бессимптомной бактериурией или острым циститом. Аналогичная ситуация прослеживается и у пациенток 2-й группы: из четырех женщин с положительным экспресс-тестом у троих были выявлены и пролечены ранее инфекции нижних отделов мочевыводящих путей.
У 1 (2,8%) новорожденного из 1-й группы и у 5 (22,7%) новорожденных из 2-й группы была диагностирована врожденная пневмония. При этом у ребенка из 1-й группы тест на СГВ был отрицательный, у детей из 2-й группы положительный тест был только в двух случаях. Ни одного случая развития сепсиса у новорожденных выявлено не было.
Целесообразность проведения скрининга заключается в выявлении контаминированных пациенток и проведении специфической антибактериальной терапии для снижения риска развития интранатального инфицирования и сепсиса у новорожденного. Внедрение программы обследования и антибиотикопрофилактики позволяет снизить данную частоту в 3 раза [2,3].
Всем беременным в сроке 35-37 нед. необходимо проводить культуральное исследование из влагалища и кишечника на определение стрептококка группы В с использованием селективных сред. Исключение составляют пациентки, у которых была диагностирована бессимптомная бактериурия и женщины, в анамнезе у которых были случаи рождения детей с подтвержденной стептококковой инфекцией. Данным пациенткам не проводится скрининговое обследование, но интранатально проводится антибактериальная профилактика [2].
Антибактериальная профилактика в родах показана женщинам с подтвержденной контаминацией СГВ, пациенткам с рождением в предыдущей беременности ребенка с СГВ-инфекцией, наличием бессимптомной стрептококковой бактериурии в данной беременности, а также при отсутствии данных о контаминации СГВ и наличии в родах лихорадки, длительности безводного промежутка 18 ч и более и преждевременных родах [3].
Антибактериальная профилактика в родах не проводится при отрицательном скрининге на СГВ, проведении кесарева сечения в случае отсутствия дородового излития околоплодных вод.
При подозрении на инфицирование новорожденного проводят быстрые тесты на определение стрептококков группы В (микроскопия желудочного секрета и мазки из носоглотки) и культуральное исследование на селективной среде (материалом для посева служит желудочный сок, кровь, спинномозговая жидкость, моча, эндобронхиальный аспират).
В связи с тем, что стрептококковая инфекция у новорожденных рассматривается как одна из основных причин тяжелых перинатальных осложнений, в странах западной Европы и США беременным в обязательном порядке проводят профилактическое лечение при отсутствии лабораторно исключенной стрептококковой инфекции [3].
Проведенное нами исследование позволило выявить, что почти каждая 5-я пациентка, вне зависимости от срока гестации, контаминирована стрептококком группы В и теоретически входит в группу высокого риска по реализации интранатального инфицирования плода.
Внедрение скрининга на СГВ в программу ведения беременности и применение экспресс-тестов в родильном доме позволит снизить частоту передачи возбудителя интранатально и улучшит перинатальные исходы.
Читайте также:


