Системная красная волчанка и эпилептические припадки
Аннотация научной статьи по клинической медицине, автор научной работы — Юсупов Ф. А., Мамасаидов А. Т., Бусарова О. В.
Актуальность Эпилептические припадки (ЭП) частое проявление неишемичес-кого поражения нервной системы (НС) при системной красной волчанке (СКВ) с антифосфолипидным синдромом (АФС). Цель работы: описание симптомов ЭП при СКВ с АФС. Материалы и методы Изучены 22 больных СКВ с АФС. I степень активности была у 14 больных, II степень у 6, III степень у 2. Острое течение было у 2 больных, подострое у 5 и хроническое у 15. Нефрит проявлялся у 4 человек, у 18 он отсутствовал. АНФ был положительным у 18 больных, у 4 отрицательным. Обследование: изучение клинических симптомов, использование инструментальных методов ЭЭГ, ЭхоЭГ, ЭНМГ, ультразвуковая доп-лерография сосудов головного мозга, исследование глазного дна, бульбо-микроскопия и ЯМРТ головного мозга. Результаты ЭП наблюдались у 7 человек. У всех были генерализованные тони-ко-клонические припадки. О связи ЭП с СКВ и АФС говорили отсутствие их до развития болезни и положительный эффект кортикостероидов. Органическая природа ЭП подтверждалась сочетанием их с грубыми неврологическими симптомами, данными ЭЭГ и ЯМРТ. ЭЭГ-картина: диффузные патологические изменения, дезорганизация альфа-ритма и пароксиз-мальная активность, увеличивающаяся при гипервентиляции и физической нагрузке. Основное место локализации патологической активности -височная область (левая у 5, правая у 2). На ЯМРТ у 1 больной очаговых изменений выявить не удалось. У 5 были множественные инфаркты малого или среднего размера, расположенные поверхностно. У 1 больной на ЯМРТ был очаг в медиальном отделе правой затылочной доли с деформацией цистерн, начальными явлениями деформации заднего рога бокового желудочка. Заключение Надо учитывать необходимость профилактики и лечения ЭП при ведении больных СКВ с АФС.
Похожие темы научных работ по клинической медицине , автор научной работы — Юсупов Ф. А., Мамасаидов А. Т., Бусарова О. В.
ВОРОНЕЖ, 24-26 МАЯ, 2006
ЭПИЛЕПТИЧЕСКИЕ ПРИПАДКИ У БОЛЬНЫХ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКОЙ И АНТИФОСФОЛИПИДНЫМ СИНДРОМОМ
Юсупов Ф. А., Мамасаидов А. Т., Бусарова О. В.
Эпилептические припадки (ЭП) - частое проявление неишемического поражения нервной системы (НС) при системной красной волчанке (СКВ) с антифосфолипидным синдромом (АФС), Цель работы: описание симптомов ЭП при СКВ с АФС.
Материалы и методм
Изучены 22 больных СКВ с АФС. I степень активности была у 14 больных, II степень - у 6, III степень - у 2. Острое течение было у 2 больных, подострое - у 5 и хроническое - у 15. Нефрит проявлялся у 4 человек, у 18 он отсутствовал. АНФ был положительным у 18 больных, у 4 - отрицательным. Обследование: изучение клинических симптомов, использование инструментальных методов - ЭЭГ, ЭхоЭГ, ЭНМГ, ультразвуковая доплерография сосудов головного мозга, исследование глазного дна, бульбо-микроскопня и ЯМРТ головного мозга.
ЭП наблюдались у 7 человек. У всех были генерализованные тони-ко-клонические припадки. О связи ЭП с СКВ и АФС говорили отсутствие их до развития болезни и положительный эффект кортикостероидов. Органическая природа ЭП подтверждалась сочетанием их с грубыми неврологическими симптомами, данными ЭЭГ и ЯМРТ. ЭЭГ-картина: диффузные патологические изменения, дезорганизация альфа-ритма и пароксизмальная активность, увеличивающаяся при гипервентиляции и физической нагрузке. Основное место локализации патологической активности -височная область (левая - у 5, правая у 2). На ЯМРТ у 1 больной очаговых изменений выявить не удалось. У 3 были множественные инфаркты малого или среднего размера, расположенные поверхностно. У 1 больной на Я М РТ был очаг в медиальном отделе правой затылочной доли с деформацией цистерн, начальными явлениями деформации заднего рога бокового желудочка.
Надо учитывать необходимость профилактики и лечения ЭП при ведении больных СКВ с АФС.
ЭФФЕКТИВНОСТЬ ПРИМЕНЕНИЯ НИМУЛИДА - СЕЛЕКТИВНОГО ИНГИБИТОРА ЦОГ-2 У БОЛЬНЫХ ОСТЕОАРТРОЗОМ
Якушин С. С, Лыгина Е. В.
Рязанский государственный медицинский универститет
Изучение эффективности и прогипертензивного действия препарата нимулид назначаемого одновременно с иАПФ лизиноприлом у больных остеоартрозом (ОА) и гипертонической болез нью (ГБ).
Машияды и ж толы
В исследование включены 40 женщин (средний возраст 59.7±3,0 года). Коксартроз наблюдался у 30 больных (II стадия у 18, III стадия у 12 больных), гонартроз у 37 (II стадия у 25, III стадия у 11 больных, ГУ стадия у 1 больной), их сочетание у 29 больных. У 21 пациентки имелся генерализованный остеоаргроз. Длительность заболевания колебалась в пределах от 6 месяцев до 30 лет (в среднем 10,5±2,7 лет). ГБ I степени диагностирована у 4 (10%) больных, II степени у 36 (9095) больных. Длительность ГБ составила в среднем 11,1±3,2 лет. В течение 14 дней подбирали терапию лизиноприлом до достижения целевого уровня АД (менее 140 и 90 мм рг.ст.) под контролем суточного мониторирования АД (СМАД). Далее добавляли нимулид в дозе 200 мг/сут. В процессе обследования оценивали по визуальной аналоговой шкале (ВАШ) боль в покое, при движении, стартовую боль, ночную боль; определяли индекс Лекена. Уровень АД оиенива ли по результатам СМАД. Срок наблюдения составил 3 месяца. Средняя дозализиноприпа 13,8± 10,7 мп
По истечении 3-х месячного курса лечения отмечалось боль в покое уменьшилась с 50,0 до 30,6 мм (р Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Аффективные расстройтсва (тревога и депрессия) широко распространены в первичной медицинской сети, в том числе у пациентов ревматологического профиля. Сочетание этих заболеваний имеет реципрокные отношения: каждый утежеляег течение другого. До настоящего момента проблема аффективных расстройств недостаточно изучена.
Мяте вдали н методы
Диагностический критерий МКБ-10, шкалы депресси и тревоги Hamilton.
В группе было 40 женщин (78,4%) и 11 мужчин (21,656) средний возраст 44,4 ± 1,25 лет. Длительность основного заболевания составила в среднем 8,1 ± 0,62 лет. Все больные этой группы (п=51) были пролечены антидепрессантами (селективными ингибиторами обратного захвата серотонина и селективными стимуляторами обратного захвата серотонина) в течение не менее чем 12 недель. В группе контроля уровень депрессии и тревоги оставался без существенных изменений на протяжение 6 месяцев, в то время как на фоне применения антидепрессантов наблюдалось достоверное его снижение. При использовании антидепрессантов у пациентов основной группы такие проявления болезни, как интенсивность боли в баллах и по визуальной аналоговой шкале, продолжительность тугопод-вижности со стороны суставов и позвоночника, а также функциональные возможности пациента (по индексу хронической нетрудоспособности Вадделя) достовено изменяются к концу первого месяца терапии антидепрессантами. При этом достоверное улучшение перечисленных характеристик продолжает нарастать к третьему месяцу и далее - к шестому.
Наряду с положительной динамикой аффективных расстройств на фоне лечения антидепрессантами отмечается четкая положительная динамика клинической симптоматики, характеризующей соматическую болезнь - болезнь опорно-двигательного аппарата.
Рассказывает Евгений Жиляев,
профессор, д.м.н., врач высшей категории.

Это классическая аутоиммунная болезнь, в основе которой лежит наследственный дефект иммунной системы, предположительно касающийся врожденного иммунитета (неспецифической защиты). Для болезни характерно появление разнообразных аутоантител, направленных против собственных белков и клеток организма. Заболевание поражает различные органы и системы: кожу, опорно-двигательный аппарат, внутренние органы, очень часто наблюдаются изменения в крови. Частое осложнение системной красной волчанки - антифосфолипидный синдром, который проявляется образованием тромбов. Для заболевания характерна очень высокая чувствительность к различного рода инфекциям.
Изначально системную красную волчанку ошибочно считали кожным заболеванием. Общепринятое международное название заболевания - Lupus (в пер. с лат. - волк), название обусловлено тем, что проявления на коже похожи на последствия укуса волка. Однако симптомы системной красной волчанки схожи с симптоматикой многих других заболеваний, что вызывает затруднения при постановке диагноза. Например, туберкулез кожи и саркоидоз имеют схожую симптоматику.
Доказано, что восполнение недостатка витамина D в некоторых случаях позволяет снизить риск развития волчанки у пациентов с отягощенной наследственностью и выявленными характерными аутоантителами.
Симптомы системной красной волчанки
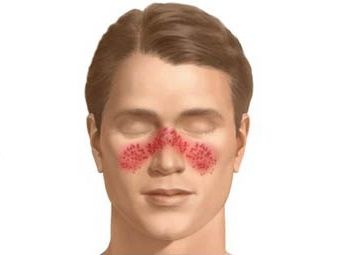
В связи с тем, что заболевание поражает все органы и системы, его проявления могут быть очень разнообразны. Наиболее характерны высыпания на лице в форме бабочки. При появлении такого рода изменений рекомендуется незамедлительно обратиться к врачу.
Другие возможные симптомы системной красной волчанки:
- длительное повышение температуры,
- непереносимость солнечного света, - выраженная слабость или повышение температуры после пребывания на солнце,
- боли в мышцах,
- увеличение лимфатических узлов – лимфаденопатия.
При волчанке могут появляться боли в суставах, может развиться артрит. Возможны изменения в клеточном составе крови. Часто к ревматологу пациентов направляет гематолог после выявления анемии, панцитопении или тромбоцитопении.
Одни из наиболее серьезных проявлений системной красной волчанки - нефрит, поражение почек, изменения в анализах мочи. Даже боли в груди могут оказаться проявлением волчанки. Эпилептические припадки также могут быть одним из первых проявлений системной волчанки.
Диагностика системной красной волчанки
Основные методы – клинический осмотр и лабораторная диагностика. Дополнительно используются инструментальные методы: компьютерная томография, в частности, позволяет подтвердить наличие плеврита, эхокардиография – перикардита или эндокардита, магнитно-резонансная томография часто используется для уточнения характера поражения головного и спинного мозга у пациентов с волчанкой.
Лабораторная диагностика незаменима при выявлении системной красной волчанки. Для подтверждения диагноза проводится целый ряд исследований на аутоантитела. Их проведение имеет критически важное значение. Активность волчанки также во многом измеряется благодаря лабораторным исследованиям.
Лабораторно оцениваются обычно: антинуклеарный фактор, антитела к двухспиральной ДНК, антитела к антигенам SS-A. Выявляется также целый ряд других аутоантител, которые специфичны для волчанки.
Лечение системной красной волчанки
Современные протоколы лечения системной красной волчанки претерпели значительные изменения. До настоящего времени считалось, что основа лечения волчанки - это гормоны. На сегодняшний день основа лечения волчанки - витамин D и гидроксихлорохин. Противовоспалительные (глюкококортикоидные) гормоны приходится использовать в большинстве случаев активной волчанки, но они требуются далеко не всем пациентам и во многих случаях могут быть отменены при достижении устойчивой ремиссии.
При поражении почек и центральной нервной системы используются иммуносупрессоры (препараты, угнетающие иммунитет) и цитостатические препараты (препараты, которые нарушают процессы роста, развития и деления всех клеток организма, тем самым вызывая их гибель). При волчаночном нефрите нередко применяется препарат азатиоприн (иммуносупрессор). В случаях, когда болезнь протекает с повышенным тромбообразованием, используются антикоагулянты (препараты, препятствующие образованию тромбов).
Для лечения системной красной волчанки в отдельных случаях используются генно-инженерные препараты.
Благодаря современным технологиям появилась возможность достигать многолетней ремиссии, в разы повысилась эффективность лечения волчанки.
Преимущества Европейского медицинского центра в лечении системной красной волчанки
- Мультидисциплинарный подход к ведению пациентов: в лечении участвуют врачи различных специальностей (ревматологи, нефрологи, терапевты, врачи лучевой диагностики и др.).
- Все ревматологи ЕМС обладают значительным опытом диагностики и лечения пациентов с волчанкой и используют протоколы, эффективность которых доказана многочисленными исследованиями. В команде ревматологов ЕМС – профессор Евгений Валерьевич Жиляев.
- Круглосуточная экстренная и неотложная помощь, полный спектр необходимых диагностических обследований.
- Результаты исследований доступны пациентам в кратчайшие сроки.

Крайне негативное впечатление от консультации доктора Табеевой, когда предлагают коллоидный узел щитовидной железы исследовать при помощи биопсии, даже если он растет. Квалификация доктора более чем достаточная, чтобы знать, что биопсии подлежат узлы TIRADS 3-5, но не TIRADS 2 (такую классификацию мне дали в Августе в Испании). Я не ( подробнее )
Крайне негативное впечатление от консультации доктора Табеевой, когда предлагают коллоидный узел щитовидной железы исследовать при помощи биопсии, даже если он растет. Квалификация доктора более чем достаточная, чтобы знать, что биопсии подлежат узлы TIRADS 3-5, но не TIRADS 2 (такую классификацию мне дали в Августе в Испании). Я не против, чтобы за счет страховой или за свои деньги для более широкого исследования сдать анализы, сделать УЗИ, КТ и тд, но предлагать сделать травмирующую биопсию это уже слишком.
 |



