Серологические маркеры инфекций расшифровка токсоплазмоз
Токсоплазмоз — широко распространенное инфекционное заболевание человека и животных, характеризующееся длительным хроническим течением, полиморфностью клинической картины (от бессимптомного носительства до летальных форм болезни) и возможностью внутриутробного инфицирования плода.
Возбудитель токсоплазмоза — Toxoplasma gondii — внутриклеточный паразит, размером 4—7 мкм. Если взглянуть на этот живой организм под микроскопом, он напоминает дольку апельсина (рис.1).
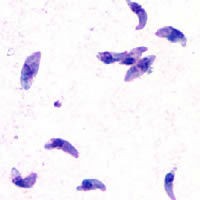
Рис. 1 Toxoplasma gondii –окрашенный препарат по Романовского-Гимзе
Можно ли заразиться токсоплазмозом от домашних животных? Да, ведь токсоплазмозом болеют около 60 видов птиц и 300 видов млекопитающих (одомашненных и диких), которые с фекалиями попадают во внешнюю среду выделяют цисты и приводят к заражению других организмов.
Но имея сложный путь развития (половой и бесполый) и тот факт, что половой процесс происходит только лишь в кишечнике животных семейства кошачьих, с образованием устойчивых форм (цист), которые долгое время сохраняются во внешней среде (до 2 лет), не боятся действия низких и высоких температур, высушивания. Бесполое размножение не приводит к образованию стойких форм паразита.
Источником инфекции выступают больные животные, которые выделяют паразитов со слюной, молоком, мочой, фекалиями. Люди лишь промежуточные хозяева этого простейшего.
Заражение возбудителем токсоплазмоза происходит:
- при употреблении в пищу сырого или плохо прожаренного мяса;
- при контакте с сырым или недостаточно термически обработанным мясом слизистой оболочки полости рта (многие хозяйки пробуют сырой фарш);
- при уходе за зараженными животными, например, уборка кошачьего туалета;
- при употреблении в пищу немытых овощей, фруктов, зелени, на которых могут быть цисты паразита;
- при пересадке внутренних органов или переливание крови.
В подавляющем большинстве случаев при токсоплазмозе наблюдается бессимптомное носительство паразита, сопровождающееся наличием специфических антител в крови. Инфицированность населения колеблется от 10 до 90%.
Клинические симптомы токсоплазмоза у человека отличаются разнообразием. Выделяют врожденный и приобретенный токсоплазмоз.
Врожденный токсоплазмоз протекает тяжелее всего. При заражении на ранних сроках беременности происходит внутриутробная гибель плода, так как у него формируются уродства, которые несовместимы с жизнью. Если инфицирование наступает во второй половине беременности, ребенок рождается с генерализованным поражением всех органов и систем. Для него характерны повышение температуры тела, желтушность кожи, слабость, низкий тонус мышц, увеличение печени, лимфатических узлов, селезенки, кожная сыпь, патологии нервной системы (энцефаломиелит). Также возможно развитие косоглазия, слепоты, нарушение формирования головного или спинного мозга.
Токсоплазмоз входит в группу TORCH- инфекций, считающихся потенциально опасными для внутриутробного развития плода. Только первичное заражение женщины во время беременности может привести к инфицированию плода. Таким образом, практически важным является вопрос о моменте инфицирования беременной: задолго до, непосредственно перед, либо во время беременности.
При попадании токсоплазм в организм человека через 7—14 дней начинается первичный гуморальный иммунный ответ — продуцируются специфические IgM. Максимальный уровень их концентрации достигается к 20— 30-му дню от момента инфицирования. Полное их исчезновение в большинстве случаев (около 70%) происходит в течение 3—4 месяцев, однако, возможно присутствие специфических IgM и более длительное время — до 1 года и более (около 10% случаев). Следовательно, присутствие в крови специфических IgM предполагает, но не доказывает свежее инфицирование, поскольку они могут находиться в крови от 3 мес. до 1,5 лет. Дифференцировать первичную инфекцию от паст-инфекции помогает комплексный подход к диагностике — это сопоставление данных всего спектра серологических маркеров инфекции, а именно:
- результатов выявления специфических IgM, IgA;
- определения индекса авидности IgG и концентрации IgG в динамике.
Анализ серологического профиля пациента позволяет определить вероятный срок инфицирования T.gondii.
В случае отрицательного результата беременные относятся к группе риска по инфицированию Toxoplasma gondii во время беременности и каждые 1—2 месяца должны обследоваться на токсоплазмоз. В случае положительного результата иммуноферментного анализа на поздние специфические антитела IgG у беременных важно определить срок инфицирования.
Приобретенный токсоплазмоз у человека чаще всего имеет латентное течение. Инкубационный период длится от 5 до 23 дней. Больные жалуются на высокую температуру тела, озноб, слабость, головные боли, болезненные ощущения в суставах и мышцах, увеличение печени, селезенки, шейных лимфатических узлов. Возможно развитие пневмонии, энцефалита, эндокардита, поражения глаз.
Течение хронического токсоплазмоза бессимптомное или характеризуется незначительными клиническими проявлениями на протяжении многих лет. Наиболее распространенные симптомы этой формы болезни:
- повышение температуры до субфебрильных цифр;
- слабость, которая возникает даже после сна, ухудшение памяти, апатия к окружающему миру, раздражительность;
- тупые головные боли;
- болезненные ощущения в мышцах и суставах, затруднение передвижения;
- увеличение в размерах селезенки, печени и лимфатических узлов;
- при поражении желудочно-кишечного тракта: тупые боли в животе, сухость во рту, снижение аппетита, метеоризм;
- патологии сердечно - сосудистой системы, которые сопровождаются снижением артериального давления, давящими болями в сердце и изменениями его ритма;
- нарушения эндокринной системы: болезни поджелудочной железы, сбои менструального цикла, импотенция;
- расстройства зрения, близорукость.
В то же время возможны и клинически выраженные варианты течения первичной инфекции (как правило, возникающие у лиц с нарушением иммунитета) с развитием энцефалита, миокардита, миозита, увеита, формированием хронической инфекции.
Весьма актуальна проблема генерализации латентного токсоплазмоза у ВИЧ-инфицированных с развитием тяжелого некротического энцефалита с большой вероятностью летального исхода.
Среди возможных осложнений токсоплазмоза выделяют: инфекционно-токсический шок, поражения центральной нервной системы (энцефалит, арахноидит, отек мозга, эпилептиформный синдром, параличи, парезы, отставание детей в развитии), болезни глаз (атрофия зрительного нерва), патологии сердца (эндокардит), недуги дыхательных органов (пневмония).
Так как клинические симптомы недуга очень разнообразны, диагностика токсоплазмоза на основании жалоб больного невозможна. Следует обязательно собрать эпидемиологический анамнез, выяснить, употреблял ли больной сырое иди недостаточно прожаренное мясо, контактировал ли с больными животными (в особенности кошками).
В лабораторной диагностике токсоплазмоза широко используются иммунологические методы, которые выявляют антитела к токсоплазмозу. Наиболее распространенным среди них является иммуноферментный анализ. Для его проведения у человека берут кровь на токсоплазмоз. Также можно применять и другие биологические жидкости. На основании выявления антител двух разных классов данное исследование позволяет судить о давности заражения, так как иммуноглобулины класса M появляются сразу после инфицирования и в течение года после него, а иммуноглобулины класса G сохраняются в крови на всю последующую жизнь.
Можно ли вылечить токсоплазмоз? У здоровых людей болезнь заканчивается полным выздоровлением с формированием иммунитета на всю дальнейшую жизнь и не имеет каких-либо последствий. Тяжелые поражения разных органов и систем при токсоплазмозе развиваются у людей с дефектами иммунитета, например, ВИЧ-инфицированных. Последствия токсоплазмоза особенно тяжелые при врожденной форме болезни. Она приводит к внутриутробной гибели плода или наличию у него выраженных патологий.
Профилактика токсоплазмоза также включает следующие мероприятия:
- тщательное мытье фруктов, овощей и зелени;
- употребление в пищу достаточно термически обработанных мясных блюд;
- мытье рук после земельных работ и ухода за животными;
- в период беременности следует избегать контакта с кошками;
- уничтожение мух, тараканов и грызунов, которые могут переносить цисты паразитов.
С целью предупреждения врожденного токсоплазмоза необходимо проводить обследование с определением уровня антител в крови всем женщинам, которые планируют беременность.

Иммуноферментный анализ (ИФА) — метод лабораторной диагностики, позволяющий обнаруживать специфические антитела и антигены при самых разных патологиях.
ИФА — один из самых распространенных и точных методов для выявления инфекций, передающихся половым путем, в частности ВИЧ, ВПЧ, гепатита В.

Для того чтобы результаты анализов были максимально достоверными, необходимо правильно подготовиться к их сдаче.

Спецпредложения, скидки и акции помогут существенно сэкономить на медицинском обследовании.
Контроль качества лабораторных исследований, осуществляемый по международным стандартам, — дополнительная гарантия точности результатов анализов.
Современная диагностика в медицине немыслима без высокочувствительных лабораторных анализов. Прежде для установления причин тех или иных симптомов врачи были вынуждены ориентироваться на косвенные признаки болезни, а также проводить многоступенчатые микроскопические исследования в попытке обнаружить возбудителя инфекции. Сегодня достаточно одного-единственного теста — такого как иммуноферментный анализ — чтобы подтвердить или опровергнуть первоначальный диагноз.
Основные понятия и принцип метода иммуноферментного анализа
Существует несколько разновидностей антител, каждая из которых вступает в действие на определенном этапе иммунного ответа. Так, первыми в ответ на проникновение антигена в организм синтезируются иммуноглобулины класса М (IgM). Содержание этих антител наиболее высоко в первые дни инфекционного процесса.
Следом за ними иммунная система выбрасывает в кровь иммуноглобулины класса G (IgG), которые помогают уничтожать антигены до полной победы над инфекцией, а также продолжают циркулировать по сосудам в дальнейшем, обеспечивая иммунитет к повторному заражению. На этом явлении основана вакцинация: благодаря прививкам, содержащим ослабленные антигены микробов и вирусов, в нашей крови появляется большое количество IgG, которые при контакте с реальной угрозой быстро подавляют инфекцию — до того, как она нанесет вред здоровью.
Как узнать, какие именно антигены или антитела присутствуют в организме человека? Когда врач предполагает, что причиной заболевания является определенная инфекция, или желает измерить концентрацию определенного гормона, он назначает пациенту иммуноферментный анализ.
ИФА бывает качественным и количественным. В первом случае подразумевается однозначный ответ: искомое вещество или найдено, или не найдено в образце. В случае с количественным анализом более сложная цепь реакций дает возможность оценить концентрацию антител в крови человека, что в сравнении с результатами предыдущих тестов даст ответ на вопрос о том, как развивается инфекционный процесс.
Бесспорные преимущества ИФА — высокая чувствительность и специфичность метода. Чувствительность — это возможность распознать искомое вещество, даже если его концентрация в образце невысока. Специфичность же подразумевает безошибочность диагностики: если результат положительный, значит, найдены именно те антитело или антиген, которые предполагались, а не какие-то другие.
Высокая степень технологичности проведения иммуноферментного анализа минимизирует влияние человеческого фактора, что снижает вероятность ошибки. Большинство используемых в современных лабораториях тест-систем и реактивов для ИФА выпускаются в промышленных условиях, что гарантирует точный результат.
В случае диагностики инфекционных заболеваний иммуноферментный анализ не может найти возбудителя и определить его специфичные свойства: он лишь указывает на наличие антител в крови у больного, косвенно свидетельствующих о присутствии чужеродного микроорганизма в теле человека.
ИФА — крайне точный, но не дешевый метод, поэтому обращаться к нему нужно с умом, а интерпретацией результатов должен заниматься квалифицированный врач.
Невозможно охватить полный список показаний к проведению ИФА. Вот наиболее распространенные цели анализа:
- Диагностика острых и хронических инфекционных заболеваний:
- IgM и IgG к вирусным гепатитам А, B, C, E, а также антигенов гепатитов В и С;
- IgG к ВИЧ;
- Ig M и IgG к цитомегаловирусной инфекции;
- Ig M и IgG к вирусу Эпштейна-Барр;
- Ig M и IgG к герпетическим инфекциям;
- Ig M и IgG к токсоплазмозу;
- Ig M и IgG к кори, краснухе, сальмонеллезу, дизентерии, клещевому энцефалиту и другим заболеваниям;
- IgG к паразитарным заболеваниям;
- Ig M и IgG к инфекциям, передающимся половым путем;
- IgG к хеликобактерной инфекции.
- Общая оценка показателей иммунитета человека и маркёров некоторых аутоиммунных заболеваний.
- Выявление онкологических маркёров (фактора некроза опухоли, простатспецифического антигена, раково-эмбрионального антигена и других).
- Определение содержания гормонов в сыворотке крови (прогестерона, пролактина, тестостерона, тиреотропного гормона и других).
Основной биоматериал для проведения ИФА — это сыворотка крови: в лаборатории у пациента берут образец крови из вены, из которого в дальнейшем удаляют форменные элементы, затрудняющие проведение анализа. В некоторых других случаях для анализа используется спинномозговая жидкость, околоплодные воды, мазки слизистых оболочек и т.д.
Для того чтобы избежать искажений в результатах, рекомендуется сдавать кровь натощак, а за две недели до исследования (если целью является диагностика хронических, скрыто протекающих инфекционных заболеваний) необходимо отказаться от приема антибиотиков и противовирусных препаратов.
При наличии необходимых реактивов и хорошей организации работы лаборатории результат анализа вы получите в течение 1–2 суток после забора крови. В некоторых случаях, при необходимости получения экстренного ответа, этот срок может быть сокращен до 2–3 часов.
- IgM — наличие этого класса иммуноглобулинов говорит об остром инфекционном процессе в организме. Отсутствие IgM может говорить как об отсутствии конкретного возбудителя в организме, так и о переходе инфекции в хроническую стадию.
- IgA при отрицательном результате теста на IgM чаще всего свидетельствует о хронической или скрыто протекающей инфекции.
- IgM и IgA (совместное присутствие) — два положительных результата говорят о разгаре острой фазы заболевания.
- IgG говорит либо о хронизации заболевания либо о выздоровлении и выработке иммунитета к инфекционному агенту.
В зависимости от содержания анализа в бланке могут быть представлены данные в виде таблицы с перечислением всех антител или антигенов с пометками об отрицательной или положительной реакции, либо будет указано количественное значение результата (отрицательный, слабоположительный, положительный или резко положительный). Последний вариант определяет, сколько антител содержится в анализируемом образце.
Еще один количественный показатель — индекс авидности антител, выраженный в процентах. Он указывает, сколько времени прошло от начала инфекционного процесса (чем выше индекс — тем больше).
Сегодня выпускаются тысячи видов тест-систем ИФА, позволяющих обнаруживать специфические антитела и антигены при самых разных патологиях. Поэтому этот анализ используется практически во всех медицинских отраслях. Диагноз, поставленный с помощью ИФА, — это гарантия назначения адекватной терапии и эффективного лечения заболевания.
Информативность ИФА делает этот анализ важным инструментом в работе многих медицинских центров. Но можно ли доверять такую диагностику государственным лабораториям или лучше самим выбрать, где провести такое исследование?
1. Этиологический фактор: Toxoplasma gondii — облигатный внутриклеточный паразит со сложным жизненным циклом. Три основные формы развития: тахизоит, тканевая циста, ооцист. Половое развитие паразита в клетках эпителия слизистой оболочки тонкого кишечника окончательного хозяина — домашнего кота и других кошачьих; бесполое развитие в тканях промежуточных хозяев — млекопитающих (в том числе человека) и некоторых видов птиц. У зараженного человека с нормальным иммунитетом формируются тканевые цисты (в основном в мышцах и головном мозге), содержащие живые, медленно делящиеся формы простейшего, сохраняющиеся в организме человека в течение всей жизни.
2. Резервуар и пути заражения: резервуар — кошки и другие кошачьи; заражение человека происходит через:
1) пищевые продукты (овощи, фрукты), воду и руки, загрязненные ооцистами, выделяемыми с калом кота;
2) употребление сырого или не до конца приготовленного мяса зараженных животных, содержащего цисты простейшего (чаще всего свиного и бараньего);
3) передача тахизоитов от матери плоду через плаценту во время паразитемии (вертикальное заражение, только во время первичного заражения);
4) случайный контакт с тахизоитами (редко переливание крови или продуктов крови — в основном лейкоцитарного концентрата, трансплантация органов, лабораторное заражение).
После перенесенного токсоплазмоза, в период иммуносупрессии возможна реактивация инфекции в результате разрыва тканевых цист и превращения спящих в них форм в инвазивные тахизоиты (эндогенная инвазия).
3. Эпидемиология: один из наиболее распространенных паразитозов и зоонозов, является эндемичным во всем мире. Из-за серьезных последствий инфекции для плода особой группой риска являются серонегативные беременные женщины.
4. Инкубационный и заразный период: инкубационный период приобретенной формы от 2 недель до 2 месяцев (ср. 4 недели). Паразитемия длится 1–3 недели. Риск заражения плода составляет 17–25 % в I триместре беременности, 25–54 % во II триместре и 60–90 % в III триместре. Больной не опасен для контактирующих с ним людей.
КЛИНИЧЕСКАЯ КАРТИНА И ЕСТЕСТВЕННОЕ ТЕЧЕНИЕ наверх
Клиническое течение зависит от вида инвазивной формы простейшего, источника заражения, патогенности штамма, эффективности иммунной системы, а также интенсивности инвазии. У иммунокомпетентных лиц обычно бессимптомное или малосимптомное (85 % случаев).
1. Узловая форма: наиболее частая у иммунокомпетентных лиц; преобладает увеличение лимфатических узлов, чаще всего шейных вдоль заднего края грудино-ключично-сосцевидной мышцы, заднешейных и затылочных (реже генерализованная лимфаденопатия); диаметр до 3 см, болезненные в острой фазе инвазии, потом безболезненные, не гноятся. Иногда гриппоподобные симптомы. В 1/3 симптоматических случаев клиническая картина напоминает мононуклеоз →разд. 18.1.9.
2. Глазная форма: прогрессирующее воспаление сетчатки и сосудистой оболочки с различной динамикой; чаще у лиц в состоянии иммуносупрессии.
3. Генерализованная форма: очень редко у иммунокомпетентных лиц, чаще всего диагностирована у пациентов в состоянии иммуносупрессии; симптомы со стороны одного или нескольких внутренних органов (воспаление сердечной мышцы, легких, плевры, печени с ее увеличением, спленомегалия, анемия, геморрагический диатез) и/или ЦНС (энцефалит, менингит, миелит, полиневрит).
4. Врожденный токсоплазмоз: заражение плода в результате паразитемии T. gondii у беременной женщины или незадолго до зачатия. Протекает следующим образом: самопроизвольный выкидыш, внутриутробная смерть плода, симптоматическое заражение плода и новорожденного (генерализованная форма с очень серьезными последствиями для развития), генерализованная или органная форма, развивающаяся в первых месяцах жизни младенца, отсроченная реактивация инфекции в подростковом периоде или у молодых людей, малосимптомная форма или бессимптомная. Наиболее серьезные последствия для плода вызывает заражение в I (выкидыш, смерть плода, тяжелые неврологические расстройства) и во II (тяжелое воспаление ЦНС с серьезными неврологическими расстройствами) триместре беременности. При отсутствии лечения (также при бессимптомной инфекции) проявляется тенденция к множественной реактивации, чаще всего во второй и третьей декаде жизни (обычно глазная форма).
Дополнительные методы исследования
1. Идентификация этиологического фактора: основной метод диагностики инфекции:
1) серологические исследования — определение специфических антител в сыворотке у иммунокомпетентных пациентов:
а) IgM — появляются через 1 неделю после инвазии, достигают максимальной концентрации через 1 месяц и обычно исчезают через 6–9 месяцев, могут сохраняться в течение многих месяцев или лет от момента заражения;
б) IgA — свидетельствуют о недавнем заражении, исчезают раньше, чем IgM (исследование более труднодоступно, особенно информативно при диагностике заражения у беременных женщин и при врожденной форме);
в) IgG — максимальная концентрация 2‑3 месяца от заражения, сохраняются на протяжении всей жизни. Если необходимо определить время заражения (напр. у беременных женщин), определяется так называемая авидность (сила связывания с антигеном) антител IgG (антитела с низкой авидностью → острая фаза токсоплазмоза; антитела с высокой авидностью → инвазия ≥20 недель назад);
2) идентификация паразита — у пациентов в состоянии иммуносупрессии, у плода, а также у иммунологически незрелых новорожденных и младенцев (материал: кровь, спинномозговая жидкость, околоплодные воды, бронхоальвеолярный смыв, внутриглазная жидкость или участок ткани, или пораженного органа): выделение паразита (выращивание и микроскопическое исследование), обнаружение его антигенов или генетического материала (ПЦР).
2. Другие исследования: при каждом случае токсоплазмоза обязательно обследование глазного дна, а при подозрении на поражение ЦНС также визуализирующие исследования головного мозга (КТ, МРТ) — характерные нерегулярные очаговые изменения.
Приобретенный токсоплазмоз (также у беременных женщин):
1) сероконверсия специфических антител IgG, или
2) значительное увеличение уровня специфических антител IgG (≥2 раза) в промежутке ≥4 недель, или
3) клинические симптомы токсоплазмоза и обнаружение специфических антител IgA/IgM в сыворотке крови и высокий уровень специфических антител IgG с низкой ( 1. Острая фаза приобретенного токсоплазмоза: в случае тяжелых системных симптомов или со стороны пораженных органов комбинированное лечение пириметамином и сульфадиазином в течение 3 недель. Во время лечения пириметамином показано назначение фолиевой кислоты для профилактики торможения функции костного мозга. В случае непереносимости сульфадиазина, особенно у пациентов, инфицированных вирусом ВИЧ → клиндамицин в сочетании с пириметамином и фолиевой кислотой (лечение следует проводить в специализированном учреждении).
2. Глазной токсоплазмоз: лечение, как и при острой форме, в течение 6–8 нед. в специализированном учреждении и под пристальным наблюдением офтальмолога. Дополнительное лечение: местно противовоспалительные препараты и капли с ГКС в конъюнктивальный мешок. Применение общей криотерапии дискутабельно, поскольку повышает риск токсоплазматического воспаления целого глазного яблока.
3. У пациентов в состоянии глубокой иммуносупрессии, с маркерами заражения T. gondii : в случае симптоматической реактивации инфекции лечение такое же, как в 1 пункте, затем многолетнее профилактическое применение противопаразитарных препаратов пролонгированного действия (напр. ко-тримоксазол, пириметамин с сульфадоксином) или азитромицин. Дозировку следует установить в специализированном учреждении. Действия в случае зараженных ВИЧ →разд. 18.2.
4. Первичное заражение у беременных женщин: с целью профилактики врожденного токсоплазмоза → спирамицин п/о 3 млн МЕ каждые 8 ч до подтверждения инвазии у плода или до родов. В моменте подтверждения инвазии у плода → пириметамин с сульфадиазином и фолиевой кислотой до окончания беременности. При первичном инфицировании T . gondii во 2-ой половине беременности рекомендуется пропустить фармакологическую профилактику спиромицином и сразу применить лечение матери и плода пириметином и сульфадиазином с одновременным добавлением фолиевой кислоты. Лечение следует проводить в специализированном учреждении.
Регулярный контроль морфологии периферической крови во время проведения лечения из-за значительного риска лейкопении и тромбоцитопении. Периодическое обследование глазного дна в случае ухудшения остроты зрения.
1. Врожденный токсоплазмоз: задержка психомоторного развития, гидроцефалия (повышение внутричерепного давления), эпилепсия, катаракта, отслойка сетчатки.
2. Глазной токсоплазмоз: воспаление глазного яблока, устойчивые дефекты поля зрения, снижение зрения, слепота.
3. Токсоплазмоз у пациентов с иммунодефицитом: полиорганная недостаточность, отторжение трансплантата, неврологические расстройства.
Благоприятный в случаях приобретенного токсоплазмоза у пациентов с нормальным функционированием иммунной системы, неопределенный у пациентов с иммунодефицитом, а также у детей с врожденной формой инфекции. Общая смертность в случаях врожденного токсоплазмоза достигает 10 %.
1. Соблюдение основных правил гигиены и питания:
1) избегание употребления и дегустации сырого или полусырого мяса и колбасных изделий, сырого молока, тщательное мытье рук и кухонных приборов после контакта с этими продуктами;
2) тщательное мытье фруктов и овощей перед употреблением;
3) использование защитных перчаток (резиновых или латексных) для работы в саду и в поле;
4) ежедневная уборка кошачьих туалетов с песком и тщательное мытье рук после контакта с кошками или предметами, загрязненными их фекалиями (если это возможно, эти мероприятия не должна выполнять беременная женщина).
2. Скрининговое серологическое обследование: показано у женщин перед планирующейся беременностью, а также периодически у серонегативных беременных женщин (мониторинг сероконверсии с целью начала фармакологической профилактики врожденного токсоплазмоза → Лечение).
3. Обязанность сообщения в органы исполнительной власти региона в сфере здравоохранения и управления Роспотребнадзора по субъекту Федерации касается всех случаев врожденного токсоплазмоза (бессимптомных и симптомных).
ПОЛУЧЕНИЕ РЕЗУЛЬТАТОВ
АНАЛИЗОВ ОНЛАЙН
Теперь вы можете получить результаты
анализов не выходя из дома на нашем сайте!
Доступно каждому!
Подарочные сертификаты
Новости, статьи, полезная информация
Расширение возможностей в лечении и профилактике инфекционных заболеваний нуждается в быстрой и точной диагностике. Ранняя диагностика первых случаев эпидемических инфекций позволяет своевременно провести противоэпидемические (профилактические) мероприятия. Установление первичного инфицирования возбудителями внутриутробных инфекций играет существенную роль в предотвращении врожденных патологий.
Традиционные иммунодиагностические методы, используемые для серологической диагностики острой фазы вирусных, бактериальных и паразитарных инфекций, имеют ряд ограничений. Часто невозможно провести четкую дифференциацию между первичной инфекцией, реинфекцией или обострением инфекционного процесса, особенно при серодиагностике инфекций с нетипичной динамикой антителообразования, когда наличие иммуноглобулинов класса М (IgM) не является достоверным и достаточным признаком для дифференциации стадий заболевания.
Определение IgM, как показателя первичной инфекции, в ряде случаев утратило свое значение, так как было доказано, что их можно выявить в сыворотке периферической крови спустя месяцы или даже годы после наступления сероконверсии (так называемые хронические IgM). Кроме того, выявление IgM может дать ложнопозитивные результаты. Например, вследствие вторичной инфекции (экзогенная реинфекция или эндогенная реактивация инфекции). Было показано, что специфические IgA также могут присутствовать в сыворотке периферической крови через 2-3,5 года с момента зарегистрированной сероконверсии.
Серологическая диагностика, основанная на определении титра специфических иммуноглобулинов класса G (IgG) может быть полезной при дифференциации активного периода болезни от перенесенной в прошлом и уже неактивной инфекции. Однако этот метод имеет ряд ограничений: не позволяет дифференцировать первичную и реинфекцию; у пациентов с реактивацией хронического процесса не всегда наблюдается достоверный рост уровня IgG; метод экономически невыгоден.
Для того, чтобы установить точный момент инфицирования и разграничивать первичную, реинфекцию или реактивацию инфекционного процесса, был предложен тест на определение авидности IgG антител.
Различают два понятия: аффинность антител (или аффинитет) и авидность (или авидитет).
Аффинность — это степень специфического сродства активного центра к антигенной детерминанте. Авидностью антител или функциональной аффиностью называется прочность связи между антителом и антигеном. Величина авидности зависит от аффиности специфических антител (выше аффиность — выше авидность) и количества связывающих центров. Первичный иммунный ответ на ранее не встречаемые организмом антигены начинается с продукции иммуноглобулинов класса М. Специфические IgG появляются позже. При первичном иммунном ответе они сменяют ранние антитела IgM и накапливаются в организме в больших количествах.
Под воздействием антигена происходит процесс отбора и стимуляции В-клеток, что приводит к увеличению аффинности IgG антител, низкой после первого контакта с антигеном и возрастающей в течение последующих недель или месяцев (от 1 до 7).
Уровень авидности пропорционален дозе и природе антигена, а также индивидуальному уровню соматических мутаций. Низкие дозы антигена приводят к более быстрому возрастанию авидности, а высокие дозы — к более медленному. Таким образом, низкоавидные антитела продуцируются в течение первой стадии инфекции, когда содержание антигенов обычно высокое.
С возрастом эффективность селекции специфических антител падает, а следовательно процесс созревания антител замедляется, этим объясняется меньшая устойчивость к инфекциям лиц старше 60-65 лет и неэффективность вакцинации в этом возрасте. Выявление в испытуемой сыворотке антител с индексом авидности ниже 15-50% (у разных производителей и разных возбудителей этот показатель разный и указывается в бланке исследования) указывает на свежую первичную инфекцию. Показатель авидности. равный или превышающий 50%, свидетельствует о наличии в сыворотке высокоавидных антител — маркеров перенесенной в прошлом инфекции или персистирующей инфекции. Показатель авидности антител в интервале 31-49% может свидетельствовать о поздней стадии первичной инфекции или недавно перенесенной инфекции только при условии выявления антител в высокой концентрации. Интерпретацию результатов определения индекса авидности необходимо проводить в соответствии с рекомендациями фирмы — производителя, так как величина ИА для одной и той же стадии заболевания может колебаться в широких пределах.
Если в исследуемой сыворотке крови при наличии или отсутствии IgM обнаруживаются IgG с низкой авидностью, то это свидетельствует о первичной (недавней) инфекции. Наличие же высокоавидных антител IgG говорит о вторичном иммунном ответе в случае попадания возбудителя в организм или обострения (реактивации).
КЛИНИЧЕСКОЕ ЗНАЧЕНИЕ ОПРЕДЕЛЕНИЯ НИЗКОАВИДНЫХ АНТИТЕЛ
Применение метода определения авидности антител представляет интерес при диагностике инфекций.
Краснуха обладает бесспорным тератогенным действием, т.е. приводит к формированию пороков развития эмбриона и плода. У беременных краснуха может протекать тяжело, легко и бессимптомно. Внутриутробное заражение плода возможно при любой форме краснушной инфекции. Распознавание инфекции, особенно в период вспышек, больших затруднений не вызывает.
Однако для точной диагностики необходимо выделение вируса, которое технически не всегда выполнимо. Лабораторная диагностика обычно заключается в определении IgG и IgM антител, в основном у беременных, так как риск рождения неполноценного или мертвого ребенка у инфицированной матери очень высок и обычно рекомендуется прерывание беременности. Однако диагностика, основанная на определении антител, может давать ложноположительные и ложноотрицательные результаты. Так, при повторной инфекции у вакцинированных, которая может произойти в случаях низкого иммунного ответа при вакцинации, или может быть вызвана мутантными штаммами вируса, IgM антитела не образуются, возрастание титров IgG антител также наблюдается не всегда. У новорожденных с первичной инфекцией вследствие внутриутробного инфицирования, IgM антитела могут не синтезироваться в силу ряда причин:
незрелость иммунной системы; блокирование вирусного антигена материнскими антителами; инфицирование на поздних стадиях беременности; иммунная толерантность. Если происходит стимуляция клонов лимфоцитов вируса краснухи, может возникать ложноположительный антительный ответ, особенно для антител класса IgM. Было показано, что IgM антитела могут персистировать в течение года или возникать в случаях реинфекции, особенно у иммунодепрессивных пациентов. Кроме того, могут возникать ложноположительные результаты вследствие наличия ревматоидного фактора или подобных соединений, даже в ловушечном варианте теста. Только определение низкоавидных антител может быть диагностическим маркером первичной инфекции вирусом краснухи, что особенно важно при диагностическом обследовании беременных, когда необходимо дифференцировать первичную инфекцию от вторичной или реактивации инфекции.
Токсоплазмоз. Известно, что проявление клинических симптомов при приобретенном токсоплазмозе имеет низкое диагностическое значение для точного определения длительности инфекционного процесса.
Увеличение лимфоузлов может возникать в разное время с момента первичной инфекции, а нередко может сохраняться длительное время или даже возобновляться в более поздний период болезни, независимо от применения специфического противопаразитарного лечения.
До настоящего времени единственными доступными серологическими тестами для определения острой фазы токсоплазмоза являлись определение IgM антител и определение IgG антител в возрастающих титрах в двух или трех образцах сывороток, что, однако, приводит к задержке постановки диагноза. Кроме того, у пациентов с реактивацией хронического токсоплазмоза значительный рост уровня антител IgG отмечается не всегда, особенно это касается детей и подростков с поражением глаз при врожденном токсоплазмозе.
Интерпретация результатов исследований других иммуноглобулинов также вызывает затруднения. Основной недостаток определения IgM антител — длительная персистенция в крови, в связи с чем возникают трудности в установлении окончания острой фазы заболевания. У 40% пациентов IgM антитела выявляются в течение года с момента заражения при использовании ИФА, у 60% — при использовании высокочувствительного метода иммуноадсорбции. Также как IgM, специфические IgA присутствовали в сыворотке периферической крови через 45 месяцев с момента зарегистрированной сероконверсии, в течение 2-летнего периода серологического наблюдения и через 8 месяцев с момента появления признаков лимфоаденопатии. С другой стороны, у определенных категорий пациентов, например у детей, IgM антитела вообще не образуются.
Определение авидности IgG антител является высокоспецифичным и чувствительным методом диагностики острого первичного токсоплазмоза, что особенно важно при обследовании беременных для устранения потенциального риска появления врожденного токсоплазмоза у детей.
Недавно была разработана методика измерения антигенсвязывающей авидности (функциональной аффинности) IgG антител к Toxoplasma gondii, позволяющая разделить низкоаффинные антитела от высокоаффинных, которые указывают на перенесенную в прошлом инфекцию. С помощью этой методики первичная инфекция может быть идентифицирована с использованием единственной порции сыворотки.
Инфекции, вызываемые вирусом простого герпеса. Частота инфицирования новорожденных у женщин субклинической формой простого герпеса составляет 3-5% при хронической инфекции и доходит до 30-50% при заражении во время беременности (первичная инфекция). Инфекции, вызываемые вирусами простого герпеса, цитомегаловирусом относятся к инфекциям с нетипичной динамикой антителообразования (когда наличие IgM не является достоверным и достаточным признаком для дифференциации стадий заболевания). Определение IgM антител может давать ложноотрицательные результаты, поскольку они могут вообще не образовываться, или присутствовать в количествах, трудных для определения.
Ложноположительные результаты могут возникать по следующим причинам: длительная персистенция IgM антител или их присутствие может быть не связано с инфекцией; IgM антитела могут определяться при реактивации инфекции или при вторичной инфекции, например, вирусом иммунодефицита человека; различные вирусы могут иметь общие эпитопы (например, вирус простого герпеса и вирус варицелла-зостер), что приводит к возникновению перекрестных реакций. Диагностика активной фазы инфекции по 4-кратному возрастанию титра IgG также может вызывать затруднения, поскольку титр IgG антител может увеличиваться достаточно быстро (в течение 1-2 суток) после проявления симптомов заболевания.
Таким образом, определение серологических маркеров этих инфекциях не может служить специфичным тестом для дифференциации между первичной инфекцией и реактивацией. Заражение вирусом простого герпеса (ВПГ) ведет к пожизненной персистенции с возможностью реактивации вируса и перекрестного заражения другим серотипом ВПГ. Преобладание хронических и бессимптомных форм течения болезни, а также возможность атипичных проявлений ставит под сомнение диагностику по внешним признакам. Приблизительно 20% больных ВПГ-2 не имеют симптомов вообще, а 60% лиц имеют признаки, которые невозможно диагностировать и которые не принимаются врачом и самими больными за герпес (нетипичные проявления). Обе эти группы имеют риск заразить своих партнеров. Специфические IgM не могут быть использованы в качестве достоверного маркера для диагностики острой и, особенно, первичной инфекции, так как IgM к ВПГ могут образовываться как при первичном инфицировании, так и при реинфекции и реактивации вируса, но в то же время они способны вырабатываться в достаточном для диагностики количестве только у 30% людей.
Единственным способом, позволяющим сразу и достоверно диагностировать первичную инфекцию, является определение индекса авидности специфических антител.
Цитомегаловирусная инфекция (ЦМВИ) — самая распространенная внутриутробная инфекция и одна из наиболее частых причин невынашивания беременности. Риск внутриутробного инфицирования и характер поражения плода зависят от наличия антител у матери и срока инфицирования плода. При первичном инфицировании серонегативной беременной риск передачи плоду составляет примерно 50%.
Диагностика первичной ЦМВИ обычно основывается на определении сероконверсии, наличия высокого титра специфичных IgM или четырехкратного возрастания титра специфических IgG. В связи с тем, что момент сероконверсии и возрастание титров IgG диагностировать достаточно трудно, IgM антитела являются наиболее часто используемым маркером для диагностики острой инфекции. Однако у некоторых больных IgM антитела сохраняются длительное время, что приводит к гипердиагностике острой инфекции.
Определение авидности антител IgG рассматривается как наиболее важный серологический маркер, поскольку низко- и высокоавидные антитела IgG доминируют соответственно при недавней или длительно текущей инфекции.
Использование теста на авидность IgG при позитивной реакции на IgM антитела помогает подтвердить или исключить наличие первичной ЦМВИ и в ряде случаев помогает избежать необоснованных инвазивных процедур.
Вирусный гепатит С. Лабораторная диагностика гепатита С (ВГС) основана на выявлении специфических маркеров инфицирования (IgM и IgG антитела к ВГС, РНК ВГС). lgM-ответ в острой фазе гепатита С не следует классическому пути антителообразования: IgM анти-HCV могут выявляться одновременно и даже позднее, чем анти-ВГС класса IgG. Поэтому обнаружение IgM анти-ВГС не может быть использовано как маркер острой HCV-инфекции. Вместе с тем, длительность циркуляции антикор-lgM (3-5 месяцев) является фактором, прогнозирующим персистентную инфекцию, а их появление при хроническом гепатите С свидетельствует о реактивации вируса, т.е. об обострении процесса. Единственным достоверным фактором подтверждения первичной инфекции ВГС является сероконверсия.
Индекс авидности IgG при первичной ВГС инфекции имеет низкие значения и возрастает с течением времени, что подтверждает целесообразность использования определения авидности IgG антител для дифференциальной диагностики первичной инфекции от хронической или перенесенного гепатита С.
Сдавайте анализы постоянно в одной и той же лаборатории – и вашему врачу будут примерно известны Ваши личные показатели нормы и любое отклонение от нормы будет сразу им замечено.
Читайте также:


