Рациональная антибиотикотерапия инфекционных заболеваний
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.

Читайте в новом номере
Антимикробные средства относятся клекарственным препаратам, эффективность которых является наиболее очевидной. Внедрение антибиотиков вмедицинскую практику привело кснижению летальности при наиболее тяжелых ишироко распространенных инфекционных болезнях (пневмония, менингит, эндокардит, туберкулез идр.), атакже уменьшению заболеваемости некоторыми социально значимыми болезнями (ревматическая лихорадка).
Основное ограничение эффективности антимикробных препаратов — это способность микроорганизмов вырабатывать устойчивость (резистентность) к их действию. Этот естественный процесс многократно ускоряется при необоснованном и избыточном применении антимикробных препаратов в качестве средств профилактики в медицине, средств самолечения широкими кругами населения, средств стимуляции роста животных и птиц в сельском хозяйстве. Угроза формирования и распространения антибактериальной резистентности была осознана научным сообществом практически сразу после появления первых антибиотиков, однако в течение многих лет проблема решалась за счет разработки и внедрения новых препаратов, преодолевающих устойчивость.
В глобальном плане наибольшее количество антимикробных препаратов назначается врачами первичного звена, прежде всего для лечения острых респираторных инфекций. Поэтому определяющими составляющими сдерживания антибиотикорезистентности являются ограничение потребления антибиотиков в амбулаторной практике и рационализация их использования. Комплекс мероприятий по рационализации применения антимикробных препаратов с целью повышения их эффективности и сдерживания антибиотикорезистентности был разработан экспертами Альянса клинических химиотерапевтов и микробиологов и опубликован в 2014 г. в виде рекомендаций по стратегии и тактике применения антимикробных препаратов в лечебных учреждениях первичного звена России [7, 8]. Ключевые положения по рациональному использованию антибиотиков у детей при инфекциях респираторного тракта, изложенные в указанных выше рекомендациях, представлены в настоящей публикации. При этом особое внимание обращается на общие положения, которые обозначены как 10 принципов рационального применения антимикробных средств в амбулаторной практике (табл. 1).

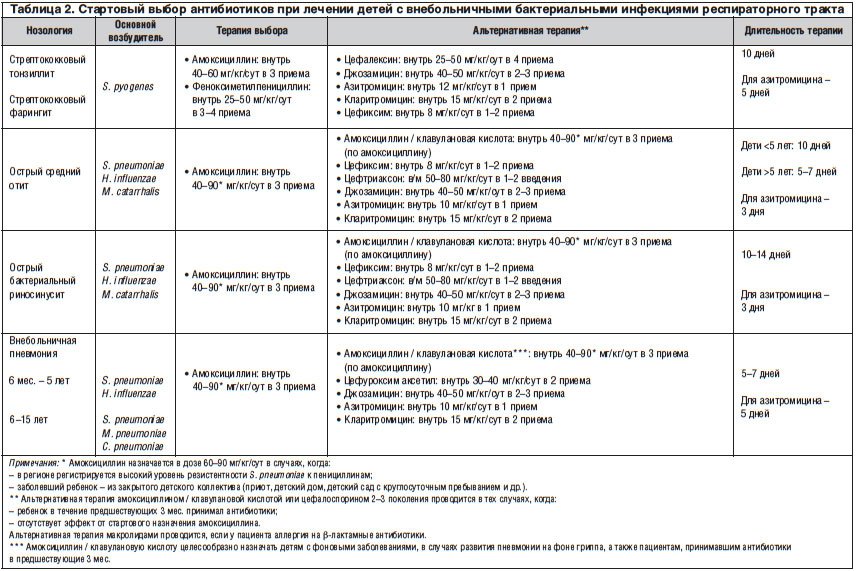
Данные об основных бактериальных возбудителях заболеваний органов дыхания у детей, а также тактика стартовой антибиотикотерапии приведены в таблице 2. Как видно из представленных данных, основным бактериальным возбудителем острого тонзиллофарингита является β-гемолитический стрептококк группы, А (БГСА) [7–10]. Однако провести дифференциальный диагноз между тонзиллофарингитами вирусной и бактериальной этиологии на основании исключительно клинических данных — весьма трудная задача. В связи с этим возрастает роль верификации. Подтверждение стрептококковой этиологии тонзиллофарингита считается обоснованием незамедлительного назначения антибактериальной терапии. Следует подчеркнуть, что БГСА продолжает сохранять высокую чувствительность к пенициллину и амоксициллину, что позволяет рекомендовать их в качестве препаратов выбора. При использовании пенициллинов в предшествующие месяцы или при рецидивирующем стрептококковом тонзиллофарингите показана альтернативная терапия амоксициллином / клавулановой кислотой или пероральными цефалоспоринами (цефалексин, цефиксим). Макролиды могут быть рекомендованы только при аллергии на β-лактамные антибиотики. Продолжительность антибактериальной терапии не должна быть меньше 10 дней (исключение — азитромицин), что является непременным условием для эрадикации возбудителя и предупреждения осложнений (табл. 2).
Основными бактериальными возбудителями острого среднего отита и синусита являются Streptococcus (S.) pneumoniaе, Haemophilus (Н.) influenzae и реже — Moraxella (М.) catarrhalis. Большинство штаммов указанных возбудителей сохраняют высокую чувствительность к аминопенициллинам (амоксициллин, амоксициллин / клавулановая кислота) и цефалоспоринам третьего поколения (цефтриаксон, цефиксим и др.), что и определяет их выбор в качестве препаратов выбора. Макролиды могут быть использованы только в том случае, если имеются указания на аллергию к β-лактамным антибиотикам (табл. 2). Особо следует отметить, что абсолютными показаниями для назначения антибиотиков при остром среднем отите являются гноетечение из уха и двустороннее поражение у детей в возрасте до 2 лет [7–10].
Среди бактериальных поражений респираторного тракта особое место занимают пневмонии. У детей дошкольного возраста наиболее частым бактериальным возбудителем внебольничных пневмоний является S. pneumoniaе, реже заболевание вызывается H. influenzaе [11–16]. Учитывая этиологические особенности пневмонии, препаратом первого ряда является амоксициллин. В том случае, когда в регионе регистрируется высокий уровень резистентности S. pneumoniae к пенициллинам, дозу амоксициллина необходимо повысить до 60–90 мг/кг/сут. Аналогичную тактику используют и тогда, когда заболевший ребенок находится в коллективе закрытого типа (табл. 2). У детей школьного возраста основным возбудителем внебольничных пневмоний также является S. рneumoniaе. Однако нередко этиологическими факторами пневмонии у детей указанной возрастной группы становятся Mycoplasma (М.) рneumoniae и Chlamydia (С.) рneumoniaе [11–16]. В связи с особенностями этиологии внебольничных пневмоний у детей школьного возраста стартовая антибиотикотерапия может проводиться не только аминопенициллинами или цефалоспоринами, но и макролидами — в случае подозрения на атипичную этиологию пневмонии (табл. 2).
Активное внедрение в педиатрическую практику принципов антибактериальной терапии, изложенных в представленных рекомендациях, позволит не только добиться положительного результата лечения и уменьшения частоты осложнений, но и существенно снизит риск селекции антибиотикоустойчивых штаммов.
Только для зарегистрированных пользователей
Хотя решение о назначении антибиотиков — прерогатива лечащего врача, первостольники должны располагать достаточной информацией о стандартно прописываемых антибактериальных средствах, чтобы суметь грамотно ответить на возможные вопросы покупателей по применению того или иного препарата.
В настоящее время в медицинском сообществе сформулированы следующие классические принципы антибактериальной терапии:
- антибиотик назначается врачом в соответствии со стандартами лечения и клиническими рекомендациями;
- при выборе антибиотика учитывается чувствительность препарата к предполагаемым возбудителям данной нозологической формы инфекции;
- препарат должен хорошо проникать в пораженные инфекционным воспалением органы и ткани, создавая терапевтическую концентрацию в очаге инфекции;
- для уменьшения риска развития побочных и нежелательных эффектов проводимой антибактериальной терапии принимаются во внимание такие факторы, как возраст пациента, его фоновая патология и сопутствующая терапия;
- критериями выбора антибиотика наряду с максимальной эффективностью и минимальной токсичностью являются также наименьшая стоимость лечения и наибольшая комплаентность.
Работники первого стола при продаже любого антибиотика должны обязательно информировать покупателя о необходимости проведения полного рекомендованного курса лечения в прописанных дозах. Как показывает опыт, многие пациенты самостоятельно снижают дозировку или прекращают принимать лекарство, почувствовав первые признаки улучшения состояния. Это не только может стать причиной развития осложнений заболевания, но и увеличивает резистентность распространенных возбудителей инфекции к антимикробным средствам.
Как in vitro, так и по результатам различных клинических исследований, амоксициллин показал высокую активность в отношении часто встречающейся этиологически значимой грамположительной флоры: Staphylococcus spp. (за исключением штаммов, продуцирующих пенициллиназу), Streptococcus spp. и др., а также аэробных грамотрицательных микроорганизмов: Neisseria gonorrhoeae, Neisseria meningitidis, Escherichia coli, Shigella spp., Salmonella spp., Klebsiella spp*. Благодаря этому сегодня амоксициллин имеет достаточно большой круг клинических показаний: его применяют при бактериальных инфекциях дыхательных путей, лор-органов, мочеполовой системы, абдоминальных инфекциях, инфекциях кожи и мягких тканей, желудочно-кишечного тракта, болезни Лайма, менингите и других заболеваниях.
Амоксициллин обладает существенными фармакокинетическими преимуществами по сравнению с рядом других пенициллинов. Так, биодоступность амоксициллина достигает 75—95%, степень связывания с белками плазмы крови — 20%*. Это обеспечивает высокую концентрацию амоксициллина в тканях при пероральном приеме, позволяя достичь эрадикации возбудителя и в то же время избежать развития нежелательных явлений. Существенным плюсом амоксициллина также является независимость всасывания из желудочно-кишечного тракта от приема пищи, что делает режим терапии более благоприятным для пациентов.
Благодаря хорошей переносимости, высокому профилю безопасности, удобству применения, возможности реализации ступенчатой терапии и относительно невысокой стоимости, амоксициллин, несмотря на открытие новых классов антибактериальных препаратов, прочно удерживает свои позиции как препарат выбора при лечении многих воспалительно-инфекционных заболеваний у детей и взрослых.
На фармрынке России амоксициллин представлен как оригинальным препаратом, так и высококачественными дженериками, отличающимися более низкой ценой. Среди дженериков есть и отечественные ЛП, выпускаемые в различных дозировках и лекарственных формах — таблетки, капсулы, порошок для приготовления суспензии (однодозовые пакетики типа саше). Возможность применения жидких лекарственных форм амоксициллина, способных обеспечить сопоставимую с инъекционными растворами концентрацию в крови активного вещества, особенно значима при лечении инфекций у детей или у пациентов с затруднением глотания. Разные формы выпуска позволяют применять препарат в зависимости от ситуации, возраста пациента и личных предпочтений, что расширяет возможности использования антибиотика и повышает приверженность терапии.
––––––––––––––––––––––––––––
* Жаркова Л.П., Козлова Т.Д. Амоксициллин в лечении внебольничных инфекций детского возраста: оправданный выбор врача-педиатра. Фарматека, 2007, № 14.
Антимикробная терапия (АТ) — вид терапии, предполагающий использование антимикробных препаратов (АМП) — группы лекарственных средств (ЛС), действие которой избирательно направлено на подавление жизнедеятельности возбудителей инфекционных заболеваний, таких как бактерии, грибы, простейшие, вирусы. Под избирательным действием понимают активность только в отношении возбудителей инфекции при сохранении жизнеспособности клеток хозяина, и действие не на все, а на определённые роды и виды микроорганизмов.
Все АМП, несмотря на различия химической структуры и механизма действия, объединяет ряд специфических свойств: мишень для их действия находится не в тканях человека, а в клетке микроорганизма; активность данной группы ЛС не является постоянной, а снижается со временем, что обусловлено формированием у микроорганизмов лекарственной устойчивости/резистентности.
Прогресс в области клинической микробиологии, существенно расширивший представления о возбудителях инфекционных заболеваний, а также неизменная потребность в новых классах АМП, обусловленная распространением антибиотикорезистентных возбудителей и растущими требованиями к безопасности фармакотерапии, превратили АМП в самую многочисленную группу ЛС. Так, в РФ в настоящее время используется более 30 групп АМП, а общее число препаратов (без учета генериков) превышает 200.
АМП, как и другие ЛС, подразделяются на группы и классы (пенициллины, цефалоспорины, макролиды и т.д.). Такое деление имеет большое значение с точки зрения понимания общности механизмов действия, спектра активности, фармакокинетических особенностей, характера нежелательных реакций (НР).
Необходимо отметить, что между АМП одного поколения или класса, незначительно отличающимися по химической структуре, могут быть существенные различия по фармакодинамике и фармакокинетике. Поэтому их неверно рассматривать как взаимозаменяемые.
АТ может быть этиотропной и эмпирической. Этиотропная АТ — это целенаправленное применение АМП, активных в отношении установленного возбудителя инфекции. Данный вид АТ является наиболее рациональным, так как позволяет выбрать препарат(-ы) узкого спектра с наиболее оптимальным соотношением эффективность/безопасность.
Эмпирическая АТ — это применение АМП до получения сведений о возбудителе инфекционного процесса и его чувствительности к АМП. Она составляет основу современной терапии внебольничных инфекций. Эмпирическая АТ проводится с учётом наиболее вероятных возбудителей данной инфекции и предполагаемой их чувствительности к доступным АМП. При этом по возможности, следует учитывать локальные данные антибиотикорезистентности потенциальных патогенов. Существует несколько общих принципов назначения системных АМП, обеспечивающих их наиболее эффективное использование в клинической практике:
- Точно поставленный диагноз, позволяющий определить с одной стороны локализацию инфекционного процесса, с другой — предполагаемого возбудителя.
- Обоснованность применения АМП. Некоторые бактериальные и многие вирусные инфекции не требуют специфического лечения. В то же время их применение способствует селекции антибиотикорезистентных штаммов микроорганизмов и создаёт потенциальный риск развития НР.
- Выбор оптимального АМП/комбинации АМП с учётом характера инфекции, её локализации и тяжести течения, а также индивидуальных особенностей пациента и фармакологических свойств ЛС. Известно, что большинство инфекционных заболеваний на сегодняшний день может успешно лечиться одним препаратом (монотерапия), однако в опредёленных случаях следует использовать одновременно два и более АМП (комбинированная терапия).
При комбинировании нескольких АМП, возможно получение in vitro различных эффектов в отношении определённого микроорганизма: аддитивное действие, синергизм, антагонизм. Существует несколько показаний для использования комбинаций АМП:
- Профилактика формирования резистентности микроорганизмов к АМП. Несмотря на то, что данное показание является одним из наиболее частых при назначении комбинированной АТ, преимущества такого подхода доказаны только в отдельных клинических ситуациях — туберкулёз, инвазивная синегнойная инфекции. Это же показание лежит в основе использования рифампицина в комбинации с другими АМП для лечения стафилококковых инфекций.
- Лечение инфекций полимикробной этиологии. При ряде полимикробных инфекций достаточно использования монотерапии АМП. В то же время, в некоторых случаях (например, при интраабдоминальных инфекциях, вызванных смешанной аэробной и анаэробной микрофлорой), возникает необходимость в использовании комбинаций препаратов. В то же время необходимо отметить, что подобному подходу существует альтернативы в виде назначения карбапенемов, ингибиторозащищённых пенициллинов или антианаэробных фторхинолонов (моксифлоксацин).
- Эмпирическая терапия у пациентов с нейтропенией или инфекциями неясной этиологии. В случае необходимости начинать терапию до получения результатов микробиологического исследования, целесообразно назначение комбинации АМП, позволяющей охватить возможно более широкий спектр предполагаемых возбудителей. В последующем после получения результатов микробиологического исследования возможен перевод пациента на монотерапию.
- Синергизм. Использование комбинаций АМП, обладающих синергизмом in vitro для лечения инфекций, вызванных микроорганизмами со сниженной чувствительностью, является чрезвычайно привлекательным подходом. Однако в условиях in vivo только при ограниченном числе инфекций комбинированная АТ оказалась более эффективной, чем монотерапия. Одним из наиболее показательных примеров является терапия энтерококкового эндокардита. Лечение данного заболевания пенициллинами в монотерапии приводит к высокой частоте неэффективности вследствие того, что энтерококки имеют сниженную природную чувствительность к данному препарату. Добавление к пенициллину гентамицина или стрептомицина приводит и in vitro, и in vivo к синергизму с достижением клинической эффективности, аналогичной таковой при стрептококковом эндокардите. Более высокая клиническая эффективность комбинаций АМП, обладающих синергизмом in vitro, по сравнению с монотерапией была продемонстрирована у пациентов с иммунодефицитными состояниями.
В то же время следует помнить, что комбинированная АТ, как правило, является более дорогой терапевтической альтернативой. Кроме того, совместное применение нескольких АМП повышает вероятность развития НР, причём в случае их появления чрезвычайно сложно определить, с каким конкретно препаратом связаны НР. Необходимо избегать использования неизученных комбинаций АМП, так как они могут ослаблять действие друг друга и ухудшать исход лечения пациента.
- Выбор оптимального режима дозирования (разовой дозы, кратности применения) и пути введения, показаний к мониторингу его концентрации в сыворотке крови.
- Определение продолжительности АТ. За некоторым исключением, оптимальная продолжительность АТ остается не до конца определённой в связи с отсутствием клинических исследований, направленных на изучение данного вопроса. Рекомендуемая продолжительность АТ основывается преимущественно на анализе клинического опыта ведения пациентов с определённой инфекцией и может зависеть от многих факторов — возбудителя, локализации инфекции, состояния иммунной системы, наличия значимых сопутствующих заболеваний и осложнений. Для пациентов с нетяжёлыми инфекциями длительность приёма АМП обычно не превышает 7-14 дней, в литературе всё чаще появляются исследования, свидетельствующие о возможности ещё большего сокращения сроков применения АМП при респираторных инфекциях; а приём одной дозы фосфамицина является высокоэффективной терапевтической альтернативой лечения острого неосложнённого цистита. В то же время пациентам с иммуносупрессией, некоторыми бактериальными (остеомиелит, эндокардит, хронический простатит) и вирусными инфекциями (хронический гепатит, ВИЧ-инфекция) необходимы продолжительные курсы АТ.
Наиболее значимые характеристики АМП и факторы со стороны пациента, определяющие выбор АМП представлены в таблице. Рациональная АТ должна обеспечивать максимально высокую вероятность клинического излечения (тактическая цель) и минимальный риск развития и распространения антибиотикорезистентности (стратегическая цель). Поскольку для лечения одной и той же инфекции на рынке обычно присутствует несколько терапевтических альтернатив со сходными микробиологическими и клиническими характеристиками, немаловажную роль при выборе АМП играют стоимость терапии и удобство применения.
Таблица. Факторы, значимые при выборе АМП для эмпирической АТ
Возраст пациента является одним из существенных факторов при выборе АМП. Так, у детей раннего возраста и пожилых пациентов существуют некоторые особенности в этиологии инфекций, что в первом случае обусловлено внутриутробным инфицированием и недостаточной зрелостью иммунной системы, во втором — наличием хронических сопутствующих заболеваний и физиологическим ослаблением факторов противоинфекционной защиты. Вероятность инфицирования микроорганизмов с определёнными механизмами вторичной резистентности также может зависеть от возраста. Так, известным фактором риска выявления пенициллинорезистентного S. pneumoniae является возраст моложе 2 и старше 65 лет.
С возрастом может меняться и фармакокинетика АМП. Так, рН желудочного сока у детей в возрасте до 3 лет и у лиц старше 60 лет выше по сравнению с другими возрастными группами. Это обусловливает, в частности, увеличение всасывания у них пероральных пенициллинов. Другим примером является функция почек, которая снижена у новорождённых и пожилых пациентов. Вследствие этого дозу АМП, которые выводятся преимущественно через почки, необходимо корригировать пропорционально степени уменьшения клубочковой фильтрации. Новорождённые также отличаются незрелостью ферментных систем печени, изменением распределения АМП вследствие большего объёма внеклеточной жидкости, более низким содержанием альбуминов в плазме крови. Лица пожилого возраста нередко получают другие ЛС в связи с наличием хронических сопутствующих заболеваний, поэтому они больше подвержены риску лекарственных взаимодействий, а НР на АМП регистрируются у них достоверно чаще. Ряд АМП (например, фторхинолоны) не разрешён к применению у детей, другие имеют возрастные ограничения (в частности, тетрациклины не применяются у детей в возрасте до 8 лет). При выборе АМП как у детей, так и у пожилых пациентов особое внимание нужно уделять удобству назначенного режима АТ. Для детей при пероральном приёме актуально использование специальных детских лекарственных форм, у пожилых пациентов нужно стремиться к назначению АМП с 1-2-кратным приёмом в сутки, что повышает комплаентность к проводимой терапии.
Анализ предшествующего приёма АМП позволяет оценить их переносимость, в том числе наличие и характер аллергических реакций. Кроме того, факт недавнего приёма АМП (1-3 месяца до развития данного эпизода инфекции) значим с точки зрения оценки структуры потенциальных возбудителей и профиля их антибиотикорезистентности.
Выбор АМП для эмпирической терапии нозокомиальных инфекций представляет непростую задачу. Он предполагает регулярный мониторинг структуры возбудителей и антибиотикорезистентности в конкретном ЛПУ и его структурных подразделениях, который должен включать оценку распространённости штаммов энтеробактерий, продуцирующих β-лактамазы расширенного спектра (БЛРС), MRSA, уровень продукции металлобеталактамаз среди P. aeruginosa и Acinetobacter spp., устойчивость возбудителей нозокомиальных инфекций к фторхинолонам, аминогликозидам и ингибиторозащищённым пенициллинам.
В чрезвычайно редких случаях возможно интратекальное или интравентрикулярное введение некоторых АМП плохо проникающих через гематоэнцефалический барьер при терапии менингитов, вызванных полирезистентными штаммами возбудителей. В то же время, внутривенное введение АМП позволяет достигать терапевтических концентраций в плевральной, перикардиальной, перитонеальной или синовиальной полостях, вследствие чего их введение непосредственно в вышеуказанные области не рекомендуется.
Функция печени и почек является одним из наиболее важных факторов при решении вопроса о выборе АМП, особенно в случае, если высокие сывороточные или тканевые концентрации препарата являются потенциально токсичными. Так как большинство АМП частично или полностью выводятся через почки, в случае нарушения их функции для многих из них требуется коррекция режима дозирования (дозы и/или кратности применения). Исходя из степени влияния почечной недостаточности на экскрецию АМП можно разделить на 3 группы:
- ЛС, которые применяются в обычной дозе. К ним, например, относится большинство макролидов, цефтриаксон, цефоперазон, феноксиметилпенициллин, клиндамицин.
- ЛС, которые противопоказаны при почечной недостаточности, так как экскретируются с мочой в активной форме и характеризуются особо выраженной кумуляцией при нарушении функции почек. В эту группу относят нефторированные хинолоны, нитрофурантоин, сульфаниламиды, тетрациклин.
- ЛС, режим дозирования которых меняется в зависимости от степени почечной недостаточности.
А — в контролируемых исследованиях у беременных женщин не выявлено риска неблагоприятного действия на плод. Повреждающее действие на плод маловероятно.
В — исследования у животных не выявлено риска для плода; в исследованиях у животных были получены данные о нежелательном действии на плод, однако эти данные не подтвердились в контролируемых исследованиях у беременных женщин.
С — исследования у животных выявили неблагоприятное действие на плод, контролируемых исследований у беременных женщин не проводилось, потенциальная польза, связанная с применением ЛС у беременной, может оправдывать его использование, несмотря на возможный риск, либо исследования у животных и беременных женщин не проводились.
D — имеются доказательства риска неблагоприятного действия ЛС на плод человека, однако потенциальная польза, связанная с применением ЛС у беременных, может оправдывать его использование, несмотря на возможный риск (ситуация, угрожающая жизни женщины, при которой другие ЛС неэффективны или не могут применяться).
Х — исследования у животных и клинические испытания выявили нарушения развития плода и/или имеются доказательства риска неблагоприятного действия ЛС на плод человека, полученные на основании опыта применения ЛС у человека; риск, связанный с применением ЛС у беременной, превышает потенциальную пользу. Данная группа ЛС противопоказана беременным и женщинам репродуктивного возраста, не использующим адекватные методы контрацепции.
Несмотря на практически полное отсутствие клинически подтверждённых данных о тератогенном потенциале АМП у людей, источником информации могут быть исследования у животных, а также анализ практического опыта применения в рамках эпидемиологических исследований. Так, на сегодняшний день известно, что большинство пенициллинов и цефалоспоринов безопасны для плода при использовании у беременных. В то же время, например, метронидазол обладал тератогенным эффектом у грызунов, поэтому его не рекомендуется назначать беременным в I триместре.
Практически все АМП проникают в грудное молоко. Количество препарата, проникающее в молоко, зависит от степени его ионизации, молекулярной массы, растворимости в воде и липидах. В большинстве случаев концентрация АМП в грудном молоке является достаточно низкой. Однако даже низкие концентрации определённых ЛС способны привести к неблагоприятным последствиям для ребёнка. Так, например, даже малые концентрации сульфаниламидов в грудном молоке могут приводить к повышению уровня несвязанного билирубина в крови (вытесняя его из связи с альбуминами) у недоношенных новорождённых.
Следует подчеркнуть, что при отсутствии достоверных данных о безопасности того или иного АМП у беременных и/или кормящих от их применения лучше воздерживаться. Кроме того, назначение любого АМП у данной категории пациентов должно тщательно мониторироваться в связи с отсутствием препаратов с подтверждённой в контролируемых исследованиях безопасностью для плода (категория А).
Основным методом оценки эффективности АТ у конкретного пациента является мониторинг клинических симптомов и признаков заболевания, а также результатов параклинических методов обследования. Для некоторых АМП (например, аминогликозиды, ванкомицин) может проводиться мониторинг их сывороточных концентраций с целью профилактики развития токсических эффектов, особенно у пациентов с нарушением функции почек.
Ещё одним методом мониторинга эффективности терапии является определение бактерицидного титра сыворотки (использовался у пациентов с остеомиелитом, бактериемией и инфекционным эндокардитом). Принцип метода основан на инкубации серийных разведений сыворотки пациента с бактериальной взвесью возбудителя с целью определения максимального разведения, при котором подавляется рост или наступает гибель выделенного у больного микроорганизма. Согласно результатам многоцентрового исследования, пиковый и остаточный титры, соответственно, по крайней мере, 1:64 и 1:32 являются прогностическими показателями эффективности терапии инфекционного эндокардита. Однако вследствие сравнительно низкой стандартизации метода, он не нашёл широкого распространения в клинической практике.
Эффективность эмпирически назначенной АТ оценивается в течение 48-72 ч с момента начала лечения, при достаточном клиническом ответе АТ продолжается, при отсутствии должного эффекта — пересматривается. Смена режима АТ проводится при документированной клинической неэффективности, развитии угрожающих здоровью или жизни пациента НР, вызванных АМП, при применении препаратов, имеющих ограничения по длительности применения вследствие кумулятивной токсичности (например, аминогликозиды, хлорамфеникол).
К смене АМП в случае неэффективности нужно подходить осмысленно с учётом особенностей клинической картины заболевания и характеристик препарата. Неудачи АТ могут быть связаны со множеством причин. При этом в первую очередь нужно оценить правильность постановки диагноза, так как многие неинфекционные заболевания вызывают сходные с инфекциями клинические симптомы. Отсутствие эффекта от проводимой АТ может быть связано с неправильным выбором АМП, который выполнен без учёта его природной активности и уровня антибиотикорезистентности ключевых патогенов, поздним началом лечения, использованием низких доз, нерационального пути введения и недостаточной продолжительностью курса АТ.
Эффективность АМП может снижаться при одновременном назначении других ЛС, обладающих антагонизмом, либо оказывающих влияние на метаболизм и выведение АМП. Даже при должной чувствительности возбудителя к АМП возможны неудовлетворительные результаты лечения из-за плохого проникновения препарата в очаг инфекции вследствие его физико-химических свойств, недостаточного кровоснабжения, образования биологического барьера вокруг очага инфекции, присоединения суперинфекции.
Следует отметить, что лихорадка, являющаяся одним из ключевых клинических проявлений инфекции, может развиваться и на приём АМП. Применение этиотропных средств должно дополняться адекватной дезинтоксикационной терапией, а также использованием препаратов или средств патогенетической терапии, улучшающих прогноз (вазопрессоры, кислородотерапия, дексаметазон, активированный протеин С и др.). Не менее важным является учёт комплаентности к проводимой терапии.
Читайте также:


