Протезирование клапанов сердца инфекционный эндокардит
, MD, North Shore Hospital, Auckland
Last full review/revision September 2017 by Guy P. Armstrong, MD







Эндокардит обычно означает инфекцию эндокарда (то есть инфекционный эндокардит). Термин эндокардит также может включать неинфекционный эндокардит, при котором стерильные тромбоциты и фибриновые тромбы фиксируются на клапанах сердца и прилегающем эндокарде. Неинфекционный эндокардит иногда может приводить к инфекционному эндокардиту. Оба могут привести к эмболизации и нарушению функции сердца.
Диагноз инфекционного эндокардита обычно устанавливается с учетом совокупности всех клинических данных, а не результата одного исследования.
Инфекционный эндокардит может возникнуть в любом возрасте. Мужчины заболевают в два раза чаще, чем женщины. Лица, употребляющие внутривенные наркотики, пациенты с ослабленным иммунитетом и пациенты с искусственными клапанами сердца и другими внутрисердечными устройствами имеют наибольший риск.
Этиология
Здоровое сердце относительно устойчиво к инфекции. Бактерии и грибы не легко адгезируются к поверхности эндокарда, и постоянный ток крови помогает предотвратить их оседание на эндокард. Таким образом, для развития эндокардита требуются, как правило, 2 условия:
Предшествующая аномалия эндокарда
Присутствие микроорганизмов в кровотоке (бактериемия)
Реже, массивная бактериемия или особо вирулентные микроорганизмы поражают нормальные клапаны.
Эндокардит часто поражает клапаны сердца. Основными предрасполагающими факторами ИЭ являются врожденные пороки сердца, ревматическое поражение клапанов, бикуспидальный или кальцинированный аортальный клапан, пролапс митрального клапана, гипертрофическая кардиомиопатия и предшествующий эндокардит. Протезирование клапанов и других внутрисердечных устройств представляет особый риск. Иногда пристеночные тромбы, дефекты межжелудочковой перегородки и область открытого аортального протока подвергаются инфицированию. Ядром инфекции является стерильная фибринозно-тромбоцитарная вегетация, формирующаяся при высвобождении поврежденными эндотелиальными клетками тканевых факторов.
Инфекционный эндокардит чаще всего поражает левые отделы сердца (например, митральный или аортальный клапаны). Примерно в 10–20% случаев поражаются правые отделы (трикуспидальный или пульмональный клапаны). Внутривенные наркоманы имеют более высокий риск развития правостороннего эндокардита (около 30–70%).
Микроорганизмы, поражающие эндокард, могут попадать из отдаленных очагов инфекции (например, кожный абсцесс, воспаленные или инфицированные десны, инфекция мочевыводящих путей) или через очевидные входные ворота, такие как центральный венозный катетер или места инъекций препаратов. Практически любой чужеродный имплантированный материал (например, желудочковый или перитонеальный шунт, протез) подвергается риску бактериальной колонизации, тем самым становясь источником бактериемии и, следовательно, эндокардита. Эндокардит может быть результатом асимптомной бактериемии, которая, как правило, возникает во время инвазивных стоматологических, медицинских или хирургических вмешательств. Даже чистка зубов и жевание могут приводить к бактериемии (обычно зеленящим стрептококком) у пациентов с гингивитом.
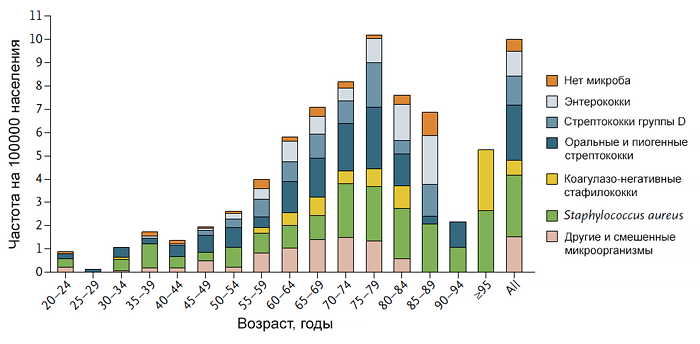
Возбудители различаются в зависимости от места инфекции, источника бактериемии и факторов риска пациента (например, внутривенные наркоманы), но в 80–90% случаев стрептококки и Staphylococcus aureus являются причиной ИЭ. Энтерококки, грам-отрицательные бациллы, микроорганизмы группы HACEK (Haemophilus, гемофильные бактерии, Actinobacillus actinomycetemcomitans, Cardiobacterium hominis, Eikenella corrodens и Kingella kingae) и грибки являются причиной большинства других случаев.
Болезнь протекает в трех стадиях:
Бактериемия: микроорганизмы присутствуют в крови
Адгезия: микроорганизм присоединяется к аномальному или поврежденному эндотелию с помощью поверхностных адгезинов
Колонизация: пролиферация организма вместе с развитием воспаления, что приводит к образованию зрелых вегетаций
Многие из возбудителей образовывают полисахаридные биопленки, которые защищают их от иммунной защиты хозяина и препятствуют проникновению антибиотиков
Патофизиология
Эндокардит имеет локальные и системные осложнения.
Местные последствия инфекционного эндокардита включают:
Абсцессы миокарда с деструкцией тканей, а иногда и с нарушением проводимости (чаще при нижне-перегородочных абсцессах).
Внезапная, тяжелая клапанная регургитация может привести к сердечной недостаточности и смерти (чаще из-за поражения митрального или аортального клапана).
Аортит в связи с распространением инфекции из прилегающих структур.
Для больных с протезированными клапанами характерно развитие абсцессов клапанного кольца, обструктивных вегетаций, абсцессов миокарда и грибковых аневризм, что проявляется клапанной обструкцией, дисфункцией клапана и нарушением проводимости.
Системные осложнения в первую очередь обусловлены
Эмболизация инфицированным материалом из сердечного клапана
Иммуно-опосредованные явления (в основном при хронической инфекции)
Поражение правых камер сердца характеризуется развитием септических эмболий легочной артерии, которые могут привести к инфаркту легкого, пневмонии или эмпиеме. Поражение левых камер сердца может приводить к эмболиям любых органов, особенно часто почек, селезенки и центральной нервной системы. Микотические аневризмы могут формироваться в любых крупных сосудах. Часто развиваются эмболии кожи и сетчатки. Вследствие отложения иммунных комплексов развивается диффузный гломерулонефрит.
Классификация
Инфекционный эндокардит может иметь вялотекущее, подострое течение или более острое, молниеносное течение с высокой опасностью развития быстрой декомпенсации.
Подострый бактериальный эндокардит (ПБЭ), несмотря на агрессивность, обычно развивается незаметно и прогрессирует медленно (т.е от нескольких недель до месяцев). Источник инфекции или входные ворота часто не выявляются. Возбудителями ПСЭ чаще всего являются стрептококки (особенно зеленящий, микроаэрофильный, анаэробный, стрептококки группы D и энтерококки), реже причиной могут быть золотистый и эпидермальный стафилококки - S. aureus, Staphylococcus epidermidis, стрептококки Gemella morbillorum, Abiotrophia defectiva (ранее, Streptococcus defectivus), Granulicatella и требовательный к питательным средам Haemophilus. Стрептококковый подострый эндокардит часто развивается на пораженных клапанах после асимптомной бактериемии, вследствие инфекций периодонта, гастроинтестинальных и урогенитальных инфекций.
Острый бактериальный эндокардит (ОБЭ) обычно развивается внезапно и прогрессирует быстро (т.е. в течение дней). Источник инфекции или входные ворота часто легко выявляются. Когда инфекция высоко вирулентна или бактериальное воздействие массивно, острый бактериальных эндокардит может поражать нормальные клапаны сердца. Он обычно вызван золотистым стрептококком S. aureus, гемолитическим стрептококком группы А, пневмококком или гонококком.
Эндокардит протезированного клапана (ЭПК) развивается у 2–3% пациентов в течение первого года после протезирования клапана и в 0,5% в последующие годы. Чаще развивается после замены аортального клапана, нежели митрального и в одинаковой степени поражает как механические, так и биологические протезы. Раннее начало инфекции ( 2 мес. после хирургического лечения) вызвано главным образом инфицированием в ходе операции бактериями, резистентными к противомикробным препаратам (S. epidermidis, дифтероиды, колиформные бациллы, Candida, Aspergillus). Позднее начало инфекции происходит в основном в результате контаминации низко-вирулентными организмами во время оперативного вмешательства или при транзиторных бессимптомных бактериемиях, чаще всего благодаря попаданию стрептококка; S. epidermidis; дифтероидов; и требовательной к средам грамотрицательной палочки Haemophilus, Actinobacillus actinomycetemcomitans, и Cardiobacterium hominis.
Клинические проявления
Клиническая картина зависит от классификации, но она неспецифична.
Первоначально симптомы подострого бактериального эндокардита смазанные: субфебрильная лихорадка ( 39 ° С), ночные поты, утомляемость, недомогание и потеря веса. Возможны озноб и артралгии. Симптомы клапанной недостаточности могут быть первым признаком, ведущим к постановке диагноза. Первоначально менее чем ( ≤ ) у 15% пациентов наблюдается лихорадка или шумы в сердце, но со временем оба эти симптома развиваются практически у всех больных. Объективное исследование может выявлять бледность, лихорадку, изменение ранее существовавшего шума или появление шума новой регугитации и тахикардию.

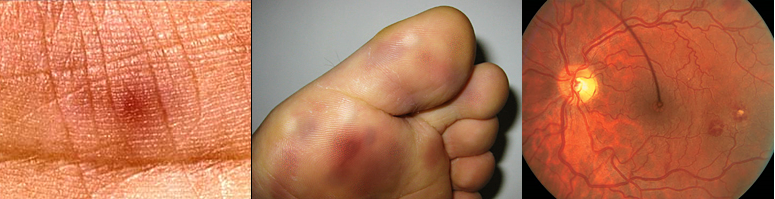
Этот пациент с инфекционным эндокардитом имеет множественные узелки Ослера (болезненные, эритематозные узелки на пальцах ног).
У данного пациента с инфекционным эндокардитом на ладонях видны множественные язвочки Джейнвея (безболезненные эритематозные папулы). На пальцах пациента также наблюдаются своеобразные узлы Ослера (болезненные, эритематозные узелки на пальцах).
На изображении слева показан узелок Ослера (мягкий эритематозный узелок) на большом пальце. На изображении справа показаны язвочки Джейнвея (безболезненные эритематозные пятна на ладони).
Точечные кровоизлияния представляют собой небольшие линейные кровоизлияния под ногтевыми пластинами.

На данной фотографии показаны конъюнктивальные петехии у пациента с инфекционным перикардитом.
На данной фотографии показано конъюктивальное кровоизлияние у пациента с инфекционным перикардитом.
На изображении слева показаны множественные пятна Рота или ретинальные кровоизлияния. Изображение справа – увеличенный снимок пятен Рота с бледной зоной в центре.
Клиническая картина острого бактериального эндокардита и эндокардита искусственного клапана подобна картине подострого бактериального эндокардита, но течение более быстрое. Лихорадка почти всегда выявляется в начале заболевания, у пациентов имеются симптомы интоксикации; иногда развивается септический шок. Сердечные шумы выявляются первоначально примерно у 50–80% пациентов и со временем у > 90%. Редко развивается гнойный менингит.
Септическая эмболия легочной артерии может вызывать кашель, плевральные боли в грудной клетке и иногда кровохарканье. Характерно наличие шума трикуспидальной регургитации.
Диагностика
Эхокардиография, иногда – другие методы получения изображения
Так как клиническая картина неспецифична, вариабельна и может развиться незаметно, диагностика требует высокой настороженности. Эндокардит следует подозревать у пациентов с лихорадкой без явных причин инфекции, особенно если есть шум в сердце. Настороженность в плане ИЭ должна быть очень велика в том случае, если имеются положительные результаты посева крови у пациентов с патологией клапанов сердца, у пациентов, которым недавно выполнялись инвазивные процедуры или у внутривенных наркоманов. Пациенты с доказанной бактериемией должны быть тщательно и многократно обследованы на предмет новых клапанных шумов и признаков эмболии.
Кроме позитивных посевов крови, других специфических лабораторных изменений нет. Установленные инфекционные поражения эндокарда часто приводят к нормохромной нормоцитарной анемии, лейкоцитозу, повышению СОЭ, увеличению уровня иммуноглобулинов, появлению циркулирующих иммунных комплексов и положительному ревматоидному фактору, но эти изменения не помогают в постановке диагноза. В общем анализе мочи часто выявляется микрогематурия, иногда эритроцитарные цилиндры, пиурия или бактериурия.
Идентификация возбудителя и определение его чувствительности к антибиотикам жизненно необходимы для определения тактики лечения.
Если заподозрен эндокардит, должно быть выполнено 3 забора крови на посев (20 мл каждый) в течение 24 ч (если клиническая картина представлена острым бактериальным эндокардитом, то 2 забора крови с интервалом между 1-м и 2-м в 1 час). Каждый новый забор крови должен быть произведен путем отдельной венепункции (т.е. не из ранее установленных внутрисосудистых катетеров). Забор крови не должен производиться во время наличия у пациента лихорадки или озноба, поскольку у большинства пациентов бактериемия носит постоянный характер. При эндокардите и в отсутствие предшествовавшей антибиотикотерапии все 3 посева образцов крови положительны, поскольку бактериемия продолжается; по крайней мере, 1 посев крови положительный в 99% случаев. Необходимо избегать преждевременного использования эмпирической антибактериальной терапии у пациентов с приобретенными или врожденными пороками во избежание эндокардитов с негативными посевами крови. Если ранее проводили антибактериальную терапию, следует также получить результаты гемокультуры, однако они могут быть отрицательными.
Посевы крови требуют 3–4-недельной инкубации для определенных микроорганизмов; однако некоторые запатентованные автоматически мониторирующие культуральные системы могут идентифицировать позитивные культуры в течение недели. Другие микроорганизмы (например, Aspergillus sp) могут не выявляться при посевах крови. Некоторые микроорганизмы (например, Coxiella burnetii, Bartonella sp, Chlamydia psittaci, Brucella sp) требуют серологической диагностики; другие микроорганизмы (например, Legionella pneumophila) требуют специальную культуральную среду или ПЦР (например, Tropheryma whippelii). Негативные результаты посевов крови могут быть следствием первичной антибактериальной терапии, инфицированности микроорганизмами, которые не растут на стандартных питательных средах, или указывать на другой диагноз (например, неинфекционный эндокардит, миксома предсердия с эмболиями, васкулит).
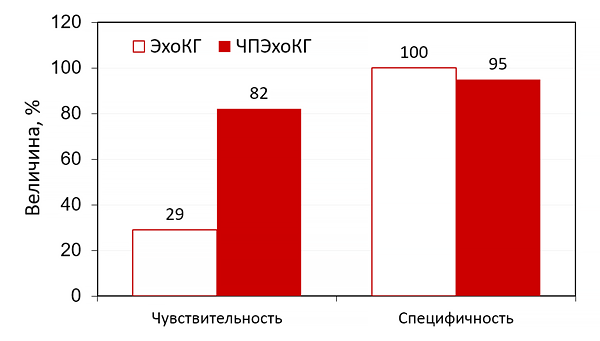
На начальном этапе необходимо выполнение эхокардиаграфии, обычно трансторакальной (ТТЭ), а не трансэзофагеальной (ТЭЭ). ТЭЭ является более чувствительной (т.е. способна выявлять вегетации маленького размера, невидимые при ТТЭ),
Чреспищеводную эхокардиографию следует проводить при таких случаях:
Пациенты имеют искусственный клапан
Трансторакальная эхокардиография не является диагностической
Диагноз инфекционного эндокардита был установлен клинически (проводится для выявления перфораций, абсцессов и свищей)
Иногда используется КТ, если при ЧПЭ не возможно точно определить околоклапанные абсцессы, а также для обнаружения микотических аневризм. ПЭТ является новым инструментом для диагностики эндокардита, который возникает в простетических и внутрисердечных устройствах. В настоящее время патологии, выявленные при КТ и ПЭТ включены в Европейские рекомендации в качестве основных критериев.
Инфекционный эндокардит достоверно диагностируется, когда микроорганизмы выявляются гистологически (или культурально) в эндокардиальных вегетациях, полученных в ходе операции на сердце, эмболэктомии или аутопсии. Так как вегетации обычно недоступны для исследования, существуют разнообразные клинические критерии для установления диагноза. К ним относятся пересмотренные критерии Дюка (с чувствительностью и специфичностью > 90%— Диагностические требования к диагнозу инфекционного эндокардита в соответствии с пересмотренными критериями Дюка а также Пересмотренные клинические критерии Дюка для диагностики инфекционного эндокардита) и модифицированные критерии Европейского общества кардиологии (ESC) 2015 года (1).
Критерии ESC аналогичны модифицированным критериям Дюка, но в качестве основных критериев включают результаты расширенной визуализации как указано далее:
Вегетации, абсцесс, псевдоаневризма, внутрисердечная фистула, клапанная перфорация или аневризма или новое частичное раскрывание створок искуссвенного клапана, которые выявлены при эхокардиографии
Аномальная активность вокруг искусственного клапана (имплантированного > 3 мес раньше), обнаруженная при ПЭТ/КТ или ОФЭКТ/КТ с лейкоцитами, меченными радиоактивными изотопами
Околоклапанные поражения, выявленные при КТ сердца
Критерии ESC также отличаются от малых модифицированных критериев Дюка, детализируя, что только лишь выявление бессимптомных сосудистых явлений при визуализации является достаточным.

Количество симптомов поражения сердца (кардиалгии, тахикардия, одышка) в дебюте заболевания выросло в несколько раз. Также появились новые ранние симптомы: кровохарканье, аритмии, рвота, подкожные кровоизлияния. При современном течении они наблюдаются в клинике заболевания достаточно часто [4].
Усугубляет процесс появление неврологической симптоматики. В 90% случаев – это эмболия среднемозговой артерии, с которой нередко начинается заболевание, приводя к диагностическим ошибкам. Но чаще клиника инсульта появляется в первые две недели антибиотикотерапии [5].
Современное течение ИЭ может сопровождаться поражением опорно-двигательного аппарата. Особенностью данного процесса является его развитие иногда за несколько месяцев до появления классических симптомов ИЭ. В дебюте данная ситуация встречается примерно в 40% случаев. Чаще всего это артралгии с поражением крупных и мелких суставов, распространенные миалгии, тендиниты, миозиты. Иногда развиваются септические артриты разной локализации.
Тяжесть клинических проявлений практически всегда зависит от скорости разрушения клапанов сердца, что обусловлено прежде всего вирулентностью возбудителя [6]. При ИЭ чаще поражается аортальный клапан. В данном случае ИЭ дебютирует с лихорадки, которая не всегда достигает фебрильных цифр. К ней могут присоединяться озноб и ночная потливость. Аускультативно может выслушиваться диастолический шум. Характерно появление неврологических симптомов, которые обусловлены эмболиями в мозг с развитием острого нарушения мозгового кровообращения. Часто выявляются артериальные эмболии в селезенку и почки, не всегда распознаваемые [6, 7]. Несколько реже встречается первичное поражение митрального клапана. Основным фактором риска, способствующим развитию ИЭ митрального клапана, в настоящее время является врожденная дисплазия створок с пролапсом. Клиника в данном случае чаще всего напоминает сепсис. Часто присутствуют лихорадка, потливость ночью, слабость, миалгии, боли в груди и спине. Практически на ранних стадиях развивается застойная сердечная недостаточность. Реже могут появляться признаки митрального стеноза с прогрессирующей клиникой, вплоть до отека легких. Данный вид ИЭ может сопровождаться эмболиями в сосуды разных органов, чаще у пациентов с грибковой этиологией заболевания. Этиология ИЭ трикуспидального клапана большей частью обусловлена внутривенным введением наркотических препаратов. Особенностью данного вида ИЭ является поражение правых отделов сердца у 80% пациентов, которое часто приводит к летальности. Считается, что причиной развития данной ситуации могут быть как нестерильные инъекции, так и иммунные нарушения [8]. Опираясь на спектр перечисленных выше клинических проявлений, можно утверждать, что пациент с дебютом ИЭ может обратиться за помощью к врачу любой специальности.
Прогноз заболевания зависит от качественно проведенной диагностики. Летальный исход наступает в результате развития сердечно-сосудистой недостаточности или тромбоэмболических осложнений [9]. В связи с появлением новых этиологических факторов, особенностей современного дебюта ИЭ, новых симптомов в клинической картине каждый случай ИЭ в клинической практике представляет как теоретический, так и практический интерес для врачей любой специальности.
Цель исследования – продемонстрировать типичные ошибки в диагностике современного течения ИЭ с целью своевременности постановки диагноза, предотвращения развития тяжелых осложнений и летальных исходов у пациентов с этим заболеванием.
Материалы и методы исследования
В качестве клинического примера представлен случай наблюдения пациента с длительно (на протяжении 8 месяцев) не диагностированным ИЭ.
Больной Г., 52 г. поступил в отделение гастроэнтерологии Дорожной больницы на ст. Н. Новгород 07.02.2019 г. При поступлении предъявлял жалобы на ноющие боли в области эпигастрия, не зависящие от приемов пищи, отсутствие аппетита, иногда запоры, слабость, потливость, особенно по ночам, повышение температуры до 38,2оС по вечерам, похудание.
Во время предыдущей госпитализации в отделение терапии в ноябре 2018 г. состояние пациента оценивалось как удовлетворительное. Во время осмотра у пациента констатировали ясное сознание и активное положение. Питание достаточное. Кожные покровы чистые, физиологической окраски. Периферические лимфоузлы не пальпируются. Перкуторно над легкими ясный легочный звук. При аускультации дыхание ослаблено, частота дыхания – 16 в минуту. Тоны приглушены, ритмичные АД – 120/80 мм рт. ст., ЧСС – 80 уд. в минуту. Пальпаторно живот безболезненный, мягкий. Печень не увеличена, селезенка не пальпируется. Физиологические отправления: в норме. Периферических отеков не наблюдалось.
В общем анализе крови (ОАК) в динамике нарастала анемия. 18.11.2018 г. – Hb – 129 г/л, 30.11.2018 г. – Hb – 103 г/л, отмечался лейкоцитоз: 18.11.2018 г. – 9 ,2×109/л, 30.11.2018 г. – 11,4×109/л без сдвига лейкоцитарной формулы влево. СОЭ 44–33–18 мм/час. Результаты биохимических исследований сыворотки крови оставались в пределах нормы. В общем анализе мочи – преходящая эритроцитурия 2–8 в поле зрения, белка нет.
По результатам инструментального обследования, полученного после проведения фиброгастродуоденоскопии (ФГДС), колоноскопии, рентгенографии грудной клетки, магнитно-резонансной томографии (МРТ) органов брюшной полости, серьезной патологии обнаружено не было.
УЗИ органов брюшной полости от 20.11.2018 г. Заключение: признаки хронического холецистита.
ЭКГ от 19.11.2018 г.: ритм синусовый регулярный 78 в минуту. Горизонтальная ЭОС. Гипертрофия левого желудочка (ЛЖ). Нарушение процессов реполяризации.
Эхокардиография (Эхо-КГ) от 23.11.2018 г. (сделана впервые через 4,5 месяца от начала заболевания). Заключение: отмечаются эхопризнаки атеросклероза аорты, фиброза створок аортального клапана с его дисфункцией – стенозированием. Гипертрофия миокарда левого желудочка с достаточной сократительной способностью. ФВ – 68%. Умеренная дилатация правого предсердия. Диастолическая дисфункция левого желудочка. Уплотнение створок митрального клапана с его дисфункцией – недостаточностью.
Несмотря на лечение, повторные курсы антибиотиков, которые на время снижали температуру, нарастали слабость, дальнейшая потеря веса, сохранялась выраженная потливость, появились приступы сердцебиения.
Из перенесенных заболеваний отмечает гипертоническую болезнь, повышение артериального давления до 170/100 мм рт. ст. Гипотензивные препараты регулярно не принимает.
Аллергологический анамнез спокойный. Вредных привычек не имеет.
24.12.2018 г. впервые от начала заболевания (около 5 месяцев) была взята кровь на стерильность – роста микроорганизмов не обнаружено.
При осмотре в отделении гастроэнтерологии было обращено внимание на ослабление II тона сердца и появившийся грубый дующий шум в проекции аортального клапана. Была назначена консультация кардиолога.
При клиническом осмотре состояние средней тяжести. Психоэмоциональный статус лабилен. Сознание ясное. Положение активное. Телосложение правильное, достаточного питания. Индекс массы тела (ИМТ) – 28 кг/м². Кожные покровы влажные, чистые, акроцианоза нет. Периферические лимфоузлы при пальпации безболезненные, не увеличены. Грудная клетка обычной формы, безболезненная при пальпации. Тип дыхания: грудной. Дыхание везикулярное, ритмичное, частота дыхания – 16 в минуту. Область сердца не изменена. Верхушечный толчок локальный, совпадает с левой границей сердца. Границы относительной сердечной тупости: правая – IV межреберье по правому краю грудины, левая – на 2 см кнаружи от левой грудино-ключичной линии в V межреберье, верхняя – III межреберье. Тоны сердца приглушены, ритмичные. Во II межреберье справа, вдоль левого края грудины и в V точке выслушивается грубый систоло-диастолический шум, проводящийся на сосуды шеи. Резкое ослабление второго тона. ЧСС – 86 уд/мин. АД – 120/60 мм рт. ст. на обеих руках. Живот при пальпации мягкий, болезненный в эпигастральной области. Печень не выступает из-под края реберной дуги, селезенка не пальпируется. Физиологические отправления: в норме. Периферических отеков нет.
Результаты исследования и их обсуждение
Экстренно было проведено трансторакальное Эхо-КГ обследование.
Эхо-КГ от 20.02.2019 г. Заключение. Стенки аорты уплотнены за счет проявлений атеросклероза. Эхоструктура миокарда левого желудочка неоднородная, гиперэхогенная. Умеренная гипертрофия миокарда левого желудочка. Глобальная сократительная функция миокарда левого желудочка сохранена. ФВ – 66%. Зоны асинергии достоверно не выявлены.
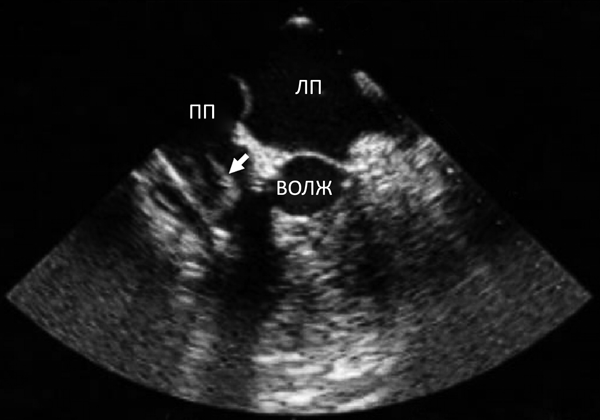
Выраженные изменения аортального клапана: створки утолщены, уплотнены, склерозированы. Распространение процесса на фиброзное кольцо. Расхождение створок ограничено, смыкание створок неполное, в проекции коронарной створки – округлое эхопозитивное образование со стороны выходного тракта левого желудочка, движущееся за створкой, 0,3×0,4 см. Складывается впечатление о разрушении левой коронарной створки. Створки митрального клапана (МК) уплотнены, утолщены. Достоверно дополнительных образований, связанных со структурами МК, не определяется, диастолическое дрожание передней створки МК. Створки трикуспидального клапана и клапана легочной артерии незначительно уплотнены без ограничения подвижности. Полость перикарда без особенностей. Нижняя полая вена не расширена, на вдохе спадается на 50%.
По результатам доплерокардиографии (ДКГ): митральная регургитация 2–3-й степени, трикуспидальная регургитация 1-й степени, регургитация на аортальном клапане 3–4-й степени. Признаков легочной гипертензии нет. Диастолическая функция левого желудочка нарушена по типу замедления релаксации.
Заключение: Атеросклероз аорты, кардиосклероз. Умеренная гипертрофия миокарда левого желудочка. Глобальная сократительная функция миокарда левого желудочка сохранена. Диастолическая функция левого желудочка нарушена по типу замедления релаксации. Данных за легочную гипертензию не выявлено.
Эхо-КГ картина может соответствовать перенесенному острому инфекционному эндокардиту аортального клапана с формированием тяжелой аортальной недостаточности и умеренного стеноза, вторичной выраженной недостаточности митрального клапана.
На ЭКГ от 21.02.2019 г. – ритм синусовый, регулярный. Гипертрофия ЛЖ. Изменения в миокарде.
Впервые был поставлен диагноз: Первичный инфекционный эндокардит подострого течения с поражением аортального клапана, недостаточность аортального клапана III–I V (тяжелой) степени. Хроническая сердечная недостаточность I (II ФК по NYHA).
Больной был переведен в кардиологическое отделение, где трижды исследовалась кровь на стерильность (на аэробные и анаэробные микроорганизмы) – рост микробов не обнаружен.
Проводилась антибактериальная терапия амикацином, метронидазолом, ванкомицином.
Температура сохранялась на субфебрильных цифрах, В анализах крови нарастали анемия, СОЭ, лейкоцитоз. Данные представлены в таблице 1.
Справочник болезней

Инфекционного эндокардита
• Ревматическая болезнь сердца.
• Врожденные (цианотичные) пороки сердца.
• Искусственные клапаны сердца.
• Гемодиализ.
• Венозные катетеры.
• Внутривенное введение препаратов.
• Иммунодепрессанты.
• Пожилой и старческий возраст.
Тромбоэмболий
• Вегетации >10 мм (Mohananey D, et al, 2018).
• Флотирующие вегетации.
• Поражение митрального клапана.
• Инфекция Staph. aureus.
БОЛЬШИЕ КРИТЕРИИ
1. Положительная культура крови
1.1. Типичные микробы в 2 пробах крови:
• Str. viridans, Str. gallolyticus (bovis), Staph. aureus, HACEK группа.
• Внебольничные Enterococci без первичного очага.
1.2. Повторные культуры крови, характерные для ИЭ:
• ≥2 культур крови с интервалом >12 ч.
• Все 3 культуры крови или большинство из ≥4 проб.
1.3. Культура Coxiella burnetti или IgG в титре >1:800.
2. Визуальные признаки
2.1. Эхокардиографические признаки:
• Вегетация,
• Абсцесс, псевдоаневризма, интракардиальная фистула.
• Перфорация или аневризма клапана.
• Новое частичное раскрытие искусственного клапана.
2.2. Аномальная активность возле искусственного клапана по 18Ф-ФДГ ПЭТ/КТ (имплантация >3 мес) или СПЕКТ/КТ сцинтиграфии с меченными лейкоцитами.
2.3. Паравальвулярное повреждение по КТ сердца.
МАЛЫЕ КРИТЕРИИ
1. Предрасполагающие заболевания сердца, инъекции.
2. Лихорадка >38°С.
3. Сосудистые феномены: эмболии крупных артерий, септические инфаркты легких, микотические аневризмы, внутричерепные кровоизлияния, кровоизлияния в конъюнктиву, повреждения Джейуэя.
4. Иммунные нарушения: гломерулонефрит, узелки Ослера, пятна Рота, ревматоидный фактор.
5. Культура крови, не соответствующая большим критериям, или серологические признаки активной инфекции микробом, способным вызвать ИЭ.
Определенный ИЭ = 2 больших, или 1 большой + 3 малых, или 5 малых.
Вероятный ИЭ = 1 большой + 1 малый или 3 малых.
Лечение острого ИЭ до выявления микроба
• Ампициллин + Оксациллин по 12 г/сут в 4 приема в/в + Гентамицин 3 мг/кг однократно в/в, в/м.
• Ванкомицин 30 мг/кг/сут в 2 приема в/в + Гентамицин 3 мг/кг однократно в/в, в/м.
• Ванкомицин 30 мг/кг/сут в 2 приема в/в + Гентамицин 3 мг/кг однократно в/в, в/м + Рифампин 900–1200 мг в 2 приема в/в, per os при нозокомиальном или раннем эндокардите искусственного клапана.
Стрептококк, чувствительный к пенициллину
• Цефтриаксон 2 г однократно или Амоксициллин 100–200 мг/кг/сут в 4 приема в/в [4 нед].
• Цефтриаксон 2 г однократно или Амоксициллин 100–200 мг/кг/сут в 4 приема в/в + Гентамицин 3 мг/кг однократно в/в, в/м [2 нед].
• Ванкомицин 30 мг/кг/сут в 2 приема в/в [4 нед].
Стрептококк, относительно нечувствительный к пенициллину
• Цефтриаксон 2 г однократно или Амоксициллин 200 мг/кг/сут в 4 приема в/в [4 нед] + Гентамицин 3 мг/кг однократно в/в, в/м [2 нед].
• Ванкомицин 30 мг/кг/сут в 2 приема в/в [4 нед] + Гентамицин 3 мг/кг однократно в/в, в/м [2 нед].
• Терапия 6 вместо 4 нед при эндокардите искусственного клапана.
Стафилококк, чувствительный к метициллину
• Оксациллин 12 г/сут в 4 приема в/в [4–6 нед].
• Оксациллин 12 г/сут в 4 приема в/в + Рифампин 900–1200 мг в 2 приема в/в, per os [≥6 нед] + Гентамицин 3 мг/кг однократно в/в, в/м [2 нед] при искусственном клапане.
Стафилококк, нечувствительный к метициллину
• Ванкомицин 30–60 мг/кг/сут в 2 приема в/в [4–6 нед].
• Даптомицин 10 мг/кг однократно в/в [4–6 нед].
• Ванкомицин 30–60 мг/кг/сут в 2 приема в/в + Рифампин 900–1200 мг в 2 приема в/в, per os [≥6 нед] + Гентамицин 3 мг/кг однократно в/в, в/м [2 нед] при искусственном клапане.
Сердечная недостаточность
• Выраженная регургитация или обструкция с симптомами СН или эхокардиографическими признаками нарушенной гемодинамики.
• Отек легких или кардиогенный шок.
Неконтролируемая инфекция
• Локальная: абсцесс, ложная аневризма, фистула, растущие вегетации.
• Инфекция грибами или мультирезистентными микроорганизмами.
• Персистирующая позитивная культура крови, несмотря на адекватную антибиотикотерапию и контроль септических метастатических очагов.
• Эндокардит искусственных клапанов, вызванный стафилококками или не-HACEK грамотрицательными бактериями.
Профилактика эмболий
• Эндокардит аортального или митрального клапанов с персистирующими вегетациями >10 мм после ≥1 эмболического эпизода, несмотря на адекватную антибиотикотерапию.
• Эндокардит аортального или митрального клапанов с изолированными вегетациями >30 мм.
Читайте также:


