При переливании плазмы возможна передача инфекций
М.Н. Губанова, С.Р. Мадзаев, К.С. Аветисян, А.В. Бахметьев, М.В. Зарубин, А.В. Караваев, Е.А. Клюева, А.В. Коденев, К.В. Кузнецов, А.Р. Максимов, У.С. Султанбаев, Н.Г. Филина, К.В. Хальзов, Л.М. Яковлева, Е.Б. Жибурт
Российская ассоциация трансфузиологов
Трансфузиология №4, 2013
Резюме
Определили распространенность и встречаемость инфекций у доноров крови России в 2010-2012 гг. Расчетный остаточный риск трансфузионного инфицирования в 2012 году составил: для ВИЧ – 162; ВГС – 337; ВГВ – 971 на 1 млн донаций. В информационной системе службы крови АИСТ необходимо разделить учет положительных результатов скринингового и подтверждающего тестов на маркеры инфекций. Высокий риск трансфузионного инфицирования ВИЧ, вирусами гепатита В и С стимулирует активное внедрение мер повышения безопасности крови: отбор доноров, повышение чувствительности методов скрининга инфекций, инактивацию патогенов в компонентах крови и рациональное назначение гемотрансфузий в клинике.
Ключевые слова: кровь, донор, переливание, риск, инфекции, ВИЧ, гепатит, распространенность, встречаемость.
Введение
Общепризнано, что, несмотря на все меры безопасности, остаточный риск передачи инфекции с донорской кровью сохраняется из-за серонегативного окна и других особенностей течения инфекционного процесса [1–5].
Распространенность, превалентность – количество случаев определенной болезни в популяции в определенный момент. В трансфузиологии – количество заболеваний у первичных доноров (чаще – в год). Встречаемость, инцидентность –количество случаев заболевания, возникших в течение определенного времени в определенной популяции. В трансфузиологии – выявление заболеваний у регулярных доноров [6]. Остаточный риск передачи гемотрансмиссивных инфекций рассчитывают как произведение продолжительности серонегативного периода инфекции и встречаемости [7]. По со- стоянию на 10.11.2013 указанная статья Schreiber G.B. и соавт. процитирована в 815 публикациях. В соответствии с нормативами Евросоюза ежегодный отчет о деятельности учреждений службы крови должен включать показатели встречаемости и распространенности маркеров гемотрансмиссивных инфекций у доноров крови и ее компонентов [8].
В первой российской публикации о распространенности и встречаемости у доноров крови встречаемость определили как частное количества выявленных инфекций и количества кадровых доноров [9].
В Астане расчетный остаточный риск трансфузионного инфицирования составил: для ВИЧ – 12; ВГС – 1377; ВГВ – 1254 на 1 млн донаций [10].
Представляет интерес определить распространенность и встречаемость инфекций у российских доноров, а также остаточный риск трансфузионного инфицирования.
Материалы и методы
В службе крови России создана информационная система, основанная на программе АИСТ [11, 12]. Разработчик программы А.И. Болотов специально для настоящего исследования создал приложение к программе, позволяющее подсчитать количество выявленных случаев инфекций у первичных и повторных доноров. За что авторы статьи приносят Андрею Исааковичу глубокую благодарность.
В исследовании приняли участие 48 организаций службы крови, представившие результаты обследования 773185 доноров крови и ее компонентов в 2010–2012 гг.
Образец крови от каждой донации обследовали на маркеры 4 гемотрансмиссивных инфекций: вирус иммунодефицита человека (ВИЧ) (антиген р24 ВИЧ-1 и антитела к ВИЧ- 1/2), вирус гепатита В (ВГВ) (поверхностный антиген ВГВ, HBsAg), вирус гепатита C (ВГC) (антитела к ВГС) и сифилис (антитела к бледной трепонеме). Доля доноров, включенных в исследование, составила 9–18% аналогичной категории доноров всей страны [13–15] (табл. 1).
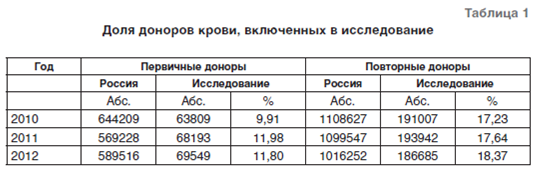
Полученные данные анализировали с использованием дескриптивных статистик и корреляционного анализа при уровне значимости 0,05. При расчете встречаемости инфекций учли, что средняя частота донаций повторных доноров в России составляет 2,4 раза в год [15]. Распространенность рассчитывали на 100000 доноров. Встречаемость рассчитывали на 100000 человеко-лет с учетом средней частоты донаций.
Результаты и обсуждение
Инфекции у доноров
Известно, что АИСТ не формирует установленную [16] российскую отчетную форму организации, заготавливающей кровь, (№39) [17]. Также на результаты исследования могло повлиять разночтение роcсийских правил [18], в которых отсутствует алгоритм выбраковки крови и отвода донора. ВОЗ рекомендует кровь браковать после получения повторного положительного результата скрининга, а донора отводить по положительному результату подтверждающего теста [19].
Высокая частота регистрации ВИЧ-положительных результатов у доноров, включенных в исследование, может быть обусловлена учетом результатов скрининга, а не подтверждающего теста (табл.2).
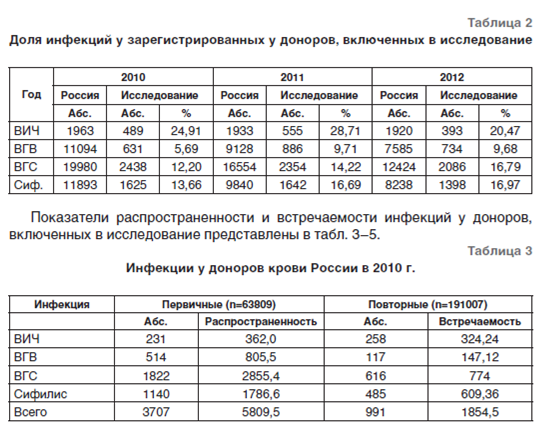
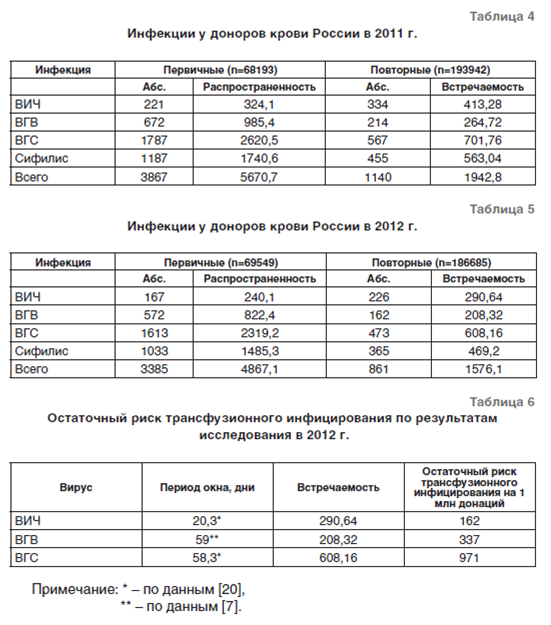
Остаточные риски трансфузионного инфицирования (ОРТИ) вирусами гепатита В (ВГВ), гепатита С (ВГС) и ВИЧ являются основными объективными количественными показателями вирусной безопасности службы крови. Оценки остаточных рисков трансфузионного инфицирования ВГС, рассчитанные на основе анализа данных обследования (скрининга) доноров крови, мониторинга реципиентов множественных трансфузий и контрольного тестирования плазмы крови для производства ее препаратов, аналогичны полученным в настоящем исследовании, и составляют 940, 1600 и 630 на 1 млн кроводач, трансфузий и единиц плазмы соответственно [21].
Рассчитанные классическим способом ОРТИ в США составили: для ВИЧ – 2,03; ВГС – 9,70; ВГВ – 15,83 на 1 млн донаций [7]. По нашим данным, ОРТИ при переливании крови доноров России для ВИЧ, ВГВ и ВГС – соответственно, в 80, 35 и 61 раз выше, чем в США.
Следует подчеркнуть ограниченность нашего исследования: корректный расчет встречаемости может быть основан на учете интервала между предпоследней и последней донациями – в каждом конкретном случае выявления инфекции у регулярного донора. Очевидно, что автоматизация такого учета – важное направление развития информационной системы службы крови России. ОРТИ ВГВ в Казахстане в 3,7 раза, а ВГС – в 1,4 раза выше, чем в России. ОРТИ ВИЧ, напротив, в России в 13,4 раза выше, чем в Казахстане [10], что еще раз подтверждает возможность ошибочной автоматизированной регистрации российской информационной системой службы крови ВИЧ-ложноположительных результатов скрининга донорской крови.
Особо следует отметить необходимость программного определения встречаемости инфекций – с индивидуальной регистрацией периода между серонегативной и серопозитивной донациями.
Показатели донорства, встречаемость и распространенность инфекций в отдельных организациях
Представляет интерес анализ распространенности и встречаемости инфекций как по отдельным организациям, так и по нозологическим формам. Обращает на себя внимание широкий диапазон масштаба организаций, участвующих в исследовании. Так, соотношение верхнего и нижнего квартиля первичных доноров в 2012 году составило 12,8, а повторных доноров – 11,8. При этом 25% наименьших организаций принимали не более двух доноров в день и вероятность попадания инфицированного человека в их число ограничивалась объемом выборки, а возможно и обследованием донорской крови во внешней крупной лаборатории (табл. 7).


Расчет распространенности и встречаемости инфекций у доноров в отдельных организациях проводили без учета частоты донаций повторных доноров, поскольку в каждом отдельном случае этот показатель не регистрируется и неизвестен (табл.8 и 9). Недостоверность данных небольших организаций послужила основанием стратометрического отбора для последующего анализа 24 организаций, количество повторных доноров в которых было выше медианы исходной выборки [22].
Эта группа была более однородной (соотношение верхнего и нижнего квартиля первичных доноров в 2012 году составило 6,2, а повторных доноров – 3,6) и каждая организация в среднем принимала более 10 тысяч доноров ежегодно (табл. 10–12).
В крупных организациях количество первичных доноров положительно коррелирует с количеством повторных доноров (r=0,70; p
Основные факты
- Ежегодно в мире собирается около 117,4 миллиона донаций крови. 42% из них приходится на страны с высоким уровнем дохода, где проживает 16% населения мира.
- В странах с низким уровнем дохода до 52% случаев переливания крови проводится детям в возрасте до 5 лет, в то время как в странах с высоким уровнем дохода переливание крови чаще всего проводится пациентам старше 65 лет — на них приходится до 75% всех случаев переливания крови.
- Число донаций на 1000 человек составляет 32,6 в странах с высоким уровнем дохода, 15,1 в странах со средне-высоким уровнем дохода, 8,1 в странах со средне-низким уровнем дохода и 4,4 в странах с низким уровнем дохода.
- Показатели безвозмездной сдачи крови добровольными донорами возросли в 2015 году на 11,6 миллиона донаций крови по сравнению с показателями 2008 года. В 78 странах национальные запасы крови более чем на 90% обеспечиваются добровольными безвозмездными донорами; однако в 58 странах более 50% национальных запасов крови предоставляют семейные/заместительные или платные доноры.
- Лишь 50 из 173 стран, предоставляющих данные, производят получаемые из плазмы лекарственные средства (ППЛС) путем фракционирования плазмы, собираемой в стране. В общей сложности, 83 страны сообщили, что они импортируют все ППЛС, 24 страны сообщили, что в течение отчетного периода ППЛС не использовались, и 16 стран не ответили на этот вопрос.
Национальная политика и организация деятельности
Переливание крови позволяет спасать человеческие жизни и улучшать здоровье, но многие пациенты, нуждающиеся в переливании, не имеют своевременного доступа к безопасной крови. Обеспечение достаточных запасов безопасной крови должно быть неотъемлемой частью национальной политики и инфраструктуры здравоохранения в каждой стране. По рекомендациям ВОЗ, всю деятельность, связанную со сбором, тестированием, обработкой, хранением и распределением крови, необходимо координировать на национальном уровне в рамках эффективной организации и интегрированной сети банков крови. Национальная система обеспечения крови должна опираться на национальную политику и законодательную базу для достижения единообразного применения стандартов и согласованности в области обеспечения качества и безопасности крови и продуктов крови.
В 2015 году 71% (или 123 из 173) стран имели национальную политику для регулирования деятельности, связанной с кровью. В целом, 60% или (104 из 173) стран имеют специальное законодательство, регулирующее вопросы безопасности и качества переливания крови. Среди них:
- 79% стран с высоким уровнем дохода;
- 55% стран со средним уровнем дохода;
- 45% стран с низким уровнем дохода.
Запасы крови
Ежегодно в мире собирается около 117,4 миллиона донаций крови. 42% из них приходится на страны с высоким уровнем дохода, где проживает 16% населения мира.
Около 12 700 центров крови из 170 стран предоставляют информацию о сборе, в общей сложности, 100 миллионов донаций крови. Количество донаций в центрах крови зависит от уровня дохода стран. В странах с низким уровнем дохода среднегодовое количество донаций на один центр крови составляет 1 300, 4 100 — в странах со средне-низким уровнем доходов, 8 500 — в странах со средне-высоким высоким уровнем доходов по сравнению с 23 000 донаций в странах с высоким уровнем дохода.
Между странами с низким и высоким уровнем дохода имеется значительное различие в уровнях доступа к безопасной крови. Показатель донорства цельной крови является индикатором общего наличия крови в стране. Средний показатель донорства крови в странах с высоким уровнем дохода составляет 32,6 донации на 1000 человек, 15,1 донации на 1000 человек в странах со средне-высоким уровнем доходов и 8,1 донации на 1000 человек в странах со средне-низким уровнем доходов, и 4,4 донации на 1000 человек в странах с низким уровнем дохода.
По сообщениям из 66 стран, в них собирается менее 10 донаций на 1000 человек. 37 из этих стран находятся в регионе Африки ВОЗ, 7 — в регионе Америки ВОЗ, 5 — в регионе Восточного Средиземноморья ВОЗ, 4 — в Европейском регионе ВОЗ, 7 — в Регионе Юго-Восточной Азии ВОЗ и 6 — в Регионе Западной части Тихого океана ВОЗ. Все эти страны с низким и средним уровнем дохода.
Доноры крови
По данным о гендерном профиле доноров крови, в глобальных масштабах 32% донаций крови обеспечивается женщинами, хотя этот показатель варьируется в широких пределах. В 14 из 119 стран, предоставляющих информацию, доноры-женщины предоставляют менее 10% донаций.
Возрастной профиль доноров крови показывает, что пропорционально больше молодых людей сдают кровь в странах с низким и средним уровнем дохода, чем в странах с высоким уровнем дохода. Демографическая информация о донорах крови важна для разработки и мониторинга стратегий по привлечению доноров.
Существуют три типа доноров крови:
- добровольные, сдающие кровь безвозмездно;
- семейные/заместительные;
- платные.
Надлежащие и надежные запасы безопасной крови могут быть обеспечены на устойчивой основе регулярного, добровольного, безвозмездного донорства крови. Такие доноры являются также самой безопасной группой доноров, так как среди них отмечается самый низкий уровень распространенности передаваемых кровью инфекций. Резолюция Всемирной ассамблеи здравоохранения WHA63.12 призывает все государства-члены развивать национальные системы обеспечения крови на основе добровольного безвозмездного донорства крови и работать над достижением цели по самообеспеченности.
Данные, поступившие в ВОЗ, свидетельствуют о значительном увеличении количества добровольных безвозмездных донаций крови в странах с низким и средним уровнем дохода.
- Показатели безвозмездной сдачи крови добровольными донорами возросли в 2015 году на 11,6 миллиона донаций крови в 139 странах по сравнению с показателями 2008 года. Самое значительное увеличение количества добровольных безвозмездных донаций крови наблюдалось в Регионе Юго-Восточной Азии (83%) и регионе стран Америки (70%). Максимальный рост в абсолютных значениях был зарегистрирован в Регионе Юго-Восточной Азии (5,9 миллиона донаций крови), за которым следуют Регион Западной части Тихого океана (2,7 миллиона донаций крови) и регионе стран Африки (1,1 миллиона донаций крови).
- 78 стран обеспечивает более 90% своих запасов крови благодаря добровольным безвозмездным донациям крови (35 стран с высоким уровнем дохода, 32 страны со средним уровнем дохода и 11 стран с низким уровнем дохода), включая 56 стран, где этот показатель составляет около 100% (или более 99%) своих запасов крови благодаря добровольным безвозмездным донациям крови.
- В 58 странах более 50% запасов крови все еще обеспечивается семейными/заместительными или платными донорами (8 стран с высоким уровнем дохода, 36 стран со средним уровнем дохода и 14 стран с низким уровнем дохода).
- В 2015 году 19 стран все еще сообщали о сборе платных донаций: примерно 370 000 донаций, в общей сложности.
Скрининг крови
По рекомендациям ВОЗ, все донации крови до их использования необходимо проверять на присутствие инфекций. Скрининг на ВИЧ, гепатит В, гепатит С и сифилис должен быть обязательным. Скрининг крови необходимо проводить в соответствии с требованиями системы по обеспечению качества.
- 13 стран из стран, предоставляющих информацию, не могут проверять все донации крови на одну или более из вышеперечисленных инфекций.
- Нерегулярные поставки комплектов для тестирования являются одним из наиболее часто сообщаемых препятствий для скрининга.
- В странах с высоким уровнем дохода 99,8% донаций проверяются в соответствии с основными процедурами проверки качества, по сравнению с 99,9% в странах со средне-высоким уровнем дохода, 83,2% в странах со средне-низким уровнем дохода и 76,2 % в странах с низким уровнем дохода.
- Показатели распространенности передаваемых при переливании инфекций (ППИ) в донациях крови в странах с высоким уровнем дохода значительно ниже аналогичных показателей в странах со средним и низким уровнем дохода (Таблица 1).
| ВИЧ | Вирус гепатита В | Вирус гепатита С | Сифилис | |
| Cтраны с высоким уровнем дохода | 0.002% | 0.02% | 0.02% | 0.02% |
| (0.004% – 0.02%) | (0.008% – 0.08%) | (0.005% – 0.11%) | (0.006% –0.14%) | |
| Cтраны со средне-высоким уровнем доходов | 0.10% | 0.36% | 0.24% | 0.44% |
| (0.02% – 0.22%) | (0.18% – 0.73%) | (0.05% – 0.38%) | (0.12% –1.09%) | |
| Cтраны со средне-низким уровнем доходов | 0.14% | 2.27% | 0.39% | 0.70% |
| (0.03% – 0.6944%) | (0.80% – 4.87%) | (0.18% –0.95%) | (0.19% – 1.27%) | |
| Страны с низким уровнем дохода | 0.86% | 3.64% | 0.93% | 0.60% |
| (0.39% – 2.40%) | (2.55% – 8.59%) | (0.50% – 1.95%) | (0.30% – 1.63%) |
Эти различия отражают уровни распространенности среди населения, отвечающего критериям донорства крови, тип доноров (например, добровольные, не получающие вознаграждения доноры крови из групп населения низкого риска) и эффективность системы разъяснительной работы и отбора доноров.
Обработка крови
Запасы получаемых из плазмы лекарственных средств
Резолюция Всемирной ассамблеи здравоохранения WHA63.12 призывает государства-члены к разработке, осуществлению и поддержке координируемых в национальных масштабах, эффективно управляемых и устойчивых программ по крови и плазме в соответствии с наличием ресурсов с целью достижения самообеспеченности. Правительства стран несут ответственность за обеспечение достаточных и справедливых запасов получаемых из плазмы лекарственных средств, а именно иммуноглобулинов и факторов коагуляции, необходимых для предотвращения и лечения целого ряда серьезных состояний, которые происходят во всем мире.
Только 50 из 173 стран, предоставляющих информацию, производят получаемые из плазмы лекарственные средства (ППЛС) путем фракционирования плазмы, собранной в стране. В общей сложности, 83 стран сообщили, что они импортируют все ППЛС, 24 стран сообщили, что в течение отчетного периода ППЛС не использовались, и 16 стран не ответили на этот вопрос.
Около 16,1 миллиона литров плазмы из 41 страны, предоставляющих информацию было фракционировано для производства ППЛС на протяжении года. Это количество включает около 36% плазмы, полученной из донаций цельной крови.
Клиническое использование крови
Из-за проведения переливаний крови, не являющихся необходимыми, и применения небезопасных методик переливания пациенты подвергаются риску развития тяжелых неблагоприятных реакций на переливание и приобретения передаваемых при переливании инфекций. К тому же, переливания, не являющиеся необходимыми, уменьшают запасы продуктов крови для пациентов, нуждающихся в них.
По рекомендациям ВОЗ, все страны должны иметь комитеты по переливанию крови для осуществления национальной политики и руководящих принципов по рациональному использованию крови в больницах и национальную систему гемонадзора для мониторинга и улучшения безопасности процесса переливания. В этой связи:
- 124 страны имеют национальные руководящие принципы по надлежащему клиническому использованию крови: 32 страны в Регионе Африки (71% стран, предоставляющих информацию в этом регионе), 17 стран в Регионе стран Америки (50%), 14 стран в Регионе Восточного Средиземноморья (74%), 34 страны в Европейском регионе (83%), 10 стран в Регионе Юго-Восточной Азии (91%) и 17 стран в Регионе Западной части Тихого океана (74%).
- Комитеты по переливанию крови имеются в 45% больниц, осуществляющих переливание: 12% больниц, осуществляющих переливание, в Регионе Африки, 17% в Регионе стран Америки, 57% в Регионе Восточного Средиземноморья, 68% в Европейском регионе, 79% в Регионе Юго-Восточной Азии и 40% в Регионе Западной части Тихого океана.
- Системы информирования о неблагоприятных реакциях на переливание имеются в 34% больниц Региона Африки, 81% больниц Региона стран Америки, 64% больниц в Регионе Восточного Средиземноморья, 86% больниц в Европейском регионе, 80% больниц в Регионе Юго-Восточной Азии и 38% больниц в Регионе Западной части Тихого океана.
- 46% стран, предоставляющих информацию, имеют систему гемонадзора. Наиболее высокую процентную долю стран, имеющих систему гемонадзора, имеет Европейский регион (76%), за которым следуют Регион Восточного Средиземноморья (53%), Регион Западной части Тихого океана (48%), Регион Африки (38%), Регион Юго-Восточной Азии (36%) и Регион стран Америки (21%).
Переливание крови
Между странами наблюдаются большие различия в распределении пациентов, которым делается переливание, по возрастным группам. Так, например, в странах с высоким уровнем дохода группой пациентов, которой наиболее часто переливается кровь, являются люди старше 65 лет — на них приходится 75% всех переливаний. В странах с низким уровнем дохода до 52% переливаний проводится детям в возрасте до 5 лет.
В странах с высоким уровнем дохода переливание чаще всего проводится в качестве поддерживающей терапии при проведении сердечно-сосудистых хирургических операций и трансплантации органов, а также в случае тяжелых травм и солидных и гематологических злокачественных опухолей. В странах с низким и средним уровнем дохода его чаще всего проводят в случае осложнений, связанных с беременностью, и при тяжелой детской анемии.
Деятельность ВОЗ
В связи с риском передачи серьезных инфекций, включая ВИЧ и гепатит, через небезопасную кровь и хроническим дефицитом крови внимание глобального сообщества привлечено к важности обеспечения безопасности и наличия крови. Выдвинув цель по достижению всеобщего доступа к безопасным крови и продуктам крови, ВОЗ возглавляет усилия по улучшению безопасности и наличия крови и рекомендует следующую комплексную стратегию по обеспечению безопасности и наличия крови:
- Создание национальной системы обеспечения крови с хорошо организованными и координированными службами переливания крови, проведение эффективной, основанной на фактических данных и учитывающей этические принципы национальной политики для регулирования деятельности, связанной с кровью и введение законодательства и регулирования, которые могут обеспечить достаточные и своевременные поставки безопасной крови и ее продуктов для удовлетворения потребностей всех пациентов в переливании.
- Сбор крови, плазмы и других компонентов крови от регулярных, добровольных и не получающих вознаграждения доноров из группы низкого риска путем укрепления систем донорства и эффективного обращения с донорами, включая медицинскую помощь и консультирование.
- Скрининг гарантированного качества всей донорской крови на передаваемые при переливании инфекции, включая ВИЧ, гепатит В, гепатит С и сифилис, подтверждающее тестирование всех донаций с реакцией на маркеры инфекции, тестирование на группу крови и совместимость и создание систем переработки крови в продукты крови (компоненты крови для переливания и получаемые из плазмы лекарственные средства), в соответствующих случаях, для удовлетворения потребностей здравоохранения.
- Рациональное использование крови и ее продуктов для уменьшения числа переливаний, не являющихся необходимыми, и минимизации рисков, связанных с переливанием, использование вариантов, альтернативных переливанию, там, где это возможно, и безопасная и надлежащая клиническая практика переливания, включая правильное обращение с кровью пациентов.
- Поэтапное введение эффективных систем обеспечения качества, включая управление качеством, стандарты, надлежащую практику производства, документацию, специальную подготовку всего персонала и оценку качества.
В рамках своей Программы по обеспечению безопасности переливания крови ВОЗ поддерживает страны в развитии их национальных систем крови в целях обеспечения своевременного доступа к достаточным запасам безопасных крови и продуктов крови и в разработке надлежащих практических методик переливания для удовлетворения потребностей пациентов. Программа предоставляет руководство для проведения политики и оказывает техническую помощь странам для обеспечения всеобщего доступа к безопасным крови и продуктам крови и продвижения к самообеспеченности запасами безопасных крови и продуктов крови на основе добровольного безвозмездного донорства крови с целью обеспечения всеобщего охвата медико-санитарными услугами.
Источник данных: Настоящий информационный бюллетень основан на данных за 2015 год, полученных через Глобальную базу данных ВОЗ о безопасности крови (ГБДБК) из 139 стран. Для предоставления более полного обзора глобальной ситуации использовались данные за 2014 год, полученные из 17 стран, из 17 стран были использованы данные за 2013 год. В общей сложности, информация получена из 173 стран, где проживает 98,03% населения мира.
Какой метод является наиболее эффективным в профилактике кровотечений у пациентов с раком крови или костного мозга, получающих интенсивную химиотерапию? Следует ли переливать тромбоциты (существующее стандартное лечение) или использовать вместо этого (или наравне с этим) другие средства?
Приблизительно каждое восьмое злокачественное новообразование поражает кровь, костный мозг или лимфатические узлы. Эти злокачественные новообразования подразделяются на множество различных типов, каждый из которых требует особого лечения. Среди примеров – острый миелоидный лейкоз и лимфома. Некоторые из этих заболеваний могут быть вылечены с помощью высокодозной (интенсивной) химиотерапии или трансплантации стволовых клеток. Такое лечение помогает в борьбе с опухолями, однако также может повредить нормальные кроветворные клетки. Одно из последствий этого – снижение числа тромбоцитов в крови. Тромбоциты необходимы для нормального свертывания крови. В результате, люди, получающие подобное лечение, подвержены кровотечениям до тех пор, пока уровень тромбоцитов у них не повысится.
Переливание тромбоцитов донора часто проводится пациентам с раком крови для профилактики кровотечений. Мы не знаем, насколько эффективно переливание тромбоцитов. Мы знаем, что переливание тромбоцитов связано с определенными рисками, такими как передача инфекций. Возможно, есть лучшие способы предотвращения кровотечений в этих условиях. В этом обзоре мы изучили, возможно ли для профилактики кровотечений использовать другие средства вместо переливания тромбоцитов (или наравне с ним). Мы также оценили риск серьезных побочных эффектов, таких как образование аномальных кровяных сгустков (тромбоэмболических осложнений). Среди потенциальных средств были искусственные тромбоциты, бедная тромбоцитами плазма, концентрат фибриногена, рекомбинантный активированный фактор VII, десмопрессин и миметики тромбопоэтина. Термины и вмешательства описаны в глоссарии в разделе "Опубликованные примечания" этого обзора.
Доказательства актуальны на май 2016 года. Мы нашли 16 клинических испытаний: 10 завершенных и шесть продолжающихся. В этот обзор мы включили 10 завершенных испытаний. В шести испытаниях участвовали взрослые с острым миелоидным лейкозом, получавшие интенсивную химиотерапию; в двух испытаниях – взрослые с лимфомой, получавшие интенсивную химиотерапию; и еще в двух испытаниях – взрослые, которым проводилась аллогенная трансплантация стволовых клеток. Возраст участников варьировал от 16 лет до 81 года. В испытаниях в равной степени принимали участие и мужчины, и женщины. Все испытания были проведены в странах с высоким уровнем доходов. В восьми испытаниях спонсором был производитель исследуемых средств; в двух испытаниях об источниках финансирования не сообщали. Мы нашли девять испытаний (536 участников), в которых изучали миметики тромбопоэтина, и одно испытание (18 участников), в котором изучали бедную тромбоцитами плазму. Эти испытания были проведены в период с 1974 по 2015 годы. Ни в одном из испытаний не рассматривали искусственные тромбоциты, концентрат фибриногена, рекомбинантный активированный фактор VII или десмопрессин.
В отношении взрослых, у которых применяли миметики тромбопоэтина, мы не можем с уверенностью сказать, имеются ли различия в числе участников по таким показателям, как любые кровотечения, риск жизнеугрожающего кровотечения, число переливаний тромбоцитов, общий риск смерти или тромбоэмболические осложнения, так как качество доказательств было очень низким. Мы не нашли испытаний миметиков тромбопоэтина, в которых рассматривали: число дней, в которые возникали кровотечения; время с начала испытания до первого кровотечения или качество жизни.
В отношении взрослых, получавших бедную тромбоцитами плазму, – мы крайне не уверены в том, имелись ли между участниками различия по таким показателям, как любые кровотечения или риск жизнеугрожающего кровотечения. Мы не нашли испытаний, в которых рассматривали: число дней, в которые возникали кровотечения; время с начала испытания до первого кровотечения; число переливаний тромбоцитов; общий риск смерти; тромбоэмболические осложнения или качество жизни.
Качество доказательств было очень низким, что не позволило нам сделать однозначные выводы или дать рекомендации относительно эффективности и безопасности миметиков тромбопоэтина или бедной тромбоцитами плазмы. Мы не нашли испытаний, в которых изучали искусственные тромбоциты, концентрат фибриногена, рекомбинантный активированный фактор VII или десмопрессин.
Читайте также:


