Патологическая анатомия при геморрагической лихорадке с почечным синдромом
Геморрагические лихорадки — группа острых инфекционных заболеваний с лихорадочными реакциями и разнообразными геморрагиями. Эти лихорадки подразделяются на отдельные нозологические формы по характеру клинического течения, особенностям возбудителя и в соответствии с географической областью распространения, обусловленной природной очаговостью этих болезней.
Известны, в частности, следующие геморрагические лихорадки: а) геморраг'ичес'кая лихорадка с почечным синдромом, называемая также геморрагическим нефрозо-нефритом, или дальневосточной геморрагической лихорадкой; б) крымская геморрагическая лихорадка; в) омская геморрагическая лихорадка.
В изучении геморрагических лихорадок важный вклад был сделан советским ученым М. П. Чумаковым и рядом других исследователей.
Этиология и эпидемиология. Каждое из перечисленных выше заболеваний вызывается особым видом фильтрующегося вируса, имеет определенные природные очаги инфекци'и, определенные резервуары и переносчиков вируса (клещи различных видов). Механизм заражения человека каждым из них отличается некоторыми особенностями.
Вирусологическая характеристика возбудителей данной группы инфекционных болезней разработана еще недостаточно полно. Природная очаговость геморрагических лихорадок целиком зависит от определенных климатических, географических и иных условий, благоприятствующих существованию переносчиков инфекции.
Патогенез и патологическая анатомия. Важнейшие проявления болезни связаны с тяжелым поражением капилляров в различных органах, коже и слизистых оболочках. Для дальневосточной геморрагической лихорадки характерно развитие тяжелых поражений клубочков и канальцевой cefn почек.
Клиническая картина. Вследствие сходства клинических проявлений отдельных заболеваний, входящих в данную группу, необходимо рассматривать их в сопоставлении.
1. Геморрагический дальневосточный нефрозонефрит (геморрагическая лихорадка с почечным синдромом) характеризуется симптомами тяжелого поражения почек (артериальное кровяное давление при этом может повышаться незначительно) с выраженным патологическим характером мочи (белок, эритроциты, цилиндры). Продолжительность инкубационного периода составляет в среднем 15 дней с колебаниями от 11 до 23 дней.
В самом начале заболевания отмечается продромальный период, который больные обычно переносят на ногах (общая слабость, недомогание, снижение аппетита).
Лихорадочный период начинается ознобом и быстрым повышением температуры до 39,5—40,5°, сохраняющимся в течение 2—6 дней.
Продолжительность начального периода болезни от повышения температуры и до первых геморрагических проявлений составляет 2—4 дня; преобладают общетоксические явления с наличием в ряде случаев менингеальных симптомов.
Жалобы больных касаются головной боли, ощущения жара, болей в мышцах и пояснице. Сознание у больного нередко спутано, отмечаются положительные с'имптомы Кернига и Брудзинского, ригидность затылочных мышц. Лицо больного гиперемировано, сосуды конъюнктивы век и склер инъецированы кровью. Рано выявляются признаки поражения почек (боли в пояснице, положительный симптом Пастернацкого), хотя выраженные симптомы почечной патологии возникают позднее.
Картина крови характеризуется лейкопенией, анэозинофи-лией и палочкоядерным сдвигом нейтрофилов влево.
Спинномозговая жидкость при пункции вытекает под повышенным давлением и содержит увеличенное количество белка.
Начиная с 3—5-го дня болезнь вступает в период своего разгара: состояние больных ухудшается; отмечается рвота, возникают кровотечения из носа и десен, на боковых поверхностях грудной клетки и в области плечевого пояса на коже появляется петехиальная сыпь. Больной в этом периоде вял, апатичен, жалуется на головную боль, резкие боли в пояснице и животе; нередко сознание затемнено.
На слизистых оболочках неба и нижней губы заметна энантема (точечные кровоизлияния), возможны также кровоизлияния в склеры (64), а в тяжелых случаях — апоплексия надпочечников. Резко выражены признаки геморрагического диатеза, увеличивается ломкость капилляров. В описываемый период болезни, по крайней мере с 4-го дня, картина крови характеризуется умеренной гипохромной анемией, небольшим лейкоцитозом и незначительным нейтрофилезом со сдвигом влево. В лихорадочном периоде характерна тром-боцитопен'ия. Симптом Пастернацкого резко положительный, отмечается олигурия, достигающая иногда состояния полной анурии; характерны низкий удельный вес мочи (1008—1002), гематурия, альбуминурия. Количество белка в моче может достигать 20—24%; моча имеет цвет мясных помоев (благодаря макрогематурии).
Лихорадочный период при геморрагической лихорадке с почечным синдромом продолжается около 8—9 дней при снижении температуры в конце его ускоренным лизисом за 2—• 3 дня.
После нормализации температуры общее состояние больного все же остается тяжелым, наблюдается повторная рвота, а нарушения со стороны почек даже прогрессируют: развивается анурия, значительная альбуминурия и гематурия, в моче, имеющей очень низкий удельный вес, обнаруживают восковидные, зернистые и фибринные цилиндры.
Остаточный азот в крови значительно повышен, возможна уремия, иногда ведущая к летальному исходу. Повышение остаточного азота возможно в пределах до 150—200 мг%. Начиная с 4—6-го дня после нормализации температуры состояние больного становится лучше и он поправляется. Картина крови нормализуется через 3—4 дня после снижения температуры, альбуминурия ликвидируется к 12— 14-му дню от начала болезни, но цилиндры, в том числе фибринные, могут обнаруживаться в моче и более длительный период. В периоде реконвалесценции наблюдается полиурия. В большинстве случаев наступает выздоровление, но прогноз болезни может быть очень серьезным, а иногда она заканчивается смертью больного. Летальность варьирует в очень широких пределах; при тяжелых формах болезни она достигает высоких показателей.
2. Крымская геморрагическая лихорадка, впервые изученная М. П. Чумаковым и его сотрудниками летом 1944 г. в степных районах Крыма, — острое инфекционное заболевание, которое начинается внезапно с озноба, рвоты, голодной боли, значительного повышения температуры. Лицо гиперемировано, отмечается инъекция сосудов конъюнктивы век и склер глаз, мягкого неба и языка. Начиная с 4—5-го дня болезни возникает ряд геморрагических симптомов: петехиальные высыпания на коже и слизистых оболочках, носовые кровотечения, рвота и стул с пр'имесью крови, гематурия; у многих больных кровоточат десны, у женщин появляются маточные кровотечения. При исследовании больных отмечается лабильность пульса, приглушение тонов сердца и артериальная гипотония. Селезенка увеличивается лишь у части больных. Тяжелые случаи болезни сопровождаются резкой сухостью во рту, болями в животе, повторным жидким стулом, содержащим примесь крови; большей частью кровь изменяется в кишечнике, превращаясь в мелену.
В морфологии крови наиболее характерен сдвиг влево нейт-рофильных клеток при умеренно выраженном лимфоцитозе и нормальной скорости РОЭ. Общее количество лейкоцитов остается в пределах нормы и лишь у отдельных больных может слегка повышаться.
3. Омская геморрагическая лихорадка характеризуется менее выраженными, чем при первых двух болезненных формах, геморрагическими явлениями и протекает достаточно благоприятно. Но и она может давать летальные исходы. Температура в первые дни болезни повышается до 39—39,5°. У половины больных наблюдаются две лихорадочные волны, разделенные безлихорадочным периодом, который продолжается от 3 до 10 дней.
Распознавание отдельных форм геморрагических лихорадок возможно на основании клинической картины болезни и наличия эпидемиологических данных (распространение болезни в данной местности, ее природная очаговость). Лабораторная диагностика сложна и возможна лишь в хорошо оборудованной лаборатории.
Лечение. Все больные должны быть госпитализированы и за ними необходим тщательный уход. Назначают полужидкую, легкоусвояемую и калорийную пищу с максимальным обогащением диеты витаминами, особенно С 'и В (свежие овощи и фрукты, натуральные фруктовые и ягодные соки, настой шиповника, дрожжи). Рекомендуется давать больному до 600—800 мг аскорбиновой кислоты внутрь ежедневно, витамин Р; ввиду наличия геморрагических явлений назначать витамин К (викасол) по 0,015 г 4 раза в день на протяжении 4 дней.
Следует иметь в виду, что геморрагические проявления могут достигнуть наибольшего развития не в л'ихорадочном периоде болезни, а после его окончания.
Применяют также внутривенные вливания глюкозы (40% раствор по 40—50 мл ежедневно). В лихорадочном периоде болезни рекомендуются переливания крови по 125—150 мл через день, внутримышечные инъекции камполона или анти-анемина (по 2 мл ежедневно на протяжении 5—7 дней), прёпараты железа внутрь. В качестве вспомогательного терапевтического средства дают внутрь десенсибилизирующий (анти-гистаминный) препарат димедрол по 0,08 г 4 раза в день в течение 4—6 дней. Выздоравливающий нуждается в постельном режиме до полного исчезновения клинических симптомов; после выписки необходимо медицинское наблюдение. Прогноз. Тяжесть клинического течения геморрагических лихорадок колеблется в очень широких пределах. Дальневосточный нефрозо-нефрит протекает значительно тяжелее, чем другие описанные здесь геморрагические лихорадки, и в отдельных случаях заканчивается летально.
Профилактика. Успех борьбы с распространением геморрагических лихорадок определяется в первую очередь результатами мероприятий по уничтожению переносчиков инфекции и по защите от их укусов здоровых людей. В местностях, где встречаются заболевания, необходима тщательная расчистка земельного участка под жилые и производственные помещения: скашивание травы, уничтожение кустарника, сжигание опавших листьев.
Лица, работающие или проживающие в местностях, где встречаются геморрагические лихорадки, должны носить сапоги, перчатки, а также специальные комбинезоны; обязательна пропитка производственной одежды препаратами, отпугивающими клещей. Необходимость проведения этих мероприятий зависит от конкретной эпидемиологической обстановки. Перечисленные средства обеспечивают защиту человека от укусов зараженных клещей, являющихся переносчиками геморрагических лихорадок.
С целью специфической профилактики омской геморрагической лихорадки в природных очагах этой болезни применяют профилактическую вакцинацию населения при помощи эмульсии вируса, убитого формалином (прививки производят по специальной инструкции).
Основная роль в профилактике геморрагических лихорадок принадлежит все же не вакцинации, а систематическому осуществлению указанных выше мероприятий.
Геморрагическая лихорадка с почечным синдромомявляется одной из разновидностей геморрагических лихорадок.
Геморрагические лихорадки- это острые инфекционные заболевания вирусной природы, характеризующиеся токсикозом, лихорадкой и геморрагическим синдромом.
ГЛПС- это острое вирусное природно-очаговое заболевание, протекающее с высокой лихорадкой, выраженной общей интоксикацией, геморрагическим синдромом и своеобразным поражением почек в виде нефрозонефрита.
Этиология.Возбудители ГЛПС - вирусы рода Hantaan, семейства Bunyavindae. Вирионы округлой формы, диаметром 85-110 нм, геном представлен РНК.
Эпидемиология. ГЛПС - природно-очаговый вироз. Резервуаром вирусов является грызуны и насекомоядные животные, у которых наблюдаются латентные формы инфекции. Выделение вируса во внешнюю среду происходит преимущественно с мочой грызунов, реже с их фекалиями или слюной.
Пути передачи инфекции человеку - воздушно-пылевой, алиментарный и контактный. Заболеваемость носит спорадический характер, возможны и групповые вспышки. Заболевание характеризуется выраженной сезонностью: максимум заболеваемости регистрируется с мая по ноябрь с подъемом в июне - сентябре, что обусловлено нарастанием численности грызунов, частыми посещениями леса, сельскохозяйственными работами, а также в ноябре-декабре, что связано с миграцией грызунов в жилые помещения и переработкой сельскохозяйственной продукции. После перенесенной инфекции формируется стойкий иммунитет. Повторные заболевания наблюдаются редко.
Патогенез.Входные ворота инфекции - поврежденная кожа и слизистые оболочки. В организме вирус захватывается макрофагами, в которых происходит его репликация. Затем вирус выходит в кровь и развивается фаза вирусемии, которая обусловливает начало болезни с развитием симптомов общей интоксикации.
Обладая вазотропным действием, вирус повреждает стенки кровеносных капилляров как непосредственно, так и в результате повышения активности гиалуронидазы с деполяризацией основного вещества сосудистой стенки.
В результате повреждения сосудистой стенки уменьшается ОЦК, повышается вязкость крови, что приводит к расстройству микроциркуляции и способствует возникновению микротромбов. Следствием развившегося ДВС-синдрома являются геморрагический синдром, проявляющийся геморрагической сыпью и кровотечениями.
Наиболее выраженные изменения развиваются в почках. Возникает серозно-геморрагический отек сосудов, который сдавливает канальцы и собирательные трубочки и способствует развитию десквамативного нефроза. Снижается клубочковая фильтрация, нарушается канальцевая реабсорбция, следствием чего является олигоанурия, выраженная протеинурия, азотемия и метаболический ацидоз. Массивная десквамация эпителия и отложение фибрина в канальцах приводят к развитию обструктивного сегментарного гидронефроза.
Клиника. Ведущими симптомами ГЛПС являются высокая лихорадка, гиперемия и одутловатость лица, возникновение с 3-4-го дня болезни геморрагического синдрома и нарушения функции почек в виде олигурии, массивной протеинурии и азотемии с последующей полиурией. Болезнь характеризуется циклическим течением и многообразием клинических вариантов. Инкубационный период ГЛПС длится от 4 до 49 дней, чаще 14-21 день.
В течении болезни выделяют четыре периода:
- лихорадочный (1-4-й день болезни);
- олигурический (4-12-й день);
- полиурический (с 8-12-го по 20-24-й день);
Заболевание начинается остро, с повышения температуры тела до 38,5-40 °С, появления мучительных головной и мышечных болей, жажды, сухости во рту. После снижения температуры через несколько дней она вновь повышается до субфебрильных цифр - "двугорбая" температурная кривая.
При осмотре отмечают одутловатость и гиперемию лица, инъекцию сосудов склер и конъюнктив, гиперемию зева.
Со 2-3-го дня болезни на слизистой оболочке мягкого неба появляются геморрагическая энантема, а с 3-4-го дня - петехиальная сыпь в подмышечных впадинах, на груди, иногда на шее и лице. Сыпь может быть в виде полос, напоминающих удар хлыста. Наряду с этим появляются крупные кровоизлияния в кожу, склеры, в места инъекций. Затем возможны носовые, маточные, желудочные кровотечения, которые могут быть причиной летального исхода.
Пульс в начале болезни соответствует температуре, затем развивается выраженная брадикардия. Границы сердца в норме, тоны приглушены. Артериальное давление, как правило, понижено. При тяжелом течении болезни развивается инфекционно-токсический шок. Нередко появляются симптомы бронхита, бронхопневмонии.
С 3-4-го дня болезни на фоне выраженной лихорадки начинается второй, олигурический период. Состояние больных заметно ухудшается. Появляются сильные боли в поясничной области, вследствие чего больной занимает вынужденное положение. Головные боли усиливаются, возникает повторная рвота, приводящая к обезвоживанию организма. Часто возникают носовые и желудочно-кишечные кровотечения, кровохарканье. Количество мочи уменьшается до 300-500 мл в сутки, в тяжелых случаях возникает анурия.
Отмечаются брадикардия, гипотензия, тахипноэ. Пальпация области почек болезненна (осмотр должен проводиться осторожно ввиду возможного разрыва почечной капсулы при грубой пальпации). С 6-7-го дня болезни температура тела снижается, однако состояние больных ухудшается. При осмотре отмечается бледность кожи, акроцианоз, выраженные признаки геморрагического синдрома. Состояние больного ухудшается вплоть до развития комы.
С 9-13-го дня от начала заболевания наступает полиурический период. Состояние больных заметно улучшается: прекращаются тошнота, рвота, появляется аппетит, диурез увеличивается до 5-8 л, характерна никтурия. Больные жалуются на слабость, жажду, одышку, сердцебиение даже при небольшой физической нагрузке. Боли в пояснице уменьшаются, но сохраняются. Характерна длительная гипоизостенурия.
В период реконвалесценции полиурия уменьшается, постепенно наступает восстановление функций организма.
В зависимости от выраженности симптомоввыделяютлегкую, средней тяжестиитяжелую формызаболевания.
Осложнения. Могут развиваться инфекционно-токсический шок, отек легких, уремическая кома, эклампсия, разрыв почки, кровоизлияния в мозг, надпочечники, миокард, поджелудочную железу, массивные кровотечения. Возможны также пневмонии, абсцессы, флегмоны, паротит, перитонит.
Геморрагическая лихорадка с почечным синдромом (геморрагический нефрозо‑нефрит)
Вирусная природа болезни установлена А. А. Смородинцевым в 1940 г. и подтверждена М. П. Чумаковым в 1956 г., однако вирус до настоящего времени не изолирован. Американские исследователи Ч. В. Ли и П. В. Ли в 1976–1977 гг. в Корее методом иммунофлюоресценции выявили вирусный агент в легких полевых мышей Apodemusagrarius .
Возбудители ГЛПС – вирусы рода Hantaan , семейства Bunyaviridae – относятся к сферическим РНК‑содержащим вирусам диаметром 85‑110 нм (группа арбовирусов).
ГЛПС – природно‑очаговая инфекция. Резервуар вирусов – несколько видов полевок, полевые мыши, лесные мыши, лемминги и другие грызуны. Заражение человека осуществляется в природных очагах контактно‑бытовым, алиментарным или аэрогенным (при вдыхании пыли, содержащей инфицированные экскременты грызунов) путем.
Резервуаром вирусов на территории СНГ являются 16 видов грызунов и 4 вида насекомоядных животных, у которых наблюдаются латентные формы инфекции. Вирус выделяется во внешнюю среду с мочой грызунов, реже с фекалиями или слюной. Среди животных наблюдается трансмиссивная передача вируса гамазовыми клещами и блохами. От грызунов человеку в естественных или лабораторных условиях вирус передается воздушно‑пылевым, алиментарным и контактным путями. Заболеваемость носит спорадический характер, возможны и групповые вспышки. Заболеваемость имеет четкую сезонность (с мая по октябрь). Иммунитет после перенесенной болезни довольно стойкий.
Спорадическая заболеваемость геморрагической лихорадкой с почечным синдромом регистрируется на протяжении всего года, преимущественно среди сельских жителей, чаще у мужчин. Групповые заболевания отмечаются летом и осенью (особенно часто в июне и октябре, что связано с более частым посещением людьми территории природного очага и миграцией грызунов в населенные пункты).
Патогенез и патологическая анатомия .
На аутопсии во внутренних органах выявляют дистрофические изменения, серозно‑геморрагический отек и кровоизлияния. Почки увеличены в объеме, дряблые. Капсула их легко снимается, под ней обнаруживаются кровоизлияния. Корковое вещество бледное, выбухает над поверхностью разреза, мозговой слой багрово‑красный, с множественными кровоизлияниями в пирамидках и лоханках, имеются очаги некроза. При микроскопическом исследовании мочевые канальцы расширены, просвет их заполнен цилиндрами, собирательные трубочки нередко сдавлены и деструктивно изменены, эпителий перерожден и десквамирован. Обнаруживают также дистрофические изменения клеток многих органов, желез внутренней секреции и вегетативных ганглиев.
Длительность инкубационного периода колеблется от 4 до 43 дней, но чаще она составляет 2–3 недели. Болезнь отличается цикличностью. В ее течении различают 4 стадии:
– лихорадочную (1‑5‑6‑й день болезни); – олигурическую (с 5‑6‑го по 8‑12‑й день); – полиурическую (с 8‑12‑го по 20‑24‑й день); – стадию реконвалесценции.
При осмотре больных в этой стадии выявляются яркая гиперемия лица, шеи и верхних отделов груди, инъекция сосудов склер и конъюнктивы, выраженная гиперемия зева и обложенность языка. Пульс вначале учащен, затем развивается относительная брадикардия, понижается артериальное давление, приглушаются сердечные тоны. Часто отмечаются явления бронхита или пневмонии. Пальпация живота чувствительна в подреберьях. Может определяться увеличение печени и селезенки.
На 2‑3‑й день болезни можно обнаружить геморрагическую энантему на твердом небе, а на 3‑4‑й день появляется петехиальная сыпь в подмышечных областях и на боковых отделах туловища, иногда в виде полос. В последующие дни может развиться пурпура, а при тяжелом течении болезни – экхимозы. Симптом щипка постоянно положителен.
В последние дни начального периода состояние больных заметно ухудшается. Нарастают явления интоксикации, появляется многократная рвота, может развиться менингеальный синдром. Более выраженными становятся признаки геморрагического синдрома. Обнаруживаются кровоизлияния в склеры, возможны носовые кровотечения.
На 6‑9‑й день болезни температура обычно понижается кризолитически до субфебрильного или нормального уровня, состояние больного резко ухудшается. Появляются бледность кожных покровов, цианоз дистальных отделов конечностей, кровоточивость слизистых оболочек, кровоизлияния в местах инъекций, кровохарканье, кровавая рвота, дегтеобразный стул. Одновременно больные отмечают сильные боли в поясничной области, часто нестерпимые, заставляющие принимать вынужденное положение в постели. Прогрессивно снижается диурез вплоть до полной анурии. Заболевание переходит в следующую – олигурическую – стадию.
Патогномоничным признаком геморрагической лихорадки с почечным синдромом является массивная протеинурия на фоне резкого уменьшения диуреза. Выведение белка достигает 33–85 г/л мочи. Интенсивность протеинурии может значительно изменяться в течение суток. Вследствие нарушения почечной функции прогрессивно нарастает азотемия, может развиваться почечная эклампсия, являющаяся в 48 % случаев причиной смерти при геморрагической лихорадке с почечным синдромом. Олигурический период нередко осложняется разрывом почечной капсулы и надрывом коркового слоя почек, часто связанными с неправильной тактикой ведения больного. Возможны кровоизлияния в миокард, легкие, головной мозг, гипофиз, надпочечники и в другие органы.
С 10‑16‑го дня болезни состояние больных геморрагической лихорадкой с почечным синдромом начинает улучшаться, увеличивается диурез – наступает полиурическая фаза болезни. Суточное количество мочи достигает 5 л, наблюдается никтурия. Плотность мочи снижается до 1,001‑1,003. Гипоизостенурия может сохраняться в течение нескольких недель. Иногда развивается пиелонефрит.
Выздоровление больных медленное, с постепенной нормализацией функции почек, лабильностью сердечно‑сосудистой системы. Повышенная чувствительность к изменению водного режима у отдельных реконвалесцентов сохраняется в течение 1–2 лет.
Диагностика и дифференциальная диагностика .
Прогноз серьезный. Летальность составляет от 1 до 10 %, в отдельные периоды – 15 % и более.
Дифференциальная диагностика геморрагической лихорадки с почечным синдромом проводится с геморрагическими лихорадками и рядом других болезней, протекающих с почечной недостаточностью (острый нефрит, хронический нефрит, токсические повреждения почек).
Из серологических методов диагностики используется выявление антител и нарастание их титра в парных сыворотках.
При геморрагической лихорадке с почечным синдромом лечение проводится в соответствии с принципами лечения больных геморрагическими лихорадками. В случаях выраженной азотемии показан гемодиализ, возможен перитонеальный диализ. В период полиурии лечение направлено на компенсацию водно‑электролитных нарушений.
Больные подлежат госпитализации в инфекционный стационар. Этиотропной терапии нет. Рекомендуют постельный режим, молочно‑растительную диету, витамины. Назначают преднизолон большими дозами. После нормализации температуры тела дозу постепенно снижают. Длительность курса – 8‑15 дней. В первые дни внутривенно вводят изотонические растворы глюкозы и изотонический раствор хлорида натрия, раствор аскорбиновой кислоты, рутин, антигистаминные препараты, анальгетики. За сутки вводят до 1–1,5 л жидкостей. При отсутствии артериальной гипотензии в фазе олигурии назначают маннитол или фуросемид (лазикс). Рекомендуются промывание желудка 2 %‑ным раствором гидрокарбоната натрия и сифонные клизмы. При сильной боли назначают пантопон. При нарастании почечной недостаточности больному необходимо проводить экстракорпоральный гемодиализ.
Больные подлежат обязательной госпитализации в инфекционный стационар. Доставка больных производится наиболее щадящим способом. Обслуживание больных предполагает соблюдение мер по предупреждению внутрибольничного заражения.
Изоляция контактных. Разобщение не применяется. Устанавливают медицинское наблюдение в течение 3‑х недель.
Допуск в коллектив разрешается не ранее 2‑х недель после выписки из стационара с полным клиническим выздоровлением, нормализацией всех лабораторных показателей, не ранее 25‑го дня болезни. Может оставаться изогипостенурия.
Диспансеризация проводится не менее 6 месяцев. Первые 3 месяца запрещается тяжелая физическая нагрузка. Лабораторное обследование (кровь, моча) – на 1‑м, 3‑м и 6‑м месяцах наблюдения. Дальнейшие сроки наблюдения и объем обследования зависят от клинических проявлений.
Специфическая профилактика не разработана. В эндемических очагах осуществляются борьба с грызунами и меры личной профилактики.


Легкость и удобство в новом объеме.
У постели пациента, в операционной или на спортивной площадке - всегда готов к использованию.
Геморрагическая лихорадка с почечным синдромом - хантавирусное природно-очаговое заболевание, широко распространенное во многих районах России, странах Европы и Азии. Поражение почек занимает ведущее место в клинике заболевания. Оно наблюдается у 100% больных и протекает в виде острого интерстициального серозно-геморрагического нефрита с развитием острой почечной недостаточности и в большинстве случаев определяет течение болезни [5,8,9].
Процесс восстановления почечных функций после геморрагической лихорадки с почечным синдромом продолжается несколько месяцев, а иногда и лет. В последующем у ряда больных отмечаются хронический пиелонефрит, тубулярные дисфункции, интерстициальный фиброз, артериальная гипертензия [7,10]. В связи с этим у перенесших заболевание возникает необходимость контроля за состоянием почек. Одним из способов такого контроля является применение ультразвуковых диагностических методик.
Цель исследования - изучение возможностей УЗИ для выявления тех или иных изменений в почках у перенесших геморрагическую лихорадку с почечным синдромом.
Ультрасонография была проведена 95 перенесшим геморрагическую лихорадку с почечным синдромом (диагноз у всех верифицирован серологически методом непрямых флуоресцирующих антител), возраст от 15 до 52 лет. Из них 23 обследованных перенесли тяжелую, 70 - среднетяжелую и 2 - легкую форму болезни. Обследование проводили от 1 мес до 10 лет после заболевания. У 16 (16,8%) человек выявлены клинико-лабораторные признаки хронического пиелонефрита, развившегося в различные сроки после геморрагической лихорадки с почечным синдромом. Ультрасонографическую картину почек оценивали по форме и размерам, правильности контуров, соотношению внутренних структур (размеры паренхимы почки и чашечнолоханочной системы, толщина коры, высота пирамид), по интенсивности эхосигнала паренхимы и его однородности, состоянию границы между паренхимой и полостной системой почек, структуре чашечно-лоханочной системы. Исследование выполнялось на эхокамерах "Aloka-SSD-280", "AlokaSSD-630" (Япония) и ультразвуковой системе "Sonoline Versa Pro" фирмы "Siemens" (Германия). У 29 переболевших методом ультразвуковой допплерангиографии исследован кровоток в почечных и дуговых артериях. Оценивали кровоток по показателям пиковой систолической скорости (V) и индекса резистентности (RI), представляющего собой отношение разности V и конечной диастолической скорости кровотока к V и отражающего состояние периферического сосудистого сопротивления [4]. В сроки от 1 до 3 мес после болезни обследовано 14 человек (I группа), от 4 до 12 месяцев - 10 (II группа) и от 1 года до 4 лет - 10 человек (III группа). Исследование состояния кровотока выполнено на ультразвуковой системе "Sonoline Versa Pro" фирмы "Siemens" (Германия), оснащенной цветным допплеровским и энергетическим блоками с использованием конвексного датчика частотой 4,5 МГц.
Анализ полученных данных показал, что размеры, форма и количественное соотношение внутренних структур почек у перенесших геморрагическую лихорадку с почечным синдромом не были изменены. При качественной же оценке их ультрасонографической картины выявлены заметные отклонения в сравнении со здоровыми лицами. У большинства перенесших геморрагическую лихорадку с почечным синдромом эхогенность пирамид оказалась пониженной, вследствие чего они всегда визуализировались, даже у тучных больных. У 32 (33,7%) обследованных в пирамидах обнаружены участки усиления эхосигнала, имевшие линейную или слегка овальную форму и обычно располагавшиеся в центре и реже - по периферии пирамид (рис. 1). Эти изменения чаще выявлялись в правой почке, которая, как известно, более значительно поражается при геморрагической лихорадке с почечным синдромом [1,7,8]. Среди перенесших заболевание в тяжелой форме описанные структуры встретились у 11 (47,8%) больных, причем у 7 из них - с обеих сторон. После среднетяжелой формы болезни они были обнаружены у 21 (30%) больного, с обеих сторон - только у 5 перенесших геморрагическую лихорадку с почечным синдромом.
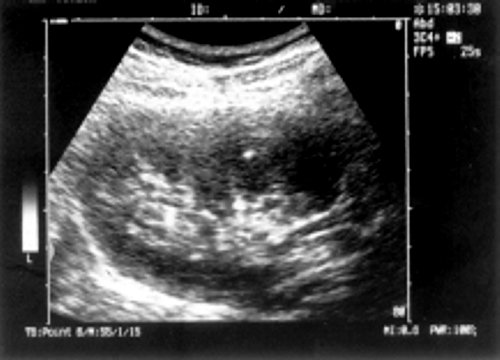
а) Участок усиления эхосигнала овальной формы у основания пирамид правой почки у пациентки, 22 года.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Самарcкий Государственный медицинский университет
Г еморрагическая лихорадка с почечным синдромом (ГЛПС) – острая вирусная зоонозная инфекция, характеризующаяся цикличным течением, синдромом интоксикации, геморрагическими проявлениями, развитием острой почечной недостаточности и имеющая в своей основе поражение вирусом мелких сосудов с последующим развитием иммунопатологических процессов.
Возбудителем данной инфекции является вирус, который относится к семейству Bunyaviridae рода Hantavirus и включает в себя около 30 серологически и генетически отличающихся друг от друга хантавирусов [20,22,26].
В настоящее время описаны две клинические формы хантавирусной инфекции: ГЛПС, возбудителями которой являются вирусы Hantaan, Seoul, Puumula и Belgrad/Dobrava, и хантавирусный пульмональный синдром (ХПС), впервые описанный в США в 1993 году, вызываемый хантавирусами Sin Nombre, New–York, Black Creek Canal, Bayou, Laguna Negra, Andes [23,24,27]. На территории России регистрируется только первая клиническая форма и установлена циркуляция семи, в том числе 4–х патогенных хантавирусных типов. В европейских очагах возбудителем заболевания в подавляющем проценте случаев является тип Пуумула, в азиатских – тип Хантаан [7]. Основной источник инфекции – мышевидные грызуны. На Европейской территории основное эпидемиологическое значение имеет рыжая полевка (Clethrionomys glareolus), обитающая в некоторых лесных регионах нашей страны. Заболевание имеет аэрогенный механизм заражения, который реализуется при посещении человеком мест обитания грызунов. ГЛПС по заболеваемости занимает первое место среди природно–очаговых инфекций в РФ. Число зарегистрированных случаев в отдельные годы может достигать 20 тысяч и более. На Европейскую территорию (Волго–Вятский, Поволжский регионы) приходится 97% всех заболевших ГЛПС [17]. Самарская область является активно действующим очагом. Заболеваемость в некоторые годы достигает 60 на 100 000 населения.
В настоящее время этиотропная терапия ГЛПС практически не разработана. В литературе имеются единичные публикации, посвященные применению специфического иммуноглобулина [16], гипериммунной плазмы [20,21], интерферона (ИФ) [10,32] и его индукторов [24] в качестве средств лечения данной инфекции. Учитывая вирусную природу заболевания и противовирусную активность ИФ, представляет интерес изучение эффективности применения индукторов эндогенного ИФ в лечении ГЛПС.
Целью настоящей работы явилась оценка эффективности применения индуктора эндогенного ИФ – Амиксина (тилорона, регистрационный номер 96/252/3) в лечении больных ГЛПС. Теоретическими предпосылками возможной эффективности препарата явились сведения о вирусемии при ГЛПС до 10–го и более дня от начала заболевания и противовирусная активность Амиксина в отношении экспериментальной формы данной инфекции [8]. Амиксин оказался эффективным также при экспериментальной форме лихорадки Западного Нила [9] и при вирусной лихорадке долины Рифт, относящейся к буньявирусным инфекциям [2]. Кроме того, доказана эффективность препарата при вирусных гепатитах [4,6,11,15,18,19], гриппе и других ОРВИ [4,13,14], герпетической инфекции [1,4].
Материалы и методы
В группу пациентов, получавших Амиксин, вошло 25 больных ГЛПС, которые лечились в клинике инфекционных болезней Самарского ГМУ. Все пациенты были старше 16 лет. Степень тяжести заболевания определялась в первые 2 дня нахождения больного в стационаре согласно классификации В.И. Рощупкина [12]. Больных со среднетяжелым течением инфекции было 12, с тяжелым – 13. Препарат назначался внутрь не позже 6 дня от начала заболевания по схеме, рекомендованной для лечения острых вирусных инфекций: 125 мг 2 раза в сутки 2 дня подряд и 125 мг однократно через 48 часов [4]. Препарат переносился хорошо, побочных эффектов выявлено не было. Контрольную группу составил 91 больной ГЛПС. Распределение больных по степеням тяжести в опытной и контрольной группах были идентичны. Проводился сравнительный анализ продолжительности клинических симптомов и синдромов в двух группах. В зависимости от периода болезни оценивались результаты общеклинических и биохимических анализов крови и мочи. Сравнивался уровень специфических антител против хантавирусов в сыворотке крови на основе непрямого метода флюоресцирующих антител (НМФА). Использовались антигены серотипов Пуумула, Хантаан, Сеул и Добрава/Белград [3]. Определение специфических IgM и IgG к вирусам Пуумала и Хантаан проводилось на основе иммуноферментного анализа с использованием рекомбинантного антигена [25]. Определение уровня интерферона в сыворотке крови проводили с помощью метода титрования в культуре диплоидных клеток человека М–19 с использованием микрометода на 96 луночных культуральных панелях. Тест–вирусом служил вирус энцефаломиокардита мышей. За единицу активности интерферона принимали величину, обратную конечному разведению интерферона, при котором наблюдается 50% защита клеток от 100 ТЦПД50 тест–вируса [5]. Для более достоверной оценки результатов использовались значения десятичных логарифмов разведений (lg).
Результаты и обсуждение
В группе больных, принимавших Амиксин, по сравнению с контрольной достоверно короче была продолжительность головной боли: 6,80±0,66 дней и 9,24±0,48 дней соответственно (р Амиксин (торговое название)
1. Баткаев Э.А., Гаврилова А.В., Тышкевич А.В., Корсунская И.М., Трубачев А.А. Амиксин в комплексной терапии урогенитального хламидиоза и рецидивирующего генитального герпеса. – Вестник последипломного медицинского образования, 1998, №19, с.18.
2. Березина Л.Ю., Носик Н.Н., Литвинова Л.А., Лаврухина Л.А., Лихов С.А. Защитный эффект амиксина и его аналогов при буньявирусных инфекциях. Итоги науки и техники. Арбовирусы и арбовирусные инфекции. Серия вирусология. Москва – 1991,Том 24, с.78.
3. Дзагурова Т.К., Ткаченко Е.А., Петров В.А. Эффективность применения культуральных антигенов для серодиагностики ГЛПС с помощью метода иммунофлюоресценции. Вопросы вирусологии, 1988, 1, с.71–75.
4. Ершов Ф.И., Баткаев Э.А., Головкин В.И., Киселев О.И., Турьянов М.Х. АМИКСИН. Применение в терапии острых и хронических вирусных заболеваний. Рекомендации для врачей. Москва, 1998, 20 с.
5. Ершов Ф.И. Вопросы вирусологии 1982 ,6, стр 92.
7. Лещинская Е.В., Ткаченко Е.А., Рыльцева Е.В. и др. К характеристике эндемических очагов ГЛПС в разных регионах СССР. Вопр.вирусол. 1990, № 1, с.42–45
10. Мавзютова Г.А., Фазлыева Р.М., Бобкова Е.В. Иммуномодулирующий эффект альфа1–интерферона в комплексной терапии геморрагической лихорадки с почечным синдромом. Журнал микробиологии и эпидемиологии, 1996, №6, с.80–81.
11. Применеие индуктора интерферона Амиксина в лечении острых и хронических вирусных гепатитов. Методические рекомендации, Москва–1999, 10 с.
12. Рощупкин В.И., Суздальцев А.А.. Геморрагическая лихорадка с почечным синдромом. Куйбышев.1990.– С.12–14.
15. Серебряков М.Ю., Тищенко М.С., Байрамова Э.Б., Серебряков Д.Ю., Гаврилов А.А. Амиксин и циклоферон в лечении вирусных гепатитов. Пятый Российский съезд врачей–инфекционистов. Тезисы докладов. Москва, 1998. С. 279–280.
16. Суздальцев А.А. Геморрагическая лихорадка с почечным синдромом (современные критерии оценки тяжести течения, эффективности лечения и прогноза). Автореферат диссертации д.м.н., Санкт–Петербург, 1992, 19 с.
17. Ткаченко Е.А. Эпидемиологические аспекты изучения геморрагической лихорадки с почечным синдромом в России. Инфекционные болезни на рубеже ХХI века. Материалы научно–практической конференции. Ч.2, Москва, 2000, 58
18. Турьянов М.Х., Алленов М.Н., Сапронов Г.В., Ловчинская О.Б., Тетова В.Б., Гуриева З.С., Алятин Ю.С., Алешкович Т.В. Лечение больных вирусным гепатитом С и вирусным гепатитом В+С индуктором интерферона Амиксином. Пятый Российский съезд врачей–инфекционистов. Тезисы докладов. С.392–393.
19. Турьянов М.Х., Алленов М.Н., Сапронов Г.В. Анализ эффективности противовирусной терапии при ОВГВ. Пятый Российский съезд инфекционистов. Тезисы докладов. С.391–392.
20. Фазлыева Р.М., Хунафина Д.Х., Камилов Ф.Х.. Геморрагическая лихорадка с почечным синдромом в республике Башкортастан. Уфа, 1995.– 243 с.
21. Хунафина Д.Х., Шамсиева А.М., Фазлыева Р.М. Комплексное лечение больных геморрагической лихорадкой с почечным синдромом. Актуальные вопросы изучения клещевого энцефалита и геморрагической лихорадки с почечным синдромом в их природных очагах. Тезисы докладов научно–практической конференции г.Ижевск. 1990, с.226–227.
22. Avsic–Zupanc T, Toney A, Anderson K, Chu YK, Schmaljohn C. Genetic and antigenic properties of Dobrava virus: a unique member of the Hantavirus genus, family Bunyaviridae. J Gen Virol. 1995, 76, p.2801–8.
24. Hunafina D.H., E.K.Alekhin, R.T.Murzabaeva et al. Interferon inducers: appication in hemorrhagic fever with renal syndrome patients. Abstracts of 5 th intern. Confer. on HFRS, HPS and Hantaviruses. Annecy, France, 2001, p.139.
25. Ivanov A.P., E.A. Tkachenko, V.A. Petrov, Y. Pashkov, T.K. Dzagurova, T.P. Vladimirova, G.M. Voronkova, G. van der Groen – Enzyme immunoassay for the detection of virus specific IgG and IgM antibody in patients with HFRS. Arch. Virol., 1988, 100: 1–7.
26. Lee Ho Wang, Charles Calisher, Connie Schmaljohn. 1998. Manual of Hemorrhagic Fever with Renal Syndrome and Hantavirus Pulmonary Syndrome. WHO collaborating Center for Virus Reference and Research, Seoul, 250 p.
27. Nichol S., Spiropoulou C., Morzunov S. et al. Genetic identification of a novel hantavirus associated with an outbreak of acute respiratory illnes in the southwestern United States. Science 1993, 262, p.914–917.
Читайте также:


