Мазь с антибиотиком от кожных инфекций

Тетрациклиновая мазь – это распространенная мазь с антибиотиком от воспаления тканей. Существует в виде глазной и наружной мазей (1-3%). Антибактериальное действие ципрофлоксацина позволяет остановить размножение болезнетворных микробов при глазных заболеваниях, при лечении гнойничковых кожных заболеваний и осложненных язв и экзем. Позиционируется, как отличная мазь от ячменя с антибиотиком. Средство наносят несколько раз в сутки до полного излечения заболевания.
Террамициновая мазь – содержит окситетрациклин, близка по свойствам с тетрациклиновой мазью. Подавляет развитие широкого спектра грамположительных и грамотрицательных микробов, применяется при лечении инфицированных ран, в том числе травматических и хирургических (ссадин, царапин, пункций). Особенностью препарата является способность кумулировать свое воздействие в течение недели с момента разового нанесения.
Мазь эритромициновая – макролидная антибактериальная мазь, которую используют в терапии инфекционных поражений глаз, кожных и слизистых покровов, пролежней и нарушений трофики (питания) тканей, ожогов. Препарат практически не имеет побочных проявлений, может использоваться у пожилых и ослабленных больных.
Полимиксиновая мазь (Полимиксин М сульфат) – антибактериальная мазь, подавляющая рост кишечных и дизентерийных бактерий, синегнойной палочки. При наружном применении не оказывает токсического действия. Не используется для лечения протея, микобактерий и грибковой инфекции. Данную мазь обычно назначают в качестве комплексной терапии с другими антимикробными препаратами внутреннего применения. Длительность лечения определяется индивидуально и составляет обычно 7-10 суток.
Мазь Левомеколь – мазь с антибиотиком для ран, трофических язв, гнойничково-воспалительных заболеваний кожи. Может применяться при ожоговых поражениях II или III степени. Левомеколь сочетает в себе действие антибактериального средства хлорамфеникола и иммуностимулятора метилурацила, что позволяет более комплексно воздействовать на патологию. Мазью пропитываются стерильные салфетки, которые затем вводят в предварительно очищенную рану, один раз в сутки. Длительное использование препарата не рекомендуется в связи с возможностью всасывания препарата в кровь.
Бактробан – мазь в нос с антибиотиком, обладает значительной антимикробной активностью по отношению к стафилококковой флоре, в частности, к метициллинрезистентным штаммам. Основная составляющая – мупироцин, антибактериальное вещество широкого спектра воздействия. Применяется мазь для терапии инфекционных патологий носовой полости. Мазь вводят в очищенные носовые ходы 2 раза в день, избегая попадания на слизистую глаз. Длительность терапии в среднем составляет 5-7 дней.
Гентаксан – мазь антибиотик для заживления ран, различного генеза и расположения, в том числе и инфицированных хирургических ран (нагноений, абсцессов). Гентаксан хорошо зарекомендовал себя, как эффективное терапевтическое средство при ожогах, пролежнях, процессах регенерации на фоне иммунодифицитных состояний, лучевой болезни, нарушений обмена веществ. Препарат наносят под повязку 1-2 раза в сутки, постепенно снижая дозировку. Разовое нанесение допускает применение 10-12 г мази.
Офлокаин – мазь антибиотик для кожи, сочетает в себе действие антимикробного фторхинолонового препарата офлоксацина и местного анестетика лидокаина. Офлокаин используется для лечения гнойных и воспалительных кожных заболеваний, для профилактики гнилостных процессов в ранах, трофических нарушениях в коже. Средство наносят от 1-2-х раз в сутки до 2-х раз в неделю в зависимости от клинических показаний. Дозировка препарата определяется доктором в зависимости от степени поражения кожи и наличия гнойного отделяемого.
Банеоцин – лечебная мазь от фурункулов с антибиотиком. Мазь содержит сочетание пары антибиотиков бацитрацина и банерцина, имеющих различную антимикробную активность и выгодно дополняющих друг друга. Препарат эффективен при лечении импетиго, фурункулеза, карбункулеза, фолликулита, гнойников потовых и сальных желез, пиодермии. Банеоцин исп
Расширение ассортимента лекарственных препаратов для локальной консервативной фармакотерапии раневого процесса позволяет проводить дифференцированное лечение ран и ожогов, которое осуществляется путем последовательного применения различных лекарственных средств с разнообразным механизмом их действия (Ляпунов Н.А. и соавт., 1995), влияющих на определенные фазы раневого процесса. Активный поиск эффективных лекарственных веществ в разных лекарственных формах является актуальным и в настоящее время.
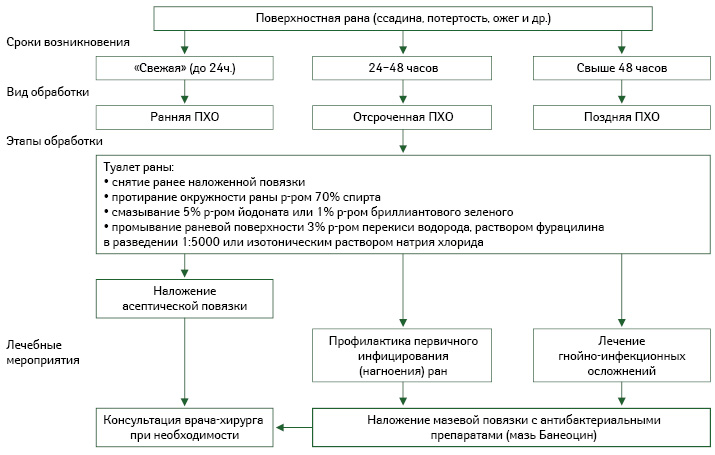
Нанесение лекарственных препаратов для наружного применения на рану определяют как местное медикаментозное лечение. Для успешной терапии ран необходимо комплексное воздействие на раневой процесс (Кузнецов Н.А., 2006) с учетом не только степени тяжести его течения, но и уровня его распространения в глубину, количества вовлеченных в воспалительный процесс анатомических структур и т.д. (таблица; алгоритм обработки поверхностных ран).
| Таблица | Классификация хирургической инфекции мягких тканей (Ahrenholz D., 1991; Блатун Л.А., 2007) |
| Уровень | Поражение | Заболевания |
| I | Собственно кожи | Фурункул |
| Фурункулез | ||
| Рожа | ||
| Эризипелоид | ||
| II | Подкожной клетчатки | Карбункул |
| Гидраденит | ||
| Абсцесс | ||
| Целлюлит | ||
| III | Поверхностной фасции | Некротизирующий фасциит |
| IV | Мышц и глубоких фасциальных структур | Пиомиозит |
| Инфекции мышечных футляров | ||
| Клостридиальный мионекроз | ||
| Неклостридиальный мионекроз |
Терапия включает локальное назначение широкого спектра лекарственных веществ в форме мазей, гелей, порошков, масел и раневых покрытий (Кузин М.И., 1999; Блатун Л.А., 2007).
Поверхностные инфицированные раны лечат дренирующими сорбентами и протеолитическими ферментами. При лечении гнойных глубоких ран в первой фазе проводят терапию мазями под повязками (Блатун Л.А., 2009), причем успех профилактики и лечения ран в данной фазе определяется своевременным назначением различных лекарственных средств с антимикробным действием. А вот во второй фазе — регенерации, образования и созревания грануляционной ткани применяют мази, раневые покрытия, гелевые повязки и масла с активными компонентами, уже способствующими стимуляции этих процессов (алгоритм обработки поверхностных ран).
Неомицин — представитель антибиотиков-аминогликозидов, оказывает бактерицидное действие путем подавления синтеза бактериального белка и угнетения генетического кода бактерий. Для него характерен широкий спектр противомикробного действия (рис. 1).
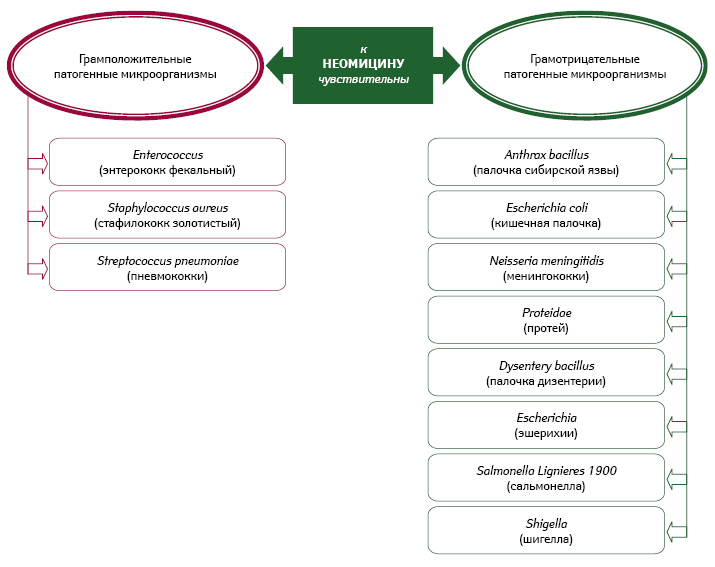
Очевидно, что неомицин проявляет широкий спектр антибактериальной активности, оказывая бактерицидное действие на чувствительную к нему микрофлору (Даценко Б.М. и соавт., 1989). Характерно медленное формирование устойчивости микроорганизмов к неомицину. Наружное применение неомицина в форме порошка или мази не позволяет развиться его токсическим проявлениям, которые могут возникать при парентеральном применении (ото-, нефротоксичность, блокада нейромышечной передачи). Неомицин не применяют перорально ввиду возможности его кумулирования в плазме крови, отмечающееся при нарушенной функции почек (Коваленко В.Н., 2012).
Бацитрацин — полипептидный антибиотик. Он угнетает синтез клеточной стенки путем подавления кругооборота липидных переносчиков субъединиц пептидогликанов (блокада синтеза пептидогликанов), что также реализуется в виде бактерицидного действия. Спектр антибактериального действия бацитрацина представлен на рис. 2.
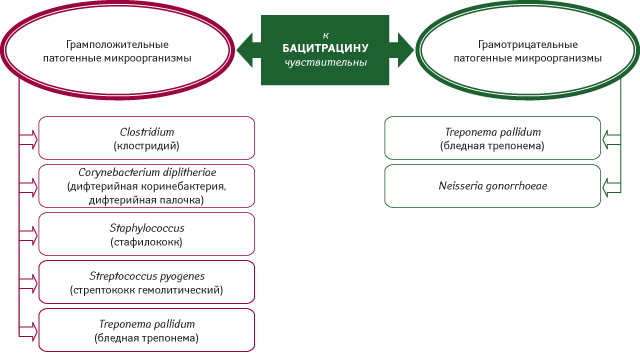
К бацитрацину устойчивость развивается крайне редко, механизмы ее развития не установлены. Он хорошо переносится тканями организма человека и не инактивируется кровью, тканевыми компонентами, биологическими продуктами (Паршина В.Л., 2007). Особенно актуально то, что при локальном его применении снижается риск проявлений повышенной чувствительности к составляющим Банеоцина .
Таким образом, фармацевтическая композиция неомицина и бацитрацина ( Банеоцин ) приводит к синергическому фармакологическому взаимодействию двух лекарственных средств. Такое объединенное действие в итоге превышает сумму действий этих действующих веществ (усиление действия друг друга) по сравнению с их раздельным использованием.
Эта комбинация антибактериальных средств выпускается в виде двух лекарственных форм — порошка и мази.
Показания к применению Банеоцина в форме мази и порошка представлены на рис. 3 и 4.

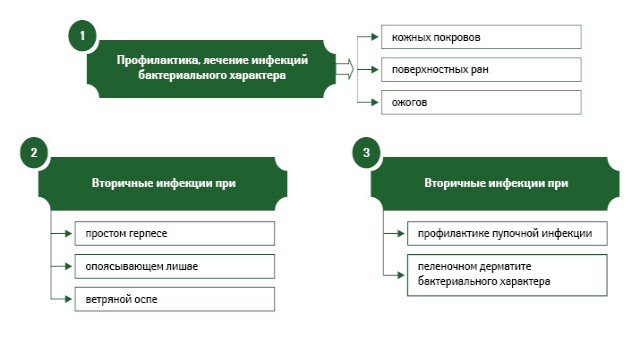
В качестве вспомогательного вещества в состав порошка Банеоцин входит крахмал кукурузный, содержащий не более 2% магния оксида (основа порошковая стерилизованная) (Коваленко В.Н., 2012). Ранее уже были отмечены высокие абсорбционные свойства порошковой основы, которые как раз и проявляются за счет легковесных аморфных порошков — магния оксида и крахмала кукурузного.
Порошок Банеоцин в короткие сроки купирует проявления воспалительного процесса, упреждает возможное возникновение нагноения (Зорин А.Н. и соавт., 2005). При нанесении на кожу порошок Банеоцин обусловливает активное поглощение раневого экссудата, осушение раны и на протяжении нескольких часов обеспечивает дренаж из раны с одновременным образованием защитного антибактериального слоя (Буслаев О.А. и соавт., 2006).
Также порошок Банеоцин обладает замечательными дополнительными действиями: охлаждающим и успокаивающим. Это особенно важно для лечения ран у пациентов детского возраста ввиду их высокой чувствительности к боли и страха перед спиртосодержащими средствами, традиционно используемыми для обработки ран.
Эффективность Банеоцина подтверждена комплексным изучением клинико-лабораторных показателей в лечении пациентов с гнойным поражением кожи и мягких тканей (бактериологическая эффективность составляла 92,5%, а клиническая — 95%) (Блатун Л.А., 2009). Это обусловлено длительным осмотическим действием порошка Банеоцин , что особенно эффективно в лечении гнойных ран в первой фазе раневого процесса, когда происходит активное впитывание раневого отделяемого. Ценным качеством Банеоцина является быстрое разрешение кожных проявлений инфекционных поражений кожи, таких как атопический дерматит, импетиго, фолликулит и т.д., которое отмечается в течение 1 или 2 сут от начала лечения (Шерстобитов А.С., 2008). Банеоцин успешно применяется в лечении пациентов с трофическими язвами и у больных с аллергологическим анамнезом, когда они не могут применять традиционные локальные препараты (Буслаев и соавт., 2006; Блатун Л.А., 2007; 2009). Кроме того, обработка ран, возникших вследствие лазерной деструкции (Соколовский Е.В. и соавт., 2004), порошком Банеоцин с дальнейшим переходом на мазь Банеоцин оказывается более щадящим методом по сравнению с традиционной обработкой (Хорук С.А., 2008).
В свою очередь, мазь Банеоцин представляет собой комбинированный мягкий лекарственный препарат с антибиотиками, введенными в дифильную абсорбционную основу, состоящую из гидрофобного компонента — вазелина, и вещества с дифильными свойствами — ланолина, обладающего эмульгирующей способностью (Хишова О.М., 2009).
Вазелин можно отнести к веществам, которые давно и успешно используют в качестве средства для смягчения кожных покровов, защиты кожи после некоторых косметических процедур и т.д. Это связано с тем, что вазелин способен удерживать влагу в клетках кожи, что, в свою очередь, позволяет смягчить загрубевшие участки кожи, устранить раздражение, защитить слизистую оболочку и саму кожу от агрессивного и вредного воздействия лекарственных препаратов или окружающей среды. При этом вазелин и введенные в него вещества, не проникают в глубокие слои кожи и, тем более, под кожу. Последнее особенно актуально, если рассматривать его в аспекте безопасности применения Банеоцина . Как уже было отмечено выше, использование как неомицина, так и бацитрацина предполагает их исключительно локальное применение с целью предотвращения побочного действия на организм.
Ланолин, относящийся к натуральным вспомогательным веществам, кроме прочего обладает увлажняющими и смягчающими свойствами, позволяющими защищать кожу от неблагоприятных внешних факторов, а также связывать и удерживать в коже влагу. Именно эти позитивные качества ланолина успешно используются в медицине и косметологии с целью обеспечения уменьшения потери влаги и восстановления натуральной мягкости и эластичности кожи. В качестве одного из свойств чистого ланолина отмечают положительное местное его применение у кормящих грудью, помогающее заживлению трещин на сосках и предотвращающее их появление.
Так, учитывая вышеизложенные свойства вспомогательных веществ, входящих в состав мази Банеоцин , можно резюмировать: мазевая основа обладает умеренными абсорбционными свойствами на фоне низких показателей осмотической активности; не нарушает аэрацию кожи и не всасывается в глубокие слои; гидрофобные компоненты, покрывая кожу, препятствуют сухости кожи вследствие исключения излишней потери влаги.
С точки зрения биофармацевтических аспектов создания мягких лекарственных средств, мазевая основа сегодня является не только носителем действующих веществ, поэтому основа мази Банеоцин , отвечая медико-биологическим требованиям к мазям определенного назначения, активно участвует в терапевтическом процессе.
Банеоцин в форме мази эффективен в лечении поверхностных ран, во второй фазе раневого процесса (где может быть использован наряду с порошком) (Буслаев и соавт., 2006). Банеоцин в высоких концентрациях скапливается в гнойном очаге, оказывая бактерицидное действие, не оказывая системного эффекта. При его нанесении образуется тонкая пленка, защищающая молодой эпителий от деструктирующих факторов. Нанесение Банеоцина под повязки приводит к полной эридикации болезнетворных микроорганизмов в короткие сроки и обеспечивает профилактику повторного инфицирования поверхности раны госпитальной инфекцией (Оболенский В.Н., 2013). Уместно использовать мазь Банеоцин в третьей фазе раневого процесса для организации рубца и эпителизации, когда пленка, образуемая мазью, защищает эпителий от повреждения и способствует ускорению эпителизации. Неоспоримые достоинства фармакологического действия Банеоцина объясняют его активное назначение и на этапе стационарного комплексного лечения больных, и в поликлинических условиях.
Доказана высокая клиническая эффективность Банеоцина при распространенной форме акне средней и тяжелой степени (Кунгуров Н.В., 2009; Шабардина О.В., 2010). При локальном применении Банеоцина снижен риск возникновения гиперчувствительности к его компонентам (Ширшов О.Н., 2008). Характерна достаточно хорошая переносимость Банеоцина . Отмечается успешное использование Банеоцина в педиатрии при топическом дерматите, осложненном вторичной инфекцией (Ahrenholz D.H., 1991; Зорин А.Н. и соавт., 2005), а также при сочетании топического дерматита с пиодермией, и даже в неонатологической практике применение порошка Банеоцина позволяет сокращать сроки эпителизации пупочной ранки новорожденных. Назначение Банеоцина предупреждает развитие серьезных гнойно-септических осложнений у новорожденных, позволяет эффективно купировать клинические проявления инфицированного пеленочного дерматита и эксфолиативного дерматита Риттера (Паршина В.Л., 2007).
Таким образом, благодаря комбинации двух антибактериальных компонентов достигается широкий спектр действия препарата и синергизм в отношении широкого ряда микроорганизмов, в который не попадают лишь псевдомонады, нокардии, грибы и вирусы. При местном нанесении на кожные покровы, раневые поверхности Банеоцин переносится хорошо, не вызывая раздражения; через интактную кожу препарат не всасывается, а через поврежденные кожные покровы всасывание незначительно, что позволяет создать максимальную концентрацию препарата непосредственно в месте применения. А две лекарственные формы Банеоцина ориентированы на последовательное его применение на различных стадиях раневого процесса (Буслаев О.А. и соавт., 2006).
Особые указания при применении Банеоцина
- Нельзя допускать попадания мази и порошка Банеоцин в глаза.
- С осторожностью наносить препарат на участки кожных покровов со значительными повреждениями.
- Нельзя применять Банеоцин в наружный слуховой проход в случае, если у пациента нарушена целостность барабанной перепонки и имеется сквозной дефект.
- Кратность нанесения порошка составляет 2–4 раза в сутки.
- Мазь Банеоцин наносится 2–3 раза в сутки.
- Суточная доза не должна превышать 1 г Банеоцина .
- Курс лечения обычно составляет 7 дней.
- При назначении повторного курса максимально допустимая доза снижается в 2 раза.
- Банеоцину присуща фотосенсибилизация. Поэтому рекомендуется предотвращать доступ прямых солнечных лучей к месту нанесения препарата.
Фармацевтическая опека при применении Банеоцина
- Не применять Банеоцин у пациентов с повышенной чувствительностью к бацитрацину, неомицину и другим антибиотикам аминогликозидного ряда.
- Не допускать сочетанного применения антибиотиков аминогликозидного ряда местного и системного действия из-за возможной их кумуляции и, как следствие, — риска развития токсичности.
- С осторожностью применять при миастении и других заболеваниях нервно-мышечной системы, а также при аллергических реакциях в анамнезе.
- При обширных поражениях кожи возникает риск абсорбции бацитрацина и неомицина, что может привести к развитию токсических проявлений у пациентов с нарушенной функцией печени или почек.
- Дисфункция вестибулярной и кохлеарной систем, патология почек с нарушением их выделительной функции является противопоказанием для приема Банеоцина , особенно при возможности его всасывания в системный кровоток.
- При ожоговых поражениях кожи площадью более 20% поверхности тела больного порошок Банеоцин наносится только 1 раз в сутки.
- При развитии аллергии или суперинфекции Банеоцин следует отменить.
- Избегать инсоляции из-за возможности возникновения фотосенсибилизации и фототоксических реакций.
- При лечении в период беременности и кормления грудью фармакотерапию Банеоцином следует проводить с осторожностью.
- Применение мази Банеоцин в педиатрии проводится по показаниям, аналогичным таковым у взрослых.
- Порошок Банеоцин применяется у детей с первых дней жизни при преобладании пользы от применения Банеоцина над риском развития его побочных эффектов.
- Нет сведений о способности Банеоцина изменять скорость реакций при управлении транспортными средствами и работе с другими механизмами.
Список использованной литературы
Информация для профессиональной деятельности медицинских и фармацевтических специалистов
БАНЕОЦИН (BANEOCIN) . Код АТС : D06A X54**. Состав и форма выпуска: мазь, туба 20 г, № 1 (бацитрацин цинк — 250 МЕ/г, неомицина сульфат — 5000 МЕ/г) — р.с. № UA/3951/01/01 от 28.04.2011 г. до 28.04.2016 г.; порошок накожный, контейнер 10 г, № 1 (бацитрацин цинк — 250 МЕ/г, неомицина сульфат — 5000 МЕ/г) — р.с. № UA/3951/02/01 от 11.05.2011 г. до 11.05.2016 г.). Показания . Порошок — бактериальное инфицирование ограниченных участков кожи при герпетических инфекциях, в том числе при ветряной оспе; инфицированные варикозные язвы; экзема; бактериальный пеленочный дерматит; профилактика пупочной инфекции у новорожденных; после хирургических манипуляций: как вспомогательная терапия в послеоперационный период (в том числе лечение разрывов промежности и эпизиотомии, мастита при дренировании, посттравматических инфекций); инфекции при ожогах. Мазь — местное лечение и профилактика бактериальных инфекций кожи, вызванных чувствительными к препарату микроорганизмами: фурункулы, карбункулы (после хирургического вмешательства), абсцессы (после разреза), сикоз, в том числе глубокий, на участке подбородка, гнойный гидраденит, псевдофурункулез, паронихии; бактериальные инфекции кожи ограниченной степени, в том числе контагиозное импетиго, инфицированные варикозные язвы, вторичные инфекции при экземе, инфекции при ожогах, после косметической хирургии и пересадки кожи (также с профилактической целью и при применении повязок); как вспомогательная терапия при лечении послеоперационных инфицированных ран (например при наружном отите, вторичном инфицировании хирургических рубцов). Побочные эффекты . Обычно препарат переносится хорошо. При продолжительном лечении возможно развитие аллергических реакций (гиперемия, сухость и шелушение кожи, сыпь, зуд). Если поражения распространяются или раны не заживают, это может быть следствием аллергической реакции (очень редко — в виде контактной экземы). Для пациентов со значительным поражением кожи следует учитывать возможную абсорбцию препарата и развитие таких побочных эффектов, как нарушения вестибулярной и кохлеарной функции, слуха, нервно-мышечной проводимости. Более детальная информация изложена в инструкции по медицинскому применению.
Изобретение относится к области медицины, а именно к дерматологии, и может быть использовано для лечения широкого спектра кожных инфицированных поражений: язв, экзем, раневых инфекций, укушенных ран, пролежней, псориаза, герпеса, лепры.
Известно средство для лечения трофических язв и ожогов у больных лепрой, содержащее антибиотик доксициклина гидрохлорид, вазелиновую основу при определенном соотношении компонентов. (Патент RU №2095065 C1, МПК А61K 31/71, А61K 9/06, приоритет от 06.04.1995 г., опубл. 10.11.1997 г.).
При использовании этого средства, лечение возлагается на один антибиотик, которым является доксициклина гидрохлорид, что и определяет узость применения этого средства в основном для больных лепрой. Поэтому востребованность этого средства незначительна. Использование данного средства для лечения других типов кожных инфекционных поражений будет менее эффективным в сравнении со средствами, имеющими в своем составе не один антибиотик.
Известно средство для лечения заболеваний кожи, выполненное в лекарственной форме для наружного применения, в состав которого входит антибиотик рифампицин и еще семь различных антибиотиков, при определенных соотношениях активных ингредиентов на 100 г основы (Патент RU №2321409 С1, МПК А61K 31/573, А61K 31/727 и др., приоритет от 23.10.2006 г., опубл. 10.04.2008 г.).
Наиболее близким по составу к заявляемому изобретению является средство для лечения кожных поражений, содержащее только рифампицин в качестве антибиотика, вазелиновую основу при определенном соотношении компонентов (А.с. SU №1196001 А, МПК А61K 9/006, приоритет от 09.07.19820, опубл. 07.12.1985).
Терапевтическим результатом, на достижение которого направлено создание данного изобретения, является эффективное преодоление факторов резистентности патогенных микробов и расширение спектра действия на все типы кожных инфекционных поражений.
Поставленная задача достигается тем, что предлагаемая мазь для лечения кожных инфекций, в составе которой используется в качестве антибиотика рифампицин, вазелиновая основа, согласно изобретению, содержит дополнительно в равной пропорции второй антибиотик доксициклина гиклат и интерферон человеческий рекомбинантный альфа-2b при следующем содержании активных ингредиентов на 100 г основы:
|
Содержание в равных пропорциях антибиотиков рифампицина вколичестве 1-3 г и доксициклина гиклата 1-3 г на 100 г основы обеспечивает оптимальную терапевтическую концентрацию в местах инфекционных очагов и синергизм антимикробного действия, образует непереносимый для микробов тандем, прекращающий деление ДНК и белковый синтез в микробной клетке.
Сам рифампицин - редко используемый антибиотик, и изначальная резистентность бактерий к нему невысокая. Кроме того, рифампицин существенно расширяет спектр действия вплоть до некоторых вирусов и обладает очень высокой проникающей способностью. Присутствие второго антибиотика - доксициклина гиклата, имеющего сходные с рифампицином фармакодинамические свойства, как бы "прикрывает" рифампицин от быстрого развития микробной устойчивости, подавляя микробы, сумевшие выработать резистентность к рифампицину.
Наличие интерферона рекомбинантного человеческого альфа-2b в количестве 250000-500000МЕ на 100 г основы определяется терапевтической самодостаточностью и способно оказывать лечебное действие даже в самостоятельном применении. В составе мази интерферон значительно усиливает защитные функции организма и расширяет спектр действия препарата за пределы действия антибиотиков, воздействуя на вирусы, грибковые инфекции и прочие микроорганизмы, не попавшие в спектр действия антибиотиков, дополнительно усиливает воздействие препарата через местную мобилизацию иммунитета и микробы, не охваченные воздействием антибиотиков, будут подавляться иммунными клетками.
Вазелин является носителем активного вещества и основой для консистенции. В его жирной основе хорошо растворяются и рифампицин, и доксициллина гиклат, и интерферон. Его содержание определяется объемом фасовки и дает возможность проникания антибиотика на всю глубину кожного покрова и достаточно длительного удержания антибиотика в очаге поражения для терапевтического воздействия.
Использование двух антибиотиков менее одного грамма и интерферона человеческого рекомбинантного альфа-2b менее 250000 МЕ на 100 г основы, ведет к значительному падению терапевтической эффективности, сужению спектра подавляемых микробов и как итог: не полному вылечиванию больного, с риском последующих рецидивов и развитию микробной устойчивости.
При использовании антибиотиков более трех граммов и интерферона человеческого рекомбинантного альфа-2b свыше 500000 ME на 100 г основы, усиливается риск побочных эффектов: аллергических реакций, раздражений, связанных с плохой переносимостью компонентов препарата, лечебное же действие прирастает незначительно от дальнейшего наращивания количественных соотношений компонентов.
Ингредиенты тщательно перемешиваются до получения гомогенного вещества с однородным цветом.
Рифампицин - лиофилизат для приготовления раствора для инфузий.
Доксициклина гиклат - официальный препарат в виде желтого кристаллического порошка, выпускаемого в капсулах.
Интерферон человеческий рекомбинантный альфа-2b, официально выпускаемый в виде лиофилизата.
Вазелин - мазь для наружного применения в тубах.
После перемешивания в 100 г мази для лечения кожных инфекций содержится:
|
Применение мази востребовано в госпитальной практике лечения кожных заболеваний в качестве самостоятельного и комплексного подхода, особенно в условиях неблагополучной санитарной обстановки.
Суммарное действие мази значительно превосходит свои аналоги в итоге:
По срокам заживления язв - до 20 суток
По проценту положительных результатов - превышает 80%
По проценту инфекционных рецидивов - не превышает 10%
Настоящее изобретение поясняется конкретными примерами исполнения, которые, однако, не являются единственно возможными, но наглядно демонстрируют возможность достижения требуемого терапевтического результата.
Пример 1. Мужчина после приезда с отдыха в тропической стране обратился с симптомами кожного воспаления на месте повреждения кожи во время плавания. Жалуется на зуд в месте воспаления в области предплечья. На коже предплечья имеется обширная зона с покраснением и припухлостью вокруг ссадин от скользящей травмы. Раны и окружающая их кожа предплечья промыты водой с мылом, осушены стерильным тампоном и смазаны сплошным тонким слоем разработанной мази с последующей ежедневной сменой повязки с мазью. При осмотре на третьи сутки покраснения кожи у ран и отека нет. Раны зажили без осложнений.
Пример 2. Мужчина 75 лет. Диагноз: 20% поверхности спины повреждены пролежнями в результате долгого лежания из-за инвалидности (долго не заживающие, несмотря на длительное лечение). На марлевых тампонах мазь наносили на пораженные участки. Быстро снялась боль, зуд и через 3 дня удалились некротические ткани и через 8 дней появилась нежная кожа на месте пролежней.
Таким образом, заявляемое качественное и количественное соотношение компонентов найдено экспериментальным путем, является оптимальным и позволяет получить указанный терапевтический результат. Преимущество мази для лечения кожных инфекций в длительном воздействии на очаг поражения синергидной композицией рифампицина и доксициклина, которые в совокупности воздействуют на самый широкий спектр патогенных микробов.
Читайте также:


