Лейкоплакия пищевода или гиперкератоз



Пищевод Барретта (ПБ) представляет собой заболевание, развивающееся в результате замещения многослойного плоского эпителия пищевода специализированным цилиндрическим эпителием [1]. ПБ является грозным осложнением гастроэзофагельной-рефлюксной болезни и в большинстве случаев протекает на фоне грыжи пищеводного отверстия диафрагмы. Частота выявления пищевода Барретта составляет от 2,4 до 4 % в среднем по популяции [2,3]. Однако значительное число больных, имеющих симптомы гастроэзофагеального рефлюкса (ГЭР), самостоятельно бесконтрольно в течение продолжительного времени применяют различные медикаментозные средства, чаще широкодоступные антациды, не обращаясь к врачам [4], поэтому значительная часть больных с пищеводом Барретта остается невыявленной [5]. Прогрессирование пищевода Барретта может приводить к дисплазии слизистой оболочки до возможного развития рака пищевода [6]. По данным ряда авторов в России, США, странах Западной Европы, а также в ряде стран Азии за последние 10 лет отмечается резкий подъем заболеваемости аденокарциномой пищевода [7]. В диагностике ПБ решающее значение имеют эндоскопическое исследование с морфологической верификацией диагноза. Эндоскопически пищевод Барретта рассматривается как ярко-розовые патологические участки на фоне бледно-розовой слизистой пищевода, отходящие от слизистой оболочки выше кардиоэзофагеального перехода (КЭП) – “языки пламени”. Обязательным критерием диагноза является наличие кишечной метаплазии. На сегодняшний день рекомендованным методом взятия биопсийного материала при ПБ является прицельная биопсия с четырехквадрантным методом забора материала через каждые 2 см. С целью повышения эффективности визуализации очагов метаплазии при проведении эндоскопического исследования широко применяются: метод хромоскопии с использованием красителей (раствора Люголя, метиленового синего, уксусной кислоты, индигокармина), осмотр слизистой оболочки с использованием увеличительной и узкоспектральной эндоскопии (режим NBI), а также конфокальная лазерная эндомикроскопия. В 2004 году в Праге Международной Рабочей Группой по классификации эзофагитов выдвинуты критерии на основании максимальной длины языков пламени (М) и максимальной длины циркулярного сегмента пищевода Барретта (С). В Пражской классификации учитываются очаги пищевода Барретта протяженностью 1 см и более, находящиеся выше КЭП [4]. По длине сегмента пищевода Барретта выделяют: короткий сегмент – от 1 до 3 см и длинный сегмент – более 3 см. Что касается вопроса лечения ПБ, то обзор отечественной и зарубежной литературы показал, что не существует единых подходов к лечению ПБ. В последнее время широко применяются эндоскопические методики, такие как аргон-плазменная коагуляция (АПК), фотодинамическая терапия, криоабляция, лазерная коагуляция и др. [8]. Тем не менее требуются дальнейшие исследования для оптимизации методов диагностики и лечения ПБ.
Цель исследования
Улучшение результатов лечения пациентов с пищеводом Барретта.
Материалы и методы
В хирургическом отделении клиники Ростовского государственного медицинского университета проходили лечение 125 пациентов с диагнозом – осложненная грыжа пищеводного отверстия диафрагмы, среди них – 27 пациентов с подозрением на метаплазию эпителия. Основными жалобами пациентов являлись изжога, боль за грудиной, отрыжка, регургитация, обусловленные наличием ГЭР. Практически все пациенты отмечали длительный анамнез симптомов гастроэзофагельной-рефлюксной болезни.
Всем пациентам выполнялось эндоскопическое исследование с биопсией подозрительных участков (в том числе применялся метод хромоскопии раствором метиленового синего и использовался режим NBI). Протокол эндоскопического исследования составлялся на основании клинических рекомендаций, принятых на XVIII Съезде Общества Эндоскопических Хирургов России, проходившем в Москве 2015 году [9].
В 19 наблюдениях был подтвержден диагноз пищевод Барретта. Возраст больных колебался от 17 до 72 лет (средний возраст составил 49,9 ± 14,7 лет). Частота заболевания у мужчин составила 47,3 %, у женщин – 52,7 %.
Алгоритм лечения пищевода Барретта включал несколько составляющих (рис. 1).

Рис. 1. Схема лечения пищевода Барретта
В до- и послеоперационном периоде проводилась медикаментозная терапия, направленная на снижение кислотности желудочного сока, нейтрализацию выработанной соляной кислоты, ускорение эвакуации пищи из желудка. Использовались следующие группы препаратов:
- Ингибиторы протонной помпы.
- Антацидные препараты.
- Прокинетики.
Всем пациентам выполнена операция Ниссена или Ниссена – Розетти из лапароскопического доступа, заключающаяся в восстановлении функции кардиального сфинктера, устранение ГЭР и клинических проявлений.
Следующим этапом выполнялись сеансы АПК с использованием электрохирургической станции ERBEVIO 300 Dсо следующими параметрами:
- режим: FORСED APC,
- мощность: 30 – 32 Вт,
- расход аргона: 2 – 2,2 л/мин.
За 1 сеанс проводилась коагуляция пораженного участка площадью не более 4 см². Время манипуляции составляло около 5–7 мин. Всем пациентам сеансы АПК проводились в амбулаторных условиях под внутривенной седацией. После лечения осуществлялся эндоскопический контроль с биопсией.
Результаты и их обсуждение
При эндоскопическом исследовании у 27 пациентов с подозрением на ПБ выявлены признаки метаплазии эпителия и рефлюкс-эзофагит различной степени тяжести. После патоморфологического заключения у 19 пациентов верифицирован эпителий кишечного типа (таблица). У 8 пациентов отмечалась желудочная метаплазия, данным пациентам выполнено хирургическое лечение по поводу грыжи пищеводного отверстия диафрагмы с медикаментозной коррекций и рекомендован эндоскопический контроль с биопсией каждые 3 года.
Распределение пациентов по патоморфологическому заключению
абс.
Кишечная метаплазия без дисплазии
Дисплазия низкой степени
Дисплазия высокой степени
Всего
27
100,0
Патоморфологическое исследование заключалось в фиксации биопсийного материала в забуференном 10 % растворе формалина в течение 24 часов от момента его поступления в патологоанатомическое отделение с последующей спиртовой проводкой по обычной методике. В последующем, фрагменты биопсийного материала заливались в парафин, проводилась микротомия с толщиной среза не более 3 мкм, после чего гистологические срезы окрашивались гематоксилином-эозином, пикрофуксином по Ван Гизон, по Хочкиссу (ШИК-реакция) с докраской альциановым – синим PH-2,0. Данные методики позволяли оценить степень секреторной активности клеток эпителия, накопление в нем кислых и нейтральных мукополисахаридов, состояние бокаловидных клеток при наличии метаплазии, дисплазии (высокой и низкой степени). Оценка морфологических изменений проводилась с использованием полуколичественных методов оценки.
Так как в настоящее время существуют разногласия в патоморфологической оценке степени выраженности дисплазии железистого эпителия при пищеводе Барретта в американских (европейских) и японских исследованиях, мы придерживались рекомендаций международной группы ученых [10].
Из 19 пациентов с ПБ в 12 случаях преобладал длинный сегмент метаплазии эпителия, у 7 пациентов – короткий сегмент. Для адекватной оценки длины сегмента метаплазированного эпителия при выполнении эндоскопического исследования особое внимание необходимо уделять определению истинной границы КЭП. Основными ориентирами КЭП принято считать дистальный край палисадных сосудов слизистой оболочки пищевода и проксимальный край складок кардиального отдела желудка. Наличие признаков рефлюкс-эзофагита, степень инсуффляции при исследовании, а также анатомические варианты сосудов пищевода могут приводить к трудностям в определении КЭП и требуют определенного навыка со стороны специалиста, проводимого исследование. Размеры сегментов ПБ необходимо определять с использованием Пражских критериев. Для лучшей визуализации патологических участков самыми оптимальными и простыми методами являются хромоскопия и осмотр слизистой оболочки пищевода в режиме NBI, не требующие дополнительных затрат и специального оборудования, но достаточно высокоэффективные. Таким образом, в комплекс диагностических мероприятий пациентов с подозрением на ПБ должны обязательно входить: эндоскопическое исследование в обычном режиме и с использованием узкоспектральной эндоскопии, биопсия подозрительных участков через каждые 2 см. С целью стандартизации описания изменений при ПБ необходимо вести протоколы эндоскопических исследований (рис. 2).
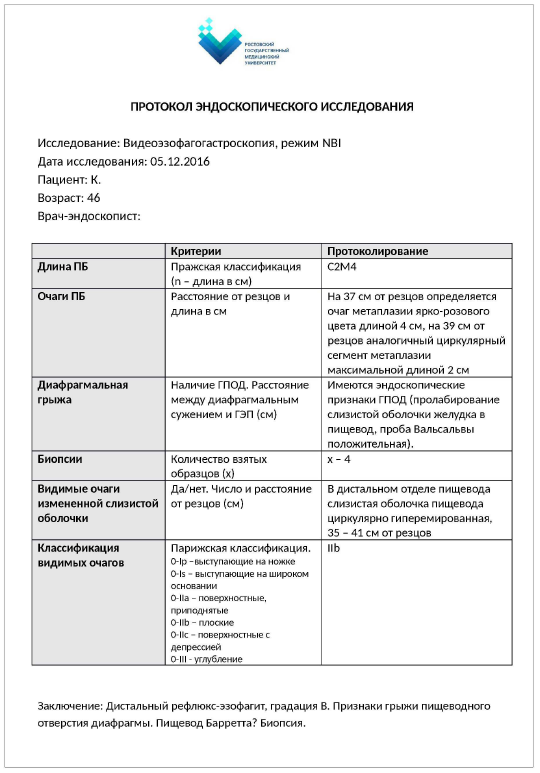
Рис. 2. Пример протокола эндоскопического исследования при пищеводе Барретта
Мы считаем, что лечение ПБ должно иметь комплексный подход, а именно, проведение медикаментозной терапии в пред- и послеоперационном периоде, выполнение антирефлюксных операций и последующие сеансы аргон-плазменной коагуляции [11].
Все наши пациенты в предоперационном периоде получали медикаментозную терапию, длительность которой зависела от степени повреждения слизистой оболочки пищевода. В настоящее время нет убедительных данных относительно регрессии метаплазии эпителия на фоне консервативной терапии. Медикаментозная терапия направлена лишь на уменьшение клинических проявлений рефлюкс-эзофагита.
Антирефлюксная хирургия не приводит к уменьшению сегментов ПБ, но это единственный метод, позволяющий восстановить функцию кардиального сфинктера и устранить гастроэзофагеальный рефлюкс с его последствиями, благодаря чему снижается воздействие кислой среды на слизистую оболочку пищевода, уменьшается воспаление тканей, тем самым создаются благоприятные условия для эффективного выполнения эндоскопического лечения ПБ. Всем пациентам с ПБ показано хирургическое лечение. Операциями выбора мы считаем операции Ниссена или Ниссена – Розетти из лапароскопического доступа. По нашим исследованиям первичное эндоскопическое лечение ПБ, т. е. до выполнения антирефлюксных операций, неэффективно и может приводить к неудовлетворительным результатам.
Через 1–1,5 мес после операции и стихания воспалительных изменений в пищеводе пациентам выполнялась эндоскопическая АПК. В ближайшем периоде после АПК осложнений лечения не отмечено. Болевой синдром после проведения АПК отмечался у 2-х пациентов, но купировался в течение 10-15 мин. применением антацидных препаратов с анестетиком. После выполнения эндоскопической АПК все пациенты возвращались к привычной деятельности на следующий день.
В зависимости от размеров сегмента метаплазии в среднем выполнялись от 1 до 5 сеансов АПК. Каждый повторный сеанс АПК проводили через 1–1,5 мес., это срок, достаточный для уменьшения посткоагуляционного отёка и визуализации границ эпителизации. За 1 сеанс площадь коагуляции поражённого участка составляла не более 4 см 2 , что практически не вызывает болевой реакции и снижает риск развития рубцовых стриктур пищевода. При проведении АПК воздействие начинали с краёв метаплазированного сегмента, что позволяло чётко отграничить патологический очаг, который требовал абляции.
Эндоскопическое лечение ПБ обеспечивает полное удаление очагов метаплазии эпителия. Из всех эндоскопических методик мы отдаем предпочтение АПК, так как данный метод лечения характеризуется высокой безопасностью применения с минимальными побочными эффектами и осложнениями.
В сроке до 3-х лет у 14 пациентов курс лечения полностью завершен. У данных пациентов отмечается полная регрессия метаплазированного эпителия и замещение его типичным многослойным плоским эпителием, подтвержденная гистологическим исследованием (Рис. 3). Еще 5 пациентов продолжают лечение.
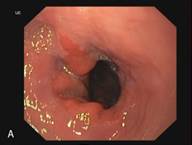
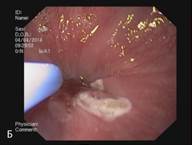
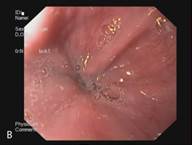
Рис. 3. Эндоскопическая картина пищевода Барретта. А – Эзофагоскопия. Слизистая оболочка пищевода до лечения, сегмент пищевода Барретта. Б – Аргон-плазменная коагуляция. В – Эзофагоскопия. Слизистая оболочка пищевода после лечения, полная регрессия метаплазированного эпителия
Обязательным условием при ведении пациентов с ПБ является эндоскопический контроль с биопсией, который необходимо осуществлять через 3, 6 и 12 мес. после лечения, затем (при длине сегмента более 3 см) – 1 раз в год, при длине сегмента менее 3 см – 1 раз в 2 года.
Выводы
- Комплекс диагностических мероприятий при пищеводе Барретта должен состоять из эндоскопического (с использованием методов, повышающих визуализацию) и морфологического исследований (прицельная биопсия + четырехквадрантный метод забора материала через каждые 2 см).
- Лечение пациентов с пищеводом Барретта должно иметь комплексный подход. Всем пациентам с пищеводом Барретта показано выполнение антирефлюксных операций. В пред- и послеоперационном периоде должна проводиться медикаментозная терапия, направленная на снижение кислотности желудочного сока, нейтрализацию выработанной соляной кислоты и ускорение эвакуации пищи из желудка.
- Аргон-плазменная коагуляция должна проводиться в зависимости от длины сегмента метаплазии, с интервалами 1–1,5 мес., с эндоскопическим и гистологическим контролем. За 1 сеанс площадь коагуляции метаплазированного участка не должна составлять более 4 см².
- Эндоскопический контроль с биопсией должен осуществляться через 3, 6 и 12 мес., а затем (при длине сегмента более 3 см) – 1 раз в год, при длине сегмента менее 3 см – 1 раз в 2 года.

По каким причинам развивается заболевание
Данной патологии подвержены как женщины, так и мужчины в возрасте до 30 лет. Причины раздражения слизистой пищевода просты и порой банальны:
- курение, постоянное вдыхание смол приводит к ороговению клеток, стенок пищевода, развитию воспалительных процессов в нем;
- злоупотребление алкоголем тоже обжигает стенки и раздражает пищевод;
- травмирование пищевода ожогами от приема горячей пищи;
- больные зубы, разрушение которых приводит к плохому пережевыванию пищи, что тоже отражается на пищеводе, раздражая его;
- зубные протезы, постоянное ношение металла во рту сказывается на пищеводе не лучшим образом.

Лейкоплакия считается предраковым состоянием органа, в частности пищевода, требует срочного избавления от вредных привычек и соответственно правильного эффективного лечения. Наиболее частой причиной(48 % случаев) развития рака, как раз и является наличие у человека лейкоплакии, в плазме крови резко повышается содержание железа, стенки пищевода со временем покрываются полипами, которые перерождаясь, влекут за собой развитие доброкачественной, но чаще – злокачественной опухоли.
Лейкоплакия – провокатор рака, протекает стадиями. По форме заболевание может быть блюдцеобразным, поражая пищевод по длине, узловым, по форме напоминающим цветную капусту, инфильтрующим, слизистая становится плотной, образуются язвочки. Новообразования начинают быстро разрастаться по лимфоузлам, метастазировать на слизистой. Язвочки становятся болезненными, образуют трещинки, не хотят заживать. Все это – почва для развития рака. Мужчины заболевают лейкоплакией гораздо чаще, чем женщины.
Как распознать заболевание
Развитие лейкоплакии начинается с полости рта. На небе, щеках, языке, деснах появляется белый или серый налет. Через несколько месяцев формируются бляшки, серозные разрастания, со временем затвердевая и утолщаясь, превращаются в утолщенные участки, возвышающиеся над стенками пищевода. Поверхность стенок пищевода становится эрозивной или бородавчатой, в итоге – малигнизируется, процесс переходит в стадию озлокачествления, то есть в рак.
Заболевание, связанное с курением, в медицине носит название Таппейнера. Сначала поражается небо, потом десны, слизистая оболочка уплотняется, становится серозной, на заднем небе нередко появляются красные точки, выводные протоки слюнных желез становятся похожими на зияющие устья. Особых симптомов лейкоплакия не вызывает, человек не чувствует боли, лишь после приема острой, или горячей пищи может появиться некое неприятное ощущение в пищеводе, может появиться изжога.
Только при первых ранних стадиях рака пищевод начинает переживать дисфагию, у больного начинает обильно выделяться слюна, нарушается глотание пищи, при плохом пережевывании пища встает комом в горле, трудно проходит, только после выпитой воды состояние улучшается, но только до последующего приема пищи. При прохождении пищи через пищевод возникает чувство царапанья, обжига стенок, больные начинают терять все за счет ограниченного поступления пищи и плохого его переваривания. Может наблюдаться токсикоз, отрыжка, неприятные запах изо рта, рвотные позывы. Пищевод начинает сужаться, нарушается обмен веществ.
Раздражителями также могут быть минеральные удобрения, кислоты, щелочи, деготь, нефть, постоянно вдыхаемые человеком в связи со своей трудовой занятостью.
Развитие лейкоплакии может иметь генетическую предрасположенность, нередко усиливают патологию заболевания желудочно-кишечного тракта, недостаток в организме витамина А.
Диагностика и лечение заболевания
При появлении подобных симптомов, а также при уже имеющихся проблемах с желудком, необходимо срочном порядке обратиться к гастроэнтерологу. Обследование тканей пищевода проводится путем гистологического исследования, берется проба тканей на ФГДС.
Лейкоплакия требует комплексного лечения. Важно устранить раздражающие факторы, воздействующие на пищевод, то есть отказаться от курения, начать правильно питаться, избегать приема горячей пищи, резких газированных напитков, удалить все имеющиеся металлические пломбы и протезы.
Если лейкоплакия вызвана эндогенным фактором, в частности патологическими изменениями в желудке, то дополнительно может быть назначена гастроскопия желудка, глотание зонда. Лечение заключается в усиленном применении витаминов А и В, внутримышечно вводится 6% раствор бромистого тиамина. Назначаются седативные препараты: транквилизаторы, настойка валерианки, пустырника, микстура Кватера.
При лейкоплакии нельзя раздражать слизистую пищевод, лечение проводится щадящими мягкими методами.
При отсутствии положительных результатов больному требуется хирургическое удаление эрозивных тканей, ороговевшего эпителия. Возможно назначение лучевой, лазерной терапии, электрокоагуляции, криотерапия. Наиболее эффективен и менее опасен метод криотерапии путем прижигания пораженных участков жидким азотом.

Лучше всего, если лечение заболевания будет проводиться комбинированными способами. При сильном деформировании пищевода врач может назначить операцию. При наличии воспаления, а также для регенерации тканей назначаются противовоспалительные, кератопластические, противовирусные средства в виде использования интерфероновых мазей, внутримышечного введения раствора интерферона.
Лейкоплакия способна перерождаться в злокачественную форму, поэтому нередко в запущенном состоянии и при наличии очевидных симптомов, больного направляют для обследования к стоматологу, онкологу.
Если лечение безуспешно, проявляются рецидивы и признаки пролиферации эпителия, лучевая терапия неизбежна.
Лечение в домашних условиях
Народные методы можно применять только после консультации с врачом. Бесконтрольное лечение травами губительно может сказаться на пищеводе, травмировать его с большей силой. В совокупности с основным лечением народные способы дают порой неплохие результаты.

Хорошо приготовить настойку и соцветий болиголова. Измельчить соцветия, уложить в банку (0,5 литра), залить водкой (5 литра). Хранить в холодильнике до 18 – 20 дней, периодически встряхивая содержимое. Перед применением состав процедить, начинать прием от 1 – 2 капли, разведенных в 0,5 стакане воды, довести прием до 40 капель на 0, 5 стакана воды. В целях профилактики данный настой принимать не рекомендуется.
Взять молодую хвою пихты, ели или сосны, 5 ст. л. добавить воды 0,5 литра, поставить на огонь, проварить 10-15 минут, дать ночь настояться, после чего пить как обычную воду.
При лейкоплакии полезно пить свекольный, или морковный сок. Важно пересмотреть питание, блюда должны быть постными, обязательно нужно кушать тыквенную, пшенную, овсяную каши, картофельное пюре, овощи и фрукты. Яйца, молоко, творог, сметану употреблять в умеренных количествах. От жареной рыбы, жирного мяса, окорочков и алкоголя следует отказаться совсем. Раздражителей на пищевод не должно быть никаких, необходима частая влажная уборка в помещении, стирка белья с добавлением хлорки.
Если появились симптомы: затруднение, боль при глотании, тошнота, рвота прямо из пищевода, застревание пищи, чувство кома в горле, нужно немедленно обратиться к врачу, пройти диагностику, отказаться от курения и прочих продуктов, раздражающих пищевод, пройти полное лечение со всеми предписаниями и указаниями врача.

- Лейкоплакия – это только клинический термин, используемый для обозначения белого пятна или бляшки, возникающее на поверхности слизистых оболочек с плоским эпителием, которое не снимается и не может быть охарактеризована клинически, как любое другое заболевание (например, сифилис, красный плоский лишай, волчанка и др.).
- Лейкоплакия имеет широкий диапазон возможных гистологических проявлений. Это может быть определенная степень утолщения верхних слоев эпителия (гиперкератоза), утолщения срединной зоны эпителия (акантоз) или атрофии, воспалительной клеточной инфильтрации, дисплазии или рака.
- Как и любое состояние, гистологические проявления лейкоплакии могут носить характер обычного простого поражения, так и атипического. При простой лейкоплакии обнаруживается нормальный плоский эпителий. При атипической лейкоплакии – атипический эпителий, с дисплазией.
Различие лейкоплакии полости рта и лейкоплакии пищевода
Лейкоплакия полости рта – это относительно распространенное, безболезненное поражение слизистой оболочки полости рта. Она возникает преимущественно у мужчин среднего и пожилого возраста и прочно ассоциируется с табакокурением и употреблением алкоголя. Всемирная организация здравоохранения считает лейкоплакию одним из наиболее распространенных предраковых или потенциально злокачественных нарушений и фактором риска развития плоскоклеточного рака.
Руководство к действию

![]()
Плюсанул и подписался. И жутковато и интересно.
Автор, ты доктор?
Да, 25 лет в эндоскопии, вот понял, что пришло время делиться опытом
Здравствуйте @drendoscopy,
Скажите пожалуйста, являетесь ли Вы автором данных статей?
Да. Все либо мое, либо компиляция научных статей, но самостоятельная
В таком случае, пожалуйста, не забывайте помечать пост маркером "моё".
@moderator, второй раз уже реклама сайта, пусть деньги платит :) Или рассказывает смешные истории хотя бы!
Не знаю как в гастроэнтерологии, но в дерматологии наличие лейкоплакии расценивается как 100% предрак и пациенты с этой патологией направляются к онкологам. Зачем на развлекательном портале статьи с сугубо медицинской терминологией - науке не известно.
Так паблик то медицинский, да и много тут такого. Моя основная идея рассказать просто о сложном, то что скрыто внутри нас с вами)) Возможно пока не получается совсем просто, но я стараюсь
Метка идентификации человека в экстренной ситуации

Вот такие метки планируем в Новосибирске сейчас раздавать людям в период Короновируса. В метке цифровая карта человека, с набором медицинской информации, необходимой в экстренной ситуации, доступ к которой осуществляется с помощью QR-кода, нанесенного на пластиковую метку. Особенностью продукта являются технологии деперсонализации QRepublik Key, позволяющей защищённо хранить медицинские данные с возможностью их предоставления, а также QRepublik AI – уникальной системы обработки и интерпретации мультиязычной медицинской информации. Вся информация переводится на 24 языка через собственную систему, в зависимости от геолокации.
Уникальная технология деперсонализации данных делает утечку персональных данных математически невозможной и невидимой оператору – непосредственно QRepublik, работа производится за счет сквозного шифрования, информация хранится на QR-коде у пользователя.
Основа системы - облачная платформа, может интегрироваться со сторонними информационными системами.
Очень удобно, когда человек приехал из другого региона, нет необходимости долго искать о нем информацию, тем самым мы имеем тот важный для врача или пациента золотой час.
Ненужные лабораторные исследования [2]
Прошу прощения за долгий перерыв. Для впервые читающих мои посты: около двух месяцев назад в "горячем" я наткнулась на пост девушки (не врача) о том, какие анализы стоит оценить, если вы жалуетесь на усталость и общее недомогание. У меня, как у эндокринолога работающего и в бесплатной поликлинике (всегда стараюсь рационально и экономно для пациента подходить к диагностике), тогда лопнул внутренний возмущатель и я решила постараться уберечь ваши кошельки от лишних трат.
Ранее мы обсуждали щитовидную железу, теперь пойдем дальше. Вероятно во время пандемии интерес к остальной медицине близок к нулю, но тем не менее.
Один из абзацев того самого поста, гласит, что для того, чтобы "провериться на диабет и преддиабет (инсулинрезистентность)", необходимо оценить глюкозу, инсулин, гликированный гемоглобин, а не только "один единственный анализ на глюкозу (как делают в поликлиниках), который покажет не норму, только если вы уже точно диабетик". Кроме того надо обязательно рассчитать индекс HOMA, без него никак. Давайте разбираться.
Начнем, как полагается, с начала. Когда-то давно на Олимпе биохимии придумали глюкозу и обязали ее быть благом для организма в нормальных количествах, и злом в повышенных. Тогда же на Олимпе анатомии придумали поджелудочную железу, которая способна вырабатывать инсулин, который помогает удерживать строптивую глюкозу на нормальном уровне. Но, как это и полагается, на Олимпах кто-то хотел уйти домой пораньше и схалтурил. Оказалось, что система глюкоза-инсулин работает не всегда: вопреки ожиданиям создателей, уровень глюкозы-таки может неминуемо увеличиваться. Этот баг в Небесной канцелярии косяков назвали сахарным диабетом (СД) и поручили смертным врачам самим во всем разбираться. В этом посте я коснусь только СД 2 типа, хотя на самом деле сахарных диабетов огромное множество.
Итак, что может натолкнуть вас на мысль о том, что у вас сахарный диабет (любого типа).
Прежде всего жалобы. Классический набор: жажда, сухость во рту, учащенное мочеиспускание, что, разумеется, логично - больше пьем, больше бегаем в туалет. Очень часто мои пациенты-дебютанты жалуются на онемение пальцев рук или ног, ощущение ползания мурашек, судороги. А еще чаще ни на что не жалуются: "Доктор, я себя прекрасно чувствую, наверно в лаборатории перепутали, тут глюкоза 18ммоль\л, такого быть не может". К сожалению, может. Да, чуть не забыла: еще одна характерная жалоба – всеми любимая слабость, упадок сил.
Логичный вопрос: "Вдруг я тот самый случай, когда симптомов нет, а заболевание есть?". Иными словами, как заподозрить у себя диабет, если жалоб нет, а заподозрить хочется.
Первый и самый главный признак – вы идеальный. Идеальный шар. Да, пациент с лишним весом с огромной вероятностью свалится в диабет. Второй признак – возраст: чем старше (и больше) пациент, тем больше вероятность развития диабета. Далее наследственность: если у вашей мамы и трёх ее сестер есть диабет второго типа, то и у вас он тоже может быть. Но обращаю ваше внимание, что роль играет совокупность данных признаков. Если диабет был только у вашего прадедушки, а вам 19 лет и вы как осинка тоненький, то не стоит разводить лабораторную панику (пока).
Что мы оцениваем, подозревая данную патологию?
1. Уровень глюкозы венозной крови натощак. До 6,1 ммоль\л – норма, от 7,0 – сахарный диабет.
2. Гликированный гемоглобин (показывает средний уровень глюкозы за последние 3 месяца). До 5,6% – абсолютная норма, более 6,5% – сахарный диабет. (Обращаю ваше внимание, что в поликлинике смотрят не только уровень глюкозы, как утверждает автор того-самого-поста).
Казалось бы все просто, но грамотного искателя болезней не обманешь. А что делать, если уровень глюкозы натощак, например 6,5 ммоль? Это не норма, но и не сахарный диабет.
Тогда на помощь приходит простейший лабораторный прием – оральный глюкозотолерантный тест. Натощак пациент сдает венозную кровь, тут же в лаборатории выпивает раствор глюкозы (это абсолютно безопасно, но максимально мерзко), затем через два часа вновь сдает кровь из вены. Что принципиально важно – накануне исследования специальная диета не соблюдается, а в течение двух часов между заборами крови пациент никуда не уходит и ничего не кушает.
Получаем результат с двумя цифрами: до и после (кому интересно, интерпретацию теста можно найти в интернетах). Данное исследование помогает уточнить диагноз -- либо вы здоровы, либо у вас диабет, либо преддиабет (когда глюкоза уже не в норме, но до диабета еще не дотягивает).
Без указания цифр и заумных терминов скажу, что преддиабет бывает двух типов и я называю сие состояние "диагноз предупреждения". Это такая яркая красная пометочка в вашей истории болезни. Если вы узнаете, что у вас есть этот недуг – пора принимать меры, которые уберегут вас от развития непосредственно диабета. Дело в том, что основная терапия преддиабета это физическая активность и соблюдение диетотерапии. Этого хватает, чтоб не рухнуть в диабет, поверьте. Но! Я сторонница того, чтоб помочь организму медикаментозно (препарат и дозировку по понятным причинам указывать не буду), потому что далеко не у всех есть возможность и сила воли, необходимые для соблюдения нового режима. В общем, если доктор сказал: "У вас преддиабет", значит ваш организм кричит: "Подумой, что в рот суёшь, нам еще жизнь жить"!

Заметили, что я ни слова пока не написала об инсулинрезистентности (ИР)?
Во-первых, инсулинрезистентность не является преддиабетом! ИР – сниженная чувствительность клеток организма к инсулину, иными словами для того, чтоб поддерживать уровень глюкозы, теперь необходимо больше инсулина, чем раньше. Почему? Потому что пациент стал круглее (или шарее), чем раньше. Одним из основных факторов ведущих к развитию ИР снова является ожирение. И вот, что интересно: если у человека имеется абдоминальное ожирение (жирок на пузике: у женщин окружность талии более 80см, у мужчин более 94см) вероятность наличия ИР близка к 100%. Что делать? Уменьшать количество жирка на пузике, очевидно. Как? Физическая активность и диета. Инсулинрезистентность у худых – немного другая история, в рамках данного поста касаться ее не хочется.
Еще раз: сахарный диабет\преддиабет – состояния, при которых уровень глюкозы не в норме; инсулинрезистентность -- состояние, при котором глюкоза в норме, но поджелудочная железа вынуждена работать усерднее, чтоб выдать больше инсулина, чтоб тот в свою очередь удерживал глюкозу от взлётов.
И снова внимательный читатель обратит внимание на то, что я не пишу об определении уровня инсулина. Почему? Потому что его уровень никак не повлияет на мою тактику ведения данного пациента, поскольку я и так предполагаю, что у "большого" пациента будет "большой" инсулин. Снова возвращаемся к нашим баранам: бесплатно инсулин не оценивается, пациент с лишним весом тратит деньги, приносит мне свои циферки, я вижу повышение, киваю головой, грозно говорю: "Диета! Активность!"; пациент не приносит циферки, я говорю: "Диета! Активность!". Кроме того, обращаю внимание на то, что уровень инсулина крайне лабилен: он меняется в течение дня, зависит от состояния печени и имеет короткий срок жизни. Короче говоря, не стоит без назначения врача определять уровень инсулина, особенно если вы по форме шарик. Да, я знаю, что есть любители оценивать инсулин, оценивать неоднократно, со словами: "О, как я вас хорошо лечу! Вот это я молодец! Инсулин был 10, стал 8!". На самом же деле, можете быть уверены, что, чем больше вы скинете килограммов, тем больше вы скинете цифр у уровня своего инсулина.
Кроме того, в-том-самом-посте обязательно рекомендуется подсчет индекса HOMA (математический показатель наличия ИР). Но здесь ситуация аналогична, у полного пациента индекс с огромной долей вероятности будет повышен, однако эта цифра вновь не повлияет на тактику ведения.
Также, периодически на прием заскакивают пациенты с определенным с-пептидом. По сути своей С-пептид – это небольшой кусочек инсулина, т.е. логика в целом такая же. Самое важное отличие – с-пептид долгожитель, в отличие от инсулина, однако опять же для его оценки существуют четкие показания, а "просто так" не входит в этот список.
Когда есть смысл искать у себя диабет?
1. Если у вас есть жалобы:
-сухость во рту, жажду,
-ощущение ползания мурашек,
-длительно незаживающие раны,
-не менее нестерпимая слабость и вялость.
2. Если у вас нет жалоб, но вы уже не так молоды как 40 лет назад, обладатель лишних килограммов и сладкой наследственности.
Какие анализы имеет смысл сдать перед ПЕРВИЧНЫМ походом к эндокринологу, если вам кажется, что вы обладатель диабета:
-глюкоза венозной крови,
-если какой-то из этих показатель не в норме, то оральный глюкозотолерантный тест;
От себя добавлю, что, у пациентов с ненормальным уровнем глюкозы я всегда требую общий анализ мочи, биохимический анализ крови ( как минимум АЛТ, АСТ, креатинин, Щф), но на постановку диагноза это никак не влияет, влияет на мою тактику ведения.
Какие анализы точно не стоит сдавать перед ПЕРВИЧНЫМ походом к эндокринологу?
-расчет индекса HOMA, Caro, QUICKI и любых других существующих индексов.
Спасибо, что дочитали, надеюсь кому-нибудь будет полезно! Если будут вопросы в комментариях, постараюсь ответить.
Читайте также:


