Интерферон при бактериальной инфекции

АМИКСИН ® — современное противовирусное и иммуностимулирующее средство; способствует образованию в организме четырех видов интерферонов (альфа, бета, гамма и лямбда).
Узнать подробнее про АМИКСИН ® …


Противовирусные препараты с иммуностимулирующей активностью могут рекомендоваться как при лечении гриппа, так и других ОРВИ. С их помощью можно сократить сроки болезни и предотвратить развитие осложнений.

Прием противовирусного препарата АМИКСИН ® возможен на любой стадии простуды и гриппа по рекомендации врача.
Как принимать препарат?


В сезон простуды и гриппа прием противовирусных и иммуномодулирующих препаратов помогает снизить вероятность заболевания.

АМИКСИН ® — современный противовирусный и иммуномодулирующий препарат, используемый в комплексной терапии целого ряда вирусных инфекционных заболеваний, в том числе гриппа, ОРВИ и герпеса.
Подробнее о препарате…


Иммуномодулирующие препараты — одни из важных составляющих комплексной терапии гриппа и других ОРВИ.
Функции и механизм действия интерферона в человеческом организме
Интерферон — это белковая молекула, которая обеспечивает противовирусный иммунитет. При этом она обладает неспецифической активностью, то есть действуют не на возбудителя какого-то конкретного заболевания, а на все вирусные частицы в целом. Если сказать обобщенно, то интерферон — универсальный защитник организма, который начинает действовать еще до того, как в работу включатся остальные звенья иммунитета [1] . Препараты интерферона применяются даже в терапии онкологии: они подавляют опухолевый рост.
Клетки вырабатывают этот защитный белок в ответ на действие вирусов, бактерий, опухолевых клеток или продуктов их метаболизма. Стимулировать их выработку могут и лекарственные препараты — индукторы интерферона. Молекулы последних, попадая в кровь и межклеточную жидкость, связываются с рецепторами зараженных или поврежденных клеток. Они запускают сложный каскад реакций, приводящих к образованию специфических белков. В результате клетка перестает воспроизводить вирусные частицы, расщепляет их генетическую структуру, а поверхность этой клетки становится менее проницаемой для внутриклеточных паразитов.
Кроме действия на сами зараженные клетки, интерфероны стимулируют активность других звеньев иммунитета, контролируют воспалительную реакцию [2] и даже могут защитить организм от опухолей. Это свойство активно изучают и уже используют для борьбы с некоторыми видами рака [3] .
Молекулы интерферона отличаются между собой по генетической структуре, типу клеточных рецепторов, на которые они действуют, даже по участкам ДНК, которые кодируют их состав. Все интерфероны делят на 3 типа.
- К первому типу относят альфа-интерферон, который имеет 13 различных структурных вариантов, а также бета-, каппа-, эпсилон- и омега-.
- Второй тип представлен только одним типом, гамма-интерфероном.
- Относительно недавно, в 2002 году, был открыт и третий тип молекул, лямбда-. Это отдельное семейство интерферонов, которое отличается от всех предыдущих генетическим строением и даже типом рецепторов, с которыми они взаимодействуют. Но по своей биологической активности лямбда-интерфероны очень похожи на первый тип [4] .
Не стоит относиться к интерферонам как к панацее от всех бед. Во-первых, некоторые вирусы могут подавлять образование специфических белков внутри зараженных клеток, что значительно снижает эффективность противовирусной защиты.
Поэтому прежде чем начинать лечение препаратами интерферона, нужно внимательно изучить пользу и возможный вред от их приема.
Лекарственные средства на основе интерферона доказали свою эффективность [5] в лечении широкого круга заболеваний: герпетических инфекций, ВПЧ, острых и хронических форм вирусного гепатита, рассеянного склероза, волчанки, гриппа и многих других вирусных и бактериальных инфекций. Применяют интерферон и при терапии онкологических заболеваний, а также СПИДа. И это притом, что по меркам медицины открыли его совсем недавно. Это произошло в 1957 году при проведении опытов на мышах. Ученые обратили внимание, что животные, заразившиеся одним вирусом, становились невосприимчивы к другому вирусному заболеванию. Это явление было названо интерференцией, а вещества, которые ему способствовали — интерферонами. Оказалось, что интерфероны вырабатываются не только у мышей, но и у всех млекопитающих, в том числе у человека. Началось изучение возможности промышленного производства веществ, обладающих противовирусным эффектом.
Однако долгое время применение интерферонов было ограничено из-за несовершенства процедуры их получения. Выделять это вещество из крови человека-донора было сложно, дорого и неэффективно.
В 1980 году в Японии впервые использовали для производства интерферона специально выращенную культуру лимфобластных клеток. А в 1981 году в США вместо клеток человека использовали культуру дрожжевых грибков. С помощью генной инженерии в геном ввели ген, который кодирует производство молекулы интерферона. Это позволило значительно упростить производство препарата [8] .
По способу производства существует четыре основных разновидности этого препарата: лейкоцитарный, лимфобластоидный, рекомбинантный и пегилированный.
После получения такой препарат очищают и концентрируют. В него могут входить все виды интерферонов и другие биологически активные вещества. Это одновременно и плюс, и минус. Преимущество такого препарата — его высокий потенциал биологического действия. Недостаток — высокая вероятность побочных эффектов при внутримышечном введении.
Лимфобластоидный интерферон получают не от человека-донора, а из культуры лимфобластных клеток, которые также обрабатывают веществами, стимулирующими иммунный ответ. Такие препараты содержат определенное соотношение различных видов интерферона и не так часто вызывают побочные эффекты.
Пегилированные, или ПЭГ-интерфероны — это рекомбинантные белковые молекулы, соединенные с полиэтиленгликолем. Такое соединение увеличило срок действия интерферона в организме.
ПЭГ растворим в воде, не вступает в биологические реакции в организме и не вызывает иммунного ответа. При присоединении ПЭГ молекула интерферона значительно увеличивается в размерах. А это, в свою очередь, увеличивает период полувыведения препарата.
Объединить интерфероны в однородные группы по методу получения, формам выпуска и показаниям не получится. Каждый препарат имеет свои особенности применения, эффективность при определенных заболеваниях. В зависимости от степени очистки и других факторов какие-то препараты с одним и тем же видом иммуноглобулина могут применяться только местно, а какие-то можно использовать в виде инъекций.
Поэтому при выборе препарата интерферона стоит ориентироваться не только на общую характеристику группы веществ, но в первую очередь на рекомендации врача и инструкцию по применению конкретного препарата.
Интерферон в виде инъекций применяют при системных заболеваниях, таких как гепатит, опухоли или рассеянный склероз. Препарат в виде капель в нос подходит для лечения риносинуситов и профилактики ОРВИ. Капли в глаза помогут при конъюнктивите. Суппозитории можно использовать при многих заболеваниях, в том числе у детей. А гель подходит для смазывания носа или кожи.
Интерфероны защищают организм от вирусов, бактерий и опухолевых клеток. Они обладают сложным биологическим действием. Но современная медицина научилась создавать аналогичные вещества и использовать их. Однако подбор подходящего препарата — задача, которую может решить только врач.
Преимущества этого препарата — максимум выработки интерферона уже в первые сутки от начала приема и активация четырех видов интерферонов. Увеличение концентрации интерферонов в отдельных органах может достигаться уже через 4 часа.
Все индукторы интерферона обладают индивидуальными характеристиками, показаниями и противопоказаниями. Поэтому препарат нужно выбирать внимательно, только после прочтения инструкции. С особой осторожностью нужно подходить к выбору лекарства, если его нужно принимать детям. Для детей существуют отдельные формы выпуска.
И, конечно, никогда нельзя заниматься самолечением. Любые препараты нужно принимать только по согласованию с врачом.

В холодное время года на первый план выступает проблема иммунитета и сопротивляемости болезням. Слово иммунитет сейчас знают все, но не многие знают, насколько сложная и многоуровневая система включается в это понятие. Кроме того, многие считают, что если ребенок болеет, значит, иммунитет у него плохой и его нужно срочно повышать. При этом терроризируют врача, требуя назначить ребенку волшебную таблетку от всех болезней, укрепляющую иммунитет. Так вот, таких таблеток нет, и в большинстве случаев болезней ребенка не нужно никаких укреплений — нужна просто рациональность и адекватная помощь по лечению и долечиванию болезней. Иммунитет можно тренировать и формировать так же как мышцы тела, вот этим и должны заниматься врачи и родители, а не искать чудо-пилюли.
Что же такое система иммунитета?
Иммунитетом называется невосприимчивость организма человека к инфекционным и неинфекционным агентам. Иммунитет не только борется с вирусами, бактериями, но и атакует глистов и раковые клетки организма. К сожалению, если с микробами и вирусами чаще всего он может справиться и самостоятельно, но вот глисты и опухоли полностью ему пока неподвластны.
Иммунитет принято разделять на две большие группы. Одна из них — врожденный иммунитет. Это когда организм из-за своих генетических особенностей не может болеть какими-то болезнями — например, люди не болеют чумой собак. Эти особенности закреплены на уровне генов и передаются по наследству от родителей к детям. Вторая часть иммунитета — это приобретенный, именно тот, о котором в большинстве своем и ведется речь, при упоминании этого слова.
Приобретенный иммунитет разделяется на две большие группы — пассивный и активный.
Пассивный иммунитет — это получение организмом готовых антител к инфекциям при помощи инъекции специальной сыворотки или от матери плоду и ребенку грудным молоком.
Активный иммунитет вырабатывается в течение жизни как результат болезни или вакцинации (прививки). Организм нарабатывает особые вещества — антитела, которые связываются с антигенами. Антигеном для организма может быть и вирус, и микроб, и простейшее, и даже компоненты собственных клеток, которые больны, повреждены и даже которые здоровы, при поломках в иммунной системе. Комплексы антиген-антитело являются безвредными для организма, обычно растворимы в плазме крови и выводятся из организма почками или печенью. За счет иммунитета организм взрослого и ребенка сопротивляется инфекции. Именно за счет работы иммунитета у нас повышается температура, развивается воспаление, и именно за счет иммунитета происходит формирование сыпи (аллергии). Просто механизмы иммунитета в каждом случае свои.
Основными клетками иммунитета являются белые клетки крови — лейкоциты и лимфоциты. Частично в механизмах иммунитета задействованы и тромбоциты. Кроме того, в формировании иммунитета задействованы многие биологические жидкости и вещества — слюна, слеза, слизь желудка и кишечника, пот и кровь.
Лейкоциты работают в зонах воспаления. Там, где возбудитель проникает и разрушает клетки организма они поглощают (поедают) поврежденные клетки, микробов и формируют гной и воспаление. Лимфоциты осуществляют синтез иммуноглобулинов — особых веществ, которые участвуют в обезвреживании возбудителей и в запоминании их на будущее. Это позволяет формировать в дальнейшем стойкий иммунитет — если возбудитель попадет повторно — болезнь уже не разовьется. По уровню этих самых иммуноглобулинов на сегодня и определяют наличие иммунитета к многим болезням и эффективность вакцинации.
Кроме иммуноглобулинов, организмом вырабатывается ряд биологически активных веществ, которые помогают противостоять инфекции. Это интерфероны, лизоцим, система комплемента и другие.
О системе интерферонов мы и поговорим более подробно…
Эта система включается в борьбу с вирусами одной из первых. Интерферонами называются особые группы белковых молекул, производимые клетками иммунной системы человека. Они предназначены для борьбы с бактериями, вирусами, трансформированными и нежизнеспособными клетками организма. Интерфероны представляют собой вид оружия, при помощи которого мы можем противостоять болезнетворным бактериям, паразитам и даже раковым клеткам. Интерферон не только самостоятельно борется со зловредными микроорганизмами и злокачественными опухолями, но и активирует другие факторы защиты — макрофаги и естественные киллеры.
Как работает интерферон? Интерферон — продукт самого организма. Было установлено, что интерферон вырабатывается любыми клетками организма как защитное средство в первые же часы внедрения в клетку каких-либо генетически чуждых агентов (антигенов), чужеродных белков и нуклеиновых кислот. Особенно интенсивно клетки синтезируют интерферон в тех случаях, когда такими антигенами оказываются вирусы.
После заражения клетки вирусом, он начинает усиленно размножаться, но одновременно с вирусом клетка начинает продуцировать и защиту в виде интерферонов. Пораженная вирусом клетка погибает из-за проникновения в нее вируса, но при этом усиливает защиту соседних клеток от вирусов. Выделяемый погибающей клеткой интерферон преследует вирусы, защищая соседние клетки. После контакта с интерфероном каждая клетка погибает вместе с проникшим в нее вирусом, но вирус при этом не оставляет потомства. Интерферон не проникает в клетки, а воздействует на особые рецепторы на мембранах. В результате он вызывает продукцию в этих клетках особых веществ, подавляющих размножение вирусов. И клетки становятся негодными для жизни вируса. Поражаемая вирусом клетка погибает, потому что в ней был вирус, при этом защищает собой другие клетки. Выделяющийся при этом интерферон сцепляется с вирусом. И если тот проникнет в другую клетку — она погибнет, не дав вирусу размножить потомство. Кроме того, интерферон током крови разносится по организму, актируя систему иммунитета и продукцию антител.
То есть, сам интерферон на вирусы не действует, но он помогает клеткам активно защищаться от заражения вирусными частицами. На каждую клетку достаточно даже одной молекулы интерферона для защиты, потому что интерферон обладает высокой биологической активностью.
Но тут очень важно понимать, что интерферон неспецифичен, он универсален, действует не избирательно против какого-то вируса, а защищает организм от любых вирусов (в отличие от многих иммуноглобулинов, которые строго специфичны для конкретного вируса или бактерии). Он вырабатывается в ответ на любое воздействие, не важно, вирус ли это, микроб или повреждение клетки. Но, даже не смотря на это, помощь интерферонов для организма крайне необходима, т. к. синтез антител в ответ на внедрение инфекции сильно запаздывает. Антитела начинают активно нарабатываться через несколько суток, на это время борьбу с инфекцией осуществляют интерфероны. Они начинают действовать с первых часов болезни и их концентрация прогрессивно увеличивается.
Интерферон можно получить искусственно, культивируя его на особых клетках крови. Это позволило применять его в качестве лечебного препарата. Однако, следует помнить, что в больших дозах он тормозит рост и дифференцировку любых клеток организма, и не только опухолевых. При применении интерферонов они практически не предотвращают развития вирусной инфекции, однако существенно сокращают время болезни и ее тяжесть.
Интерферон получают путем экстрагирования из лейкоцитов донорской крови человека. Его очищают от балластных и опасных веществ, затем концентрируют и делают высокоактивным. Это дает возможность использовать его более успешно.
В связи с такими трудностями стали применяться особые вещества — индукторы (стимуляторы) выработки собственного интерферона организма. Одними из таких препаратов являются кагоцел, амиксин, циклоферон и др…
Наиболее перспективным и безопасным на сегодня является использование синтетических, полученных с помощью особых рекомбинантных генно-инженерных технологий. Они не имеют даже чисто теоретического шанса на перенос инфекций с кровью.
Всегда нужно помнить, что это лекарственные препараты, имеющие побочные эффекты, и применяться они должны только по рецепту врача.
А. С. Боткина, канд. мед. наук, доц. кафедры госпитальной педиатрии им. акад. В. А. Таболина ФГБОУ ВО им. Н. И. Пирогова Минздрава России, Москва
Резюме: актуальность проблемы респираторных вирусных заболеваний обусловлена их чрезвычайно широким распространением, зачастую тяжелым течением, возможностью развития жизнеугрожающих осложнений и высоким экономическим ущербом, наносимым обществу в целом. В статье в сравнительном аспекте рассматриваются различные лекарственные средства, используемые в комплексной терапии острых респираторных вирусных инфекций у детей.
Ключевые слова: респираторные инфекции, индукторы интерферона, иммуномодуляция, дети, Циклоферон®
Abstract: the urgency of the problem of respiratory viral diseases is due to their extremely high spread, often severe, the possibility of developing life-threatening complications and the high economic damage caused to society as a whole. The article in a comparative aspect discusses the various drugs, used for the prevention and treatment of acute respiratory viral infections in children.
Keywords: respiratory infections, interferon inductors, immunomodulation, children, Cycloferon®
Этиологическими факторами данной группы заболеваний являются около 300 эпителиотропных вирусов, из которых наиболее часто встречающимися у детей являются риновирусы, парагрипп, аденовирусы, грипп. В последние годы нарастает удельный вес таких возбудителей, как корона-, бока- и метапневмовирусы. Также ежегодно увеличивается доля различных микст-инфекций, вызывающих более тяжелое по течению респираторное заболевание, что существенно усложняет диагностику и лечение таких пациентов.
Клинические симптомы респираторных вирусных инфекций у детей во многом похожи и проявляются различной по степени тяжести и длительности лихорадкой, интоксикацией, катаральным синдромом и поражением дыхательных путей (табл. 1).
Таблица 1. Тропизм различных вирусов, вызывающих ОРВИ
| Вирус | Наиболее часто поражаемый орган |
| Гриппа | Трахея, носоглотка, сосуды |
| Парагриппа | Гортань |
| Аденовирус | Глотка, конъюнктива, кишечник |
| Риновирус | Полость носа |
| Реовирус | Носоглотка, кишечник |
| Коронавирус | Носоглотка, бронхи, кишечник |
| РС-вирус | Бронхиолы, альвеолы |
| Бокавирус | Носоглотка, кишечник |
| Метапневмовирус | Носоглотка, трахея, бронхи |
При гриппе на первый план выходит выраженный интоксикационный синдром и лихорадка, аденовирусная инфекция характеризуется болью в горле, конъюнктивитом, продуктивным кашлем, нередко - развитием обструктивного синдрома и болями в животе; при парагриппе часты ларингиты с развитием стеноза гортани, а при респираторно-синцитиальной инфекции -бронхит и/или бронхиолит с выраженным и длительным обструктивным синдромом. Однако различия симптоматики в зависимости от этиологии вирусного заболевания не всегда четко различимы, следовательно, практикующему врачу важно иметь в своем арсенале средства, одинаково эффективные для профилактики и лечения как гриппа, так и других ОРВИ.
Выбор метода лечения ОРВИ у детей зависит от возраста ребенка, клинической картины заболевания, выраженности симптомов, степени тяжести и наличия осложнений. Лечение обязательно должно включать режим, диету, медикаментозную и немедикаментозную терапию. Лекарственная терапия респираторных заболеваний у детей ориентирована на использование всего арсенала современных препаратов, отвечающих определенным критериям [3, 4]:
- высокая эффективность относительно большинства возбудителей;
- минимальный спектр побочных эффектов;
- отсутствие токсичности;
- сочетание противовирусного и иммуномодулирующего эффекта;
- наличие различных лекарственных форм;
- этиотропные, действующие на возбудителя заболевания;
- патогенетические (иммуномодулирующие), исправляющие нарушения системы иммунитета, возникающие и развивающиеся в процессе болезни;
- симптоматические, предназначенные для купирования отдельных симптомов заболевания.
Таблица 2. Механизм действия различных противовирусных препаратов, применяемых при ОРВИ
| Действие | Механизм действия | Препарат |
| Ингибиторы нейраминидазы | Конкурентно и избирательно ингибирует нейроминидазу, что нарушает проникновение вируса в здоровые клетки, тормозит выход вирионов из инфицированной клетки | Осельтамивир, занамивир |
| Блокатор М-йонного канала (адамантаны) | Блокирует специфические ионные М-2 каналы, что приводит к нарушению процесса дезинтеграции вириона и высвобождению рибонуклеопротеида | Ремантадин, орвирем |
| Блокатор слияния, индуктор ИФН | Ингибирует слияние липидной вирусной оболочки с клеточной мембраной | Арбидол |
| Ингибитор РНК и ДНК вирусов | Конкурентное подавление образования гуанозин трифосфата, приводящее к нарушению синтеза вирусных РНК и ДНК | Рибавирин |
Так, ингибиторы нейраминидазы обладают избирательной активностью только против вирусов гриппа типа А и В, эффективны при назначении не позднее 48 ч от начала клинических симптомов заболевания, оказывают раздражающее действие на слизистую оболочку респираторного и пищеварительного тракта, вызывают тяжелые аллергические реакции вплоть до развития токсического эпидермального некролиза, а также имеют высокую стоимость. Препараты из группы адамантинов также обладают избирательной активностью против вируса гриппа А, вызывают побочные эффекты со стороны желудочно-кишечного тракта в виде тошноты и рвоты, нервной системы, проявляющиеся галлюцинациями и психозом, аллергическими реакциями. Кроме того, все противовирусные препараты эффективны только при раннем их применении, не позже 24-48 ч и приводят к возникновению штаммов вирусов с низкой чувствительностью или резистентностью к терапии. Лекарственная устойчивость является результатом мутаций вирусов и развивается, как правило, при многократном использовании препарата [5, 6].
Основными патогенетически действующими группами препаратов являются интерфероны и их индукторы. Интерфероны - это группа биологически активных белков или гликопротеидов, синтезируемых клеткой в процессе защитной реакции на чужеродные агенты (экзогенные и/или эндогенные). Образование и действие интерферона составляет важнейший механизм врожденного (естественного) иммунитета. Доказано, что течение и исход вирусных инфекций во многом зависит от способности системы интерферона быстро реагировать на внедрение возбудителя [7]. Всего в настоящее время описано более 100 различных эффектов интерферонов, основными из которых являются:
- подавление роста внутри- и внеклеточных инфекционных агентов вирусной и невирусной (хламидии, простейшие, бактерии) природы;
- антипролиферативная активность;
- антитуморогенный эффект;
- антимутагенный эффект;
- антитоксическое действие;
- радиопротективный эффект;
- иммуномодулирующий эффект(подавление или усиление продукции антител, стимуляция макрофагов, усиление фагоцитоза и др.).
Рис. 1. Побочные эффекты препаратов интерферонового ряда 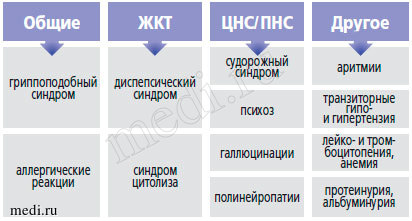
Таблица 3. Классификация индукторов интерферона (Ершов Ф.И., Романцов М.Г., Петров А.Ю., 2008)
| Химическая природа | Препарат |
| А. Синтетические соединения с основной интерферон-индуктивной активностью | |
| Низкомолекулярные: Флуореноны Акриданоны Олигопептиды Производное имидазо (4,5-С) квинолина | Амиксин Циклоферон® аллокин-альфа имиквимод |
| Полимеры (дс-РНК) | Полудан, полигуацил |
| Б. Природные соединения с основной интерферон-индуктивной активностью | |
| Полифенолы | Кагоцел, мегосин, саврац рагосин, гозалидон |
| Полимеры (дс-РНК) | Ридостин, ларифан |
| Производные флавонидов и аминокислот | протефлазид |
| В. Иммунотропные препараты с вторичной интерферон-индуктивной активностью | |
| Т-миметики | Тимоген, тактивин, изопринозин, гроприносин, иммунофан |
| Иммуномодуляторы бактериального происхождения - эубиотики | Лактобактерин, биоспорин |
| Вакциноподобные препараты | Бронхомунал, рибомунил, ИРС-19, уроваксом |
| Липополисахариды | Пирогенал, продигиозан |
| Производные нуклеиновых кислот | Натрия нуклеинат |
| Препараты пурина и пиримидина | Метилурацил, пентоксил |
| Производные бензимидазола | Дибазол |
| Производные индола | Арбидол |
| Растительные иммунокорректоры | Родиола розовая, экстракт эхинацеи |
| Г. Препараты других фармакологических групп с вторичной интерферон-индуктивной активностью | |
| Метилксантины | Теофиллин, эуфиллин, дипиридамол, кофеин |
| Производные изохинолина | Папаверин, дротавирин |
| Производные бензофурана | Кордарон |
| Производные хромена | Интеркордин |
Немаловажным является то, что образование эндогенного интерферона при введении его индукторов является более физиологичным процессом, чем повторное введение экзогенных интерферонов, которые, помимо побочных эффектов, быстро выводятся из организма и угнетают образование собственных (аутологичных) интерферонов по принципу отрицательной обратной связи, что может привести к формированию хронического инфекционного процесса в организме ребенка [10]. Имея основные свойства интерферона, его индукторы не обладают антигенностью и даже при однократном введении обеспечивают длительную циркуляцию синтезированных цитокинов на терапевтическом уровне. Стимулированный ими синтез эндогенного интерферона находится под контролем интерлейкинов и белков-репрессоров и не вызывает гиперинтерферонемии и развития связанных с ней побочных эффектов. Проведенные исследования показали, что индукторы интерферона обладают универсально широким диапазоном фармакологической активности, обладая одновременно прямым противовирусным и иммуномодулирующим действием. Введенные в организм индукторы интерферона стимулируют выработку эндогенного интерферона трех типов (α,β,γ) в разных пропорциях, что зависит от химической структуры индуктора. В зависимости от времени продукции интерферона в крови различают индукторы ранние (4-8 ч) и поздние (18-24 ч) [11].
Среди индукторов интерферона в профилактике и лечении ОРВИ у детей широко применяется препарат Циклоферон®, являющийся синтетическим производным акридонуксусной кислоты. Препарат повышает уровень интерферона α/β-типа в органах и тканях, содержащих лимфоидные элементы: в слизистой тонкого кишечника, селезенке, печени, легких, активирует стволовые клетки костного мозга, стимулируя образование гранулоцитов, преодолевает гематоэнцефалический барьер. Циклоферон® обладает чрезвычайно широким спектром биологической активности: прямым противовирусным, иммуномодулирующим и противовоспалительным действиями. Прямая противовирусная активность Циклоферона® доказана относительно различных респираторных вирусов и гриппа А и В, вируса простого герпеса 1-го и 2-го типов, цитомегаловируса, гепатитов В и С, клещевого энцефалита, вируса папилломы человека. Препарат нарушает репликацию вирусов, блокирует инкорпорацию вирусных ДНК и РНК в капсиды, что приводит к увеличению количества дефектных вирусных частиц и снижает вирус-индуцированный синтез белка в клетках. Иммунотропное действие препарата реализуется путем активации фагоцитов, Т-лимфоцитов и NK-клеток, нормализации баланса между CD4+- и СБ8+-клетками, снижении уровня В-лимфоцитов в периферической крови, с одновременным повышением синтеза высокоаффинных антител и индукции синтеза мРНК для ИФН-γ[12; 13]. Противовоспалительное действие Циклоферона® обусловлено ингибированием основных провоспалительных цитокинов (IL-1-p, IL-8, IL-10 и TNF-ot).
Циклоферон® относится к ранним индукторам интерферона, так как пик его выработки приходится на период от 4 до 8 ч с момента приема, что позволяет рекомендовать препарат для купирования вирусного заболевания на ранней стадии или в качестве экстренной профилактики. Кроме того, Циклоферон® хорошо сочетается с симптоматическими препаратами, вакцинами, химиопрепаратами, препаратами интерферона, усиливая действие последних и уменьшая побочные эффекты от их применения, что позволяет получить оптимальный фармакотерапевтический эффект. Исследование эффективности применения Циклоферона® в комплексном лечении ОРВИ у детей, проведенное Е.И. Кондратьевой, выявило более быстрое купирование симптомов интоксикации и выраженности катаральных явлений, обусловленное противовоспалительным и цитопротективным действием на слизистую оболочку дыхательных путей, а также увеличением уровня секреторного IgA. М.В. Гаращенко в своем исследовании отмечает почти 10-кратное уменьшение числа заболевших ОРВИ в период эпидемического подъема заболеваемости на фоне применения Циклоферона® (6 и 58% соответственно), а также более легкое течение и отсутствие осложнений [14; 15].
Помимо высокой эффективности, препарат отличается высоким профилем безопасности, который подтверждается отсутствием токсичности, аллергенности, мутагенности, хорошей растворимостью в биологических средах и проникновением в ткани, быстрым выведением из организма и отсутствием кумуляции [16].
Таким образом, широкий спектр биологической активности при низкой токсичности, наличие иммуномодулирующего действия позволяют рекомендовать Циклоферон® как препарат первой линии в лечении острых респираторных инфекций у детей. Для наибольшей эффективности рекомендуется начинать применять Циклоферон® как можно раньше, дополняя его препаратами направленного этиотропного действия и иммуномодуляторами, что обеспечит достижение оптимального фармакотерапевтического эффекта.
ЛИТЕРАТУРА
- Руководство по вирусологии. Вирусы и вирусные инфекции человека и животных / Под ред. Д.К. Львова. М.: МИА, 2013. 1200 с.
- Грипп и гриппоподобные инфекции, включая особо опасные формы гриппозной инфекции. Фундаментальные и прикладные аспекты изучения // Бюллетень проблемной комиссии / Под ред. В.И. Покровского, Д.К. Львова, О.И. Киселева, Ф.И. Ершова. СПб.: Роза мира, 2008. 109 с.
- Ершов Ф.И., Коваленко А.Л., Романцов М.Г. Вопросы лечения гриппа и ОРВИ у детей // Экспериментальная и клиническая фармакология. 2011. № 6. С. 41-45.
- Ющук Н.Д., Бокова Н.О., Знойко О.О. Оптимизация диагностических подходов в тактике ведения больных гриппом // Лечащий врач. 2012. № 10. С. 64-67.
- Ершов Ф.И., Романцов М.Г. Лекарственные средства, применяемые при вирусных заболеваниях: Руководство для врачей. М.: ГЭОТАР-Медиа, 2007.
- Fiore А.Е., Fry A., Shay. D. Antiviral agents for the treatment and chemoprophylaxis of infl uenza. Recommendations of the advisory committee on immunization practices (ACIP) // Recommendations and Reports, 60 (RR01): 1-24 (2011).
- Ершов Ф.И., Наровлянский А.Н. Основные итоги изучения системы интерферона к 2011 году // Интерферон-2011: Сборник научных статей. М., 2012. С. 14-34.
- Григорян С.С. Индукторы интерферона: итоги и перспективы // Интерферону - 50 лет: Юбилейный сборник, посвященный открытию интерферонов / Под ред. акад. РАМН проф. Ф.И. Ершова. М., 2007. С. 66-71.
- Романцов М.Г., Ершов Ф.И. Иммунный ответ при вирусных инфекциях // Часто болеющие дети: современная фармакотерапия. М.: ГЭОТАР-Медиа, 2009. С. 134-142.
- Лыткина И.Н., Малышев Н.А. Профилактика и лечение гриппа и острых респираторных вирусных инфекций среди эпидемиологически значимых групп населения // Лечащий врач. 2010. № 10. С. 66-69.
- Романцов М.Г. и др. Антиоксиданты и иммунотропные препараты в терапии больных туберкулезом легких // Врач. 2005. № 9. С. 66-67.
- Применение Циклоферона при социально значимых заболеваниях у детей и подростков. Новейший справочник практикующего врача-педиатра / Под ред. М.Г. Романцова, Л.Г. Горячевой. А.А. Шульдякова. СПб., 2010. 165 с.
- Исаков В.А. и др. Эффективность Циклоферона® в терапии и профилактике гриппа и ОРЗ // РМЖ. 2011. № 23. С. 1-8.
- Кондратьева Е.И. Экстренная неспецифическая профилактика ОРВИ и гриппа препаратом Циклоферон® у детей в эпидемический период // Вестник Санкт-Петербургской государственной медицинской академии им. И.И. Мечникова. 2005. № 1.
- Гаращенко М.В. Новые технологии в медикаментозной профилактике острых респираторных заболеваний у детей школьного возраста в условиях мегаполиса: Автореф. дис. . канд. мед. наук. М., 2007.
- Татаурщиков Н.С., Сепиашвили Р.И. Современные подходы к использованию иммуномодуляторов в аллергологической практике. М: Тактик-Студио, 2012. 39 с.
Читайте также:


