Инфекция при беременности эхогенность

В последние годы плацентарная недостаточность (ПН) занимает одно из ведущих мест в общей структуре перинатальной смертности и заболеваемости и остается важнейшей проблемой современного акушерства [1, 2]. В структуре акушерских осложнений частота встречаемости плацентарной недостаточности составляет 52,0 %. Внутриутробная инфекция (ВУИ) относится к тяжелым осложнениям беременности и зачастую обнаруживается вместе с плацентарной недостаточностью, существенно влияя на перинатальные исходы. Инфицирование плаценты и плода происходит в различные сроки беременности. В первом триместре беременности основными показателями УЗ обследования являются размеры плодного яйца и эмбриона, а также состояние и размеры желточного мешка и хориона. Большинство исследователей отмечают высокую диагностическую ценность данного метода обследования [3, 4, 5, 6].
Безусловно, определяя характерные признаки ВУИ, необходимо провести дифференциальную диагностику с пороками развития сердца, хромосомными заболеваниями, синдромами мальформаций, чтобы выявить группу инфекций, относящихся к TORCH (Т – токсоплазмоз, О – другие инфекционные агенты (корь, парвовирус В19, сифилис, ветряная оспа, вирус Коксаки, вирусы гепатита С, В, Е, Д, папилломавирус, листериоз, гонорея, боррелиоз, ВИЧ-инфекция, эпидемический паротит, микоплазма, грипп, малярия, инфекционный мононуклеоз, хламидии, стрептококки группы В), R – краснуха, C – цитомегаловирус, H – простой герпес). В связи с тем, что ультразвуковые маркеры в полной мере не могут исключить или подтвердить пренатальную инфекцию с точной достоверностью, обнаружение ультразвуковых критериев, типичных для ВУИ плода, имеет важное значение для выработки дальнейшей тактики ведения беременности.
Целью исследования явилось выявление ультразвуковых маркеров внутриутробного инфицирования плода у женщин с плацентарной недостаточностью.
Материалы и методы исследования
Для получения достоверной картины внутриутробного инфицирования у беременных мы провели исследования среди 169 женщин репродуктивного возраста, которые были разделены на 2 группы. Первую группу составили 123 женщины, обратившиеся за гинекологической помощью, т.е. имевшие на период проведения работу ту или иную гинекологическую заболеваемость. Вторую группу составили 46 женщин, которые в отмеченном периоде не имели текущей гинекологической заболеваемости. Возраст женщин колебался от 18 до 39 лет.
Критериями включения беременных в основную группу были следующие эхографические признаки ВУИ: изменение количества околоплодных вод, гиперэхогенный кишечник, синдром задержки развития плода, изменения кровотока у плода, инфекционная кардиопатия, гепатоспленомегалия, амниотические тяжи, кальцификаты или гиперэхогенные включения в паренхиматозных органах. Наличие этих маркеров, как единственных, так и в различных сочетаниях, явилось показанием проведения в дальнейшем динамической допплерометрии.
Состояние фетоплацентарного комплекса (ФПК) изучали с помощью инструментальных методов исследования, включающих комплексное ультразвуковое исследование (плацентографию, фетометрию, развитие внутренних органов плода и оценку количества околоплодных вод), допплерометрическое исследование кровотока в артериях пуповины (АП), маточных артериях (МА), венозном протоке плода (ВП) и средней мозговой артерии (СМА).
Диагноз плацентарной недостаточности устанавливали при выявлении двух и более из перечисленных ниже признаков:
– выявление по данным эхографии задержки внутриутробного роста плода;
– выявление по данным КТГ хронической внутриутробной гипоксии плода;
– выявление внутриутробной гибели плода на любом сроке беременности;
– выявление нарушения плодово-плацентарного кровотока по данным допплерографии;
– выявление маловодия по данным эхографии;
– выявление характерных изменений в структуре плаценты по данным УЗИ: обнаружение тромбозов, инфарктов и изменения в эхогенности базальной мембраны.
В ходе исследования использовались различные функции УЗИ: 2D-сканирование, 3D/4D сканирование плаценты, плода, пуповины, для оценки кровотоков в ФПК применялась спектральная допплерометрия. Статистический анализ данных осуществлялся с помощью программы электронного пакета Microsoft Excel 2007, которые были сформированы в соответствии с запросами настоящего исследования.
Результаты исследования и их обсуждение
В ходе проведенных исследований произведен анализ эхографических особенностей ФПК. Выявленные эхографические признаки, характеризующие внутриутробное инфицирование плода, представлены в табл. 1.
При проведении эхографического исследования у плодов основной группы определялись различные сочетания ультразвуковых признаков, характерных для ВУИ. При помощи УЗИ в I триместре беременности было установлено, что наиболее часто у беременных встречалось многоводие, которое в 1 группе беременных составило соответственно – 55,2 ± 4,5 % и во 2 группе беременных – 45,6 ± 7,3 %, значительно реже наблюдалось маловодие (соответственно – 17,0 ± 3,4 % и 10,9 ± 4,6 в группах; χ2 = 21,43, р Примечание . Одновременно у пациенток выявлялись 2 и более признаков.
Эхографические признаки, характеризующие состояние ФПК в III триместре беременности
Самые часто встречающиеся ультразвуковые маркеры хромосомной аномалии:
Оценка этого параметра проводится в первое скрининговое УЗИ (11-14 недель)
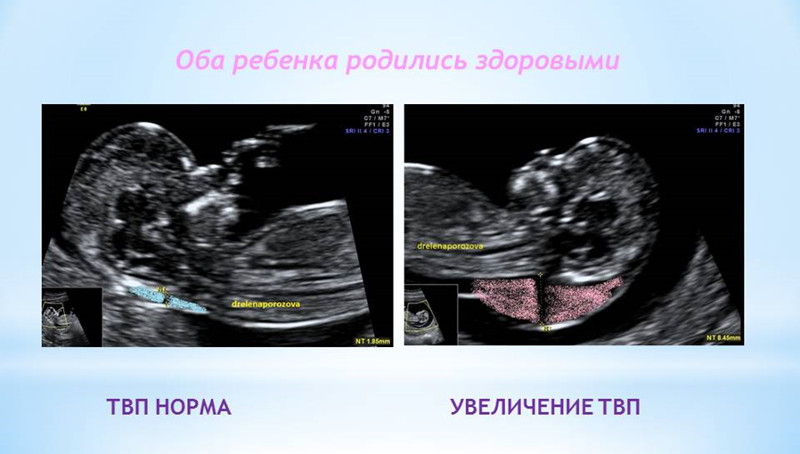
ТВП (толщина воротникового пространства) может оказаться больше нормы по нескольким причинам.
Почему у плода может выявляться увеличение ТВП?
Родители бывают крайне взволнованы и хотят сразу же получить ответы на все, возникающие у них вопросы – с чем связано, что делать и многие другие. Вопросы, на которые невозможно ответить сразу. Ведь причин увеличения ТВП множество. Данная находка может встречаться у абсолютно здоровых плодов, это не порок развития, это лишь сигнал к более глубокому обследованию, потому что такая особенность может иметь место у плодов с хромосомной патологией, аномалиями сердца либо другими врожденными или наследственными заболеваниями. При увеличении максимального порога ТВП ВАЖНО, чтобы врач оценил все остальные ультразвуковые маркеры (признаки), а также провел детальную оценку анатомии плода. Возможно, причина увеличения ТВП кроется в нарушении развития плода (например, аномалии строения сердца).
Что делать при выявлении увеличения ТВП у плода?
Если у вашего плода обнаружили расширение ТВП, Вас обязательно направят на консультацию к врачу генетику, который собрав анамнез, оценив все риски, даст рекомендации по дополнительным методам исследования (инвазивная диагностика). Далее потребуется экспертное УЗИ плода на сроке 20 недель для детальной оценки анатомии. Если по всем этим исследованиям отклонений не выявлено, то шансы родить здорового ребенка велики даже при значительной величине ТВП.
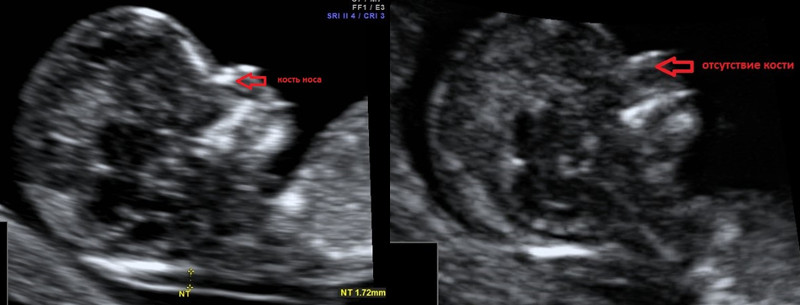
Гипоплазия костей носа – уменьшение размеров косточки носа в зависимости от КТР вашего малыша.
Аплазия костей носа – отсутствие визуализации косточки носа у вашего малыша.
Отсутствие видимости костной части спинки носа у плода или ее недоразвитие (недостаточно яркая) на первом скрининге связана с задержкой отложения кальция. Такая ситуация несколько чаще может встречаться у плодов с синдромом Дауна, однако важно, что:
- само по себе отсутствие костей носа на УЗИ не является аномалией развития; может встречаться у абсолютно здоровых плодов (в 3% случаев);
- для оценки степени индивидуального риска необходима оценка остальных ультразвуковых маркеров (толщина воротникового пространства плода, показатели кровотока на сердечном клапане, показатели кровотока в венозном протоке, ЧСС плода) и биохимического анализа материнской сыворотки (РАРР-А, ХГЧ);
- Если результат комбинированного скрининга (оценка в специальной программе данных УЗИ и анализа крови) показывает НИЗКИЙ риск хромосомной патологии – беспокоиться не стоит. Обязательно пройдите контрольное УЗИ в 19-20 недель беременности, где будет проведена тщательная оценка анатомии плода и исследованы определенные ультразвуковые маркеры второго триместра беременности.
- Что делать если результат комбинированного скрининга оказался ВЫСОКИМ? – Переживать не стоит. Вас обязательно направят на консультацию к врачу генетику, который собрав анамнез, оценив все риски, даст рекомендации по дополнительным методам исследования (инвазивная диагностика).
Это термин, говорящий о повышенной эхогенности (яркости) кишечника на ультразвуковом изображении. Выявление гиперэхогенного кишечника НЕ является пороком развития кишечника, а просто отражает характер его ультразвукового изображения. Необходимо помнить, что эхогенность нормального кишечника выше, чем эхогенность соседних с ним органов (печени, почек, легких), но такой кишечник не считается гиперэхогенным. Гиперэхогенным называется только такой кишечник, эхогенность которого сравнима с эхогенностью костей плода.
Почему кишечник у плода может быть гиперэхогенным?
Иногда гиперэхогенный кишечник выявляется у абсолютно нормальных плодов, и при УЗИ в динамике этот признак может исчезать. Повышенная эхогенность кишечника может быть проявлением хромосомных болезней плода, в частности, синдрома Дауна. В связи с этим при обнаружении гиперэхогенного кишечника проводится тщательная оценка анатомии плода. Однако при выявлении гиперэхогенного кишечника можно говорить лишь о повышенном риске синдрома Дауна, так как подобные изменения могут встречаться и у совершенно здоровых плодов. Иногда гиперэхогенный кишечник может быть признаком внутриутробной инфекции плода. Гиперэхогенный кишечник часто обнаруживается у плодов с задержкой внутриутробного развития. Однако при этом будут обязательно выявляться отставание размеров плода от срока беременности, маловодие и нарушение кровотока в сосудах плода и матки. Если ничего из вышеперечисленного не выявлено, то диагноз задержки развития плода исключен.
Что делать при выявлении гиперэхогенного кишечника у плода?
Вам следует обратиться к специалисту генетику, который еще раз оценит результаты биохимического скрининга и даст необходимые рекомендации по дальнейшему ведению беременности.
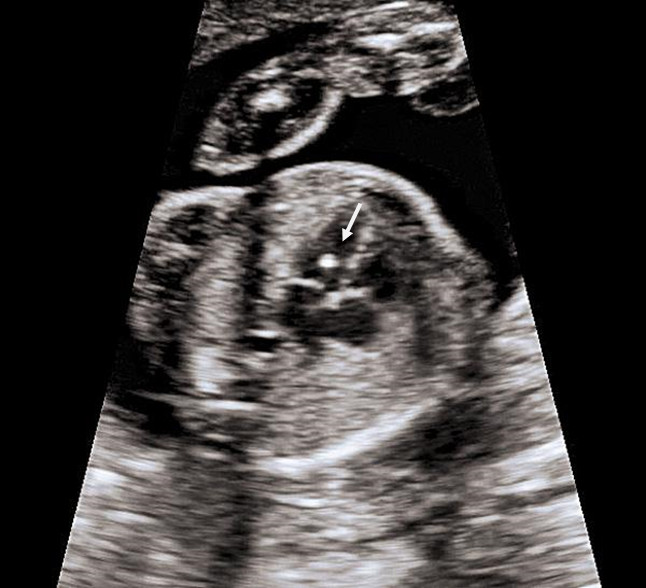
Это термин, говорящий о повышенной эхогенности (яркости) небольшого участка сердечной мышцы на ультразвуковом изображении. Выявление гиперэхогенного фокуса в сердце НЕ является пороком развития сердца, а просто отражает характер его ультразвукового изображения. Гиперэхогенный фокус возникает в месте повышенного отложения солей кальция на одной из мышц сердца, что не мешает нормальной работе сердца плода и не требует никакого лечения.
Почему у плода может выявляться гиперэхогенный фокус в сердце?
Что делать при выявлении гиперэхогенного фокуса в сердце плода?
Если у плода выявлен ТОЛЬКО гиперэхогенный фокус в сердце, то никаких дополнительных обследований не требуется; риск болезни Дауна не увеличивается. На плановом УЗИ в 32-34 недели еще раз будет осмотрено сердце плода. В большинстве случаев гиперэхогенный фокус в сердце исчезает к этому сроку беременности, но даже если он продолжает оставаться в сердце, это никак не влияет на здоровье плода и тактику ведения беременности.
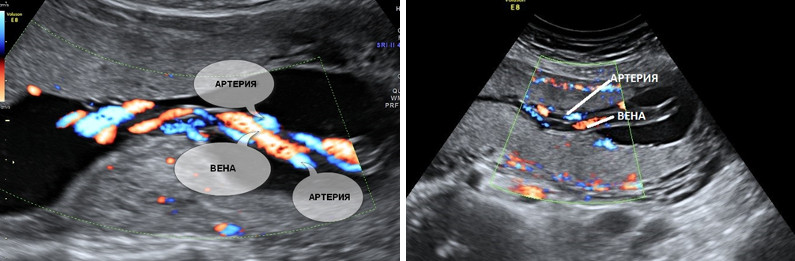
Нормальная пуповина состоит из трех сосудов – две артерии и одна вена. Иногда вместо двух артерий в пуповине формируется только одна артерия и одна вена, таким образом, в пуповине определяется всего два сосуда. Данное состояние считается пороком развития пуповины, однако этот порок не оказывает никакого влияния на послеродовое состояние ребенка и его дальнейшее развитие.
Почему у плода может определяться единственная артерия пуповины?
Что делать при выявлении единственной артерии пуповины у плода?
Выявление только единственной артерии пуповины не повышает риск наличия синдрома Дауна и не является показанием к консультации генетика и проведению других диагностических процедур. Необходимо контрольное УЗИ в 26-28 и 32 недели беременности для оценки темпов роста плода и оценки его функционального состояния.
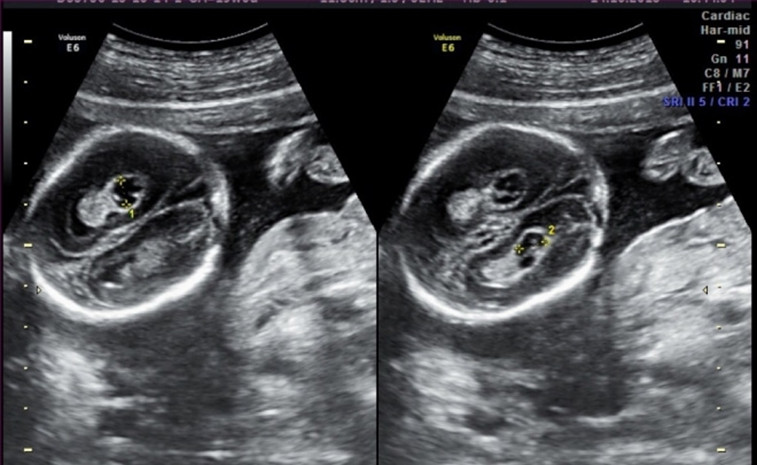
Сосудистые сплетения - одна из первых структур, которая появляется в головном мозге плода. Это сложная структура, и присутствие обоих сосудистых сплетений подтверждает, что в мозге развиваются обе половины. Сосудистое сплетение производит жидкость, питающую головной и спинной мозг. Иногда жидкость образует скопления внутри сосудистых сплетений, которые при УЗИ имеют вид "кисты". Кисты сосудистых сплетений иногда могут быть найдены при ультразвуковом исследовании в сроках 18-22 недели беременности. Наличие кист не оказывает влияния на развитие и функцию головного мозга. Большинство кист самопроизвольно исчезает к 24-28 неделям беременности.
Часто ли встречаются кисты сосудистых сплетений?
В 1-2 % всех нормальных беременностей плоды имеет КСС, в 50 % случаев обнаруживаются двусторонние кисты сосудистых сплетений, в 90 % случаев кисты самопроизвольно исчезают к 26-ой неделе беременности, число, размер, и форма кист могут варьировать, кисты также найдены у здоровых детей и взрослых. Несколько чаще кисты сосудистых сплетений выявляются у плодов с хромосомными болезнями, в частности, с синдромом Эдвардса (трисомия 18, лишняя 18 хромосома). Однако, при данном заболевании у плода всегда будут обнаруживаться множественные пороки развития, поэтому выявление только кист сосудистого сплетения не повышает риск наличия трисомии 18 и не является показанием к проведению других диагностических процедур. При болезни Дауна кисты сосудистых сплетений, как правило, не выявляются. Риск синдрома Эдвардса при обнаружении КСС не зависит от размеров кист и их одностороннего или двустороннего расположения. Большинство кист рассасывается к 24-28 неделям, поэтому в 28 недель проводится контрольное УЗИ. Однако, если кисты сосудистых сплетений не исчезают к 28-30 неделям, это никак не влияет на дальнейшее развитие ребенка.
Почечные лоханки это полости, где собирается моча из почек. Из лоханок моча перемещается в мочеточники, по которым она поступает в мочевой пузырь.
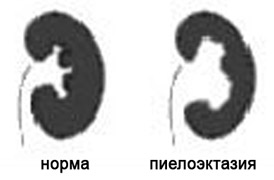
Пиелоэктазия представляет собой расширение почечных лоханок. Пиелоэктазия в 3-5 раз чаще встречается у мальчиков, чем у девочек. Встречается как односторонняя, так и двухсторонняя пиелоэктазия. Легкие формы пиелоэктазии проходят чаще самостоятельно, а тяжелые иногда требуют хирургического лечения.
Причина расширения почечных лоханок у плода.
Если на пути естественного оттока мочи встречается препятствие, то моча будет накапливаться выше данного препятствия, что будет приводить к расширению лоханок почек. Пиелоэктазия у плода устанавливается при обычном ультразвуковом исследовании в 18-22 недели беременности.
Опасна ли пиелоэктазия?
Умеренное расширение почечных лоханок, как правило, не влияет на здоровье будущего ребенка. В большинстве случаев при беременности наблюдается самопроизвольное исчезновение умеренной пиелоэктазии. Выраженная пиелоэктазия (более 10 мм) свидетельствует о значительном затруднении оттока мочи из почки. Затруднение оттока мочи из почки может нарастать, вызывая сдавление, атрофию почечной ткани и снижение функции почки.
Нужно ли обследовать ребенка после родов?
У многих детей умеренная пиелоэктазия исчезает самопроизвольно в результате дозревания органов мочевыделительной системы после рождения ребенка. При умеренной пиелоэктазии бывает достаточно проводить регулярные ультразвуковые исследования каждые три месяца после рождения ребенка. При присоединении мочевой инфекции может понадобиться применение антибиотиков. При увеличении степени пиелоэктазии необходимо более детальное урологическое обследование.
В случаях выраженной пиелоэктазии, если расширение лоханок прогрессирует, и происходит снижение функции почки, бывает показано хирургическое лечение. Хирургические операции позволяют устранить препятствие оттоку мочи. Часть оперативных вмешательств может с успехом выполняться эндоскопическими методами – без открытой операции, при помощи миниатюрных инструментов, вводимых через мочеиспускательный канал. В любом случае вопрос об оперативном лечении решается после рождения ребенка и полного его обследования.
Что делать при выявлении ультразвуковых маркеров хромосомной патологии у плода?
Вам следует обратиться к специалисту генетику, который еще раз оценит результаты ультразвукового исследования и биохимического скрининга, рассчитает риск индивидуально для вашего случая и даст необходимые рекомендации по дальнейшему ведению беременности.

Одной из важнейших проблем современной перинатологии является прогрессирующий рост инфекционной патологии у плода и новорожденного. В структуре заболеваемости новорожденных внутриутробные инфекции (ВУИ) занимают второе место после гипоксии и асфиксии в родах [4].
В структуре перинатальной смертности удельный вес ВУИ достигает 65,6% [11]. В настоящее время насчитывается более 2500 возбудителей, способных вызывать внутриутробное инфицирование плода, при этом количество их постоянно пополняется [14]. Чаще диагностируется смешанное инфицирование вирусно-бактериальной, вирусно-вирусной природы и их различные ассоциации с трихомонадами и дрожжевыми грибами рода Candida [12].
Возбудители этих инфекций обладают прямым и непрямым действием на фето-плацентарную систему. Дегтярев Д.Н. и соав. (1998) утверждают, что чем меньше гестационный возраст плода, тем более выражена альтерация тканей. В результате этого основным клиническим проявлением инфекции плода, возникающих на ранних сроках беременности являются пороки развития [2]. По мере увеличения сроков беременности в клинической картине инфекционного заболевания плода начинают преобладать симптомы классического системного воспаления, обусловленные выраженной пролиферацией и экссудацией, что проявляется в виде гепатита, пневмонии менингита, энтероколита и других заболеваний [6].
Непрямое воздействие возбудителей на фето-плацентарную систему приводит к таким осложнениям беременности как угроза прерывания, внутриутробная гипоксия плода, ЗВУР, метаболические нарушения без специфических клинически признаков ВУИ 8.
Учитывая неспецифичность клинических проявлений ВУИ во время беременности, диагностика ее затруднена и возможна лишь в результате сочетания клинических и лабораторно-инструментальных методов исследования [5]. Метод ультразвуковой диагностики является доступным, высоко информативным, не инвазивным и позволяет провести эхографическую оценку структурной патологии плода, плаценты, амниона, а также определить степень гемодинамических нарушений фето-плацентарного комплекса у беременных с высоким инфекционным индексом [3,12].
Материалы и методы
Под наблюдением находились 123 беременных женщины, которым проводились все необходимые клинико-лабораторные обследования, а также ультразвуковое исследование в сроке 30-36 недель гестации. В зависимости от выраженности ВУИ и степени тяжести состояния все новорожденные разделены на 4 клинические группы.
1 группа (n=40) - контрольная, новорожденные от матерей с неосложненной беременностью, состояние ребенка при рождении удовлетворительное. 2-я группа (n=30) - состояние ребенка при рождении удовлетворительное или средней степени тяжести с локальными проявлениями ВУИ в виде пиодермии, ринита, отита, конъюнктивита, пневмонии. 3-я группа (n=25) - состояние ребенка при рождении тяжелое или средней степени тяжести с ухудшением в раннем неонатальном периоде с локальными формами ВУИ в виде пневмонии, энтероколита, менингита, фетального гепатита и др. заболеваний. 4-я группа (n=28) - состояние ребенка при рождении тяжелое или крайней степени тяжести с генерализованными или локальными проявлениями ВУИ, потребовавшими проведения искусственной вентиляции легких. Матери детей 2-4 групп имели высокий инфекционный индекс.
Таблица 1.
Фетометрия позволила установить соответствие размеров плода гестационному сроку, диагностировать задержку внутриутробного развития.
При исследовании сердечной деятельности плода использовали шкалу Фишера, 1976., основными показателями которой были: базальная частота сердечных сокращений, амплитуда осцилляций, частота осцилляций, акцелерации, децелерации. Критерии состояния плода следующие: 8 - 10 баллов - нормальное состояние; 5 - 7 баллов - сомнительное; 0 - 4 балла - неудовлетворительное.
Таблица 2. Заболеваемость беременных урогенитальными инфекциями
Диагностическими критериями нарушения маточно-плацентарного и плодово-плацентарного кровотока при доношенной беременности считали следующие числовые значения СДО: в артерии пуповины 3,0 и выше, а также нулевые и отрицательные значения диастолического кровотока; в маточных артериях 2,4 и выше; в аорте плода 8,0 и выше; для средней мозговой артерии менее 4 и более 7 у.е. [10].
Для оценки степени нарушений маточно-плацентарно-плодовой гемодинамики пользовались шкалой А.Н. Стрижакова (1991).
I А степень - изолированное нарушение кровотока в маточных артериях; I Б степень - изолированное нарушение кровотока в артерии пуповины; II степень - сочетанное нарушение кровотока в маточных артериях и артерии пуповины; III степень - критическое нарушение плодового кровотока, характеризующееся нулевым или ретроградным диастолическим компонентом в артерии пуповины.
Результаты исследований
На основании ранее проведенных исследований [1] выделяют 3 группы эхографических маркеров внутриутробного инфицирования: 1) маркеры внутри-утробного инфицирования плаценты (плацентит); 2) маркеры внутриутробного инфицирования околоплодных вод (амнионит); 3) маркеры внутриутробного
инфицирования плода (инфекционные фетопатии).
По данным ультразвукового исследования структурной организации плаценты получены следующие результаты. В контрольной (первой) группе нарушения зарегистрированы у 4 (10%) женщин, из них у 2 (5%) отмечалось преждевременное созревание плаценты, которое регистрировалось с 33 недель, и у 2 (5%) - расширение межворсинчатого пространства, что связано с низким артериальным давлением в период плацентации. Сочетания признаков не отмечалось. Во второй клинической группе преждевременное созревание плаценты зарегистрировано в 5 (16,6%) случаях, увеличение толщины плаценты в 2 (6,6%) случаях, расширение межворсинчатого пространства в 6 (20%) случаях. В 4 (13,3%) случаях отмечалось сочетание признаков. В третьей клинической группе преждевременное созревание плаценты выявлено у 9 (36%) женщин, а незрелость плаценты (I степень) у 2 (8%) женщин. Увеличение толщины плаценты отмечалось у 6 (24%) женщин, расширение межворсинчатого пространства у 9 (36%) женщин. Сочетание признаков наблюдалось в 12 (48%) случаях. В 4 клинической группе преждевременное созревание плаценты отмечалось у 12 (42,8%) женщин, незрелость плаценты у 5 (17,8%) женщин, увеличение толщины плаценты у 10 (35,7%) женщин, расширение межворсинчатого пространства у 15 (53,6%) женщин. Количество сочетания признаков увеличилось до 19 (67,8%) случаев, причем, наиболее частыми сочетаниями были преждевременное созревание плаценты и расширение межворсинчатого пространства (вне зависимости от клинических групп). Кроме того, в 4 группе у 6 (21,4%) пациентов плацента была кистозно изменена, в двух случаях (7,1%) отмечено формирование псевдокист.
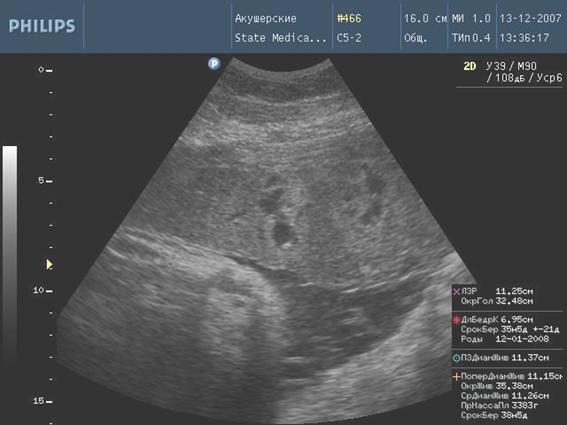
Рис. 1. Формирование псевдокист
При оценке объема и качества околоплодных вод были выявлены следующие закономерности. В контрольной группе данная патология определялась у 6 (15%) пациентов, из них у 1 (2,5%) в виде умеренно выраженного маловодия, у 2 (5%) - в виде умеренно выраженного многоводия, гиперэхогенные включения в околоплодных водах зарегистрированы у 3 (7,5%) пациентов. Сочетания признаков не выявлено. В основных группах патология околоплодных вод обнаружена у 63 (75,9%) пациентов. Так, во 2 клинической группе маловодие выявлено у 6 (20%) женщин, многоводие - у 2 (6,6%) женщин, гиперэхогенные включения отмечались у 8 (26,6%) женщин. Сочетание признаков зарегистрировано в 5 (16,6%) случаях. В 3 клинической группе маловодие наблюдалось в 11 (44%) случаях, многоводие в 5 (20%) случаях, гиперэхогенные включения в 9 (36%) случаях. Кроме того, в 2 (8%) случаях было зарегистрировано наличие амниотических тяжей, свободно располагающихся в амниотической полости. В 4 клинической группе маловодие выявлено у 18 (64,3%) беременных, многоводие у 7 (25%) беременных; наличие гиперэхогенных включений и амниотических тяжей в 12 (42,8%) и 4 (14,3%) случаях соответственно. Кроме того, в основных группах многоводие с множественными гиперэхогенными включениями сочеталось в 26 (31,3 %) случаях, у 4 (4,8 %) беременных многоводие сочеталось с амниотическими тяжами.
Рис. 2. Эхографический маркер внутриутробного инфицирования околоплодных вод (свободно расположенный амниотический тяж)
При ультразвуковом исследовании у плодов с инфекционными фетопатиями обнаружены следующие эхографические особенности. Расширение чашечно-лоханочной системы выявлено у 4 (14,3%) плодов 4-ой группы и у 2 (8%) плодов третьей группы (рис. 3), вентрикуломегалия у 4-х (14,3%) плодов 4 группы и у 2 (8%) плодов 3 группы (рис. 4), гепатомегалии у 5 (17,8%) плодов 4 группы и у 2 (8%) плодов в 3 группе. Кардиомегалия с гидроперикардом зарегистрированы у 2-х (7,1%) плодов 4 группы. Отмечено появление линейных гиперэхогенных включений в перивентрикулярных зонах головного мозга плода в 4 (14,3%) случаях в 4 клинической группе, в 2 (8%) случаях в 3 клинической группе и в 1 (3,3%) случае во 2 группе. Кисты в сосудистых сплетениях головного мозга плода обнаружены в 2 (7,1%) случаях в 4 группе, в 1 (4%) случае в 3 группе и в 1 (3,3%) случае во 2 группе. Патологическое расширение петель толстого кишечника зарегистрировано у 2 (7,1%) плодов 4 группы и у 1 (4%) плода в 3 группе. Асцит выявлен у 1 (3,6%) плода 4 группы. Таким образом, наибольшее число инфекционных фетопатий было выявлено у беременных 4 клинической группы.
Рис. 3. Эхографический маркер внутриутробного инфицирования плода (правосторонняя пиелоэктазия)
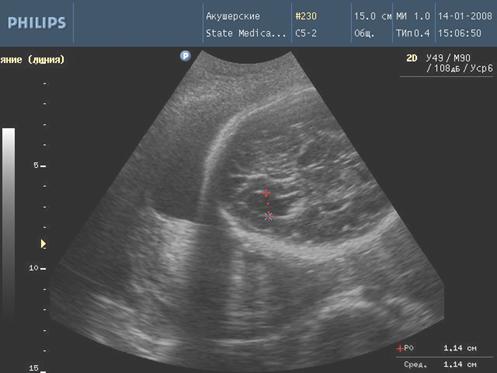
Рис. 4. Вентрикуломегалия
ЗВУР плода зарегистрирована в 29 случаях (34,9%) в основных группах и в 1 (2,5%) случае в контрольной группе. Во 2 клинической группе ЗВУР I-II степени выявлена у 7 (23,3%) плодов. В 3 клинической группе ЗВУР диагностирована у 8 (32%) плодов, из них у 5 (20%) зарегистрирована ЗВУР плода I степени, у 2 (8%) - II степени, у 1 (4%) - III степени. В 4 клинической группе количество случаев ЗВУР плода увеличилось до 14 (50%), причем ЗВУР I степени отмечалась у 8 (28,6%) плодов, ЗВУР II степени - у 4 (14,3%) плодов, ЗВУР III степени у 2 (7,1%) плодов.
Исследования биофизической активности плода выявили следующие результаты. При оценке дыхательной активности плода в 1 клинической группе максимальная продолжительность одного эпизода дыхательных движений более 60 секунд определена у 35 (87,5%) плодов. У 5 (12,5%) отмечалось снижение дыхательной активности, из них у 4 (10%) продолжительность составила от 30 до 60 сек. и у 1 (2,5%) отмечалось резкое снижение данного параметра. В этой группе адекватная двигательная активность сохранялась у 38 (95%) плодов, небольшое снижение двигательной активности зарегистрировано у 2 (5%) плодов. Тонус у плодов был удовлетворительным в 100% случаев.
Во 2 клинической группе снижение дыхательной активности наблюдалось у 14 (46,6%) плодов, из них у 2 (6,6%) она не регистрировалась вообще. Снижение тонуса и двигательной активности отмечалось одномоментно у 3 (10%) плодов.
В 3 клинической группе снижение дыхательной активности наблюдалось у 16 (64%) плодов, из них у 11 (44%) продолжительность одного эпизода дыхательных движений составила от 30 до 60 сек., а у 5 (20%) плодов - менее 30 сек. В 4 группе в 82,1% случаев отмечалось снижение дыхательной активности, у 9 (32,1%) плодов - резкое снижение данного параметра. Тонус и двигательная активность плода являются наиболее точными маркерами тяжести внутриутробного страдания плода. Так в 3 клинической группе снижение данных показателей отмечалось у 17 (68%) плодов, в 4 группе - у 25 (89,2%) плодов, причем отсутствие общей двигательной активности за время наблюдения определялось у 6 (24%) плодов 3 группы и у 15 (53,5%) плодов 4 группы.
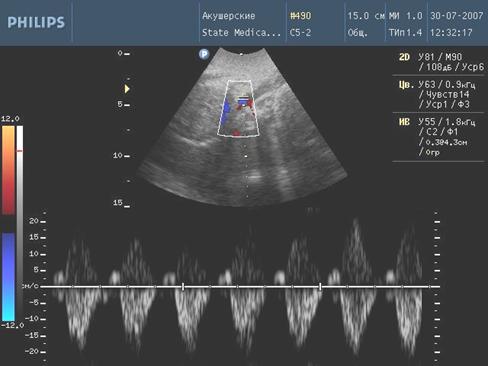
Рис. 5. Нарешение гемодинамики III ст. (ретроградный кровоток)
С целью изучения особенностей гемодинамических нарушений в фетоплацентарном комплексе у беременных с высоким инфекционным индексом были использованы значения систоло-диастолического отношения (СДО) в маточных артериях, артерии пуповины и средней мозговой артерии.
Таблица 3. Средние значения СДО в изучаемых сосудах

Современное акушерство располагает богатым арсеналом методов оценки состояния плода: кардиотокография с обязательным проведением нестрессового теста; оценка биофизического профиля плода; оценка двигательной и дыхательной активности плода; допплерометрия кровотока в артерии пуповины и средней мозговой артерии; исследование кислотно-основного состояния крови, полученной из предлежащей части (проба Залинга); во время родов применяют пульсовую оксиметрию; о гипоксии плода в родах можно судить по окраске и густоте околоплодных вод при головном предлежании плода. Однако все предложенные методики лишь констатируют состояние плода на момент диагностики и не дают прогнозов о состоянии плода в родах. Тем не менее, подготовка беременных женщин к родам проводится без функциональной пробы на устойчивость их плодов к внутриутробной гипоксии, поэтому адаптационные возможности плодов к гипоксии остаются неизвестными [1, 2, 3, 4, 5].
Известна проба Штанге, применяемая у взрослого человека, суть ее сводится к определению максимальной продолжительности периода добровольной задержки дыхания с выдачей заключения об отличной, хорошей, средней или плохой устойчивости к гипоксии в случае задержки дыхания на срок 60, 40-60, 30-40 или менее 30 секунд (соответственно) [6, 7].
Кратковременное прекращение вентиляции легких у беременной женщины может быть использовано для безопасного моделирования внутриутробной гипоксии и изучения устойчивости плода к ней перед родами. При этом размеры дефицита кислорода, резерва адаптационных возможностей плода к гипоксии и тяжести гипоксического повреждения его организма могут быть определены путем определения длительности гипоксии и динамики уровня оксигемоглобина в крови плода.
Цель исследования
В связи с этим нами решено разработать функциональную пробу, применимую в условиях родильных домов и женских консультаций и позволяющую оценивать адаптационные возможности к гипоксии у плодов аналогично пробе Штанге у взрослых людей.
Материалы и методы
Ультразвуковые исследования беременных женщин и их плодов проведены в условиях женской консультации родильного дома № 5 МУЗ ГКБ №7 города Ижевска во время плановых ультразвуковых исследований беременных женщин в скрининговые сроки II и III триместра. Первая группа исследованных пациенток состояла из 20 беременных женщин в возрасте от 18 до 28 лет со сроками беременности 20-24 недели без признаков фетоплацентарной недостаточности (ФПН), вторая группа исследованных пациенток состояла из 20 беременных женщин в возрасте 19-32 лет со сроками беременности 32-34 недели без признаков ФПН, третья группа состояла из 5 беременных женщин в возрасте 26-30 лет со сроками беременности 32 недели с признаками фетоплацентарной недостаточности по результатам регистрации гемодинамических нарушений в системе мать - плацента - плод при помощи допплера.
Для ультразвукового исследования был использован прибор экспертного класса ALOKASSD - ALPHA 10. В качестве датчика был использован стандартный датчик конвексного типа с частотой 3 - 7 МГц. Ультразвуковые исследования проведены по стандартной методике [8, 9].
Результаты и обсуждение
Поскольку безопасная и качественная визуализация плода в утробе матери возможна с помощью ультразвукового исследования, информацию о поведении плода при возникновении кислородного голодания предполагалось получить при ультразвуковом мониторинге. Причем, для повышения точности и расширения диапазона получаемой информации ультразвуковое исследование проведено в сагиттальной проекции плода.
Кроме того, у взрослых людей остановка дыхания или пережатие плечевой артерии провляются акроцианозом, преимущественно на подушечках пальцев рук, визуализировать который возможно на глаз и в инфракрасном диапазоне спектра при помощи тепловизорачерез 10-15 секунд, после задержки ими дыхания или пережатия плечевой артерии [10].
Проверка высказанного предположения была начата с исследования ультразвуковой плотности подушечек пальцев взрослой здоровой женщины, проведенного при добровольной задержке ею дыхания или при пережатии у нее плечевой артерии. Ишемия создавалась на уровне нижней трети плеча с помощью манжетки от аппарата, предназначенного для измерения величины артериального давления. Выяснено, что и гипоксия, и ишемия приводят к уменьшению ультразвуковой плотности и к осветлению изображения структуры мягких тканей пальцев на экране ультразвукового прибора.
Показано, что ультразвуковая эхогенность мягких тканей пальцев правой и левой рук уменьшается при задержке дыхания через 33,0 ± 0,5 с (n = 5, Р ≤ 0,05) и 40 ± 1,0 с (n = 5, Р ≤ 0,05) (соответственно), а при пережатии соответствующей плечевой артерии - через 15,0 ± 0,2 с (n = 5, Р ≤ 0,05) и 30 ± 1,0 с (n = 5, Р ≤ 0,05) (соответственно). Установлено, что уменьшение ультразвуковой эхогенности и осветление изображения мягких тканей подушечек пальцев на экране ультразвукового прибора сохраняется на протяжении всего периода ишемии или гипоксии. Восстановление кровоснабжения рук после минутной их ишемии приводит к восстановлению ультразвуковой эхогенности и плотности изображения мягких тканей подушечек пальцев правой и левой рук на экране прибора соответственно через 2,5 ± 0,1 с (n = 5, Р ≤ 0,05) и 1,0 ± 0,1 с (n = 5, Р ≤ 0,05). Возобновление дыхания после минутной его задержки приводит к восстановлению ультразвуковой эхогенности и изображения мягких тканей подушечек пальцев правой и левой руки на экране прибора соответственно через 9,5 ± 0,3 с (n = 5, Р ≤ 0,05) и 10,5 ± 0,4 с (n = 5, Р ≤ 0,05).
Вслед за этим нами была изучена динамика ультразвуковой эхогенности мягких тканей кончиков пальцев рук плодов при искусственной внутриутробной гипоксии. Полученные результаты подтверждают достаточную информативность и перспективность предложенного способа.
Ультразвуковые исследования подушечек пальцев рук плодов показали, что в начале периода искусственной внутриутробной гипоксии ультразвуковая эхогенность их остается неизменной. Она изменяется после появления дыхательной экскурсии ребер у плодов и разжимания ими кулаков. При этом происходит уменьшение ультразвуковой эхогенности мягких тканей подушечек и осветление их изображения на экране ультразвукового прибора. Выявленное нами уменьшение ультразвуковой эхогенности мягких тканей подушечек пальцев рук плодов оказалось аналогичным изменению ультразвуковой эхогенности подушечек пальцев рук у взрослого человека при задержке им дыхания или при пережатии у него плечевой артерии.
В связи с этим нами было сделано заключение о том, что уменьшение ультразвуковой эхогенности подушечек пальцев рук плода в период задержки дыхания беременной женщиной свидетельствует о развитии в них акроцианоза.
Читайте также:
- Как лечить красную волчанку у взрослых в домашних условиях
- Лунная лихорадка графический роман
- Государственное бюджетное учреждение здравоохранения республики коми воркутинская инфекционная больница
- Сдать анализы на инфекции в ясенево
- Чем лечить дисбактериоз у взрослого кишечника после приема антибиотиков


