Гематогенная инфекция последа что это значит
8.3. ПУТИ РАСПРОСТРАНЕНИЯ ИНФЕКЦИИ
В зарубежной и отечественной литературе описано пять основных пу-тей проникновения возбудителей инфекции в организм плода (Анкирская А.С., 1985; Радзинский В. Е, 1992; Кира Е.Ф., 1996; Левицкая С. К., 1991):
1) восходящий (через шейку матки и оболочки плодного яйца);
2) трансплацентарный, или гематогенный (через плацентарный барьер к плоду);
3) нисходящий (из воспалительно измененных придатков матки, аппен-дикса);
4) интранатальный (при прохождении плода через инфицированные ро-довые пути матери);
Антенатально инфекционный агент попадает к плоду гематогенно (трансплацентарно) или через инфицированные околоплодные воды. Чаще при антенатальном заражении возбудители поступают в организм плода ге-матогенно. Вначале они с кровью матери поступают в плаценту, где возмож-но размножение возбудителя и последующее развитие воспалительного про-цесса (плацентита). Преодолев маточно-плацентарный барьер, возбудитель проникает к плоду и может привести к развитию генерализованной инфекции с поражением печени, легких, почек, головного мозга и других органов (Ан-кирская А.С., 1989; Айламазян Э.К., 1995; Есаулова Н.Е., 1996; Сидельникова В.М., 1996; Сидорова И.С., 1999; Михайлов А.В., Лаврова Д.Б., Коляченко Е.С., 2003). Следует отметить, что распространение возбудителей может происходить и по вартонову студню пуповины, чему способствует внесосу-дистый ток жидкости от плаценты к плоду (Mindel A., 1995).
Околоплодные воды могут быть инфицированы восходящим (из влага-лища) и нисходящим (из маточных труб) путём, а также самим плодом, ин-фицированным гематогенно и выделяющим возбудителя с калом и мочой с последующим инфицированием околоплодных вод. При синдроме инфици-рования амниона может произойти преждевременный разрыв околоплодных оболочек с последующим развитием эндометрита, инфекционных осложне-ний новорожденного (Анкирская А.С., 1985). Учитывая ведущую роль трансплацентарного (гематогенного) инфицирования при антенатальной ВУИ, важно отметить, что состояние барьерной функции плаценты в значи-тельной мере определяет возможность развития инфекции и количество по-павшего к плоду инфекционного агента. Известно, что фетоплацентарная не-достаточность резко увеличивает риск развития генерализованной ВУИ при наличии хронического очага или остром заболевании у беременной.
Гематогенный путь передачи инфекции характерен для цитомегалови-русной, энтеровирусной инфекции, вируса простого герпеса, ветряной оспы, а также наблюдается при листериозе, микоплазмозе, некоторой бактериаль-ной инфекции и приводит к тяжёлым диссеминированным поражениям фе-топлацентарной системы, жизненно важных органов плода (мозга, печени, лёгких) (Девис П. А., 1987; Лозовская Л. С., 1995; Самохин П. А., 1987; Си-макова М. Г., 1995).
Восходящий путь инфицирования характерен для условно - патогенной микрофлоры, грибковой инфекции, а также наблюдается при хламидиозе, микоплазмозе, листериозе, других инфекциях. При восходящем пути инфи-цирования микроорганизмы проникают через плодные оболочки в около-плодные воды, где происходит размножение возбудителя. При этом плод оказывается в инфицированной среде. Заражение внутренних полостей плода происходит при заглатывании и аспирации инфицированных вод (Гуртовой Б. Л., Анкирская А. С., 1994; Цинзерлинг А. В., 1986).
Нисходящий путь инфицирования менее характерен для ВУИ, хотя его риск высок при персистенции возбудителей в эндометрии и маточных трубах (хламидии, микоплазмы, уреаплазмы) (Радзинский В. Е., 1996; Тареева Т. Г., 1994).
Интранатальный путь инфицирования (заражение плода во время родов путём аспирации или заглатывания содержимого родовых путей матери) наиболее характерен для бактериальной инфекции (стрептококк группы В, E.сoli, стафиллококк, Proteus, клебсиелла, анаэробная флора), но возможен и для вирусной (ВПГ, ЦМВ) инфекции, грибов рода Кандида. Причем передача инфекции возможна как при наличии симптомов поражения в области шейки матки и вульвы, так и при бессимптомном выделении возбудителя (Адаске-вич В. П., 1996; Барашнев Ю. И., 1994; Кудашев Н. И., 1991; Carmack M. A., 1993).
Таким образом, при наличии у беременной урогенитальной инфекции внутриутробное инфицирование плода и новорожденного может произойти любым из вышеперечисленных путей.

Российская Академия Естествознания приняла участие в выставке BUCH WIEN 2019, (Австрия, Вена , 6-10 ноября 2019 года).

С 12 по 15 октября 2019 г. в г. Сочи состоялся заключительный очный этап VII международного конкурса научно-исследовательских и творческих работ учащихся "СТАРТ В НАУКЕ" и итоговое заседание педагогов высшей и средней школы в рамках научно-практической конференции "Современные проблемы школьного образования".

Российская Академия Естествознания (Международная ассоциация учёных, преподавателей и специалистов) приняла участие в 32-й Московской международной книжной выставке-ярмарке, г. Москва, ВДНХ, 4-8 сентября 2019 года.

Российская Академия Естествознания Приняла участие в выставке HONG KONG BOOK FAIR 2019, (КНР, Гонконг, 17-23 июля 2019 года).

Российская Академия Естествознания Приняла участие в выставке BOOKEXPO AMERICA 2019, (США, Нью-Йорк, 29-31 мая 2019 года).

Рубрика: 11. Прочие отрасли медицины и здравоохранения
Статья просмотрена: 2138 раз
Цель исследования рассмотреть возможные причины и факторы риска возникновения внутриутробной инфекции.
Материал и методы исследования. Проанализировано 100 протоколов патологоанатомических вскрытий из Объединенной детской прозектуры КДКБ.
Актуальность. Внутриутробные инфекции (ВУИ) — группа инфекционно-воспалительных заболеваний плода и детей раннего возраста, которые вызываются различными возбудителями, но характеризуются сходными эпидемиологическими параметрами и нередко имеют однотипные клинические проявления. Врожденные инфекции развиваются в результате внутриутробного (анте- и/или интранатального) инфицирования плода. При этом в подавляющем большинстве случаев источником инфекции для плода является мать. [2] В последние годы наблюдается увеличение частоты внутриутробных инфекций и возрастание их роли в перинатальной смертности. Несмотря на рост рождаемости, показатели детской смертности в период новорожденности остаются высокими. Группу повышенного риска внутриутробного инфицирования плода также составляют беременные с обострениями хронических инфекционных и соматических заболеваний, ОРВИ, инфицирование вирусом корьевой краснухи.Одним из наиболее распространенных путей инфицирования плода является гематогенный путь. Однако проникновение вирусной инфекции может произойти через дыхательные пути, пищеварительный тракт и кожу плода при инфицировании околоплодной жидкости. Факторами риска развития антенатальных инфекций являются: отягощенный акушерский анамнез (выкидыши, мертворождения, невынашивание при предыдущих беременностях, рождение детей с множественными пороками развития или умерших в раннем возрасте); аномалии течения текущей беременности и родов (угроза прерывания беременности, многоводие, приращение, неполная и преждевременная отслойка плаценты); заболевания мочеполовой системы у матери (эрозия шейки матки, эндоцервицит, кольпит, вульвовагинит, киста яичников, внутриматочные сращения, мочевая инфекция в виде уретрита, цистита, пиелонефрита и др.) Внутриутробныемикозымогут возникнуть при заражении плода Candida albicans восходящим путем или в родах в результате аспирации плодом содержимого родовых путей,а также гематогенно. [3]
Результаты исследования. При анализе материала 46 % летальных исходов в результате ВУИ зарегистрировано в первую неделю неонатального периода, причем 42 % детей погибло в первые сутки. Во вторую неделю погибло 14 % новорожденных. Во второй половине неонатального периода (3–4 неделя) погиб 21 ребенок (21 %); с 1 мес. до года жизни — 21 % летальных исходов (рис1).
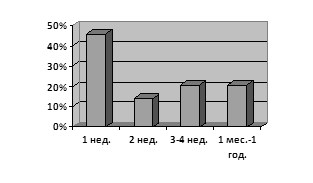
Рис. 1 Возраст умерших детей.
При анализе факторов риска, способствующих развитию внутриутробных инфекций, получены следующие результаты. Угроза прерывания беременности на разных сроках наблюдалась в 9,5 % случаев; маловодие — 2,4 %; длительный безводный период в 9,5 % наблюдений. 47,6 % родов разрешились преждевременно. В течение беременности у 9 % была диагностирована анемия 1–2ст. 22 % женщин перенесли во время беременности поздние гестозы. У повторнородящих гестоз отмечался и во время первой беременности.
При анализе гестационного срока родов установлено, что 67 % новорожденных родились в гестационном периоде менее 30 недель, 31 % родилось досрочно до 30 нед., родилось в срок 3 % детей. (рис2).
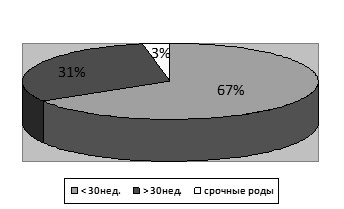
Рис. 2 Гестационный срок родов.
Из посмертных эпикризов выявлено, что 56 % матерей не были обследованы на Тorch — инфекции. ОРВИ во второй половине беременности переболело 14,3 % женщин. Инфицирование женщин ЦМВИ составило около 30 %. Аденовирусная инфекция обнаружена у 1,2 % женщин; ВПГ — 23,8 %; ВГС — 2,4 %; ВГВ — 1,2 %; зафиксирован 1 случай ВИЧ — инфекции. Титры антител к вирусу краснухи были выделены в 23,8 % случаях. 15 % матерей имели в анамнезе хронический пиелонефрит. Сравнительно редкой внутриутробной инфекцией считается токсоплазмоз, но последствия этой инфекции для плода и ребенка более пагубны, чем при других инфекциях. Титры антител к токсоплазме были выделены в 10,7 % случаев.
В последние годы в развитии внутриутробных инфекций важное значение приобретают хламидии. У беременных хламидийная инфекция проявляется в виде хронического продуктивного цервицита, однако риск внутриутробного инфицирования плода достаточно высок. У 7 % женщин в течение беременности был выявлен хламидиоз. У 2 % беременных был обнаружен кандидозный кольпит.
При анализе аутопсий детей установлено, что Enterococcus faecalis выявлены у 21 %; Mycoplasma — 8 %; Candida albicans — 8 %; Pseudomonas aeruginosa — 6 %; Escherichia coli -6 %; Klebsiella oxytoca — 4,8 %; Сandida krusei — 3,6 %; Staphylococcus epidermidis — 3,6 %; Klebsiella pneumoniae — 3,6 %; Аcinetobacter haemolyticus 2,4 %; Klebsiella mobilis — 1,2 % и другие.
Причинами смерти детей были генерализованные внутриутробные инфекции, бактериальный сепсис, пневмония, гепатит, энтероколит.
Заключение. В проведенном исследовании установлено, что 56 % матерей не были обследованы на Тorch — инфекции, что дает основания предполагать о наличии не выявленных очагов инфекций. У обследованных беременных преобладали цитомегаловирусная инфекция (30 %) и ВПГ (23,8 %). Антитела к вирусу краснухи были выделены у 23,8 % беременных. Токсоплазмы обнаружены у 10,7 % матерей. Хронический пиелонефрит выявлен в анамнезе у 14 % женщин. Данные результаты свидетельствуют о недостаточной ранней диагностике и профилактике ВУИ.
1. В. В. Власюк Морфологическая диагностика внутриутробных инфекций. Учебное пособие. СПб, 2010 — С. — 47.
2. А. В. Цинзерлинг, В. А. Цинзерлинг Патологическая анатомия. Учебник для педиатрических факультетов медицинских вузов. СПб 1996 — С. — 334.
3. А. Я. Сенчук, З. М. Дубоссарская. Перинатальные инфекции: практич. пособие. — М.: МИА, 2004 — С. — 448.
4. Дегтярев Д. Н., Дегтярева М. В., Ковтун И. Ю., Шаламова Л. В. Принципы диагностики внутриутробных инфекций у новорождённых и тактика ведения детей группы риска. — М.: Перинатология сегодня, 1997. — Т. 3. — С. 18–24.
Похожие статьи
Осложнения беременности у женщин с высоким риском. Ключевые слова: внутриутробное инфицирование плода, беременные, фетопатия. В 1 группу вошли 62 женщины группы высокого инфекционного риска, родивших детей без признаков ВУИ.
Важнейшим фактором развития внутриутробного инфицирования является период беременности, в котором происходит инфицирование беременной женщины.
ВУИ плода ЦМВ у беременных с первичным инфицированием достигает 30–50 %, при этом только у 5–18 % инфицированных детей
Осложнения беременности у женщин с высоким риском. Важнейшим фактором развития внутриутробного инфицирования является период.
Внутриутробные инфекции (ВУИ) являются одной из ведущих причин перинатальной
Под внутриутробным инфицированием плода и новорожденного понимают патологическое
Если при беременности анализы и клинические признаки доказывают у женщины ТОРЧ комплекс.
Таблица 2. Особенности течения беременности и инфекционных заболеваний у обследуемых женщин в 2 триместре.
Риск инфицированности плода и возможность реализации инфекции в виде болезни у новорожденных обусловлены ВУИ и степенью инфицирования и характером.
Также обследовали на наличие ТОRCH — инфекции влияющей на течение беременности и состояние плода, при выявлении какой-либо одной из них нами
48 % беременных основной группы и 15,56 % женщин контрольной группы перенесли вирусный гепатит.
Внутриутробные инфекции (ВУИ) на современном этапе являются одной из важнейших проблем акушерства и перинатологии.
Изучение перинатальных исходов при родах у женщин с высокой степенью внутриутробного риска инфицирования плода.
Ключевые слова: беременные, высокий риск, инфицирование плода. Внутриутробное инфицирование плода, как заболевание
Нами было принято решение исследовать ФПР у беременных с ЗВУР различной степени в сроки гестации: 16–23 недели, 24–29, 30–36, 37–40.
Основные термины (генерируются автоматически): беременная, вирусный гепатит, беременность, хронический пиелонефрит, родовая
Особенности течения беременности, родов и перинатальные.
Аннотация научной статьи по клинической медицине, автор научной работы — Булавенко О. В.
В структуре смертности новорожденных внутриутробное инфецирование занимает 1-3 место. Перинатальные исходы зависят от пути передачи инфекции, вирулентности инфекционного агента, соматического здоровья беременной и правильности выбора акушерской тактики.
Похожие темы научных работ по клинической медицине , автор научной работы — Булавенко О. В.
музеиних штаммів мікроорганізмів ита можливо рекомендувати його для лікування ускладненого карієсу з вираженим інфікуванням кореневого каналу. Цитофіл Са антимікробної дії не має.
Ключові слова: пломбування кореневих каналів, антимікробна дія.
Стаття надійшла 14.10.2012 р.
of microorganisms and is recommended for treatment of complicated caries with severe infection of the root canal. Tsitofil Ca has shown no antimicrobial activity.
Key words: root canal filling, antimicrobial activity.
ПЕРИНАТАЛЬНЫЕ ПОСЛЕДСТВИЯ ВНУТРИУТРОБНОГО ИНФИЦИРОВАНИЯ
В структуре смертности новорожденных внутриутробное инфецирование занимает 1-3 место. Перинатальные исходы зависят от пути передачи инфекции, вирулентности инфекционного агента, соматического здоровья беременной и правильности выбора акушерской тактики.
Ключевые слова: внутриутробное инфицирование, преждевременный разрыв оболочек, интранатальный путь, гематогенный путь.
Среди причин смертности новорожденных за последние годы внутриутробное инфицирование (ВУИ) плода занимает 1-3-е место, обусловливая от 11 до 45 % потерь [5, 15].
Целью работы был анализ перинатальных последствий и факторов развития внутриутробного инфицирования.
Риск инфицирования плода колеблется от 0,01 до 75 %, что обусловлено видом и типом возбудителя, характером инфекции у женщины, сопутствующей патологией [5, 8, 10]. При внутриутробном инфицировании плода мертворождаемость достигает 14,9-16,8 %, а ранняя неонатальная заболеваемость - 5,3-27,4 %. Наиболее высокий риск инфицирования плода наблюдается при первичной инфекции беременной женщины. Большая часть заболеваний беременных, приводящих к ВУИ плода, протекает в субклинической, латентной форме с активизацией процесса при любом нарушении гомеостаза под влиянием стресса, неблагоприятных экологических факторов, осложнений беременности, что затрудняет клиническую диагностику данного состояния. К сожалению, многие ВУИ в период новорожденности также не имеют специфической клинической картины, а диагностика по клиническим проявлениям, без привлечения специфических микробиологических исследований, приводит к диагностическим ошибкам в 90-95 % случаев. Анализ структуры смертности детей 1го года жизни за 10 мес. 2011 года по Винницкой области показал (рис. 1, 2), что смертность от внутриутробного инфецирования находится на первом месте и ее частота неуклонно растет с каждым годом (с 13 % в 2010 году до 23 % в 2011 году).
родовая I травма і врожд%нн
Рис. 1. Структура смертности детей 1-го года жизни за 10 мес 2011 года по Винницкой области.
В/У ИНФЕКЦИЯ асфиксия
глубокая р морфофункц. незрелость
Рис. 2. Динамика смертности детей 1 -го года жизни по Винницкой области за 2010-2011 годы.
Инфицирование плода в I триместре беременности приводит к развитию у него микро-, гидроцефалии, пороков сердца, желудочно-кишечного тракта, мочеполовой системы, скелета, катаракты, глухоты. Инфицирование во II и III триместрах вызывает у плода гепатоспленомегалию, анемию, желтуху, гипотрофию, пневмонию, менингоэнцефалит, сепсис. Существует несколько основных путей инфицирования плода. Наиболее частый - это восходящий, в результате которого инфекция проникает через шейку матки и оболочки
плодного яйца. Также существует трансплацентарный, или гематогенный путь, когда инфекционные факторы попадают через плацентарный барьер к плоду. Вначале с кровью матери они поступают в плаценту, где возможно размножение возбудителя и последующее развитие воспалительного процесса (плацентита). Преодолев маточно-плацентарный барьер, возбудитель проникает к плоду и может привести к развитию генерализованной инфекции с поражением печени, легких, почек, головного мозга и других органов [2, 11]. Распространение возбудителей может происходить и по вартонову студню пуповины, чему способствует внесосудистый ток жидкости от плаценты к плоду. Учитывая ведущую роль трансплацентарного (гематогенного) инфицирования при антенатальной ВУИ, важно отметить, что состояние барьерной функции плаценты в значительной мере определяет возможность развития инфекции и количество попавшего к плоду инфекционного агента. Фетоплацентарная недостаточность резко увеличивает риск развития генерализованной ВУИ при наличии хронического очага или остром заболевании у беременной. Кроме того, возможны нисходящий путь - из воспалительно измененных придатков матки, аппендикса, интранатальный (при прохождении плода через инфицированные родовые пути матери), смешанный и госпитальный пути передачи.
Для каждого пути передачи инфекции характерны определенные возбудители. Так, гематогенный путь передачи инфекции характерен для цитомегаловирусной, энтеровирусной инфекции, вируса простого герпеса, ветряной оспы, а также наблюдается при листериозе, микоплазмозе, некоторой бактериальной инфекции и приводит к тяжёлым диссеминированным поражениям фетоплацентарной системы, жизненно важных органов плода (мозга, печени, лёгких) [7, 13, 14]. Околоплодные воды могут быть инфицированы восходящим (из влагалища) и нисходящим (из маточных труб) путём, а также самим плодом, инфицированным гематогенно и выделяющим возбудителя с калом и мочой с последующим инфицированием околоплодных вод. При синдроме инфицирования амниона может произойти преждевременный разрыв околоплодных оболочек с последующим развитием эндометрита, инфекционных осложнений новорожденного [3]. Восходящий путь характерен для условно-патогенной микрофлоры, грибковой инфекции, а также наблюдается при хламидиозе, микоплазмозе, листериозе, других инфекциях. При восходящем пути инфицирования микроорганизмы проникают через плодные оболочки в околоплодные воды, где происходит размножение возбудителя. При этом плод оказывается в инфицированной среде. Плацента также может быть вовлечена в инфекционный процесс уже вторично, через инфицированные околоплодные воды. При этом плацента становится не столько барьером, сколько резервуаром для инфекции. Развитие плацентита в случаях внутриутробного инфецирования плода характеризуется типовым нарушением структуры и функции, микроциркуляции, гемостаза, гемореологии и трофики плода. Развитие комплекса сосудистых и тканевых изменений в плаценте, свойственных воспалению, сопровождается, безусловно, нарушением гормоно- и цитокинпродуцирующей функций плаценты.
Заражение внутренних полостей плода происходит при заглатывании и аспирации инфицированных вод [6, 15]. Факторами, способствующими восходящему инфицированию, является преждевременный разрыв плодных оболочек (ПРПО), истмико-цервикальная недостаточность (ИЦН), внешняя урогенитальная инфекция. В норме амниотическая жидкость стерильна. При нарушении целостности плодных оболочек через 6 ч у 50 % беременных, а через 24 часа - в 100 % происходит инфицирование вод. Нисходящий путь инфицирования менее характерен для ВУИ, хотя его риск высок при персистенции возбудителей в эндометрии и маточных трубах (хламидии, микоплазмы, уреаплазмы) [12]. Интранатальный путь инфицирования наиболее характерен для бактериальной инфекции (стрептококк группы В, Е.соН, стафиллококк, Proteus, клебсиелла, анаэробная флора), возможен для вирусной (ВПГ, ЦМВ) инфекции, грибов рода Кандида. Передача инфекции возможна как при наличии симптомов поражения в области шейки матки и вульвы, так и при бессимптомном выделении возбудителя [1, 4, 9]. Внутриутробное инфицирование плода достаточно часто формируется в результате хирургической коррекции истмико-цервикальной недостаточности, при длительном безводном промежутке. Широкое применение антибиотиков, формирующее штаммы с множественной лекарственной устойчивостью, также является одним из факторов риска развития ВУИ, на фоне физиологического иммунодефицита у плода и новорожденного. Во время беременности могут проявляться неблагоприятные последствия перинатальных инфекций. Среди них: задержка внутриутробного развития плода; преждевременные роды; врожденные пороки развития; перинатальные потери; острые инфекции у новорожденного; персистирующие инфекции у новорожденного; бессимптомные инфекции с поздними клиническими проявлениями; инвалидность с детства.
Внутриутробное инфецирование плода чаще происходит восходящим путем, ассоциированным с урогенитальной инфекцией, что обуславливает необходимость скрининга и коррекции данной патологии на прегравидадном этапе. При геметогенном пути передачи инфекции и развитии фето-плацентарной дисфункции, плацента может становиться резервуаром для инфекции и увеличивать риск развития генерализованной ВУИ.
1. Адаскевич В.П. Заболевания, передаваемые половым путем / В.П. Адаскевич. - Витебск, 1996. - 279 с.
2. Айламазян Э.К. Прогнозирование высокого риска внутриутробного инфицирования / Э.К. Айламазян // Рос. вестн. перинатол. и педиатрии. - 1999. - № 3. - С. 6-11.
3. Анкирская А.С. Микроэкология влагалища. Коррекция микрофлоры при вагинальных дисбиозах / А.С. Анкирская // Акуш. и гинекол. -1999. - № 3. - С. 8-9.
4. Барашнев Ю.И. Перинатальная патология у новорожденных / Ю.И. Барашнев, А.Г. Антонов, Н.И. Кудашов // Акуш. и гинекол. - 1994. -№ 4. - С. 26-31.
5. Башмакова М.А. Особенности морфологической картины биологических жидкостей при плацентарной недостаточности различного генеза / М.А. Башмакова, А. М. Савичева // Вестн. Российской ассоциации акушерства и гинекологии. - 1997. - № 3. - С. 79-81.
6. Внутриутробная бактериальная вирусная инфекция плода / Гуртовой Б.Л., Анкирская А.С., Ванько Л.В. [и др.] // Акуш. и ги-нек. - 1994. - № 4. - С. 20-26.
7. Девис П. А. Бактериальные инфекции плода и новорожденного / П.А. Девис, Л.А. Готефорс. - М.: Медицина, 1987. - С. 193-197.
8. Евсюкова И.И. Сахарный диабет: беременные и новорожденные / И.И. Евсюкова, Н.Г. Кошелева. - Спб.: Специальная литература, 1996. - 270 с.
9. Кудашов Н.И. О роли вируса герпеса в патогенезе церебральных поражений и висцеральных нарушений у новорожденных / Н.И. Кудашов // Вопр. охр. мат-ва и дет-ва. - 1991. - № 5. - С. 3-7.
10. Микоплазменная инфекция при бесплодии в браке / Акунц К.Б., Авакян Т.С., Акунц Н.С. [и др.] // Вопр. охр. мат. и дет-ва. - 1991. - Т. 36, № 2. - С. 54-57.
11. Михайлов А.В. Предварительные результаты инфекционного скрининга беременных и новорожденных в Саратовской области / А.В. Михайлов, Т.А. Гасанова, Е.С. Коляченко // Актуальные вопросы хирургии: Сб. науч. работ. - Саратов, 2003. - С. 99-105.
12. Плацентарная недостаточность при гестозе/ Радзинский В.Е., Тареева Т.Г., Микаелян А. В. [и др.] // Вестник рос. ассоц. акуш. и гинек. -1996. - № 4. - С. 105-112.
13. Самохин П. А. Цитомегаловирусная инфекция у детей (клинико-морфологические аспекты) / П. А. Самохин. - М.: Медицина, 1987. - 160 с.
14. Стефани Д.В. Иммунология и иммунопатология детского возраста: Руководство для врачей / Д.В. Стефани, Ю.Е. Вельтищев. - М., 1996. - 384 с.
15. Цинзерлинг В.А. Значение внутриутробной вирусной инфекции в органной патологии детей грудного возраста / В.А. Цинзерлинг // Мед. научный и учебно-методич. журнал. - 2001. - № 5. - С. 81-87.
ПЕРИНАТАЛЬНІ НАСЛІДКИ ВНУТРІШНЬОУТРОБНОГО ІНФІКУВАННЯ Булавенко О. В.
В структурі смертності новонароджених
внутрішньоутробного інфікування займає 1-3 місце. Перинатальні наслідки залежать від шляхів передачі інфекції, вірулентності інфекційного агенту, соматичного здоров’я вагітної та вірного вибору акушерської тактики.
Ключові слова: внутрішньоутробне інфікування,
передчасний розрив оболонок, перинатальні наслідки, інтранатальний шлях, гематогенний шлях.
Стаття надійшла 15.10.2012 р.
PERINATAL CONSEQUENCES OF PRENATAL INFECTION Bulavenko O. V.
In structure of newborns’ mortality prenatal infection takes 1-3 places. Perinatal outcomes depend on a way of the transmission of infection, a activity of the infectious agent, somatic health of the pregnant woman and correctness of a choice of obstetric tactics.
Key words: prenatal infection, premature rupture of covers, intranatalny way, hatmatogenic way.
ТОПОГРАФОАНАТОМІЧНІ ОСОБЛИВОСТІ ДВАНАДЦЯТИПАЛОЇ КИШКИ В ПЕРИНАТАЛЬНОМУ ПЕРІОДІ ОНТОГЕНЕЗУ ЛЮДИНИ
Методами анатомічного дослідження встановлено, що типовою формою дванадцятипалої кишки у перинатальному періоді є кільцеподібна. Починаючи з 7-го місяця внутрішньоутробного розвитку, чітко диференціюються тканинні шари кишкової стінки. Упродовж перинатального періоду для дванадцятипалої кишки властиві два періоди прискореного розвитку (5 і 8-10 місяці) та період сповільненого розвитку (6-7 місяці).
Ключові слова: дванадцятипала кишка, анатомія, перинатальний період.
Робота є фрагментом науково-дослідної роботи Буковинського державного медичного університету “Закономірності перинатальної анатомії та ембріотопографії. Визначення статево-вікових особливостей будови і топографоанатомічних взаємовідношень органів та структур в онтогенезі людини” (№
В останні роки науковці зосереджують увагу на діагностиці та лікуванні природжених вад органів травлення, які потребують хірургічного лікування [8, 9]. У структурі смертності дітей з хірургічними захворюваннями питома вага летальних наслідків сягає 90 % [3]. Особливу увагу приділяють своєчасній перинатальній діагностиці, яка дозволяє визначити тактику ведення вагітності [6]. Розширення анатомічних досліджень людини у перинатальному періоді онтогенезу є назрівшою необхідностю, оскільки численні захворювання дітей і дорослих етіологічно пов’язані з внутрішньоутробним періодом розвитку [2, 4].
Відомості літератури щодо закономірностей будови дванадцятипалої кишки у перинатальному періоді фрагментарні, нечисленні та безсистемні. Здебільшого вони присвячені дослідженню або анатомії дванадцятипалої кишки певної вікової групи, або ембріональним перетворенням на ранніх стадіях розвитку [1, 5, 7]. Відсутність комплексних робіт щодо визначення динаміки морфометричних параметрів дванадцятипалої кишки у перинатальному періоді зумовлюють актуальність дослідження.
Метою роботи було встановити типової і варіантної анатомії та кореляційні зв’язки морфометричних параметрів дванадцятипалої кишки у перинатальному періоді онтогенезу людини.
Матеріал і методи дослідження. Дослідження проведено на 120 препаратах трупів плодів і новонароджених дітей in situ, методами макромікропрепарування, виготовлення послідовних гістологічних
В статье рассматривается инфекционный фактор как причина ранних потерь беременности и преждевременных родов. И если роль инфекции в этиологии ранних потерь беременности минимальна, то большинство поздних выкидышей, а также ранних и сверхранних преждевременных родов обусловлено инфекционно-воспалительными заболеваниями. Отмечается, что основная стратегия профилактики потерь беременности подразумевает своевременное установление урогенитальной инфекции и ее лечение до того, как инфекционный и/или воспалительный процесс приведет к необратимым изменениям шейки матки, миометрия, плаценты, плодных оболочек и плода.
В статье рассматривается инфекционный фактор как причина ранних потерь беременности и преждевременных родов. И если роль инфекции в этиологии ранних потерь беременности минимальна, то большинство поздних выкидышей, а также ранних и сверхранних преждевременных родов обусловлено инфекционно-воспалительными заболеваниями. Отмечается, что основная стратегия профилактики потерь беременности подразумевает своевременное установление урогенитальной инфекции и ее лечение до того, как инфекционный и/или воспалительный процесс приведет к необратимым изменениям шейки матки, миометрия, плаценты, плодных оболочек и плода.
Инфекционный фактор в генезе ранних потерь беременности
Невынашивание – частое осложнение беременности [1]. Даже у молодых здоровых женщин 11–13% первых беременностей заканчиваются самопроизвольным выкидышем. Риск повторной потери беременности прогрессивно возрастает до 14–21% после одного самопроизвольного выкидыша, до 24–29% после двух и до 31–34% после трех выкидышей [2].
Несмотря на то что достоверных данных о причинах ранних потерь беременности недостаточно, спорадический выкидыш считается результатом случайных нарушений деления и повреждений половых хромосом [2, 3]. При этом большинство хромосомных аномалий возникает на этапах оогенеза, сперматогенеза и/или раннего эмбриогенеза под влиянием различных внешних или внутренних факторов в парах с нормальным кариотипом [4].
Инфекционный фактор в генезе ранних спорадических потерь беременности несущественен и ассоциирован, как правило, с острыми инфекционно-воспалительными заболеваниями, среди которых основную роль играют возбудители TORCH-инфекций (Toxoplasma, Rubella, Cytomegalovirus, Herpes simplex virus) [5] и Listeria monocytogenes [6].
Прямой связи между инфекционно-воспалительными заболеваниями и привычным невынашиванием не обнаружено [2], поэтому углубленное инфекционное обследование данной группы пациенток считается нецелесообразным [7]. Широко практикуемый в нашей стране скрининг, направленный на выявление ДНК вирусов, Ureaplasma и Mycoplasma в цервикальном канале, также имеет небольшое практическое значение. Исследование остатков плодного яйца у 108 женщин после самопроизвольного выкидыша не выявило ДНК Ureaplasma urealyticum, Mycoplasma hominis, Cytomegalovirus и Adenovirus [8]. В 2019 г. проведено исследование, в ходе которого с помощью метода полимеразной цепной реакции качественно и количественно оценивались ДНК таких бессимптомных инфекций, как Ureaplasma parvum, Ureaplasma urealyticum, Mycoplasma hominis, Mycoplasma genitalium и Chlamydia trachomatis [9]. Изучались образцы ткани ворсин хориона и лимфоциты периферической крови у 100 женщин с самопроизвольным выкидышем и 100 женщин с искусственным прерыванием беременности до 12 недель. ДНК всех внутриклеточных бактерий были обнаружены с одинаково низкой частотой и сходной бактериальной нагрузкой в обеих группах, что позволило сделать вывод об отсутствии корреляции между инфекцией и ранними потерями беременности.
Инфекционный фактор в генезе преждевременных родов
Этиология преждевременных родов многофакторная, но исследования последних лет показали, что основная причина их развития – инфекционное поражение фетоплацентарного комплекса [10–13].
Ведущая роль инфекции в генезе преждевременных родов подчеркивается в обновленных рекомендациях Европейской ассоциации перинатальной медицины [14]. При этом степень влияния инфекционного фактора на показатель преждевременных родов напрямую зависит от срока гестации. Если при преждевременных родах, произошедших после 34 недель беременности, внутриматочная инфекция встречается редко, то при родах до 30 недель она присутствует в большинстве случаев [15]. Чем меньше срок беременности, тем больше вероятность связи преждевременного родоразрешения с инфекционным фактором [16] и тем выше частота обнаружения острого хориоамнионита, которая в 37–40 недель составляет 3,8%, в 33–36 – 10,7%, в 29–32 – 35,4%, в 25–28 – 39,6% и в 21–24 недели беременности – 94,4% [17]. Чаще всего инфицирование амниотической полости и плода происходит восходящим путем через цервикальный канал при аномальной микрофлоре нижних отделов генитального тракта, ассоциированной с бактериальным вагинозом [10, 18]. Исследования показывают статистически значимую связь бактериального вагиноза с поздним выкидышем и преждевременными родами, причем степень риска тем выше, чем раньше он был диагностирован [19].
В генезе преждевременных родов не менее значимы инфекции мочевых путей [20], среди которых чаще всего (у 2–13% беременных) встречается бессимптомная бактериурия [21, 22]. При отсутствии антибактериального лечения бессимптомной бактериурии на ранних сроках беременности риск развития пиелонефрита во втором – третьем триместре составляет 30–40% [23], что в свою очередь доказанно повышает риск преждевременных родов [24]. Кроме того, длительная бактериурия, особенно ассоциированная со стрептококком группы В, приводит к бактериальной колонизации нижних отделов генитального тракта, что тоже считается фактором риска преждевременного излития околоплодных вод, преждевременных родов, развития инфекций у плода и новорожденного [20, 25].
Гистологическое исследование последов у 266 родильниц, перенесших урогенитальную инфекцию во время беременности, выявило признаки и гематогенного инфицирования фетоплацентарного комплекса с распространенным воспалительным поражением сосудов и стромы ворсин плаценты, и восходящего инфицирования с тотальной лимфогистиоцитарной инфильтрацией плодных оболочек [26, 27]. Таким образом, инфицирование фетоплацентарного комплекса может происходить двумя путями. Первый – гематогенный через плаценту в результате бактериемии, ассоциированной с острым пиелонефритом. Второй – восходящий через цервикальный канал в результате колонизации влагалища патогенной микрофлорой при длительной бактериурии.
Как правило, микробное обсеменение амниотической полости начинается с децидуального слоя плодного пузыря и/или плаценты. В дальнейшем микробы диффузно распространяются через все слои плодных оболочек с развитием гистологического хориоамнионита, поражают структуры плаценты и проникают в околоплодные воды [10, 28]. Воспалительная инфильтрация при гистологическом исследовании последа обнаруживалась у 86% родильниц, перенесших во время беременности урогенитальную инфекцию. В каждом третьем случае она распространялась на все структуры плаценты, плодных оболочек и пуповины с развитием плацентита, гистологического хориоамнионита и фуникулита [27]. Риск рождения ребенка с клиническими проявлениями внутриутробного инфицирования (врожденной пневмонией, конъюнктивитом, энцефалитом, менингитом, синдромом инфицированности, сепсисом) в случае лимфогистиоцитарной инфильтрации в последе составил 44%. При дальнейшей миграции полиморфноядерных лейкоцитов в околоплодные воды риск инфицирования плода значительно повышался. Обнаружение большого количества полиморфноядерных лейкоцитов и бактерий при цитологическом исследовании проб околоплодных вод, полученных путем амниоцентеза во время операции кесарева сечения, всегда сочеталось с гистологическим хориоамнионитом и плацентитом, а также внутриутробной пневмонией у новорожденного. При этом у всех беременных инфицирование амниотической полости протекало бессимптомно в отсутствие каких-либо клинических признаков хориоамнионита. Бессимптомное интраамниотическое инфицирование часто ассоциировано и с другими неблагоприятными исходами беременности: преждевременными родами, преждевременным излитием околоплодных вод, короткой шейкой матки, преждевременной отслойкой нормально расположенной плаценты [28–30]. Патогенез осложнений беременности обусловлен воспалительной реакцией со стороны фетоплацентарного комплекса в ответ на агрессивное воздействие микробных возбудителей.
Микробная инвазия в амниотическую полость вызывает воспалительную реакцию со стороны амниотического эпителия плодных оболочек и пуповины, а также кожных покровов и слизистой дыхательных путей плода, что приводит к выработке провоспалительных цитокинов (интерлейкинов 1, 6, 8, фактора некроза опухоли альфа и др.), хемокинов, матриксных металлопротеиназ и активации синтеза простагландинов [31–33]. Возникающий воспалительный ответ становится триггером маточной сократительной активности, укорочения шейки матки и преждевременных родов [31–34]. Резкое увеличение уровня матриксных металлопротеиназ, эластазы нейтрофилов и ряда других ферментов – один из факторов, который может привести к разрыву плодных оболочек [35]. С повышением концентрации матриксной металлопротеиназы 8 и интерлейкина 6 в околоплодных водах связывают увеличение риска преждевременных родов, детского церебрального паралича и сепсиса у новорожденного [28, 36, 37].
Бактерии в составе биопленок трудно идентифицируются традиционными методами исследования, обладают большей резистентностью к антимикробной терапии и плохо распознаются клетками иммунной системы матери, поэтому часто не вызывают миграции полиморфноядерных лейкоцитов в околоплодные воды [52]. Микробные биопленки в амниотической полости определяются с помощью ультразвукового исследования трансвагинальным датчиком в виде скопления плотного эхопозитивного осадка – сладжа, расположенного пристеночно в нижнем полюсе плодного пузыря у внутреннего зева шейки матки. Установлено, что сладж в околоплодных водах ассоциируется с гистологическим хориоамнионитом [48, 53–56], высоким риском внутриутробных инфекций и развитием сепсиса у новорожденного [57, 58]. Кроме того, сладж – независимый фактор риска преждевременных родов [55, 59–62] и преждевременного излития околоплодных вод [49]. Анализ исходов беременности у 99 женщин с высоким риском преждевременных родов (преждевременные роды в анамнезе, многоводие, инфекции мочевых путей во время беременности, конизация/эксцизия шейки матки в анамнезе) показал, что при наличии сладжа в околоплодных водах частота преждевременных родов составила 66,7%, а неонатальной заболеваемости – 50%, тогда как при отсутствии сладжа – 27 и 24% соответственно [61].
В другом исследовании изучались исходы беременности у 29 женщин со сладжем в околоплодных водах в 15–24 недели беременности [63]. Все они перенесли инфекционно-воспалительные заболевания в первом триместре: бактериальный вагиноз (72,4%), бессимптомную бактериурию или острый цистит (41,4%), вульвовагинальный кандидоз (31,0%) и заболевания дыхательных путей, в частности острый трахеит, бронхит, гайморит (13,8%). Важно, что абсолютное большинство (80%) женщин с бактериальным вагинозом и вульвовагинальным кандидозом и все женщины с бессимптомной бактериурией/острым циститом не получали противомикробной терапии до включения в исследование. Лечение инфекций дыхательных путей в течение трех – пяти недель также проводилось только симптоматическими средствами. В результате частота бактериального вагиноза на момент обнаружения сладжа составила 100%, вульвовагинального кандидоза – 53,9%, острого пиелонефрита – 17,2% (42,7% среди женщин с бессимптомной бактериурией/острым циститом в первом триместре), сохранялись симптомы заболеваний дыхательных путей. Длительная персистенция микробных возбудителей в организме и контаминация ими фетоплацентарного комплекса привела к появлению сладжа в околоплодных водах, причем риск преждевременных родов составил 46,2%, послеродового эндометрита – 23,1%, а 61,5% детей родились с клиническими признаками внутриутробных инфекций.
Как правило, сладж в околоплодных водах выявляется во втором триместре беременности на скрининговом ультразвуковом исследовании длины шейки матки. На сегодняшний день доказано, что ее преждевременное укорочение – высокоинформативный прогностический маркер риска развития преждевременных родов [64, 65]. При длине шейки матки ≤ 25 мм на 18–23-й неделе беременности риск преждевременных родов составляет 20%, а ≤ 15 мм – 50% [66, 67]. В сочетании со сладжем прогноз беременности значительно ухудшается. Если чувствительность длины шейки матки ≤ 25 мм в прогнозировании риска преждевременных родов, по данным I. Adanir и соавт., составляет 34%, то в сочетании со сладжем она достигает 56% [61].
Короткая шейка матки
Согласно рандомизированным клиническим исследованиям, пролонгированное применение вагинального прогестерона до 36 недель у беременных с короткой шейкой матки достоверно снижает риск преждевременных родов [66, 68, 69]. Более того, назначение вагинального прогестерона при угрожающих преждевременных родах совместно с токолитическими средствами потенцирует их действие (р
Читайте также:


