Циклофосфан отзывы больных красной волчанкой
Trusted evidence. Informed decisions. Better health.
Select your preferred language for Cochrane Reviews. You will see translated Review sections in your preferred language. Sections without translation will be in English.
Select your preferred language for the Cochrane Library website.
We noticed your browser language is Russian.
You can select your preferred language at the top of any page, and you will see translated Cochrane Review sections in this language. Change to Russian.
Cochrane Systematic Review - Intervention Version published: 28 February 2013 see what's new
- New search
Abstract
Neuropsychiatric involvement in systemic lupus erythematosus (SLE) is complex and it is an important cause of morbidity and mortality. Management of nervous system manifestations of SLE remains unsatisfactory. This is an update of a Cochrane review first published in 2000 and previously updated in 2006.
To assess the benefits and harms of cyclophosphamide and methylprednisolone in the treatment of neuropsychiatric manifestations of SLE.
We searched the Cochrane Central Register of Controlled Trials (CENTRAL), MEDLINE, EMBASE, LILACS, SCOPUS and WHO up to and including June 2012. We sought additional articles through handsearching in relevant journals as well as contact with experts. There were no language restrictions.
We included all randomised controlled trials that compared cyclophosphamide to methylprednisolone in patients with SLE of any age and gender and presenting with any kind of neuropsychiatric manifestations.
Two review authors independently extracted, assessed and cross‐checked data. We produced a 'Summary of findings' table. We presented dichotomous data as risk ratios (RRs) with 95% confidence intervals (CIs).
We did not include any new trials in this update. One randomised controlled trial of 32 patients is included. Concerning risk of bias, generation of the allocation sequence was at low risk; however, allocation concealment, blinding and selective reporting were at high risk. Treatment response, defined as 20% improvement from basal conditions by clinical, serological and specific neurological measures, was found in 94.7% (18/19) of patients using cyclophosphamide compared with 46.2% (6/13) in the methylprednisolone group at 24 months (RR 2.05, 95% CI 1.13 to 3.73). This was statistically significant and the number needed to treat for an additional beneficial outcome (NNTB) of treatment response is three. We found no statistically significant differences between the groups in damage index measurements (Systemic Lupus International Collaborating Clinics (SLICC)). The median SLE Disease Activity Index (SLEDAI) rating favoured the cyclophosphamide group. Cyclophosphamide use was associated with a reduction in prednisone requirements. All the patients in the cyclophosphamide group had electroencephalographic improvement but there was no statistically significant difference in decrease between groups in the number of monthly seizures. No statistically significant differences in adverse effects, including mortality, were reported between the groups.
This systematic review found one randomised controlled trial with a small number of patients in the different clinical subgroups of neurological manifestation. There is very low‐quality evidence that cyclophosphamide is more effective in reducing symptoms of neuropsychiatric involvement in SLE compared with methylprednisolone. However, properly designed randomised controlled trials that involve large numbers of individuals, with explicit clinical and laboratory diagnostic criteria, sufficient duration of follow‐up and description of all relevant outcome measures, are necessary to guide practice. As we did not find any new trials to include in this review at update, the conclusions of the review did not change.
Резюме на простом языке
Эффективен ли циклофосфамид для лечения волчанки центральной нервной системы (психоневрологической волчанки)?
Исследователи Кокрейновского Сотрудничества провели обзор о влиянии циклофосфамида на людей с волчанкой центральной нервной системы по сравнению с обычным лечением метилпреднизолоном. После поиска всех соответствующих исследований, они обнаружили одно исследование с участием 32 людей. В исследовании сравнивали лиц, которые принимали циклофосфамид внутривенно (или через вену) с лицами, принимавшими стероиды (метилпреднизолон внутривенно). В начале исследования все пациенты принимали стероидные таблетки (преднизон), и их количество было уменьшено в течение исследования. Исследование длилось два года.
Результаты приведены ниже:
У людей с волчанкой центральной нервной системы:
‐ Мы не уверены, улучшает ли циклофосфамид признаки и симптомы или активность заболевания по сравнению с метилпреднизолоном.
‐ Между двумя группами не было обнаружено каких‐либо различий в отношении повреждения тканей или органов, или в числе ежемесячных судорог, но это могло произойти случайно.
‐ После шести месяцев лечения, лица, которые принимали циклофосфамид, приняли меньше таблеток преднизона, чем пациенты, принимавшие метилпреднизолон.
‐ И в конце второго года, большее число лиц, принимавших циклофосфамид, продолжали лечение, чем принимавших метилпреднизолон.
Мы часто не имеем точной информации о побочных эффектах и осложнениях. Это особенно актуально для редких, но серьезных побочных эффектов. Побочные эффекты, такие как инфекции, высокий уровень сахара в крови и высокое кровяное давление, проблемы с поджелудочной железой и смерть произошли примерно одинаково у пациентов, принимавших циклофосфамид или метилпреднизолон.
Что такое волчанка центральной нервной системы и как может помочь циклофосфамид?
Системная красная волчанка (СКВ) это заболевание, при котором иммунная система организма поражает тело. При волчанке ЦНС (центральной нервной системы) тело может поражать и повреждать клетки головного и спинного мозга. Это повреждение может вызвать у человека судороги/конвульсии, хронические головные боли, спутанность сознания и психозы. Лекарственные средства, такие как кортикостероиды (преднизон или метилпреднизолон), как правило, используются при волчанке, чтобы уменьшить воспаление и контролировать иммунную систему. Также могут быть использованы иммунодепрессивные или цитотоксические средства, такие как циклофосфамид (CTX или Cytoxan).
Что происходит с людьми с волчанкой центральной нервной системы, которые принимают циклофосфамид по сравнению с метилпреднизолоном?
‐ на 49 человек больше получили улучшение среди принимавших циклофосфамид по сравнению с принимавшими метилпреднизолон.
‐ 95 из 100 человек имели по крайней мере 20%‐е улучшение симптомов при использовании циклофосфамида.
‐ 46 из 100 человек имели по крайней мере 20%‐е улучшение симптомов при использовании метилпреднизолона.
За последние два десятилетия благодаря рациональному использованию кортикостероидных гормонов (КГ) и цитотоксических иммунодепрессантов (ЦИ) удалось значительно улучшить жизненный прогноз больных системной красной волчанкой (СКВ). Проведение пульс-терапи
За последние два десятилетия благодаря рациональному использованию кортикостероидных гормонов (КГ) и цитотоксических иммунодепрессантов (ЦИ) удалось значительно улучшить жизненный прогноз больных системной красной волчанкой (СКВ). Проведение пульс-терапии метилпреднизолоном (МП) и циклофосфаном (ЦФ) у больных с волчаночным нефритом, поражением центральной нервной системы (ЦНС) и цитопеническим кризом способствует ускорению сроков достижения клинического улучшения. Патофизиологическим обоснованием для применения ударных доз метилпреднизолона является его способность активно влиять на систему иммунитета и подавлять воспалительные реакции. Один из важнейших эффектов ударных доз КГ — подавление активности нейтрофилов и моноцитов и способность вызывать транзиторную перераспределительную лимфопению. Угнетающее воздействие мегадоз кортикостероидов на функцию В-лимфоцитов приводит к стойкому снижению продукции иммуноглобулинов, а следовательно, и аутоантител, а также к уменьшению образования патологических иммунных комплексов. Из других важных компонентов механизма действия ударных доз КГ заслуживают внимания воздействие на систему цитокинов-интерлейкинов-1,6, фактора некроза опухоли, металлопротеиназ и липокортина, ингибиция экспрессии и функциональной активности Fc и СЗ рецепторов мононуклеарных фагоцитов.
Консервативная терапия с использованием подавляющих доз преднизолона и цитостатиков, назначаемых внутрь, у некоторых больных улучшает клиническую картину, но почти не влияет на жизненный прогноз, особенно в случаях прогрессирующего волчаночного нефрита, церебрального криза и геморрагического пневмонита. Однократное трехдневное применение ПТ МП может за сравнительно короткое время уменьшить клиническую и лабораторную активность при нефротическом синдроме. Однако 5-летняя выживаемость пациентов, как правило, не превышает 60%. Другими словами, ударные дозы МП прекрасно зарекомендовали себя в качестве фактически ургентной терапии, с успехом применяющейся в ситуациях, непосредственно угрожающих жизни пациента, при нарастании симптоматики и в случаях неэффективности или невозможности использования консервативной схемы лечения.
Практически при всех прогрессирующих хронических заболеваниях, в том числе и аутоиммунных, жизненный и социальный прогноз в огромной степени зависит от системного, программного подхода к терапии.
Различные схемы и программы интенсивной терапии у больных СКВ стали появляться уже с середины 80-х годов и сводились к назначению ПТ в ежемесячном режиме в течение полугода. Несколько позже появилась схема программного назначения ПТ в комбинации с циклофосфаном: 1 г циклофосфана может быть добавлен к стандартной пульс-терапии обычно на 2-3-й день лечения или дополнительно к метипреду при ежемесячном режиме. Показанием для комбинированного использования циклофосфана и метипреда является манифестная высокоактивная СКВ с выраженными иммунологическими нарушениями. Программное применение пульс-терапии ЦФ у больных быстро прогрессирующим люпус-нефритом впервые в стране предложила группа исследователей во главе с профессором И. Е. Тареевой. Согласно этой методике, ЦФ вводится внутривенно из расчета 1 г на 1 м 2 поверхности тела 1-2 раза в месяц в течение года. По сравнению с пероральным назначением ЦФ эта программа позволяет добиться хороших и стабильных результатов более чем у 70% больных с прогрессирующим нефритом. Особенно важным представляется то, что внутривенное введение мегадоз ЦФ оказывает значительно меньшее токсическое воздействие на эпителий мочевого пузыря и костный мозг, практически не вызывая геморрагических циститов и агранулоцитоза.
Другое направление интенсивной терапии ревматических заболеваний — экстракорпоральные методы лечения: плазмаферез (ПФ) и практически все сорбционные технологии, гемо- и плазмосорбция. В современном исполнении ПФ осуществляется с помощью центрифужной или мебранной технологии с удалением 40-60 мл плазмы на 1 кг веса больного. Для замещения потери белка используется альбумин или свежезамороженная плазма. Стандартные курсы ПФ состоят из 3-6 процедур, проводимых последовательно или с короткими интервалами, с суммарной эксфузией плазмы до 15 л.
Интерес к ПФ у ревматологов возник на рубеже 60-80-х годов после фундаментальных исследований, посвященных иммунокомплексной природе СКВ, изучению механизмов иммунокомплексного поражения органов и тканей и патогенетической роли антител к нативной ДНК. Представлялось вполне рациональным уменьшить степень тканевых повреждений за счет удаления из циркуляции иммунных комплексов (ЦИК), антител к ДНК (а-ДНК), криоглобулинов и цитокинов.
Первые попытки применения терапевтического ПФ у больных СКВ продемонстрировали возможности этого метода в первую очередь в ситуациях, когда кортикостероидная и иммуносупрессивная терапия оказывается неэффективной, при наличии высокого уровня ЦИК, а-ДНК, криоглобулинемии, цитопениях. Выявлена прямая зависимость между адекватным удалением из циркуляции патологических белковых структур и клиническим эффектом, изучены механизмы деблокирования РЭС и повышения естественного клиренса.
Эффективность плазмафереза (от нескольких процедур до многократно повторяемых серий при неблагоприятном течении СКВ) хорошо известна и доказана в ходе многочисленных, в основном зарубежных, исследований 80-90-х годов. Пока не получено убедительных данных об эффективности ПФ у больных люпус-нефритом. Результаты проведенных в США и Канаде открытых и контролируемых испытаний весьма противоречивы.
Идея синхронной ИТ материализовалась уже в 80-х годах и является практически неотъемлемой частью лечения некоторых системных васкулитов, синдрома Гудпасчера, Вегенера, Хаммана-Ричи, криоглобулинемической пурпуры и поражения центральной и периферической нервной системы при болезни Шегрена. Первые успешные попытки применения синхронной ИТ у больных СКВ были предприняты в 1984 году в Японии, России и Германии: за рубежом — плазмаферез в комбинации с ЦФ, в России — ПФ в комбинации с пульс-терапией МП и ЦФ.
В Институте ревматологии начиная с середины 80-х изучалась эффективность синхронного применения ПФ и пульс-терапии МП и ЦФ у 56 больных СКВ с неблагоприятным жизненным прогнозом. Методика проведения синхронной интенсивной терапии (СИТ) заключалась в следующем: в течение первого месяца больным проводились три процедуры ПФ с удалением не менее 1500 мл плазмы за сеанс, интервалы между процедурами составляли 5-6 дней. После каждой процедуры назначался внутривенно 1 г метипреда, а после второй процедуры к МП добавлялся 1 г ЦФ. Далее в течение года через каждые 3 месяца проводилась одна процедура ПФ с последующим введением 1 г МП и 1 г ЦФ. Основу группы составляли молодые женщины, в подавляющем большинстве с небольшим сроком заболевания, с развернутой клиникой СКВ. Почти у каждого пациента наблюдался прогрессирующий волчаночный нефрит, более чем у половины — нефротический синдром, церебропатия, у трети больных на фоне криоглобулинемии наблюдался распространенный генерализованный васкулит кожи и слизистых оболочек. Высокая клиническая активность сопровождалась значительным повышением уровня антител к ДНК, ЦИК и гипокомплементемией.
Особо следует подчеркнуть, что у половины больных этой группы стандартная терапия, включавшая в себя массивные дозы кортикостероидов и иммунодепрессантов, была неэффективной, а почти трети пациентов адекватная терапия вообще не проводилась.
Многолетнее наблюдение за этой группой больных по окончании 12-месячной СИТ позволило сделать заключение о ее высокой эффективности. Среди этих пациентов 5-летняя выживаемость составила 81%. Наиболее показательными оказались результаты применения СИТ в группе из 12 подростков, у которых течение волчанки, как правило, приобретает фатальный характер. За весь период наблюдения состояние, близкое к клинико-лабораторной ремиссии, было отмечено у 8 из 12 больных, у 2 пациентов эпизодически наблюдались кратковременные обострения СКВ. Ежедневная доза преднизолона составляла от 2,5 до 15 мг, у одной пациентки кортикостероиды были полностью отменены. Большинству больных удалось вернуться к нормальной жизни, учебе, посильной работе, некоторые пациентки вышли замуж и имеют здоровых детей.
Таким образом, программа синхронной интенсивной многомесячной терапии оказывает значительное влияние на клинико-лабораторные проявления и существенно улучшает жизненный и социальный прогноз у больных СКВ с прогностически неблагоприятным вариантом течения. Синхронное назначение ПФ и внутривенное введение ударных доз МП и ЦФ могут использоваться по жизненным показаниям в случаях так называемого волчаночного криза — при тромбоцитопенической пурпуре, церебральной коме, развитии тромбозов, инфарктов и инсультов у больных с антифосфолипидным синдромом и геморрагическим пневмонитом. В этих ситуациях проведение СИТ обычно ограничивается 3-4 последовательными процедурами — вплоть до купирования ургентной ситуации. В случаях с заведомо неблагоприятным долгосрочным жизненным прогнозом — прогрессирующий гломерулонефрит или поражение ЦНС, язвенно-некротический васкулит, острое начало болезни у подростка — требуется проведение длительных программ СИТ.
Нам представляется, что возможности программной СИТ далеко не исчерпаны. Перспективным может оказаться добавление в схему внутривенного иммуноглобулина, моноклональных антител и интерферонов, применение которых способно блокировать образование аутоантител и патологических ЦИК. Весьма актуальным остается индивидуальный подбор программы с более частым (ежемесячным, еженедельным) назначением плазмафереза и ПТ. Особенно важным аспектом, обеспечивающим возможность проведения более длительных и полноценных курсов экстракорпоральных процедур, является внедрение новых технологий обработки плазмы, таких, как каскадная фильтрация и иммуносорбция, применение которых позволяет сводить к минимуму потерю альбумина и селективно удалять из циркуляции патологические аутоантитела и иммунные комплексы.

Системная красная волчанка (СКВ) – хроническое полисиндромное заболевание, преимущественно поражающее молодых женщин и девушек, развивающееся на фоне генетически обусловленного несовершенства иммунорегуляторных процессов, с развитием аутоиммунного и иммунокомплексного воспаления [5, 6].
В Казахстане системная красная волчанка встречается повсеместно. По нашим клиническим наблюдениям, это заболевание в последние годы имеет тенденцию к росту и отличается агрессивностью течения.
Клиника СКВ характеризуется полиморфизмом. Наиболее часто заболевание начинается незаметно, с неспецифических симптомов: повышения температуры, болей в суставах, недомогания и слабости, трофических расстройств, похудания, различных кожных высыпаний.
Суставной синдром – наиболее частое клиническое проявление, наблюдающийся почти у 90 % больных. У ряда больных может развиться деформирующий неэрозивный артрит кистей (синдром Жакку).
Наиболее характерными признаками поражения сердца при СКВ является перикардит, но при люпус-кардите могут поражаться все оболочки сердца. По современным литературным данным российских и зарубежных исследователей при СКВ с антифосфолипидным синдромом, в частности у мужчин, наблюдалась ассоциация венозных тромбозов с атеросклеротическими изменениями сосудов, которые могут явиться факторами риска инфаркта миокарда. У больных СКВ рано развивается атеросклеротическое поражение коронарных сосудов, атеротромбоз, приводящие к сосудистым катастрофам. Выявляются аневризмы коронарных артерий, а в некоторых случаях и коронарииты.
При вовлечении в патологический процесс сосудов мелкого и среднего калибра наблюдаются симптомы васкулита-сетчатое ливедо, дигитальные инфаркты, рецидивирующий тромбофлебит и хронические язвы голеней, ассоциирующиеся с антифосфолипидным синдромом заболевание, в основе которого лежит выработка специфических антител к фосфолипидам [4].
При СКВ патология со стороны легких развивается на 2-3 году болезни и характеризуется одышкой, иногда кровохарканьем, аускультативно -ослаблением дыхания, наличием незвучных влажных хрипов в нижних отделах. В наших наблюдениях был случай инфаркт пневмонии, клиника тромбоэмболии мелких ветвей в легочную артерию на фоне антифосфолипидного синдрома.
При длительном течении СКВ классический люпус-нефрит отмечается у половины больных. В некоторых случаях люпус-нефрит может быть в дебюте заболевания, проявляющийся изолированным мочевым, нефритическим синдромами, повышением артериального давления до очень высоких цифр, как систолического, так и диастолического, высокими показателями азотистых шлаков, подтверждающих развитие почечной недостаточности.
Также при длительном течении СКВ отмечается поражение ЖКТ почти у половины больных. Могут наблюдаться различные гастропатические явления, желудочно-кишечные кровотечения и боли в животе. Необходимо помнить, что абдоминальный синдром может быть следствием проводимой патогенетической терапии [1, 2].
За последнее время стали встречаться тяжелые формы поражения ЦНС, сопровождающиеся упорными головными болями, повышением внутричерепного давления, диплопией в основе которого вероятно, лежит васкулит. В нашей клинике в течение 10 лет наблюдения наиболее запоминающим были два случая тяжелого быстропрогрессирующего менингоэнцефалита с исходом в отек мозга.
Изучение эффективности синхронной терапии при тяжелом течении и высокой степени активности СКВ с системными проявлениями.
Материалы и методы исследования
Обследовано 40 больных СКВ с системными проявлениями с различной тяжестью течения и степенью активности. Возраст больных – от 16 – 49 лет (женщин – 38; 94 %, мужчин – 2; 6 %). По системности поражения выделены больные с люпус-нефритом – 7 (17 %), с поражением ЦНС – 6 (16 %), с АФС синдромом – 7 (17 %). У 20 больных (50 %) в большей степени отмечались поражения кожи, сосудов (синдром Рейно), суставов. У больных с люпус-нефритом (артериальной гипертензией, нефротическим синдромом), АФС синдромом, поражением ЦНС, менингоэнцефалитическим синдромом наблюдались высокая степень активности и тяжелое течение, что явилось основанием для подбора синхронной терапии на фоне проводимого патогенетического лечения.
Результаты исследования и их обсуждение
При СКВ клиника заболевания настолько полиморфна, что единой схемы лечения, приемлемой для всех больных нет. Должен быть строгий индивидуальный подход к терапии в каждом конкретном случае.
Применяемые нестероидные противовоспалительные препараты эффективны при болях в мягких тканях, суставах, головных болях, а также при индуцированной медикаментами волчанке.
Аминохинолиновые препараты делагил 0,5 г/сутки, плаквенил 0,4 г/сутки применяются при низкой активности болезни на фоне фотосенсибилизации и умеренного поражения кожи и суставов. Аминохинолиновые препараты также, как и НПВП назначаются в комбинации с глюкокортикостероидами (ГКС).
При высокой степени активности и с системными проявлениями заболевания (поражением внутренних органов), ГКС терапия обязательна. Начальная доза определяется из расчета 1-2 мг преднизолона на 1 кг массы тела в день и обычно составляет 50 мг/день и более.
В лечении СКВ широко применяются иммунодепрессанты, такие как азатиоприн, циклофосфан, метотрексат в обычных стандартных дозах.
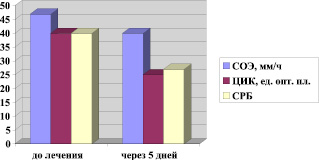
Влияние синхронной терапии на динамику лабораторных показателей
В качестве интенсивной терапии при СКВ применяется пульс- терапия метилпреднизолоном (солу-медрол) в/венно, чаще всего по 1000 мг 3 дня подряд в один или в 2 приема, а также комбинированная терапия метилпреднизолоном и циклофосфаном (при этом в первый день в/венно вводят 1000 мг метилпреднизолона и 1000 мг циклофосфана, а в последующие 2 дня вводится только метилпреднизолон по 1000 мг). Комбинированная пульс-терапия может быть терапией выбора при СКВ с тяжелым люпус-нефритом с нефротическим синдромом и нейролюпусом, генерализованным васкулитом. При неэффективности терапии ГКС и цитостатиками применяются экстракорпоральные методы (плазмаферез, гемосорбция).
В последние годы в практику терапевтической деятельности прочно вошла альтернативная интенсивная и синхронная терапия /пульс-терапия с предварительным я и резистентности к проводимой стандартной терапии.
Назначали синхронную терапию: предварительный плазмаферезпроведением плазмафереза, которая применяется при тяжелом течении заболевани с последующим введением 1000 мг метилпреднизолона и 1000 мг циклофосфана в течение 3-х дней. В дальнейшем в синхронную терапию повторяли ежемесячно однократно с минимальной дозой метилпреднизолона и циклофосфана в течение от 6 до 12 месяцев.
При применении синхронной терапии были получены положительные результаты в динамике заболевания. Субъективная оценка эффективности проводимой терапии отмечалась больными уже на 2-3й день: значительные улучшения 12 больных, улучшение – 27 больных, положительного результата не получено у 1 больного. На 4-5 день лечения нормализовались общеклинические лабораторные показатели: значительно снизилась скорость оседания эритроцитов, уровень С-реактивного белка и циркулирующих иммунных комплексов.
Нами была изучена эффективность синхронной терапии в лечении СКВ с системными проявлениями высокой степенью активности и тяжелым течением. Результаты исследования показали значительную эффективность синхронной терапии в лечении СКВ с системными проявлениями как по клиническим данным, так и по анализу лабораторных данных.
Полученные результаты свидетельствуют о несомненном преимуществе применения синхронной терапии в лечении СКВ с поражением жизненно важных органов, тяжелым течением и высокой степенью активности.
Что такое системная красная волчанка?
Системная красная волчанка (СКВ) – одно из наиболее тяжелых и часто встречающихся заболеваний из группы диффузных болезней соединительной ткани, характеризующееся образованием широкого спектра антител к собственным тканям и поражением практически всех органов и систем.
Как часто встречается встречается СКВ?
Распространенность СКВ достоверно возросла на протяжении второй половины XX в. И в настоящее время составляет в разных регионах от 4 до 250 случаев на 100000 населения. Частота СКВ у детей до 15 лет составляет 1:100000. Заболевание редко встречается у детей дошкольного возраста, в основном болеют девочки-подростки в возрасте 12-14 лет. Мальчики болеют СКВ редко, соотношение между мальчиками и девочками до 15 лет составляет 4,5:1.
Почему возникает СКВ?
Причины возникновения СКВ до настоящего времени неизвестны. Большую роль играет наследственный фактор. Так, частота ревматизма и ревматоидного артрита в семьях детей, больных СКВ в 2-5 раз превышает частоту этих заболеваний в общей популяции. Риск заболевания СКВ среди однояйцевых близнецов в 50 раз выше, чем у разнояйцевых близнецов, что также подтверждает роль наследственности в возникновении этого заболевания.
Среди факторов внешней среды первостепенное значение имеет инсоляция, воздействие которой часто провоцирует начало и последующие обострения СКВ. Преобладание среди больных девочек пубертатного возраста и молодых женщин, частые обострения заболевания после беременности и родов, позволяют предположить значение гормонального фактора в развитии СКВ. Имеются данные о том, что для больных СКВ, как для мужчин, так и для женщин, характерны повышенный уровень эстргенов и сниженный уровень андрогенов в крови.
Под воздействием неблагоприятных факторов (инсоляция, вирусная инфекция, переохлаждение, вакцинация, психическая травма), у ребенка, предрасположенного к развитию СКВ начинается неконтролируемая выработка антител к собственным тканям организма, в результате которой поражаются практически все органы и системы.
Опасна ли системная красная волчанка?
СКВ - это тяжелое заболевание, при отсутствии лечения нередко приводящее к смерти больного. Однако, правильным лечением можно достичь состояния продолжительной ремиссии (то есть относительного благополучия), длящейся месяцы, а иногда - и годы. Больные СКВ должны четко выполнять все рекомендации врача, так как при воздействии неблагоприятных факторов или при резкой отмене лечения возможно новое обострение заболевания, даже при многолетней ремиссии.
Как проявляется системная красная волчанка?
Для СКВ характерно поражение многих органов и систем. Наиболее часто в процесс вовлекаются кожные покровы, суставы, сердце, почки, нервная система, легкие.
Поражение суставов – артрит (синовит) – наблюдается у 80-90% больных, обычно в виде мигрирующих артралгий или артритов, реже – стойкого болевого синдрома с болевыми контрактурами. Поражаются преимущественно мелкие суставы кистей, лучезапястные, голеностопные. У ряда больных может развиться деформация мелких суставов, сопровождаемая мышечной атрофией. Суставному синдрому обычно сопутствуют упорная миалгия, миозит.
Поражение сердечно-сосудистой системы весьма характерно для СКВ (около 50% больных). При люпус-кардите поражаются все оболочки сердца (редко одновременно); обычно регистрируется воспаление отдельных оболочек или их последовательное вовлечение в процесс. Перикардит – наиболее частый признак СКВ. Массивный выпот при этом наблюдается редко. Атипичный бородавчатый эндокардит Либмана-Сакса, считавшийся ранее только патологоанатомической находкой, сейчас, благодаря эхокардиографическому методу, стал диагностироваться значительно чаще, является характернейшим патоморфологическим признаком СКВ и относится к категории признаков высокой активности болезни. Для детей и подростков в первую очередь характерно поражение миокарда (практически в 100%), миоперикардит отмечается в 41% случаев, а панкардит (т.е. одновременное поражение всех трех оболочек сердца) – в 46% случаев.
Поражение легких отмечается довольно часто и проявляется волчаночным пневмонитом и/или интерстициальной пневмонией. Крайне редко развивается тяжелый, угрожающий жизни больного гемаррагический альвеолит. У детей чаще всего встречаются мало- и бессимптомные формы течения волчаночного пневмонита, физикальные признаки поражения легких могут отсутствовать или быть весьма скудными.
Поражения ЦНС и периферической нервной системы в виде менингоэнцефаломиелита и альтеративно-продуктивного радикулита, неврита, плексита обусловлены преимущественно васкулитом сосудов мозга. Для СКВ характерны рассеянные очажки микронекрозов с локализацией в подкорковых ядрах. Клинически проявляется астено-вегетативным синдромом, полиневритами, лабильностью эмоциональной сферы, иногда бредовыми состояниями, слуховыми или зрительными галлюцинациями, эпилептиформными припадками и др.
Поражение почек (волчаночный нефрит, люпус-нефрит) – наблюдается в 70% случаев. Клинически встречаются различные варианты поражения почек – изолированный мочевой синдром, нефритический и нефротический; у больных, леченных кортикостероидами и цитостатиками – пиелонефритический. Поражение почек при СКВ может отмечаться как в дебюте заболевания, так и присоединяться позже по мере прогрессирования заболевания. Наиболее часто волчаночный нефрит у детей бывает представлен нефротической формой, самой тяжелой по течению. Он проявляется отеками, вплоть до развития анасарки, появление в моче большого количество белка, эритроцитов, цилиндров. У детей развивается артериальная гипертензия, в биохимическом анализе крови повышается уровень мочевины, креатинина, снижается уровень общего белка.
Поражение селезенки и лимфатических узлов – отмечается генерализованная лимфаденопатия, увеличение селезенки и печени.
Осложнения. Наиболее опасные из них связаны с поражением почек – развитием их недостаточности на почве люпус-нефрита. Осложнениями стероидной и цитостатической терапии являются гнойные инфекции, “стероидный” туберкулез, гормональные нарушения. У некоторых больных с СКВ встречается так называемый антифосфолипидный синдром (АФС) – повышенная склонность к тромбообразованию. При этом синдроме очень часто отмечается поражение кожи и подкожно-жировой клетчатки с развитием некрозов и гангрены, а также внутренних внутренних органов – головного мозга, легких, почек и т.д.
Как диагностируют СКВ?
Какого-либо специфичного анализа, который позволил бы установить диагноз СКВ, не существует. При постановке диагноза врачи основываются на совокупности клинических проявлений заболевания и данных лабораторно-инструментального обследования больного. Особенно важным для постановки диагноза является иммунологическое обследование, позволяющее выявить ряд характерных для волчанки признаков.
В общем анализе крови у больных СКВ чаще всего отмечается снижение уровня лейкоцитов (лейкопения), тромбоцитов (тромбоцитопения), анемия. Очень важным для постановки диагноза СКВ является определение антикулеарного фактора (АНФ), антител к двуспиральной ДНК, антител к кардиолипинам, волчаночного антикоагулянта. Обнаружение антинуклеарного фактора у больного с характерной клинической картиной СКВ позволяет правильно поставить диагноз практически в 100% случаев. Также необходим контроль за общим анализом мочи, биохимическим анализом крови, коагулограммой, проведение ультразвукового исследования сердца, органов брюшной полости и почек, электрокардиографии, при наличии показаний – рентгенография органов грудной клетки, магнитно-резонансное исследование головного и спинного мозга, электромиография.
Какие существуют методы лечения и профилактики СКВ?
СКВ - очень серьезное заболевание, которое без лечения приводит к тяжелым последствиям вплоть до летального исхода. Лечение больных должно проводиться в специализированном отделении под наблюдением врача-ревматолога, имеющего опыт лечения СКВ. При тяжелом течении заболевания лечение должно осуществляться в отделении реанимации и интенсивной терапии.
Для лечения СКВ используются различные препараты, но основными из них являются глюкокортикоиды. Наиболее часто для лечения СКВ применяются преднизолон и метилпреднизолон. Преднизолон - это препарат, близкий по структуре к гормонам, вырабатывающимся в человеческом организме. Он назначается больным на длительный срок и помогает справиться с агрессией иммунной системы при волчанке. Метилпреднизолон является препаратом, аналогичным преднизолону, но его действие несколько мягче, он в меньшей степени вызывает развитие побочных эффектов, свойственных этой группе лекарственных средств. Одна таблетка преднизолона (5 мг) соответствует одной таблетке метилпреднизолона (4 мг), эти лекарства могут взаимозаменяться. Однако вопрос о смене препарата должен решать лечащий врач. Также нельзя самостоятельно снижать суточную дозу или отменять глюкокортикоиды, так как в этом случае возникает опасность обострения заболевания или развития надпочечниковой недостаточности, которая может привести к гибели пациента.
Помимо преднизолона, в лечении волчанки применяют и другие лекарственные средства.
Циклофосфан. Этот препарат, также как и преднизолон, подавляет патологические иммунные реакции у больных СКВ. Чаще всего его назначают при поражении почек, нервной системы. Чтобы избежать развития различных неблагоприятных побочных эффектов, его применяют в виде так называемой пульс-терапии, когда лекарство вводится
внутривенно в большой дозе, через определенные интервалы времени. Сначала пульс-терапию проводят ежемесячно. В дальнейшем интервалы между введениями постепенно увеличивают до 2-3 месяцев, а затем препарат отменяют совсем.
Обычно введение циклофосфана не сопровождается побочными реакциями. Иногда после введения препарата дети жалуются на тошноту, расстройство стула, головокружение, которые обычно проходят самостоятельно. Для того чтобы вовремя выявить и предупредить нежелательное воздействие циклофосфана на кроветворную систему, через 7-10 дней после проведения пульс-терапии необходимо сдать анализ крови (в первую очередь врачи обращают внимание на количество тромбоцитов и лейкоцитов в крови).
Мофетила микофенолат. В последние годы для лечения больных СКВ используется препарат Селлсепт (Мофетила микофенолат). Этот препарат также относится к иммуносупрессивным средствам, он применяется при лечении волчаночного нефрита, цитопений. В некоторых случаях для лечения СКВ используются азатиоприн, циклоспорин А, метотрексат, делагил. Выбор иммунодепрессанта зависит от формы заболевания, тяжести состояния больного и решается лечащим врачом в ревматологическом отделении.
При высокой активности заболевании, развитии угрожающего жизни состояния, больным СКВ проводят плазмаферез. Это серьезная процедура, которая осуществляется в условиях отделения реанимации и интенсивной терапии. Обычно ее проводят при тяжелом течении СКВ с поражением почек, плохой эффективности стандартных схем лечения болезни и в некоторых других случаях. Во время процедуры плазмафереза через внутривенный катетер у пациента забирается часть крови, которая затем разделяется на плазму и клеточные элементы. Плазма больного удаляется, и заменяется таким же количеством донорской плазмы. На втором этапе в кровеносную систему больного возвращаются клеточные элементы и донорская плазма. Обычно делают несколько процедур плазмафереза подряд (3-5). После сеансов плазмафереза проводят пульс-терапию циклофосфаном или метилпреднизолоном. Плазмаферез позволяет быстро удалить из кровеносного русла активные иммуноагрессивные компоненты, повреждающие ткани и органы, а пульсовое введение циклофосфана и метилпреднизолона - предотвратить их образование в течение достаточно длительного периода.
При повреждении почек и антифосфолипидном синдроме обязательно назначается гепарин. Гепарин улучшает кровоснабжение почек, уменьшает воспаление, препятствует тромбообразованию. Гепарин вводится подкожно в область живота 3-4 раза в день, обычно в течение 3-5 недель. В последние годы наряду с гепарином используют синтетические низкомолекулярные гепарины (фраксипарин, фрагмин и т.д.), они вводятся подкожно один раз в сутки. Затем препарат постепенно отменяют, заменяя на другие лекарства с аналогичным действием, которые пациент может принимать дома в виде таблеток (варфарин, тромбо-АСС).
Лечение с использованием высоких доз глюкокортикоидов и иммунодепрессантов, снижает общую сопротивляемость организма и может вызывать развитие различных инфекционных осложнений (гнойничконовое поражение кожи, пневмонии, инфекции мочевыводящих путей). В этом случае ребенку необходимо назначение антибактериальной терапии в сочетании с внутривенным иммуноглобулином.
Помимо влияния на инфекционный процесс, внутривенный иммуноглобулин оказывает положительное воздействие на течение волчанки и активность антифосфолипидного синдрома.
Помимо глюкокортикоидов, иммунодепрессантов, внутривенного иммуноглобулина, больные СКВ нуждаются в назначении препаратов, улучшающих кровообращение и микроциркуляцию (дипиридамол, пентоксифиллин), антигипертензивные препараты (нифедипин, каптоприл, амлодипин). Всем пациентам, получающим глюкокортикоиды необходимо назначение препаратов кальция в сочетании с препаратами, влияющими на костеобразование и предотвращающими развитие остеопороза (кальцитонин лосося, алендроновая кислота). Также им необходимо назначение препаратов, защищающих слизистую оболочку желудка и двенадцатиперстной кишки от негативного влияния глюкокортикоидов (омепразол, эзомепразол, рабепразол, висмута трикалия дицитрат, сукральфат).
Таким образом, лечение лечение СКВ должно быть комплексным и осуществляться под наблюдением опытного врача-ревматолога и в тесном контакте с педиатром по месту жительства. Больные СКВ должны избегать пребывания на солнце, большинству детей необходимо обучение на дому с предоставлением дополнительного выходного дня. Им также противопоказано проведение профилактических прививок и назначение препаратов, влияющих на иммунитет (препаратов интерферона, других иммуномодуляторов). В семье где живет ребенок, больной СКВ необходимо создать спокойную гармоничную обстановку, оберегать ребенка от стрессов и психических травм.
Специфической профилактики СКВ не существует.
Читайте также:


