Антибиотики при инфекциях головного мозга
Ученые из Санкт-Петербурга исследовали воздействие широко применяемых в больницах цефалоспориновых антибиотиков на деятельность мозга и опровергли предположения о причинах возникновения побочных эффектов у пациентов, например, эпилептических припадков. Исследования проводились сотрудниками лаборатории молекулярных механизмов нейронных взаимодействий Института эволюционной физиологии и биохимии имени И.М. Сеченова РАН. Они были поддержаны грантом Российского научного фонда (РНФ) в рамках Президентской программы исследовательских проектов. Результаты работы опубликованы в журнале Biochemical and Biophysical Research Communications, кратко о них рассказывается в пресс-релизе РНФ.
Судороги после терапии антибиотиками ― достаточно распространенное явление (около половины от всех возможных побочных эффектов цефалоспоринов). На данный момент не существует возможности эффективно прогнозировать их возникновение, а арсенал методов борьбы с ними ограничен. Даже однократно перенесенное эпилептическое состояние может приводить к очень серьезным долговременным последствиям, вплоть до развития регулярных неспровоцированных спонтанных приступов ― эпилепсии как таковой. Среди антибактериальных препаратов одно из ведущих положений занимают антибиотики цефалоспоринового ряда. Они воздействуют на широкий спектр бактерий и легко проникают в ткани, поэтому в больницах довольно часто прибегают к терапии этими антибиотиками, однако, иногда могут вызывать эпилептические судороги у пациентов.
Нейроны головного мозга непрерывно получают различные входные сигналы, которые в первом приближении можно разделить на два основных типа: возбуждающие и тормозные. Преобладание возбуждающих сигналов может привести к тому, что нейрон начнет генерировать разряды (так называемые потенциалы действия) и сможет передать свой сигнал (возбуждающий или тормозной) другим нейронам. Тормозные входные сигналы имеют обратный эффект: они снижают вероятность того, что нейрон начнет передавать свои сигналы другим нейронам.
При эпилептическом приступе, как правило, нейроны головного мозга получают избыточное количество возбуждающих сигналов, но мало тормозных, то есть баланс возбуждения-торможения смещен в сторону возбуждения. Обеспечивает передачу тормозного сигнала в головном мозге гамма-аминомасляная кислота (ГАМК), которая при действии на нейрон связывается с его ГАМКа-рецепторами. Активация этих рецепторов приводит к торможению активности нейрона. Некоторые химические вещества способны связываться с ГАМКа-рецепторами нейронов и так или иначе мешать их нормальной работе (блокировать их). Они либо не дают ГАМК связываться с рецептором, либо препятствуют возникновению тормозного входного сигнала после связывания рецептора с ГАМК. Попадание таких веществ в нервную систему может спровоцировать эпилептические судороги. Подобным свойством обладают некоторые лекарственные препараты, например, цефалоспориновые антибиотики. Предполагалось, что именно по этой причине применение цефалоспоринов довольно часто провоцирует судороги у пациентов, которым назначаются эти препараты.
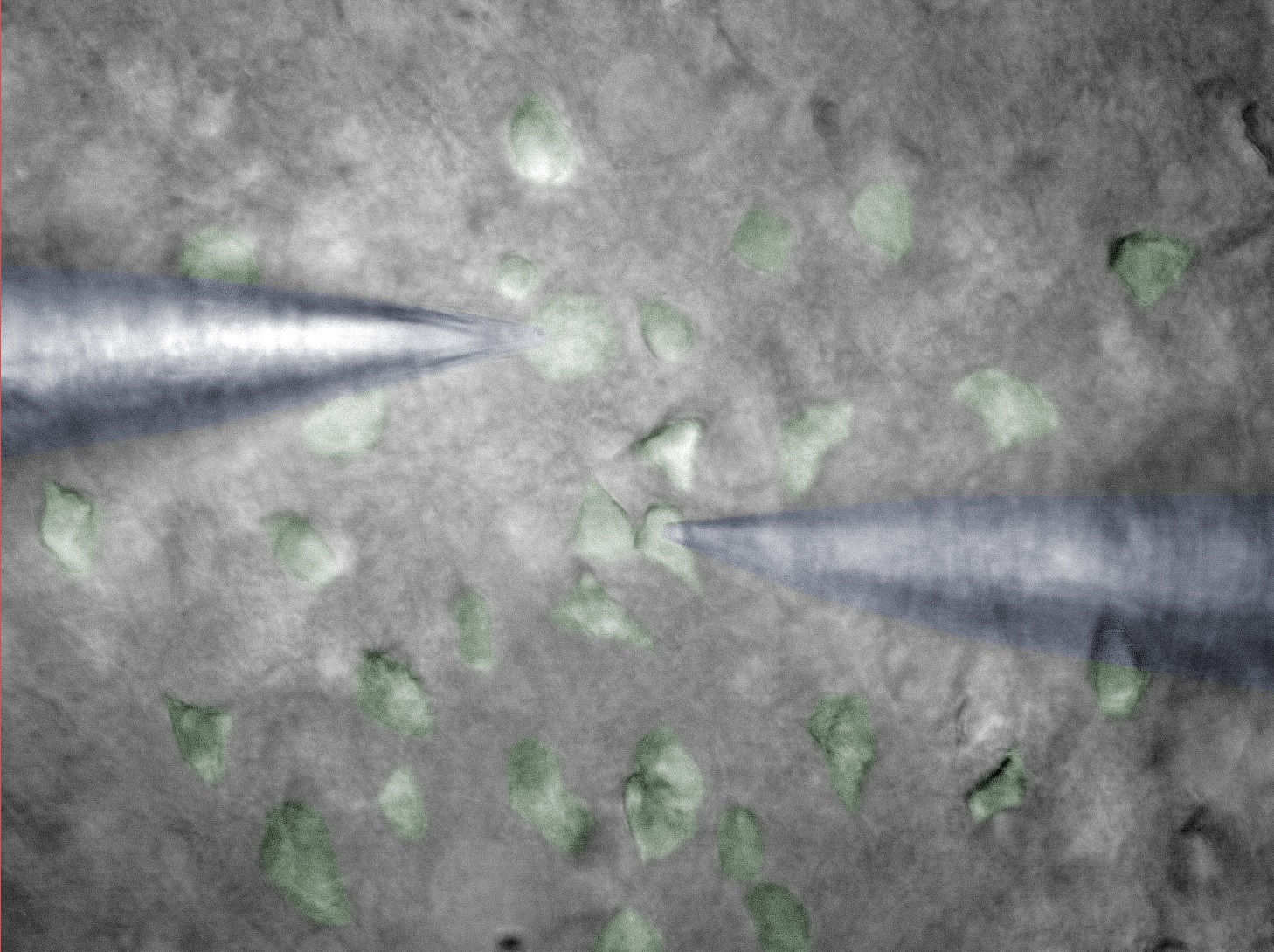
Для проведения экспериментов изготавливались тонкие срезы головного мозга крыс, содержащие энторинальную кору и гиппокамп. В срез устанавливались тонкие электроды, позволяющие провоцировать ответ нейронов (стимулирующий
электрод) и регистрировать этот ответ (регистрирующий электрод). Источник: Дмитрий Амахин
Оказалось, чтобы существенно повлиять на тормозные входные сигналы, получаемые нейронами энторинальной коры, нужны очень высокие концентрации цефалоспоринов. Ощутимое влияние на тормозной сигнал цефалоспорины оказывали в концентрациях почти в 100 раз выше, чем реально достижимые в спинномозговой жидкости пациентов или подопытных животных. И даже в таких больших концентрациях выбранные цефалоспориновые антибиотики провоцировали очень слабую эпилептоподобную активность в срезах мозга. Эти результаты указывают на то, что, по всей видимости, в условиях in vivo (в живом организме) существуют какие-то еще неизвестные механизмы, которые запускаются цефалоспориновыми антибиотиками и приводят к эпилептическим судорогам, а блокирование ГАМКа-рецепторов может быть ни при чем. Также ученым удалось показать, что цефепим и цефтриаксон по-разному блокируют ГАМКа-рецепторы. Цефепим мешает ГАМК связываться с рецептором, тогда как цефтриаксон приводит к снижению эффекта от связывания.
Известно, что вероятность возникновения судорог после приема цефалоспоринов у пациентов с почечной недостаточностью существенно выше. Очень часто почечная недостаточность может сопровождаться повышенной концентрацией ионов калия и сниженной концентрацией ионов магния в различных жидкостях организма. Ученые выяснили, что при определенных нарушениях ионного баланса цефалоспорины гораздо эффективнее приводят к возникновению эпилептоподобной активности в срезе мозга.
В дальнейшем ученые планируют описать закономерности развития этих эпилептоподобных состояний и то, как изменяется процесс передачи сигналов между нейронами во время приступов.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
В настоящей работе представлены антимикробные препараты, которые могут быть применены для этиотропной терапии бактериальных менингитов и инфекций ЦНС.
В настоящей работе представлены антимикробные препараты, которые могут быть применены для этиотропной терапии бактериальных менингитов и инфекций ЦНС.
This paper outlines antimicrobial agents which can be used for the etiotropic therapy of bacterial meningitis and CNS infections.
Е.Н. Падейская - д.м.н., профессор, г. Москва
Ye.N. Padeiskaya - prof., MD, Moscow
Гнойно-воспалительные процессы в оболочках и ткани мозга относятся к наиболее тяжелым формам инфекционной патологии. В схемах лечения бактериальных инфекций центральной нервной системы (ЦНС) основное место занимают препараты, высокоактивные в отношении возбудителей заболевания. Важное значение при этой патологии имеют также средства патогенетической и симптоматической терапии, без применения которых практически не может быть обеспечен полный успех лечения. Объем публикации, к сожалению, не позволяет рассмотреть схемы и особенности терапии (в том числе комбинированной) менингитов в зависимости от возбудителя инфекции (включая вопросы лекарственной резистентности), возраста больного, особенностей течения заболевания и ряда других факторов.
К концу ХХ столетия разработано большое число высокоэффективных антибактериальных средств, но далеко не все могут применяться для лечения инфекций ЦНС. Основным препятствием является плохое проникновение препарата через гемато-энцефалический барьер (ГЭБ) при воспалительных процессах в оболочках мозга, а также побочные реакции и узкая терапевтическая широта, исключающая повышение дозировки.
Таблица 1. Возбудители гнойных менингитов и гнойно-воспалительных процессов ЦНС бактериальнй этиологии
Haemophilus influenzae*
Streptococcus pneumoniae*
Streptococcus gr. "B"
Streptococcus viridans
Staphylococcus aureus
Enterococcus
Escherichia coli
Salmonella spp., в том числе
S.typhi, S.enteritidis
Klebsiella pneumoniae
Serratia marcescens
Proteus spp.
Pseudomonas aeruginosa
Citrobacter diversus
Listeria monocytogenes
Bacteroides spp.
Peptostreptococcus
Fusobacterium meningosepticum(возможны и другие представители анаэробных бактерий)
При инфекции ЦНС лечение должно начинаться как можно раньше, и на первых этапах, до идентификации возбудителя, речь идет всегда об эмпирической терапии. При установленном микробиологическом диагнозе (что не всегда просто в случае успешной ранней эмпирической терапии) этиотропное лечение должно проводиться в соответствии с данными по чувствительности возбудителя. Необходимо учитывать возможность смешанной инфекции, в том числе аэробно-анаэробной, в частности при гнойных процессах в ткани мозга.
Таблица 2. Химиотерапевтические препараты, которые могут применяться для лечения бактериальных менингитов и бактериальных инфекций ЦНС
Оптимальный препарат для лечения инфекций ЦНС должен удовлетворять следующим требованиям:
1. Это должно быть высокоактивное in vitro соединение с активностью в отношении большинства возбудителей бактериальных менингитов.
2. Предпочтительными являются препараты с низкой молекулярной массой, липофильными свойствами и низкой степенью связывания с белками плазмы.
3. Препарат должен хорошо проникать через ГЭБ при воспалительных процессах в оболочках мозга, обеспечивая бактерицидный эффект в очаге инфекции. Последнее следует специально подчеркнуть, так как даже препарат с бактерицидным типом действия не всегда может обеспечить этот эффект в связи с недостаточной концентрацией в ликворе и ткани мозга. Бактерицидные концентрации особенно важны, так как ЦНС является органом, практически не обеспеченным иммунной защитой, в том числе факторами клеточного иммунитета. Степень проникновения через ГЭБ зависит от особенностей патогенеза заболевания (связано с возбудителем инфекции), стадии болезни, дозы препарата. Концентрационные показатели определяются сроками исследования по отношению к введению препарата, началу курсового лечения и началу заболевания.
4. Преимущество имеют препараты с продленным действием,особенно те, которые медленно (более медленно, чем из крови) выводятся из спинномозговой жидкости (СМЖ).
5. Препарат должен характеризоваться низкой токсичностью, хорошей переносимостью при системном применении, большой терапевтической широтой и не вызывать нежелательных реакций со стороны ЦНС. Не менее важно, чтобы препарат хорошо переносился при введении в спинномозговой канал, интратекально или при орошении раны в случаях мозговой травмы или оперативного вмешательства. Необходимы лекарственные формы для парентерального введения. С другой стороны, несомненную ценность представляют препараты с высокой степенью биодоступности при пероральном введении (более 80%) и одновременно с высокой степенью проникновения в ликвор при менингитах. Такие препараты могут быть применены для лечения менингита перорально обычно после стартовой парентеральной терапии (а иногда - только перорально) у больных со среднетяжелым течением заболевания, сохраненным сознанием, ненарушенным глотанием.
Гнойные менингиты относятся к тяжелой патологии, которая требует ранней, срочной терапии. Антимикробные препараты должны назначаться в максимальных дозах, обеспечивающих бактерицидную концентрацию в ликворе. Нельзя снижать дозы по мере клинического улучшения и нормализации ликвора, так как процесс выздоровления ведет одновременно и к снижению проницаемости ГЭБ для лекарственного препарата.
Таблица 3. Препараты группы цефалоспоринов, применяющиеся для лечения бактериальных менингитов
Дозы* разовые, взрослым внутривенно или внутримышечно, г
Число введений в сутки
Приникновение в СМЖ: % ликвор/сыворотка
Таблица 4. Основные характеристики препарата цефтриаксон
| Показатель | Цефтриаксон (основные характеристики) |
| Антимикробный спектр | Высокочувствительны большинство аэробных грамположительных и грамотрицательных бактерий, некоторые анаэробы; штаммы P.aeruginosa умеренно-чувствительны или устойчивы; устойчивы энтерококки, листерии |
| Т1/2 , ч | Взрослые - 8 ч; дети первых дней жизни и лица старше 75 лет - до 16 ч |
| Сmax мг/л в крови | После введения: 2 г внутривенно - до 270 мг/л 1 г внутривенно - до 150 мг/л |
| Концентрация в СМЖ | После введения внутривенно 50 - 100 мг/кг - более 1,4 мг/л; средняя при курсовом лечении - 3,5 мг/л (МПК* для чувствительных штаммов: 0,003 - 0,025 мг/л; для штаммов стафилококков - возможно 2 - 4 мг/л ) |
| Дозы и частота введения в сутки при менингитах | Взрослые и дети старше 12 лет: 2 - 4 г 1 раз/сутки Дети грудные и младшего возраста - 100 мг /кг (не более 4 г) 1 раз в сутки; в некоторых наблюдениях - суточная доза в 2 введения, интервал 12 ч |
| * МПК - минимальная подавляющая концентрация. | |
В табл. 1 и 2 представлены микроорганизмы - возбудители бактериальных менингитов и основные группы химиотерапевтических препаратов, которые могут применяться для лечения бактериальных инфекций ЦНС.
Не применяются для лечения бактериальных менингитов и инфекций ЦНС препараты группы макролидов, линкозаминов, производные нитрофурана и хинолина, нефторированные хинолоны, тетрациклины, так как они плохо проникают через ГЭБ при воспалении мозговых оболочек и не обеспечивают в ликворе и ткани мозга необходимых терапевтических концентраций.
Таблица 5. Эффективность фторхинолонов при бактериальных менингитах при отсутствии лечебного эффекта от предшествующей терапии*
Препараты, дозы, внутривенно
Эффективность (выздоровление, улучшение )
Среди этиотропных препаратов, которые применяют для лечения бактериальных инфекций ЦНС, пока еще нет препарата, удовлетворяющего всем вышеперечисленным ранее требованиям. Тем не менее высокая бактерицидная активность, широкий антибактериальный спектр, концентрации в ликворе, обеспечивающие бактерицидное действие в отношении подавляющего большинства возбудителей бактериальных менингитов, в сочетании с низкой токсичностью и хорошей переносимостью позволяют рассматривать цефалоспорины III и IV поколений ( табл. 3 и 4 ) как важнейшие препараты для лечения бактериальных менингитов, в том числе и для эмпирической терапии, хотя они не решают всех вопросов этиотропного лечения [1 - 7].
Эти препараты различаются по фармакокинетическим характеристикам (определяющим частоту введения в сутки) и особенностям антимикробного спектра. Соответственно различен и выбор препарата для эмпирической терапии и при установленном микробиологическом диагнозе. Особый интерес представляет цефтриаксон. Его высокая активность и достаточно широкий спектр сочетаются с продленным действием; препарат рекомендуется к применению 1 раз в сутки (см. табл. 4) . Показана высокая эффективность цефтриаксона при менингитах, вызванных N.meningitidis, H.influenzae, S.pneumoniae, Streptococcus gr.B, S.viridans, S.aureus и S.epidermidis (за исключением штаммов, устойчивых к метициллину), K.pneumoniae, E.coli [3, 6, 8]. Цефтриаксон устойчив к действию b -лактамаз гемофильной палочки и эффективен, когда выделяются штаммы, устойчивые к пенициллинам по этому механизму [1].
Таблица 6. Проникновение офлоксацина (ОФЛ) в СМЖ при гнойном менингите*
Время забора проб после третьего введения в крови
Длительность лечения (ОФЛ 200 мг внутривенно каждые 12 ч)
Основные факты
Возбудителями менингита являются различные микроорганизмы, включая бактерии, грибок и вирусы. Менингококковый менингит — это бактериальная форма менингита, серьезная инфекция, поражающая оболочки мозга. Он может приводить к тяжелому поражению мозга, а при отсутствии лечения в 50% случаев заканчивается смертельным исходом.
Бактерия Neisseria meningitidis, вызывающая менингококковый менингит, особенно опасна из-за способности провоцировать масштабные эпидемии. Выявлено 12 серогрупп N. meningitidis, 6 из которых (A, B, C, W, X и Y) могут вызывать эпидемии.
Масштабы поражения менингококковым менингитом варьируются от спорадических случаев и небольших кластеров до масштабных эпидемий во всем мире при сезонных колебаниях. Заболеть может любой человек любого возраста, но в основном эта болезнь поражает младенцев, детей дошкольного возраста и молодых людей.
Передача инфекции
Бактерия Neisseria meningitidis инфицирует только людей, животного резервуара не существует. Бактерия передается от человека человеку через капли выделений из дыхательных путей или горла носителя. Курение, а также тесный и продолжительный контакт, такой как поцелуй, чихание или кашель в сторону другого человека или проживание в непосредственной близости с инфицированным человеком-носителем, способствует распространению болезни. Массовые мероприятия (свежий пример — паломничество мусульман (хадж) и народные гуляния) облегчают передачу бактерии N. meningitidis.
Бактерии могут переноситься в горле, и иногда, подавляя защитные силы организма, инфекция попадает через кровоток в мозг. Считается, что в любой момент времени 1%–10% населения являются носителями N.meningitidis в горле. Однако в эпидемических ситуациях число носителей может быть выше (от 10% до 25%).
Симптомы
Обычно инкубационный период длится четыре дня, но может варьироваться от 2 до 10 дней. Самыми распространенными симптомами являются ригидность затылочных мышц, высокая температура, чувствительность к свету, спутанность сознания, головная боль и рвота. У младенцев также часто наблюдается выбухание родничка и вялость. Менее распространенной, но еще более тяжелой (часто смертельной) формой менингококковой инфекции является менингококковый сепсис, для которого характерны геморрагическая сыпь и быстро развивающийся циркуляторный коллапс. Даже в случае диагностирования и надлежащего лечения на ранних стадиях болезни 8%–15% пациентов умирают, как правило, через 24–48 часов после появления симптомов. При отсутствии лечения менингококковый менингит в 50% случаев заканчивается смертельным исходом. У 10%–20% выживших людей бактериальный менингит может приводить к повреждению мозга, потере слуха или инвалидности.
Диагностика
Первоначальный диагноз менингококкового менингита может быть поставлен при клиническом осмотре с последующим проведением спинномозговой пункции для выявления гнойной спинномозговой жидкости. Иногда бактерии можно увидеть при исследовании спинномозговой жидкости под микроскопом. Диагноз поддерживается или подтверждается путем выращивания бактерий из образцов спинномозговой жидкости или крови на основе реакции агглютинации или полимеразной цепной реакции (ПЦР). Для определения мер по борьбе с инфекцией важно идентифицировать серогруппы и провести тестирование на чувствительность к антибиотикам.
Эпидемиологический надзор
Эпидемиологический надзор — от выявления случаев заболевания до их расследования и лабораторного подтверждения — крайне важен для борьбы против менингококкового менингита.
Основные цели эпиднадзора:
- обнаружение и подтверждение вспышек заболевания;
- обнаружение и подтверждение вспышек заболевания;
- оценка бремени болезни;
- мониторинг профилей устойчивости к антибиотикам;
- мониторинг циркуляции, распространения и эволюции отдельных менингококковых штаммов (клонов);
- оценка эффективности стратегий по контролю над менингитом, в частности, программ профилактического вакцинирования.
Лечение
Менингококковая инфекция потенциально смертельна и всегда должна рассматриваться как медицинская чрезвычайная ситуация. Пациента необходимо госпитализировать в больницу или центр здравоохранения, но изолировать его необязательно. Соответствующее лечение антибиотиками необходимо начинать как можно раньше, в идеале сразу же после проведения спинномозговой пункции в случае, если такая пункция может быть выполнена незамедлительно. В случае лечения, начатого до проведения спинномозговой жидкости, выращивание бактерий из спинномозговой жидкости и подтверждение диагноза может быть затруднено. Однако необходимость подтверждения диагноза не должна являться причиной промедления с лечением.
Инфекцию можно лечить с помощью целого ряда антибиотиков, включая пенициллин, ампициллин и цефтриаксон. В условиях эпидемий в районах Африки со слабой инфраструктурой здравоохранения и ограниченными ресурсами предпочтительным препаратом является цефтриаксон.
Профилактика
Уже более 40 лет для борьбы с менингококковой инфекцией используются лицензированные вакцины. В течение этого времени произошло три серьезных улучшения с точки зрения охвата штаммов и доступности вакцин, однако универсальная вакцина против менингококкового менингита до сих пор не разработана. Вакцины эффективны против конкретных серогрупп, а срок действия их защиты различен.
Существует три типа вакцин:
Полисахаридные вакцины используются в основном в Африке в ответ на вспышки заболевания:
Они бывают двухвалентными (группы А и С), трехвалентными (группы А, С и W) или четырехвалентными (группы А, С, Y и W).
Полисахаридные вакцины не действуют на детей в возрасте до 2 лет.
Срок действия вакцины — три года, но вакцинация не приводит к формированию коллективного иммунитета.
Конъюгированные вакцины используются для профилактики (включены в календарь профилактических прививок и в кампании профилактической иммунизации) и для реагирования на вспышки заболевания:
Такие вакцины позволяют сформировать длительный иммунитет (свыше 5 лет), предотвращают перенос инфекции и приводят к формированию коллективного иммунитета.
Кроме того, они могут быть использованы для вакцинации детей старше одного года.
Доступны следующие вакцины:
моновалентная (группа С),
моновалентная (группа А),
четырехвалентная (группы A, C, Y, W).
Вакцина на основе белков против N. meningitidis B. Данная вакцина была включена в календарь профилактических прививок (в одной стране по состоянию на 2017 г.) и также используется для реагирования на вспышки заболевания.
Незамедлительное профилактическое назначение антибиотиков лицам, находившимся в тесном контакте с больным, снижает риск передачи инфекции.
Предпочтительным антибиотиком является ципрофлоксацин, а альтернативным — цефтриаксон.
Меры реагирования в области глобального общественного здравоохранения: успешное введение конъюгированной вакцины против менингококковой инфекции серогруппы А в Африке
ВОЗ содействует реализации стратегии, предусматривающей обеспечение готовности к эпидемиям, проведение профилактики и принятие ответных мер. В основе обеспечения готовности лежит эпиднадзор — от выявления случаев заболевания до их расследования и лабораторного подтверждения. Профилактика включает иммунизацию всех людей из возрастных групп, подверженных наибольшему риску инфицирования, конъюгированной вакциной против соответствующей серогруппы. Ответные меры включают безотлагательное и надлежащее ведение случаев заболевания, а также последующую массовую вакцинацию еще неохваченного населения.
Эпидемии менингита в африканском менингитном поясе ложатся тяжелым бременем на системы общественного здравоохранения. В декабре 2010 г. в Африке была проведена массовая кампания вакцинации новой конъюгированной вакциной против менингококка группы А для целевой группы в возрасте от одного года до 29 лет. По состоянию на ноябрь 2017 г. в 21 стране из менингитного пояса было вакцинировано свыше 280 миллионов человек.
Эта вакцина намного безопаснее и дешевле по сравнению с остальными вакцинами (примерно 0,60 долл. США за одну дозу; цена других менингококковых вакцин колеблется от 2,50 до 117,00 долл. США за одну дозу(1)). Кроме того, ее термостабильность позволяет использовать ее в условиях систем с регулируемой температурой (СТС). Вакцина продемонстрирована высокую эффективность с точки зрения сокращения заболеваемости и эпидемиологической опасности: на 58% сократилась заболеваемость менингитом и на 60% — риск возникновения эпидемий. В настоящее время данная вакцина используется при плановой иммунизации детей. Ожидается, что при сохранении широкого охвата вакцинации, эпидемии менингококковой инфекции А в этом регионе Африки будут ликвидированы. Однако другие менингококковые серогруппы, такие как W, X и C, продолжают вызывать эпидемии и около 30 000 случаев заболеваний ежегодно в менингитном поясе. ВОЗ намерена ликвидировать менингококковые заболевания как проблему общественного здравоохранения.
(1) Ориентировочные цены в государственном и частном секторах, согласно данным ЮНИСЕФ, ПАОЗ и Центров США по контролю и профилактике заболеваний.
Лечение такого опасного заболевания, как менингит должно осуществляться сильнодействующими препаратами, поэтому антибиотики при менингите у взрослых являются важной составляющей общего плана лечения.
В общих чертах о болезни
Менингит – это острое воспалительное заболевание (чаще инфекционного характера), которое поражает головной мозг человека, вызывая резкое повышение температуры, сильные головные боли, повышенную свето— и шумочувствительность, а также другие менингеальные симптомы.
- гнойный;
- серозный;
- реактивный;
- бактериальный;
- туберкулезный.
Особенности лечения
Основу лечения составляют антибиотики при менингите, однако, существует особенность диагностики, которая заключается в том, что определить тип болезни удается не всегда, и, как правило, доктор назначает больному препараты широко спектра действия.
Назначенные лекарства, как правило, вводятся пациенту внутривенно, однако, в особо тяжелых случаях антибиотик при менингите может направляться прямо в спинной мозг.
Препараты широкого спектра
В зависимости от внешних проявлений и результатов анализов врач может назначить:
- Антибиотики с хорошими проникающими свойствами.
- Антибиотики со средними проникающими свойствами.
- Антибиотики с низкими проникающими свойствами.
Низкая проникающая способность не означает плохую действенность, лекарство от менингита должно иметь не только хорошие проникающие свойства, но и уметь бороться с вирусами. Поэтому в зависимости от тяжести болезни доктор может комбинировать введение препаратов, ровно как и назначать введение лекарства непосредственно в спинной мозг.
К препаратам 1 группы относятся:
- Амоксицилиллин (пенициллиновая группа);
- Цефуроксим (цефалоспориновая группа 2 поколения);
- Азтреонам (монобактамы).
Препараты 2 группы:
Препараты 3 группы:
Препараты не антибиотики
Лечение антибиотиками не является единственным, так как данная болезнь довольно коварная и требует комплексного подхода в лечении.
Так, для снятия отека мозга доктора назначают препараты, которые обладают противоотечными свойствами так называемые диуретики, или мочегонные препараты к которым относят:
Кроме того, при менингите у взрослых необходимо проводить терапию, направленную на интоксикацию организма. Достигается это назначением больному 5% раствора глюкозы либо физраствор, который способствует насыщению организма необходимыми веществами и выведению накопившихся токсинов.
Следует помнить, что основа успешного лечения заключается не в таблетках, а комплексном подходе к устранению проблемы и наблюдении за больным докторами. Поэтому ни в коем случае не следует заниматься самолечением, так как это может привести к серьезным последствиям, ну а при особо запущенных случаях даже к смерти больного.
Возможно ли предотвратить болезнь?
Для того чтобы предотвратить появление этого опасного заболевания, сейчас существует прививка от менингита. Однако, таких прививок несколько и направлены они на борьбу с разными видами болезни.
К примеру, вакцинация против кори, краснухи или паротита защищает человека от возникновения менингита, так как данные заболевания провоцируют воспалительные процессы в головном мозге человека, а соответственно и возникновение менингита.
Также существует непосредственно вакцина против менингита или менингококковая вакцина, которая способна защитить организм человека от возникновения гнойного или серозного менингита, но не способна справиться с туберкулезным менингитом.
Помимо прочего, в качестве профилактики болезни можно придерживаться стандартных правил поведения, таких как:
- соблюдение гигиены;
- поддержание иммунитета;
- избегание контактов с инфицированными людьми;
- применение одноразовых масок, во время нахождения в опасном для заражения месте.
Наличие сведений о применяемых во время лечения препаратов не позволит больному эффективно вылечить болезнь самостоятельно, а может лишь усугубить его состояние, поэтому не пытайтесь использовать полученные данные для самолечения.
Читайте также:


