Зовиракс при гепатите с
ЗАМЕТКИ ИЗ ПРАКТИКИ А.С. Логинов, В.Д. Ткачев, С.Д. Шепелева
Центральный научно-исследовательский институт гастроэнтерологии. Москва
Лечение хронического активного гепатита С вирусной этиологии до настоящего времени остается сложной задачей. Одной из причин этого выступает патогенетическая гетерогенность заболевания, связанная, главным образом, с наличием 6 основных генотипов и ряда подтипов вируса С, о чем нами упоминалось в предшествующей публикации [2]. Следует также отметить, что вирус гепатита С (HCV), в отличие от HBV, оказывает прямое цитопатическое действие на клетки-мишени [4]. С 1994 года в России была введена государственная регистрация случаев заражения HCV. За последние годы отмечен рост числа заболеваний хроническим гепатитом С до 7,6 на 100 тысяч населения. Согласно специально проведенным исследованиям Д.К. Львова с соавторами установлено, что в Центральной и северо-западной России преобладает наиболее патогенный генотип вируса С - 1b [10]. Практически, гепатит, вызванный HCV с генотипом 1b, не поддается монотерапии интерфероном [9]. В последние годы появились сообщения о более эффективной терапии больных хроническим гепатитом вирусной этиологии интерфероном в сочетании с ингибиторами обратной транскриптазы (ацикловир - зовиракс, рибавирин - виразол, ламивудин - эпивар, зидовудин - ретровир), а также ингибиторами протеазы (криксиван), расщепляющей вирусный белок [6, 8, 13]. Монотерапия рибавирином и при продолжительном лечении (12 мес.) оказалась малоэффективной [5]. Если оптимальный срок продолжительности лечения гепатита, вызванного HCV, интерфероном составляет 12-18 мес. [11], то, согласно рандомизированному исследованию Chemello L. с соавторами [14], при комбинированном лечении интерфероном и рибавирином продолжительность лечения может быть сокращена до 6 мес. Общепринятыми критериями для прекращения терапии является нормализация уровня аминотрансфераз и контролируемое с помощью ГЩР исчезновение из сыворотки РНК HCV [12]. Приводим наше наблюдение.
Больная С. 28 лет оперирована в 1991 г. по поводу гнойного аднексита (резекция правого яичника), проводились гемотрансфузии. В 1992 г. выполнена резекция 2-х метров тонкой кишки (острая кишечная непроходимость). В 1995 г. перенесла ОВГ А, после реконвалесценции оставалось умеренное повышение содержания билирубина. В апреле 1997 г. обнаружено повышение аминотрансфераз и наличие анти-HCV. При обследовании в гепатологическом центре г. Ростова произведена пункционная биопсия печени: хронический активный гепатит С - вирусной этиологии. Дополнительное обследование с помощью метода ПЦР позволило выявить у больной РНК HCV, генотип 1b. Больная направлена в ЦНИИГ для проведения противовирусной терапии.
Госпитализирована 24.11.97 г. При поступлении жалобы на тупые боли в правом подреберье, общую слабость. Объективно: состояние удовлетворительное. Склеры субиктеричны. Кожные покровы обычной окраски. Система дыхания и кровообращения без отклонений от нормы. Живот умеренно болезненный при пальпации в эпигастрии. Печень выступает из-под края реберной дуги по грудинно-ключичной линии на 3-4 см, несколько уплотнена. Селезенка не пальпируется. Со стороны других органов патологии не выявлено. Проведенное УЗИ органов брюшной полости выявило диффузное изменение паренхимы печени без признаков портальной гипертензии. Проведенная эзофагогастродуо-деноскопия позволила диагностировать умеренно выраженный хронический гастрит. Консультация гинеколога: хронический кольпит. Исследование крови: Нв 140 г/л; эр. 4,6; ЦП 0,92; лейкоциты 5,2; эозинофилы 2; п/я 2; с/я 58; лимфоциты 32; моноциты 6. Тромбоциты 276, СОЭ 6 мм. Протромбин 86%. Сахар 4,0 мг%. Общий билирубин 37 мкмоль/л (прямой 6,0), холестерин 4,4 мг%, щелочная фосфатаза 2,4 (N 2,2), АсАТ 0,42, АлАТ 0,58 (N 0,40), тимоловая проба 3,1, формоловая проба - отр, общий белок 78 г%, альбумины 52, глобулины 48, альфа1 - 5,2, альфа2 - 8,3, (бета - 10,9, гамма - 26,6. Маркеры вирусной инфекции: HBsAg (-), anti-HCV (+). Генотип 1b. lgM - 150 мг%, lgG - 1500 мг%, lgA - 210 мг%. РНК ПЦР HCV (+).
Клинический диагноз: Хронический активный гепатит С - вирусной этиологии, генотип Ib, фаза репликации вируса. Хронический умеренно выраженный гастрит. Хронический кольпит. Частично резецированная тонкая кишка.
Результаты обследования больной в ЦНИИ гастроэнтерологии свидетельствовали о прямых показаниях к проведению более эффективной сочетанной противовирусной терапии интерфероном и рибавирином. Интрон А (интерферон - 2бета) назначался по 3 млн. ЕД 3 раза в неделю. Рибавирин - по 200 мг 3 раза в день, ежедневно. Через 2 месяца после проводимого лечения в отделении патологии печени ЦНИИГ отмечена нормализация аминотрансфераз, методом ПЦР выявлено исчезновение РНК HCV. Рекомендовано продолжить лечение в течение 6 мес. под контролем картины периферической крови и функциональных проб печени.
Повторная госпитализация в ЦНИИГ 14.4.98 г (через 6,5 мес.). На фоне проводимого лечения больная отметила значительное уменьшение общей слабости, ноющие боли в правом подреберье приняли эпизодический характер. Объективно: состояние удовлетворительное. Склеры субиктеричны. Кожные покровы обычной окраски. Система дыхания и кровообращения без отклонений от нормы. Живот мягкий, безболезненный при пальпации во всех отделах. Печень выступает из-под края реберной дуги по грудинно-ключичной линии на 1,5-2 см. Со стороны других органов патологии не выявлено. УЗИ: признаки диффузного поражения печени. Исследование крови: Нв 115 г/л; эр. 4,0; ЦП 0,85; лейкоциты 3,8; эозинофилы 4; п/я 4; с/я 54; лимфоциты 32; моноциты 6. Тромбоциты 120. СОЭ 13 мм. Протромбин 85%. Сахар 4,3. Общий билирубин 24,0 (прямой 4,0 мкмоль/л), холестерин 3,5, щелочная фосфотаза 1,9, АсАТ 33,7, АлАТ 26,0, тимоловая проба 3,4 (N до 5), общий белок 81 г%, альбумины 49,5, глобулины 50,0, (альфа1 - 3,8, альфа2 - 9,2, бета - 11,7, гамма - 25,6. HBsAg (-), anti-HCV (+), РНК ПЦР HCV (-).
В результате сочетанного лечения интроном А и рибавирином в течение 6,5 мес. получена ремиссия, стабильность которой предполагалось оценить через 6 месяцев. Рибавирин отменен. Лечение интроном А рекомендовано продолжить в течение последующих 6 месяцев. Контрольное исследование крови, проведенное 11.11.98 г, т.е. через 11 мес. показало: анти-HCV (+), РНК ПЦР HCV (-). Общий билирубин 41,0 мкмоль/л (прямой 10,0), холестерин 2,6, щелочная фосфатаза 0,96, АсАТ 40,0, АлАТ 37,0, тимоловая проба 5,7, формоловая проба - отр. Общий белок 92,0, альбумины 50,3, глобулины 49,7, (альфа1 - 5,6, альфа2 - 9,3, бета - 13,1, гамма - 21,0.
Приводим результаты морфологического исследования ткани печени до лечения (Рис. 1) и через 6,5 мес. после лечения (Рис. 2).
Рисунок 1
Инфильтрация портального тракта лимфоцитами, проникновение инфильтрата в дольку (до лечения). Окр. гематоксилин-эозин, х 300
Рисунок 2
Незначительно выраженная лимфоидноклеточная инфильтрация портального тракта, пограничная пластинка сохранена (после лечения). Окр. гематоксилин-эозин, х 300
В первой биопсии (1997 г, до лечения) наблюдалось поражение портальных трактов. Наряду с умеренно расширенными, склерозированными и умеренно инфильтрированными портальными трактами встречались значительно расширенные и существенно инфильтрированные. В одном из них инфильтрат имел вид лимфатического фолликула. На серийных срезах можно было проследить как один из умеренно расширенных и значительно инфильтрированных портальных трактов на последующих срезах был значительно расширен, обильно инфильтрирован лимфоидными клетками, имелась выраженная пролиферация дуктул. Пограничная пластинка в некоторых портальных трактах была разрушена проникающим на небольшую глубину в дольку инфильтратом. Несмотря на незначительную инфильтрацию портальных трактов, желчные протоки в них отсутствовали или эпителий их был фрагментарно дистрофически изменен. Внутридольковые лимфо-идно-клеточные инфильтраты были единичны, "растекание" инфильтрата наблюдалось только в одном из них. Ядра многих гепатоцитов содержали крупные вакуоли. Паренхима была представлена в основном, "светлыми" клетками.
ЗАКЛЮЧЕНИЕ: Умеренно выраженный портальный, незначительно выраженный перипортальный и лобулярный гепатит С - вирусной этиологии.
Во второй биопсии, проведенной больной через год, в морфологической картине ткани печени отмечалось меньшее расширение портальных трактов, снижение интенсивности воспалительного инфильтрата, наряду с этим встречались расширенные, склерозированные, но неинфильтрированные портальные тракты. Не наблюдалось и разрушения пограничной пластинки. Желчные протоки не выявлялись только в некоторых портальных трактах. В одном незначительно инфильтрированном портальном тракте наблюдалась пролиферация дуктул. Внутридольковая инфильтрация отсутствовала. Вакуоли в ядрах наблюдались лишь в единичных гепатоцитах.
ЗАКЛЮЧЕНИЕ: Умеренно выраженный портальный гепатит. Сравнение морфологической картины обоих биоптатов позволяет сделать заключение о снижении выраженности портального воспаления, исчезновении перипортальной и внутридольковой инфильтрации, вакуолизации ядер гепатоцитов.
Обнаружение РНК HCV с помощью ПЦР не является однозначным свидетельством экспрессии вирусного генома, поэтому исследованиям, направленным на определение вируса гепатита С в клетках печени человека придается особое значение. Существует мнение, согласно которому, определение вируса в ткани печени должно быть проведено после лечения гепатита, так как критерием эффективности терапии служит отсутствие инфекционного агента в печени [15]. Специально проведенное исследование в НИИ Вирусологии РАМН с помощью моноклональных антител (А.А. Кущ и соавторы) не обнаружило в ткани печени данной больной С-вирусного белка, что позволяет с большей уверенностью допускать возможность полной элиминации вируса С из организма больной и ее выздоровления.
В заключение отметим, что в представленном случае мы располагаем ближайшими результатами сочетанного лечения интроном А и рибавирином хронического активного гепатита С - вирусной этиологии, генотип 1b, свидетельствующими о достижении клинико-лабораторно-морфологической ремиссии.
-->
Несмотря на широкое распространение герпетической инфекции (маркеры вируса простого герпеса 1/2 типа (HSV‑1/2) выявляются у 13-22% жителей Европы и США, в том числе у 25-64% пациентов клиник, занимающихся лечением инфекционных заболеваний, передающихся половым путем), гепатиты этой этиологии относят к редким заболеваниям [1]. Для них характерны крайне тяжелое течение, частое развитие фульминантного гепатита (ФГ) и высокий уровень летальности [2].
Традиционно под ФГ подразумевают развитие печеночной недостаточности (энцефалопатии) у больного острым гепатитом в течение 2-8 нед от появления первых признаков болезни при условии отсутствия у него хронической патологии печени в анамнезе [3]. В общей структуре причин летальных исходов от острой печеночной недостаточности (ОПН) на герпетический гепатит (ГГ) приходится
1% случаев [4]. В 40% случаев причиной фульминантного герпетического гепатита (ФГГ) является HSV-1, в 60% – HSV-2 [5].
Еще одним аспектом, определяющим актуальность гепатитов этой этиологии, является превалирование в 3-4 раза постмортальной диагностики над прижизненной, что связано с отсутствием каких-либо патогномоничных признаков инфекции у подавляющего большинства больных [6]. В одной из серий наблюдений прижизненный диагноз ФГГ был установлен только у 23% пациентов [7]. Ключом к нему могли бы служить типичные высыпания на коже и слизистых оболочках, однако при гепатите они встречаются достаточно редко [8]. В этой связи необходимо вспомнить о том, что своевременно назначенная терапия ацикловиром потенциально могла бы оказать существенное влияние на структуру исходов ГГ, что, в свою очередь, определяет необходимость совершенствования как клинической, так и лабораторной диагностики этого заболевания [8].
HSV-1 и HSV-2 относятся к ДНК-содержащим вирусам и принадлежат к подсемейству α-herpesviridae семейства Herpesviridae. Заражение происходит при тесном контакте c имеющими клинические проявления больными или бессимптомными выделителями вируса через поврежденную кожу или слизистые оболочки ротоглотки, шейки матки и конъюнктивы [9]. После инокуляции вирус размножается в клетках эпидермиса или дермы, после чего нуклеокапсид по чувствительным или автономным нервам попадает в соответствующие ганглии 12. К примеру, HSV-1 чаще персистирует в ганглиях тройничного нерва, хотя может быть обнаружен в верхних и нижних шейных ганглиях [15]. В случае генитальной инфекции HSV-2 чаще выявляется в сакральных ганглиях [16].
Реактивация инфекции с клиническими проявлениями, в том числе и диссеминированными формами, зависит от состояния иммунитета организма-хозяина. У иммунокомпрометированных пациентов диссеминированные и тяжелые формы инфекции встречаются намного чаще. Риску подвержены в первую очередь больные с нарушением Т-клеточного звена иммунитета (врожденные иммунодефициты, ВИЧ-инфекция, ятрогенная иммуносупрессия после трансплантации и пр.) [17]. У иммунокомпетентных пациентов любые события, нарушающие иммунный контроль над инфекцией, ведут к ее реактивации, что чаще всего сопровождается появлением более или менее распространенных высыпаний на слизистых и коже. Считается, что у таких пациентов причинами развития гепатита могут быть: большая инфицирующая доза возбудителя; реактивация латентной инфекции после инфицирования другим штаммом HSV с более высокой вирулентностью; наследственный дефект иммунной системы, не позволяющий развиться адекватному ответу на инфекцию [18].
Манифестация и течение HSV-инфекции зависят от места внедрения возбудителя, возраста, иммунного статуса хозяина и антигенного варианта вируса. Первый эпизод, особенно в случае первичной инфекции, возникает на фоне отсутствия или недостаточного титра антител к вирусу, часто сопровождается системными проявлениями и развитием тяжелого стоматита или фарингита, как правило, более длительным течением и вирусовыделением, возможностью развития осложнений в виде диссеминированной инфекции [19]. Напротив, рецидив чаще ассоциирован с типичными высыпаниями на слизистых оболочках и коже и характеризуется меньшей частотой генерализации процесса [20].
Клинические проявления инфекции, вызванной HSV-1 и HSV-2, схожи, но частота реактивации определяется местом инокуляции вируса и его типом (например, HSV-1 чаще рецидивирует в случае его персистенции в тройничном нерве, а не в сакральных ганглиях) [21].
Впервые ГГ был описан в 1969 г. [22]. Он является следствием гематогенной диссеминации вируса. Проявлениями последней могут быть обширные кожные высыпания в области грудной клетки, конечностей, а также развитие асептического менингита, эзофагита, пневмонита или артрита [23]. Диссеминированная инфекция может сопровождаться тромбоцитопенией и миоглобинурией [24]. Сочетание гепатита с упомянутыми состояниями может быть ключом к постановке диагноза на основе клинической симптоматики [5]. Однако на самом деле предположение о герпетической этиологии гепатита на основании клинических критериев возникает не более чем в 10-30% случаев.
У иммунокомпетентных взрослых ГГ является результатом первичного инфицирования. Случаи поражения печени вследствие реактивации инфекции у этой категории пациентов не описаны [25]. Обычно между моментом инфицирования и появлением высыпаний проходит от 3 до 7 дней.
Клиническая картина острого ГГ включает в себя высокую температуру (98%), болезненность в правом подреберье, повышение уровней конъюгированного билирубина и аминотрансфераз, а также лейкопению и тромбоцитопению (71 и 93% соответственно). Концентрации сывороточных трансаминаз иногда превышают верхнюю границу нормы в 100-1000 раз. Относительно трансаминаз уровень билирубина может быть не очень высоким (4927±4099 Ед/л и 98±102 мкмоль/л соответственно) [5]. Поскольку гепатит имеет тяжелое течение (в ряде случаев фульминантное), признаки тяжелой печеночной недостаточности также выявляются довольно часто (геморрагический синдром – 84%, энцефалопатия, кома – 80%, олигурия – 65%). Уровень летальности высокий и колеблется, по данным различных авторов, от 40 до 80% [5, 26, 27]. Высыпания, как уже упоминалось, встречаются менее чем у половины больных (44%), в основном на слизистых оболочках (27%). У 17% они имеют диссеминированный характер [5].
С целью улучшения результатов клинической диагностики пациентов всегда следует спрашивать о боли в горле, дисфагии, дизурии или выделениях из половых органов. Тем не менее, независимо от того, жалуется пациент на высыпания на коже или нет, его слизистые оболочки и кожные покровы необходимо осматривать на предмет патологических изменений; иногда существует потребность в гинекологическом осмотре (наличие везикул на шейке матки не всегда могут сопровождаться высыпаниями (везикулами) на наружных половых органах или во влагалище). Если обнаружены изменения на коже или слизистых оболочках, то окрашивание мазка, полученного путем соскоба, по Гимзе или Райту (тест Тцанка), позволяет заподозрить диагноз на основании обнаружения гигантских многоядерных клеток с характерными матово-стекловидными включениями Cowdry в ядрах.
К сожалению, реалии таковы, что у многих пациентов герпетическая этиология ФГ устанавливается на основании данных аутопсии. Так, по данным Norvell и соавт. [5], аутопсия была первоначальным методом установления диагноза у 58% больных, еще у 31% герпетическая этиология гепатита была подтверждена после биопсии печени, у 3% – при исследовании эксплантированной печени.
Гистологически при ФГГ выявляют большие участки некроза паренхимы печени. В гепатоцитах с помощью реакции гибридизации in situ может быть выявлена ДНК вируса. Иногда при микроскопии удается обнаружить тельца Cowdry типа А – эозинофильные включения, состоящие из нуклеиновых кислот и белка. После начала противовирусной терапии они могут исчезать [28]. Помимо некроза существенную роль в поражении печени может играть апоптоз [29].
Наряду с иммунодефицитом еще одним важным состоянием, предрасполагающим к диссеминации инфекции, является беременность [30, 31]. В отделениях, занимающихся трансплантацией печени, беременные составляют не менее 20-25% от общего числа больных с ФГГ [5]. Гепатит, вызванный HSV (как первого, так и второго типа) во время беременности, может быть следствием как первичной инфекции, так и ее реактивации. Беременность является особой формой иммуносупрессии, что подтверждается сниженным ответом созревающих лимфоцитов на стимуляцию фитогемагглютинином, уменьшением числа Т-клеток, а также уровня IgG с 27-й по 33-ю нед беременности, что коррелирует с гемодилюцией, характерной для этого периода. Особенно опасно инфицирование во время третьего триместра беременности, когда вирус может преодолевать плацентарный барьер, что связано с высоким риском смерти и матери, и плода [32].
По различным данным, сыпь встречается у 33-70% беременных [7, 33, 34]. Поскольку диссеминированная герпетическая инфекция редко предполагается как причина гепатита у иммунокомпетентных лиц при отсутствии высыпаний на слизистых оболочках и коже, у беременных следует исключить альтернативные причины поражения печени: острую жировую дистрофию печени, HELLP-синдром, а также подкапсульное (реже в паренхиму) кровоизлияние вследствие тяжелой преэклампсии. Не следует сбрасывать со счетов возможность гепатита, вызванного другими вирусами, или воздействием экзогенных субстанций, таких как наркотики [35].
Гепатит при врожденной HSV-инфекции также является следствием ее диссеминации. Он встречается примерно у 25% новорожденных, инфицированных HSV, или с частотой 1 установленный случай на 2-5 тыс. новорожденных в год [36]. ГГ рассматривают как наиболее частую инфекционную причину ОПН у новорожденных [37]. Помимо поражения печени отмечаются нарушения со стороны других органов и систем: центральной нервной системы (ЦНС), легких, надпочечников, кожи, глаз, слизистой оболочки ротовой полости. У 60-80% женщин, дети которых рождаются с HSV-инфекцией, не удается выявить признаков генитального герпеса или указаний на него в анамнезе, а также наличия сексуального партнера(ов) с данной инфекцией [38]. Показатели материнской смертности и новорожденных по причине ГГ могут достигать 39% [39].
В отличие от иммунокомпетентных лиц у пациентов с иммуносупрессией всегда следует рассматривать вероятность герпетической этиологии гепатита. В этом случае заболевание является, как правило, следствием реактивации латентной инфекции [40]. Типичные для этих больных обширные поражения кожи и слизистых оболочек упрощают диагностику патологии. У пациентов, имеющих антитела к HSV и получающих иммуносупрессивную терапию после трансплантации солидных органов или костного мозга, с высоким постоянством вирус обнаруживается в слюне в течение первых 2-3 нед лечения, хотя диссеминированные формы инфекции встречаются у меньшей части больных [41]. Интересно, что в случае трансплантации костного мозга от HSV-серонегативных доноров HSV-серопозитивные реципиенты подвергаются более высокому риску рецидива, у них с большей вероятностью могут появиться штаммы HSV, устойчивые к ацикловиру, по сравнению с пациентами, которым пересаживают костный мозг от HSV-серопозитивных доноров [5]. Сообщалось о летальных исходах вследствие ГГ, развившегося у пациентов с неопластическими заболеваниями, в результате лечения кортикостероидами [43].
Несмотря на высокую летальность, ГГ является потенциально курабельным заболеванием, т. к. ацикловир и валацикловир проявляют высокую терапевтическую активность как in vitro, так и in vivo. Теоретически возможность серологической диагностики, выявления вируса с помощью полимеразной цепной реакции (ПЦР) по данным биопсии печени может улучшить своевременную диагностику и выживаемость. Основанием для лабораторного обследования на HSV-инфекцию может быть тяжелое течение заболевания с развитием ФГ или без него при отрицательных результатах анализа на маркеры гепатитов А-Е.
Выявить антитела к HSV-1 и HSV-2 в сыворотке HSV-инфицированных лиц легко, но их нельзя использовать для диагностики острой инфекции. Наличие сывороточных антител – IgM, а также увеличение титра антител IgG в 4 раза не указывают на первичную инфекцию, так как они могут появляться при реактивации. Тем не менее серологические методы считаются достоверными для выявления лиц, находящихся в ремиссии или являющихся носителями HSV [44]. Антитела IgG к HSV-1 и HSV-2, которые различаются по антигенным свойствам, могут быть обнаружены в сыворотке; скрининг на HSV-2 рекомендуется в отдельных группах риска [45]. Вестерн-блот может быть полезен для дифференциации инфекции, вызванной HSV-1, от таковой, спровоцированной HSV-2, с чувствительностью и специфичностью >98% [46].
Обнаружение ДНК HSV методом ПЦР обладает высокой специфичностью (99%) и чувствительностью (≥90%), особенно когда вирусная нагрузка составляет >500 копий/мм 3 [47]. Наибольшей же значимостью обладает выявление вируса в пораженных тканях (гепатоцитах). Для этого используют различные методы, в частности выявление вирусных антигенов при помощи меченных флуоресцеином антител, ДНК вируса при помощи ПЦР [26]. Всегда следует проводить культивирование, поскольку оно обеспечивает выделение вируса, который может быть типирован. Для этого подходят кровь, соскобы кожи, содержимое везикул.
Цитопатический эффект, как правило, наблюдается спустя 24-48 ч после заражения культуры вирусом. Тем не менее противовирусную терапию не следует откладывать в ожидании подтверждения диагноза вирусологическим методом [41].
Один из предложенных алгоритмов действий при подозрении на ГГ представлен на рисунке.
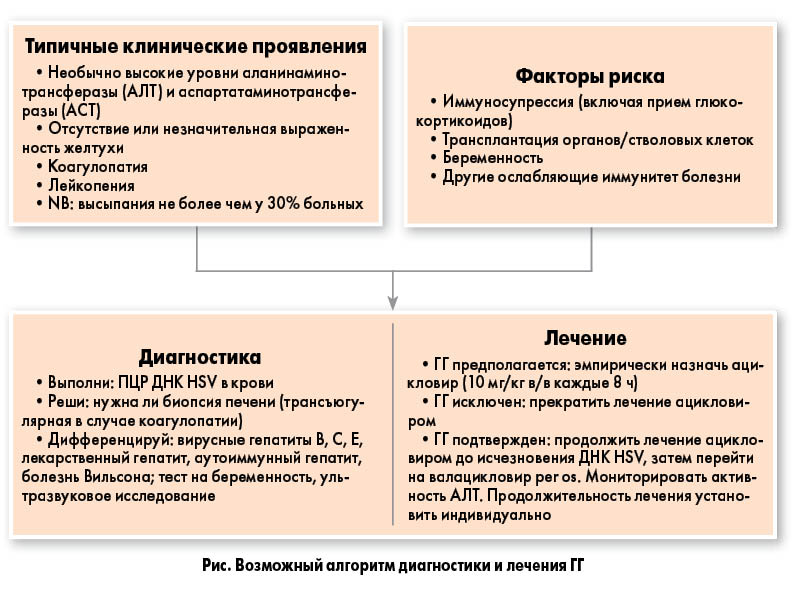
Без адекватной противовирусной терапии и трансплантации печени прогноз при ГГ, как правило, неблагоприятный. Лечение ацикловиром может существенным образом повлиять на выживаемость пациентов, которая у пролеченных больных выше, чем у не получавших терапию ацикловиром (88 vs 51% в одной серии наблюдений) или тех, у кого лечение было начато позже [5].
Пока не ясно, как долго и в каких дозах должен назначаться ацикловир при лечении гепатита. При большинстве форм герпетической инфекции рекомендуемая продолжительность парентерального введения ацикловира составляет 5-7 дней. Исключение составляет энцефалит, при котором лечение должно длиться не менее 14-21 дня вследствие высокого риска развития рецидива в случае меньшей продолжительности терапии [48]. Rimawi и соавт. сообщают об успешной терапии 2 пациентов с ГГ, продолжавшейся 7 дней. Нормализация активности трансаминаз была подтверждена результатами исследования спустя месяц после начала заболевания [49].
Haag и соавт. сообщают об успешном лечении ацикловиром (10,5 мг/кг каждые 8 ч) ГГ у больной с иммунодефицитом (болезнь Крона) [50]. После 14 дней лечения (клиническое улучшение отмечено на 7-й день) пациентка была переведена на терапию валацикловиром (1000 мг 2 р/день), которая также продолжалась 2 недели с последующим постепенным снижением дозы препарата (500 мг 2 р/день).
В случае ФГ некоторые авторы допускают возможность эмпирической противовирусной терапии в ожидании результатов лабораторного обследования. У больных с иммуносупрессией, поражением костей, обширными ожогами о герпетической природе гепатита необходимо думать в первую очередь. У пациентов с иммунодефицитом, особенно после индукционной химиотерапии или трансплантации, профилактический прием ацикловира снижает вероятность развития клинических симптомов герпетической инфекции. Сопоставимую эффективность имеют фамцикловир и валацикловир [35].
Прием ацикловира per os связывают с развитием почечной недостаточности у лиц пожилого возраста [51]. Риск нефротоксичности может быть уменьшен за счет медленной инфузии препарата и обеспечения адекватной гидратации. Внутривенное введение ацикловира иногда сопровождается нарушениями со стороны ЦНС (возбуждение, галлюцинации, дезориентация, тремор и миоклонии). Теоретически (поскольку ацикловир проникает через плаценту и накапливается в амниотической жидкости) существует вероятность нефротоксического воздействия препарата на плод. Тем не менее пока в клинической практике таких случаев не зафиксировано [52].
Преодолеть резистентность к препарату можно с помощью альтернативных схем лечения. В этом случае средством выбора является фоскарнет [55]. В случае устойчивости как к ацикловиру, так и к фоскарнету возможно применение цидофовира – нуклеотидного аналога, активного в отношении широкого спектра ДНК-содержащих вирусов, в том числе HSV [56].
Профилактический прием противовирусных препаратов может снизить частоту осложнений, связанных с реактивацией HSV-инфекции у больных с иммуносупрессией. Так, в одном из исследований было показано, что прием ганцикловира снижал частоту клинически манифестных форм герпетической инфекции после трансплантации печени до 3,5 vs 23,5% у реципиентов, получавших плацебо [57].
Трансплантация печени в случае ФГ является методом выбора. Использование прогностических маркеров может быть полезным в разграничении больных, нуждающихся в трансплантации печени, и пациентов, у которых возможно спонтанное выздоровление [58]. Необходимо учесть, что у пациентов с иммуносупрессией трансплантация печени и последующая иммуносупрессия могут осложнить течение инфекции в посттрансплантационном периоде. У пациентов с криптогенным гепатитом, этиология которого была установлена при исследовании эксплантированной печени, лечение ацикловиром в посттрансплантационном периоде было успешным [59]. К сожалению, времени на принятие решения о необходимости лечения ацикловиром не так много, т. к. период от момента начала заболевания до развития ФГ, требующего трансплантации, очень короток.
Таким образом, ГГ является редким заболеванием, а его своевременная диагностика чрезвычайно важна с учетом риска развития ФГ. Лечение ацикловиром может существенно улучшить прогноз заболевания, снизить частоту летальных исходов и уменьшить потребность в трансплантации печени.
СТАТТІ ЗА ТЕМОЮ Діагностика
Успішне ведення пацієнта більш ніж на 50% залежить від встановлення правильного діагнозу. Визначення терапевтичної стратегії, оцінювання ризику та прогнозу в онкологічного хворого неможливі без патоморфологічного висновку. У всьому світі першими кроками в боротьбі з раком були впровадження ефективних методів ранньої діагностики захворювань, скринінгових програм, профілактичних заходів. Необхідною умовою покращення надання медичної допомоги в Україні є можливість і доступність проведення якісної патоморфологічної, цитологічної, генетично‑молекулярної діагностики.
Сахарный диабет (СД) – это хроническое метаболическое заболевание, вызванное абсолютной или относительной недостаточностью инсулина, нарушением чувствительности тканей к инсулину, что проявляется гипергликемией. В настоящее время заболеваемость СД приобрела характер эпидемии и является проблемой для здравоохранения во всем мире. На сегодня, согласно статистическим данным, 415 млн человек болеют СД. По прогнозу Международной федерации диабета (IDF), к 2040 г. количество больных составит 642 млн.
Дефицит альфа1-антитрипсина (А1АТ) – генетически детерминированное заболевание, вызванное недостаточностью А1АТ в сыворотке крови, возникающее вследствие различных мутаций в гене Pi и проявляющееся в виде хронической обструктивной болезни легких (ХОБЛ), эмфиземы легких, идиопатического фиброза, бронхоэктазов, развития рака легкого, поражения печени и сосудов.
Владелец регистрационного удостоверения:
Произведено:
Лекарственная форма
рег. №: ЛП-000199 от 09.02.11 - ДействующееФорма выпуска, упаковка и состав препарата Ацикловир
| Таблетки | 1 таб. |
| ацикловир | 200 мг |
10 шт. - упаковки ячейковые контурные (2) - пачки картонные.
Фармакологическое действие
Противовирусный препарат - синтетический аналог ациклического пуринового нуклеозида, обладающего высоко избирательным действием на вирусы герпеса. В инфицированных вирусом клетках под действием вирусной тимидинкиназы происходит фосфорилирование и дальнейшая последовательная трансформация ацикловира в моно-, ди- и трифосфат. Ацикловиртрифосфат встраивается в цепочку вирусной ДНК и блокирует ее синтез посредством конкурентного ингибирования вирусной ДНК-полимеразы.
In vitro ацикловир эффективен против вируса простого герпеса - Herpes simplex 1 и 2 типов; против вируса Varicella zoster, вызывающего ветряную оспу и опоясывающий лишай; более высокие концентрации требуются для ингибирования вируса Эпштейна-Барр. Умеренно активен в отношении цитомегаловируса.
In vivo ацикловир терапевтически и профилактически эффективен, прежде всего, при вирусных инфекциях, вызываемых вирусом Herpes simplex 1 и 2 типов. Предупреждает образование новых элементов сыпи, снижает вероятность кожной диссеминации и висцеральных осложнений, ускоряет образование корок, снижает боль в острой фазе опоясывающего герпеса.
Фармакокинетика
После приема внутрь биологическая доступность составляет 15-30%, при этом создаются дозозависимые концентрации, достаточные для эффективного лечения вирусных заболеваний. Пища не оказывает значительного влияния на всасывание ацикловира. Ацикловир хорошо проникает во многие органы, ткани и жидкости организма. Связывание с белками плазмы составляет 9-33% и не зависит от его концентрации в плазме. Концентрация в спинномозговой жидкости составляет около 50% от его концентрации в плазме. Ацикловир проникает через гематоэнцефалический и плацентарный барьеры, накапливается в грудном молоке. После приема внутрь 1 г/сут концентрация ацикловира в грудном молоке составляет 60-410% от его концентрации в плазме (в организм ребенка с молоком матери ацикловир поступает в дозе 0.3 мг/кг/сут).
C max препарата в плазме крови после приема внутрь по 200 мг 5 раз/сут - 0.7 мкг/мл, C min - 0.4 мкг/мл; время достижения C max в плазме - 1.5-2 ч. Метаболизируется в печени с образованием фармакологически неактивного соединения 9-карбоксиметоксиметилгуанина. Выводится почками путем клубочковой фильтрации и канальцевой секреции: около 84% выводится почками в неизменном виде, 14% - в форме метаболита. Почечный клиренс ацикловира составляет 75-80% от общего плазменного клиренса.T 1/2 у взрослых людей с нормальной функцией почек составляет 2-3 ч. У больных с тяжелой почечной недостаточностью T 1/2 - 20 ч, при гемодиализе - 5,7 ч, при этом концентрация ацикловира в плазме уменьшается до 60% от исходного значения. Менее 2% ацикловира выводится из организма через кишечник.
Показания препарата Ацикловир
- лечение инфекций кожи и слизистых оболочек, вызываемых вирусами Herpes simplex 1 и 2 типов, как первичных, так и вторичных, включая генитальный герпес;
- профилактика обострений рецидивирующих инфекций, вызываемых Herpes simplex 1 и 2 типов, у пациентов с нормальным иммунным статусом;
- профилактика первичных и рецидивирующих инфекций, вызываемых вирусами Herpes simplex 1 и 2 типов, у больных с иммунодефицитом;
- в составе комплексной терапии пациентов с выраженным иммунодефицитом: при ВИЧ-инфекции (стадия СПИД, ранние клинические проявления и развернутая клиническая картина) и у пациентов, перенесших трансплантацию костного мозга;
- лечение первичных и рецидивирующих инфекций, вызываемых вирусом Varicella zoster(ветряная оспа, а также опоясывающий лишай - Herpes zoster).
| Код МКБ-10 | Показание |
| A60 | Аногенитальная герпетическая вирусная инфекция [herpes simplex] |
| B00 | Инфекции, вызванные вирусом простого герпеса [herpes simplex] |
| B01 | Ветряная оспа [varicella] |
| B02 | Опоясывающий лишай [herpes zoster] |
| B20 | Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], проявляющаяся в виде инфекционных и паразитарных болезней |
Режим дозирования
Ацикловир принимают во время или сразу после приема пищи и запивают достаточным количеством воды. Режим дозирования устанавливают индивидуально в зависимости от степени тяжести заболевания.
Лечение инфекций кожи и слизистых оболочек, вызываемых Herpes simplex 1 и 2 типов
Ацикловир назначают по 200 мг 5 раз/сут в течение 5 дней с 4-часовым интервалами в течение дня и с 8-часовым интервалом на ночь. В более тяжелых случаях заболевания курс лечения может быть продлен по назначению врача до 10 дней. В составе комплексной терапии при выраженном иммунодефиците, в т.ч. при развернутой клинической картине ВИЧ-инфекции, включая ранние клинические проявления ВИЧ-инфекции и стадию СПИД; после трансплантации костного мозга или при нарушении всасывания из кишечника назначают по 400 мг 5 раз/сут.
Лечение необходимо начинать как можно раньше после возникновения инфекции; при рецидивах ацикловир назначают в продромальном периоде или при проявлении первых элементов сыпи.
Профилактика рецидивов инфекций, вызываемых Herpes simplex 1 и 2 типов у пациентов с нормальным иммунным статусом
Рекомендованная доза составляет по 200 мг 4 раза/сут (каждые 6 ч) или 400 мг 2 раза/сут (каждые 12 ч). В ряде случаев оказываются эффективными более низкие дозы - по 200 мг 3 раза/сут (каждые 8 ч) или 2 раза/сут (каждые 12 ч).
Профилактика инфекций, вызываемых Herpes simplex 1 и 2 типов , у пациентов с иммунодефицитом .
Рекомендуемая доза составляет по 200 мг 4 раза/сут (каждые 6 ч). В случае выраженного иммунодефицита (например, после трансплантации костного мозга) или при нарушении всасывания из кишечника дозу увеличивают до 400 мг 5 раз/сут. Продолжительность профилактического курса терапии определяется длительностью периода существования риска инфицирования.
Лечение инфекций, вызываемых вирусом Varicella zoster(ветряная оспа)
Назначают по 800 мг 5 раз/сут каждые 4 ч днем и с 8-часовым интервалом на ночь. Продолжительность курса лечения 7-10 дней.
Назначают по 20 мг/кг 4 раза/сут в течение 5 дней (максимальная разовая доза 800 мг), детям от 3-х до 6 лет : по 400 мг 4 раза/сут, старше 6 лет : по 800 мг 4 раза/сут в течение 5 дней.
Лечение необходимо начинать при появлении самых ранних признаков или симптомов ветряной оспы.
Лечение инфекций, вызываемых вирусом Herpes zoster (опоясывающий лишай)
Назначают по 800 мг 4 раза/сут каждые 6 ч в течение 5 дней. Детям в возрасте старше 3 лет препарат назначают в той же дозе, что и взрослым.
Лечение и профилактика инфекций, вызываемых Herpessimplex 1 и 2 типов , пациентов детского возраста с иммунодефицитом и нормальным иммунным статусом .
Дети от 3-х лет до 6 лет - 400 мг раза/сут; старше 6 лет - 800 мг 4 раза/сут. Более точную дозу определяют из расчета 20 мг/кг массы тела, но не более 800 мг раза/сут. Курс лечения составляет 5 дней. Данные о профилактике рецидивов инфекций, вызываемых вирусом простого герпеса, и лечении опоясывающего герпеса у детей с нормальными показателями иммунитета отсутствуют.
Для лечения детей старше 3 лет назначают по 800 мг ацикловира 4 раза/сут каждые 6 ч (как и для лечения взрослых с иммунодефицитом ).
В пожилом возрасте происходит снижение клиренса ацикловира в организме параллельно со снижением клиренса креатинина. принимающие большие дозы препарата внутрь, должны получать достаточное количество жидкости. При почечной недостаточности необходимо решить вопрос о снижении дозы препарата.
Необходимо соблюдать осторожность при назначении ацикловира пациентам с почечной недостаточностью . У таких пациентов прием препарата внутрь в рекомендованных дозах с целью лечения и профилактики инфекций, вызываемых вирусом простого герпеса, не приводит к кумуляции препарата до концентраций, превышающих установленные безопасные уровни. Однако, у больных с выраженной почечной недостаточностью (КК меньше 10 мл/мин) дозу ацикловира следует снизить до 200 мг 2 раза/сут с 12-часовыми интервалами.
При лечении инфекций, вызываемых вирусом Varicella zoster, Herpes zoster , a также при лечении пациентов с выраженным иммунодефицитом рекомендуемые дозы составляют:
- терминальная почечная недостаточность (КК менее 10 мл/мин) - по 800 мг 2 раза/сут каждые 12 ч;
- тяжелая почечная недостаточность (КК 10-25 мл/мин) - по 800 мг 3 раза/сут каждые 8 ч.
Побочное действие
Препарат обычно хорошо переносится.
Использована следующая классификация нежелательных реакций в зависимости от частоты встречаемости: очень часто (>1/10), часто (>1/10, 1/1000, 1/10 000, Со стороны пищеварительной системы: часто - тошнота, рвота, диарея; очень редко - гепатит, желтуха, в единичных случаях - абдоминальные боли.
Со стороны системы кроветворения: редко - преходящее незначительное повышение активности ферментов печени, небольшое повышение концентрации мочевины и креатинина, гипербилирубинемия; очень редко - лейкопения, эритропения, анемия, тромбоцитопения.
Со стороны ЦНС: часто - головная боль, головокружение; очень редко - возбуждение, спутанность сознания, тремор, атаксия, дизартрия, галлюцинации, психотические симптомы, судороги, сонливость, энцефалопатия, кома.
Обычно эти побочные эффекты наблюдались у пациентов с почечной недостаточностью или при наличии других провоцирующих факторов, и были, в основном, обратимыми.
Со стороны дыхательной системы: редко - одышка.
Аллергические реакции: анафилактические реакции, кожная сыпь, зуд, крапивница, синдром Лайелла, синдром Стивенса-Джонсона.
Со стороны кожи и подкожной клетчатки: часто - зуд, крапивница, сыпь, в том числе сенсибилизация, редко - алопеция, быстрое диффузное выпадение волос (поскольку такой тип алопеции наблюдается при различных заболеваниях и при терапии многими лекарственными средствами, связь ее с приемом ацикловира не установлена); очень редко синдром Лайелла, синдром Стивенса-Джонсона.
Прочие: часто - утомляемость, лихорадка; редко - периферические отеки, нарушение зрения, лимфаденопатия, миалгия, недомогание.
Противопоказания к применению
- период лактации;
- детский возраст до 3 лет (для данной лекарственной формы).
С осторожностью: беременность; лицам пожилого возраста и пациентам, принимающим большие дозы ацикловира, особенно на фоне дегидратации; нарушение функции почек; неврологические нарушения или неврологические реакции на прием цитотоксических лекарственных средств (в т.ч. в анамнезе).
Применение при беременности и кормлении грудью
Ацикловир проникает через плацентарный барьер и накапливается в грудном молоке. Применение препарата при беременности возможно только в том случае, когда предполагаемая польза для матери превышает потенциальный риск для плода. При необходимости приема ацикловира в период лактации требуется прерывание грудного вскармливания.
Применение при нарушениях функции почек
Принимать с осторожностью при нарушении функции почек.
Необходимо соблюдать осторожность при назначении ацикловира пациентам с почечной недостаточностью . У таких пациентов прием препарата внутрь в рекомендованных дозах с целью лечения и профилактики инфекций, вызываемых вирусом простого герпеса, не приводит к кумуляции препарата до концентраций, превышающих установленные безопасные уровни. Однако, у больных с выраженной почечной недостаточностью (КК меньше 10 мл/мин) дозу ацикловира следует снизить до 200 мг 2 раза/сут с 12-часовыми интервалами.
При лечении инфекций, вызываемых вирусом Varicella zoster, Herpes zoster , a также при лечении пациентов с выраженным иммунодефицитом рекомендуемые дозы составляют:
- терминальная почечная недостаточность (КК менее 10 мл/мин) - по 800 мг 2 раза/сут каждые 12 ч;
- тяжелая почечная недостаточность (КК 10-25 мл/мин) - по 800 мг 3 раза/сут каждые 8 ч.
Применение у детей
Применение у пожилых пациентов
Особые указания
Ацикловир применяется строго по назначению врача во избежание осложнений у взрослых и детей старше 3-х лет.
Длительность или повторное лечение ацикловиром больных со сниженным иммунитетом может привести в появлению штаммов вирусов, нечувствительных к его действию. У большинства выявленных штаммов вирусов, нечувствительных к ацикловиру, обнаруживается относительная нехватка вирусной тимидинкиназы; были выделены штаммы с измененной тимидинкиназой или с измененной ДНК-полимеразой. In vitro действие ацикловира на изолированные штаммы вируса Herpes simplex может вызвать появление менее чувствительных штаммов.
С осторожностью препарат назначают пациентам с нарушением функции почек, больным пожилого возраста в связи с увеличением периода полувыведения ацикловира.
При применении препарата необходимо обеспечить поступление достаточного количества жидкости.
При приеме препарата следует контролировать функцию почек (концентрацию мочевины крови и креатинина плазмы крови). Ацикловир не предупреждает передачу герпеса половым путем, поэтому в период лечения необходимо воздержаться от половых контактов, даже при отсутствии клинических проявлений. Необходимо информировать пациентов о возможности передачи вируса генитального герпеса в период высыпаний, а также о случаях бессимптомного вирусоносительства.
Влияние на способность к вождению автотранспорта и управлению механизмами
Нет данных. Однако следует учитывать, что в период лечения ацикловиром может развиваться головокружение, поэтому необходимо соблюдать осторожность при вождении автотранспорта и занятии потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Передозировка
Не зарегистрировано случаев передозировки при пероральном приеме ацикловира. Сообщалось о приеме внутрь 20 г ацикловира. Симптомы: ажитация, кома, судороги, летаргия. Возможна преципитация ацикловира в почечных канальцах, если его концентрация превышает растворимость в почечных канальцах (2.5 мг/мл).
Лекарственное взаимодействие
Одновременное применение с пробенецидом приводит к увеличению среднего T 1/2 и снижению клиренса ацикловира.
Усиление эффекта ацикловира отмечается при одновременном назначении иммуностимуляторов.
При одновременном приеме с нефротоксичными препаратами повышается риск развития нарушения функций почек.
Условия хранения препарата Ацикловир
Препарат хранить в сухом, защищенном от света месте при температуре не выше 25°С. Хранить в недоступном для детей месте.
Читайте также:


