Воздействие лазерного излучения на вирусы
Лазер - Эффективный помощник в борьбе с герпесом!

Герпесом называют такое заболевание кожи, что проявляется на вирусной основе и выглядит как пузырьковая сыпь на покровах кожи и ее слизистых оболочках. На данный момент распознают около 80 типов герпесных вирусов. Но только 8 из них можно встретить у человека. Но наиболее часто встречаемым является герпес 1 типа или же простой герпес, который приводит к сыпи на губах.
На сегодня пока нет такого препарата, который бы вывел вирус герпеса из человеческого организма раз и навсегда. Но при этом есть такие методы, который препятствуют размножению клеток вируса. Такие лекарства нужно принимать на ранней стадии инфицирования. Так вы можете предотвратить проявления вируса в виде пузырьков. Однако нужно учитывать, что лечением одними таблетками или мазями малоперспективно, ведь рецидивы герпеса все равно будут присутствовать и нужно позаботиться о том, чтобы они появлялись как можно реже. Естественно, сначала нужно заняться укреплением иммунитета.
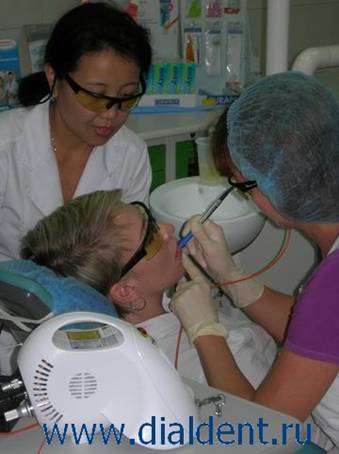
Однако на сегодняшний момент существует метод лечения герпеса - лазером. Это является эффективным методом лечения данного недуга. Если начать применение лазерного лечения герпеса еще на первой недели, это поможет предотвратить разрыванию пузырьков. Благодаря воздействию лазерных лучей не только уменьшается зуд, дискомфорт, боль, но и исключается возможность распространения вируса по слизистой оболочке.
Процедура занимает всего 5-8 минут, а самым важным моментом является снижение вероятности рецидива. Герпес уменьшается в размере, если пузырек уже лопнул до процедуры, тогда лечение лазером ускорит подсыхание и заживление ранки. Для того чтобы полностью избавится от герпеса, нужно пройти от 1 до 3 абсолютно безопасных процедур.
Лазерное воздействие разрушает вирусы, для этого используется безопасная для тканей длина волны 810 нм. Лазерное излучение с длиной волны 810 нм убивает вирусы и бактерии, не травмируя ткани организма. Этот же эффект применяется в пародонтологическом лечении и при стерилизации каналов зубов. Такое излучение является губительным для данного типа вируса, но при этом хорошо влияет на местный и общий иммунитет.
Многие пациенты интересуются болезненностью при использовании лазера, однако, по этому поводу переживать не стоит, ведь во время лечения герпеса лазером больной не чувствует дискомфорта и боли. В наше время, довольно многие выбирают именно этот метод борьбы с герпесом. Лечение лазером приобретает все большую популярность, так как решает проблему за короткие сроки и предотвращает рецидив.
Лазер эффективен на всех стадиях развития герпеса:
- на первой стадии лазерное излучение помогает снять болевые ощущения и снизить интенсивность высыпаний;
- на второй стадии лазерное излучение позволяет остановить дальнейшее развитие высыпаний, что приводит к заживлению;
- на третьей стадии лазер снимает болевые ощущения, уменьшает воспаление;
- на четвертой стадии лазерное воздействие приводит к более быстрому заживлению тканей.
Важно: Лечение лазером проявлений герпеса на губах , не отменяет лечения с помощью противовирусных препаратов!
Преимущества лечения герпеса лазером:
- лазеротерапия приводит к более бессимптомному течению данного заболевания и усиливает эффект от принятия разного рода медикаментозных препаратов;
- лазеротерапия также способна уменьшить количество рецидивов и возможность осложнений;
- лазер доставляет минимальный дискомфорт, никаких болезненных ощущений;
- благодаря такому методу лечения можно избавиться от симптомов герпеса уже за пару процедур. А срок выздоровления при этом сократиться на 2-4 дня.
В нашей клинике квалифицированные специалисты помогут справиться с герпесом с помощью лазерного диодного стоматологического лазера DOCTOR SMILE(Италия).
Записаться на прием и уточнить любые вопросы, вы можете по телефону 79-000. Имеются противопоказания, необходима консультация специалиста.
Оплата кредитными картами
и по безналичному расчету

|
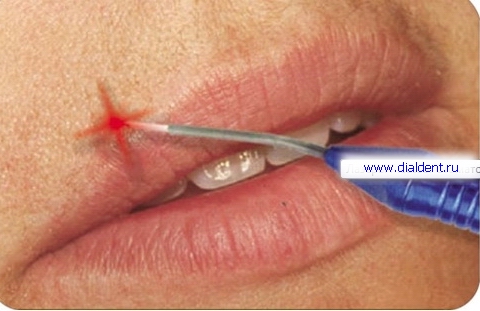
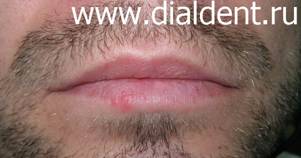
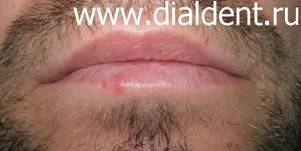
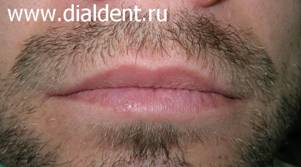
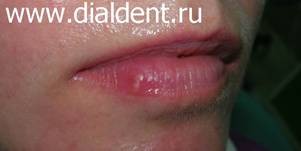
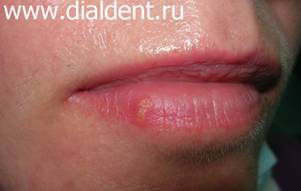
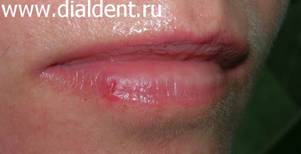
Герпес – вирусное заболевание, которое характеризуется высыпаниями пузырькового вида на коже и слизистых. Первая причина – это снижение иммунитета организма человека. Вторая причина – травма губ, слизистых, органов полости рта, десен. Иногда эти причины действуют совместно. - Стоматологическое лечение. При длительном стоматологическом лечении или при часто повторяющихся визитах к стоматологу (когда человек проходит сложное лечении или протезирование зубов) неизбежно возникают микротравмы губ, слизистых, десен которые могут приводить к активизации вируса герпеса. Есть ряд людей, около 5%, которые не восприимчивы к вирусу герпеса, и не болеют им ни при каких обстоятельствах. Причина этой невосприимчивости неизвестна. Воздействие лазерного луча эффективно на всех этапах развития герпеса: О лечении герпеса лазером коротко можно сказать так: применение лазера позволяет герпесу исчезнуть за 2-4 дня и делает его протекание безболезненным и маловыраженным. Лечить герпес только лазером возможно только при несложных случаях герпеса. Лечение герпеса лазером не отменяет лечения, направленного на стимуляцию иммунных сил организма. В некоторых случаях лечение герпеса лазером может заменить прием противовирусных препаратов или снизить их дозу. Борисова Ю.А. детский стоматолог. Стоимость лечения герпеса лазером: один визит - обработка одного очага - 350 рублей. Иногда хватает однократного воздействия, иногда приходиться обрабатывать герпес лазером два-три раза. Крайне редко возникает необходимость в обработке герпеса в большем количестве раз. - резкая боль при контактах с губой Однократная обработка герпеса. Время процедуры 5 минут. Стоимость лечения герпеса лазером 500 рублей. Через день после обработки лазером герпеса на губах. Повторная обработка лазером очага герпеса. Время процедуры 5 минут. Стоимость лечения герпеса лазером 500 рублей. Еще через два дня. Полное отсутствие симптомов. Больше процедуры не проводились. - резкая боль при контактах с губой Однократная обработка герпеса. Время процедуры 5 минут. Стоимость лечения герпеса лазером 350 рублей. Через день после обработки герпеса лазером. Повторная обработка лазером очага герпеса. Время процедуры 5 минут. Стоимость лечения герпеса лазером 350 рублей. Еще через два дня Значительное улучшение. Боли и отека нет. Больше процедуры не проводились. Ожидается полное заживление через два дня.
Автореферат диссертации по медицине на тему Низкоинтенсивное лазерное излучение и реальдирон в комплексном лечении больных острыми вирусными гепатитамиНа правах рукописи ЧЁРНЫХ Марина Викторовна низкоинтенсивнЬё лазерное излучение и реальдирон в комплексном лечении вольных острыми вирусными гешт-тами (14.00.10 - инфекционные болезни) диссертации на соискание ученой степени кандидата медицинских наук Работа выполнена в Российской медицинской академии последипломного образования. Доктор медицинских наук, профессор М.Х.Турьянов Доктор медицинских наук, профессор ВА-Малов Доктор медицинских наук, профессор Ф.А.Туманов Ведущее учреждение: Московский-медицинский стоматологический институт им.Н.А.Семашко. Публикации. По темегдиссертации опубликованы 3 научные работы. Объем и структура работы. Диссертация состоит из введения, 6 глав, заключения, выводов, практических рекомендаций и указателя литературы. Работа изложена на 132 страницах машинописи, иллюстрирована 9 рисунками и содержит 23 таблицы. Указатель литературы включает 155 отечественных и 71 зарубежных источников. Исследования произведены у 125 пациентов, находившихся на лечении в инфекционном- секторе Московской клинической больницы им. С.П.Боткина, за период с декабря 1992 по сентябрь 1994 гг. По характеру лечения все больные были разделены на 3 группы: в 1 группу вошло 69 (55.2%) пациентов, подвергшихся лечению лазером,. 2 группу - 26 (20.8%) больных, получавших в комплексе лечебных средств препараты группы интерферона, 3 группу - 30 (24%) пациентов, получавших лишь стандартную базисную терапию (контрольная группа). Контрольная (сравнительная) группа формировалась методом случайной выборки. Эта группа больных по полу, возрасту и тяжести болезни была сопоставима (р>0.05) с группами больных, которым дополнительно к базисной терапии применяли специальные методы лечения. К моменту обследования и • лечения возраст больных колебался от 13 до,76 лет и составил в среднем 28.6±0.9 лет. Большинство больных находились в возрасте 25 - 30 лет. Мужчин было несколько больше, чем женщин. ■ Диагноз острого вирусного гепатита ставился на основании эпидемиологических данных, клинико-биохимических признаков болезни и подтверждался обнаружением у всех обследованных маркеров вирусной инфекции. У большинства пациентов (88%) диагностировался острый вирусный гепатит В и острый вирусный гепатит А (таблица 1). РАСПРЕДЕЛЕНИЕ БОЛЬНЫХ ПО ДИАГНОЗУ ДИАГНОЗ КОЛ-ВО БОЛЬНЫХ % БОЛЬНЫХ (НВУ+НСЛО . 8 ' , /-6.4% Основная масса больных (согласно задачам исследования) относилась к среднетяжелому течению. По течению процесса больные с ОВГ делились на острое циклическое и затяжное течение (рисунок 1). СТЕПЕНЬ ТЯЖЕСТИ, ФОРМЫ И ТЕЧЕНИЕ ЗАБОЛЕВАНИЯ ИССЛЕДУЕМЫХ БОЛЬНЫХ С ОВГ Клиническая эффективность проведенного лечения оценивалась по следующим критериям: • фоки исчезновения симптомов интоксикации; • сроки исчезновения желтухи; • динамика специфических маркеров вирусной инфекции; • динамика уровня ферментемии, показателей пигментного и жирового обменов. Группа больных, которым проводилось лечение лазером, была разделена на 2 подгруппы: с лечением ИЛИ длиной волны 0.63 мкм (красный диапазон) и с лечение.НЛИ длиной волны 0.89 мкм (инфракрасный диапазон). В качестве лечебного фактора применялось НЛИ, генерируемое прибором АФДЛ-2. Эта установка имела световод с выходной мощностью 15-20 мВт в красном диапазоне (длина волны 0.63 мкм) и излучатель с выходной мощностью 2 мВт в инфракрасном диапазоне (длина волны 0.89 мкм). Клинические эффекты низкоинтенсивного лазерного излучения красного диапазона с длиной волны (0.63 мкм) были изучены у 54 больных. Контрольная группа составила 30 пациентов. Большинство больных в обеих группах было с ВГА'й ВГВ. Исследуемая и контрольная группы достоверно не отличались по диагнозу (р>0.05). . Преимущественное количество пациентов имело острое циклическое течение ВГ средней степени тяжести с преобладанием цитолитического синдрома. При всех формах заболевания в основной и контрольной группах применялась базисная терапия. На основании данных литературы (Боцвадзе ЭШ. 1989; Лапрун И£. 1991, 1993; Корепанов ВЛ. 1992; Макашова В£. 1992, 1993) и собственных предварительных исследований нами была разработана методика лечения ОВГ гелий-неоновым лазером, проводимая при следующих параметрах облучения: длина волны -0.63 мкм; характер излучения - непрерывный; выходная мощность (Р) - 15 мВт; длительность 1 сеанса - 5 мин.(ЗООсек); кратность сеансов - ежедневно; количество сеансов - 8-10; курсовое время - 40-50 мин.; разовая доза (ЕБ) - 4.5 Дж/см2; курсовая доза (Е3курс) - 36-450 Дж^см2; зона воздействия- 5 точек проекции печени; методика - ко;пактио-етабильная и контактно- компрессионная (таблица 2). ________ —---------- МЕТОДИКА ЛЕЧЕНИЯ ЛАЗЕРОМ ДИАПАЗОНА 0.63 МКМ ПАРАМЕТРЫ КРАСНЫЙ ДИАПАЗОН харахстер излучения непрерывный выходная мощность(Р) У';*. длительность 1 сеанса 5 мин.(ЗООсек) кратность сеансов ежедневно количество сеансов 8.3±0.3 курсовое время 41.5±1.4 мин. разовая доза (Ед) 4.5 Дж/см2 курсовая доза (Е^курс) 29 7±1.04 Дж/см2 зона воздействия 5 точек проекции печени методика ■ - контактно-стабильная к контактно-компрессионная При оценке совокупности клинических, биохимических и ■серологических данных нами установлено, что излучение гелий-неонового лазера в апробированном диапазоне обладает рядом положительных свойств. Так при анализе лечения больных красным лазером выя^л^-по, *тго уже первых, процедур лазерной тергпии отмечалось улучшение общего состояния: уменьшение слабости, еялос. ■ . прекращалась тошнота, улучшался, аппетит, меаыаались болк в овладев, правого подреберья, дискомфорт * зпегг стрни. Ни у одного пациента после включения лазера в комплексную терапию не отмечалось ухудшения состояния. К коццу курса лазерной терапии (в среднгм на 13.7±0.9 день желтухи) интоксикации у больных основной группы не было. Однако интоксикация к этому же времени сохгиш;".- л у 12.5% больных ь контрольной группе. В целом лнтоксикацпя у больных оспогной группы исчезла на 2-3 дня раньше, чем г .:олтролькой группе. ' ^ Под влиянием лазерной, терапии у Сольных основной группы наблюдалась более быстрая нормализация размеров печени (р после лечения 329.02*43.4 583.8*121.03 p=o:oooi при выписке • 117.8*13.7 . 122.1*19.4 р==0.37 при поступлении • 277.8*15.6 291.1*20.02 р=0.4. после лечения 177.8*13.2 253.6*20.9 р-ОЯШ при выписке , . 113.8*9.3 150.4*11.6 при поступлении ' 184.o*ló.9 165.8*24.3 р=0.2г после лечения 116.1*10.9 134.1*10.4 р=0.09 при выписке 106.4*13.6 105.1*8.9 р=0.06 при поступлении 116.2*15.7 71.9*15.8 р=0.001 после лечения 107.2*22.2 54.9*2.8 - р=0.001 при выписке 62.6*22.6 44.1*3 '!Л р=0.001 зггздаш и p-липопротеидов (р>0.05). Анализу подвергнута динамика изменения биохимических показателе;,! у больных с вирусным гепатитом А и с вируезым :\.па.к.том В в гру.члгз больных, леченцым красным леером. При ср?тг. енки чфф-чс-ч. лечения лазером обнаружено, уровень биллруоина достоверно быстрее нормализовался в группе больных с гпрускьтч гепатитом А. ВГА - 39.4*5.2 мкмоль/л, чем у больных с БГВ - 59.1*3.4 мкмоль/л (р 0.1). Основная масса больных, которым было проведено лечение инфракрасным лазером так же была представлена острым циклическим гепатитом средней степени тяжести с преобладанием цитолнтического синдрома. Для получения эффекта нами б;:ла выбрана доза не менее 0.01 Дж/см2 (0.36 Дж/см2). Серия проведенных наблюдений, когда доза энергии была значительно выше, чем 1 Дж/см2 показала возникновение отрицательных эффектов инфракрасного излучения, в частности возникновение болевого синдрома. Мы связываем это со спазмом артериол с последующим их стойким расширением и, как следствие - увеличением отека печени с проявляющейся болевой реакцией. Инфракрасный лазер был включен в комплекс базисной терапии Лечение инфракрасным лазером начиналось до .10 дня желтухи - в среднем 6.1±0.9 дня. Суммарная доза воздействия составила 3.2±0.3 Дж/см2. При этой дозе воздействия мы не наблюдали у пациентов отрицательных реакцвй л виде болевого синдрома. Применяемая методика воздействия была такова: длина волны - 0.89 мкм; характер излучения - непрерывный; выходная мощность (Р) - 2 мВт; длительность 1 сеанса - 3-5 мин; кратность сеансов - ежедневно; курсовое время - 30-35 мин.; количество сеансов - 8; разовая доза (Ез) - 0.36 Дж/см2; курсовая доза (Е3курс) - 3-3.5 Дж/см2; зона воздействия - область правого подреберья; методика - контактно-лабильная (таблица 4) МЕТОДИКА ЛЕЧЕНИЯ ЛАЗЕРОМ ДИАПАЗОНА 0.89 МКМ ПАРАМЕТРЫ ИНФРАКРАСНЫЙ ДИАПАЗОН длина волны . " 0.89 мкм характер излучения выходная-мопщость(Р) . непрерывный длительность 1 сеанса 228±15.7 сек (3.8±0.3 мин) кратность сеансов ' ежедневно количество сеансов 8.9±0.4 курсовое время 33.8±2.9 мин. разовая доза-(Ед)-• 0.36 Дж/см2 курсовая доза (Едкурс) ; 3.2±0.3 Дж/см2 зона воздействия область правого подреберья Ни у одного пациента после включения лазера в комплексную терапию не отмечалось ухудшения состояния. Однако при лечении больных инфракрасным лазером не было выявлено достоверного уменьшения сроков интоксикации по сравнению с контрольной группой. К концу курса лазерной терапии (в среднем на 15±1.3 день желтухи) интоксикации у больных" основной группы не было. К этому же времени исчезала интоксикация и у больных в контрольной группе. Под влиянием лазерной терапии в инфракрасном диапазоне не выявлено различий в сроках, нормализации размеров печени (р>0.05) по сравнению с контрольной группой. Исследование больных основной и контрольной груцд выявило, что применение лазеротерапии не влияло на продолжительность желтушного периода и при сравнении обеих групп не было иыявлено достоверных различий в сроках желтушного периода (р>0.05). Сравнение ■ динамики биохимических показателей производилось так же в три временных промежутка (таблица. 5): на момент поступления, после курсового воздействия лазарол (для контрольной группы это время соответствовало 15*1.3 дею желтухи) и на момент выписки (соответственно в каждой группе). ДИНАМИКА ИЗМЕНЕНИЯ ОСНОВНЫХ БИОХИМИЧЕСКИХ ПОКАЗАТЕЛЕЙ ПОСЛЕ ЛЕЧЕНИЯ ИНФРАКРАСНЫМ ЛАЗЕРОМ (М±га) БИОХИМ.ПОКАЗАТЕЛИ ИНФРАКРАСН. ЛАЗЕР КОНТРОЛ. ГРУППА Р при поступлении 107.5*12.7 135.9*9.9 р=0.3 после лечения 54.3*10.9 80.6*11.4 р=0.06 при выписке . 22.2*1.4 29.4*2.1 р—0.006 при поступлении 1780.3*244.1 1646.2±140_7 р после лечения 360.5±67.01 798.4*126.2 p-O.OGO при выписке 158.9*30.3 223.5*32.2 p--0.ll . при поступлении 1214.7*204.43 1141.8*113.4 р 0.10 после лечения —0. 0.05). При анализе показателей цитолиза выявлена отчетливая тенденция к более быстро!! нормализации АЛТ и ACT у больных основной группы по сравнению с контрольной. К концу курса лечения инфракрасным лазером уровень АЛТ составил 360.5±67.01 ME, в контроле - 738.4±126.2 ME (р 0.05). При сравнении динамики изменения уровня БЛ в основной и контрольной группах отмечались более низкие показатели в контрольной группе. В то же время, исходно уровень БЛ в контроле был достоверно ниже (р 0.005) быстрее происходила лишь нормализация показателей цитолиза (ACT, АЛТ). В то же время в контрольной группе в аналогичные сроки достоверно снижались показатели и пигментного обмена, и цитолиза, однако не обнаружено достоверного снижений уровня щелочной фосфатазы, у-глютамилтранспептидазы и р-липопротеидов (р>0.05). Средний койко-день в основной группе составил 24.7±2.1 -дней и 26.7±1.9 дней в контрольной группе, но это различие не было статистически достоверным (р>0.05). Динамика серологических маркеров в связи с небольшим количеством наблюдений в этой группе не рассматривалась. ■ Таким образом, на основании проведенных нами . исследований, получены данные, подтверждающиеся клинико-биохимическими исследованиями, которые свидетельствуют, что ' активация функции печени -нзкоинтенсивным лазерным излучением заключается в изменении энергетической активности клеточных мембран. Более быстрое снижение активности трансамиваз (AJIT, ACT) при лечении как красным, так и инфракрасным лазером свидетельствует о выраженном мембраностабилизирующем действии НЛИ. На наш взгляд, это подтверждает литературные данные о том, что НЛИ активирует. антиоксидантную систему, снижает интенсивность перекисного окисления липидов, что в конечном итоге приводит R перестройке и организации мембраны гепатоцита. "Уменьшение сроков интоксикации при лечении лазером, по-видимому, связано с оптимизацией процессов саморегуляции . организма в целом, что подтверлсдает мнение об адаптогенных свойствах НЛИ. Найденная нами более быстрая элиминация . HBsAg у больных ВГВ при лечении красным лазером, по сразнению с контрольной группой, по нашему мнению свидетельствует об иммуностимулирующем действии этого вида излучения. При сравнении действия НЛИ красного и инфракрасного диапазонов на печень при ОВГ, мы обнаружили, что эффективность лазера с длиной волны 0.63 мкм была более направленной и выраженной. Несмотря на то, что в ряде . . исследований приводятся данные- о применении больших доз инфракрасного излучения при патологии печени, мы получили негативную реакцию (появление ' болевого синдрома) при аналогичных дозах. Поэтому в наших исследованиях доза КК-излучения была снижена в несколько раз. Кроме того, данные экспериментальных и клинических исследований по определению специфических фотоакцепторов свидетельствуют о различных точках приложения излечении красно, л и хи^ракрасного спектрг. Так как г- красной области ene.; ¿a ¿"лг:: фотоакцептора-:и . являются ферменты, запускающие антиоксидантную систему, у этого вида излучения был более выражен мембраностабилизирующий аффект за счет снижения интенсивности перекисного окисления липидов. Было произведено изучение терапевтической эффективности нового рекомбинактного геььо-и^н:Еяерного человеческого сс^-интерферона (реальдирона). Эффективность реальдирона была изучена у 17 больных с ВГ. Результативность действия реальдирона сравнивалась с 9 пациентами, получавшими в комплексной -терапии другие препараты группы интерферона (реаферон) и с 30 больными контрольной группы, получавшими стандартную базисную терапию. Большинство больных в исследуемых группах страдало острым вирусным гепатитом В. Исследуемая и контрольные группы достоверно не отличались по диагнозу (р>0.1). Лечение реальдироном начинали в первые десять дней желтушного периода, в среднем на 7.5±1.2 день. При острых вирусных гепатитах всех клинических форм реальдирон вводили по 1-3 млн. МЕ 1 раз в сутки в течение 5-10 дней. Курсовая доза для. одного больного в среднем составила 9.85±1.38 млн.МЕ. Сравнительная характеристика методик применения реальдирона и реаферона показана в таблице 6. МЕТОДИКА ПРИМЕНЕНИЯ ПРЕПАРАТОВ ГРУППЫ ИНТЕРФЕРОНА ПАРАМЕТРЫ РЕАЛЬДИРОН РЕАФЕРОН Способ введения Кратность введения -Разовая доза Курс Курсовая доза внутримышечно ежедневно. 2.1±0.2 млн. МЕ 4.7±0.3 дня 9.8±1.4 млн. МЕ внутримышечно ■ ежедневно 1.2±0.2 млн. МЕ 6.9+0.8 дня 7.8±0.9 млн. МЕ
При воздействии лазерного излучения на живую биосистему поглощается лишь его часть, в то время как другая отражается. При внешнем облучении отражается от 43 до 55% электромагнитных волн оптического диапазона. Глубина проникновения лазерного излучения зависит от его длины волны, самая высокая наблюдается в инфракрасном спектре. Поглощение лазерного света зависит от свойств облучаемых тканей: паренхиматозные органы поглощают до 95–100% излучения, костная и мышечная ткань — до 70–80%, кожный покров — до 30%. На молекулярном уровне под воздействием лазерного излучения происходит следующая последовательность реакций:
На клеточном уровне под действием лазерного света запускаются следующие биологические реакции:
Таким образом, механизмы биологического воздействия лазерного излучения на организм человека крайне многообразны. В основе данного воздействия лежат каскадные биофизические и биохимические реакции, происходящие при поглощении лазерного излучения тканями и клетками, восприятием и передачей действия лазерного излучения жидкими средами организма органам и тканям, что приводит к корректировке работы регуляторных комплексов. В результате действия лазерного излучения изменяются энергетические параметры внутренней среды организма человека. В связи со снижением чувствительности болевых рецепторов, уменьшением отека и напряжения тканей проявляется его обезболивающее и противовоспалительное действие. Увеличение скорости кровотока и рост количества функционирующих капилляров улучшает питание периферических тканей, что вместе с ускорением метаболических реакций и усилением деления клеток способствует процессу регенерации. Доказано, что лазерное излучение в терапевтическом диапазоне оказывает четко выраженный спазмолитический и десенсибилизирующий эффекты, повышает активность общих и местных факторов иммунной защиты, стабилизирует мембраны клеток. Это позволяет рассматривать его как антиоксидант физической природы, который по результату своего действия не отличается от химических антиоксидантов. В связи с высоким интересом к применению неинвазивных методик лечения патологии печени нами было проведено изучение влияния инфракрасной лазерной терапии (ИКЛТ) на клетки печени при её хронических заболеваниях, а также воздействие данного метода терапии на обменные и регенераторные процессы, происходящие в гепатоцитах. Стала оценка эффектов ИКЛТ в комплексной терапии больных хроническими диффузными заболеваниями печени (ХДЗП). Практическая значимость работы заключалась в получении новых данных по использованию инфракрасной лазерной терапии в клинике, установлении данных о пролонгированном действии лазеротерапии, получении достоверной информации об эффективности использования ИКЛТ в комплексном лечении ХДЗП. При исследовании в сыворотке крови больных опытной и контрольных групп стандартных печеночных проб — трансаминаз, билирубина, продуктов перекисного окисления липидов (ПОЛ) — малонового альдегида, диеновых конъюгатов, ферментов антиоксидантной защиты (АОЗ) — каталазы, супероксиддисмутазы, глутатионпероксидазы, печеночно-специфических ферментов — серин — и треониндегидрогеназы, N-ацетил-β-D-глюкозаминидазы, сывороточных уроканиназы и гистидазы выявлено, что более отчетливая и достоверная стабилизация лабораторных показателей происходила у больных, получавших наряду с базисным лечением терапию ИКЛТ. У пациентов после лечения наблюдалось улучшение аппетита, нормализация сна, уменьшение болезненности в проекции печени. Побочных эффектов ИКЛТ отмечено не было. Спустя 3 и 6 месяцев после окончания курса лечения наблюдалось стабилизация исследуемых показателей, что говорило об отсроченном эффекте инфракрасной лазеротерапии. ИКЛТ обладает достоверным корригирующим воздействием на цитолитический, мезенхимально-воспалительный синдромы, пигментообразующую функцию печени, субъективное состояние больных ХДЗП. ИКЛТ обладает также выраженным антиоксидантным эффектом при заболеваниях печени, что выражается в снижении концентрации продуктов ПОЛ и активации ферментов АОЗ. Метод является неинвазивным. Все это позволяет рассматривать инфракрасную лазеротерапию в качестве эффективного компонента комплексной терапии больных хроническими диффузными заболеваниями печени. Было изучено структурно-функциональное состояние компонентов периферической крови у 20 пациенток с типичной формой генитального герпеса при проведении эндоваскулярной лазерной терапии. Контрольную группу составили 10 здоровых женщин репродуктивного возраста. Выявленные в работе ультраструктурные особенности состояния эритроцитов, тромбоцитов, нейтрофилов, моноцитов и неклеточных макромолекулярных компонентов периферической крови у женщин с генитальным герпесом дают более полную информацию для понимания влияния лазерного излучения на вирусную инфекцию. Эндоваскулярное лазерное облучение крови может явиться методом выбора лечения больных с данной патологией. В.Н. Серов, С.Г. Цахилова, П.Д. Бонарцев, А.М. Абубакирова, Т.А. Федорова, Н.В. Орджоникидзе, Т.Г. Хлыстова, Э.М. Бакуридзе В настоящее время известен ряд хронических заболеваний влагалища и шейки матки, возникающих в результате инфицирования половых путей аденовирусами, цитомегаловирусом, Вирусами Коксаки A, ECHO и др. [15]. Но чаще всего гениталии поражаются вирусом простого герпеса (ВПГ). Эта инфекция представляет значительную проблему для репродуктивного здоровья населения, так как первичное инфицирование вирусом простого герпеса или рецидивы заболевания во время беременности могут привести к внутриутробной инфекции, вызывающей повреждения, после которых дальнейшее развитие плода становится невозможным или сопровождается тяжелыми осложнениями, а инфицирование во время родов может быть причиной тяжелых неонатальных и постнатальных заболеваний новорожденных [12, 16, 19, 20]. Вирус герпеса относится к ДНК-содержащим вирусам, имеет сложную структуру, вирионы диаметром 150-200 нм содержат протеин, спермин, глико- и липопротеиды. Вирус чувствителен к эфиру, фенолу, формалину, алкоголю, нагревание до 55 о С разрушает его в течение 30 мин [1]. Вирус начинает размножаться в месте инокуляции, где появляются типичные пузырьковые высыпания, и проникает в кровяное русло. Установлено, что вирус может оседать в виде элементарных телец в эритроцитах, а также поражать лейкоциты, лимфоциты, макрофаги. Таким образом, вирусемия является одной из причин диссеминации вируса в организме, обусловливает интенсивность клинических проявлений болезни [1]. Выявлены два серотипа ВПГ: ВПГ-1 и ВПГ-2. По общепринятому мнению, ВПГ-2 отводится этиологическая роль при генитальных, а ВПГ-1 - при экстрагенитальных поражениях. Генитальный герпес - одно из наиболее распространенных заболеваний, передаваемых половым путем, занимающий второе место после трихомоноза [18]. Первичное инфицирование половой сферы происходит преимущественно в период начала активной половой жизни в возрасте 18-25 лет при контакте с партнером, страдающим генитальным герпесом. Второй пик заболеваемости у женщин в отличие от мужчин приходится на возраст 45 лет и старше [14]. Для генитального герпеса характерно тяжелое течение с частыми рецидивами болезни, нарушающими нормальную половую функцию пациента. Многие исследователи подчеркивают, что болезнь создает конфликтные ситуации в семье, является источником нервно-эмоциональных нарушений у больного, приобретая социальный характер. Предполагают, что 50-60% лиц в группе с низким уровнем жизни имеют антитела к ВПГ-2 к середине жизни, эти антитела обнаружены только у 10-20% лиц в группе с высоким уровнем жизни и у 35% женщин среднего класса [20]. Клинические проявления первичного герпеса наблюдаются обычно в течение 2-3 нед. Сроки возникновения рецидива варьируют, но у 50% больных они появляются в ближайшие 6 мес. При этом симптомы выражены слабее и менее продолжительны, чем при первичной инфекции (7-10 дней). При увеличении длительности заболевания и в связи с проводимым лечением клиническая картина может изменяться [19]. Характерным для патогенеза герпетической болезни является нарушение иммунного ответа [6, 8, 13, 17]. В противовирусной защите организма принимают участие факторы клеточного и гуморального иммунитета. Факторы клеточного иммунитета участвуют в подавлении репродукции вируса, в процессах миграции и удержании макрофагов, лимфоцитов в очаге воспаления. Кроме того, факторы клеточного иммунитета, с одной стороны, вызывают лизис инфицированных клеток и способствуют высвобождению внутриклеточного вируса для последующей нейтрализации его антителами, с другой - влияют на соседние нормальные клетки, предупреждая их инфицирование [4, 17]. Лечение больных с генитальным герпесом представляет собой сложную задачу. Оно должно быть комплексным, направленным на подавление репродукции вируса при одновременной стимуляции факторов специфической и неспецифической защиты организма. Одним из перспективных немедикаментозных методов лечения является фотогемотерапия, в частности эндоваскулярное лазерное облучение крови (ЭЛОК). Лечебный эффект достигается за счет воздействия лазерного излучения на форменные элементы крови, белковые структуры плазмы, антиоксидантную систему. В результате облучения крови отмечается активизация ферментов в эритроцитах, улучшение реологических показателей и снижение коагуляционных свойств крови, происходят изменения в иммунной системе, нормализуются процессы перекисного окисления липидов, энергетический баланс организма, отмечается бактерицидный эффект [7]. Все большее подтверждение находит концепция о едином потоке каскадных клеточных и ферментативных реакций, обеспечивающих взаимодействие указанных систем регуляции [10]. Электронная микроскопия дает уникальную возможность изучать одновременно функциональное состояние элементов систем гемостаза, иммунитета и неспецифической резистентности, их макромолекулярных комплексов, т. е. проводить многотестовое исследование компонентов крови на ультраструктурном (биохимическом) уровне. Целью настоящей работы являлось изучение структурно-функционального состояния компонентов периферической крови у женщин (вне беременности) с типичной формой генитального герпеса при проведении эндоваскулярной лазерной терапии. В исследуемую группу были включены 20 пациенток в возрасте от 20 до 45 лет с типичной формой генитального герпеса. Под наблюдением гинеколога они находились в течение 5 лет и более. Контрольную группу составили 10 здоровых женщин репродуктивного возраста. Диагноз генитального герпеса подтвержден наличием антигенов ВПГ, обнаруженных прямым методом флюоресцирующих антител в соскобах эпителия вульвы, влагалища, шейки матки. Результаты считались положительными при двукратном выявлении изумрудно-зеленого свечения ВПГ и специфических герпес-вирусных включений в цитоплазме эпителиальных клеток в исследуемом материале. Больные жаловались на эпизодически появляющиеся типичные герпетические мелкопузырьковые высыпания различного диаметра, расположенные группами или одиночно на малых половых губах, слизистой оболочке влагалища или шейке матки. Пациентки отмечали общее недомогание, головную боль, выраженное увеличение лимфатических узлов, пониженную работоспособность. Больных беспокоили изнурительный зуд и жжение в области наружных половых органов, не поддающиеся какому-либо лечению, что в значительной мере являлось препятствием для половой жизни, приводило к нервно-психическим нарушением, неврастеническим и депрессивным расстройствам. Медикаментозное лечение этих больных давало временный эффект. Частота рецидивов заболевания колебалась от 3 до 12 раз в год и составила 4,8+/-1,2 раза в год, средняя продолжительность ремиссии была 2,4+/-0,8 мес. Все пациентки имели регулярный менструальный цикл. Половой жизнью вне брака жили 8 женщин, остальные 12 состояли в браке. Смена 2-3 половых партнеров и более имела место у всех пациенток. Удалось выяснить, что у 4 половых партнеров периодически на половых органах отмечались герпетические высыпания. У 4 (20%) пациенток исследуемой группы было невынашивание беременности, 2 (10%) женщины страдали бесплодием. У всех больных с типичной формой генитального герпеса отмечался хронический сальпингоофорит. Для эндоваскулярного лазерного облучения крови использовалось гелий-неоновое излучение с применением аппарата УЛФ-01. Мощность излучения на выходе составила 1 мВт, длина волны - 0,63 нм, время экспозиции - 15-30 мин. Процедуры проводились ежедневно в течение 7-10 дней. Одновременно осуществлялось лечение половых партнеров пациенток исследуемой группы лекарственными средствами и ЭЛОК. Забор крови у больных производился из локтевой вены до и после курса ЭЛОК. У женщин контрольной группы забор крови для исследования производился однократно на 5-б-й день менструального цикла. Для исследования клеточных и макромолекулярных компонентов использовался электронно-микроскопический препарат концентрата клеток периферической крови. Изучали эритроциты, тромбоциты, гранулоциты, лимфоциты, моноциты и компоненты плазмы, находящиеся между клетками: ультрамикрофибриллы, ультрамикрогранулы, макромолекулярные комплексы, фрагменты клеток и атипичные компоненты. Исследуемую венозную кровь с гепарином отстаивали 15-20 мин, использовали верхний слой плазмы образовавшегося лейкоконцентрата. Собранную в конические пробирки плазму с клетками центрифугировали при скорости 1000 об/мин в течение 10 мин. Надосадочную жидкость удаляли, а к осадку приливали для префиксации клеток 1% раствор глутаральдегида на 0,1 М фосфатном буфере (рН 7,4) и центрифугировали в течение 10 мин, а затем 3 раза промывали в процессе центрифугирования в буферном растворе и дополнительно фиксировали 1% раствором четырехокиси осмия в 0,1 М фосфатном буфере (рН 7,4) в течение 30 мин. После окончания процедуры фиксации электронно-микроскопический препарат концентрата клеток крови готовился по обычной методике [2,3]. Ультратонкие срезы получали с помощью ультрамикротома LKB-V (Швеция), контрастировали уранил-ацетатом и цитратом свинца, анализировали и фотографировали на трансмиссионном электронном микроскопе JEM-100 СХ (Япония). Исследовали несколько ультратонких срезов каждого экспериментального варианта и параллельных препаратов, оценивали качественные и количественные ультраструктурные признаки клеток и клеточных популяций. Важно подчеркнуть, что приготовленные описанным способом электронно-микроскопические препараты структурных компонентов периферической крови позволяют изучать клетки в их естественной совокупности без предварительного повреждающего фракционирования, поскольку только электронная микроскопия дает возможность исследовать сколь угодно сложную структурную смесь. Кроме того, предварительная процедура обработки клеток крови, включающая осаждение и центрифугирование, как бы повторяет стадии ряда иммунологических тестов (например, реакции розеткообразования и т. п.), вследствие чего создаются условия для контактного взаимодействия клеток. Перечисленные условия способствуют выявлению наиболее полного разнообразия функциональных состояний клеток крови. В результате электронно-микроскопического исследования структурных компонентов крови у больных до начала ЭЛОК выявлено наличие остатков микроорганизмов между клетками крови, которые были, очевидно, в состоянии деструкции в результате действия иммунных механизмов (рис. 1, 2). Однако микроорганизмы находили и внутри клеток (лимфоцитах), но в спорообразном состоянии (наличие толстой оболочки). Наблюдался также фагоцитоз нейтрофилами фрагментов клеток, содержащих микроорганизм (рис. 3,4). Наряду с обнаружением микроорганизмов в крови были выявлены и признаки цитопатического эффекта, которые можно предположительно связать с вирусной инфекцией. Так, отмечались повреждения поверхностной мембраны эритроцитов в виде почкообразных выпячиваний, часто отрывающихся от клетки в окружающую плазму (рис. 5, 6). Вирусоподобные частицы также наблюдались в углубленнях эритроцитов (рис. 7). Цитопатический эффект в более ярком виде выявлялся при исследовании тромбоцитов: на их поверхности имелись тонкие короткие и длинные отростки, а рядом множество вирусоподобных частиц (рис. 8). В межклеточной плазме также находили скопления вирусоподобных частиц, разделенных и контактирующих между собой (рис. 9, 10). Среди клеток имелись сильно поврежденные клетки (цитолитическое состояние) или их крупные фрагменты, в которых можно было видеть множество вирусоподобных частиц, часто прилегающих к внутренней поверхности мембраны клеток. Подобная ультраструктурная картина периферической крови была выявлена и после курса ЭЛОК, но значительно чаще отмечалось присутствие бактерий и вирусоподобных частиц вне клеток, межклеточной плазме или во фрагментах разрушенных клеток. В межклеточной плазме обнаружены высокая контрацепция (плотность) неклеточных компонентов в виде макромолекулярных хлопьев и высокая активация тромбоцитов, нейтрофилов, лимфоцитов и моноцитов, которая выражалась в виде дегрануляции (высвобождении специфических гранул и лизосом), реакции фагоцитоза и синтеза иммуноглобулинов в развитой гранулярной эндоплазматической сети (активированные В-лимфоциты), а также в виде сильной контактной активности и особенно в местах нахождений бактерий и вирусоподобных частиц (рис. 11, 12). Таким образом, многофакторный электронно-микроскопический анализ структурных компонентов периферической крови у женщин с генитальным герпесом позволил получить определенное представление о лечебном эффекте ЭЛОК. Известно, что при лазерном облучении клеток крови in vitro отмечена высокая фоточувствительность эритроцитов, содержащих естественный пигмент гемоглобин и обладающих большой светопоглощающей способностью. Вместе с тем некоторые авторы показали, что лазерное облучение клеток крови, не вызывая повреждения эритроцитов человека, обусловливает повышение их резистентности, активацию функции мембраны клеток с изменением электрических и сорбционных свойств ее поверхности [5]. Воздействие на лимфоциты красным светом гелий-неонового лазера с длиной волны 0,63 нм оказывает стимулирующее влияние на их функциональную активность, активирует иммунокомпетентные клетки крови [9]. При морфологическом исследовании периферической крови наблюдается повышение содержания нейтрофилов, эозинофилов, базофилов, моноцитов [11]. Это связано со стимуляцией лейкопоэза, с выбросом зрелых клеток из синусов костного мозга, сосудов селезенки и легких. Основной точкой приложения действия лазерного гелий-неонового излучения в лимфоцитах являются поверхностная мембрана клетки с ее рецепторами и ядрышко, которые активизировались при лазерном воздействии. Есть также достаточные основания связать увеличение в крови числа нейтрофилов и моноцитов в состоянии сильно выраженной активации с высоким уровнем иммунных и антигенных комплексов, фрагментов клеточных рецепторов. В связи с этим, активацию нейтрофилов, моноцитов можно отнести к компенсаторным процессам, направленным на удаление из кровеносного русла в плазму разрушенных инфекционных агентов под воздействием гелий-неонового излучения. Никоэнергетическое лазерное облучение крови прежде всего вызывает разрушение поврежденных клеток с выходом бактерий и вирусов из клеток в межклеточную плазму, где они в свою очередь становятся доступными для иммунокомпетентных клеток и обезвреживаются в процессе фагоцитоза, действия специфических иммуноглобулинов с последующим контактным связыванием иммунных комплексов для нейтрализации инфекционных частиц. Такое представление подтверждается присутвием в периферической крови у пациенток высокоактивированных тромбоцитов, нейтрофилов, лимфоцитов и моноцитов на фоне высокой концентрации в плазме макромолекулярных компонентов. В плазме они подвергаются воздействию иммунокомпетентных клеток. Эти результаты согласуются с вирусологическими исследованиями, проведенными через 2-3 нед. после лазеротерапии. Выявлено незначительное увеличение экскреции вирусов. Кроме того, у 5 женщин в первую неделю после лазеротерапии отмечались легкие явления ОРЗ, что было расценено как активация элиминации вирусов слизистой оболочки верхних дыхательных путей. По результатам катамнеза и наблюдения пролеченных пациенток в течение 2-8 мес. выявлено увеличение продолжительности ремиссии на 5,4-1,1 мес. После повторного обследования в 72% случаев вирус простого герпеса не обнаружен. Таким образом, реакция крови, развивающаяся при лазерном облучении, является одной из важных составляющих клинического эффекта биостимуляционной лазерной терапии. Выявленные в настоящей работе ультраструктурные особенности состояния эритроцитов, тромбоцитов, нейтрофилов, моноцитов и неклеточных макромолекулярных компонентов периферической крови у женщин с генитальным герпесом, как нам представляется, дают более полную информацию для понимания влияния лазерного излучения на вирусную инфекцию. ЭЛОК может явиться методом выбора лечения больных с данной патологией. Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу. Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции
|



.png)