Вирусы использование в промышленности

Вирусы имеют важное значение для исследований в молекулярной и клеточной биологии, поскольку они представляют собой простые системы, которые можно использовать для управления и изучения функционирования клеток. Изучение и использование вирусов дало ценную информацию о различных аспектах клеточной биологии. К примеру, вирусы применялись в генетических исследованиях, и они помогли нам прийти к пониманию ключевых механизмов молекулярной генетики, как то: репликация ДНК, транскрипция, процессинг РНК, трансляция, транспорт белков.
Генетики зачастую используют вирусы как векторы для ввода генов в изучаемые клетки. Это даёт возможность заставить клетку производить чуждые вещества, и кроме этого изучить эффект от ввода нового гена в геном. Аналогично в виротерапии вирусы используют как векторы для лечения различных болезней, поскольку они избирательно действуют на клетки и ДНК. Это даёт надежды, что вирусы смогут помочь в борьбе с раком и найдут своё применение в генотерапии. Некоторое время восточноевропейские учёные прибегали к фаговой терапии как к альтернативе антибиотикам, и интерес к таким методам возрастает, поскольку сегодня у некоторых патогенных бактерий обнаружена высокая устойчивость к антибиотикам.
Биосинтез заражёнными клетками чужеродных белков лежит в основе некоторых современных промышленных способов получения белков, к примеру, антигенов. Не так давно промышленным способом были получены некоторые вирусные векторы и лекарственные белки, сегодня они проходят клинические и доклинические испытания.
Из-за своих размеров, формы и хорошо изученной химической структуры вирусы использовали как шаблоны для организации материалов на наноуровне. Примером такой недавней работы могут служить исследования, проведённые Исследовательской лабораторией Наваля в Вашингтоне (округ Колумбия) с использованием вируса мозаики коровьего гороха (англ. Cowpea Mosaic Virus (CPMV) ) для усиления сигналов в сенсорах с ДНК-микрочипами. В данном случае вирусные частицы разделяли частицы флуоресцентных красителей, которые использовались для передачи сигнала, предотвращая, таким образом, скопление нефлуоресцентных димеров, выступающих как гасители сигнала. Другим примером использования CPMV является применение его как наноразмерного образца для молекулярной электроники.
Многие вирусы могут быть получены de novo, то есть с нуля, а первый искусственный вирус был получен в 2002 году. Несмотря на некоторые неправильные трактовки, помимо этого синтезируется не сам вирус как таковой, а его геномная ДНК (в случае ДНК-вирусов) или комплементарная копия ДНК его генома (в случае РНК-вирусов). У вирусов многих семейств искусственная ДНК или РНК (последняя получается путём обратной транскрипции синтетической комплементарной ДНК), будучи введённой в клетку, проявляет инфекционные свойства. Иными словами, они содержат всю необходимую информацию для образования новых вирусов. Эту технологию в настоящее время используют для разработки вакцин нового типа. Возможность создавать искусственные вирусы имеет далеко идущие последствия, поскольку вирус не может вымереть, пока известна его геномная последовательность и имеются чувствительные к нему клетки. В наши дни полные геномные последовательности 2408 различных вирусов (в том числе оспы) находятся в публичном доступе в онлайн-базе данных, поддерживаемой Национальными институтами здравоохранения США.
Есть другая статья: Биологическое оружие
Способность вирусов вызывать опустошительные эпидемии среди людей порождает беспокойство, что вирусы могут использоваться как Биологическое оружие. Дополнительные опасения вызвало успешное воссоздание вредоносного вируса испанского гриппа в лаборатории. Другим примером может служить вирус оспы. Он на всём протяжении истории опустошал множество стран вплоть до его окончательного искоренения. Официально образцы вируса оспы хранятся лишь в двух местах в мире — в двух лабораториях в России и США. Опасения, что он может быть использован как оружие, не совсем беспочвенны; вакцина против оспы в некоторых случаях имеет тяжёлые побочные эффекты — в последние годы до официально объявленного искоренения вируса больше людей серьёзно заболели из-за вакцины, чем от вируса, поэтому вакцинация против оспы больше не практикуется повсеместно. По этой причине большая часть современного населения Земли практически не имеет устойчивости к оспе.
Природа создала множество биологических наноустройств и наномашин, элементы которых могут быть перепрограммированы для решения задач современной биологии и медицины. Одна из областей их применения – биофармацевтика. Молекулы белка, ДНК, РНК и их комплексы успешно применяются для конструирования терапевтических препаратов и вакцин. Это основа медицины будущего, которая будет базироваться на применении интеллектуальных лекарств, избирательно действующих на инфекционные агенты или на биополимеры, определяющие функционирование клеток человека
Широкое использование вирусов обусловлено их уникальным строением и образом жизни: они полностью инертны вне организма хозяина и не имеют клеточного строения. Структура их генома очень разнообразна: вирусы могут содержать одну или несколько молекул РНК или ДНК, которые могут принимать линейную, кольцевую или сегментированную форму.
Роль клеточного ядра, защищающего геном вируса, выполняет капсид, состоящий из структурных белков и ферментов. Более сложно организованные вирусные частицы могут иметь дополнительные оболочки – суперкапсиды. Эти липопротеидные структуры включают в себя гликопротеины – белки, взаимодействующие с поверхностными клеточными рецепторами, что обеспечивает проникновение вирусов внутрь заражаемой клетки. Вирус может содержать более одного типа гликопротеинов, например, у вируса гриппа их два: гемагглютинины и нейраминидаза.
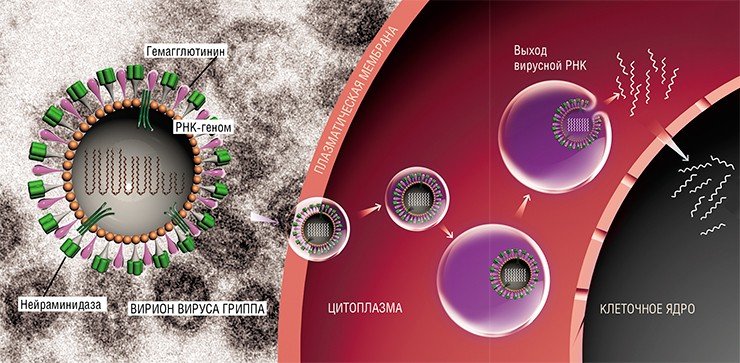
Природные наноконтейнеры
Так возникла идея решить эту проблему с помощью виросом – вирусных частиц, освобожденных от генетического материала, но содержащих поверхностные гликопротеины. Подобные частицы обладают важным свойством: сохраняют способность избирательно связываться с определенными клетками, доставляя в них свое содержимое.
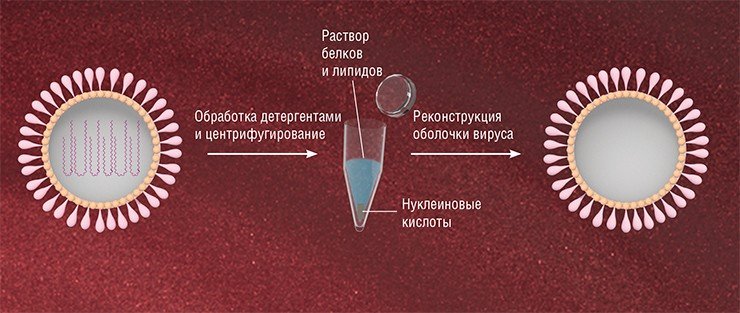
Возможность доставки лекарственных средств с помощью виросом была показана на примере подавления синтеза белков вируса гепатита С в организме животных. В виросомы, сделанные на основе вируса Сендай, заключили короткие шпилечные РНК, способные ингибировать наработку белка вируса гепатита С в зараженных клетках. В результате внутривенного введения такого препарата удалось эффективно снизить количество исследуемого вирусного белка в клетках печени больных мышей (Subramanian et. al., 2009).
Безопасные вакцины
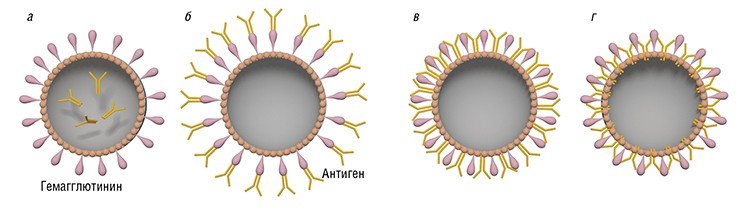
Виросомы могут применяться в качестве вакцин не только против вирусов, но и других патогенов. Так, у мышей происходит наработка антител против возбудителя малярии после введения им виросом на основе вируса гриппа, несущих на поверхности синтетические пептиды, соответствующие фрагментам белков плазмодия (Okitsu et al., 2008). Эффективные вакцинирующие препараты были разработаны на основе виросом, содержащих дифтерийный и столбнячный токсины. Сравнение действия таких препаратов и анатоксинов (токсинов, вызывающих иммунный ответ, но не проявляющих токсикологических свойств и служащих традиционными вакцинами против дифтерии и столбняка) показало, что в первом случае антитела нарабатываются более эффективно (Zubrrigen & Gluck, 1999).
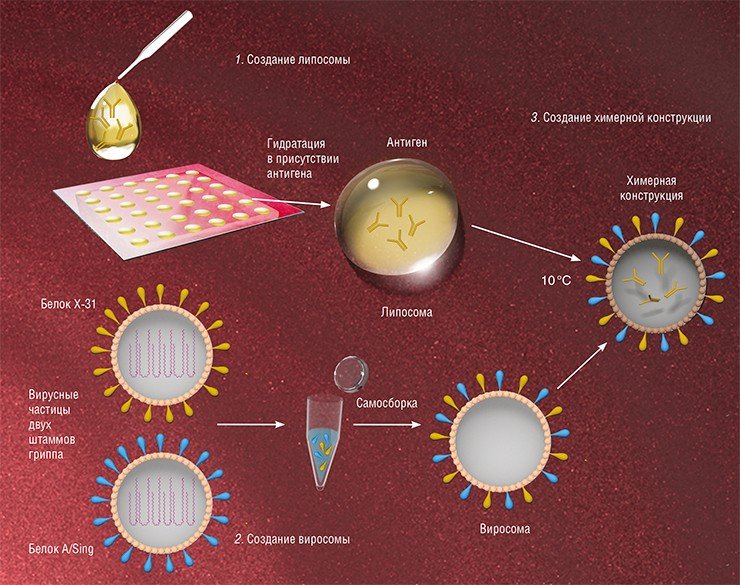
Виросомы можно использовать и для иммунотерапии онкологических заболеваний – доставки в опухоль ассоциированных с раком антигенов в виде плазмидной ДНК или коротких пептидов. Такие виросомы способны активировать клетки иммунной системы даже более эффективно, чем антиген в нативном виде. В экспериментах на животных было показано, что антиген, специфичный для клеток меланомы Melan-A, доставляемый в виросомах на основе вируса гриппа, успешно проникает в плазматические дендритные клетки иммунной системы (популяция антигенпрезентирующих клеток крови). В результате происходит более эффективная активация Т-клеток, способных уничтожить раковые клетки, чем при введении свободного пептида. Этот эффект, по-видимому, обусловлен хорошей защищенностью антигена, находящегося в виросомах (Angel et al., 2007).
Использование виросом в терапии болезней человека и животных имеет существенные достоинства, главные из которых – нетоксичность и совместимость с большинством лекарственных средств. Кроме того, липидная оболочка обеспечивает надежную защиту заключенного в виросомах материала от преждевременной деградации. С помощью виросом-опосредованной терапии уже удалось добиться весьма многообещающих результатов. Некоторые созданные на их основе препараты, в основном вакцины, находятся на разных стадиях доклинических и клинических испытаний. К их числу относятся интраназальные вакцины против вируса гриппа, вакцина против РСВ-вируса, ВИЧ-инфекции.
Примером коммерчески доступных виросомных вакцин является препарат Инфлексал производства Швейцарии, который представляет собой виросомы, содержащие антигены против вирусов гриппа типов А и В. В последнее десятилетие именно Швейцария занимает лидирующие позиции по числу средств, вкладываемых в исследование и разработку препаратов на основе виросом.
На сегодняшний день в мире можно выделить несколько групп, занимающихся доставкой терапевтических нуклеиновых кислот, в том числе и малых интерферирующих РНК (siRNA), в клетки млекопитающих с помощью вирососм (de Jonge et al., 2006). Основные затруднения, с которыми приходится сталкиваться при приготовлении таких виросомных препаратов, связаны с эффективностью включения препарата в состав виросом, а также адресной доставкой в определенные типы клеток. Сегодня в Институте химической биологии и фундаментальной медицины СО РАН (Новосибирск) ведутся работы по получению виросом стандартного качества со стабильными свойствами, в том числе обладающих способностью к адресной доставке терапевтических нуклеиновых кислот. Уже разработаны методы включения этих макромолекул в оболочки вируса (Власов и др., 1988, 1989). В дальнейшем планируется создать виросомные препараты, содержащие терапевтические нуклеиновые кислоты, и оценить их воздействие на различные типы раковых клеток человека.
Власов В. В., Иванова Е. М., Кренделев Ю. Д. и др. Оболочки вируса Сендай и тени эритроцитов – мембранные переносчики для введения реакционноспособных производных олигонуклеотидов в клетки // Биополимеры и клетка. 1989. Т. 5. № 4. Р. 52—58.
Власов В. В., Кренделев Ю. Д., Овандер М. Н. и др. Эффективный метод включения ДНК в реконструированные оболочки вируса Сендай // Биополимеры и клетка. 1988. Т. 4. № 5. Р. 250—254.
Шамшева О. В., Ртищев А. Ю.. Ультрикс – отечественная вакцина нового поколения // Педиатрия. 2014. Т. 93. № 6. P. 121—124.
Angel J., Chaperot L., Molens J. et al. Virosome-mediated delivery of tumor antigen to plasmacytoid dendritic cells // Vaccine. 2007. V. 25. P. 3913—3921.
de Jonge J., Holtrop M., Wilschut J. et al. Reconstituted influenza virus envelopes as an efficient carrier system for cellular delivery of small-interfering RNAs // Gene Therapy. 2006. V. 13. P. 400—411.
Okitsu S. L., Mueller M. S., Amacker M. et al. Preclinical profiling of the immunogenicity of a two-component subunit malaria vaccine candidate based on virosome technology // Human Vaccines. 2008. V. 4 N. 2. Р. 106—114.

Недалёкое будущее. Высшее руководство одной из крупнейших стран мира собралось на экстренное совещание. Высокопоставленные чиновники заметно встревожены: группа террористов захватила на одной из военных баз новейшее оружие – настолько секретное, что даже первые лица страны называют его только кодовым обозначением.
Как выяснилось, эта жидкость содержит опасный вирус, способный за считанные часы уничтожить половину человечества. К бойцам подбегают люди в специальных защитных скафандрах – учёные-вирусологи.
Они забирают опасный груз, тщательно укладывают его в металлические контейнеры и увозят для деактивации в недрах своих зашифрованных лабораторий.
Ещё одна трактовка: вирусы – внутриклеточные паразиты, которые не могут сами ничего синтезировать, и имеют, в зависимости от семейства, различные системы репликации и транскрипции. И это далеко не полный спектр определений, предложенных учёными для вируса.
Почему же для такого крошечного и, казалось бы, такого простого объекта не существует единого универсального определения? Наверное, потому, что вирус до сих пор остается одной из самых больших загадок для исследователей.
Вирусы присутствуют как зависимые паразиты в любой форме земной жизни – в бактериях, археях, простейших, растениях, грибах и животных. Несмотря на то, что они более чем доступны для исследования, учёные до сих пор спорят даже об их роли в эволюции.

Например, существует теория о том, что вирусы участвовали в появлении клеточного ядра и других компонентов эукариотической клетки. А вот эволюционное влияние вирусов на живые организмы на более поздних этапах эволюции уже доказано.
Есть основания предполагать, что интеграция генома ретровирусов в ДНК предка человека вблизи гена PRODH сыграла важную роль в развитии умственных способностей homo sapiens. Кроме того, вирусы являются важным природным средством обмена генетической информации между разными видами, что приводит к появлению генетическое разнообразие и направляет эволюцию.
Они играют определяющую роль в регуляции численности популяций некоторых видов живых организмов. В некоторых случаях вирусы образуют со своими хозяевами симбиоз. Вирусы имеют генетические связи с представителями флоры и фауны Земли.
Согласно последним исследованиям, геном человека более чем на 32% состоит из вирусоподобных элементов и транспозонов. Так, в геноме высших приматов существует ген, кодирующий белок синцитин, который считают, был привнесен ретровирусом.
На данный момент вирусы являются одним из крупнейших живых хранилищ неисследованного генетического разнообразия на Земле.
Таким образом, вирусы были и остаются важнейшей составляющей земной жизни на всех этапах эволюции. Однако, человечество начало изучать этот удивительный инфекционный агент совсем недавно. Более того – о самом факте его существования учёные узнали чуть больше века назад, хотя представления о заразности таких болезней, как оспа, корь и многих других, зародились еще у древних народов. Конечно, эти отрывочные наблюдения и догадки были очень далеки от настоящих научных знаний, и к концу XVIII века понимание природы инфекций было относительно примитивным.

Дмитрий Иосифович Ивановский
(1864-1920)
Настоящая революция в изучении вирусов произошла в 1892 г., когда выдающийся естествоиспытатель Дмитрий Иосифович Ивановский отправился в командировку на юг Украины для изучения мозаичной болезни табака. Исследуя эту болезнь, которая наносила огромный ущерб табачным плантациям, молодой учёный обнаружил, что возбудитель этой болезни проходит сквозь бактериальные фильтры.
После Ивановского и Бейеринка открытия совершались одно за другим. В 1898 г. Леффлер и Фрош открыли первый вирус животных – вирус ящура, а Род и Кэрролл в 1901-1902 гг. – первый вирус человека (вирус жёлтой лихорадки).
В том же 1902 г. были открыты вирусы чумы крупного рогатого скота, оспы коз, оспы овец; в 1905 г. – вирусы чумы собак, оспы коров; в 1907 г. – вирус натуральной оспы, вирус денге; в 1908 г. – вирусы полиомиелита, лейкоза кур и др.
И хотя царство вирусов было открыто ещё в конце XIX в., их глубокое изучение стало возможным лишь во второй половине XX века после изобретения электронного микроскопа и адекватных моделей для культивирования.

Мартин Бейеринк (1851—1931)
В настоящее время вирусологию определяют как медико-биологическую науку, изучающую вирусы и субвирусные агенты (вироиды, сателлиты и прионы): их строение, генетику, систематику, эволюцию, их способы заражать и эксплуатировать клетку-хозяина для размножения, их взаимодействие с иммунитетом организма-хозяина, болезни, которые они вызывают, методы их выделения и культивирования, а также использование вирусов в научных исследованиях и терапии.
Вирусы могут быть классифицированы в соответствии с теми хозяевами, которых они поражают: вирусы животных, вирусы растений, вирусы бактерий и др.
Наиболее распространённой является классификация вирусов в соответствии с типом их генетического материала и способа размножения (репликации) в клетке-хозяине. Классификация вирусов обновляется каждые пять лет по решению Международного комитета по таксономии вирусов (МКТВ).
Этот комитет предлагает классифицировать все известные вирусы по четырём иерархическими уровнями: вид, род, семья (иногда подсемейство) и порядок. Сейчас реестр классифицированных вирусов и вироидов включает 3704 вида, входящих в состав 609 родов, 27 подсемейств, 111 семей и 7 порядков.
Основной причиной изучения вирусов является их реальная угроза для человечества. Вирусы являются причиной острых массовых инфекций, на их долю приходится 90% всех инфекционных заболеваний.
Только от острых кишечных и респираторных вирусных инфекций в мире погибает 10-14 млн. человек. Кроме того, вирусы могут быть причиной развития злокачественных заболеваний и вызвать обострение хронических болезней.
Сегодня известно более 2 тысяч различных болезней человека, спектр которых постоянно пополняется за счёт ранее неизвестных: вирусные лихорадки Ласса, Эбола, Марбург, Зика, ВИЧ-инфекция, ряд вирусных кишечных болезней, вирусные гепатиты C, D, E и G, хантавирусная легочный синдром, ТОРС-коронавирус, болезни нервной системы, вызванные прионами.
Одновременно расширение спектра вирусных болезней происходит за счёт установления природы заболеваний, которые ранее считались неинфекционными (хронические гепатиты, лимфома Беркитта, саркома Капоши, Т-клеточные лейкозы и другие опухоли). Некоторые вирусные варианты онкопатологий так же отнесли к инфекционным болезням.
Давно обсуждается вопрос об инфекционной природе некоторых психических расстройств. Сегодня доказано, что в структуре причин самоубийств определённое место занимает инфекционный фактор – вирус Борна.
Также определена вирусная природа многих аутоиммунных (рассеянный склероз, сахарный диабет I типа) и аллергических (сенная лихорадка) болезней человека и животных.
Не менее 300 известных вирусов способны вызывать пандемии (грипп А, оспа, ВИЧ-инфекция, полиомиелит), эпидемии (лихорадка денге, жёлтая лихорадка, Западного Нила, Эбола, Зика), эпидемические вспышки (гепатит Е, вирус Нипа и др.) и спорадические заболевания.
Вирусы имеют большое значение для исследований в молекулярной и клеточной биологии. Поскольку они являются простыми системами, их используют для управления и изучения функционирования клеток.
Например, вирусы применяются в генетических исследованиях. Именно благодаря изучению вирусов были описаны ключевые механизмы молекулярной генетики, такие как: репликация ДНК, транскрипция, процессинг РНК, трансляция, транспорт белков, функционирования рибозимов.
Вирусы могут быть использованы как векторы для введения нужных генов в исследуемые клетки. Это дает возможность заставить клетку производить необходимые чужеродные вещества и изучать последствия введения нового гена в геном. Весьма вероятно, что вирусы найдут широкое применение в генотерапии.
Кроме того, вирусы используют с диагностической целью, для лечения бактериальных болезней, для борьбы с насекомыми-вредителями, и даже для регуляции численности популяции нежелательных животных (например – ограничение численности кроликов в Австралии).
Многие вирусы могут быть получены de novo, то есть с нуля. Первый искусственный вирус был получен в 2002 году.
Сегодня в свободном доступе в специализированных онлайновых базах данных опубликованы полные геномные последовательности 2408 различных вирусов (в том числе вируса натуральной оспы).
Вирусы являются самой распространенной формой существования органической материи на планете, оказывающей огромное влияние на другие формы жизни. Включая так называемых Homo sapiens, т.е. нас с вами. Их изучение и использование в интересах человечества – одна из важнейших задач для учёных.
В Украине развитие вирусологической науки исторически связано с Киевским национальным университетом. Так сложилось, что вот уже более 100 лет, наше учебное заведение занимает лидирующие позиции в этой области науки.
В 1962 г. в Киевском государственном университете имени Т. Г. Шевченко была открыта первая во всем СССР кафедра вирусологии, которая начала подготовку специалистов-вирусологов.
Организатором и первым заведующим кафедрой вирусологии была известный вирусолог и эпидемиолог, профессор, доктор медицинских наук Нина Петровна Корнюшенко. С декабря 2003 кафедру возглавляет профессор, доктор биологических наук, академик Высшей школы Украины, лауреат премии Украины в области науки и техники, премии НАНУ имени Д.К. Заболотного – Валерий Петрович Полищук.
Студенты, специализирующиеся на кафедре, получают основательную теоретическую и практическую подготовку по целому ряду научных направлений современной вирусологической науки, включая фитовирусологию, бактериофагию, медицинскую и ветеринарную вирусологию.
- 16130
- 9,3
- 2
- 4
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Строение вирусов и иммунный ответ организма

Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).

Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].

Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).

Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.

Рисунок 5. Схема развития феномена ADE при вирусных инфекциях. а — Взаимодействие между антителом и рецептором FcR на поверхности макрофага. б — Фрагмент С3 комплемента (компонент комплемента, после присоединения которого весь этот комплекс приобретает способность прилипать к различным частицам и клеткам) и рецептор комплемента (complement receptor, CR) способствуют присоединению вируса к клетке. в — Белки комплемента С1q и С1qR способствуют присоединению вируса к клетке (в составе молекулы C1q имеется рецептор для связывания с Fc-фрагментом молекулы антитела). г — Антитела взаимодействуют с рецептор-связывающим сайтом вирусного белка и индуцируют его конформационные изменения, облегчающие слияние вируса с мембраной. д — Вирусы, получившие возможность реплицироваться в данной клетке посредством ADE, супрессируют противовирусные ответы со стороны антивирусных генов клетки. Рисунок с сайта supotnitskiy.ru.
Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.

Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.

Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.

Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.
Читайте также:


