Вирус папилломы человека рак полости рта
Исследователь Онкологического центра им. Киммела при Университете Джонса Хопкинса (Johns Hopkins Kimmel Cancer Center) в своих двух исследованиях сообщила о необходимости изучения более широкого использования вакцин против ВПЧ (вируса папилломы человека) и утверждения простого орального скрининг-теста для выявления рака ротовой полости, причиной которого является ВПЧ.
В отчете CDC, который считается первой и наиболее полной оценкой данных о заболеваемости раком вследствие инфицирования ВПЧ в Соединенных Штатах, исследователи проанализировали зафиксированные случаи возникновения рака в период с 1998 по 2003 годы и пришли к заключению, что ежегодно в центрах по изучению рака было выявлено 25 000 случаев этого заболевания, связанных с инфекцией ВПЧ. В результате проведения дополнительных исследований Джиллисон и ее коллеги из Национального института по изучению раковых заболеваний (National Cancer Institute) установили, что инфекция ВПЧ является основной причиной примерно 20 000 из этих случаев заболевания раком.
Джиллисон и ее команда обнаружили, что каждый год в США примерно в 20 000 случаев заболевания раком его причиной является инфекция ВПЧ. Рак ротовой полости является вторым наиболее распространенным видом рака, связанным с ВПЧ. В Соединенных Штатах этот вид раковой опухоли получает все большее распространение, в особенности среди мужчин. Добавьте к этому количество случаев возникновения рака заднего прохода, мужских половых органов, вагинальной области и женских наружных половых органов, которые также связаны с инфекцией ВПЧ, и, по словам доктора Джиллисон, в комбинации эти показатели будут равны количеству заболеваний раком шейки матки, который является наиболее распространенным и известным видом рака, причиной которого является ВПЧ.
Сведения, полученные Джиллисон, были частью проекта, получившего название ABHACUS (Assessing the Burden of Human Papillomavirus-Associated Cancers - оценка тяжести рака, связанного с вирусом папилломы человека). Во время исследований были использованы данные, полученные в результате проведения Национальной программы по выявлению раковых заболеваний (National Program of Cancer Registries), а также Программы по наблюдению, проведению эпидемиологии и обработке конечных результатов Национального института по изучению раковых заболеваний (National Cancer Institute's Surveillance, Epidemiology, and End Results). Эти программы проводились при поддержке Центров по контролю над заболеваниями и их предотвращению. Более 80 исследователей по всей стране приняли участие в этом проекте, который изучил многие вопросы, связанные с заболеванием раком, причиной которого является ВПЧ, включая расовое неравенство, влияние экономики, поведенческие факторы риска и смертность от злокачественных опухолей.
Помимо предупреждения, обнаружение рака на ранней стадии считается экспертами в области заболевания раком наилучшим способом контроля за этим заболеванием.
Во время проведения Клинических исследований раковых опухолей (Clinical Cancer Research), которые являются первой попыткой проанализировать саму болезнь и связанные с ней оральные инфекции в течение длительного периода, Джиллисон обнаружила, что обычные средства для полоскания полости рта со временем способны успешно содействовать выявлению инфекции ВПЧ ротовой полости. Эта информация открывает двери для использования потенциального бесконтактного скрининг-тестирования с целью обнаружения заболевания и наблюдения за повторным появлением опухоли. Злокачественные опухоли головы и шеи включают в себя несколько видов рака: рак ротовой полости, включая миндалевидную железу, основание языка, а также боковые и заднюю стенки гортани.
В ходе исследований было установлено, что полоскание полости рта позволило успешно выявить ВПЧ-инфекции с высокой степенью риска у пациентов с ВПЧ 16-положительными видами рака головы и шеи вплоть до пяти лет после прохождения курса лечения. Джиллисон утверждает, что полученные данные свидетельствуют о высоком уровне постоянной инфекции и вновь подтверждают наличие связи между ВПЧ с высокой степенью риска и ВПЧ-положительными видами рака головы и шеи.
В этом исследовании специалисты использовали средства для полоскания для сбора клеток из внутренней поверхности ротовой полости у 135 пациентов с раком головы и шеи. Исследователи выстроили генетическую последовательность ДНК, полученных из средств для полосканий, и образцов опухоли для определения рака, вызванного ВПЧ, и установления типа ВПЧ. Существуют около 120 типов ВПЧ, но ВПЧ 16 является одним из двух типов, который наиболее часто связан с раковой опухолью.
В ходе анализа было выявлено 44 пациента с опухолями, возникшими из-за ВПЧ 16 (HPV 16). Было также установлено, что эти пациенты, скорее всего, могли иметь длительную инфекцию ВПЧ 16 (HPV 16) как до лечения рака, так и после него. Несмотря на то, что это исследование не установило связь продолжающихся инфекций после окончания курса лечения с повторным появлением опухоли, было отмечено, что у пациентов с ВПЧ-инфекциями ротовой полости высокой степени (high-risk oral HPV) риска до прохождения терапии был выявлен высокий уровень содержания этой инфекции после ее завершения. Группа ученых планирует продолжать дальнейшие долгосрочные исследования для выяснения, способна ли такая продолжительная инфекция стать причиной повторного возникновения раковой опухоли.
В 2000 году Джиллисон определила ВПЧ-положительный (HPV-positive) рак головы и шеи как отдельный подтип заболевания и связала его с возможностью увеличения уровня выживаемости.
В число ученых, принявших участие в исследовании, входят Юрий Агравал (Yuri Agrawal), Уэйн Кох (Wayne M. Koch), Уэйхонг Ксиао (Weihong Xiao), Уильям Вестра (William H. Westra), Анна Трайветт (Anna L. Trivett) и Дэвид Саймер (David E. Symer).
Исследования проводились при финансовой поддержке Фонда раковых заболеваний ротовой полости (Oral Cancer Foundation), Национального исследовательского института в области стоматологии и черепно-лицевой хирургии (National Institute of Dental and Craniofacial Research) и Национального института по изучению раковых заболеваний (National Cancer Institute).
Перевод Натальи Болотиной
27.11.2008 г.
г. Смоленск, ул. Фрунзе, 74. ул. Фрунзе, 40.















Некоторые факты о раке полости рта
ПАМЯТКА
НЕКОТОРЫЕ ФАКТЫ О РАКЕ ПОЛОСТИ РТА
Что такое рак полости рта?
Рак полости рта – это атипичное разрастание клеток в тканях ротовой полости. Такие процессы могут затрагивать губы, язык, ротоглотку. Существует два вида ракового поражения ротовой полости:
· рак, развивающийся непосредственно во рту, на слизистой оболочке щек, неба, языка, десен и губ (называемый раком полости рта и губ);
· рак, развивающийся в глубине ротовой полости в области миндалин, именуемый раком ротоглотки.
Каковы факторы риска развития рака полости рта?
Среди факторов, провоцирующих развитие рака полости рта, современная онкология первое место отводит канцерогенам, образующимся при сгорании табака. Алкоголь потенциирует действие канцерогенов табачного дыма и в 2 раза увеличивает вероятность развития рака полости рта у курильщика.
Раннее диагностированный рак полости рта, наследственная предрасположенность (наличие онкологического заболевания ротовой полости в роду) и возраст старше 40 лет также сильно увеличивают риск развития рака ротовой полости. Носительство Вируса Папилломы Человека, (вируса, вызывающего рак шейки матки у женщин) известного как ВПЧ (HPV) 16 является серьезным фактором риска развития онкологического поражения ротовой полости, также как и носительство Вируса простого герпеса (HSV-1). Еще одним фактором риска является кандидоз, а также солнечный свет (ультрафиолет). 25% пациентов имеющих рак ротовой полости не имели ни одного фактора риска развития онкологического заболевания.
Каков коэффициент выживаемости от рака полости рта?
Коэффициент выживаемости от рака полости рта удручающий, если он выявлен на запущенных стадиях. Ежегодно от рака ротовой полости умирает около 13000 человек в России, и лишь малая часть больных проживает пятилетний период.
Какие виды лечения рака полости рта существуют?
Раннее выявление рака ротовой полости может в значительной степени влиять на выбор того или иного метода лечения. Лечение рака ротовой полости на ранней стадии обычно заключается в хирургическом удалении пораженных тканей. Если участок, пораженный опухолью уже велик, то хирургическим путем могут быть удалены большая доля языка, нижней челюсти или глотки. Когда рак дает метастазы или распространяется на прочие органы пациента, лечащий врач может назначить проведение курса химиотерапии или облучения в дополнение к хирургической резекции пораженных тканей
Профилактика рака полости рта
Профилактика в отношении рака полости рта состоит в отказе от таких вредных привычек, как курение и прием алкоголя; регулярной профессиональной гигиене полости рта. При проведении осмотра полости рта стоматолог должен внимательно отнестись к любым изменениям со стороны слизистой полости рта и своевременно направить пациента на консультацию онколога.
ЖАЛОБЫ
1. Наличие длительно незаживающей язвы во рту,
2. Непроходящая боль в полости рта,
3. Припухлость или утолщение щеки,
4. Белые или красные пятна на деснах, языке, миндалинах или слизистой оболочке полости рта,
5. Ощущение инородного тела при глотании,
6. Затруднение жевания или глотания,
7. Затруднение движения челюстью или языком,
8. Онемение языка,
9. Появление припухлости на шее.
ВАЖНО ПОМНИТЬ!
Заключительный диагноз, на основании которого определяется тактика лечения, имеет право ставить только онколог, работающий в специализированном медицинском учреждении. Не доверяйте мнению знакомых, родственников, случайных людей, это ведет к потере времени, постановке неправильного диагноза и, в конечном итоге, к неутешительным результатам лечения.
Это информация поможет узнать, что такое вирус папилломы человека и как он может вызывать рак головы и шеи.
Что такое вирус папилломы человека?
Вирус папилломы человека (Human Papilloma Virus (HPV)) — это вирус, который может инфицировать кожу и слизистую оболочку рта, горла, гениталий и анальной области. Инфицирование HPV широко распространено. У большинства людей с HPV не возникает никаких симптомов, а их иммунная система избавляется от вируса без какого-либо лечения. В некоторых случаях HPV может приводить к раку. Мы не знаем, почему одним людям удается избавиться от HPV до того, как он вызовет рак, а другим нет.
Существуют ли разные типы HPV?
Да, существуют разные типы HPV. Некоторые типы этого вируса приводят к росту бородавок на коже, во рту или на гениталиях. Другие типы могут приводить к раку. Их называют типами высокого риска. HPV высокого риска может вызывать различные виды рака, включая рак шейки матки и наружных половых органов у женщин, полового члена у мужчин, а также анального отверстия. Самым распространенным видом является рак шейки матки. Именно поэтому у женщин берут мазок из шейки матки (также называемый мазком Папаниколау для проверки на рак шейки матки), который включает и проверку на наличие HPV.
HPV высокого риска также может вызывать раку головы и шеи у мужчин и женщин.
Как люди заражаются HPV?
HPV может попасть в ваш организм при контакте вашей кожи или слизистой оболочки с кожей или слизистой оболочкой зараженного человека. Обычно это происходит во время вагинального, анального или орального секса с человеком, у которого есть вирус. Поскольку HPV столь широко распространен, сложно установить, когда инфекция попала в организм и кто ее передал. Более того, первые симптомы HPV могут появиться у вас через несколько лет после секса с зараженным человеком. По этой причине сложно выяснить, когда вы были заражены впервые.
Заразен(-на) ли я?
HPV не передается при физическом контакте (например, при касании и поцелуе в щеку или губы), однако вы можете заразиться HPV во время вагинального, анального и орального секса. Это означает, что если у вас есть HPV, то у ваших сексуальных партнеров также может быть этот вирус. Поскольку большинство людей избавляется от инфекции самостоятельно, вероятность того, что у вашего партнера будет рак, вызванный HPV, очень мала даже при заражении типом высокого риска. Если у вас обнаружили рак, вызванный HPV, вам не требуется каким-либо образом менять свое сексуальное поведение.
Можно ли вылечить HPV?
В настоящее время лекарства от HPV не существует. Большинство людей, инфицированных HPV, избавляется от вируса без какого-либо лечения.
Следует ли моему партнеру сделать анализ на HPV?
- Женщинам следует придерживаться обычных рекомендаций, касающихся женского здоровья, в число которых входит регулярное взятие мазка из шейки матки.
- Мужчинам не требуется проходить какие-либо специальные осмотры или исследования, поскольку для них не предусмотрены никакие регулярные или стандартные анализы на HPV.
Вероятность развития у вашего партнера рака, вызванного HPV, очень мала. При наличии симптомов или обеспокоенности вашему партнеру следует обсудить это со своим врачом.
Что я могу сделать, чтобы не заразиться HPV и не заразить им другого человека?
Презервативы и коффердамы (тонкий, прямоугольный лист из латекса или силикона, который закрывает гениталии женщины, получающей оральный секс) не так эффективны против HPV, как против других инфекций, передаваемых половым путем (sexually transmitted infections (STIs)), например хламидии и вируса иммунодефицита человека (HIV), однако их использование позволяет снизить вероятность передачи HPV. Всегда используйте презервативы или коффердамы во время вагинального, анального или орального секса.
Вам также следует пройти вакцинацию против HPV и посоветовать своему партнеру сделать то же самое.
Следует ли мне пройти вакцинацию против HPV?
Любой человек в возрасте от 9 до 26 лет может пройти вакцинацию против HPV для защиты от генитальных бородавок и различных типов HPV, способных вызывать рак. Детям рекомендуется проходить вакцинацию в возрасте 11–12 лет, чтобы они были защищены за несколько лет до начала половой жизни.
Обычно эту вакцину не делают людям старше 26 лет. Однако, вне зависимости от вашего возраста, поговорите со своим врачом, чтобы узнать, может ли вакцина против HPV принести вам пользу.
Если я уже заражен(-а) HPV, смогу ли я вылечиться с помощью вакцины?
Если вы уже заражены HPV, вакцинация не поможет вам вылечиться, но она сможет защитить вас от других типов HPV.
Если вы инфицированы HPV, поговорите со своим врачом или медсестрой/медбратом, чтобы узнать, какие исследования или какое лечение вам необходимо.
Каким образом HPV вызывает раковые образования головы и шеи?
Мы не знаем наверняка, каким образом HPV вызывает раковые образования головы и шеи. У большинства людей с HPV высокого риска не будет рака. Однако некоторым людям не удается избавиться от HPV. В этом случае вирус способен вызвать повреждения, которые в конченом счете станут причиной развития опухоли. Зачастую процесс превращения инфицированных HPV клеток в раковые клетки занимает долгие годы. Невозможно предсказать, у кого инфекция исчезнет из организма, а у кого будет развиваться рак. Большинство видов раковых образований головы и шеи, вызванных HPV, формируются в той части горла, где находятся корень языка и миндалины.
Как я могу узнать, стал ли HPV причиной моей раковой опухоли?
В ходе диагностики рака головы и шеи возможна проверка опухоли на наличие HPV. В настоящее время это единственный способ узнать, вызван ли рак HPV.
Может ли у меня развиться рак другого вида из-за HPV?
Риск развития второго вида рака из-за HPV невелик, однако ваш врач будет и впредь регулярно осматривать вас. Обязательно сообщайте врачу обо всех новых симптомах и беспокойствах.
Влияет ли наличие HPV на мое лечение или на мои шансы излечиться?
Люди, у которых рак головы и шеи вызван HPV, лучше реагируют на лечение, чем люди, у которых HPV не является причиной раковых образований головы и шеи. Тем не менее, оба вида рака лечатся одинаково. Связанные с лечением решения принимаются на основании размера и местоположения опухоли, стадии заболевания и общего состояния здоровья человека. В настоящее время ученые исследуют вопрос, следует ли вносить изменения в лечение рака, если он связан с HPV.
А как насчет табака и алкоголя?
Вероятность развития рака головы и шеи выше у курящих людей и людей, злоупотребляющих алкоголем. Однако виды рака, вызываемые HPV, могут развиваться вне зависимости от того, пьете ли вы алкоголь и используете ли табакосодержащие продукты. Продолжительность жизни больных раком, некурящих и непьющих алкоголь людей больше, а вероятность развития у них новых видов рака меньше. По этой причине людям с раком головы и шеи следует бросить курить и ограничить употребление алкоголя. Если вам необходима помощь в отказе от этих привычек, вам могут помочь в центре MSK. Попросите дополнительную информацию о наших программах у своего врача или медсестры/медбрата, либо позвоните в Центр по предоставлению консультаций (Counseling Center) по номеру 646-888-0200.
Ресурсы
В Интернете можно найти много информации о HPV и раке, но иногда она противоречива и недостоверна. Мы рекомендуем обращаться за дополнительной информацией в следующие организации:
Что такое рак полости рта?
Рак ротовой полости – это атипичное разрастание клеток в тканях ротовой полости. Такие процессы могут затрагивать губы, язык, ротоглотку.
Существует два вида ракового поражения ротовой полости: рак, развивающийся непосредственно во рту, на слизистой оболочке щек, неба, языка, десен и губ(называемый раком полости рта и губ), и рак, развивающийся в глубине ротовой полости в области миндалин, именуемый раком ротоглотки.
Насколько распространен рак ротовой полости?
Согласно статистике раком ротовой полости ежегодно заболевают 13500 жителей России.
Каковы факторы риска развития рака ротовой полости?
Табакокурение в любом виде, жевание табака и систематическое употребление алкоголя – вот наиболее значимые факторы риска развития рака ротовой полости.
Раннее леченный рак ротовой полости, наследственная предрасположенность (наличие онкологического заболевания ротовой полости в роду) и возраст старше 40 лет также сильно увеличивают риск развития рака ротовой полости.
Носительство Вируса Папилломы Человека, (вируса, вызывающего рак шейки матки у женщин) известного как ВПЧ (HPV) 16 является серьезным фактором риска развития онкологического поражения ротовой полости, также как и носительство Вируса простого герпеса (HSV-1).
Еще одним фактором риска является кандидоз, а также солнечный свет. (Ультрафиолетовое излучение по результатам исследований вызывает рак красной каймы губ).
Но. 25% пациентов имеющих рак ротовой полости не имели ни одного (!) фактора риска развития онкологического заболевания.
Возможные факторы риска развития рака слизистой оболочки полости рта
Раздражение и высыпания вокруг губ
Некоторых беспокоит, что длительные раздражения подобного рода могут привести к развитию раковой опухоли. В частности, не должным образом подогнанные зубные протезы могут вызвать раздражение слизистой. Необходимо проходить профилактический осмотр у стоматолога, как минимум, 1 раз в год.
Гигиена полости рта
Исследования доказывают, что люди, редко посещающие стоматолога и чистящие зубы не более одного раза в день, подвергаются большему риску заболевания раком слизистой оболочки полости рта.
Семейная история заболевания
Предполагают, что большему риску подвергаются те, у кого есть близкий родственник с подобным заболеванием.
Шаги, которые помогут вам предотвратить появление и развитие рака ротовой полости:
Не курите и не используйте какие-либо табачные изделия (нюхательный или жевательный табак), не злоупотребляйте алкоголем.
Питайтесь по хорошо сбалансированной диете.
Ограничьте пребывание на солнце. Чрезмерное пребывание на солнце повышает риск развитие рака нижней губы. Используйте солнцезащитные крема и бальзамы для губ.
Кроме того, занимайтесь самообследованием хотя бы раз в месяц. Используйте зеркало и яркий свет, обследуйте ротовую полость, горло, губы, зубы и десны на наличие подозрительных симптомов, перечисленных ниже. Если вы заметили что-то подозрительное, немедленно обратитесь к врачу. Не игнорируйте регулярное посещение стоматолога.
К симптомам рака полости рта относят следующее:
- Кровоточащая ранка во рту, которая долго не заживает
- Изменение цвета десен
- Шишки, наросты, уплотнения белесоватые пятна во рту
- Боли локального характера или иррадиируюшие в висок, ухо
- Онемение, повышенная чувствительность в зоне поражения
- Повышенное слюноотделение
- Неприятный запах изо рта
- Проблемы с зубами
- Трудности при глотании, жевание, приеме пищи
- Припухлости, утолщение щеки
- Потеря веса
- Изменение голоса
- Припухлости на шее
- Затруднение дыхания
СТАТИСТИЧЕСКИЕ ДАННЫЕ
- Более 13500 случаев заболевания раком полости рта и губ регистрируется в России ежегодно.
- Почти 37 человек в день! в России узнают свой страшный диагноз – рак полости рта.
- 78% всех случаев заболевания раком полости рта и губ в России диагностируется на III-IV клинических стадиях, среди таких пациентов коэффициент выживаемости не превышает 5 лет.Если поставлен диагноз рака полости рта без метастазов, то 82% этих больных уверенно живут более 5 лет, а если уже есть метастазы, то лишь 28% таких больных живут более 5 лет.
- Исследования ОнкоцентраJohnHopkins (США) и других медицинских учреждений показывают, что Вирус Папилломы Человека (HPV) 16, передаваемый половым путем (в том числе через поцелуи), является причиной возникновения рака полости рта и губ, преимущественно глотки и корня языка.
- Риск развития рака полости рта у мужчин в 6 - 8 раз,превышает аналогичны риск у женщин.
- Лица в возрасте 65 лет и старше с наличием одного или нескольких факторов риска развития рака ротовой полости находятся в группе наивысшего риска.
- 25% жертв рака полости рта и губ не курят, не употребляют алкоголь систематически и не имеют прочих факторов риска.
- Выявление начальной стадии рака полости рта дает большой шанс излечить болезнь.

Заболеваемость и смертность раком органов полости рта (РОПР) в последние годы имеет тенденцию к росту во всем мире и в структуре онкопатологии, составляя 2,3 %. Ежегодно у 90 тысяч человек в мире впервые диагностируются опухоли данной локализации [9].
Стандартизированный показатель заболеваемости в Европе равен 1,6 на 100 тысяч населения, а в мире этот показатель составляет 1,15 [7, 9].
В России в структуре онкологической заболеваемости населения в 2013 году рак слизистой оболочки полости рта составляет около 5,5 % [4]. Среди опухолей головы и шеи данная патология занимает второе место, после рака гортани [6].
Рост данной патологии связывается с курением, употреблением крепких алкогольных напитков, плохой гигиеной полости рта, неполноценным питанием, неудовлетворительными результатами лечения предраковых заболеваний [5].
Рак орофарингеальной зоны среди причин летальности стоит на 4-м месте, после рака легкого, желудка и колоректальной зоны [6].
Несмотря на появление различных современных методик лечения, смертность от рака органов полости рта в Российской Федерации у мужчин занимает 7 место, у женщин – 16-е и в 2007 году составила 8,1 и 1,1 на 100 тысяч населения [6], эти данные указывают на необходимость продолжения изучения онкогенеза с других сторон.
В последние годы появилось много исследований, посвященных связи онкопатологии и вирусных инфекций, изучающих так называемый вирус-ассоциированный онкогенез. Было доказано, что более чем в 15 % этиологическими агентами новообразований являются вирусы [10].
Из всех вирусов наибольший интерес исследователей вызывают вирус Эпштейна ‒ Барр (ВЭБ) и вирус папилломы человека (ВПЧ), им посвящено большое количество научных работ [3].
По данным зарубежных авторов, доказательствами связи вируса Эпштейна ‒ Барр и развития новообразований являются: моноклональность ДНК ВЭБ в опухолевых клетках, высокий уровень свободной вирусной ДНК в плазме крови пациентов, наличие корреляции между титром антивирусных антител, уровнем свободной вирусной ДНК в плазме пациента и тяжестью заболевания, также повышенный титр антивирусных антител часто предшествует появлению новообразования и остается высоким на момент постановки диагноза [8].
Перерождение же папилломы в злокачественное новообразование прямо пропорционально связи между онкогенным белком и опухолевым супрессорным белком, например Е6 связывается с р53, Е7 с Rb. Папилломавирусы – единственная группа вирусов, для которых доказано, что они индуцируют образование опухолей у человека в естественных условиях. Онкопротеин Е6 экспрессирует телемеразу, ответственную за активацию пролиферации клеток. Онкобелок Е7 в сочетании с метаболизированием эстрадиола и как следствие образования 16а-гидроксистерона (16а-ОНЕ1), активирующего экспрессию гена Е7, является патогенетической основой вирус-индуцированного онкогенеза. Все это обеспечивает пролиферацию опухолевых клеток и подавляет иммунный ответ [2]. Наличие Е7 (Е6) в цервикальных пробах свидетельствует о процессе малигнизации эпителиальных клеток. Так, для выявления онкопротеина Е7 были созданы тест-системы, для ИФА [2].
Оценка локального уровня некоторых цитокинов при данных процессах представляет отдельный интерес, поскольку воспалительный процесс вызывает их гиперпродукцию иммунокомпетентными клетками, и некоторые из них могут быть факторами роста и распространения опухоли [1].
Исследование микрососудистой инвазии опухолевых клеток в эндотелиальный слой сосудов вызывает интерес как предиктор высокой стадии, степени и распространённости опухоли и, как следствие, возможность ее использования с прогностической целью для оценки течения и прогноза заболевания.
Таким образом, с учетом мониторинга совокупности факторов, ассоциированных с онкогенезом, представляется целесообразным уточнение их прогностической значимости для оценки прогрессирования процесса при раке органов полости рта.
Цель исследования – оценить роль вирусов Эпштейна – Барр и папилломы человека, микрососудистой инвазии и локального уровня цитокинов (ИЛ-2, ИЛ-8, ИЛ-6, ИЛ-10, ИЛ-1β, ИЛ1RА, ИНФ-α, ИНФ-γ, ФНО-α) на течение РОПР.
Материалы и методы исследования
Мужчин было 56, женщин – 16. Возраст больных составлял 34–73 года. По распространенности процесса: со II стадией (T2N0M0) было 13 человек, III – 30 (T2N1M0 – 4, T3N0M0 – 18, T3N1M0 – 8), IV – 29 (T3N2M0 – 4, T4N0M0 – 15, T4N1M0 – 10).
У 59 (81,9 %) больных опухолевым процессом был поражен язык, у 13 (18,1 %) – слизистая дна полости рта. На языке опухоль располагалась чаще на боковой поверхности (52,8 %).
У всех больных был плоскоклеточный рак. Высокая степень дифференцировки (G1) имела место у 22 больных, средняя степень (G2) – 35 и низкая степень (G3) – 15.
Материалом для исследования служили фиксированные в формалине и парафине (FFPE ткани) интраоперационно взятые образцы ткани опухоли и перитуморальной зоны.
Из гомогената ткани опухоли, взятой интраоперационно, ДНК вируса выделяли методом сорбции на магнитных частицах в автоматическом режиме на приборе MagNa Pure Compact с использованием набора реагентов MagNa Pure Compact Nucleic Acid Isolation Kit I-Large Volume на приборе MagNa Pure Compact (Roche, Швейцария). Амплификацию с последующей детекцией ДНК осуществляли методом полимеразной цепной реакции (ПЦР) с гибридизационно-флуоресцентной детекцией в режиме реального времени на термоциклере RotorGene 6000 (QIAGEN, Германия).
Методом ELISA определяли локальные уровни интерлейкинов (ИЛ-2, ИЛ-8, ИЛ-6, ИЛ-10, ИЛ-1β, ИЛ1RА, ИНФ-α, ИНФ-γ, ФНО-α) в гомогенатах фрагментов ткани опухоли и пограничной с опухолью макроскопически неизмененной ткани, взятые интраоперационно. Рассчитывали удельное содержание цитокинов (пг/мл на 1 г белка).
Для оценки ангиогенеза в опухолях применяли окрашивание микрососудов антителом CD34. Количество сосудов определяли в каждом поле зрения препарата при использовании объектива х40.
Для оценки пролиферативной активности опухоли подсчитывали количество ki-67-положительных опухолевых клеток, приходящихся на 200–300 опухолевых клеток, использовали антиген ki-67. Также определяли нормальный и мутантный тип p53.
Статистическая обработка осуществлялась программой Statistica 6,0.
Результаты исследования и их обсуждение
Данные молекулярно-биологических исследований показали, что уровень инфицирования ткани опухоли вирусами папилломы человека составил 20,8 %, в том числе низкого онкогенного риска 5,4 %, высокого 15,3 % Чаще других были выявлены 16 тип (11,1 %) и 11 тип ВПЧ (4,2 %). Частота инфицирования пациентов в зависимости от группы представлена на рис. 1.
Установлена зависимость частоты метастазирования и рецидивирования опухоли от группы вируса. ВПЧ низкого и высокого онкогенного риска чаще были обнаружены в образцах без метастазов.
Частота инфицирования ткани опухоли вирусами группы герпеса составила 68,1 %, в т.ч. вируса простого герпеса 1 типа (ВПГ 1 типа) 5,5 %, цитомегаловируса (ЦМВ) 11,1 %, вируса Эпштейна ‒ Барр (ВЭБ) 62,5 %, вируса герпеса человека 6 типа (ВГЧ 6 типа) 16,7 %. На рис. 2 представлено распределение инфицированности вирусами группы герпеса в зависимости от группы больных.
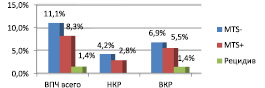
Рис. 1. Частота инфицирования FFPE ткани у пациентов с метастазами, без метастазов, с рецидивами
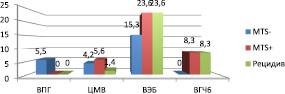
Рис. 2. Частота инфицирования ткани опухоли вирусами группы герпеса у пациентов с метастазами, без метастазов и с рецидивами
С увеличением распространенности опухолевого процесса было отмечено увеличение частоты инфицирования ткани опухоли вирусами группы герпеса. В большей степени это положение характерно для ВЭБ, ВГЧ 6 типа. Так, суммарная частота инфицирования всеми представителями этой группы для стадии Т2 составила 70,6 %, Т3 – 80 %, Т4 – 84 %. Для цитомегаловируса эти показатели составили 5,9; 12,5 и 16 %, для вируса Эпштейна – Барр – 64,7; 80 и 80 %, для вируса герпеса 6 типа 11,7; 16,7 и 20 % соответственно.
При анализе клинических данных в сопоставлении с полученными лабораторными было установлено, что у больных с регионарными метастазами ВЭБ встречался в 17 случаях (70,8 %) от общего числа больных данной группы), в то время как ВПЧ – в одном (25 %). У больных без метастазов ВЭБ был выявлен в 11 случаях (45,8 %), в то время как ВПЧ – у 8 (33,3 %). Для больных с рецидивами ВЭБ составил – 17 случаев (70,8 %), а ВПЧ – 1 (1,4 %). Таким образом, у больных с метастазами и рецидивами выявление ВЭБ-ассоциированного рака было выше (70,8 %), чем у больных без метастазов (45,8 %), в то время как ВПЧ-позитивные больные встречались чаще в группе без метастазов (33,3 %), в отличие от других групп (25 и 1,4 %).
При изучении локальных уровней цитокинов (ИЛ-2, ИЛ-8, ИЛ-6, ИЛ-10, ИЛ-1β, ИЛ1RА, ИНФ-α, ИНФ-γ, ФНО-α) отмечено статистически значимое (р Примечания:
* – отличия показателей статистически достоверны по отношению к группе без метастазов (Р ≤ 0,05);
º – отличия показателей статистически достоверны по отношению к группе с метастазами (Р ≤ 0,05).
1. Инфицированность вирусами папилломы человека ткани опухоли можно рассматривать как благоприятный прогностический признак в отношении развития метастазов у больных с раком органов полости рта (в группе без метастазов (33,3 %), в отличие от других групп (25 и 1,4 %)). Инфицирование вирусами группы герпеса ткани опухоли можно рассматривать как неблагоприятный прогностический признак (выявление ВЭБ-ассоциированного рака – 70,8 % у больных с метастазами и рецидивами, у больных без метастазов 45,8 %).
2. Различия тканевого цитокинового состава между больными раком языка и полости рта без регионарных метастазов, с регионарными метастазами и при рецидивах статистически не значимы. При этом показаны различия их уровня между тканью опухоли и перитуморальной области с преобладанием содержания провоспалительных цитокинов ИЛ-1ß, ИЛ-6, ИЛ-8 в опухолевой ткани. Вероятно, избыток провоспалительных цитокинов, у которых описаны ростостимулирующие свойства, наблюдается за счет их продукции опухолевыми клетками, а также присутствующими в очаге активированными макрофагами, что способствует росту и распространению опухоли.
3. Преобладание сосудов крупного диаметра с утолщенной стенкой может коррелировать с наличием или возможным развитием метастазов и рецидивов, таким образом, иметь неблагоприятный прогностический характер.
ВГЧ – вирус герпеса человека,
ВПГ 1 типа – вирус простого герпеса 1 типа,
ВГЧ 6 типа – вирус герпеса человека 6 типа,
ВПЧ – вирус папилломы человека,
ВПЧ 16 типа – вирус папилломы человека 16 типа,
ВПЧ ВКР – вирус папилломы человека высокого канцерогенного риска,
ВПЧ НКР – вирусы папиллом человека низкого канцерогенного риска,
ВЭБ – вирус Эпштейна ‒ Барр,
ДНК – дезоксирибонуклеиновая кислота,
ИЛ-1β – Интерлейкин – 1β,
ИЛ1RА – Интерлейкин 1RА,
ИФА – Иммуноферментный анализ,
ПЦР – полимеразная цепная реакция,
РОПР – рак органов полости рта,
ФНО-α – Фактор некроза опухоли – α.
Рецензенты:
Каймакчи О.Ю., д.м.н., ассистент кафедры онкологии, Ростовский государственный медицинский университет, г. Ростов-на-Дону;
Шихлярова А.И., д.б.н., профессор, руководитель лаборатории изыскания новых противоопухолевых средств и изучение механизма их действия, ФГБУ РНИОИ МЗ РФ, г. Ростов-на-Дону.
Читайте также:


