Вирус мышиного лейкоза молони
| Gammaretrovirus | |
|---|---|
| классификация Вирус | |
| (Неоцениваемый): | Вирус |
| Тип: | incertae SEDIS |
| Учебный класс: | incertae SEDIS |
| Порядок: | Ortervirales |
| Семья: | Retroviridae |
| Подсемейство: | Orthoretrovirinae |
| Род: | Gammaretrovirus |
| Типовой вид | |
| Мышиный вирус лейкемии | |
Gammaretrovirus является родом в ретровирусах семье . Пример вида являются мышиный вирус лейкемии , и вирус кошачьей лейкемии . Они вызывают различные саркомы, лейкозы и иммунодефициты у млекопитающих, рептилий и птиц.
содержание
Вступление
Многие эндогенные ретровирусы , тесно связанные с экзогенными gammaretroviruses, присутствуют в ДНК млекопитающих (включая человека), птиц, рептилий и амфибий. Многие также разделяют консервативную РНК структурный элемент , называемый инкапсидации сигнал ядра .
В вирусах птичьего ретикулоэндотелиоза не являются строго вирусами птичьих-то кажется, что ретикулоэндотелиоз вирусы вирусы млекопитающих, которые были случайно введены в птица в 1930-х годах в ходе исследования по малярии.
В качестве потенциального вектора для генной терапии , gammaretroviruses имеют некоторые преимущества по сравнению с ВИЧ в качестве вектора лентивирусов . В частности, gammaretroviral система упаковки не требует включения каких - либо последовательностей перекрывающихся с кодирующих последовательностей генов затычки, POL или аксессуар.
Gammaretroviruses имеет широкий спектр последствий для животных. Они были связаны с несколькими заболеваниями, включая рак, в частности лейкозов и лимфом, различных неврологических заболеваний, а также некоторых иммунодефицитов во многих различных видов. Gammaretroviruses похожи на другие ретровирусы и обратной транскрипции положительный одиночный цепь РНК в двухцепочечную ДНК. Двухцепочечной ДНК, обладает высокой стабильностью и легко интегрированы в геном хозяина. Несколько примеров вируса Молони вируса мышиного лейкоза, Xenotropic MuLB связанных с вирусом, кошачий вирус лейкемии, и кошачий вирус саркомы.
Gammaretroviruses очень популярны ретровирусные векторы в лабораторных исследованиях. Эти векторы имеют решающее значение для генной терапии и переноса генов. Причина , по которой они так полезны, потому что их геномы очень просты и удобны в использовании. Ретровирусы обладают способностью интегрировать в клетки - хозяина геномов очень хорошо, что позволяет в течение длительного срока экспрессии генома. Одним из конкретных gammaretrovirus , который обычно используется в качестве ретровирусного вектора является вирус мышиного лейкоза Молони.
Конкретным gammaretrovirus называется Xenotropic вирус мышиной лейкемии, связанных с вирусом (XMRV) был обнаружен в ткани рака простаты. Есть более 50 линий раковых клеток человека, которые были идентифицированы с Xenotropic мышиного лейкоза вирусом связанных вируса или вируса мышиной лейкемии. Там также были открытия мышиных gammeretroviruses в клеточных линиях рака легких. Пока неясно, какую роль эти вирусы в развитии рака, полагают, что они являются наиболее распространенными на стадии опухоли развивается рака путем ингибирования опухоли подавления генов. XMRV представляет собой рекомбинантный вирус создан в лаборатории аварии в середине 1990-х годов. Хотя он может заразить ткани человека, не известна болезнь связана с инфекцией.
Вирусная классификация
Gammaretrovirus является частью ретровирусы семьи. Gammaretroviruses считаются зоонозных вирусов , потому что они встречаются во многих различных видов млекопитающих, таких как мыши, кошки, свиньи, приматы, коров и птиц. Однако, летучие мыши являются основным резервуаром для многих gammaretroviruses. Летучие мыши могут иметь длительное воздействие различных патогенных микроорганизмов , не проявляя какие - либо предупреждающие знаки, что приводит к обсуждаемому убеждению , что летучие мыши имеют возможность выработать иммунитет к вирусам , которые могут нанести вред другим видам. Таким образом, это возможно для летучих мышей укрывать не только один, а несколько видов gammaretroviruses. Это утверждение поддерживается с помощью методики профилирования секвенирование транскриптом и полимеразной цепной реакции. Исследователи также рассмотрели несколько различных типов видов летучих мышей , чтобы укрепить утверждают , что летучие мыши являются основным резервуаром для gammaretroviruses. В gammaretroviruses могут быть распределены по горизонтали, животного к животному, или по вертикали от родителей к потомству.
Другой gammaretrovirus резервуар был обнаружен в геноме афалин . Это gammaretrovirus называется Tursiops обрезает эндогенный ретровирус, считалось, что из дошедших до наших дней mammaliam эндогенных gammretroviruses. Tursiops обрезает эндогенный ретровирус оригинальный нашествие датируется примерно 10-19 миллионов лет назад, и был идентифицирован в косатка эндогенного gammaretrovirus , который вторгся более 3 миллионов лет назад. В 2009 годе , еще эндогенные gammretroviruses были обнаружены в разновидности касатки, а также девять других китообразных геномов. Так gammaretrovirus геномы присутствуют в обоих водных и наземных видов млекопитающих.
Состав
Gammaretrovirus является сферическим, оболочкой вириона в пределах от 80-100 нм в диаметре. Она содержит нуклеокапсида, обратной транскриптазы, интегразы, капсида, протеазы, конверт и поверхностные единицы. Нуклеокапсид представляет собой нуклеиновую кислоту сборки белка в вирусной частицы, это подструктура вириона. Обратный транскриптазы является фермент, ответственный за превращение РНК в ДНК во время цикла репликации вирионов. Интеграза работает с обратной транскриптазы для преобразования РНК в ДНК. Капсида является белок оболочки, которая окружает геном вирусной частицы, его основные функции для защиты и доставки генома в клетке-хозяине. Оболочка вируса является мембрана, которая окружает вирусный капсид, он является производным клетка-хозяин липидный бислой.
геном
Геном gammaretrovirus является одноцепочечной РНК (+) , геном , который составляет примерно 8,3 кб в размере. Он имеет колпачок с 3' 5' поли-A хвостом, и он содержит две длинные участки терминала повторителя как на 5' и 3' концы. Эти длинные участки концевого повтора имеют U5, R и U3 областей, а также полипуриновый тракт на 3' - конце и сайт связывания праймера на 5' - конце. Типичный gammretrovirus геном содержит ген рвотного , ген Pol , и ген ENV .
цикл репликации
Gammaretrovirus будет выступать в качестве паразита , чтобы использовать клеточные факторы хозяина для доставки генома в ядро клетки - хозяина , , где они будут использовать машины ячеек для репликации вирусного генома и продолжают распространяться по всему организму хозяина. Поскольку это одноцепочечный РНК (+) , с ДНК промежуточного геномом, он имеет возможность копировать это вирусный РНК - геном непосредственно в мРНК. Против центральной догмы биологии, но и в противоположном направлении расшифровывает его РНК - геном в ДНК.
Вирион прикрепить рецепторы клетки - хозяина с помощью SU гликопротеина , то ТМ гликопротеина передач с слиянием с клеточной мембраной. Вирус будет затем начать декапсидацию, а линейная молекула двухцепочечной ДНК образуется из одноцепочечной РНК (+) генома с помощью обратной транскрипции. Фермент , ответственный за обратной транскрипции является обратной транскриптазы . Принимающая ядерная мембрана разобрала во время митоза и вирусная двухцепочечная ДНК способна въезжают в ядро. Вирусный двухцепочечной ДНК затем интегрируют в геном клетки - хозяина с помощью вирусной интегразы, фермента , который позволяет для интеграции вирусной ДНК в ДНК хозяина. Вирус теперь упоминается как провируса , что означает gammaretrovirus ДНК интегрирована в геном клетки - хозяина , и в настоящее время является шаблон для формирования вирусной мРНК и геномной РНК. Двухцепочечной ДНК транскрибируется Pol II и будет производить как сплайсинга и unspliced нити РНК, эти сращивания нити РНК покидает ядро клетки - хозяина. Unspliced вирусное перевод РНК производит окр, кляп, и кляп-Pol полипротеинов. Ко становятся предшественником полипептида и расщепляют для получения поверхности связывания рецептора. Далее вириона собран в мембране клетки - хозяина, и вирусный РНК - геном упакован. Вирионы бутон из плазматической мембраны и выпустить в хозяина. После того, как вирионы освобождение от клеток - хозяев процесс повторяется на следующей клетке активной вирусной частицы попадается.
Сопутствующие заболевания и вспышки
Вспышки Gammaretrovirus распространены в коал. На самом деле, они были связаны с Koala иммунного синдрома дефицита (моторизованные), который похож на синдром иммунодефицита человека. Коала иммунный синдром дефицита влияет на иммунную систему различных популяций медведей коала, что делает их более склонными к инфицируются заболеваниями или с диагнозом рак. Подобно ВИЧ, Koala иммунный синдром дефицита может быть передан потомству, а также передаваться другим коал или вида на животных. Вирус распространен в неволе коал. В самом деле, в популяции в неволе коал в Квинсленде 80% смертей связаны с gammaretroviruses. Эта колония находится в состоянии повышенной готовности, что их популяция коал может быть вымершей в ближайшем будущем, исследователи обеспокоены тем, что эпидемия может вспыхнуть в Квинсленд.
ограничение хоста
Вакцины были обнаружены и предназначены для различных gammaretroviruses. Намибия принимает наибольшее население диких гепардов в мире, что делает его жизненно население для понимания биологии и естественного поведения этого вида. В июне 2002 года исследователи начали тестирование животных на наличие вируса лейкоза кошачьих, поскольку беспокойство возникло, что вирусная инфекция может привести к серьезной проблемой здравоохранения в гепарда населения Намибии. С помощью этого тестирования, были собраны антитела к разработке вакцины кошачьего вируса лейкемии. Эта вакцина оказалась успешной в намибийскими гепардов, а 86% вакцинированных гепардов дали положительный результат на вирус лейкоза кошачьих антител. При таком высоком привитом проценте, гепарды находятся в состоянии, где есть более чем достаточное количество населения, которое привито, чтобы предотвратить Amor вспышку gammaretrovius, такие как кошачий вирус лейкемии.
Наряду с вакцинацией, ограничение множество gammaretroviruses и других видов ретровирусов распространены среди животных. Многие хосты имеют ген, который блокирует цикл репликации ретровирусов, в том числе gammaretrovirus. Этот ген был обнаружен используется не ядовитый белком вируса мышиной лейкемии. Этот белок блокирует репликацию некоторых вируса мышиного лейкоза штаммов следующей обратной транскрипции. Ограничение вируса зависит от взаимодействия белка и вируса вторгшегося.
1 Moloney virus
2 Moloney leukemia virus
- вирус лейкоза Молони
вирус лейкоза Молони
Патогенный для большинства линий мышей и крыс вирус, вызывающий лимфосаркомы и лимфолейкозы.
[Арефьев В.А., Лисовенко Л.А. Англо-русский толковый словарь генетических терминов 1995 407с
3 Moloney leukemia virus
4 Moloney leukemia virus
5 Moloney murine leukemia virus
6 Moloney sarcoma virus
7 Moloney leukemia virus
8 Moloney sarcoma virus
9 Moloney leukemia virus
10 Moloney mouse sarcoma virus
11 Moloney murine leukemia virus
12 Moloney murine sarcoma virus
13 Moloney sarcoma virus
14 Moloney's leukemogenic virus
15 Moloney's sarcoma virus
16 Moloney murine leukemia virus
17 一种可引起小鼠淋巴性白血病的鼠白血病病毒
18 莫洛尼病毒
19 莫洛尼小鼠肉瘤毒
20 莫洛尼小鼠肉瘤病毒
Moloney virus — n a strain of murine leukemia virus that causes lymphocytic leukemia in mice called also Moloney leukemia virus, Moloney murine leukemia virus Moloney John Bromley (b 1924) American biologist. Moloney devoted his career to research at the… … Medical dictionary
Moloney murine leukaemia virus — (= Moloney murine leukemia virus (USA) ) Replication competent retrovirus (Oncovirinae) that causes leukaemia in mice, isolated by Moloney from cell free extracts made from a transplantable mouse sarcoma … Dictionary of molecular biology
Virus de la leucémie murine — Le virus de la leucémie murine (MuLV, Murine Leukemia Virus) est un rétrovirus appartenant au type C des mammifères (Morphologie démontrant un nucléoïde clair en position centrale qui mûrit en bourgeonnant à la surface de la cellule)[1]. Classe… … Wikipédia en Français
Virus — A microorganism smaller than a bacteria, which cannot grow or reproduce apart from a living cell. A virus invades living cells and uses their chemical machinery to keep itself alive and to replicate itself. It may reproduce with fidelity or with… … Medical dictionary
Moloney — John B., 20th century U.S. oncologist. See M. virus. Paul J., Canadian physician, 1870–1939. See M. test … Medical dictionary
Moloney murine sarcoma virus — Replication defective retrovirus, source of the oncogene v mos, responsible for inducing fibrosarcomas in vivo, and transforming cells in culture … Dictionary of molecular biology
murine leukemia virus — n a retrovirus (species Murine leukemia virus of the genus Gammaretrovirus) that includes several strains producing leukemia in mice see friend virus, moloney virus * * * a species of the genus Gammaretrovirus that infects mice; it includes a… … Medical dictionary
Murine leukemia virus — MMLV redirects here. It is also the Roman numeral for 2055. Murine leukemia virus Virus classification Group: Group VI (ssRNA RT) Family: Retroviridae Subfamily … Wikipedia
Murines Leukämie-Virus — Murines Leukämievirus Systematik Reich: Viren Ordnung: nicht klassifiziert Familie: Retroviridae Unterfamilie: Orthoretrovirinae … Deutsch Wikipedia
Abelson murine leukemia virus — Taxobox name = PAGENAME virus group = vi familia = Retroviridae subfamilia = Orthoretrovirinae genus = Gammaretrovirus species = Murine leukemia virus subdivision ranks = Serotype subdivision = Abelson murine leukemia virus The Abelson murine… … Wikipedia
Abelson leukaemia virus — A replication defective virus originating from the Moloney murine leukemia virus by acquisition of c abl. The virus induces B cell lymphoid leukemias within a few weeks. The v abl product has tyrosine kinase activity … Dictionary of molecular biology
MLV — Moloney leukemia virus; Mono Lake virus; multilaminar vesicle; murine leukemia virus … Medical dictionary
MLV — • Moloney leukemia virus; • Mono Lake virus; • multilaminar vesicle; • murine leukemia virus … Dictionary of medical acronyms & abbreviations
MMLV — Moloney murine leukemia virus; Montana myotis leukoencephalitis virus … Medical dictionary
MMLV — • Moloney murine leukemia virus; • Montana myotis leukoencephalitis virus … Dictionary of medical acronyms & abbreviations
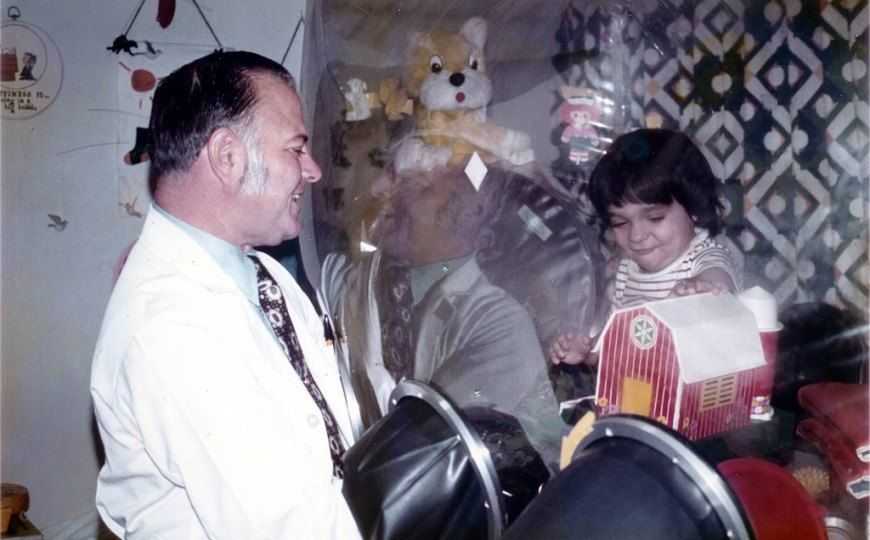
Дэвид Веттер (1971—1984), мальчик, страдавший тяжелым комбинированным иммунодефицитом и с рождения вынужденный жить в стерильной среде, и доктор Джон Монтгомери из Медицинского колледжа Бейлора | commons.wikimedia.org/
В середине апреля New England Journal of Medicine опубликовал промежуточные результаты экспериментальной генной терапии для восьми детей с Х-сцепленным тяжелым комбинированным иммунодефицитом (SCID, или ТКИД). Ученые из Детской исследовательской больницы Св. Иуды и Калифорнийского университета в Сан-Франциско использовали лентивирус для доставки функционального гена гамма-рецептора интерлейкина в гемопоэтические стволовые клеткам пациента ex vivo. После трансплантации клетки восстанавливали иммунную систему пациентов, включая Т-клетки, В-клетки и естественные клетки-киллеры (см. подробности на PCR.news).
Эти успехи сделали генную терапию ТКИД привлекательной областью для инвестиций. В августе 2018 года Mustang Bio лицензировала платформу лентивирусной генной терапии от больницы Св. Иуды, переименовав ее в MB-107. А после апрельской публикации несколько компаний выразили желание обсудить возможность сублицензирования.
Тем временем лондонский стартап Orchard Therapeutics в феврале объявил о своем клиническом успехе с лентивирусным препаратом для терапии ТКИД, связанного с дефицитом аденозин-деаминазы (ADA), — второй наиболее распространенной формы заболевания после Х-сцепленного ТКИД. На конференции по трансплантации и клеточной терапии 2019 года в Хьюстоне Дональд Кон из Калифорнийского университета в Лос-Анджелесе, научный соучредитель Orchard, рассказал, что все 20 молодых людей, получавших терапию OTL-101, разработанную компанией, два года спустя были здоровы, и их иммунная система была полностью функциональной. При этом около трети пациентов в контрольной группе, которым трансплантировали гемопоэтические стволовые клетки, нуждались в дополнительной экстренной трансплантации или заместительной ферментной терапии.
Исследователи впервые начали тестировать генную терапию Х-сцепленного ТКИД в клинике почти три десятилетия назад. Но в первых двух исследованиях у 6 из 20 пациентов развился лейкоз, вызванный активацией протоонкогенов из-за инсерции вектора, один молодой пациент умер. Регуляторы надолго приостановили клинические испытания генной терапии. Дополнительным препятствием для клинических применений стал тот факт, что генная терапия ТКИД первого поколения с использованием гамма-ретровирусных векторов помогла исправить дефекты Т-клеток, но не восстановила другие иммунные функции.
Примечательно, что генная терапия дефицита ADA Strimvelis, принадлежащая GlaxoSmithKline,— первая генная терапия ex vivo, разрешенная в любой точке мира — использует не лентивирусную систему, а гамма-ретровирусный вектор, но при этом не дает таких осложнений. Тем не менее, после того как в 2016 году Strimvelis был одобрен европейскими регуляторами, только пять пациентов получили продукт в течение следующих двух лет. Причины — большая редкость заболевания (около 15 новых случаев в Европе ежегодно) и цена в 594 000 евро (при этом компания Orchard Therapeutics продолжает испытания своей лентивирусной терапии OTL-101, и участие в них бесплатно). Кроме того, для лечения нужно ехать в Милан и оставаться там в течение месяца.
Терапия Strimvelis тем не менее сыграла важную роль, продемонстрировав преимущество стратегии кондиционирования — низких доз ДНК-алкилирующей химиотерапии бусульфаном, которая стала стандартом для увеличения приживления генно-модифицированных клеток крови. Ранее приживление клеток было настолько низким, что большинство пациентов с ADA-ТКИД оставались на заместительной ферментной терапии.
Клинические испытания генной терапии для других форм SCID только начинаются, и все они используют лентивирусы (список можно посмотреть здесь). Среди них Артемис-дефицитный ТКИД, распространенный среди коренного населения Северной Америки. В ближайшие месяцы в Медицинском центре Лейденского университета в Нидерландах планируют начать испытания терапии RAG-дефицитного ТКИД, вызванного мутациями в RAG1. Оба эти вида ТКИД регулируют сборку сегментов в геноме клетки иммунной системы для генерации разнообразия антигенных рецепторов. Есть основания полагать, что их генная терапия потребует более точной настройки уровней экспрессии трансгена, чем вирусные препараты для ADA - или Х-сцепленного SCID. Возможно, эту задачу смогут выполнить CRISPR-Cas9 или редакторы оснований. Хотя технологии CRISPR тоже не идеальны с точки зрения безопасности, этот подход полностью исключает возможность активации генов, связанной со вставкой вектора. Эксперименты по генной коррекции Х-сцепленной ТКИД с помощью CRISPR уже проводились (2019, 2017). Интереса у компаний они пока не вызвали, поскольку было неясно, в чем их преимущество перед MB-107 и зачем вкладывать деньги в ее альтернативу. Однако применительно к другим видам тяжелого комбинированного иммунодефицита преимущество может стать более явным, и ситуация изменится.
Онкорнавирусы мышей по морфологии разделяются на вирионы типов В и С.
По способности репродуцироваться в гомологичных и гетерологичных клетках вирусы типа С мышей (MuLV) разделяют на 4 группы: N-тропные, способные к репродукции в клетках мышей линии NIH; В-тропные, способные к репродукции в клетках мышей линии BALB; NB-тропные, репродуцирующиеся в клетках мышей обеих линий, и ксенотропные, способные к репликации в гетерогенных клетках (кролика, крысы). Чувствительность клеток к вирусам типа С, по-видимому, контролируется геном Fvl.
По способности вызывать первичную реакцию в инфицированном хозяине вирусы типа С классифицированы на 3 категории: лейкемические вирусы (MuLV), вирусы, вызывающие фокусы в селезёнке (SFFV), и мышиные саркоматозные вирусы (MSV). Лимфатическую лейкемию в основном индуцируют MuLV. Оии способны реплицироваться в различных тканях, но не могут их трансформировать. SFFV выделены в лабораториях Френд, Раушера и Попе. Они легко трансформируют гемопоэтические клетки в костном мозге и селезёнке. Эти вирусы высоколетальны, дефектны и реплицируются в присутствии вируса-помощника.
Вирус саркомы мышей (MSV) вызывает характерные опухоли у мышей и способен трансформировать клетки, но также дефектен. Биологический эффект проявляется только в присутствии вируса-помощника - MuLV. Клетки, трансформированные MSV, разделяются на 2 класса: 1) непродуцирующие, не освобождающие вирусных частиц и негативные по gs- АГ клетки. Вирус из них может быть активирован суперинфекцией лейкемическим вирусом; 2) саркомо-позитивные лейкемия негативные (S+ L‘) клетки, содержащие геном саркоматозного вируса, продуцирующие gs-AT и незначительное количество вирусных частиц. В препаратах мышиных онкорнавирусов обнаружены 5 АГ, различия между которыми устанавливают в 2-х тестах: цитотоксическом, с помощью которого определяют клеточные поверхностные АГ в инфицированных клетках (тест CSA), и тест нейтрализации (тест VEA). По тесту VEA онкорнавирусы мышей делят на 2 группы: Гросса и группу, подразделяющуюся на 4 типа: - тип а (вирусы Френд, Граффи, Роусон-Парр, SimLV); тип b - (вирусы Молони, Абельсон; тип с - вирусы Раушер, Рич, Брейар); тип d - (вирус Буффей). По тесту CSA также выделены 2 группы: Гросс (G) и Френд-Молони-Раушер (FMR).
В оболочке вирусов лейкемии мышей (MuLV-F), кошек (FeLV-T), саркомы кошек (FeSV-st) и эндогенном вирусе крыс (NWR-1) имеются общие АГ. Так, вирусы MuLV-F и ; FeLV-T содержат общие поверхностные АГ, вирус FeSV-st, продуцируемый клетками кры- ; синой опухоли, имеет общие поверхностные АГ с эндогенным вирусом крыс (NWR-1).
Кроме указанных вирусов, адаптированных к клеточным системам, от мышей выделены эндогенные вирусы типа С (из первичных опухолей, спонтанных или индуцированных из нормальных неопластических клеток в культуре). Так, из клеток мышей линии В ALB с помощью йод-дезуксеуредина удалось активировать 2 эндогенных вируса типа С: N-тропный BALB-1, и ксенотропный BALB-2. В последнее время из этих клеток удалось активировать ещё один эндогенный вирус. Активированные частицы типа С содержат обратную транс- криптазу. По спектру чувствительных клеток эндогенные вирусы типа С разделяются на 2 группы ксенотропные, инфекционные только в клетках других видов, и экотропные, среди которых имеется группа, инфекционная для мышей линии BALB.
Эндогенные вирусы типа С, как правило, вообще не обладают онкогенными потенциалами либо обладают ими в очень слабой степени. В настоящее время биологическую функцию этих вирусов сводят к тому, что они либо выполняют определённую физиологическую роль в развитии опухоли путём регулирования процессов узнавания клеток и их дифферен- цировки, либо обусловливают частичную резистентность клеток к суперинфекции экзогенными вирусами. Передаются вирусы типа С генетически, вертикально.
Мишенью действия вирусов лейкоза мышей Гросса, AKR и Молони являются Т- лимфоциты, вируса Абельсона - В-лимфоциты, вирусы Френд и Раушера - эритробласты, вируса Граф фи - миелобласты и Т-лимфоциты.
1 Moloney Leukaemia Virus
2 Moloney murine leukemia virus
3 Молоуни
4 вирус лейкоза Молони
5 вирус мышиного лейкоза Молони
6 вирус саркомы Молони
7 вирус саркомы Молони
8 кожан Молони
9 кожаны Молони
10 1670
11 1671
12 вирус лейкоза Молони
- Moloney leukemia virus
вирус лейкоза Молони
Патогенный для большинства линий мышей и крыс вирус, вызывающий лимфосаркомы и лимфолейкозы.
[Арефьев В.А., Лисовенко Л.А. Англо-русский толковый словарь генетических терминов 1995 407с.]
13 вирусный инсерционный мутагенез
- viral-induced insertional mutagenesis
вирусный инсерционный мутагенез
Мутагенез, имеющий место в клетках, зараженных вирусами, способными интегрировать свой геном в различные участки генома клетки-хозяина и, соответственно, вызывать инсерционные мутации; примером В.и.м. является индуцирование мутантной окраски шерсти у мышей линии DBA/2J, зараженных вирусом лейкоза Молони Moloney.
[Арефьев В.А., Лисовенко Л.А. Англо-русский толковый словарь генетических терминов 1995 407с.]
14 вирусы лейкоза
- leukemia viruses
вирусы лейкоза
Вирусы, вызывающие различные формы лейкозов (лимфоидная и миелоидная лейкемия, ретикулолейкоз и т.д.) у лабораторных млекопитающих (мышей, крыс, хомячков) в лабораторных условиях; к В.л. относятсы вирусы Граффи (Graffi l.v.), Гросса (Gross l.v.), кошачьих (feline l.v.), Молони (Moloney l.v.), Раушера (Rauscher l.v.), Френда (Friend l.v.), Кирстена (Kirsten l.v.), Абельсона (Abelson l.v.), Мазуренко (Mazurenko l.v.).
[Арефьев В.А., Лисовенко Л.А. Англо-русский толковый словарь генетических терминов 1995 407с.]
Moloney — ist der Familienname folgender Personen: Brendan Moloney (* 1989), irischer Fußballspieler Cornelius Alfred Moloney (1848–1913), Gouverneur von Gambia sowie Trinidad und Tobago Frederick Moloney (1880–1941), US amerikanischer Leichtathlet Janel… … Deutsch Wikipedia
Moloney — may refer to: Moloney (surname), people with the surname Moloney Moloney (TV series), 1996–97 American television police drama See also Maloney Moloney s Mimic Bat This disambiguation page lists articles associated w … Wikipedia
Moloney — Recorded in the spellings of O Moloney, Moloney, Maloney, and Maleney, this interesting name is of Irish origin. It is a derivative of the pre 10th century Gaelic O Maol Dhomhnaigh, translating as the descendent of the servant of the Church ,… … Surnames reference
Moloney — Cette page d’homonymie répertorie les différents sujets et articles partageant un même nom. Patronyme Janel Moloney est une actrice américaine ; John Moloney est un ancien joueur de rugby à XV irlandais ; Paddy Moloney est un musicien… … Wikipédia en Français
Moloney — John B., 20th century U.S. oncologist. See M. virus. Paul J., Canadian physician, 1870–1939. See M. test … Medical dictionary
Moloney (surname) — Moloney is a surname of Irish origin (Irish translation is Ó Maoldomhnaigh). The name may refer to: Tom Moloney (b. 1996), Australian rules footballer for the Richmond Football Club Cornelius Alfred Moloney (1848–1913), British colonial… … Wikipedia
Moloney (TV series) — Moloney Format Drama Created by Ronald Bass Jane Rusconi Starring Peter Strauss Nestor Serrano Wendell Pierce Cherie Lunghi Giuliana Santini Ashley Johnson … Wikipedia
Moloney virus — n a strain of murine leukemia virus that causes lymphocytic leukemia in mice called also Moloney leukemia virus, Moloney murine leukemia virus Moloney John Bromley (b 1924) American biologist. Moloney devoted his career to research at the… … Medical dictionary
Moloney's Mimic Bat — Conservation status Least Concern (IUCN 3.1) Scientific classification Ki … Wikipedia
Moloney murine leukaemia virus — (= Moloney murine leukemia virus (USA) ) Replication competent retrovirus (Oncovirinae) that causes leukaemia in mice, isolated by Moloney from cell free extracts made from a transplantable mouse sarcoma … Dictionary of molecular biology
Related JoVE Videos




The JoVE video player is compatible with HTML5 and Adobe Flash. Older browsers that do not support HTML5 and the H.264 video codec will still use a Flash-based video player. We recommend downloading the newest version of Flash here, but we support all versions 10 and above.
If that doesn't help, please let us know.
Лентивирусов являются ценным исследовательским инструментом для изучения функции генов, однако, исследователи, возможно, пожелают, чтобы избежать производства пантропный кодирования лентивирус известных или подозреваемых онкогенов. В качестве альтернативы, мы представляем безопаснее протокол для использования ecotropic лентивирус на клетки человека изменен, чтобы выразить ecotropic mSlc7a1 рецепторов.
Barrilleaux, B., Knoepfler, P. Transduction of Human Cells with Polymer-complexed Ecotropic Lentivirus for Enhanced Biosafety. J. Vis. Exp. (53), e2822, doi:10.3791/2822 (2011).
Translate text to:
Please note that all translations are automatically generated.
Рекомбинантный ecotropic gammaretrovirus на основе Молони мышиного вируса лейкоза (MLV) и его рецептор mSlc7a1 хорошо изучены и широко доступны, что оно использовалось более 20 лет для доставки трансгенов в мышиных клетках. Ecotropic gammaretrovirus также используется в последнее время для доставки онкогенов в клетках человека;. В контексте сотовых перепрограммирования, использование mSlc7a1, чтобы избежать поколения amphotropic вирус укрывательство человека онкогенов хорошо известна 4,5 Тем не менее, лентивирус обеспечивает значительные преимущества по сравнению с gammaretrovirus В трансдуцирующих огнеупорных клеточных популяций, 6, включая первичные клетки, которые часто желательно цели для перепрограммирования, так как лентивирусов предварительной интеграции комплекса позволяет трансдукции, не делящихся клеток. 7
Лентивирусов были произведены с десятками различных pseudotypes, в том числе MLV, в попытке изменить вирус тропизм, токсичность и другие свойства. 8 MLV-pseudotyped ecotropic лентивирус была использована для трансдукции клеток мыши, 9, но редко используется на клетки человека 10. Поэтому мы предлагаем использование MLV-pseudotyped ecotropic лентивирус как безопасный, экономичный и высокоэффективный автомобиль для доставки известных или подозреваемых онкогенов, в том числе сотовых перепрограммирования факторов, в клетках человека.
Важно отметить, что этот протокол не полностью избавляет от необходимости производить и использовать пантропный лентивирус, а, скорее, этот протокол отделяет онкоген (ы) из пантропный вирус, изоляционные исследователей из потенциальных самостоятельной прививки связанных с раком вирусов. MSlc7a1 белка и его гомолог человеческого hSlc7a1 являются повсеместно выразил аминокислоты перевозчиков кислоты, не известны туморогенность или способность даровать селективное преимущество роста на клетки-реципиенты, 11 решений mSlc7a1 сравнительно низким уровнем риска для включения в amphotropic вируса. Это добавило шаг может быть особенно полезным в лабораториях не хватает посвященный вирусу или объектов культуры тканей необходимого уровня биобезопасности.
В некоторых ситуациях это может быть возможным, чтобы полностью отказаться от использования пантропный вируса путем трансфекции плазмидой Slc7a1 непосредственно в клетки-мишени, однако многие клетки, которые были бы полезными целями этой техники также поддаются трансфекции. В качестве альтернативы, способность изолировать Slc7a1-трансдуцированных клеток выбор blasticidin означает, что VSV-G pseudotyped лентивирус может быть использован только один раз, чтобы создать запас рецепторами клеток, экспрессирующих, после чего ecotropic вирус может быть использован для трансдукции обычно эти клетки для многих экспериментов. Исследователи должны всегда следовать их институциональных правил техники безопасности при работе с любым лентивирус, независимо от его тропизм.
Титры ecotropic вируса достигнуты с этим протоколом умеренно ниже, чем VSV-pseudotyped вирус, как правило, 10-20% пантропный титр вируса, в соответствии с предыдущими исследованиями. 9 Эти титры были измерены в клетках человека стабильно трансдуцированных с Slc7a1, так что нижняя наблюдается титр для ecotropic вирус может быть частично обусловлено разнообразными экспрессии рецептора гена в клетки-мишени. Тем не менее, вирусные титры достигнута в наш протокол более чем достаточно для большинства приложений и привести к трансдукции большинства клеток, в некоторых случаях> 90% клеток.
Центрифугирование методы на основе широко используются для сконцентрироваться вирусных частиц. Тем не менее, центрифугирования требует нескольких часов, генерирует инфекционных аэрозолей, и может привести к значительной потере вирусных частиц. 12 В качестве альтернативы, комплексообразование с НЦБ / PB может быть использован для повышения трансдукции без изменения вирусной тропизм. 3 Этот метод быстрого (5 минут ) и недорогая ($ 0,03 за 10 мл вируса), в то время как примерно в три раза наблюдалось титр. Никакого специального оборудования или собственности реагенты необходимы, и мы наблюдали минимальную острую токсичность после воздействия HDFS для CS / PB, по согласованию с предыдущей работы в других клеточных линий. 13 Одним из потенциальных недостатков этого протокола является то, что некоторые микроскопически видимые полимерных комплексов придерживаться клетки в течение нескольких дней в культуре. Мы не можем исключить возможность того, что эти комплексы, а не открыто токсичны для клеток, может иметь более тонкие эффекты на клеточные процессы.
Здесь мы описали методологию безопасно и эффективно трансдуцирующих человеческие клетки с онкогенными факторами. Этот подход должен быть очень утилита для исследователей, изучающих онкогенов и биологии стволовых клеток, в том числе плюрипотентных клеток.
Нет конфликта интересов объявлены.
Финансирование этого проекта была предоставлена Калифорнийского института регенеративной медицины.
| Name | Company | Catalog Number | Comments |
| pLenti6/UbC/mSlc7a1 | Addgene | 17224 | Murine MLV receptor |
| pMD2.G | Addgene | 12259 | VSV-G envelope |
| pCMV-dR8.91 | Addgene | D. Trono lab 14 Packaging plasmid (equivalent plasmid psPax2 is available from Addgene, Cat. Number 12260) | |
| pHCMV-Ec–nv | Addgene | 15802 | Ecotropic envelope |
| FUGW | Addgene | 14883 | GFP control plasmid |
| OptiMEM | Invitrogen | 31985 | |
| Fugene HD | Roche Group | 04 709 705 001 | |
| Hexadimethrine bromide (Polybrene) | Sigma-Aldrich | H9268 | |
| Chondroitin sulfate sodium salt from shark cartilage | Sigma-Aldrich | C4384 | |
| Blasticidin S | Fisher Scientific | BP 2647100 | |
| Methylthiazolyldiphenyl-tetrazolium bromide (MTT) | Sigma-Aldrich | M2128 | |
| Igepal CA-630 | Sigma-Aldrich | I3021 |
- Davis, H. E., Rosinski, M., Morgan, J. R., Yarmush, M. L. Charged polymers modulate retrovirus transduction via membrane charge neutralization and virus aggregation.Biophys J. 86, 1234-1242 (2004).
- Marino, M. P., Luce, M. J., Reiser, J. Small- to large-scale production of lentivirus vectors.Methods Mol Biol. 229, 43-55 (2003).
- Landazuri, N., LeDoux, J. M. Complexation of retroviruses with charged polymers enhances gene transfer by increasing the rate that viruses are delivered to cells.J Gene Med. 6, 1304-1319 (2004).
- Ohnuki, M., Takahashi, K., Yamanaka, S. Generation and characterization of human induced pluripotent stem cells.Curr Protoc Stem Cell Biol. 4, 4A.2-4A.2 (2009).
- Hotta, A. EOS lentiviral vector selection system for human induced pluripotent stem cells.Nat Protoc. 4, 1828-1844 (2009).
- Reiser, J. Transduction of nondividing cells using pseudotyped defective high-titer HIV type 1 particles.Proc Natl Acad Sci U S A. 93, 15266-15271 (1996).
- Cullen, B. R. Journey to the center of the cell.Cell. 105, 697-700 (2001).
- Cronin, J., Zhang, X. Y., Reiser, J. Altering the tropism of lentiviral vectors through pseudotyping.Curr Gene Ther. 5, 387-398 (2005).
- Schambach, A. Lentiviral vectors pseudotyped with murine ecotropic envelope: increased biosafety and convenience in preclinical research.Exp Hematol. 34, 588-592 (2006).
- Koch, P., Siemen, H., Biegler, A., Itskovitz-Eldor, J., Brustle, O. Transduction of human embryonic stem cells by ecotropic retroviral vectors.Nucleic Acids Res. 34, e120-e120 (2006).
- Yoshimoto, T., Yoshimoto, E., Meruelo, D. Molecular cloning and characterization of a novel human gene homologous to the murine ecotropic retroviral receptor.Virology. 185, 10-17 (1991).
- Cepko, C. Large-scale preparation and concentration of retrovirus stocks.Curr Protoc Mol Biol. Chapter 9, Unit 9.12-Unit 9.12 (2001).
- Doux, J. M. L. e, Landazuri, N., Yarmush, M. L., Morgan, J. R. Complexation of retrovirus with cationic and anionic polymers increases the efficiency of gene transfer.Hum Gene Ther. 12, 1611-1621 (2001).
- Zufferey, R. Self-inactivating lentivirus vector for safe and efficient in vivo gene delivery.J Virol. 72, 9873-9880 (1998).
You must be signed in to post a comment. Please sign in or create an account.
This content is Open Access.
Читайте также:


