Стволовые клетки лечить гепатит в
ДЛЯ ТОГО ЧТОБЫ СКАЧАТЬ СТАТЬЮ В ФОРМАТЕ PDF ВАМ НЕОБХОДИМО АВТОРИЗОВАТЬСЯ, ЛИБО ЗАРЕГИСТРИРОВАТЬСЯ
Согласно современным представлениям, восстановление поврежденных тканей и органов взрослого организма осуществляется при участии низкодифференцированных или стволовых клеток. Основным источником стволовых клеток является костный мозг, способный генерировать клетки-предшественники для большого числа тканей организма. В экспериментах на животных была показана возможность стимуляции регенерации печени аутогенными стволовыми клетками костного мозга [1, 2] и аллогенными стволовыми клетками пуповинной крови [3]. Получены первые положительные результаты лечения заболеваний печени у людей - установлена высокая эффективность применения ал-логенных стволовых клеток пуповинной крови при лечении вирусных гепатитов [4]. Более того, стволовые клетки с фенотипом CD133+, полученные из крови больных и введенные в печень через воротную вену, в 2,5 раза ускоряли процесс регенерации печени после резекции опухоли [5]. Положительная динамика функциональных проб печени была отмечена в рамках первой фазы клинических исследований, когда больным хроническими гепатитами [5 человек] была проведена трансплантация аутогенных стволовых клеток с фенотипом CD34+ [6]. Таким образом, к моменту начала нашей работы имелись теоретические, экспериментальные и клинические предпосылки для проведения ограниченных клинических испытаний применения аутологичных гемопо-этических клеток в терапии хронических гепатитов.
Методика исследования
На первом этапе после тщательного анализа литературы нами был разработан протокол клинических исследований. Отличительными чертами разработанного протокола являются: 1) способ трансплантации стволовых клеток в печень; 2) критерии оценки эффективности трансплантации.
Выбор способа трансплантации
В экспериментах на животных для стимуляции регенерации печени стволовые клетки чаще всего вводят внутри-брюшинно или в селезёнку, из которой они через воротную вену поступают в печень. В протоколах клинических исследований по применению стволовых клеток при хронических гепатитах и после резекции печени клетки вводили либо в периферический кровоток [7] [при этом большая часть клеток диссеминировалась по организму), либо в воротную вену -в этом случае все клетки поступали в печень с венозной кровью [5, 6].
Целью нашего исследования было изучение возможности использования стволовых клеток в лечении не просто хронических гепатитов, а хронических гепатитов в стадии тяжелого фиброза и цирроза. В этой стадии у больных развивается портальная гипертензия, причем введение клеток в воротную вену на фоне портальной гипертензии может вызвать внутреннее кровотечение в месте введения иглы. Исходя из этого, мы предположили, что клетки безопаснее вводить не в воротную вену, а в артериальный кровоток. Причем стволовые клетки целесообразнее вводить не в печёночную артерию, а в чревный ствол [рис. 1), от которого отходят печёночная артерия, левая желудочная артерия и селезёночная артерия [рис. 2). В результате такого введения часть клеток сразу попадает в печень по общей печёночной артерии, а те клетки, которые ушли к желудку и селезёнке, могут попасть в печень с венозной кровью через воротную вену [рис. 3).
Преимуществом предложенного метода введения, по нашему мнению, является не только его безопасность, но и возможность воздействовать стволовыми клетками на разные участки печеночной дольки. Дело в том, что кровь в печень поступает по двум сосудам - воротной вене [венозная кровь от всех непарных органов брюшной полости) и печеночной артерии [артериальная кровь из аорты). Венозная кровь составляет до 80% всей крови, проходящей через печень, и из мелких портальных вен она напрямую поступает в синусоидные капилляры железы. Артериальная кровь, перед тем как попасть в синусоиды, снабжает питательными веществами и кислородом все структуры портальных трактов и, в частности, желчные протоки [8]. Даже при легком перипортальном фиброзе происходят изменения в желчных протоках, которые сначала приводят к их компенсаторной пролиферации [дуктулярной реакции), а в дальнейшем к дук-топении с нарушением экскреторной функции печени [9]. В предложенном нами методе стволовые клетки могут действовать как внутри дольки [с венозной кровью), так и в области портальных трактов [с артериальной кровью).
Критерии оценки эффективности трансплантации
Кроме того, в протокол исследований, наряду с обязательным определением степени активности и стадии заболевания, были введены методы иммуногистохимической оценки: 1) пролиферативной активности клеток печени [по экспрессии ядерного антигена пролиферирующих клеток, Proliferating Cell Nuclear Antigen, PCNA); 2) активации миофибробластов [по экспрессии альфа-гладкомышечного актина, а-ГМА); 3] капилляризации синусоидов [по экспрессии CD34).
Уровень пролиферации позволяет судить о выраженности регенераторного ответа гепатоцитов на повреждение.
а-ГМА - это один из контрактильных белков гладкой мышцы, который в здоровой печени обнаруживается только в мышечных клетках сосудов печени. При хроническом повреждении печени происходит трансдифференцировка перисинусоидальных клеток печени в миофибробласты, которые усиленно синтезируют коллаген, что приводит к развитию фиброза. Маркером миофибробластов является а-ГМА. Появление а-ГМА-позитивных миофибробластов, таким образом, приводит к отложению новых волокон коллагена и прогрессированию фиброза.
CD34 - это гликопротеин, который находится на наружной поверхности мембраны эндотелиальных клеток и проге-ниторных кроветворных клеток. В частности, его используют при выделении стволовых кроветворных клеток в качестве их маркера. При морфологическом исследовании биопта-тов CD34 интересовал нас как маркер эндотелия синусои-дов печени. Дело в том, что эндотелий синусоидов печени отличается от эндотелия капилляров других органов. Во-первых, он фенестрированный, во-вторых, у него нет сплошной базальной мембраны, и поэтому на мембране эндотелиальных клеток нет молекулы CD34. CD34 появляется в эндотелии синусоидов только при так называемой капилляризации последних. В этом случае в пространстве Диссе откладывается коллаген [перисинусоидальный фиброз), формируется подобие базальной мембраны и нарушается диффузия веществ из крови к гепатоцитам. Таким образом, появление CD34 в синусоидах позволяет судить о нарушении гемодинамики в синусоидах печени.
Для проведения морфологического анализа биоптаты печени фиксировали в 10% нейтральном формалине и заливали в парафин по стандартной методике. Иммуногисто-химическое окрашивание срезов печени проводили стреп-тавидин-биотиновым методом [10] с использованием коммерческих моноклональных антител к PCNA, а-ГМА, CD34 и визуализационных систем фирм DAKO [Дания] и NOVOCASTRA [Великобритания).
Отбор больных
Критерием включения пациентов в программу клинических исследований было, согласно утвержденному протоколу, наличие хронического токсического [этанолового) гепатита и тяжелого фиброза печени. В настоящий момент в клиническом исследовании находятся 3 пациента и отобрано еще 12. Все больные до включения в программу исследований прошли курс стационарного лечения, состоявший из гепа-тотропных препаратов [Урсосан, Карсил и т.д.). У пациентов не было выраженных изменений функциональных проб печени: отмечены повышение аланинаминотрансферазы [АЛТ, в среднем в 2 раза) и у-глутаминтранспептидазы [у-ГТП, в 2-4 раза) и снижение протромбинового индекса [до 70%). При ультразвуковом исследовании печени обнаружены повышение эхогенности и диффузная неоднородность ее паренхимы. Перед началом лечения всем больным была проведена пункционная биопсия печени.
Получение стволовых клеток
Результаты и обсуждение
Наблюдение за больными в течение 4-х недель после введения стволовых клеток показало улучшение общего самочувствия, повышение работоспособности, исчезновение слабости и дискомфорта в правом подреберье. Через месяц после введения стволовых клеток у всех больных снизились показатели цитолиза, повысился протромбиновый индекс, произошло снижение у-ГТП [в одном случае до нормы) [табл. 1).
Согласно протоколу, всем больным была проведена пунк-ционная биопсия печени до трансплантации стволовых клеток и через месяц после трансплантации. Сравнительный анализ индекса гистологической активности [ИГА) представлен в табл. 2.
Через месяц после трансплантации у всех больных произошло снижение ИГА на 2-3 балла. За счет чего произошло это снижение? В первую очередь, за счет уменьшения внутридольковых некрозов и дегенераций паренхимы и портального воспаления. К сожалению, выраженность некрозов вокруг портальных трактов не изменилась, и в био-птатах отмечены порто-портальные мостовидные некрозы. Эти некрозы всегда были локализованы в области портопортальных соединительнотканных септ, за счет которых у больных был диагностирован тяжелый фиброз [3 балла).
Очевидно, что один месяц - недостаточный срок для разрешения фиброза. В то же время снижение ИГА за счет уменьшения внутридольковых дегенераций и портального воспаления отражает позитивные изменения в состоянии печени после трансплантации. Более того, благоприятные морфологические изменения в паренхиме печени объясняют и положительную динамику биохимических показателей.
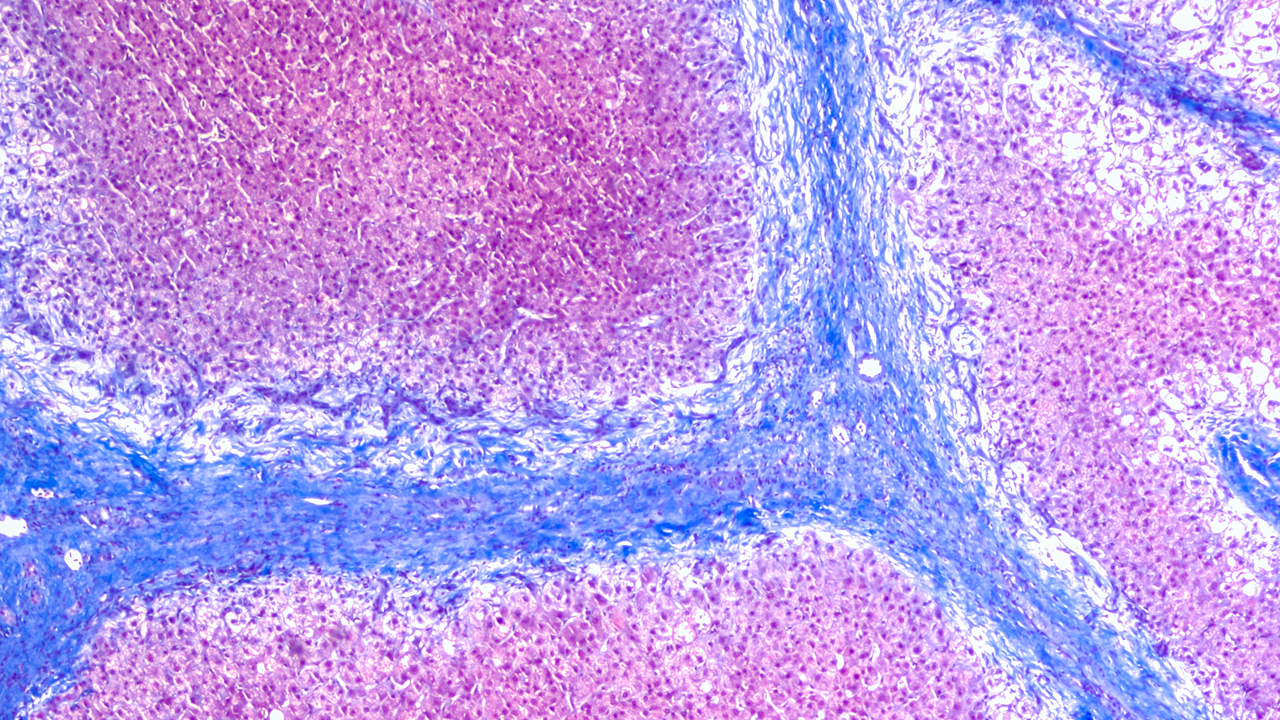
Наиболее выраженным морфологическим изменением, которое мы обнаружили, было исчезновение соединительной ткани из пространства Диссе. До трансплантации у всех больных был выявлен перисинусоидальный фиброз, а через месяц после трансплантации стволовых клеток мы не обнаружили отложения коллагеновых волокон между эндотелием и гепатоцитами [рис. 4). Согласно протоколу, биоптаты окрашивали антителами против PCNA, а-ГМА и CD34. Данные иммуногистохими-ческого исследования представлены в таблице 3. Два факта обращают на себя внимание - резкое снижение пролиферативной активности гепатоцитов и исчезновение CD34 в мембранах эндотелия синусоидов после трансплантации.
Высокая пролиферативная активность в гепатоцитах до трансплантации [рис. 5А) указывает на напряженность регенераторного ответа. Такого рода напряженность всегда наблюдается при повреждении гепатоцитов и является ответной реакцией на уменьшение клеточной массы или повреждение гепатоцитов. Через месяц после трансплантации число пролиферирующих гепатоцитов было в пределах 1-5%, что является показателем, близким к норме [рис. 5Б).
Интересные изменения произошли после трансплантации стволовых клеток с эндотелием синусоидов. У всех больных до трансплантации была выражена капилляризация си-нусоидов - эндотелиальные клетки экспрессировали CD34 [рис. 6А). Такого рода изменения фенотипа эндотелия в синусоидах печени указывают на то, что фенестрированный эндотелий стал менее проницаемым. Через месяц после трансплантации ситуация кардинально изменилась - в синусоидах обнаруживали лишь единичные CD34+ эндотелиальные клетки [рис. 6Б).
Определенные изменения наблюдались и в экспрессии а-ГМА. До трансплантации у всех больных внутри соединительнотканных септ присутствовали миофибробласты [рис. 7А), что указывало на продолжающийся синтез компонентов соединительной ткани и прогрессирование фиброза. У одного больного миофибробласты были обнаружены и в синусоидах, что является неблагоприятным прогностическим фактором в плане дальнейшего фиброзирования паренхимы печени. После трансплантации количество миофибробластов заметно уменьшилось, и немногочисленные а-ГМА+ клетки обнаруживали только в пределах уже сформированных соединительнотканных септ, в основном же а-ГМА присутствовал в гладкомышечных клетках кровеносных сосудов [рис. 7Б).
Поскольку именно миофибробласты являются основным источником соединительной ткани в регенерирующей печени, уменьшение их числа объясняет как восстановление нормальной структуры синусоидных капилляров, так и исчезновение перисинусоидального фиброза.
Результаты проведенного исследования позволяют заключить, что трансплантация аутогенных гемопоэтических стволовых клеток в чревный ствол больным хроническим гепатитом в стадии тяжелого фиброза является безопасной процедурой. Через месяц после трансплантации аутогенных гемопоэтических стволовых клеток улучшаются общее состояние больного и показатели функциональных проб печени, происходят положительные изменения в морфологии печени [снижается индекс гистологической активности за счет уменьшения выраженности портального воспаления и внутридольковых некрозов). Однако самым важным результатом трансплантации гемопоэтических стволовых клеток является то, что в печени происходят качественные структурные изменения - значительно снижается пролиферация гепатоцитов, уменьшается число миофибробластов в паренхиме, что приводит к разрешению перисинусоидального фиброза и восстановлению нормального строения синусоидных капилляров. Таким образом, полученные результаты позволяют сделать вывод о перспективности данного метода лечения для подавления прогрессирования гепатита и фиброзирования печени и о высокой информативности иммуногистохимических методов в оценке эффективности трансплантации.
Уже доказано — стволовые клетки могут помочь там, где бессильны фармацевтика и хирургия. В свое время в клинике Мешалкина трансплантация стволовых клеток помогла продлить жизнь пациентов, которые фактически были обречены. Сегодня в Новосибирске лицензия на работу со стволовыми клетками есть только у одного института — иммунологии. Что мешает распространению клеточных технологий в медицине — и на что способны супер-клетки — обсуждали на этой неделе ведущие специалисты России, Германии и Индии в Академгородке на первом всероссийском симпозиуме. И оказалось — в вопросе применения стволовых клеток нет единства даже среди ученых.
Еще два месяца назад жил спокойной жизнью и не знал, что такое больница — рассказывает Вячеслав. А потом как обухом по голове.
При циррозе печень перерождается — ее клетки отмирают, их место занимает клетки соединительной ткани, и орган перестает выполнять свои функции. Вылечить болезнь нельзя. Только пересадка печени. Но процесс можно затормозить. В новосибирском институте иммунологии первыми в мире начали применять для этого самое мощное оружие человека — стволовые клетки.
Это титопотентные клетки. Только из них может развиться новый организм целиком. Эту суперсилу эмбриональные клетки теряют уже на пятые сутки развития. Тем не менее, они все еще могущественны — плюрипотентны. Именно из них берут начало все ткани. У взрослого человека стволовые клетки тоже есть, но не так универсальны — могут превратиться в определенные ткани. Они поддерживают организм. Например, клетки крови живут около 4-х месяцев. Умирающих заменяют стволовые кроветворные клетки. Выстилающие клетки кишечника полностью обновляются за 4 дня — за восстановление их отвечают находящиеся за ними стволовые.
Эмбриональные стволовые клетки могущественны, но опасны. Уже доказано — они могут перерождаться в опухолевые клетки, вызывая рак. Кроме того, исследования на человеческих эмбрионах запрещены. Возможный выход из тупика нашли недавно — в 2007-м японцы доказали — клетку ткани взрослого человека можно индуцировать — превратить в стволовую, плюрипотентную
Вот так, в жидком азоте в лаборатории института цитологии и генетики СО РАН хранятся коллекции индуцированных стволовых клеток. Как лучше получать такие клетки, как управлять процессом их дальнейших превращений в ткани — вопросы, на которые сегодня ищут ответы сибирские ученые. Более того — в клетки вносят мутацию, вызывающую болезнь — чтобы изучить генетические поломки и, возможно, найти новые способы их лечения. В этих пробирках — болезни Паркинсона, сахарного диабета, боковой амиотрофический склероз — тот самый, ради которого по всему миру сейчас обливаются ледяной водой с Айс Бакет Челендж. Перспективы молекулярных исследований грандиозны. Это порождает вокруг стволовых клеток множество спекуляций.
Но наука не стоит на месте. Ученые ищут возможности обойти ловушки природы. На международном конгрессе в Академгородке докладывают — москвичи сумели вырастить биоисскуственную печень! И успешно вживили ее крысам. Заменить доноров собственными стволовыми клетками пациента — светлое будущее транспланталогии. Такие органы не должны отторгаться.
Чтобы доказать, что биоискусственные органы безопасны для человека — одного примера мало. Однако, как подчеркивают все специалисты — в России исследовать стволовые клетки сложнее, чем на Западе. Элементарно — дороже.
Сдерживает развитие технологий отсутствие федерального закона. Нет правовой основы — нет финансирования исследований. Закон разрабатывают уже пять лет. А пока инициатива снизу.
И все же — хотя выращивание органов — будущее, в настоящем стволовые клетки уже лечат людей. Не эмбриональные — взятые у взрослого человека и обработанные. Им даже не надо превращаться в ткань — они способны заставить работать другие клетки в организме.
Именно так в институте иммунологии лечат цирроз печени и неврологические болезни — у пациента берут костный мозг, выделяют из него стволовые клетки, специальным образом обрабатывают, размножают и заново пересаживают. Ради таких клеточных технологий Вячеслав приехал в Новосибирск за пять тысяч километров. И уже получил свою порцию стволового чуда.
Клетки печени начнут восстанавливаться — их перерождение остановится, это доказывают уже две сотни пациентов. Это подтверждают участники исследований в клинике Мешалкина — которым стволовые клетки помогали дожидаться пересадки сердца годами. Это то, что сибиряки уже могут предложить миру. Вопреки всему.

Цирроз печени. Стволовые клетки как надежда для неизлечимо больных.
Регенеративная медицина занимается восстановлением функции органа или его поврежденной части. Настоящий прорыв в лечении даже смертельных патологий – это трансплантация органов и клеток. Однако нехватка донорских органов не позволяет спасти всех пациентов. В Швейцарии, например, ежегодно погибают более 500 пациентов, имеющих алкогольный (токсический) цирроз печени. Как оказалось, цирроз печени – неизлечимая болезнь
В развитых странах пересадка клеток и органов используется при многих неизлечимых заболеваниях. Однако данная терапия не всегда доступна по причине её высокой стоимости и отсутствия доноров. С одной стороны, трансплантация органов – инвазивная операция, которая подразумевает наличие большого количества рисков, но с другой стороны, трансплантация часто является единственным шансом на выздоровление.
Многие пациенты не теряют надежду и верят, что трансплантация островков Лангерганса, гепатоцитов, мезенхимальных стволовых клеток и дофаминергических нейронов сможет им помочь.
Швейцария занимает одно из последних мест по количеству доноров, поэтому Швейцарские учёные особое внимание уделяют биомедицине. Биомедицина является менее инвазивной, а культивирование клеток in vitro делает этот процесс более доступным с точки зрения этики. Трансплантация клеток уже давно широко используется в медицине наряду с аллогенной трансплантацией гемопоэтических стволовых клеток, которая с 1960-х годов применяется при лечении лейкемий, миелом и лимфом.
В Женеве трансплантация клеток островков Лангерганса поджелудочной железы начала применяться с 1992 года для лечения сахарного диабета первого типа. Клетки островков Лангерганса после трансплантации начинают вырабатывать инсулин, регулируя при этом уровень глюкозы в крови. С 1992 по 2018 год в Женеве было произведено более 275 трансплантатов, в результате чего Женева и сеть GRAGIL стали мировым лидером в данной области.
Следуя этому примеру, французские лаборатории в настоящий момент разрабатывают трансплантацию гепатоцитов для лечения фульминантного гепатита, мезенхимальных стволовых клеток (MSC) для лечения цирроза и дофаминергических нейронов для лечения болезни Паркинсона.
Данные методы лечения уже показали свою эффективность, однако, чтобы их широко применять на практике, требуется дополнительное изучение принципа их работы. Исследования пересаженных клеток показали, что некоторые клетки со временем могут трансформироваться в опухоль.
ПЕРЕСАДКА МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК ПРИ ЦИРРОЗЕ ПЕЧЕНИ.

В западных странах, цирроз печени является третьей по распространенности причиной смерти среди пациентов 45-65 лет, страдающих от данного недуга. Лечение цирроза печени может включать симптоматическую терапию, лечение сопутствующих заболеваний (гепатита B и С), отсутствие токсического воздействия на печень (прекращение употребления алкоголя), а также трансплантацию печени.
К сожалению, данное лечение может быть применимо не ко всем пациентам – могут иметься противопоказания: отсутствие необходимых прививок, неудачный опыт лечения алкоголизма, частые рецидивы, возраст пациента, общее состояние здоровья…
Именно поэтому внимание ученых привлекли, взрослые стромальные клетки-предшественники MSC (mesenchymal stem cells), первоначально идентифицированные в костном мозге. Данные клетки ученые хотят использовать для разработки антифибротической терапии.
Действительно, MSC имеют способность превращаться в клетки, выполняющие функции гепатоцитов. Они обладают иммуномодулирующими свойствами и синтезируют множество противовоспалительных цитокинов. Данные свойства и относительно несложное культивирование мезенхимальных стромальных клеток in vitro позволяют считать MSC идеальным аутологичным источником антифибротических методов лечения.
В доклинических исследованиях, трансплантация МСК позволила снизить уровень смертности животных, страдающих печеночной недостаточностью, и использовалась при лечении фиброза печени.
Клинические исследования, во время которых люди принимали капсулированные МSC, показали некоторое улучшение состояния печени и уменьшение степени фиброза. Исследования фазы I,II показали также улучшения функций печени, повреждённой алкоголем или гепатитом B и С. Однако данные улучшения остаются незначительными, так как позволяют опустить результаты анализов на один балл по шкале MELD (Model For End-Stage Liver Disease).
Данная терапия также назначалась больным непосредственно перед трансплантацией, чтобы способствовать приживаемости имплантируемого органа. Это является очень важным открытием, так как после трансплантации может быть отторжение вживляемого органа, что предполагает пожизненное тяжелое лечение.
Несмотря на благоприятные результаты, в некоторых случаях пересаженные клетки ведут себя не совсем понятным образом. Наблюдается частая трансформация в злокачественные опухоли или же необъяснимое инфицирование.
Врачи и учёные не опускают руки и продолжают искать эффективный способ лечения цирроза печени. В настоящий момент самыми действенными способами остаются пересадка печени и отказ от разрушающего агента (алкоголя). В некоторых случаях прописываются витамины, БАДы и поддерживающая терапия. Однако данная терапия не способна восстановить функции печени и тем более противостоять токсическому воздействию алкоголя.
Стволовые клетки — это особые клетки, способные преобразовываться в любые другие клетки организма: кости, мышцы, сердце, печень и т. д. В случае массового разрушения клеток из-за болезни или травмы мезенхимальные стволовые клетки активируются и из них образуются новые клетки взамен поврежденных.
По прогнозу ВОЗ, через десять лет 30% пациентов клиник будут получать инъекции мезенхимальных стволовых клеток.
1. Эмбриональные, фетальные (из плода) и взрослые.
2. Мезенхимальные (мультипотентные), олиго- или юнипотентные (гемопоэтические, например).
Из мезенхимальных могут образовываться клетки большинства органов и тканей, из гемопоэтических — только клетки крови. Поэтому для лечения лучше использовать первые.
3. Стволовые клетки, полученные из жировой или костномозговой ткани.
Наилучшими свойствами обладают стволовые клетки, полученные из костного мозга. Костномозговые клетки в четыре раза активнее и эффективней. Находясь в кости, они наиболее защищены от внешних воздействий.
4. По источнику: собственные и донорские;
Использование клеток молодых здоровых доноров наиболее эффективно.
При введении в организм донорские стволовые клетки не только восстанавливают поврежденные ткани, но и вырабатывают биологически активные вещества, стимулирующие собственные стволовые клетки пациента и обновляющие клеточный состав больного органа. В результате происходит быстрый метаболизм печеночных токсинов и стабилизация гемодинамических параметров, которая отмечается значительным улучшением биохимических показателей крови (альбумин, билирубин, АЛТ, АСТ).
Мезенхимальные стволовые клетки обладают уникальной особенностью — после инъекции пациенту они самостоятельно мигрируют к пораженным участкам в организме. Это объясняется присутствием в них особых хеморецепторов, подобных тем, которые известны у лейкоцитов. Таким образом, стволовые клетки сами находят места, требующие лечения.
Также доказано свойство мезенхимальных стволовых клеток подавлять пролиферацию звездчатых клеток печени, называемых клетками Ито. Это открытие успешно используется в клеточной терапии фиброзов печени, так как известно, что на ранних стадиях фиброгенеза активируются именно клетки Ито.

Печень — жизненно важный орган, расположенный в брюшной полости под диафрагмой и выполняющий множество функций.
- Детоксикация (обезвреживание) различных вредных веществ, поступающих с пищей, аллергенов, токсинов и других ядовитых веществ, образующихся в процессе жизнедеятельности.
- Участие в процессах пищеварения, а именно обеспечение энергетических потребностей организма глюкозой и преобразование различных источников энергии (свободных жирных кислот, аминокислот и т. д.) в глюкозу.
- Пополнение и хранение энергетических запасов в виде гликогена, витаминов A, D, B12, Fe, Cu, Co и др.
- Участие в метаболизме витаминов A, B, C, D, E, K, ПП и фолиевой кислоты.
- Синтез белков, жиров, гормонов, крови.
- Синтез желчи.
Клетки печени обновляются каждые 300–500 дней. Если не использовать алкоголь, ограничить потребление жирного, острого, фастфуда, лекарств, то печень может быть полностью очищена через восемь недель. Кстати, печень является единственным органом в нашем организме, который способен полностью справиться с потерей 75% своей ткани.
Цирроз — осложнение многих заболеваний печени, которое характеризуется изменением структуры печени и ее функции. При этом хроническом заболевании гепатоциты (клетки паренхимы печени) теряют свою функциональность и замещаются рубцовой (соединительной тканью).
Основные причины, которые приводят к циррозу печени:
- хронический алкоголизм;
- вирусные гепатиты В, С, D;
- нарушения обмена веществ и некоторые наследственные заболевания;
- действие некоторых токсинов и лекарственных препаратов;
- заболевания желчевыводящих путей и паразиты.
Внутривенная инъекция стволовых клеток была предложена сравнительно недавно и на сегодняшний день стала наиболее перспективной терапией для заболеваний печени.
Многочисленные исследования продемонстрировали, что мезенхимальные стволовые клетки способны к дифференциации в функциональные клетки печени — гепатоциты. После чего пораженная паренхима печени регенерируется за счет замещения больных клеток здоровыми.
На данный момент во многих странах уже существуют специализированные клиники по лечению стволовыми клетками, поэтому самая важная вещь в клеточной терапии цирроза — как можно раньше начать лечение, так как это дает больше шансов на восстановление ткани печени. Лечение цирроза печени стволовыми клетками основано на их уникальном свойстве — способности заменить поврежденные клетки тканей.
И есть ли смысл в клеточной косметике


О стволовых клетках в последние годы приходится слышать в самом разном контексте: их предлагают использовать в косметических процедурах и даже добавляют в кремы, учатся добывать из молочных зубов и пуповины, используют в лечении самых разных заболеваний. Часто в новостях сообщают о новых возможностях их использования, которые ещё долго предстоит изучать в лаборатории; в итоге одним стволовые клетки представляются чем-то из будущего, а другим кажется, что они уже стали обыденностью и используются в любом салоне красоты. Разбираемся, что вообще представляют собой стволовые клетки, для чего они часто применяются уже сейчас и какая польза возможна пока только в теории.

Откуда добывают
стволовые клетки
Стволовые клетки — это так называемые недифференцированные клетки, которые могут превращаться в разные клетки организма — а у человека их более двухсот — с различными свойственными им функциями. Например, у нервных клеток или клеток крови есть узкие, специфические задачи — и всю энергию они тратят на выполнение этих задач, не растрачиваясь на размножение. А новые эритроциты или нейроны возникают из стволовых клеток, которые есть у каждого человека в любом возрасте. Они бывают разных видов: одни способны дифференцироваться только в один тип клеток, другие — в несколько; стволовые клетки эмбриона на раннем сроке беременности могут преобразоваться в любой тип клеток организма.
Для чего их используют
Сама процедура пересадки костного мозга не похожа на классическую трансплантацию — доктор не распиливает кости и не заменяет их содержимое новым. Трансплантация костного мозга выглядит как переливание крови — кстати, и донорство костного мозга может осуществляться как сдача крови. С другими тканями пока дело обстоит сложнее: для пересадки кожи или роговицы ткань из стволовых клеток сначала нужно вырастить в питательной среде, а это дорогостоящие процессы, для которых нужны идеальные условия. По словам исследователей, государства пока не готовы финансировать такие методы, а для коммерческих структур это не очень выгодно из-за относительно низкого спроса.

Возможны ли зубы из пробирки
Когда стало понятно, что нервные клетки всё-таки восстанавливаются благодаря стволовым, началось активное изучение того, как с их помощью лечить пациентов с заболеваниями нервной системы. Это болезнь Паркинсона, боковой амиотрофический склероз, болезнь Альцгеймера, травмы спинного мозга, рассеянный склероз. Учитывая, что эмбриональная стволовая клетка может превратиться в любую другую, они теоретически могут использоваться и у пациентов с заболеваниями сердца, печени или костей.
Нужно ли хранить клетки
про запас
Ещё один распространённый вариант — банк пуповинной крови; чтобы сохранить в нём стволовые клетки, пуповину нужно перерезать как можно раньше после рождения ребёнка, буквально в течение пары секунд. Эти банки бывают двух видов: частные и публичные (чаще всего с государственным финансированием). В публичный банк кровь отдаётся бесплатно — но воспользоваться ею конкретный ребёнок уже не сможет. Образец анонимизируют для хранения, полностью описав его характеристики, и могут через какое-то время выдать по запросу той или иной больницы, чтобы провести трансплантацию. Пуповинная кровь и стволовые клетки из публичных банков могут использоваться и в исследовательских целях.
В частном банке за хранение крови нужно платить, но в случае необходимости — например, если у ребёнка диагностировали лейкоз — собственные стволовые клетки действительно могут спасти жизнь. Правда, пока, по данным исследователей, вероятность того, что до двадцати одного года у человека разовьётся заболевание, вылечить которое можно будет его собственными стволовыми клетками, составляет от 0,005 % до 0,04 % — то есть стремится к нулю. Вероятность того, что стволовые клетки пригодятся для лечения кого-то из кровных родственников, ещё ниже. Вероятно, эти показатели повысятся, когда стволовые клетки действительно начнут использоваться в лечении частых заболеваний — инсультов или сахарного диабета. Но на сегодняшний день услуги частного банка пуповинной крови лишь способ потратить немалые деньги.
Зачем стволовые клетки добавляют в кремы
В косметику действительно добавляют стволовые клетки — но не человеческие или животные, а растительные; один из самых популярных источников клеток для этого — яблоня. Понятно, что в составе крема ни размножаться, ни дифференцироваться клетки не могут — но это и не нужно. Этими растительными клетками никто не пытается заменить человеческие: из стволовой клетки яблони, даже если бы она могла сохранить свойство к размножению, не получились бы новые клетки кожи человека.
У разработчиков косметики совсем другие задачи: стволовые клетки растений содержат активные субстанции, поддерживающие чувствительность клеток кожи к гормонам и нейромедиаторам — веществам, передающим самые разные сигналы в организме. Эксперименты показывают, что составы с растительными стволовыми клетками делают обратимыми возрастные изменения кожи и замедляют старение волосяных фолликулов — но нужно понимать, что в данном случае действие стволовых клеток не прямое, как при лечении лейкоза, а косвенное.
Читайте также:


