Разрешившийся острый гепатит в сероконверсия что это
Серодиагностика вирусного гепатита В
 |
| Рисунок 1. Структура вируса гепатита В |
Основой лабораторной диагностики HBV инфекции является определение серологических маркеров инфицирования вирусом: HBsAg, HBeAg, анти-НВс класса IgM и IgG, анти-НВе и анти-HBs, HBV ДНК и активности вирусной ДНК - полимеразы. В зависимости от течения вирусного гепатита В спектр изменения серологических маркеров выглядит по-разному.
HBeAg – вирусспецифический белок, является отдельным антигеном вируса. При острой инфекции, которая завершается выздоровлением, HBeAg появляется в сыворотке крови вслед за поверхностным белком вируса и перестает обнаруживаться до исчезновения HBsAg. При хронической инфекции HBeAg присутствует в крови длительные сроки, свыше 6 месяцев. Обнаружение HBeAg в сыворотке крови служит косвенным доказательством активной вирусной репликации.
HBсAg – сердцевинный антиген, обнаруживается только в ткани печени, поэтому практического значения этот маркер не имеет.
Большую диагностическую значимость имеют антитела к этому антигену (анти-НВс). Анти-НВс начинают определяться в крови после появления первых клинических симптомов заболевания. Маркером ранней инфекции являются анти-НВс класса IgM. Определение их является одним из достоверных серологических критериев острого вирусного гепатита В.
Анти-HBc IgM выявляются через 1-2 недели после обнаружения HBsAg и сохраняются на протяжении 2-18 месяцев. У 4-20 % больных острым гепатитом В анти-HBc IgM являются единственным маркером инфекции. При хроническом вирусном гепатите В анти-НВс IgM могут быть выявлены у некоторых больных в меньших титрах, чем при острой инфекции, причем титр антител отражает тяжесть гепатита.
Анти-HBc IgM постепенно замещаются анти-НВс класса IgG. Антитела этого класса удается обнаружить как у больных острым гепатитом В на различных стадиях инфекционного процесса, так и у больных хроническим вирусным гепатитом В, а также у лиц, перенесших в прошлом гепатит В и выздоровевших. Интерпретацию результатов в тестируемом образце проводят только с учетом выявления других маркеров инфекции.
Антитела к HBsAg (анти-НВs) свидетельствуют о ранее перенесенной инфекции или о наличии поствакцинального иммунитета (защитный уровень - 10 МЕ/мл). Они появляются в период выздоровления, через 4 недели после исчезновения HBsAg, достигая максимальной концентрации через 1-2 года, с последующим постепенным снижением уровня, недоступного выявлению современными методами диагностики. Анти-HВs обычно персистируют длительно, возможно в течении всей жизни. Появление анти-HBs на фоне клинического улучшения у больного гепатитом В является хорошим прогностическим признаком. Важно отметить, что в динамике острой инфекции HBV имеется "окно", когда HBsAg уже не определяется, а анти-HBs еще не появились. При этом выявляются анти-HBc IgM и IgG. Из этого следует вывод о необходимости обследования больных ОВГ на анти-HBc IgM даже при отрицательных результатах исследования HBsAg и анти-НВs.
Антитела к HBeAg (анти-НВе) появляются в крови после элиминации HBeAg и завершения репликации вируса. К концу 9-й недели острого периода гепатита В более 90% больных имеют анти-НВе. В период выздоровления анти-НВе могут исчезать. Однако, наличие анти-НВе не является показателем отсутствия инфекционности конкретной сыворотки крови. Показано, что у ряда больных в ходе развития гепатита В (около 10%) под влиянием "иммунного давления" на вирус возникают мутантные формы, которые "избегают" иммунного надзора и не элиминируются. У носителей анти-HBe был выделен мутант, неспособный продуцировать HBeAg из-за дефектов в области precore и получивший обозначение HBeAg-отрицательного. Появление HBeAg-отрицательного мутанта приводит к прогрессированию поражения печени при продолжающейся репликации вируса (наличие ДНК HBV в сыворотке крови). При первичном инфицировании HBeAg-отрицательным мутантом существенно возрастает риск развития фульминантного гепатита.
Таблица №1. Основные маркеры гепатита В при различных клинических формах.
Комплексное обследование, подтверждающее наличие у больного острого или хронического вирусного гепатита В (HBsAg, HBV, ДНК количественно [реал-тайм ПЦР]) и его активность (anti-HBc, IgM), что позволяет определить необходимость и схему специфической противовирусной терапии.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Детям в возрасте до 1 года не принимать пищу в течение 30-40 минут до исследования.
- Детям в возрасте от 1 до 5 лет не принимать пищу в течение 2-3 часов до исследования.
- Исключить из рациона жирную пищу в течение 24 часов до исследования.
- Не принимать пищу в течение 12 часов до исследования, можно пить чистую негазированную воду.
- Исключить (по согласованию с врачом) прием эстрогенов, андрогенов в течение 48 часов до исследования.
- Полностью исключить (по согласованию с врачом) прием лекарственных препаратов в течение 24 часов перед исследованием.
- Исключить физическое и эмоциональное перенапряжение в течение 24 часов до исследования.
- Не курить в течение 3 часов до исследования.
Общая информация об исследовании
Целью проведения противовирусной терапии хронического гепатита В является профилактика цирроза печени, печеночной недостаточности и печеночно-клеточного рака. Не у всех пациентов хронический вирусный гепатит В приводит к этим заболеваниям, поэтому для оценки эффективности проводимой терапии используют контрольные показатели: подавление репликации вируса, исчезновение е-антигена вируса гепатита В (HBeAg), исчезновение поверхностного антигена гепатита В (HBsAg), нормализация активности аланинаминотрансферазы (AЛT) и улучшение гистологической картины печени. Результаты исследований, в которых приняли участие пациенты, не получающие терапию, свидетельствуют о стойкой активной репликации вируса гепатита В или воспалении печени, что отражает высокий уровень репликации ДНК вируса гепатита В в сыворотке крови, повышение активности AЛT и выявление HBeAg. Все это указывает на повышенный риск прогрессирования патологии. Таким образом, при определении показаний для проведения терапии хронического вирусного гепатита В необходимо исходить из уровня репликации вируса, а также активности и стадии патологических изменений в печени.
Решение о начале проведения противовирусной терапии пациентам с жизнеугрожающим состоянием печени, связанным с вирусным гепатитом В, у которых предполагаемая польза от действия лекарственных средств существенно преобладает над риском для здоровья, не представляет затруднений. Сложнее принять такое решение на ранней стадии заболевания, поскольку современные лекарственные препараты не приводят к эрадикации вируса и большинству пациентов требуется многолетняя, а иногда и пожизненная терапия в целях предупреждения неблагоприятных клинических исходов. Перед началом лечения и выбором той или иной схему терапии нужно определить активность гепатита. Активность гепатита определяется с помощью современного метода ПЦР (полимеразной цепной реакции) в режиме реального времени. ПЦР не только находит вирус, но и определяет его количество (вирусную нагрузку) в заданном объеме биоматериала. В острый период заболевания назначается лишь поддерживающая и выводящая токсины терапия, восстанавливающая гепатоциты. В это время врачи могут порекомендовать инозин (рибоксин), желчегонные препараты. Хроническая форма недуга лечится несколькими типами препаратов, превалирует противовирусная терапия: средства группы альфа-интерферонов
Данное исследование позволяет определить стадию заболевания, одномоментно провести комплексную оценку инфекционного процесса и определить форму и стадию ВГВ, что необходимо для назначения адекватной этиотропной терапии.
Когда назначается исследование?
- При ВГВ – вне зависимости от формы и стадии заболевания для решения вопроса о схеме этиотропной терапии.
Что означают результаты?
anti-HBc, IgM
Концентрация: 0 - 9,99 Ед/мл.
HBsAg
Референсные значения (норма HBsAg): отрицательно.
HBV, ДНК количественно [реал-тайм ПЦР]:
- не обнаружено – ДНК ВГВ не обнаружена или значение ниже предела чувствительности метода (200 копий/мл = 90 МЕ/мл);
- 2 копий/мл ( 2 МЕ/мл) - ДНК обнаружена в концентрации ниже линейного диапазона концентраций;
- 5 копий/мл (2х10 4 МЕ/мл) – умеренная виремия (решение о терапии зависит от биохимических показателей функции печени, результатов биопсии печени);
- > 10 5 копий/мл (2х10 4 МЕ/мл) – высокая вирусная нагрузка, активный инфекционный процесс (необходимо проведение противовирусной терапии);
- > 1,0х10 8 копий/мл (> 4,8х10 7 МЕ/мл) - ДНК вируса обнаружена в концентрации выше линейного диапазона концентраций[1].
Для решения о выборе схем терапии важно определить форму ВГВ по комплексной оценке полученных данных:
Вирус гепатита В (hepatitis B virus, HBV) относится к семейству Hepadnoviridae. Геном вируса представлен частично сдвоенной кольцевой молекулой ДНК размером 3200 п.н. При электронной микроскопии HBV выглядит сферической частицей диаметром 42 нм (частица Дейна), состоящей из ядра - нуклеотида, имеющего форму икосаэдра диаметром 28 нм, внутри которого находится двуцепочечная ДНК, концевой белок и фермент ДНК-полимераза. В состав нуклеоидного белка входят HBcAg и HBeAg. Внешняя оболочка (толщиной 7 нм) образована поверхностным антигеном HBV - HBsAg. Вирус гепатита В является псевдоретровирусом, т. е. его ДНК может частично встраиваться в геном гепатоцитов.
При ОВГ и обострении ХГ вирусные частицы можно обнаружить в гепатоцитах и сыворотке крови больного. При интегративной форме ХГ В и в стадии ремиссии HBV в сыворотке крови не выявляется.
Основой лабораторной диагностики инфекции HBV является определение серологических маркеров инфицирования вирусом: HBsAg, HВeAg, анти-НВс класса IgM и IgG, анти-НВе и анти-HBs, HBV ДНК и активности вирусной ДНК - полимеразы. В зависимости от течения вирусного гепатита В спектр изменения серологических маркеров выглядит по-разному.
HBsAg - основной маркер инфицирования HBV. При остром вирусном В в большинстве случаев (90-80 %) HBsAg удается выявить в инкубационном периоде, начиная с 3-5-й недели заражения. Средняя продолжительность циркуляции антигена - 70-80 дней. Быстрое исчезновение HBsAg (в первые дни желтухи) с появлением антиНВs - плохой прогностический признак. При хроническом гепатите В HBsAg может циркулировать в крови больного на протяжении многих лет. Следует отметить, что применяющиеся в настоящее время методы определения HBsAg, в том числе ИФА, имеют порог чувствительности. Поэтому при наличии клинических признаков гепатита и отсутствиии HBsAg в сыворотке крови необходимо исследовать другие маркеры инфекции HBV. Наличие HBsAg в крови свидетельствует о присутствии вируса в печени и с большой долей вероятности в крови. Не всякая сыворотка, содержащая HВsAg, содержит вирус гепатита В. В ряде случаев ДНК вируса встраивается в ДНК гепатоцита не полностью, а частично, только тем участком, который кодирует синтез HBsAg. В этих случаях синтезируется HBsAg без других компонентов вириона (то есть без других антигенов). Считают, что такая ситуация возникает при “здоровом” носительстве HBsAg.
HBeAg вируса гепатита В характеризует высокую инфекционность крови, являясь показателем активной репликации HBV. HBeAg циркулирует в крови больного только в присутствии HBsAg. В первую неделю желтушного периода он выявляется у 85-95 % больных. Выявление HBeAg в течение двух и более месяцев служит прогностическим признаком развития хронического гепатита. У большинства больных хроническим гепатитом с высокой активностью процесса HBeAg сохраняется на длительный срок (до нескольких лет).
Антитела к ядерному антигену вируса гепатита В класса M (анти-НВc IgM) - маркер активной репликации НВV и острой инфекции. Выявляются через 1-2 недели после обнаружения HBsAg и сохраняются на протяжении 2-18 месяцев. У 4-20 % больных острым гепатитом В анти-HBc IgM являются единственным маркером инфекции. При ХГ В анти-НВс IgM могут быть выявлены у некоторых больных в меньших титрах, чем при острой инфекции, причем титр антител отражает тяжесть гепатита.
Антитела к HBcAg класса G (анти-НВс IgG) появляются практически одновременно с анти-НВс IgM. Как првило, они остаются у всех лиц, переболевших гепатитом В, пожизненно. У 95 % носителей HBsAg наряду с HBsAg циркулируют и анти-НВс IgG.
Антитела к HBsAg (анти-НВs) свидетельствуют о ранее перенесенной инфекции или о наличии поствакцинального иммунитета (защитный уровень - 10 МЕ/мл). Они появляются в период выздоровления, через 4 недели после исчезновения HBsAg, достигая максимальной концентрации через 1-2 года, с последующим постепенным снижением уровня, недоступного выявлению современными методами диагностики. В некоторых случаях анти-HВs могут циркулировать пожизненно. Появление анти-HBs на фоне клинического улучшения у больного гепатитом В является хорошим прогностическим признаком. Важно отметить, что в динамике острой инфекции HBV имеется “окно”, когда HBsAg уже не определяется, а ан-ти-HBs еще не появились. При этом выявляются анти-HBc IgM и IgG. Из этого следует вывод о необходимости обследования больных ОВГ на анти-HBc IgM даже при отрицательных результатах исследования HBsAg и анти-НВs.
Антитела к HBeAg (анти-НВе) появляются в крови после элиминации HBeAg и завершения репликации вируса. К концу 9-й недели острого периода гепатита В более 90 % больных имеют анти-НВе. В период выздоровления анти-НВе могут исчезать. Однако, наличие анти-НВе не является показателем отсутствия инфекционности конкретной сыворотки крови. Показано, что у ряда больных в ходе развития гепатита В (около 10%) под влиянием “иммунного давления” на вирус возникают мутантные формы, которые “избегают” иммунного надзора и не элиминируются. У носителей анти-HBe был выделен мутант, неспособный продуцировать HBeAg из-за дефектов в области precore и получивший обозначение HBeAg-отрицательного. Появление HBeAg-отрицательного мутанта приводит к прогрессированию поражения печени при продолжающейся репликации вируса (наличие ДНК HBV в сыворотке крови). При первичном инфицировании HBeAg-отрицательным мутантом существенно возрастает риск развития фульминантного гепатита.
Описанные маркеры гепатита В исследуются методом ИФА. Спектр антител (анти-НВе, анти-НВs, анти-НВc IgM, анти-НВc IgG) и антигенов (HBsAg, HBeAg) позволяет установить диагноз гепатита В и определить стадию заболевания (таблица 5). Недостатком данного метода является невозможность его использования при заражении мутантными формами вируса, при иммуносупрессии (больные онкологическими заболеваниями, наркоманы и т.д.) и для количественной оценки присутствующего в организме возбудителя. Решение этих задач стало возможным в результате внедрения молекулярно-биологических методов в практику клинико-диагностических лабораторий.
Таблица 5. Различные сочетания серологических маркеров инфицирования вирусом гепатита В и их интерпретация
Гепатит и HBsAg
Итак, антиген HBsAg – один из компонентов оболочки вируса гепатита В (HBV). В контексте лабораторных исследований он является маркёром (индикатором) вируса.
Если говорить о составе капсида (внешняя оболочка вируса) гепатита В подробнее, то это сложная комбинация белков, гликопротеинов, липопротеидов и липидов клеточного происхождения. HBsAg в данном случае отвечает за процесс адсорбции вируса клеткой, то есть обеспечивает поглощение HBV гепатоцитами – клетками печени. Как и любой другой вирус, после внедрения в благоприятную среду, он начинает реплицировать (продуцировать) новые ДНК и протеины, необходимые для дальнейшего размножения (копирования) вируса. Фрагменты вируса, в нашем случае – HbsAg, поступают в кровоток, по которому распространяются дальше.
Возбудитель гепатита В относится к гепаднавирусам ( Hepadnaviridae ), само название которых указывает на их отношение к печени ( hepa ) и к ДНК ( DNA ). Таким образом, HBV – это гепатотропный вирус, при этом единственный среди всех вирусов гепатита, содержащий ДНК. Его активность (контагиозность и вирулентность) зависит от многих факторов:
- возраста (например, до 1 года – ≈90%, до 5 лет – ≈20–50%, старше 13 лет – ≈5%);
- индивидуальной восприимчивости;
- штамма вируса;
- инфицирующей дозы;
- гигиенических условий жизни и труда;
- эпидемиологической обстановки.
Но в целом контагиозность вируса гепатита B невысокая, ниже средней, если только полностью не пренебрегать всеми правилами безопасной половой жизни и гигиены.
Но как же передается вирус гепатита B? Процесс инфицирования происходит посредством крови и биологических жидкостей следующими путями:
- Парентеральным , то есть при попадании напрямую в кровь или слизистую оболочку, минуя защитные барьеры организма, такие как кожный покров или желудочно-кишечный тракт. Примерами такого инфицирования может служить нестерильный шприц или любой хирургический инструмент.
- Вертикальным – трансплацентарным, то есть внутриутробно от матери к ребенку, во время родов, после них.
- Половым (во всех его формах).
- Бытовым , то есть через предметы личной гигиены (бритвы, расчески, зубные щетки), при нанесении татуировок, пирсинге и др.
По окончании инкубационного периода наступает так называемая продромальная фаза заболевания, предшествующая острому периоду и предвещающая его. Тогда проявляются первые признаки болезни в виде общего недомогания, слабости, усталости, лихорадки с температурой на грани 37°C, понижения аппетита, тошноты, нарушений стула, суставно-мышечных болей, чувства сдавленности и тяжести в правом подреберье, раздражительности и апатии, кожных высыпаний в области суставов и зуда. Здесь следует отметить, что все эти симптомы могут быть выражены в разной степени у различных людей, вовсе отсутствовать или оставаться незамеченными. Продромальный, или преджелтушный, период может длиться от 1 до 30 дней. О его окончании свидетельствуют увеличенная печень и селезенка (30–50% случаев), повышенный уробилиноген в моче, обесцвечивание кала, а в сыворотки крови можно обнаружить рост концентраций АлАт и АсАт, пониженное содержание лейкоцитов, хотя в целом лейкоцитарная формула в норме.
Желтушность кожного покрова и иктеричность склер (желтая пигментация белковой оболочки глаз) знаменуют вступление в острую фазу , или в период разгара гепатита B. Повышение содержания общего и прямого билирубина в сыворотке крови нарастает первую неделю-две желтушного периода заболевания, достигая своего максимума, после чего происходит стагнация и постепенный спад в пигментации кожи вплоть до полного исчезновения желтой окраски, на что может уйти до 180 дней и даже более.
В пиковых точках болезни в большинстве случаев фиксируют брадикардию, пониженное артериальное давление, ослабление сердечных тонов. Кроме того, если гепатит протекает в тяжелой форме, обнаруживаются:
- угнетение центральной нервной системы;
- выраженные нарушения в работе ЖКТ;
- склонность к кровотечениям в слизистых оболочках (сильно понижен протромбиновый индекс);
- концентрация АлАт выше АсАт;
- пониженная сулемовая проба, реакция СОЭ – 2–4 мм/час, лейкопения;
- лимфоцитоз.
После острого периода (не путать с тяжелой формой!) болезнь развивается по одному из следующих сценариев (см. рис . 1 и 2):
- наступает период реконвалесценции (выздоровления) , с постепенным снижением (исчезновением) признаков гепатита B на клиническом, биохимическом и морфологическом уровнях;
- присоединяется суперинфекция в виде гепатита D и/или заболевание переходит в фульминантную форму, в так называемый молниеносный тяжелый гепатит (менее 1% случаев);
- болезнь переходит в активную хроническую форму :
- a. выздоровление;
- b. цирроз печени (20%), карцинома (1%);
- болезнь переходит в состояние устойчивой ремиссии ( стабильная хроническая форма ):
- a. излечение;
- b. внепеченочные патологии.

Рис. 1. Прогноз развития гепатита B
С точки зрения нагрузки на организм, врачи определяют три основных формы протекания острого гепатита B: легкая, средняя и тяжелая. С позиций выраженности симптомов заболевания, выделяют его желтушную (типичную), безжелтушную и субклиническую (атипичные) формы. В типичном варианте болезнь протекает в точности, как описано выше, однако это только 35% от всех случаев. Примерно 65% приходится на атипичные формы, когда не происходит пигментации кожных покровов и слизистой, а другие симптомы выражены слабо (безжелтушный вариант), или когда любые клинические проявления отсутствуют вовсе (субклиническая форма).
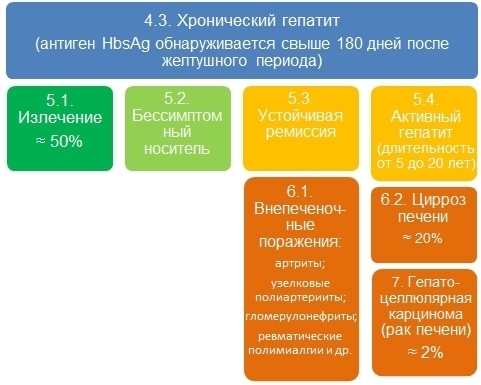
Рис. 2. Исход болезней при инфецировании HBV
Диагностические критерии бессимптомного носительства следующие:
- антиген HBsAg определяется в крови после 180 дней;
- маркёр HBeAg ( см. таблицу ) в сыворотке не обнаруживается;
- анти- HBe ( см. таблицу ) – присутствует;
- уровень HBV ДНК в сыворотке крови менее 105 копий/мл;
- концентрации АлАт/АсАт показывают норму при повторных анализах;
- при биопсии печени гистологический индекс активности (МГА) воспалительно-некротического процесса в печени обычно ниже 4.
Как можно увидеть, серологический маркер HBsAg является первым, основным, самым надежным, но далеко не единственным показателем инфекции гепатита B, кроме него требуют определения в сыворотке крови следующие антигены, антитела и молекулы ДНК вируса:
HBeAg
указывает на репликацию HBV в гепатоцитах, высокую активность вируса в крови и высокий риск перинатальной передачи вируса
HBcAg
маркирует репликацию HBV в гепатоцитах, обнаруживается только при морфологическом исследовании биоптатов печени и на аутопсии, в крови в свободном виде не выявляется
анти-НВс (total) (НВсАb)
суммарные антитела к HBcAg, выявляются через 7–14 дней после HBsAg
важный диагностический маркер, особенно при отрицательных результатах индикации HBsAg, используется для ретроспективной диагностики гепатита B и при неверифицированных гепатитах, определяют НВсАg без разделения на классы
IgM анти-НВс (НВсАb IgM)
антитела класса М к ядерному антигену , присутствуют в крови от 60 до 540 дней
один из наиболее ранних сывороточных маркеров гепатита В, наличие его в крови указывает на острую инфекцию (фазу болезни), при хроническом ГВ маркирует репликацию HBV и активность процесса в печени
анти-НВе (HBeAb)
может указывать на начало стадии реконвалесценции (исключение – мутантная форма HBV)
анти-HBs (HBsАb)
защитные антитела к поверхностному антигену HBV
указывают на перенесенную инфекцию или наличие поствакцинальных антител (их защитный титр от HBV-инфекции >10 МЕ/л); обнаружение же антител в первые недели гепатита В прогнозирует развитие гипериммунного варианта фульминантного гепатита В
HBV-DNA
ДНК вируса ГВ
маркер наличия и репликации HBV
Вышеуказанные маркёры появляются и исчезают в определенной последовательности в соответствии с этапами прохождения заболевания. Некоторые из них, такие как IgG анти-НВс, остаются на всю жизнь. Полную и достоверную диагностическую картину дает только весь набор маркёров. Кроме того, для острого, хронического, фульминантного и смешанного гепатитов существуют свои серологические профили (об этом ниже).
Нельзя не затронуть такое редкое, но чрезвычайно опасное явление, как параллельное инфицирование гепатитом D (HDV), оно может возникнуть в двух вариантах:
HDV – это своеобразный паразит вируса гепатита B, его сателлит, он не может реплицироваться в отсутствие HBV , поскольку синтез белков его внешней оболочки невозможен без наличия в гепатоцитах вируса гепатита B. Таким образом, переболеть гепатитом B можно и без дельта-инфекции, а вот наоборот не получится. Присоединение HDV вызывает в 30% случаев молниеносный (фульминантный) гепатит с развитием острой печеночной недостаточности и печеночной энцефалопатии, которые нарастают стремительно, в 60% случаев приводя к летальному исходу. Однако общий исход гепатита B в фульминантную форму находится в пределах 0,4–1% случаев. Поэтому при положительном результате на антиген HBsAg в обязательном порядке следует проводить диагностику дельта-инфекции. Для этого используются серологические маркеры:
IgM анти-HDV
антитела класса М к вирусу гепатита D
маркируют репликацию HDV в организме
IgG анти-HDV
антитела класса G к вирусу гепатита D
свидетельствуют о возможной инфицированности HDV или перенесенной инфекции
HDAg
антиген вируса гепатита D
маркер наличия HDV в организме
HDV-RNA
РНК вируса гепатита D
маркер наличия и репликации HDV
Анализ может быть сдан любым желающим, но есть определенные категории лиц, у которых подобное тестирование проводится обязательно:
- сотрудники медицинских учреждений, в особенности те, которые работают с кровью пациентов: медицинские сестры манипуляционных кабинетов, гинекологи, хирурги, фельдшеры, стоматологи;
- лица с повышенным уровнем ферментов АсАт и АлАт;
- больные, которым предстоит хирургическое вмешательство;
- потенциальные доноры крови;
- лица, являющиеся носителями вируса гепатита B, больные с хронической формой данного заболевания;
- беременные женщины.
Кроме того, исследование рекомендуется делать при наличии таких симптомов, как тошнота, рвота, потеря аппетита, изменение цвета мочи и кала, желтушность – то есть всех тех признаков гепатита B, которые были описаны в начале статьи. Но в целом каждый человек, если подходит к своему здоровью ответственно, должен делать серологическое исследование на HBsAg один раз в год.
Сегодня существует уже три поколения методов серологической диагностики HBsAg , и самые информативные и чувствительные из них, способные выявлять концентрации до 0,05 нг/мл, постепенно вытеснили своих предшественников.
I
Реакция преципитации в геле, РПГ (Gel precipitation test)
II
Встречный иммуноэлектрофорез, ВИЭФ (Counter immunoelectrophoresis),
Реакция связывания комплемента, РСК (Complement fixation test)
Реакция латекс-агглютинации, РЛА (Latex agglutination test)
Метод флюоресцирующих антител, МФА (Immunofluorescence)
Иммуноэлектронная микроскопия, ИЭМ (Immune electron microscopy)
III
Реакция обратной пассивной гемагглютинации, РНГА (Indirect hemagglutination test)
Радиоиммунный анализ, РИА (Radioimmunoassay)
Иммуноферментный анализ, ИФА (Enzyme immunoassay)
Почему ИФА и РИА более информативны в сравнении с предшественниками? Дело в том, что они способны выявлять IgM и IgG по отдельности, что позволяет делать определенные выводы о динамике инфекционного процесса или о состоянии реконвалесценции.
Качественные и количественные варианты ДНК-зондирования методом ПЦР имеют 100% точность и могут использоваться на самых ранних сроках после заражения. С помощью ПЦР выявляют персистирующие вирусы, которые находятся в клетке, продолжающей выполнять свои функции, а потому они с трудом обнаруживаются или не обнаруживаются другими методами.
Подобную диагностику можно проводить уже через 1–3 недели с момента предполагаемого заражения. Для такого тестирования используется венозная кровь (5–10 мл), которая берется натощак. Для получения ответа требуется один день.
НВsAg -качественный тест указывает лишь на наличие либо отсутствие заболевания. Очевидно, что отрицательный результат означает отсутствие заболевания, а положительный – наличие патологии. Последнее также может свидетельствовать о ранее перенесенном заболевании или носительстве. Любые сомнения подобного рода снимаются проведением количественного исследования на определение HBV-DNA методом ПЦР. Таблицы с трактовками маркеров острого и хронического гепатита B мы приводим ниже:

По оценкам многих экспертов, в мире насчитывается около 300-400 млн носителей вируса гепатита В. От заболеваний, вызванных этим вирусом, ежегодно погибают около 2 млн человек.
Российские статистические данные свидетельствуют, что в структуре хронических вирусных гепатитов (ХВГ) у детей в 29,2% случаев регистрируют ХВГ В, в 33,3% – ХВГ С, в 16,7% – ХВГ В+С, в 4,1% – ХВГ В+D, в 16,7% – гепатит невыясненной этиологии [3]. К сожалению, в Украине этот показатель установить невозможно ввиду отсутствия регистрации этиологической структуры ХВГ у детей и взрослых.
Путями передачи вируса гепатита В являются парентеральный, половой, перинатальный, а также контактно-бытовой, реализующийся, вероятно, при тесном контакте с открытыми поврежденными участками тела, ранами и особенно распространенный внутри детских коллективов, семьи и в регионах с высокой заболеваемостью HBV-инфекцией [13, 15, 16]. Вирус гепатита В может длительное время сохраняться вне организма, а HBeАg-позитивные лица с HBV-инфекцией при наличии открытых ран во время контакта с поверхностями окружающей среды способны оставлять на них большое количество вирусных частиц [13, 21].
В Украине, по данным Л.В. Мороз [10], инфицированность беременных вирусом гепатита В составляет 24,3%. В случае заболевания женщины острым ВГ В в І триместре беременности вероятность инфицирования новорожденного составляет около 10%, во ІІ-ІІІ триместре – 30-60% [6]. Трансплацентарная передача от HBsАg-положительных матерей не превышает 8%, но с практической точки зрения каждую HBsАg-положительную беременную следует считать представляющей большую опасность в плане инфицирования ребенка и проводить соответствующие профилактические мероприятия [8].
ХВГ у детей характеризуются субклиническим течением, которое проявляется преимущественно астеновегетативными расстройствами, незначительным увеличением печени при нормальном или незначительном повышении уровня трансаминаз крови [2].
Естественное течение ХВГ В зависит от клинической формы заболевания (HBeАg-позитивный или HBeАg-негативный), возраста, в котором имело место инфицирование, а также пути заражения. Вероятность развития хронического поражения печени при HBV-инфекции резко возрастает при инфицировании ребенка внутриутробно, а также в грудном и раннем детском возрасте. При инфицировании внутриутробно и на 1-м году жизни частота развития хронических форм заболевания достигает 90-100%, в возрасте старше 2 лет – 20-30%, у подростков и взрослых – менее 5% [8].
У детей с HBeАg-позитивным вариантом ХВГ В при перинатальном инфицировании иммунотолерантная фаза может продолжаться от 10 до 30 лет. При этом отмечается высокий уровень ДНК HBV в крови, нормальное или близкое к нормальному содержание трансаминаз крови. Спонтанная сероконверсия HBeАg в анти-HBeАg при этом встречается крайне редко.
В случае инфицирования детей в старшем возрасте ХВГ В отличается более тяжелым течением. Манифестация заболевания наступает в 30-40 лет. Спонтанная сероконверсия имеет место у 8-15% больных. Чем выше уровень АЛТ, тем чаще она возникает. Вероятность спонтанного исчезновения HBsАg не превышает 0,5%. Заболеванию свойственно прогрессирующее течение. Частота осложнения ХВГ В развитием цирроза печени при HBeАg-позитивном гепатите составляет 2-5,5%, при HBeАg-негативном – 8-10%. Формирование цирроза печени у детей отмечается реже, чем у взрослых [5].
Детям с нормальным уровнем АЛТ и активной репликацией вируса гепатита В, носителям HBsАg противовирусная терапия не показана.
Заключение
1. Эффективность противовирусной терапии ХВГ В у детей до конца не определена.
2. Доказана необходимость проведения противовирусной терапии при ХBГ В у детей с целью предупреждения развития цирроза печени.
3. Необходимость проведения полного курса противовирусной терапии ХВГ В у детей связана с индукцией сероконверсии после отмены интерферонотерапии.
Читайте также:


