“Стеатоз печени” – это описательный термин, означающий накопление капель жира, жировых включений в гепатоцитах. Стеатоз может быть очаговым или диффузным.
Неалкогольный стеатогепатит (НАСГ) – клинический синдром стеатоза и воспаления печени, который устанавливается по результатам биопсии печени, после исключения других причин заболевания печени. НАСГ, как правило, носит характер диффузного процесса.
Гистологические изменения в печени, сходные с картиной алкогольного гепатита, впервые описаны в 1980г. Ludwig и сотр. у пациентов, не употреблявших алкоголь в количествах, вызывающих повреждение печени.
Частота выявления НАСГ среди больных, которым проводилась биопсия печени, составляет примерно 7—9% в западных странах и 1,2% в Японии. Алкогольный гепатит встречается в 10—15 раз чаще.
Обследование больших групп пациентов с криптогенным циррозом печени, включавшее оценку сопутствующих заболеваний и факторов риска, позволило выдвинуть предположение, что во многих случаях (до 60-80%) цирроз печени “неясной этиологии” развивается на фоне нераспознанного НАСГ.
Этиологические факторы и факторы риска. Выделяют случаи первичного и вторичного стеатоза печени и НАСГ (табл. 7.1).
Таблица 7.1. Этиологические факторы неалкогольного стеатогепатита
| Первичный НАСГ | Вторичный НАСГ |
Ожирение
Сахарный диабет (в особенности - синдром резистентности к инсулину)
Гиперлипидемия | Лекарственные препараты (амиодарон, глюкокортикоиды, синтетические эстрогены, тамоксифен, пергексилина малеат, метотрексат, тетрациклин, нестероидные противовоспалительные средства (аспирин, вальпроат натрия, ибупрофен, др.), нифедипин (?), дилтиазем (?) и пр.)
Синдром мальабсорбции (как следствие наложения илео-еюнального анастомоза, билиарно-панкреатической стомы, гастропластики по поводу ожирения, расширенной резекции тонкой кишки и пр.).
Быстрое похудание
Длительное (свыше 2 нед.) парентеральное питание (в особенности - не содержащее жиров или не сбалансированное по содержанию углеводов и жиров)
Смешанные нарушения (синдром избыточного бактериального обсеменения кишечника (на фоне дивертикулеза тонкой кишки и пр.))
Абеталипротеинемия
Липодистрофия конечностей
Болезнь Вильяма-Крисчена
Болезнь Вильсона-Коновалова |
Первичный НАСГ, как правило, ассоциирован с эндогенными нарушениями липидного и углеводного обмена. Наиболее высок риск развития стеатоза печени у лиц с ожирением, инсулинонезависимым сахарным диабетом, гипертриглицеридемией.
Вторичный НАСГ индуцируется внешними воздействиями и развивается на фоне некоторых метаболических расстройств, приема ряда медикаментов, синдрома мальабсорбции. Отмечены случаи развития НАСГ на фоне недостаточности альфа-1-антитрипсина.
Примерно у 42% пациентов не удается выявить факторов риска развития заболевания. Исследуется роль наследственной предрасположенности. Среди пациентов с НАСГ чаще встречаются гетерозиготы по C282Y.
Патогенез. Патогенез стеатоза печени и НАСГ плохо изучен. Принято считать, что стеатоз печени является ступенью, предшествующей развитию стеатогепатита. Ряд исследователей выражает сомнение, что избыточное накопление липидов как таковое может быть причиной вторичного воспаления, поскольку выраженному стеатозу печени не всегда сопутствуют явления гепатита.
На рис. 7.1 и 7.2 схематично представлена роль печени в липидном обмене.
![]()
Рис. 7.1. Участие печени в жировом обмене
![]()
Рис. 7.2. Основные этапы метаболизма липидов в гепатоците
Избыточное накопление жира в ткани печени (в гепатоцитах и звездчатых клетках) может быть следствием:
- повышения поступления свободных жирных кислот (СЖК) в печень;
- снижения скорости β-окисления СЖК в митохондриях печени;
- повышения синтеза жирных кислот в митохондриях печени;
- снижения синтеза или секреции липопротеинов очень низкой плотности (ЛПОНП) и экспорта триглицеридов в составе ЛПОНП.
Предполагают, что, независимо от причин развития стеатоза, в основе воспалительно-некротических изменений в печени лежат универсальные механизмы. Будучи высокореактогенными соединениями, СЖК служат субстратом перекисного окисления липидов (ПОЛ). ПОЛ сопровождается повреждением митохондрий, лизосом, клеточных мембран. Продукты ПОЛ стимулируют коллагенообразование, образование телец Мэллори (агрегатов мономеров цитокератина).
Существует противоположная гипотеза, согласно которой воспалительные изменения, индуцируемые неизвестными стимулами, вызывают дисфункцию гепатоцитов с развитием жировой дистрофии.
При НАСГ наблюдается повышенная активность цитохрома P450 2E1 в печени, что сопровождается образованием активных радикалов кислорода и усилением реакций ПОЛ.
Предполагается, что для инициации стеатонекроза необходимо определенное воздействие, приводящее к формированию активных форм кислорода в митохондриях.
Первичный НАСГ. У пациентов с избыточной массой тела имеются более выраженные запасы СЖК в организме, и нередко - повышенное содержание СЖК в плазме крови. Кроме того, для этой категории больных достаточно характерна пониженная чувствительность периферических рецепторов к инсулину. Уровень инсулина крови нередко повышен. Инсулин активизирует синтез СЖК и триглицеридов (ТГ), снижает скорость бета-окисления СЖК в печени и секрецию липидов в кровоток. Таким образом, при синдроме резистентности к инсулину содержание жира в органе может возрастать.
Вторичный НАСГ. Механизм развития стеатогепатита как осложнения длительного тотального парентерального питания остается неизвестным. Возможно, он носит мультифакторный характер (табл. 7.2).
Таблица 7.2. Возможные механизмы развития стеатоза печени и стеатогепатита на фоне длительного тотального парентерального питания
Чрезмерно высокая скорость инфузии растворов глюкозы (при превышении максимальной скорости утилизации глюкозы (4-5 г/кг) происходит синтез жиров).
Избыточное введение липидных эмульсий (фагоцитоз липидных капель в печени).
Питание, несбалансированное по аминокислотам, жирам и углеводам (приводит к возрастанию внутрипеченочного синтеза липидов).
Дефицит поступления карнитина, холина, эссенциальных жирных кислот, глутамина.
Воздействие токсичных метаболитов аминокислот и желчных кислот.
Отрицательное влияние дисбаланса желудочно-кишечных гормонов. |
При синдроме мальабсорбции патогенетическое значение имеют дефицит поступления пищевых факторов (метионина, холина, необходимых для синтеза лецитина, обеспечивающего тонкое диспергирование липидов в клетке), а также быстрое похудание (повышенная мобилизация СЖК из жировых депо).
Исследованы некоторые механизмы развития вторичного лекарственного НАСГ.
В качестве примеров можно привести следующие.
В метаболизме аспирина и вальпроата натрия участвует коэнзим А - катализатор бета-окисления СЖК. При применении данных препаратов возможно развитие “перераспределительного дефицита” коэнзима А.
Тетрациклин, помимо подавляющего влияния на бета-окисление СЖК, нарушает секрецию ТГ гепатоцитами.
Амиодарон не только угнетает бета-окисление в митохондриях (приводит к накоплению субстратов ПОЛ), но и нарушает процесс переноса электронов в дыхательной цепи, способствуя формированию активных форм кислорода. Поэтому гепатотоксичное влияние амиодарона обычно не ограничивается стеатозом, и выражается в развитии НАСГ. Предполагается также, что амиодарон (его метаболиты?) и триметоприм/сульфаметоксазол подавляют лизосомальный катаболизм фосфолипидов, что приводит к развитию фосфолипидоза.
Эстрогены вызывают ультраструктурные изменения митохондрий, с подавлением процессов бета-окисления.
Интерферон – альфа блокирует транскрипцию митохондриальной ДНК.
Генетическая предрасположенность к развитию НАСГ также связана с накоплением потенциально токсичных СЖК в цитоплазме в результате дефектов бета-окисления, обусловленного нарушением захвата карнитина гепатоцитом, “челночного механизма” переноса жирных кислот в митохондрии (протекающего с участием ряда ферментов и карнитина),дисфункцией какого-либо звена мультиферментного комплекса бета-окисления. Изменения структуры митохондриальной ДНК сопровождаются угнетением системы окислительного фосфорилирования и восстановления необходимых для бета-окисления NADH и FADH2. В этих случаях развиваются, как правило, полиорганные расстройства.
Врожденные нарушения синтеза мочевины сопровождаются накоплением в печени аммиака, угнетающего бета-окисление жирных кислот.
Существуют патогенетические параллели с морфологическими особенностями стеатоза печени (табл. 7.3).
Клинические проявления. Большинство пациентов, страдающих стеатозом печени и НАСГ (65%-80%), - женщины, и большинство из них имеет избыточную массу тела, на 10-40% превышающую идеальную. Инсулин-независимый сахарный диабет обнаруживается у 25% - 75% пациентов.
Средний возраст больных на момент диагностики НАСГ составляет 50 лет.
У большинства пациентов (48-100%) симптомы, характерные для заболеваний печени, отсутствуют. У меньшей части отмечаются неопределенный дискомфорт в животе или тяжесть, ноющие боли в верхнем правом квадранте живота, выражен астенический синдром. При мелкокапельном стеатозе возможно развитие эпизодов геморрагий, а также обморока, гипотензии, шока (вероятно, опосредованы влиянием высвобождающегося при воспалении туморнекротизирующего фактора).
При осмотре у 75% больных обнаруживается гепатомегалия. Увеличение селезенки имеет место примерно в 25% случаев. Желтуха, асцит, “печеночные знаки” выявляются редко.
Индекс массы тела выступает как единственный независимый фактор для оценки степени жировой инфильтрации печени.
Мы стремились оценить различные лекарства для лечения людей с неалкогольной жировой болезнью печени.
Неалкогольная жировая болезнь печени (НЖБП) представляет собой накопление жира в печени у людей, которые не употребляли алкоголь в больших количествах, не применяли лекарств, не имели заболеваний, таких как гепатит С, или других состояний, таких как голодание, которые могли бы вызвать повреждение печени. Жировая болезнь печени может привести к повреждению печени в результате воспаления (неалкогольный стеатогепатит или НАСГ) или рубцевания печени (цирроз печени). Лучший способ лечения людей с НЖБП не ясен. Мы стремились разрешить эту проблему, проведя поиск существующих испытаний по этой теме.
Критерии отбора и дата поиска
Мы включили все рандомизированные клинические испытания (клинические исследования, в которых людей в случайном порядке распределяют в одну из двух или более групп лечения), отчеты которых были опубликованы к августу 2016 года.
Мы включили 77 рандомизированных клинических испытаний, в которых приняли участие всего 6287 человек. Из них 41 испытание (3829 участников) представило информацию по одному или более исходам для этого обзора. Тридцать пять испытаний включали только участников с НАСГ; пять включали только людей с сахарным диабетом и 14 испытаний включали только людей, у которых не было сахарного диабета. Средний период наблюдения в испытаниях варьировал от одного месяца до двух лет в тех испытаниях, где эта информация была указана. Мы исключили испытания, в которых участники с НЖБП подверглись трансплантации печени до начала испытания. Помимо проведения стандартного Кокрейновского анализа, мы также планировали провести сетевой мета-анализ (метод, который позволяет сравнивать различные виды лечения, которые непосредственно не сравниваются друг с другом в испытаниях). Однако, характер доступной информации означал, что мы не могли определить, будут ли результаты сетевого мета-анализа надежными.
К конкретным исходам, которые мы рассматривали, относились число смертей, неблагоприятных событий, и оценка качества жизни, связанного со здоровьем.
Источники финансирования исследований
Двенадцать испытаний не получали какого-либо дополнительного финансирования или финансировались из источников, не заинтересованных в результатах; 26 были профинансированы фармацевтическими компаниями, которые потенциально могли извлечь пользу из результатов испытаний; в 39 испытаниях не было данных об источниках финансирования.
Во включенных испытаниях сравнивали такие виды лекарственной терапии, как желчные кислоты, антиоксиданты, ингибиторы фосфодиэстеразы 4-го типа, ингибиторы глюкокортикостероидов, лекарства для снижения уровня холестерина и антидиабетические лекарства, с плацебо или отсутствием лечения.
Антиоксиданты в сравнении с отсутствием вмешательства
Смертельных исходов в обеих группах не было (87 участников, 1 клиническое испытание). Ни у одного из участников не было серьезных неблагоприятных событий в испытании, в котором сообщали о проценте людей с серьезными неблагоприятными событиями (87 участников, 1 клиническое испытание). Не было различий в числе серьезных неблагоприятных событий между группой с применением антиоксидантов и группой с отсутствием вмешательства (254 участника, 2 клинических испытания).
Желчные кислоты в сравнении с отсутствием вмешательства
Не было доказательств различий в числе смертей при максимальном периоде наблюдения (659 участников, 4 клинических испытания), проценте людей с серьезными неблагоприятными событиями (404 участника, 3 клинических испытания), или числе серьезных неблагоприятных событий (404 участника, 3 клинических испытания) между группой с применением желчных кислот и группой с отсутствием вмешательства. Ни в одном из испытаний не сообщали о качестве жизни, связанном со здоровьем.
Тиазолидиндионы в сравнении с отсутствием вмешательства
Смертельных исходов не было в обеих группах (74 участника, 1 клиническое испытание). Ни у одного из участников не было выявлено серьезных неблагоприятных событий в двух испытаниях, в которых сообщали о проценте людей с серьезными неблагоприятными событиями (194 участника, 2 клинических испытания). Не было доказательств различий в числе серьезных неблагоприятных событий между группой с применением тиазолидиндионов и группой с отсутствием вмешательства (357 участников, 3 клинических испытания). Ни в одном из испытаний не сообщали о качестве жизни, связанном со здоровьем.
Мы не нашли доказательств пользы какого-либо из сравниваемых вмешательств у людей с жировой болезнью печени. Существует значительная неопределенность в этом вопросе, и нам необходимы дальнейшие рандомизированные клинические испытания высокого качества с достаточно большой группой участников.
В целом, качество доказательств было очень низким, а риск смещения был высоким. Это означает, что есть вероятность сделать выводы, которые будут неправильно интерпретировать пользу или вред от лечения из-за способов проведения исследований.
Неалкогольная жировая болезнь печени (НАЖБП ) характеризуется связанным с инсулинорезистентностью избыточным накоплением жира в печени у лиц, не злоупотребляющих алкоголем. Определение согласно EASL: стеатоз >5 % гепатоцитов при гистологическом исследовании или содержимое жира в печени >5,6 % при протонной магнитно-резонансной спектроскопии (Н-МРС) либо при магнитно-резонансной томографии с пофазным контрастированием. НАЖБП является печеночной манифестацией метаболического синдрома (→разд. 13.5) и связана с повышенным риском преждевременного атеросклероза и смерти, вызванной сердечно-сосудистыми причинами; НАЖБП включает как простой неалкогольный жировой гепатоз (НАЖГ) — отсутствуют причины вторичного стеатоза →табл. 7.11-1, так и развивающийся на его фоне неалкогольный стеатогепатит (НАСГ ) . Причины НАЖБП включают высококалорийную диету (блюда фаст-фуд), обогащенную рафинированными углеводами, особенно фруктозой, насыщенными жирами и подслащенными напитками, которая вместе с неудовлетворительной физической активностью ведет к избыточному весу и ожирению. Главную роль в патогенезе играет инсулинорезистентность, нарушения регуляции адипонектина и оксидативный стресс; значительным является влияние генетических факторов.
К основным факторам риска НАЖБП относятся: ожирение (особенно — абдоминальное), сахарный диабет 2 типа, дислипидемия, метаболический синдром и мужской пол; слабее связь с синдромом поликистозных яичников, гипотиреозом, гипопитуитаризмом, гипогонадизмом и синдромом обструктивного апноэ сна. Факторы риска развития фиброза и цирроза печени у больного с НАЖБП/НАСГ: возраст ≥45 лет, сахарный диабет 2 типа, ожирение (особенно, абдоминальный тип), тромбоцитопения, гипоальбуминемия, МНО >1,2, АСТ/АЛТ >1, признаки портальной гипертензии при визуализирующих исследованиях.
Таблица 7.11-1. Причины стеатоза печени
– ЛС: антибиотики (тетрациклин, блеомицин, пуромицин), цитостатики (метотрексат, L-аспарагиназа), витамины (витамин A в высокой дозе), другие (амиодарон, эстрогены, глюкокортикостероиды, гидразин, салицилаты, вальпроат натрия, варфарин)
– химические вещества: хлорированные углеводороды, тетрахлорметан, сероуглерод, фосфор, соли бария
– токсины, содержащиеся в грибах (α-аманитин)
нарушения обмена веществ и пищевые факторы
– перекармливание и ожирение, голодание, белковая недостаточность (квашиоркор)
– полное и длительное парэнтеральное питание (дефицит холина и карнитина)
нарушение питания и всасывания
– болезни поджелудочной железы
– кишечные анастомозы (напр., еюно-илео-анастомоз)
– неспецифические энтероколиты (неспецифический язвенный колит, болезнь Крона)
врожденные нарушения метаболизма
– дефицит арил-дегидрогеназы среднецепочечных жирных кислот
– болезни накопления: эфиры холестерина (болезнь Вольманна), сфингомиелина (болезнь Нимана-Пика), ганглиозидов (болезнь Тея-Сакса), глюкоцереброзидов (болезнь Гоше), меди (болезнь Вильсона-Коновалова), железа (гемохроматоз), гликогена (гликогеноз), галактозы, фруктозы, тирозина, гомоцистеина, фитиновой кислоты (синдром Рефсума)
– врожденные расстройства цикла мочевины
– вирусный гепатит С
– фульминантный гепатит D
– осложнения беременности: острая жировая дистрофия печени беременных, эклампсия, синдром HELLP (гемолиз, повышение активности ферментов печени и тромбоцитопения)
КЛИНИЧЕСКАЯ КАРТИНА И ЕСТЕСТВЕННОЕ ТЕЧЕНИЕ наверх
Субъективные симптомы: как правило, без симптомов, может возникать усталость, общая слабость, плохое самочувствие, ощущение дискомфорта в правом верхнем квадранте живота. Болезнь часто диагностируется случайно во время УЗИ обследования по другим причинам или после определения неправильной активности печеночных ферментов.
Объективные симптомы: обычно ожирение, гепатомегалия ( Дополнительные методы исследования
1. Лабораторные анализы: обычно небольшое или умеренное повышение активности АЛТ и АСТ (АСТ/АЛТ 2. Визуализирующие обследования: УЗИ — повышенная эхогенность печени (стеатоз), реже гепатомегалия; при циррозе симптомы портальной гипертензии (обследование технически сложно при ожирении, не визуализирует незначительный стеатоз (20 % массы печени), не дифференцирует простой стеатоз от НАСГ). КТ — качественная оценка печени и других органов (не показано рутинное выполнение в связи с ионизирующим облучением). МРТ — детальная оценка незначительного стеатоза (5–10 % гепатоцитов), но доступность ограничена; Н-МРС является единственным проверенным методом количественного измерения содержимого жира в печени.
3. Неинвазивная оценка фиброза печени: проводится с целью селекции больных с умеренно выраженным фиброзом (F0–F1), у которых можно отказаться от проведения биопсии печени. Методы:
1) эластография (точность ограничена в случае ожирения):
2) шкалы, основанные на сывороточных биомаркерах — NAFLD Fibrosis Score (http://nafldscore.com), FIB‑4, Enhanced Liver Fibrosis (ELF), FibroTest.
4. Гистологическое исследование биоптата печени: золотой диагностический стандарт (необходимо, чтобы с уверенностью различить между НАЖГ и НАСГ), но несет риск осложнений. Показания:
1) подозрение на НАСГ, особенно, если неинвазивные исследования указывают на существенный фиброз (≥F2);
2) диагностические сомнения (напр., другие причины стеатоза печени, высокая концентрация железа в сыворотке, наличие аутоантител (АNA, SMA, AMA), злоупотребление ЛС;
3) сосуществование НАЖБП с другими хроническими заболеваниями печени.
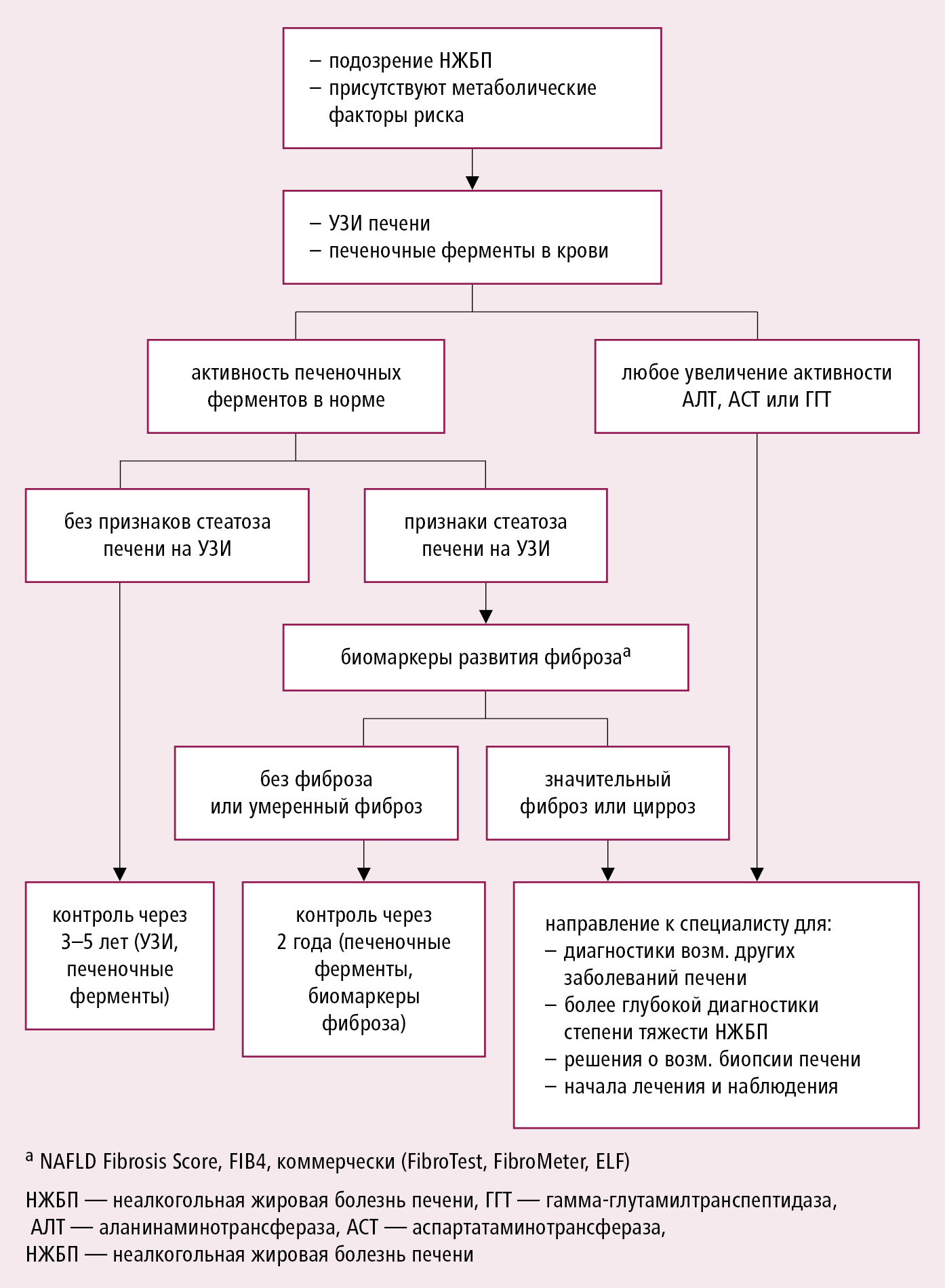
![]()
Рисунок 7.11-1. Стратегия диагностики и лечения НАЖБП
Оценка больного с подозрением на НАЖБП:
1) употребление алкоголя;
2) индивидуальный и семейный анамнез относительно сахарного диабета, артериальной гипертензии и заболеваний сердечно-сосудистой системы;
3) ИМТ, окружность талии, изменения массы тела;
4) маркеры инфекции HBV и HCV;
5) применение ЛС, ассоциированных со стеатозом;
6) активность печеночных ферментов (АСТ, АЛТ, ГГТП);
7) гликемия натощак, HbA1c, ОГТТ (возм. инсулин натощак и индекс HOMA-IR);
8) морфология крови;
9) концентрация общего холестерина, ХС-ЛПВП, триглицеридов и мочевой кислоты в плазме;
Расширенная диагностика в зависимости от изначальной оценки вероятности или результатов обследований:
1) концентрация ферритина и насыщение трансферина железом;
2) обследования для диагностирования целиакии, заболеваний щитовидной железы и синдрома поликистозных яичников;
3) обследования для диагностирования редких заболеваний печени — болезни Вильсона-Коновалова, аутоиммунных заболеваний, дефицита α 1 ‑антитрипсина.
1) исключение употребления алкоголя в значительных количествах (еженедельно 2. НАСГ : такие же, как при НАЖБП, а также дополнительно признаки НАСГ в биопсии печени — необходимо наличие стеатоза, гепатита и баллонной дистрофии гепатоцитов.
Как при хроническом вирусном гепатите типа В →разд. 7.2.
1. Изменение стиля жизни : средиземноморская или похожая диета (DASH), а также физическая активность (→табл. 7.11-2). У больных с ожирением для редукции стеатоза печени может быть достаточно снижения массы тела на 3–5 %, для достижения регрессии воспалительно-некротических процессов — на ≈10 %. В случае неэффективности у больных с НАСГ и патологическим ожирением рассмотрите показания к бариатрической операции.
Таблица 7.11-2. Модификация образа жизни при лечении неалкогольной жировой болезни печени (НАЖБП) (на основании рекомендаций EASL, EASD и EASO 2016)
поступление энергии с пищей
– ограничить поступление энергии на 500–1000 ккал для снижения массы тела на 0,5–1 кг/нед.
– цель: потеря 7–10 % массы тела
– применять длительно, совместно с увеличенной физической активностью и когнитивнокогнитивно-поведенческой терапией
– низкое или умеренное употребление жира, а также умеренное или значительное употребление углеводов
– диеты, богатые белком, либо кетогенные диеты с низким содержанием углеводов
избегать употребление напитков и продуктов с высоким содержанием фруктозы
абсолютно нельзя превышать употребление алкоголя выше порога риска (т. е. 30 г/сут для мужчин и 20 г/сут для женщин)
ограничения, связанные с печенью, отсутствуют
тренировка и физическая активность
– 150–200 мин/нед. аэробных упражнений умеренной интенсивности, разделенных на 3–5 тренировок (напр., быстрая ходьба, стационарный велосипед)
– упражнения на сопротивление также являются эффективными, увеличивают функциональность опорно-двигательного аппарата, оказывают положительное влияние на метаболические факторы риска
– преградой для регулярного выполнения рекомендованных упражнений являются высокий уровень усталости, приводящий к ограничению активности, а также сонливость в течение дня
2. Гепатопротекторная терапия: у пациентов с НАЖБП, подтвержденным при биопсии можно назначить витамин Е 800 МЕ/сут (противопоказан при сахарном диабете или циррозе печени), или пиоглитазон 30 мг/сут.
3. Симптоматическое лечение осложнений цирроза печени →разд. 7.12.
4. Трансплантация печени: в случае декомпенсированного цирроза и гепатоцеллюлярной карциномы.
Контроль АЛТ и АСТ каждые 2–3 мес. Отсутствуют однозначные рекомендации относительно систематического контроля УЗИ или определения α-фетопротеина. Наблюдение за больным циррозом печени →разд. 7.12.
Резюме. У взрослых и детей
![]()
Неалкогольная жировая болезнь печени — наиболее распространенная патология этого органа во всем мире. У около 25% жителей Соединенных Штатов Америки (США) диагностируют неалкогольную жировую болезнь печени и предполагают, что у четверти из них уже присутствует неалкогольный стеатогепатит. В настоящее время окончательный диагноз неалкогольного стеатогепатита устанавливают на основе гистологических доказательств не только относительно наличия повышенного количества жира в гепатоцитах (стеатоз), но и повреждения клеток, некротических их изменений и накопления воспалительных клеток в ткани печени.
Неалкогольный стеатогепатит имеет выраженную взаимосвязь с избыточной массой тела, ожирением и метаболическим синдромом. Результаты недавнего анализа исследований с участием более 8,5 млн человек из 22 стран свидетельствуют, что более 80% пациентов с неалкогольным стеатогепатитом имеют избыточную массу тела или ожирение, 72% — дислипидемию, а 44% — диагностированный сахарный диабет 2-го типа. Эти данные подтверждают концепцию, что неалкогольный стеатогепатит является не только печеночным коррелятом метаболического синдрома, но также и системным нарушением энергетического гомеостаза, который часто сопровождает висцеральное ожирение.
В отличие от неалкогольной жировой болезни печени, неалкогольный стеатогепатит выраженно ассоциируется с фиброзом ткани этого органа в соответствии с результатами гистологических исследований, но также имеет свойство регрессировать обратно к стеатозу печени. Считается, что тяжесть фиброза печени является единственным гистологическим показателем, независимо прогностически достоверным в отношении дальнейшей прогрессии заболевания, показаний для трансплантации печени и смертности пациентов с неалкогольным стеатогепатитом. Тем не менее стоит понимать, что темпы прогрессии фиброза (и регрессии) значительно различаются у отдельных пациентов и могут быть нелинейными во времени даже у одного человека.
Неалкогольный стеатогепатит обусловливает рост заболеваемости и распространенности первичных злокачественных новообразований печени во многих странах. Частота развития гепатоцеллюлярной карциномы составляет по меньшей мере 1–2% в год среди американских пациентов с циррозом печени, связанным с неалкогольным стеатогепатитом. Более того, по мнению авторов, неалкогольный стеатогепатит, скорее всего, станет главной причиной трансплантации печени в США к 2020 г.
К сожалению, неалкогольную жировую болезнь печени и неалкогольный стеатогепатит все чаще диагностируют и у детей, причем в педиатрической популяции эти заболевания также наиболее выраженно связаны с ожирением. Исследование, проведенное при участии более чем 250 тыс. датских детей, показало, что ожирение у этой популяции значительно повышает риск развития гепатоцеллюлярной карциномы во взрослом возрасте, что вызывает обеспокоенность в связи с тем, что эпидемия детского ожирения потенциально может породить эпидемию хронических заболеваний печени, цирроза и злокачественных новообразований этого органа, которые будут преследовать население всего мира ближайшие десятилетия. Экономическое бремя неалкогольной жировой болезни печени уже огромно, ведь только лишь в США оно оценивается ежегодно в 100 млрд дол. США, при этом бо`льшая часть расходов связана именно с неалкогольным стеатогепатитом и его последствиями.
Авторы отмечают, что неалкогольный стеатогепатит всегда развивается на фоне стеатоза печени. Однако наличие стеатогепатита не всегда коррелирует с выраженностью стеатоза печени, оцениваемой по результатам биопсии органа или при помощи современных визуализационных методов диагностики. Поскольку в этих тестах главным образом фиксируется содержание триглицеридов в печени, а сами триглицериды не являются непосредственно гепатотоксичными, предполагается, что повреждение гепатоцитов вызвано токсичными предшественниками триглицеридов или продуктами их метаболизма.
Повреждение и гибель гепатоцитов — ключевые отличительные признаки при дифференциальной диагностике неалкогольного стеатогепатита от изолированного стеатоза печени. Однако остается спорным, является ли повреждение клеток причиной или же вторичным следствием воспаления. Ученые не исключают генетической составляющей и эпигенетических факторов риска развития как неалкогольной жировой болезни печени в целом, так и неалкогольного стеатогепатита в частности.
Также существуют и модифицируемые факторы риска развития неалкогольной жировой болезни печени и стеатогепатита. Результаты исследований демонстрируют взаимосвязь этих заболеваний с изменением микробиома кишечника, в связи с чем необходимо изучить, может ли непосредственное манипулирование кишечной микробиотой при помощи антибиотиков, пребиотиков или пробиотиков использоваться в рамках профилактики или лечения пациентов с неалкогольным стеатогепатитом. Считается, что ненормированная посменная работа и путешествия, нарушающие нормальный режим питания, циклы сна и циркадные ритмы, способствуют развитию ожирения, метаболического синдрома и неалкогольной жировой болезни печени.
Неалкогольный стеатогепатит и его осложнения гораздо менее распространены, чем изолированный стеатоз печени у населения в целом. Это свидетельствует о том, что большинство людей с неалкогольной жировой болезнью печени способны избегать, сдерживать или компенсировать стрессоры, которые приводят к развитию или прогрессированию неалкогольного стеатогепатита.
Лицам группы повышенного риска развития неалкогольного стеатогепатита или фиброза печени авторы рекомендуют проводить диагностические мероприятия, чтобы подтвердить или опровергнуть клинические подозрения о повреждении печени, связанном с неалкогольным стеатогепатитом, оценить тяжесть поражения печени и определить тяжесть фиброза, поскольку эта информация имеет принципиально важное значение при разработке планов менеджмента заболевания. Биопсия печени в настоящее время является наиболее широко распространенным методом диагностики неалкогольного стеатогепатита и выявления фиброза печени. Однако разрабатываются и менее инвазивные подходы, которые в конечном итоге позволят диагностировать неалкогольный стеатогепатит путем объединения панелей биомаркеров в сыворотке крови, новых визуализационных методов, которые могут диагностировать фиброз печени, и динамических тестов функции печени, а генетический скрининг может еще больше улучшить диагностическую точность.
Для эффективного управления течением неалкогольного стеатогепатита необходима точная и своевременная диагностика, поскольку в настоящее время основным и вполне достаточным вмешательством при неалкогольном стеатогепатите без фиброза печени является модификация образа жизни. Безусловно, на усмотрение лечащего врача может быть назначена противовоспалительная или витаминотерапия.
Согласно заявлению авторов, в настоящее время проводится ряд крупных клинических исследований, направленных на выявление эффективных и безопасных методов лечения пациентов с неалкогольным стеатогепатитом и фиброзом печени, основные усилия которых сосредоточены на таргетинге трех общих патологических процессов, которые приводят к развитию и прогрессированию неалкогольного стеатогепатита: метаболический стресс, воспаление и фиброз.
Многие из испытуемых фармакологических агентов влияют более чем на одну из предполагаемых мишеней, а также рассматриваются их комбинации. Результаты нескольких испытаний уже представлены общественности, но ни один агент еще не получил одобрение Управления по контролю за пищевыми продуктами и лекарственными средствами США (US Food and Drug Administration) для лечения пациентов с неалкогольным стеатогепатитом.
Разрабатывается консенсус относительно общих принципов лечения пациентов с неалкогольным стеатогепатитом. Во-первых, относительно рискованное и довольно дорогостоящее лечение заслуживает внимания у пациентов с высоким риском прогрессирования заболевания и развития осложнений, но не оправдано у пациентов с более низким риском. Во-вторых, не может быть использована терапия, повышающая риск развития сердечно-сосудистых заболеваний или злокачественных новообразований, потому что эти заболевания и так являются ведущими причинами смерти среди пациентов с неалкогольным стеатогепатитом.
В-третьих, необходимо активно продвигать меры общественного здравоохранения, направленные на профилактику и управление неалкогольным стеатогепатитом и другими заболеваниями, связанными с метаболическим синдромом, путем пропаганды и поощрения приверженности здоровому питанию и физической активности, ограничения ненормированного и посменного графика работы, а также минимизации негативного воздействия факторов окружающей среды.
В заключение авторы акцентируют внимание, что неалкогольный стеатогепатит, связанный с висцеральным ожирением и метаболическим синдромом, является основной причиной развития цирроза и злокачественных новообразований печени. Распространенность неалкогольного стеатогепатита в США приближается к распространенности сахарного диабета 2-го типа, а его экономическое бремя дополнительно подчеркивает важность разработки мер по профилактике и лечению пациентов с этим заболеванием.
Однако позитивным является тот факт, что этиология и патогенез как неалкогольной жировой болезни печени, так и неалкогольного стеатогепатита становятся все более изученными и понятными, уже выделены ключевые процессы (метаболический стресс, воспаление и фиброз), исследован ряд генетических и экологических факторов, повышающих риск развития и влияющих на прогрессирование неалкогольного стеатогепатита. Более того, активно проводятся исследования различных фармакологических агентов, нацеленных на вышеуказанные механизмы.
Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции