Лечение рака вирусом оспы

5 декабря стало известно, что специалисты австралийской биотехнологической компании Имуген модернизировали вирус коровьей оспы, создав новый искусственный вирус. Эта смертоносная для рака конструкция получила название CF33.
Были проведены лабораторные исследования, во время которых вирус убил раковые клетки 60 различных видов. затем провели испытания на мышах. Учёных вновь ждал успех. В ближайшее время онколог из США Юман Фон намерен проверить убойную силу вируса в Австралии. Вирусом заразят пациентов с раком груди, желудка, лёгких, мочевого пузыря и раком кожи. Вирусы будут впрыскивать непосредственно в опухоли. Затем проведут исследования на пациентах, которые страдают от нескольких видов рака одновременно. Если испытания закончатся успешно, то человечество получит долгожданное лекарство от рака.
Правда скептики сомневаются и предполагают, что этот вирус может убить иммунная система человека. Но, как говорится, надежда умирает последней.
Американский онколог Юман Фонг объявил о начале испытаний на людях нового потенциального средства против рака, разработанного австралийской биотехнологической компанией Imugene, сообщает издание naked-science.ru.
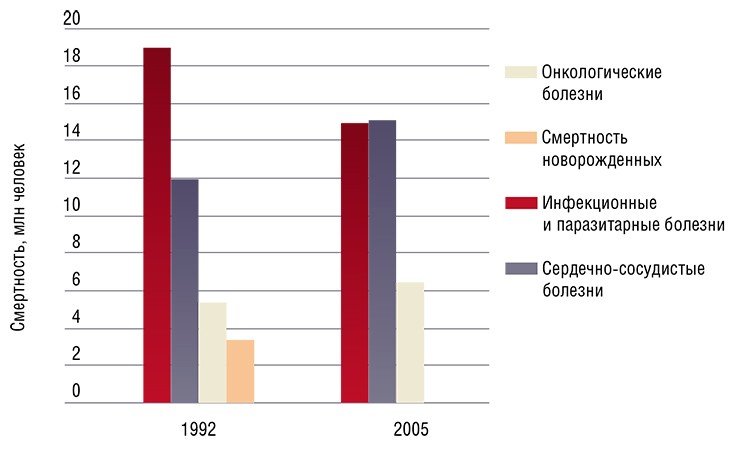
Ранее врачи заявили, что в ближайшее время число больных раком увеличится на 30 процентов. Об этом сообщил главный внештатный онколог Минздрава, академик РАН Андрей Каприн. По данным Всемирной организации здравоохранения, ежегодно в мире выявляется более 18 миллионов случаев заболеваемости раком, половина пациентов умирает.
Отметим, в России продолжает расти число умерших от рака людей. Только за первое полугодие 2019 года смертность от рака увеличилась на 1,5% по сравнению с аналогичным периодом 2018 года и составила 149 384 человека.
Онкология в Смоленской области занимает второе место по причинам смертности. Напомним, каждый седьмой смолянин умирает от рака. За шесть месяцев 2019 года, по данным ведомства, в Смоленской области умерло 7283 человек. От новообразований в нашем регионе погибли 1 005 человек, что больше на 11 пациентов, чем за аналогичный период прошлого года. Из них от злокачественных образований погибли 996 смолян.
Ранее мы рассказывали, что россиянам стала доступна иммунотерапия при лечении онкологии. Иммунотерапия отличается тем, что не воздействует на клетки злокачественной опухоли напрямую, позволяя иммунной системе самостоятельно обнаруживать и уничтожать опухолевые клетки. Поскольку применение иммунотерапии активирует собственную иммунную систему организма, эффективность лечения может быть значительно выше по сравнению с другими видами лекарственной терапии. Иммуноонкологические препараты входят в перечни ЖНВЛП и ОНЛС, поэтому многие пациенты с онкологическими заболеваниями имеют право на их получение.
Ранее медики назвали 5 признаков рака, которые люди часто не воспринимают всерьёз. Так, например, увеличение лимфатических узлов, которые не болят, говорят о развитии рака лимфатических узлов. Именно с этого началось заболевание у Кирилла Малышева. Смоленск сравнительно небольшой городок, где все друг друга знают. Весть о его болезни сразу же разлетелась не только по всем редакциям, в силу специфики его работы, но и по всему городу. Пожалуй, это первый в Смоленске человек, который не только спокойно, но ещё и с юмором может рассказывать о страшном заболевании – раке. Причём не о чужом, а о своём. О раке из первых уст.
Smolnarod решил выяснить причины смертности от онкологических заболеваний в Смоленской области. За комментариями мы обратились к главному врачу Смоленского областного онкологического диспансера Александру Эфрону. О самых распространённых в нашем регионе видах рака, причинах заболеваемости и способах выявления читайте в нашем материале.
Ученые Калифорнийского университета в Сан-Франциско создали генетически модифицированный вирус, который убивает раковые клетки, а также стимулирует иммунную реакцию против опухоли. Об этом сообщается в пресс-релизе на MedicalXpess.
Онколитический вирус Pexa-Vec представляет собой модифицированную версию вируса коровьей оспы. В него добавлен ген, кодирующий небольшую пептидную молекулу, которая стимулирует рост иммунных клеток. Кроме того, из вируса убран ген тимидин киназы, в результате чего инфекционный агент способен размножаться только в раковых клетках, в которых уровень киназы высок из-за мутации в специфических генах — RAS и p53.
Показано, что Pexa-Vec ограничивает рост кровеносных сосудов, которые питают злокачественную опухоль, снижая ее рост. При этом вакцину можно вводить внутривенно, а не непосредственно в тело опухоли, как другие онколитические вирусы. Это позволяет модифицированному инфекционному агенту атаковать не только первичный рак, но и метастазы, находящиеся в других местах организма.
Pexa-Vec был испытан на мышах, которые страдали от нейроэндокринного рака поджелудочной железы. Оказалось, что вирус не мог заразить здоровые органы, но поражал кровеносные сосуды. Хотя инфекционный агент уничтожил лишь часть злокачественных клеток, вызванный им иммунный ответ привел к исчезновению новообразования.
Мы попросили прокомментировать это сообщение главного научного сотрудника отделения биологии и биотехнологии Института фундаментальной медицины и биологии Казанского федерального университета, доктора биологических наук Альберта Ризванова.
- Исследование коллег из Калифорнийского университета представляется весьма перспективным и, я бы сказал, оригинальным, - говорит Альберт Анатольевич. - Само по себе использование в качестве агента версий вируса коровьей оспы не ново. Метод хорошо изучен, ученые, в том числе и мы, в КФУ часто используют вирусы для доставки генетического материала и для инфекции клеток с различной целью. Нюанс в том, что коллеги из США – как сказано в сообщении MedicalXpess – модифицировали вирус таким образом, что он реплицируется только в опухолевых клетках, не затрагивая здоровые, а также сумели заставить вирус синтезировать особый белок, который стимулирует иммунные клетки. Поэтому когда раковые клетки умирают из-за жизнедеятельности этого вируса, то они ещё и высвобождают белок, который служит своего рода раздражителем иммунных клеток, что приводит к выработке иммунитета против раковых клеток.
Таким образом получается, что вирус и убивает клетки, и натравливает иммунную систему организма на борьбу с онкологическим заболеванием. И такие результаты, насколько можно судить по открытым источникам, уже подтверждены доклиническими испытаниями на грызунах. Проводятся и первые фазы клинических исследований.
Тем не менее, должен разочаровать тех, кто, возможно, решит, что мы имеем дело с некоей панацеей, спасающей от всех онкологических заболеваний. Пока что речь идет о препарате для лечения лишь орфанных, то есть редко встречающихся, видов онкологических заболеваний. Это нисколько не умаляет значимости проделанной коллегами работы, скорее, наоборот, ведь фармацевтический бизнес не очень заинтересован в производстве таких препаратов в силу малой емкости рынка, и прекрасно, что государство поощряет компании, устанавливая более легкие условия для доклинических и клинических испытаний подобных средств, и есть люди, которые готовы вести в данном направлении продуктивные исследования. Думаю, не покажусь нескромным, если сообщу, что мы в КФУ тоже проводим исследования в области новых методов лечения онкологических заболеваний. Это, например, разработка препаратов на основе собственных опухолевых клеток пациента, генетически модифицированных специальным образом и кодирующих белки иммунной системы так, что усиливается иммунный ответ против собственных раковых клеток пациента.
Другой подход связан с применением уже нормальных стволовых клеток человека. Такие клетки способны к миграции в очаги опухолевого образования, метастазы, и если в них загрузить химические препараты или генетические конструкции, обладающие противоопухолевой активностью, то мы достигнем эффекта направленной доставки. Это работа в области создания таргетной терапии онкологических заболеваний. Кроме того, ведутся работы в области онкодиагностики. Например, мы проводим исследования связанные с анализом циркулирующих опухолевых клеток, циркулирующих в крови нуклеиновых кислот, таких как ДНК и РНК, наследственной онкогенетикой.
Подводя итог, позволю себе выразить надежду, что, по меньшей мере, по орфанным видам онкологии решение близко. Может, через 5-7 лет вакцина и таргетные препараты на основе генно-клеточных технологий могут стать доступной клиникам.
Исследования ученых показывают, что основная причина онкологических заболеваний заключается в вирусной этиологии. Это значит, что страшная болезнь поддается терапии. Главное, вовремя определить вирус, чтобы выстроить тактику лечения. Об этом рассказывает директор Единого лабораторного комплекса УрГЭУ, кандидат ветеринарных наук Наталья Кольберг.
– Наталья Александровна, неужели ученым удалось распознать природу раковых опухолей?
– Это не секрет, но об этом мало говорится. Рак шейки матки вызывает вирус папилломы человека, рак желудка – хеликобактер пилори и т.д. У заболевших наблюдается симбиоз вирусов, в основном, рода герпеса – это вирусы Эпштейна-Барр, Варицелла-Зостер (вирус ветряной оспы), Уреаплазма. В этой области ведутся большие исследования, например, Московским научно-исследовательским институтом вирусологии, в ходе которых ученые определяют наличие вирусов в злокачественных опухолях. На этапе раннего выявления проводится серологическая диагностика инфекционных заболеваний, проще говоря, пациенту назначают анализ крови на скрытую инфекцию в зависимости от наличия симптомов.
– Неужели вирус герпеса может способствовать образованию раковой опухоли?
– При наличии высоких значений вируса в организме нарушается нормальное деление клеток, как следствие происходит сбой иммунитета. При стрессе на фоне эндокринного и гормонального нарушений идет выработка третьей (лишней) безинформационной клетки. В таких клетках и развиваются вирусы, что становится питательной средой для развития онкологического заболевания.
Посмотрите результаты анализа пациентки N, у которой выявлен рак костной ткани. Анализ на онкомаркеры подтвердил заболевание. Затем она сдала кровь на выявление вирусов. Количественный показатель цитомегаловируса (вирус рода герпеса) при норме 6 единиц составляет 120! Не избавившись от цитомегаловируса, создающего питательную среду для онкоклеток, остановить рак, изменить онкомаркер не получится. Потому что злокачественная опухоль питается цитомегаловирусом. Смотрим далее, вирус Эпштейна-Барр – 57 единиц при норме 0,75. Не столь разительно, но также выше нормативного содержания других вирусов. Получается, масса разных видов герпеса приводит к мутации клетки, которая, в свою очередь, запускает механизм роста злокачественной опухоли.
Таким образом, повышая иммунитет, проводя противовирусную терапию, можно на 70% профилактировать онкоболезни. При возникновении сомнений, вопросов раз в год нужно делать серологический анализ крови на скрытые вирусы. Обязательно лечите вирусы, передающиеся по наследству.
– Наталья Александровна, почему наблюдается омоложение наследственных, семейных заболеваний? Болезни, характерные для людей зрелого возраста, все чаще выявляются у молодежи.
– Исследования ученых показывают, что болезни передаются не генетически, а при нарушении деления клеток, о чем говорилось выше, то есть при зачатии – оплодотворении яйцеклетки сперматозоидом. Говоря простым языком, если у мамы 100 клеток герпеса I типа, а у папы – 200 уреаплазмы, то при оплодотворении количество вирусных клеток у плода умножается на два. Так, у малыша уже 600 нежелательных бактерий, из-за этого начинается генетическая мутация, поэтому заболевания, передающиеся по наследству, возникают у ребенка не в 40-50 лет, как у родителей, а значительно раньше – в 20-30. Ревматоидный артрит или аденомы появляются не в 60 лет, а в 40-50. Соответственно, у внуков – ещё раньше. Посмотрите, сколько пациентов в детском онкоцентре!
– Анализы на скрытые вирусы дорогие, как правило, сделать их можно в частных клиниках и лабораториях. Видимо, в этом корень проблемы?
– У государства таких средств нет, поэтому в обычной поликлинике эти анализы не делают, и, скорее всего, так будет продолжаться долго. Далеко не каждый пациент может оплатить такие анализы в частном порядке. Лечение в случае выявления вирусов индивидуальное и тоже недешевое. Но знать об этом люди должны. Излечение возможно, если знать наследуемые вирусы и вовремя предпринять меры профилактики, не дожидаясь страшного диагноза.
– Что ещё нужно знать про вирус герпеса, меры профилактики?
Те, кто соблюдает посты, очищая организм, делают правильно. Во время поста отказ от мяса обусловлен отказом от белка животного происхождения. При недостаточной прожарке мяса белок становится питательной средой для нежелательных микроорганизмов. На первом уровне идут вирусы, на вирусах растут грибы, на грибах – бактерии. Поэтому при лечении нужно обязательно проводить противовирусную терапию. Не будет питательной среды для вируса – бактерия исчезнет.
– К какому врачу идти со своими жалобами и сомнениями, чтобы сохранить здоровье?
– Этими проблемами занимаются иммунологи, вирусологи, микробиологи. К сожалению, вирусология и микробиология отделены от медицины, но у нас много знающих, прошедших обучение врачей и в городских поликлиниках – урологи, гинекологи, дерматологи, гастроэнтерологи. При онкозаболевании грамотный врач сначала проведет противовирусную терапию. Только потом направит к хирургу, потому что если вирус герпесной этиологии, то при попадании воздуха он начнет развиваться молниеносно.
– Затраты на противовирусную терапию в десятки раз меньше, чем на лечение рака. Может, назовете эффективные препараты?

Исследования ученых показывают, что основная причина онкологических заболеваний заключается в вирусной этиологии. Это значит, что страшная болезнь поддается терапии. Главное, вовремя определить вирус, чтобы выстроить тактику лечения. Об этом рассказывает директор Единого лабораторного комплекса УрГЭУ, кандидат ветеринарных наук Наталья Кольберг.
По-видимому, есть вирусы, которые паразитируют на человеке, размножаясь ограниченно в группах клеток и не причиняя видимого вреда своему хозяину. Однако при определенных условиях они могут мутировать с образованием более патогенных вариантов. В этом случае возникает острая вирусная инфекция, которая заканчивается, когда в организме сформируется специфический иммунитет к патогену.
Но несмотря на относительно слабую изученность вирусного сообщества человека, практически сразу после открытия вирусов был обнаружен удивительный факт: у онкобольных вирусная инфекция может повлиять на протекание злокачественного процесса. Были зафиксированы случаи улучшения состояния таких пациентов и даже наступление длительной ремиссии после перенесенного вирусного заболевания либо вакцинации.
На основе этой информации еще в начале XX в. родилась идея использовать вирусы в борьбе с раковыми заболеваниями человека.
Взлеты и падения
Возможность создания принципиально новой формы терапии онкологических заболеваний, основанной на присущей вирусам способности убивать клетки, в которых он размножается, была впервые показана в середине прошлого века на примере рака шейки матки (Newman, 1954).
В результате удалось выделить и типировать ряд непатогенных для людей энтеровирусов, на основе которых были созданы живые энтеровирусные вакцины для профилактики сезонных вирусных заболеваний. При этом в ряде случаев удалось наблюдать положительный клинический эффект и в отношении злокачественных заболеваний, вплоть до полного исчезновения первичной опухоли и метастазов.

В ходе дальнейших исследований вакцинотерапию получили более полутора тысяч больных на поздних стадиях опухолевого процесса, и у части из них было отмечено улучшение состояния (Ворошилова, Ваганова, 1969; Ворошилова и др., 1977; Ворошилова, 1988).
Но уже в начале 1990-х гг. онколитические вирусы вновь стали объектом пристального внимания исследователей после публикации работы, посвященной лечению глиобластомы модифицированным вирусом простого герпеса (Martuza, 1991).
За последующие десятилетия благодаря выдающимся достижениям в молекулярной биологии и генетике и стремительному развитию биотехнологических методов исследования удалось проделать огромную экспериментальную работу по описанию специфических взаимодействий онколитических вирусов с раковымм клетками и выявить перспективные для терапии вирусные штаммы и типы опухолей, которые они могут поражать.
Почему же вирусы – и не какая-нибудь специфическая группа, а все в целом – поражают в первую очередь именно опухолевую ткань? Причин этому несколько.
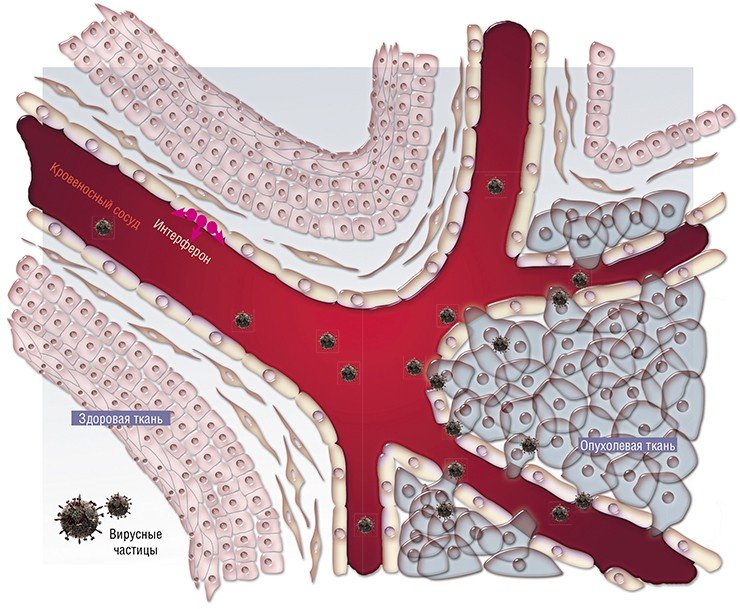
Таким образом, первая причина высокой чувствительности раковых клеток к вирусам – их физическая доступность.
Вторая причина связана со способами размножения самих инфекционных агентов. Дело в том, что вирусы в этом смысле не самодостаточны и используют для размножения ресурсы зараженной клетки. Обычно это происходит тогда, когда клетка сама находится в процессе деления и в ней присутствуют все ферменты, необходимые для репликации генетического материала и синтеза белков.
Некоторые вирусы имеют специальные механизмы, которые позволяют перевести клетку из покоящегося состояния в делящееся (к ним относятся и так называемые онкогенные вирусы, например, вирус папилломы, который вызывает рак шейки матки именно за счет стимуляции клеточного деления). Однако очень многие вирусы могут размножаться только в уже активно делящихся клетках, например, клетках слизистой (которая, как известно, в первую очередь поражается при сезонных вирусных инфекциях). И в этом смысле раковые клетки, главное занятие которых – деление, особенно беззащитны перед вирусной интервенцией.
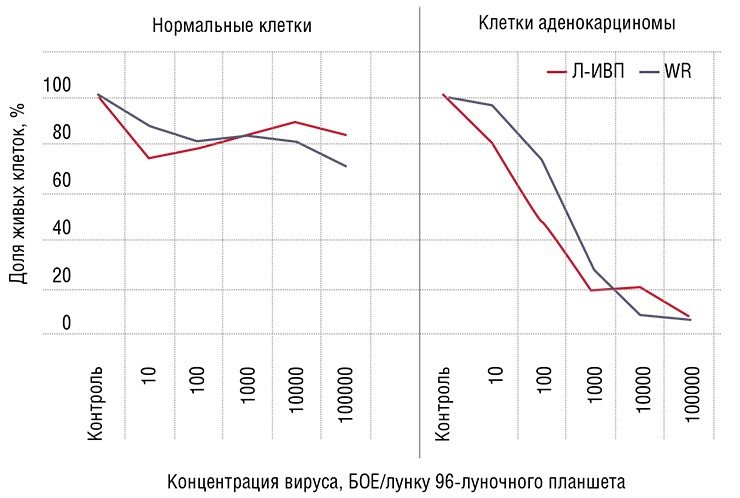
Здоровые – в безопасности
Таким образом, раковые клетки по милости самой природы служат готовой мишенью для вирусов. С использованием современных биотехнологий сегодня можно создавать вирусные препараты, которые будут специфически поражать и уничтожать только раковые клетки, не затрагивая здоровые.
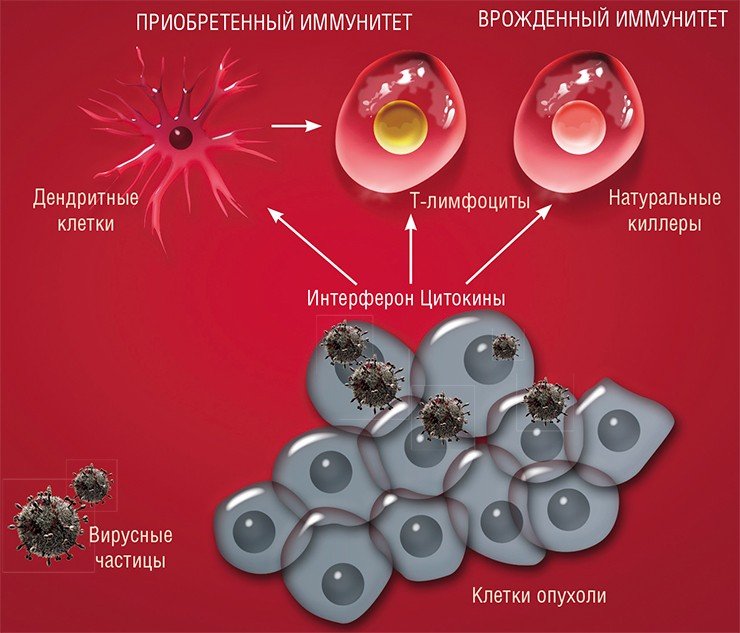
Поэтому мишенью вируса должны стать хаотичные скопища активно делящихся клеток. При этом в первую очередь будут поражаться наименее дифференцированные, наиболее злокачественные клетки. Здоровые же дифференцированные клетки будут защищены от проникновения такого дефектного вируса механизмами противовирусной защиты.
Персональный подход
Для решения этой задачи, в частности, проводится селекция вирусов на их способность размножаться в различных культурах раковых клеток. На основе анализа генетической структуры таких вирусов можно определить, какие из приобретенных вирусом мутаций делают его наиболее действенным в отношении определенного типа опухолевых клеток.
Имея панель таких онколитических вирусов, можно будет, взяв биопсию опухоли от конкретного пациента, подобрать для него наиболее эффективный набор вирусных штаммов. Причем эту процедуру можно повторять по мере лечения, поскольку сама опухоль может меняться, ускользая от действия онковируса. В таком случае сможет помочь уже другой вариант вируса, а так как он будет отличаться по антигенной структуре от предыдущего, то не уничтожится под действием механизмов противовирусного иммунитета, сформировавшегося в ходе предыдущего лечения.
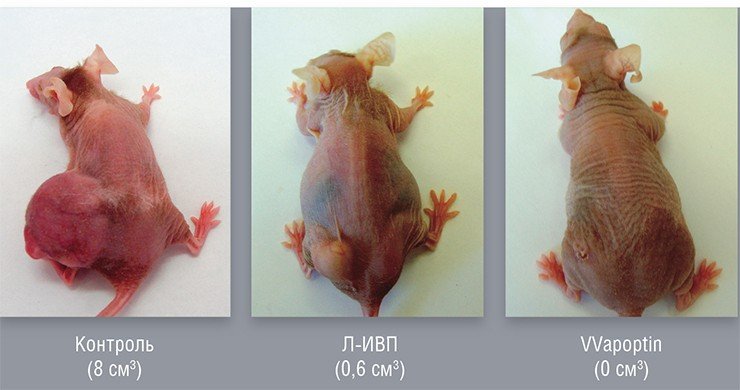
Онколитические вирусы можно дополнительно вооружить и генами, продуцирующими в раковой клетке белки, опасные лишь для этих клеток. Например, белок апоптин, выделенный из вируса птичьей анемии, по еще не совсем понятному механизму вызывает самоубийство исключительно только раковых клеток. На основе вируса осповакцины генно-инженерным способом уже создан такой штамм, способный эффективно уничтожать клетки опухоли человека, подсаженные лабораторным мышам.
Еще одна проблема терапии с помощью онколитических вирусов связана с разработкой наиболее эффективных способов их введения в организм. Ведь на пути вируса в организме встает много барьеров. К примеру, та же печень, являющаяся своего рода мощнейшим антивирусным фильтром.
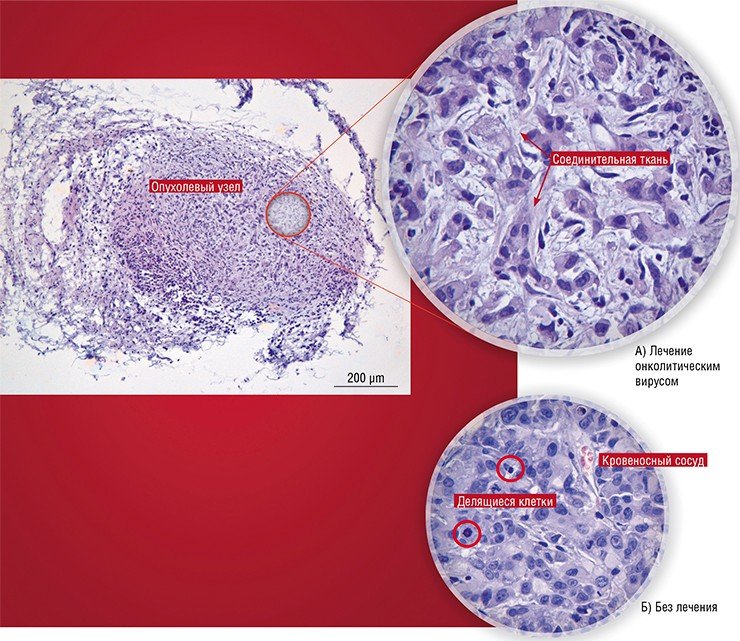
За и против
В настоящее время, несмотря на все успехи в изучении онколитических свойств вирусов, их применение в онкотерапии является, скорее, исключением, чем правилом.
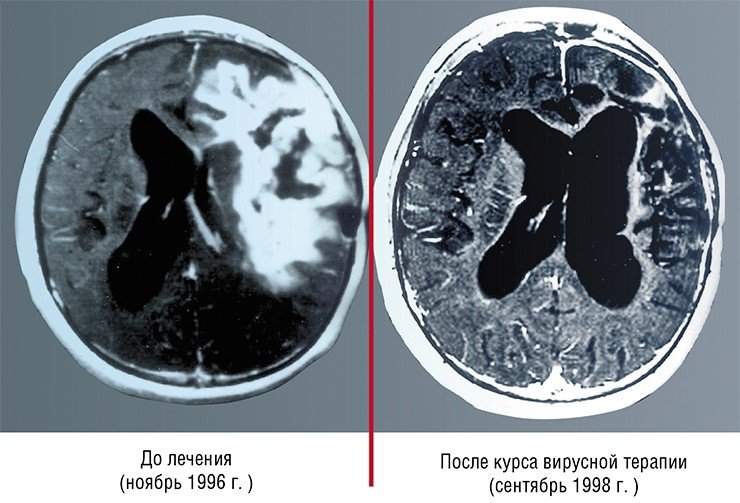
Так, разработанный в США препарат сегодня применяется с согласия пациента при лечении глиобластомы в качестве дополнительной терапии. В Китае лицензирован и успешно применяется для терапии карцином один из штаммов аденовируса, несущий две генетические делеции (Yu, 2007).
В Латвии после распада СССР были продолжены работы по изучению онколитических вирусов, начатые в рамках противополиомиелитных исследований. В результате на основе одного из энтеровирусов был создан и сегодня используется на практике препарат Ригвир, направленный против меланом, который можно вводить непосредственно в кровяное русло.
Всего же сегодня в мире проходят клинические испытания свыше тридцати разнообразных онколитических вирусных препаратов. И основная проблема здесь не столько научная, сколько экономическая. Дело в том, что терапия рака (в первую очередь химиотерапия) – это большие деньги. В условиях сложившегося и процветающего рынка химиотерапевтических препаратов применение новых, пусть даже и более безопасных биотерапевтических средств потребует весьма дорогостоящей перестройки всей системы лечения. А это не может не затронуть интересы крупных фармацевтических компаний.
Стратегия таких компаний в отношении нарождающихся разработок в области онколитических вирусов неоднозначна. Так, права на один из первых онколитических препаратов ONYX-015 вместе с самой компанией-разработчиком были приобретены одной известной фармацевтической фирмой, после чего исследования по этой теме были закрыты. С другой стороны, по¬скольку полностью остановить прогресс в этой области невозможно, уже сегодня во многих фармацевтических компаниях создаются подразделения, занимающиеся изучением вирусных онколитиков. Оптимизма добавляет и тот факт, что за последние пятнадцать лет число работ по этой тематике растет как снежный ком.
Одновременно с прогрессом в создании вирусных противораковых средств в обществе, как и в случае пресловутых генетически модифицированных организмов (ГМО), возникают разнообразные фобии и слухи. Они во многом базируются на недостаточной осведомленности широкой общественности в сути дела и раздуваются благодаря действиям некоторых заинтересованных компаний.
Действительно, вопрос о безвредности тех или иных вирусов пока изучен не до конца. Поэтому приходится мириться с тем, что на пути к широкому внедрению этих очень перспективных методов лечения рака будут вставать многие преграды. В любом случае, исследователи должны действовать очень обдуманно, осторожно взвешивая все возможные последствия.
Но, как учит история науки, подобные проблемы всегда вставали на пути любого нового перспективного метода лечения и, как правило, успешно преодолевались.
Сейчас крепнет уверенность, что знания, накапливающиеся в области вирусологии, иммунологии, биологии клетки и других смежных дисциплин, позволят (и уже позволяют!) создавать такие варианты вирусов, которые будут не только эффективно и избирательно уничтожать раковые клетки, не затрагивая нормальные, но еще и стимулировать в организме естественные механизмы противоопухолевой защиты.
В будущем основой для терапии рака могут стать искусственные вирусы. Уже сейчас дальней целью разработок московских и новосибирских специалистов является создание модульной вирусной системы (в будущем – полностью синтетической) – своего рода молекулярного конструктора, из которого исследователь по желанию сможет собрать из отдельных генетических компонентов нужный вариант онколитического вируса.
Такие синтетические вирусы не должны структурно напоминать природные. Это важно потому, что схожие вирусы способны рекомбинировать друг с другом, обмениваясь участками своего генома, благодаря чему терапевтический вирус может приобрести неполезные гены и, соответственно, нежелательные, опасные свойства. Можно разработать такой синтетический вирус, который по функциям и общему плану строения будет похож на природный, но по нуклеотидной последовательности будет настолько от него отличаться, что утратит способность к рекомбинации со своими природными собратьями.
Ворошилова М. К. Полезные для организма непатогенные штаммы энтеровирусов: профилактическое и лечебное их применение. М.,1988. С. 24–29.
Качко А. В. и др. Рекомбинантная плазмидная ДНК pAd5 f, несущая фрагмент генома аденовируса 5 типа с делецией в гене Е 1 В 55 К, и штамм мутантного аденовируса Adel2, обладающий селективной противоопухолевой активностью. Патент РФ № 2194755 (467) 05.03.01.
Качко А. В. и др. Варианты аденовируса типа 5 с делениями в ранних генах: способность к селективной репликации в р53 дефектных опухолевых клетках человека // Молекулярная биология. 2003. № 37 (5). С. 868–875.
Martuza R. L.et al. Experimental therapy of human glioma by means of a genetically engineered virus mutant//Science. 1991. V. 252. P. 854–856.
Первый за Уралом
Победители первого конкурса научных мегагрантов Правительства РФ, направленных на поддержку исследований под руководством ведущих ученых в российских вузах, были названы в октябре 2010 г. Всего на конкурс подавалось 507 заявок, которые были рассмотрены международными экспертами и утверждены Советом по грантам. Победители, среди которых оказался и Новосибирский национальный исследовательский государственный университет, получили финансирование в размере 150 млн рублей
Новосибирский национальный исследовательский государственный университет (НГУ) получил в 2010 г. три мегагранта правительства РФ, один из которых под руководством д.б.н., профессора П. М. Чумакова, предназначался для создания университетской лаборатории по исследованию онколитических вирусов.

В 2010—2012 гг. за счет средств мегагранта и софинансирования в НГУ реконструированы помещения для проведения практических занятий по микробиологии и частично – по аналитической химии. На этой базе был создан исследовательский комплекс из лаборатории микробиологии и вирусологии (руководитель П. М. Чумаков) и лаборатории бионанотехнологий (руководитель – проректор по научной работе НГУ, д.б.н., профессор С. В. Нетесов).
В вирусологическом боксе, оснащенном всем необходимым современным оборудованием для высокопроизводительной работы с непатогенными вирусами и их геномами, могут одновременно проводить исследования три сотрудника. Весной 2013 г. заканчивается реконструкция помещений для генно-инженерных работ, секвенирования геномов, а также биоинформационных и биотехнологических исследований.

В штат лабораторий вошли на долговременной основе несколько специалистов – докторов и кандидатов наук, а также аспиранты и студенты, ориентированные на научные исследования и разработки в самых современных областях микробиологии и молекулярной биологии. Во-первых, это изучение молекулярного разнообразия геномов вирусных возбудителей желудочно-кишечных и респираторных заболеваний человека и животных на территории азиатской части России. Во-вторых – создание онколитических рекомбинантных вирусов, а также бактерий, производящих рекомбинантные биологически активные белки человека, которые на сегодня признаются одними из самых перспективных противораковых препаратов.
Таким образом, принимая во внимание наличие в Научно-образовательном комплексе по наноматериалам и наносистемам НГУ нескольких суперсовременных электронных микроскопов, можно с утверждать, что в университете вступил в строй первый за Уралом современный лабораторный мини-комплекс по изучению микроорганизмов и разработке на их основе новых биомедицинских приложений.
Работы по этой тематике планируется проводить в сотрудничестве с передовыми биотехнологическими компаниями Новосибирской области и всего Сибирского федерального округа, а также, в случае взаимной заинтересованности, и с ведущими зарубежными предприятиями аналогичного профиля.
* Этот уровень биологической безопасности, по зарубежной классификации, используется для работы с возбудителями заболеваний человека, представляющими умеренную опасность для персонала и окружающей среды
Читайте также:


