Иммуноблоттинг гепатита с что это
Оригинал взят у в Про гепатит С
Гепатит С (гепатит ц)
Гепатит С (часто используют латинскую букву - “гепатит С”) - заболевание, при котором одноименным вирусом поражается печень. У большинства пациентов, несмотря на заражение вирусом, никаких симптомов долгое время (десятки лет) не возникает. Многие даже не знают, что они заражены.
Чаще всего гепатитом С заражаются при переливании крови или при использовании загрязненных игл (медработники, наркоманы, люди с татуировками).
Вакцины против гепатита С в настоящее время нет.
Симптомы гепатита с
Как уже было сказано, чаще всего гепатит С в течение многих лет протекает бессимптомно. Если симптомы все-таки возникают, они могут быть следующими:
боли в мышцах и суставах
болезненность в области печени
Как передается гепатит С
Чаще всего заражение происходит при контакте с зараженной кровью, т.е. при переливании крови или при пересадке органов от донора-носителя гепатита С. Всех доноров, разумеется проверяют на носительство инфекций, в том числе и на гепатит С, однако ошибки случаются.
Еще один важный механизм заражения гепатитом С - через грязные иглы, поэтому многие наркоманы больным гепатитом С.
Через половой контакт гепатит С передается редко (в отличие от гепатита Б), но этот путь также возможен, особенно при наличии более одного полового партнера, наличии других венерических заболеваний, у гомосексуалистов.
Перинатальное заражение - в редких случаях ребенок может заразиться гепатитом Ц от больной матери во время родов.
Факторы риска заражения гепатитом С
Риск заболеть гепатитом Ц выше у следующих групп населения:
у лиц с татуировками
у пациентов, получавших множественные переливания крови
у пациентов на гемодиализе
Осложения гепатита С
Цирроз печени. Как уже было сказано выше, гепатит Ц течет очень медленно. Цирроз может развиться через 20-30 лет после заражения.
Цирроз приводит к печеночной недостаточности (т.е. печень перестает выполнять свои функции) и к смерти.
Рак печени. Рак печени при гепатите Ц развивается редко (чаще рак печени возникает при гепатите Б)
Диагностика гепатита С
Самый распространенный анализ на гепатит + C - это проверка наличия к нему антител, anti-HCV. Положительный результат анализа говорит о присутствии антител против гепатита Ц в организме, а присутствие антител к гепатиту Ц автоматически говорит о наличии в организме и самого вируса гепатита Ц. Т.е. положительный анализ на гепатит Ц - это плохо! Следует учесть, что анализ на антитела может оставаться отрицательным, несмотря на наличие вируса в течение 6 месяцев после заражения.
Для подтверждения диагноза и выбора дальнейшей тактики лечения после получения положительного анализа на антитела к гепатиту + С
1. Измеряют количество вирусных копий в крови (анализ на вирусную нагрузку). Чем меньше вирусная нагрузка, тем лучше. По изменению вирусной нагрузки судят об эффективности лечения.
2. Проводят генотипирование вируса. От генотипа вируса зависит схема лечения.
3. Проводят биопсию печени. Биопсия - забор иглой небольшого кусочка печени для анализа. Забранный материал исследуют, чтобы определить, насколько вирус повредил печень.
Дополнительно о диагностике гепатита С
Аланин аминотрансфераза (АЛТ)
Аланин аминотрансфераза (АЛТ) используется для отслеживания эффективности лечения гепатита Ц. Однократный нормальный уровень АЛТ не исключает активной инфекции, прогрессирования гепатита Ц и цирроза. Нормализация АЛТ в результате терапии не является доказательством полного излечения.
Антитела к гепатиту Ц
Антитела к гепатиту C (анти-HCV) определяются при помощи иммуноферментного анализа (ИФА) второго и третьего поколений. Этот анализ обладает очень высокой специфичностью (97%), но не может отличить острую инфекцию от хронической, поэтому чаще всего используется только для скриннинга (первичного обнаружения) инфекции гепатита Ц. ИФА третьего поколения определяет антитела к кор-протеину и неструктурированным белкам 3, 4 и 5, он может стать положительным уже спустя 8 недель после заражения. Ложноположительный анализ на антитела к гепатиту Ц встречается у пациентов с иммунодефицитом, например, у больных ВИЧ первого типа, при почечной недостаточности.
Этот анализ используется для подтверждения наличия гепатита Ц. Положительным иммуноблот считается при обнаружении антител против двух и более антигенов гепатита Ц. Если обнаруживаются антитела только против одного антигена, анализ считается недостоверным. Если у пациента положительный результат иммуноблота, а два последующих анализа на наличие ДНК HCV отрицательны, считается что пациент вылечился от гепатита Ц. Если у пациента положительный ИФА, а иммуноблот отрицательный, то считается, что результат ИФА на самом деле ложноположительный, и дальнейшего обследования не нужно — у пациента нет гепатита Ц.
| ИФА | Иммуноблот | ДНК HCV | Интерпретация |
| положительный | не сделан | неподтвержденный гепатит Ц | |
| положительный | положительный | подтвержденный гепатит Ц | |
| положительный | положительный | отрицательный х 2 раза | излеченный гепатит Ц |
| положительный | отрицательный | гепатита Ц нет |
Качественное и количественное определение ДНК вируса гепатита Ц
Качественное определение ДНК вируса гепатита Ц проводится с помощью реакций амплификации - либо полимеразной цепной реакции (ПЦР) либо транскрипционно-опосредованной амплификации (ТОА). В настоящее время применяют два тест-набора: Amplicor Hepatitis C Virus Test, версии 2.0 (Roche Molecular Systems; Pleasanton, Calif) - ПЦР Cobas Amplicor Hepatitis C Virus Test (Roche Molecular Systems; Branchburg, NJ) Versant HCV RNA Qualitative Assay (Bayer HealthCare; Tarrytown, NY) - ТОА.
У первых двух наборов нижний порог чувствительности 50 МЕ/мл, а у третьего - 9.6 МЕ/мл.
Количественное определение ДНК гепатита Ц в крови проводится с помощью метода сигнальной амплификации либо с помощью метода целевой амплификации. Количественное определение ДНК используют для прогнозирования ответа на лечение и для мониторирования эффективности лечения. В настоящее время используется набор Versant HCV RNA, version 3.0 (Bayer HealthCare; Tarrytown, NY) с диапазоном 615-7,700,000 МЕ/мл.
Генотипы гепатита С
Генотипирование используют для прогнозирования ответа на лечение и длительности лечения. Пациентам, у которых обнаруживается вирус гепатита Ц первого и четвертого генотипов назначают курс лечения длительностью 12 месяцев, при обнаружении остальные генотипов курс лечения составляет 6 месяцев.
Генотипирование проводят одним из двух наборов 1. Trugene HCV 5‘NC Genotyping kit (Visible Genetics; Toronto, Canada) Line Probe Assay (Inno LiPA HCVII, Innogenetics; Ghent, Belgium)
Лечение гепатита Ц
Положительный анализ на гепатит Ц не означает автоматически, что пациента надо лечить. Во многих случаях выбирается выжидательная тактика, т.к. риск осложнений относительно невелик, а риск побочных эффектов от лечения может быть существенно больше.
В настоящее время в лечении гепатита Ц используются несколько противовирусных препаратов, которых можно будет почитать тут: лечение гепатита Ц.
Если печень поражена вирусом настолько, что не может больше выполнять свои функции, у больного развивается печеночная недостаточность. Единственное эффективное лечение печеночной недостаточности - пересадка печени.
Во время операции по пересадке печени хирург удаляет пораженную вирусом печень и пересаживает здоровый трансплант. Донорскую печень либо извлекают из трупа, либо - реже - берут у живого донора.
После пересадки вирус гепатита Ц (он все равно остается в организме) начинает повреждать и донорскую печень, поэтому даже после пересадки печени больные должны продолжать получать противовирусную терапию, чтобы заторомозить этот процесс.
Лечение гепатита Ц преследует следующие цели:
достичь долговременной эрадикации вируса гепатита Ц - устойчивого вирусный ответа (УВО), который определяется как отсутствие РНК вируса гепатита Ц в крови пациента после окончания лечения в течение 6 месяцев и более
предотвращение развития цирроза печени, рака печени и печеночной недостаточности.
После 12 недель лечения оценивают ранний вирусный ответ, повторяя анализ на количество РНК копий и проводят скриннинг на дисфункцию щитовидной железы, вызванной интерфероном. Если РНК вируса не определяется или отмечается снижение количества копий в 2-log (6.32 раза), лечение должно быть продолжено, т.к. у 65% этих пациентов будет достигнут устойчивый вирусный ответ. Если ситуация обратная, и ранний вирусный ответ не получен, то лечение целесообразно прекратить, потому что устойчивый вирусный ответ будет получен менее чем у 3% пациентов.
Через 6 месяцев лечения снова проверяют количество копий РНК вируса гепатита Ц, если РНК в крови определяются, у пациента произошел рецидив, и нужна альтернативная схема лечения. Если РНК не определяются, значит у пациента достигнут устойчивый вирусный ответ.
Показания к противовирусной терапии при гепатите C
у пациента должно быть повышение АЛТ
пациент должен быть старше 18 лет
у пациента должны быть антитела anti-HCV и в крови определяться РНК гепатита Ц
желательно до начала лечения выполнить биопсию печени
у пациента не должно быть противопоказаний к лечению
Схемы лечения гепатита С
В настоящее время чаще всего используют два рекомбинантных интерферона:
интерферон альфа-2б - Интрон-А (Intron-A; Schering-Plough, Kenilworth, NJ)
и интерферон альфа-2а — Роферон (Roferon; Hoffmann-La Roche, Basel, Switzerland)
Они отличаются друг от друга всего лишь одной аминоксилотой.
Исследуется т.н. консенснусный интерферон Альфакон-1 alfacon-1 (Infergens; Amgen, Thousand Oaks, Calif), который сконструирован из 12 наиболее часто встречающихся аминокислотных последовательностей натуральных интерфероном. Теоритически он должен обладать большей способностью к активации цитокинов, лучшими антивирусными, антипролиферативными свойствами, сильнее активировать натуральные киллеры, чем интерфероны альфа-2а и альфа-2б, однако в исследованиях консенснусного интерферона в дозе 9 мкг его эффективность не превышала эффективности стандартных альфа-интерферонов.
Развитие интерфероновых технологий привело к появлению пег-интерферонов. К интерферону добавляется молекула полиэтиленгликоля (этот процесс называется пегилирования), в результате пег-интерферон лучше усваивается, медленее выводится из организма и обладает более длительным временем полужизни, поэтому пег-интерфероны вводят один раз в неделю.
В настоящее время используют два пег-интерферона:
Пег-интрон - PEG-Intron (Schering-Plough), который состоит из двух молекул альфа-2б интерферона присоединенных к 12-кД пег-цепи. Он преимущественно метаболизируется печенью
Пегасис - Pegasys (Hoffmann-La Roche), который состоит из двух молекул альфа-2а интерферона, присоединенных к 40кД разветвленной пег-молекуле. Этот препарат преимущественно выводится почками.
В нескольких исследованиях было показано, что при в сравнении с обычными интерферонами при использовании пег-интерферонов устойчивый вирусный ответ достигался чаще, при этом частота побочных эффектов была одинакова.
Рибавирин
Добавление к монотерапии интерферонами перорального препарата рибавирина открыло новую эру в лечении гепатита Ц.
Эффективность добавления к терапии рибавирина хорошо видна на рисунке.
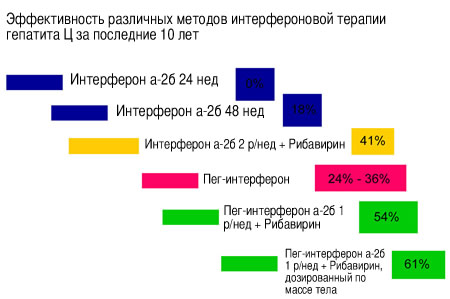
По рекомендациям 2002 г. стандартная терапия на сегодняшний день (2011 г) следующая: пег-интерферон + рибавирин в течение 48 недель при лечении гепатита Ц генотип 1, и пег-интерферон+рибавирин в течение 24 недель при лечении гепатита Ц генотипа 2 или 3.
Комбинированная терапия интерферон + рибавирин в 75% случаев вызывает побочные эффекты:
Интерферон — гематологические осложнения (нейтропения, тромбоцитопения), нейропсихиатрические осложенения (ухудшение памяти и концентрации, нарушения зрения, головные боли, депрессия, раздражительность), гриппоподобные состояния, метаболические нарушения (гипотиреоз, гипертиреоз), желудочно-кишечные осложнения (тошнота, рвота, потеря веса), дерматологические (алопеция), легочные (интерстициальный фиброз)
Рибавирин — гематологические (гемолитическая анемия), репродуктивные, легочные (интерстициальный фиброз).
Некоторые побочные фактор поддаются лечению:
нейтропения — назначение колоний стимулирующего фактора
Телапревир
Телапревир — специфический ингибитор неструктурной 3/4A протеазы вируса гепатита Ц. Этот перспективный препарат, быстро снижающий количество РНК копий сейчас проходит испытания. Его применяют в комбинации с пег-интерфероном и рибавирином.
Что еще можно сделать?
Если больной гепатитом C заболеет гепатитом А или Б, то последствия могут быть самыми тяжелыми, поэтому больные вирусным гепатитом С должны быть вакцинированы против гепатитов А и Б. Вакцины от гепатитов А и Б эффективны и безопасны.
Отказаться от приема алкоголя даже в минимальных количествах.
Быть острожнее с безрецептурными лекарствами. Некоторые препараты, считающиеся абсолютно безопасными (напр., ацетаминофен (панадол, парацетемал)) для больных с пораженной печенью вовсе не являются таковыми.

Молочный чертополох или Расторопша пятнистая (Silybum marianum) - препарат, предположительно способствующий улучшению детоксификационной функции печени и улучшающий регенерацию печеночной ткани.


- Главная /
- Лабораторная диагностика /
- ИФА, иммуноблот, иммунофлуоресценция /
- Реагенты для ИФА /
- Вирусные инфекции /
- Иммуноблот HCV IgG
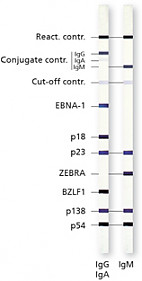
Набор реагентов для определения HCV IgG методом иммуноблота
Упаковка: 20 тестов
Доставка: Складская позиция
Цена: по запросу
Назначение: набор recomLine HCV IgG предназначен для качественного определения человеческих IgG-антител к вирусу гепатита С (HCV) в образцах сыворотки или плазмы методом иммуноблота с целью подтверждения сомнительных результатов скрининговых тестов.
Анализируемые антигены: ядерный антиген 1, ядерный антиген 2, хеликаза, NS3, NS4, NS5.
Приложения теста:
Вирус гепатита С (НCV)
До того, как он был идентифицирован, вирус гепатита C был классифицирован как так называемый вирус гепатита не A/не B, вызывающий наибольшее число случаев гепатита, передающегося при переливании крови или с другими продуктами крови. Случай не A/не B гепатита характеризуется инкубационным периодом от 2 до 26 недель (в среднем: 8 недель) и, в большинстве случаев, относительно умеренными проявлениями в острой фазе. У до 80% пациентов развивается хронический гепатит, в некоторых случаях приводит к циррозу печени и гепатоклеточной карциноме. В мире насчитывается около 170 миллионов пациентов с хронической инфекцией. Частота заболевания в Германии составляет 0.6%.
Инфекционный агент данного типа гепатита был идентифицирован в 1989, это одноцепочечный РНК-вирус, который назвали вирус гепатита C (HCV). Патоген принадлежит к семейству флавивирусов, которое также включает вирус желтой лихорадки и вирус клещевого энцефалита (TBE). Длина его генома составляет 9.5 Kb, он кодирует один капсидный белок (поверхностный), два мембранных белка (E1 и E2) и четыре неструктурных белка (NS2 - NS5).
Эпидемиология и инфицирование
До тех пор, пока не стали доступны подходящие методы детекции, вирус гепатита C был причиной 80 - 90% случаев инфекции гепатита не A/не B. Этот вирус заражается только людей и обычно передается при переливании крови или с другими продуктами крови. Один из каждых 3-5 тысяч доноров крови имеет положительный результат. Риск развития инфекции после получения дозы положительной крови составляет примерно 75%.
80% новых случаев инфицирования наблюдается у наркоманов, из-за общих шприцов и игл для инъекций. Другие потенциальные пути передачи включают половые контакты и бытовые контакты с инфицированными людьми при плохих гигиенических условиях. Больничный персонал относится к группе риска из-за возможных травм иглами для инъекций. Вирус может передаваться от матери к ребенку во время беременности. Путь передачи неизвестен в примерно 30% случаев.
Патогенез и клинические аспекты
Вирус непосредственно попадает в кровоток, обычно с зараженной кровью или продуктами крови. Он переносится в печень инфицированными макрофагами, где инфицирует и и разрушают гепатоциты. В результате развивается воспаление печени (гепатит) и некроз ткани.
Примерно в 75% случаев инфекция протекает бессимптомно, тяжелой течение заболевания встречается достаточно редко. У до 80% инфицированных людей развивается хронический персистирующий или хронический реактивный гепатит. В 10 - 20% хронических случаев в итоге развивается цирроз печени, и в примерно 4% этих случаев развивается первичная гепатоцеллюлярная карцинома.
Диагностика
Первым шагом лабораторной диагностики инфекции гепатита C является определение специфических антител к белкам HCV с помощью скрининговых тестов иммуноферментным методом (ELISA). Затем реактивность ELISA подтверждается более специфичным методом блота, и тем самым уровень их специфической реактивности может быть оценен раздельно.
При положительных результатах определения антител к HCV рекомендуется проводить определение вирусной РНК с использованием метода амплификации нуклеиновых кислот (NAT, nucleic acid amplification technique), например, RT/PCR (ПЦР в реальном времени). NAT должна подтвердить или исключить персистенцию, что может иметь терапевтические последствия. В случае, если получен отрицательный результат ПЦР при положительном результате подтверждающего теста на присутствие антител, исследование RT/PCR необходимо повторить с интервалом в несколько месяцев. Только после этого может быть сделан относительно надежный вывод о хроническом характере инфекции HCV.
Антитела к специфическим антигенам HCV обычно выявляются через 3 – 4 недели после HCV инфекции. Исключением является "диагностическое окно", во время инкубационного периода и ранней острой фазы инфекции. В этот период очень небольшие количества вируса задерживают иммунный ответ. У пациентов с ослабленным иммунитетом и новорожденных с перинатальной инфекцией также наблюдается "искаженная" картина иммунного ответа (у новорожденных из-за материнских антител). Подтверждение диагноза инфекции HCV в этих случаях возможно только при повторяющихся положительных результатах выявления генома HCV с помощью NAT.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
После идентификации в 70-е годы вирусов гепатитов А и В перед клиницистами и вирусологами возникла проблема выявления этиологического фактора большого количества сывороточных гепатитов, при которых отсутствовали маркеры инфицирования вышеуказанными вирусами. Длительное время диагноз устанавливался методом исключения, и этот тип гепатита был известен как гепатит ни А ни В. В 1989 г. Houghton и соавт. идентифицировали вирус гепатита С (HCV), и это название пришло на смену термину "гепатит ни А ни В с парентеральным механизмом передачи".
Выявление антител к HCV. Наибольшее распространение благодаря своей надежности и чувствительности получил иммуноферментный метод (enzyme linked immunosorbent assay, ELISA). Тест-система первого поколения (ELISA-1) выявляла антитела к антигену С100. В дальнейшем были получены новые клоны РНК HCV, продуцирующие другие вирусные антигены для обнаружения соответствующих антител (см. таблицу ), и появились второе и третье поколения тест-систем ELISA. Будучи значительно более чувствительной и специфичной по сравнению с тест-системами предыдущих поколений, ELISA-3 широко используется для скрининга доноров. Важно, что ELISA-3 позволяет выявлять антитела к NS5-pemoHy, так как до 5% вирусоносителей имеют в крови только данный тип антител, вследствие чего при использовании первых поколений ELISA получают ложноотрицательные результаты.
ELISA-3 дает почти 100% гарантию выявления носителей анти-HCV при скрининге доноров и диагностике вирусных заболеваний печени. Однако в двух случаях антитела могут не быть обнаружены. Во-первых, антиHCV в крови могут появляться в срок до 6 мес после инфицирования (в среднем через 12 нед), т.е. в определенный период течения инфекции имеется так называемое "серологическое окно". Во-вторых, антитела могут не быть обнаружены у больных, получавших иммуносупрессивную терапию (например, после трансплантации органов). Кроме того, несмотря на высокую специфичность ELISA-3 (99,7%), возможны также ложноположительные результаты.
Таблица
Для исключения ошибки используют подтверждающие тесты, такие как рекомбинантный иммуноблоттинг (recombinant immunoblot assay, RIBA), и, реже, анализ синтетических пептидов (Inno-Lia). При использовании RIBA антигены HCV наносят раздельно на полоски нитроцеллюлозы и инкубируют с сывороткой больного. При наличии соответствующих антител происходит их визуализация. Тест-система третьего поколения (RIBA-3), широко распространенная в Европе, содержит синтетические пептиды c o re-региона и NS4 и рекомбинантные NS3 и NS5 (см. таблицу). Результаты RIBA считаются положительными при выявлении антител более чем к одному региону HCV [30].
У большей части RIBA-положительных больных вирус находится в состоянии репликации, что подтверждает обнаружение у 75 - 80% из них РНК HCV. Отсутствие РНК при наличии анти-HCV может быть обусловлено элиминацией вируса после перенесенной инфекции, уровнем виремии ниже порога чувствительности ПЦР, либо это может означать, что результат анализа на наличие антител является ложноположительным. А.Alberti и соавт. [3] отмечена связь между отсутствием РНК HCV у анти-HCV положительных больных и отсутствием воспалительных изменений в биоптатах печени, что, по-видимому, является свидетельством элиминации вируса. Однако вирусная РНК может не выявляться у больных после курса противовирусной терапии; в таких случаях не исключены ее наличие в подпороговых титрах или персистенция вируса в тканях, делающая его недоступным для детекции. Следовательно, лиц, положительных по анти-HCV, даже при отсутствии признаков виремии, необходимо рассматривать как потенциально опасных в плане заражения HCV.
Рекомбинантные белки, используемые в тест-системах ELISA и RIBA [32].
Выявление вирусной РНК. Определение наличия в сыворотке РНК HCV необходимо для:
1 ) подтверждения инфекции HCV у анти-HCV положительных пациентов или при подозрении на инфицирование при отсутствии антител к вирусу;
2) ранней диагностики острого гепатита;
3) контроля за перинатальной передачей вируса;
4) определения показаний к назначению противовирусной терапии;
5) контроля за эффективностью противовирусной терапии [30].
Наибольшее распространение получила ПЦР, заключающаяся в синтезе множества копий ДНК на основе вирусной РНК при помощи обратной транскриптазы с последующим электрофорезом в полиакриламидном геле [15]. С помощью ПЦР можно обнаруживать РНК как в сыворотке, так и в биоптатах печени. В последнее время получает распространение количественное определение РНК, для которого применяются такие методики, как анализ серийных разведений и амплификация разветвленной ДНК [ 16].
Следует отметить, что последний метод, позволяющий наиболее точно определить степень виремии, является менее чувствительным (его чувствительность составляет около 70% таковой ПЦР) и, следовательно, одновременно с ним необходимо использовать ПЦР.
Реже применяют другие методики, такие как лигазная цепная реакция и изотермическая амплификация нуклеиновых кислот.
В настоящее время основным препаратом для лечения гепатита С, как и других вирусных гепатитов, является интерферон (ИФН). По современным представлениям, выделяют два типа ИФН. К типу 1 относятся a - и b -ИФН, к типу II - g -ИФН. Подразделение на типы обусловлено различной биологической ролью: если a - и b -ИФН свойственна в основном противовирусная активность, то g -ИФН (имукин) является универсальным эндогенным иммуномодулятором. Наибольшее распространение в качестве средства этиотропной терапии вирусных гепатитов получил a -ИФН, как нативный (получаемый из культуры лейкоцитов человека), так и рекомбинантный; различий в терапевтической эффективности между этими формами не обнаружено. Реже встречаются работы, посвященные применению b -ИФН.
Высокая частота хронизации гепатита С побуждает к поиску средств воздействия на вирус в острой фазе инфекции. При использовании ИФН для лечения остро го гепатита С получают неоднозначные результаты. М.
Omata и соавт. [23] лечили b -ИФН 14 больных в течение 30 дней, общая доза составила 52 ME. Ремиссия наступила у II, остальным был назначен повторный курс ИФН. Через 3 года наблюдения активность АЛТ оставалась повышенной у 1 больного (в контрольной группе нормализовалась только у 3). Больные, у которых отмечалась биохимическая ремиссия, стали также негативными по РНК HCV [24]. Еще в трех исследованиях с использованием рекомбинантных a -2a (роферон) и ( a -2b (интрон А) ИФН показано снижение частоты хронизации гепатита, но в двух из них результаты были статистически недостоверными [3, 7, 31]. Окончательный вывод, снижает ли терапия ИФН частоту хронизации острого гепатита С, можно будет сделать на основе результатов длительного наблюдения.
Основным показанием к назначению ИФН при хроническом гепатите С является обнаружение в сыворотке вирусной РНК. Дополнительными критериями являются повышение уровня сывороточных трансаминаз не менее чем в 1,5 раза и гистологическая картина хронического гепатита. К основным факторам, определяющим хороший ответ на ИФН, относятся: молодой возраст, гетеросексуальная ориентация, отсутствие ВИЧинфекции, парентеральное заражение вирусом, небольг шая продолжительность заболевания, отсутствие гистологических признаков перехода в цирроз, отсутствие биохимического синдрома холестаза, слабовыраженный аутоиммунный компонент. Наряду с вышеперечисленными прогностическими факторами в последние годы большое значение придается низким исходным титрам РНК HCV и генотипу вируса [9, 15, 27, 29].
Разные генотипы HCV обладают различной чувствительностью к ИФН. Наиболее чувствительным считается генотип 3 (до 70% положительных результатов лечения ИФН). Существенно меньшей чувствительностью обладает генотип 2. Генотип 1 (распространенный в Северной Европе), особенно подтип 1Ь, характеризуется тяжелым течением и резистентносью к противовирусной терапии; данный подтип распространен на Дальнем Востоке и в Японии [ 18, 30]. Однако, по другим данным, генотип вируса не является значимым фактором, определяющим ответ на ИФН. Решающее значение имеют титры РНК HCV, выявленные перед началом лечение [II, 14]. При низких титрах РНК быстро наступает стойкая серологическая и биохимическая ремиссия. Некоторые авторы отмечают корреляцию между генотипом вируса и степенью виремии. Так, М. Omata и соавт. [23] у инфицированных вирусом с генотипом 2 наблюдали более высокие титры РНК HCV, чем у инфицированных вирусом с генотипами 3 и 4, что коррелировало с худшим ответом на лечение ИФН. Y. Kobayashi и соавт. [15] указывают на высокую частоту инфицирования вирусами с различными генотипами, что снижает значение идентификации генотипа HCV и выводит на первое место количественное определение виремии [ 15 ].
Средние дозы ИФН составляют 3-5 ME 3 раза в неделю на протяжении 6 мес., хотя некоторые авторы указывают, что более низкие дозы (от I ME) также могут быть эффективны [12, 21]. Основным критерием успешности лечения служит исчезновение из сыворотки вирусной РНК, что также коррелирует с нормализацией или снижением уровня трансаминаз и улучшением результатов гистологического исследования биоптатов печени [8,21,25,26,33]. Положительный эффект отмечается в среднем у 50% больных, из них у половины в течение полугода после окончания лечения происходит рецидив [4, 6, 11, 30]. Имеются данные, что 12-месячный курс с последовательным снижением дозы имеет ряд преимуществ [19]. P. Jouet и соавт. [ 13] провели исследование с участием 108 больных хроническим гепатитом С, у части из которых имелись признаки цирроза. Больным 1-й группы ИФН назначали по обычной схеме (3 ME 3 раза в неделю в течение 6 мес), 2-й - в течение 12 мес с постепенным снижением дозы (по 3 ME 3 раза в неделю в течение 6 мес, по 2 ME следующие 3 мес и по 1 ME еще 3 мес). Через 6 мес после окончания лечения ремиссия сохранялась в среднем у 13,5% больных 1-й группы и у 28,6% больных 2-й группы; при отсутствии цирроза частота стойкой ремиссии была значительно выше .
В качестве возможного механизма резистентности к ИФН рассматриваются изменения структуры гипервариабельного региона (ГВР), находящегося на 5'конце гена E2/NSI РНК HCV, который является мишенью иммунологического надзора и играет важную роль в персистенции вируса. Отсутствие эффекта от назначения ИФН может быть обусловлено "ускользанием" от иммунного ответа хозяина структурно измененного ГВР. Эволюция ГВР может происходить непосредственно в процессе лечения ИФН [10] .
Большое количество больных с хроническими вирусными поражениями печени, резистентных к терапии ИФН, а также высокая частота рецидивов диктуют необходимость поиска комбинаций ИФН с другими противовирусными средствами. Не останавливаясь подробно на каждой из них, следует отметить, что во многих исследованиях выявлена их невысокая эффективность. R. Mtiller [20] на основании анализа контролируемых клинических испытаний делает вывод об отсутствии преимуществ комбинированной противовирусной терапии перед монотерапией ИФН. В то же время в последние годы снова стали появляться данные о выраженном положительном эффекте комбинаций ИФН с рибавирином при повторном курсе у ИФН-резистентных больных. S .
Brillanti и соавт. [5] проводили дифференцированное лечение двух групп больных, не давших положительного ответа на 6-месячный курс a -ИФН. 1-й группе было продолжено введение ИФН в прежней дозировке (3 ME 3 раза в неделю) в течение следующих 6 мес, больным 2-й группы к ИФН добавили 800 мг рибавирина per os. В обеих группах отмечено значительное снижение уровня трансаминаз, однако через 9 мес после окончания лечения биохимическая ремиссия сохранялась только у пациентов 2-й группы. Исчезновение РНК HCV наблюдалось у 40% больных 2-й группы и лишь у 1 больного 1-й группы. Положительный ответ на комбинированную терапию коррелировал с уменьшением воспалительно-некротических изменений в печени [5]. Обнадеживающие результаты получены G. Mazella и соавт. [17] при комбинированном лечении ИФН и урсодезоксихолевой кислотой (УДХК) (600 мг УДХК ежедневно и ИФН в обычной дозировке) больных хроническим гепатитом С, резистентных к ИФН. Ремиссия наблюдалась у 13 из 29 больных, в том числе у 7 на протяжении 6-месячного периода наблюдения. В контрольной группе, продолжавшей монотерапию ИФН, только у 2 отмечена нестойкая ремиссия. Положительный эффект обусловлен, по-видимому, иммуномодулирующим влиянием УДХК, которая, таким образом, потенциировала действие ИФН .
Кроме комбинации с противовирусными препаратами, некоторые авторы предлагают проведение короткого курса терапии глюкокортикостероидами с последующим назначением ИФН [20]. Теоретически эффективность такого лечения может быть обусловлена усилением репликации вируса на фоне иммуносупрессии и последующим ее подавлением ИФН .
1. Ивашкин ВТ, Хазанов АИ, Ивлев АС и др. Рос. ж . гастроэнтерол., гепатол. 1994:2:12-4 .
2. Логинов АС, Царегородцева ТН, Зотина ММ Рос . ж. гастроэнтерол., гепатол. 1994:2:63-5 .
3. Alberti A, Chemello ., Benvengu L, et al. Viral hepa titis and liver disease. - Baltimore: Williams and Wilking 1991:656-8.
4. Brestress D. Current studies in hematology and blood transfusion: hepatitis С virus.-Basel: Karger 1994:121-36.
5. Brillanti S, Garson J, Foli M, et al. Gastroenterology 1994:107:812-7.
6. Cirelli R, Tyring SK. Clin. Immunother 1995:3:2887.
7. Colombo M, Lampertico P, Rumi M. Gut 1993:34:141.
8. David E, Pucci A, Palladin D, et al. Am J Clin Pathol 1992:98:397-401.
9. Davis GL. J Hepatol 1994:21:1-3.
10. Enomoto N, Sato C, Kurosaki M, Marurno F. J Hepatol 1994:20:252-61.
11. Hagiwara H, Hayashi N, Mita E, et al. Gastroenterology 1993:106:686-90.
12. Hoofnagle JH, DiBisceglie AM. Viral hepatitis and liver disease New York: Alan R. Liss Inc 1988:82330.
13. Jouet P, Roudot-Thoraval F, Dhumeaux D, et al. Gastroenterology 1994:106:686-90.
14. Kleter GE, Brouwer JT, Heijtink RA, et al. Antimicrob Agents Chemother 1993:37:595-7.
15. Kobayashi Y, Watanabe S, Koniski M, et al. Hepatology 1993:18:619-24.
16. Lau JYN, Davis GL, Kniffen J, et al. Lancet 1993:341:1501-4.
17. Mazzella G, Cipolla A, Novelli V, et al. United European Gastroenterological Week Oslo 1994:1042:272.
18. McOmish F, Yap PL, Dow ВС, et al. J Clin Microbiol 1994:32:884-94.
19. Metreau JM and the French group for the study of NANB. С chronic hepatitis treatment Gut 1993:1112-3.
20. MuUerR. Hepatogastroenterology 1991:38:4-9.
21. Muller R, Klein H, Niehoff G. Z ges inn Med 1988:43:705-10.
22. Negro F, Baldi M, Mondardini A, et al. Gastroenterology 1994:107:479-85.
23. Omata M, lto Y, Yokosura 0, et al. Dig Dis Sci 1991:36:1217-22.
24. Omata M, Yokosura 0, Takano S, et al. Lancet 1991:338:914-5.
25. Rizzetto M. Executive summary of a Seminar on hepatitis С Luxemburg 1994:7-8 .
26. Saracco G, Rosina F, Torrani Cerenzia MR, et al. J Hepatol 1990:11:43-9.
27. Takada N, Takase S, Enomoto N, et al. J Hepatol 1992:14:35-40.
28. Toyoda H, Nakano S, Takeda I, et al. J Gastroenterol 1994:89:437-42.
29. Tsubota A, Chayama K, Ikeda K, et al. Hepatology 1994:19:1088-94.
30. Van der Poel CL, Cuypers ТН, Reesink HW . Lancet 1994:344:267-9.
31. Viladomiu L, Genesca J, Esteban JL, et al. Hepatology 1992:15:767-9.
32. Weiland 0. Executive summary of a Seminar on Hepatitis С Luxemburg 1994:5-7 .
33. Weiland 0, Scwarcz R, Wejstai R, et al. J Hepatol 1990:11:57-62.
Читайте также:


