Гепатит с пегасис рибавирин побочные эффекты
Актуальность. Проблема этиотропного лечения хронического вирусного гепатита С (ХВГС), несмотря на большое количество исследований, по-прежнему остается актуальной и до конца не решена.
Эффективность лечения по данным разных исследователей не превышает 46-51% у больных ХВГС с 1-м генотипом и 70-80% у больных ХВГС с не 1-м генотипом 2. Так же ограничивают их применение высокая стоимость препаратов и большое количество побочных эффектов от проводимой терапии. Целью проведения этиотропной терапии ХВГС является подавление вирусной репликации, эрадикация вируса из организма и, соответственно, прекращение инфекционного процесса. Даже отсутствие вирусологического эффекта при специфической терапии приводит к замедлению прогрессирования заболевания, стабилизации или регрессии патологических изменений в печени, предупреждению формирования цирроза печени и первичной гепатоцеллюлярной карциномы, а также повышению качества жизни.
Оценку эффективности специфического лечения осуществляют на основании нескольких критериев: вирусологического (исчезновение рибонуклеиновой кислоты (РНК) вируса из сыворотки крови), биохимического (стойкая нормализация уровня ферментов печени) и морфологического (уменьшение индекса гистологической активности и стадии фиброза).
В целом около 5% больных [1,5] вынуждены отказаться от специфического противовирусного лечения в начале курса из-за многочисленных побочных эффектов, а 20% не доводят его до конца.
Побочные эффекты интерферона (ИФН) и рибавирина иногда вынуждают временно или постоянно снижать их дозы или отменять препараты. Некоторыми исследователями [5] показано, что для достижения устойчивого вирусологического ответа (УВО) необходимо получение не менее 2/3 дозы ИФН и рибавирина, поэтому эффективность комбинированной противовирусной терапии (КПВТ) напрямую зависит от наличия побочных эффектов и возможностью их коррекции.
Некоторые побочные эффекты не требуют медикаментозной терапии, так как носят легкий или среднетяжелый характер, другие - тяжелый и угрожающий жизни характер, при этом необходима специфическая коррекция. Как правило, после окончания терапии большинство побочных эффектов полностью исчезает без применения симптоматической терапии.
Проблема побочных эффектов на фоне проводимой КПВТ остается до конца не изученной, несмотря на проведенные многочисленные исследования.
Основными побочными явлениями, описанными в литературе, являются: гематологические изменения; гриппоподобный, диспепсический, неврологический и астеновегетативный синдромы; аутоиммунные поражения; снижение массы тела; выпадение волос; огрубение кожи; аллергические реакции различной степени выраженности; местная реакция в области введения интерферонов.
Таким образом, проблема побочного действия комбинированного противовирусного лечения ХВГС, его влияние на достижение УВО является актуальной в настоящее время.
Целью данного исследования было изучение побочных явлений КПВТ в зависимости от схемы лечения, сопутствующих заболеваний, влияние на достижение УВО. Для достижения поставленной цели были сформулированы следующие задачи: оценить переносимость КПВТ пациентами с различными схемами терапии, выявить частоту побочных эффектов КПВТ и взаимосвязь их с достижением УВО.
Материалы и методы. В исследование были включены 50 пациентов с установленным диагнозом ХВГС, которые получали КПВТ. Диагноз был подтвержден согласно общепринятым методикам.
Из исследования исключались пациенты с микст-инфекцией (вирусный гепатит В, ВИЧ-инфекция) а так же наличием сопутствующей патологии печени (первичный билиарный цирроз, болезнь Вильсона-Коновалова, синдром Бадда-Киари, гемохроматоз, аутоиммунный гепатит, дефицит альфа-1 антитрипсина) и предшествующего специфического противовирусного лечения по поводу ХВГС, больные с наличием любого из общепринятых противопоказаний для проведения КПВТ.
Продолжительность лечения составила 48 недель для пациентов, инфицированных генотипом 1в вирусного гепатита С или при наличии у больного цирроза печени; 24 недели для пациентов, инфицированных генотипом 2 и 3а. Согласно рекомендациям по ведению пациентов с ХВГС, КПВП включала комбинацию стандартного (Интрон или Альтевир 3 млн МЕ 3 раза в неделю) или пегилированного (ПегИнтрон 120 мкг или Пегасис 180 мкг в неделю) ИФН и рибавирина в дозировке 800-1200 мг в зависимости от массы тела.
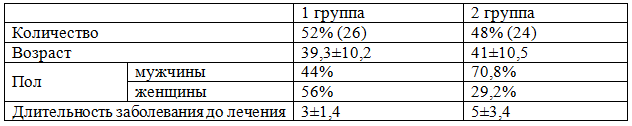
Устойчивый вирусологический ответ (УВО) определялся как отсутствие РНК вируса в сыворотке крови спустя 24 недели после окончания КПВТ. Больные находились под наблюдение в течение терапии на базе Воронежской областной клинической инфекционной больницы и поликлиник Воронежа. Все пациенты были разделены на 2 группы: получающие в составе КПВТ стандартные ИФН – 52,0% (26 человек) или пегилированные ИФН – 48,0% (24 человек). Пациенты были сопоставимы по возрасту и полу: средний возраст составил 40,3 ±10,4, количество мужчин - 57,1%, женщин 42,9%. Распределение по группам показано в табл. 1.
Таблица 1. Характеристика пациентов в исследуемых группах
При анализе полученных результатов использовались описательные методы математической статистики с применением пакета программ Microsoft Excel 2010. Достоверность различий оценивалась методами непараметрической статистики, статистически значимыми считались различия результатов при р≤0,05.
Результаты. При анализе эпидемиологических данных выяснено, что в большинстве случаев (34% случаев) ХВГС выявлен случайно, без клинических проявлений. Одинаковое количество пациентов (по 8 человек - 19,2%) обследовались по поводу диспепсических жалоб и длительного повышения печеночных ферментов. У 30 % пациентов в анамнезе отмечались неоднократные операции или переливание крови; употребление внутривенных наркотиков - у 16% человек. Длительность заболевания до начала противовирусной терапии составила в 1 группе 3±1,4 лет, во 2 группе 5±3,4лет. Степень фиброза по Metavir в среднем составил в 1 группе 1±0,85 балла, во второй группе выше - 1,9±1,5 баллов.
Соотношение генотипов вируса гепатита С, определенных до начала КПВТ, показано в табл. 2.
Таблица 2. Соотношение генотипов вирусного гепатита С
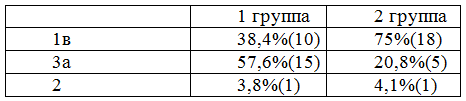
Среди всех пациентов УВО определялся в большинстве случаев - 80,0%, при применении обоих видов терапии, но при этом достоверных различий между группами по этому признаку не выявлено. Эффективность терапии в 1 группе составила 75,1%, во 2 группе - 78,2%. Отсутствие вирусологического ответа в половине случаев связано с отменой препаратов из-за развития выраженных побочных эффектов (прогрессирование неврологической симптоматики с развитием энцефалопатии в 1 группе, длительная некупируемая лихорадка во 2 группе).
Частота побочных эффектов в общей выборке была достаточно высокой - 72,3% среди всех пациентов, при этом в 1 и 2 группе нежелательные явления встречались с одинаковой частотой (69,1% и 73% соответственно).
На протяжении всей терапии у большинства пациентов встречался астеновегетативный синдром в виде выраженной слабости, усталости, нарушения сна, при этом значительно чаще эти проявления отмечали пациенты 2 группы - принимающие пегилированные ИФН (30,7%), что в 2,1 раза чаще, чем во 1 группе (66,6%). Снижение настроения, появление раздражительности, неконтролируемой агрессии при опросе отмечали 23,0% пациентов 1 группы и 25,0% пациентов 2 группы. Данные жалобы чаще встречались на 24±2 неделе терапии. Описанная в литературе депрессия, индуцированная КПВТ, среди данной выборки не встречалась. Для выявления депрессии у всех пациентов применялся опросник Цунга в начале и при завершении КПВТ.
Гриппоподобный синдром, проявляющийся лихорадкой до 38±0,85?С, миалгией, артралгией, выявлен достоверно чаще в у пациентов 1 группы (38,4%), чем у 2 группы (30,1%). Длительность лихорадки составляла в среднем 14±2 недель, первый подъем температуры всегда сопровождал начало КПВТ. Лихорадка купировалась применением препаратов НПВС в стандартных дозировках.
Жалобы со стороны желудочно-кишечного тракта в виде снижения аппетита, тошноты, периодической диареи, боли, вздутия в животе отмечались у 34,6% пациентов 1 группы, что в 2,08 раза чаще, чем во 2 группе (16,6%) .Желтуха на фоне КПВТ встречалась у 2 человек в каждой группе (по 8,3% и 7,6% соответственно).
Снижение веса в среднем на 10,5±5,1 кг, регистрируемое к концу КПВТ, встречалась в 2,3 раза чаще у пациентов 1 группы (19,2%) чем у пациентов среди пациентов 2 группы (8,3%).
Выпадение волос, жалобы на сухость кожи, зуд кожи регистрировались редко: в 1 группе у 2 человек (7,6%среди группы), во 2 группе чаще - у 3 человек(12,5%).
Обострение имеющихся сопутствующих соматических заболеваний встречались в обеих группах приблизительно с одинаковой частотой (30,1% и 27,6% соответственно). Чаще всего встречались обострения хронического панкреатита, язвенной болезни желудка, сахарного диабета.
Частота манифестации впервые выявленных соматических заболеваний на фоне проведения КПВТ имеет прямую корреляционную связь с используемыми препаратами, то есть значительно чаще выявляется при применении ИФН короткого действия, чем пролонгированных форм. При этом в 1 группе на фоне КПВТ манифестировали псориаз (7,6%), аутоиммунный тиреодит (15,3%). А во 2 группе выявлялись гипотиреоз и сахарный диабет (по 4,1% пациентов).
Гематологические осложнения встречались в обеих группах. Анемия, регистрируемая в виде снижения гемоглобина ниже 110г/л, встречалась чаще всего в середине терапии (24±3недели КПВТ). Во второй группе анемия выявлена достоверно чаще – в 2,4раза чаще (38,4%случаев), чем в 1 группе (16% случаев). Эритропоэтин для коррекции анемии применялся в 4 случаях (8%), у остальных коррекции анемии не требовалось.
Среди пациентов обеих групп при наличии анемии УВО встречается в 49,7% случаев, при отсутствии анемии достоверно реже (в 1,35 раз) - у 36,6% пациентов. Таким образом, наличие анемии, в сочетании с другими факторами можно считать предиктором эффективности КПВТ.
Напротив, частота тромбоцитопении на фоне КПВТ коррелировала с отсутствием УВО. Пациенты со снижением уровня тромбоцитов в 1,8 раз реже достигали УВО. Среди всех пациентов тромбоцитопения встречалась только у 8,0% пациентов, что реже, чем по литературным данным. В обеих группах частота данного побочного действия была одинаковой.
Выводы
1. Эффективность терапии с применением препаратов пегилированных или стандартных интерферонов оказалась сходной.
2. Гематологические нежелательные эффекты выявлены достоверно чаще при использовании пегилированных ИФН в составе противовирусной терапии.
3. Гриппоподобный на фоне КПВТ встречались достоверно чаще у пациентов, получающих стандартные ИФН.
4. Астеновегетативный синдром зарегистрирован чаще у пациентов на фоне терапии пегилированными ИФН.
5. Выявлена зависимость между достижением устойчивого вирусологического ответа и величиной снижения уровня гемоглобина.
Список использованных источников:
1. Беляева Н.М., Турьянов М.Х., Рабинович Э.З. Комбинированная терапия гепатита С рибавирином и альфа-интерфероном: Пособие для врачей. - М.: РМАПО. – 2002.
2. Громова Н.И. и Богомолов Б.П. Клиническая эффективность этиотропной терапии хронического вирусного гепатита С// Клин. мед. - 2003.-№1. - С.48.
3. Ивашкин В.Т. Комбинированное лечение хронического гепатита В// Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 1998. №5. С. 57-60.
4. Ferenci P., Fried M., Shiffman M. et al. Predicting sustained virological responses in chronic hepatitis C patients treated with peginterferon alfa-2a// J. Hepatol. – 2005. – Vol. 43. – P. 425–433.
5. Fried M.W. Side effects of therapy of hepatitis C and their management. Hepatology. 2002. - P.237-244
6. Князькина О.В., Каган Ю.Д., Скачков М.В. Микробиоценоз кишечника у больных хроническим вирусным гепатитом С и его лечение// Врач-аспирант, №3.4(52), 2012. – С.579-586.
7. Пирогова И.Ю., Пышкин С.А. Неинвазивная диагностика стадии фиброза у пациентов с хроническими гепатитами В и С// Врач-аспирант, №2(45), 2011. – С. 21-27.
8. Попов С.С., Попов С.Ф. Динамика биохимических показателей гепато-билиарной системы рабочих основных цехов металлургического завода, инфицированных вирусами гемоконтактных гепатитов В и С// Врач-аспирант, №6(55), 2012. – С.55-61.
9. Рихсиева Г.М. Особенности клинико-иммунологических показателей детей, больных острыми вирусными гепатитами А и В, родившихся от матерей, злоупотребляющих алкоголем// Врач-аспирант, №4.4(47), 2011. – С. 675-681.
10. Рюмин А.М., Корочкина О.В., Соболевская О.Л. Закономерности естественного течения хронического гепатита В// Врач-аспирант, №4.1(53), 2012. – С. 214-223.
Коррекция побочных эффектов противовирусной терапии при хроническом вирусном гепатите С
В статье освещен собственный опыт применения сочетанной противовирусной терапии у больного хроническим гепатитом С (препарата пегилированного интерферона альфа-2а (пегасис) в комбинации с рибавирином (копегус)). Представлена тактика ведения пациента с учетом негативных побочных реакций на терапию.
хронический гепатит С, противовирусная терапия, аутоиммунный тиреоидит.
Пациент В., 43 лет, наблюдался в клинике гастроэнтерологии Военно-медицинского клинического центра Центрального региона Министерства обороны Украины (г. Винница) с диагнозом хронического вирусного гепатита С (HCV-RNA полож., генотип 1b, виремия 1,4 х 10 6 копий/мл), минимальной степени активности.
Наличие хронического вирусного гепатита С выявлено случайно, при обследовании по поводу забора донорской крови (ноябрь 2005 г.). В анамнезе — множественные стоматологические процедуры. В январе 2006 г. при УЗИ зарегистрирована небольшая гепатомегалия, степень активности процесса минимальная (АЛТ в 2 раза выше нормы), другие биохимические показатели не изменены. Выполнена биопсия печени. По данным биопсии, дольковое строение сохранно. Портальные тракты расширены за счет фиброза и умеренной лимфомакрофагальной инфильтрации (в том числе с образованием лимфоидных фолликулов), проникающей в дольку с формированием лестничных очагов некроза. Отмечается умеренный склероз стенки желчного протока в одном из портальных трактов. Внутри долек — мелкие (до 3–5 клеток) некрозы с очаговой лимфомакрофагальной инфильтрацией, очаговая гипертрофия клеток стенок синусоидов, слабая очаговая гидропическая и мелкокапельная жировая дистрофия гепатоцитов. Больной в полном объеме обследован по программе подготовки к противовирусной терапии (ПВТ), ограничений и противопоказаний не выявлено.
В марте 2006 г. амбулаторно начато проведение ПВТ по стандартной комбинированной схеме: пегинтерферон альфа-2а в виде инъекции 1 раз в неделю и рибавирин 3 табл. 2 раза в день ежедневно (1200 мг/сут). Масса тела пациента 98 кг. При первой инъекции отмечено развитие гриппоподобного синдрома (лихорадка до 38,8 °С, головная боль, артралгия, миалгия). При последующих инъекциях реакция снизилась (субфебрильная лихорадка, периодическая головная боль). Подобные симптомы перестали беспокоить после 6-го введения препарата. В первые две недели лечения пациент отмечал тошноту и снижение аппетита, что расценено как побочное действие ПВТ. Эти проявления были выражены умеренно, прошли самостоятельно, без какой-либо коррекции терапии. Других клинически значимых отклонений в самочувствии пациента, а также лабораторно-инструментальных показателях не отмечалось. К 12-й неделе лечения зарегистрированы нормализация уровня аминотрансфераз и исчезновение HCV-RNA из крови.
К 18-й неделе терапии отмечено постепенное снижение уровня гемоглобина с исходных 142 г/л до 100 г/л, в связи с чем был назначен рекомбинантный эритропоэтин (рекормон) в дозе 100 МЕ/кг 3 раза в неделю п/к до момента стабильного увеличения уровня гемоглобина (до 120 г/л) на 22-й неделе лечения. Однократно на 46-й неделе терапии в связи с нейтропенией доза пегинтерферона альфа-2а была уменьшена до 135 мкг.
При подготовке пациента к ПВТ был определен тиреоидный статус: УЗИ щитовидной железы, оценка уровня гормонов Т3, Т4, тиреотропного гормона (ТТГ) и наличие антител к тиреопероксидазе (АТП). До начала лечения и через 12 недель проведения ПВТ все показатели находились в пределах нормы. Однако через 24 недели после начала лечения у пациента произошло повышение уровня АТП — 28,0 МЕ/мл (в 5 раз выше нормы). В связи с этим пациент был направлен на консультацию к эндокринологу. На УЗИ щитовидной железы отмечено незначительное увеличение размеров щитовидной железы, диффузное снижение ее эхогенности. Каких-либо клинических проявлений аутоиммунного тиреоидита выявлено не было. Принято решение о продолжении ПВТ с ежемесячным контролем тиреоидного статуса.
Общая продолжительность ПВТ составила 48 недель. Сопоставление данных морфологического исследования биоптата печени, полученного до и через 2 недели после окончания ПВТ, показало значительную положительную динамику. Отмечено уменьшение выраженности лимфомакрофагальной инфильтрации портальных трактов, исчезновение лимфоидных фолликулов и мелких фокусов внутридольковых некрозов. Степень фиброза портальных трактов осталась неизменной.
После окончания ПВТ при ежемесячном контроле уровень трансаминаз находился в пределах нормы, на 6, 12, 18 и 24-м месяцах HCV-RNA в крови не выявлялось.
При обсуждении приведенного случая необходимо подчеркнуть, что терапия хронической HCV-инфекции является одной из наиболее актуальных проблем современной медицины [1]. Сегодня в терапии хронических вирусных заболеваний печени используют комбинацию ИФН-α с аналогами нуклеозидов [2–6]. Основу ПВТ хронического вирусного гепатита С составляет интерферон-α (ИФН-α), обладающий противовирусным и иммуностимулирующим действием в сочетании с антифибротическим и противоопухолевым эффектом. Присоединение к молекуле ИФН-α крупной инертной молекулы полиэтиленгликоля позволило в значительной степени замедлить клиренс препарата из организма, обеспечивая постоянство его концентрации в крови на протяжении недели (пегилированный ИФН-α) и, как следствие, более значимые результаты современной ПВТ. Представителем аналогов нуклеозидов является рибавирин, который непосредственно влияет на жизненный цикл вирусов, а также обладает иммуномодулирующим действием. Эта комбинация и была использована в качестве ПВТ нашего больного.
В то же время ИФН-α и рибавирину свойственны многочисленные и дозозависимые побочные реакции, из-за которых 5 % больных отказываются от лечения в начале курса, а 20 % пациентов не доводят его до конца. Это необходимо учитывать при проведении ПВТ, предупреждая вследствие их возникновения плохую приверженность пациента к ПВТ (прерывание ее, снижение доз или полное прекращение лечения).
ИФН-α наиболее часто ассоциируется с гриппоподобным синдромом. В приведенном клиническом случае он наблюдался у пациента в первые 1,5 месяца. Как правило, такие проявления редуцируются в течение первого месяца ПВТ. На практике данный синдром адекватно корригируется достаточным приемом жидкости в день инъекции, рекомендовано введение пегасиса во второй половине дня, а также прием, в том числе превентивный, парацетамола (0,5–1 г через 5 часов после инъекции).
В результате антипролиферативного эффекта ИФН-α и образования антител к клеткам периферической крови развивается лейко- и тромбоцитопения, реже анемия. При развитии лейкопении под влиянием ИФН-α (при снижении гранулоцитов менее 500 клеток/мкл) препарат отменяют. Именно при мягкой нейтропении было показано кратковременное (недельное) снижение дозы пегинтерферона альфа-2а у нашего пациента.
О критической тромбоцитопении свидетельствует уровень тромбоцитов ниже 25 тыс/мкл. В то же время тромбоцитопения — наиболее частое поражение системы крови, наблюдающееся при HCV-инфекции, что связано с непосредственным ингибирующим эффектом вируса, реплицирующегося в клетках-предшественниках гемопоэза, на продукцию тромбоцитов в костном мозге. Наблюдающаяся при HCV-инфекции тромбоцитопения требует тщательной оценки (в первую очередь — исключения аутоиммунного механизма) и избирательного подхода к лечению. Данные литературы свидетельствуют о возможности положительного эффекта ПВТ в отношении тромбоцитопении при хроническом гепатите С при применении ее в качестве терапии выбора в случаях, резистентных к предшествующей кортикостероидной терапии [7]. В случаях тяжелой миелосупрессии при лечении ИФН-α возможно применение колониестимулирующих факторов (филграстим, молграстим).
Рибавирин вызывает доброкачественный гемолиз, который отмечают у 30 % больных. Отменять рибавирин следует, если уровень гемоглобина снижается до 85 г/л, при уровне 85–100 г/л дозу рибавирина уменьшают в 2 раза. У пациентов с заболеванием сердца препарат отменяют, когда концентрация гемоглобина составляет менее 120 г/л. При развитии анемии возможно применение рекомбинантного эритропоэтина, что позволяет избежать редукции дозы рибавирина у 80 % больных. Нашему больному в связи со значимым снижением уровня гемоглобина был назначен рекормон.
Прогнозирование таких побочных реакций возможно на основании известных факторов риска развития цитопении при ПВТ хронического вирусного гепатита С: наличие цирроза печени; исходный уровень гемоглобина у женщин ниже 120 г/л, у мужчин — ниже 130 г/л; снижение концентрации гемоглобина на 2-й неделе терапии более чем на 20 г/л; исходно низкий уровень тромбоцитов (менее 110 тыс/мкл); наличие гемолитической анемии или гемоглобинопатии в анамнезе; нарушение функции почек и др. Профилактика этих осложнений ПВТ заключается в назначении высоких доз витаминов Е и С из расчета 25–28 мг/кг/сут.
Одним из наименее освещенных в медицинской литературе остается вопрос о разнообразных аутоиммунных феноменах, возникающих на фоне ПВТ, из которых чаще других отмечают поражение щитовидной железы. По данным разных исследований, частота развития аутоиммунного тиреоидита при ПВТ составляет от 2,5 до 42 % [8]. Считают, что вирус гепатита С может играть роль одного из этиологических факторов аутоиммунного тиреоидита. Возможно, при хроническом течении вирусной инфекции С нередки его латентные формы, проявляющиеся под влиянием интерферонотерапии.
Наличие аутоиммунного тиреоидита с компенсированной функцией щитовидной железы не рассматривается в качестве абсолютного противопоказания к ПВТ. В то же время врач может ошибочно трактовать симптомы проявления хронического гепатита С и побочные эффекты ПВТ (слабость, утомляемость, сонливость и пр.) как клинические проявления гипотиреоза. Необходимо обратить внимание на то, что, кроме усиления выработки антител к щитовидной железе, ИФН-α имеет и прямой угнетающий эффект на синтез и секрецию тиреоидных гормонов.
К сожалению, на практике увеличение титров антитиреоидных антител и снижение уровня тиреоидных гормонов является частой причиной ошибочного прекращения ПВТ и длительного лечения у эндокринолога по поводу нарушений щитовидной железы.
Безусловно, пациентам, получающим ПВТ, необходимо постоянное врачебное наблюдение с проведением клинических и биохимических анализов крови, мочи, изучением спектра иммунных тестов, гормонов щитовидной железы (1 раз в 3 месяца, при патологии ежемесячно), выполнением УЗИ щитовидной железы (1 раз в 6 месяцев, при патологии — 1 раз в 3 месяца). При формировании гипофункции щитовидной железы (снижение уровня Т4 и повышение уровня ТТГ) обязательна консультация эндокринолога, ориентирующегося в специфике течения хронического вирусного гепатита С и особенностях ПВТ. Как продемонстрировано на клиническом примере, заместительная терапия L-тироксином позволяет стабилизировать состояние щитовидной железы и продолжить ПВТ. В последующем возможно титрование дозы L-тироксина.
В последнее десятилетие интенсивного изучения факторов эффективности ПВТ показано, что терапию необходимо проводить с доказанной длительностью и дозами препаратов для конкретного пациента. Важное условие при этом — следовать предписанной терапии, избегая необоснованных пропусков приема препаратов. Приведенный клинический случай показывает, что нужно вдумчиво оценивать изменения в состоянии пациента в ходе ПВТ. Кроме известных побочных действий ПВТ, приведенных в клиническом случае, обращаем внимание на ведение пациента при возникновении такого осложнения, как аутоиммунный тиреоидит. Своевременная коррекция побочных эффектов дает возможность увеличить число больных, получающих адекватные дозы препаратов, на протяжении всего лечения, и обеспечить оптимальный по продолжительности курс терапии. Это важно понимать, так как субоптимальные дозы препаратов и непродолжительное лечение способствуют появлению резистентных к ПВТ форм хронического вирусного гепатита С, что потребует проведения в последующем повторных курсов лечения.
1. Малый В.П., Звягинцева Т.Д., Титовский С.П. НСV-инфекция (острая и хроническая) клинико-патогенетические и терапевтические аспекты. — К., 2005. — 291 с.
2. Ferenci P. Peginterferon alfa-2a (40 kD) (Pegasys) for the treatment of patients with chronic hepatitis C // Int. J. Clin. Practice. — 2003. — Vol. 57, № 7. — P. 610-615.
3. Fried M.W., Hadziyannis S.J. Treatment of chronic hepatitis C infection with peginterferons plus ribavirin // Seminars in Liver Disease. — 2004. — Vol. 24 (Suppl. 2). — P. 47-54.
4. Keating G.M., Curran M.P. Peginterferon-α-2a (40 kD) Plus Ribavirin. A review of its Use in the Management of Chronic Hepatitis C // Drugs. — 2003. — 63(7). — P. 701-730.
5. Zeuzem S., Welsch C., Herrmann E. Pharmacokinetics of Peginterferons // Seminars in Liver Disease. — 2003. — Vol. 23 (Suppl. 1). — P. 23-28.
7. Игнатова Т.М. Лечение внепеченоч-ных проявлений хронической HCV-ин-фекции // Сучасна гастроентерологія. — 2006. — № 3(27). — С. 20-29.
8. Oppenheim Y., Ban Y., Tomer Y. Interferon induced autoimmune thyroid disease (AITD): a model for human autoimmunity // Autoimmun. Rev. — 2004. — 3. — Р. 388-393.
Показания для проведения противовирусной терапии
Принятие решения о целесообразности лечения пациента с ХГС должно быть индивидуализировано и основано на степени поражения печени, потенциальных рисках побочных эффектов, наличии сопутствующих заболеваний, вероятности успеха терапии и готовности больного начать ее.
Поскольку установить индивидуальный для пациента риск прогрессирования заболевания печени в настоящее время невозможно, то следует считать, что каждый больной ХГС с виремией является потенциальным кандидатом для проведения противовирусного лечения.
Для определения строгих показаний к нему сегодня используются результаты морфологического исследования печени:
- пациентам с отсутствием или минимальным фиброзом (Ishak 0–1, METAVIR 0–1) противовирусная терапия может быть отложена в связи с низким риском развития неблагоприятных исходов заболевания,
- строго показана она пациентам с мостовидным фиброзом или компенсированным циррозом при отсутствии противопоказаний к ее проведению.
Комбинированное противовирусное лечение
Целью противовирусной терапии является профилактика неблагоприятных исходов хронического гепатита С: цирроз печени (ЦП) и/или гепатоцеллюлярная карцинома (ГЦК).
В настоящее время для лечения ХГС используется сочетание препаратов интерферона и препаратов рибавирина. В России зарегистрированы
- пегилированные интерфероны (Пег-ИФН-α-2a - пегасис, α-2b - пегинтрон) и интерфероны короткого действия (ИФН-α-2a или α-2b) от различных производителей
- рибавирины различных производителей (под разными торговыми марками: ребетол, рибамидил, рибапег. )
Ключевыми факторами успеха терапии являются оптимальная доза препаратов и достаточная продолжительность лечения.
Доза пегинтрона определяется из расчета 1,5 мг на 1 кг массы тела/нед.
Доза рибавирина также зависит от массы тела:
- менее 65 кг – 800 мг/сут,
- 65–85 кг – 1000 мг/сут,
- 86–105 кг – 1200 мг/ сут,
- более 105 кг – 1400 мг/сут.
Доза пегасиса является фиксированной – 180 мкг/нед. При этом доза рибавирина составляет 1000 мг/сут для пациентов с массой тела до 75 кг и 1200 мг/сут при ее величине более 75 кг.
Оптимальная продолжительность лечения зависит от генотипа вируса гепатита С:
- при инфицировании 1-м генотипом она составляет 48 нед,
- при 2-м и 3-м – 24 нед.
- по 4-му и 6-му генотипам рекомендуется 48-недельный курс,
- по генотипу 5 информация недостаточна для формулировки лечебных рекомендаций
В России используется также комбинированная терапия ХГС стандартным интерфероном (3 млн МЕ 3 раза в неделю внутримышечно или подкожно) в сочетании с рибавирином (из расчета на массу тела, как указано выше), однако эффективность такой схемы лечения ниже, чем при применении комбинации пегилированного интерферона и рибавирина.
С целью повышения эффективности терапии применяют видоизмененные схемы лечения, с увеличением дозы простых интерферонов до 5-6 млн МЕ и/или более частым их использованием (через сутки или даже каждый день). Иногда такие схемы используют только до момента, когда РНК HCV перестает определяться в крови.
С 2011 года в стандартную терапию больных с первым генотипом HCV стали включать третий компонет - ингибитор протеазы вируса гепатита С. Подобная схема противовирусной терапии при клинических испытаниях показала значительное увеличение эффективности. Однако в России ингибиторы протеазы вируса гепатита С в настоящее время еще не прошли регистрацию.
Предикторы ответа на противовирусное лечение ХГС:
- генотип вируса не 1-й.
- вирусная нагрузка менее 600 000 МЕ/мл.
- пол женский.
- возраст моложе 40 лет.
- раса европейская.
- масса тела менее 75 кг.
- отсутствие резистентности к инсулину.
- повышенная активность трансаминаз.
- отсутствие выраженного фиброза или цирроза по данным морфологического исследования печени.
Общая частота побочных эффектов, по поводу которых лечение должно быть прекращено, составляет 10–14%. Наиболее распространены гриппоподобные симптомы (слабость, головная боль, подъем температуры тела) и психические нарушения (депрессия, раздражительность, бессонница), которые отмечаются у 22–31% пациентов.
Среди лабораторных изменений наиболее часто обнаруживается нейтропения (18–20%). При выраженном снижении количества нейтрофилов инфекционные осложнения крайне редки, поэтому применение гланулоцитарных колониестимулирующих факторов показано лишь в отдельных случаях.
При развитии психической симптоматики рекомендуется консультация психиатра.
Пегилированные интерфероны могут индуцировать развитие аутоиммунных заболеваний (аутоиммунный тиреоидит) или ухудшать течение предсуществовавших аутоиммунных расстройств.
Необходимо различать пациентов, у которых гепатит С протекает с признаками аутоиммунного гепатита (показано противовирусное лечение), и пациентов с первичным аутоиммунным гепатитом, на который наслоился гепатит С (показана иммуносупрессивная терапия).
Самым частым побочным эффектом рибавирина является гемолитическая анемия. Модификация дозы препарата требуется у 9–15% пациентов.
Эритроцитарные факторы роста (эритропоэтин) несколько улучшают самочувствие больных и уменьшают необходимость снижения дозы, но их благоприятное влияние на частоту достижения УВО доказано не было и безопасность окончательно не установлена. Использование их, хотя и редко, может сопровождаться тромбоэмболией, красноклеточной аплазией, прогрессированием ряда онкологических заболеваний и наступлением смертельного исхода.
На сегодняшний день применение факторов роста на фоне комбинированной ПВТ гепатита С не может быть рекомендовано к широкому практическому использованию.
Предпочтительным методом коррекции цитопений остается модификация дозы соответствующих препаратов.
Поскольку рибавирин выводится через почки, следует соблюдать осторожность при назначении его пациентам с почечной патологией.
Препарат обладает тератогенным действием, поэтому на протяжении лечения и в течение 6 мес после его завершения необходимо избегать наступления беременности; мужчинам, чьи партнерши беременны, лечение рибавирином также не проводится.
При возникновении серьезных нежелательных явлений или отклонений в лабораторных показателях во время применения монотерапии ПегИФН или комбинированной терапии Пег-ИФН и рибавирином дозу следует скорректировать или приостановить прием препаратов до прекращения нежелательных явлений (табл. 14 и 15).
Если после коррекции дозы переносимость терапии не улучшится, применение Пег-ИФН-a и/или рибавирина следует прекратить.
Возникновение серьезных аутоиммунных нарушений и депрессивных состояний требует индивидуального подхода в коррекции дозы ИФН и/или решения вопроса (коллегиального) о прекращении лечения.
Таблица 14 Коррекция схемы лечения при возникновении нежелательных явлений при монотерапии ХГС
Таблица 15 Коррекция схемы лечения при возникновении нежелательных явлений при комбинированной терапии ХГС
*Пациенты, которым сократили дозу рибавирина до 600 мг/день, должны принимать 1 капсулу утром и 2 капсулы вечером.
**ВПН – верхний предел нормальных значений.
Отбор пациентов на противовирусное лечение
При решении вопроса о противовирусном лечении конкретного больного необходимо учитывать соотношение потенциальной пользы и риска, связанного с терапией. Основные ориентиры, которые могут помочь в ее выборе, изложены в табл. 16.
Таблица 16 Критерии отбора пациентов для противовирусной терапии
Повторное лечение больных, не ответивших на противовирусную терапию
Определение тактики лечения больных в случае неэффективного курса противовирусной терапии в анамнезе требует учета ряда факторов. Это разнородная группа больных – среди них те,
- кто не ответил на лечение,
- у кого репликация вируса гепатита С возобновилась на фоне терапии,
- у кого после ее окончания развился рецидив гепатита.
Необходимо учитывать характер предшествовавшего лечения – стандартный или пегилированный ИФН, монотерапия или комбинация с рибавирином.
Повторная терапия пациентов, не ответивших на комбинированное лечение Пег-интерферонами и рибавирином, приводит к достижению УВО менее чем у 5% больных. Эффективность применения невысоких доз пегинтерферонов с антифибротической целью заключается в снижении некровоспалительной составляющей гепатита на фоне Пег-ИФН-α-2а (90 мкг/нед) при сохранении сопоставимых темпов и степени фиброзирования у больных, получавших и не получавших лечение.
Чаше всего рецидивы отмечаются в течение первых 12 нед после прекращения лечения.
Сведений об эффективности повторного лечения больных, у которых рецидив развился после курса комбинированной терапии Пег-интерфероном и рибавирином, нет.
Рекомендации в отношении больных, которые не ответили на терапию или у которых развился рецидив, сводятся к следующему:
Специальные группы больных
Рекомендации в отношении лиц, употребляющих наркотики, сводятся к следующему.
- Лечение этих больных проводится с учетом тяжести поражения печени и приверженности к терапии.
- Во время лечения целесообразно противовирусную терапию проводить с участием специалистов психиатрического профиля.
Рассматривать лечение у данной категории больных целесообразно только в случаях тяжелого поражения печени, всестороннего анализа рисков, связанных с усугублением основного психического заболевания, при наличии условий для постоянного психиатрического мониторинга в течение всего курса ПВТ.
Противопоказания к проведению противовирусной терапии
Противопоказания к рибавирину:
- гиперчувствительность к компонентам препарата.
- острые заболевания печени и почек.
- патология щитовидной железы.
- беременность, кормление грудью.
- тяжелые заболевания сердца.
- гемоглобинопатии.
- детский и юношеский возраст.
Мониторинг пациентов на фоне противовирусной терапии
Рекомендуемые диагностические тесты и кратность лабораторного и инструментального обследования больных хроническим гепатитом С, получающих противовирусное лечение, приведены в табл. 17.
Таблица 17 Тесты и кратность выполнения исследований у больных, получающих противовирусную терапию
Критерии ответа на противовирусное лечение
- Биохимические (нормализация активности трансаминаз)
- Вирусологические (исчезновение РНК HCV из крови)
- Гистологические (снижение некровоспалительной активности более чем на 2 балла при отсутствии нарастания фиброза)
Характеристика вирусологического ответа в зависимости от времени его наступления представлена в табл. 18.
Таблица 18 Критерии эффективности противовирусного лечения
Читайте также:


