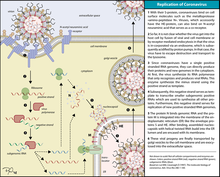
Этапы репликации в ядре у вируса гриппа
Репродукцией (лат. productio - производство) вирусов называют процесс размножения вирусных частиц в чувствительных к ним клетках.
В цикле репродукции тех и других вирусов различают четыре стадии: 1) подготовительную, или инициальную, включающую фазы адсорбции вируса на клетке, проникновения и раздевания в клетке; 2) собственно репродуктивную стадию образования структурных белков и вирионных нуклеиновых кислот; 3) сборку вирионов; 4) заключительную, сопровождающуюся выходом зрелых вирусных частиц из клетки.
Следующая за адсорбцией фаза проникновения вируса в цитоплазму клетки реализуется двумя способами - пассивным путем виропексиса или активным путем слияния (интеграции) вирусной оболочки с клеточной мембраной.

-
Более 80 курсов для обучения Всего 20 минут в день на занятия Персональный преподаватель
Виропексис представляет собой своеобразную форму эндоцитоза, при котором вирус проникает в клетку путем впячивания мембраны с образованием вокруг него вакуоли и поэтапным ее слиянием вначале с более крупной цитоплазматической вакуолью, а далее - с лизосомой или же с внутриклеточными мембранами, включая ядерную.
Второй, более редкий путь проникновения вирусов в клетку происходит посредством интеграции вирусных оболочек с наружной мембраной. Отмечается он лишь у тех видов вирусов, которые наделены белками слияния. Как и прикрепительные, белки слияния содержатся в капсидах простых и суперкапсидах сложных вирусов.
Способность к репродукции вирусы приобретают только после освобождения их нуклеиновых кислот от оболочек, что принято называть фазой раздевания (депротеинизации). Осуществляется раздевание вирусов ферментами поверхностных плазматических мембран клеток-хозяев при слиянии с ними вирусных оболочек, а при виропексисе - ферментами лизосом и внутриклеточных цитоплазматическйх и ядерных мембран.
Конечными продуктами раздевания у ряда вирусов являются, правда, не голые нуклеиновые кислоты, а НК, связанные с внутренним вирусным белком (пикорна-, аденовирусы), нуклеокапсидом (вирус гриппа) или сердцевиной (аденовирусы).
Собственно репродуктивная стадия. Истинно репродуктивная стадия, включающая фазы транскрипции, трансляции и репликации, у разных групп вирусов и семейств неодинакова.
Так, транскрипция, или переписывание нуклеиновых кислот вирусов на иРНК, как первый ее этап, у ДНК-содержащих семейств папова-, адено- и герпесвирусов, репродукция которых происходит в ядре, осуществляется клеточной РНК-полимеразой, а у репродуцирующихся в цитоплазме иридо- и поксвирусов — вирусоспецифической, попадающей в клетку вместе с их геномом.
Второй этап реализации генетической информации вирусов - трансляция, в процессе которой синтезируется их белок, начинается с узнавания клеточными рибосомами вирусных иРНК, чему способствуют особые вирусоспецифические инициаторные факторы.
В процессе трансляции у вирусов, кодирующих синтез одной длинной иРНК, синтезируется гигантский полипептид-предшественник, впоследствии нарезающийся на несколько различных белков, а у вирусов, кодирующих короткие иРНК, - соответствующее им число полностью созревших белков.
Репликация ДНК-содержащих вирусов, или копирование их генома, представленного линейной двухцепочечной структурой, сходна с репликацией ДНК клеток и осуществляется их ДНК-полимеразами. Другими словами, синтез гомологичных нуклеиновых кислот происходит на обеих расплетенных цепях, в результате чего каждый вновь образующийся вирион получает ДНК, состоящую из старой цепи и ее новой копии. Следует, правда, подчеркнуть, что раскручиванию кольцевых двухцепочечных ДНК предшествует разрезание одной из ее нитей, а репликация однонитчатых ДНК-содержащих парвовирусов происходит после синтеза второй цепи ДНК и образования промежуточных двухцепочечных его форм.
Репликация вирусных РНК тоже происходит не на родительских, а на промежуточных комплементарных нитях. При этом синтез тех и других нитей РНК, так же как иРНК, осуществляют не клеточные, а вирусоспецифические РНК-полимеразы. Процесс репликации комплементарных нитей РНК у минус-нитевых вирусов хотя и очень схож с процессом синтеза иРНК при транскрипции, но они не аналогичны друг другу. В отличие от относительно коротких иРНК, комплементарных отдельным участкам генома, комплементарно-репликативные РНК считываются с полного генома и по существу представляют собой антигеном. Следовательно, в инфицированных вирусами клетках существует механизм переключения частичного считывания генома (транскрипции) на сквозное (репликацию).
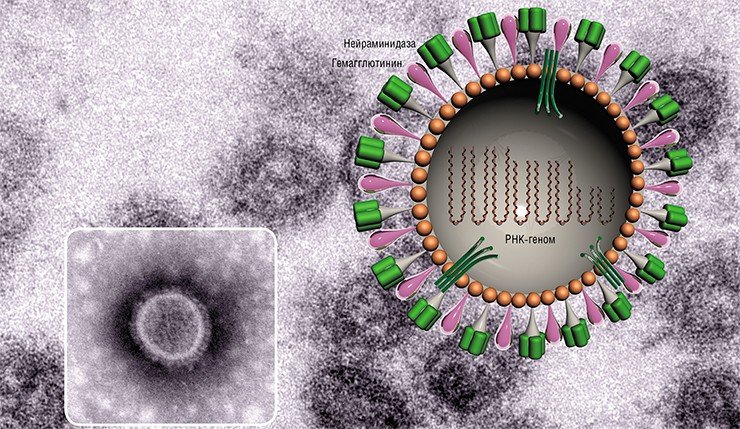
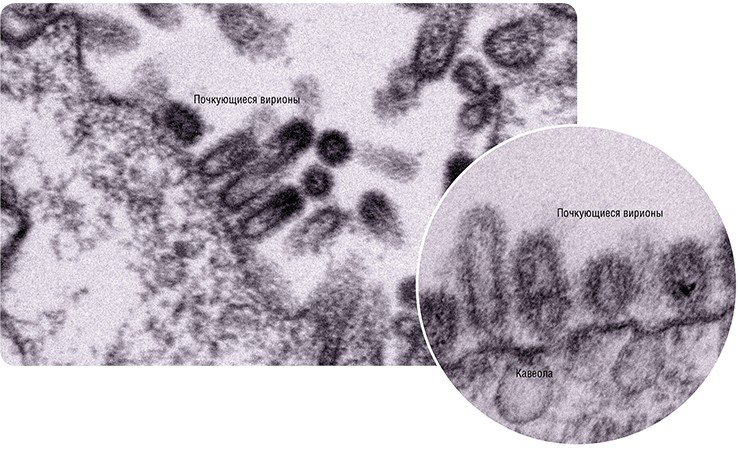
Внешне вирус гриппа выглядит как пузырек или вытянутая палочка. Под мембранной оболочкой скрывается необычный РНК-геном, состоящий из восьми отдельных частей. Поверхность щетинится шипиками, представляющими собой наружные части встроенных в мембрану белков – гемагглютинина и нейраминидазы. Именно молекулы этих двух гликопротеинов ответственны за связывание вирусной частицы с рецепторами клетки-хозяина.
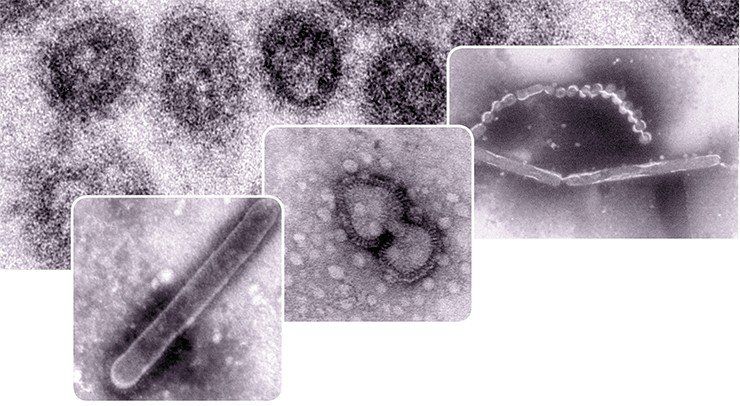
Опасные связи
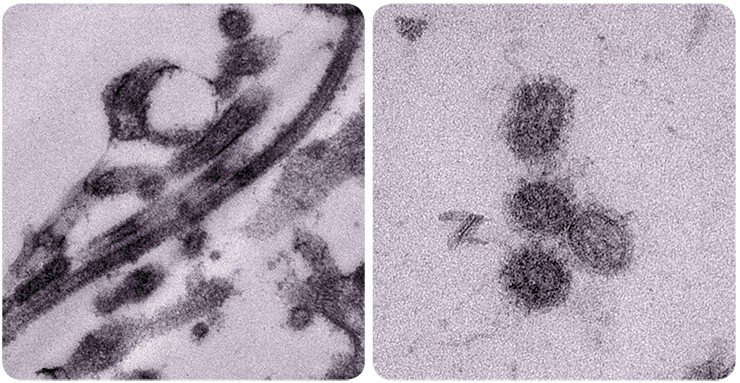
Добавим, что на стадии проникновения в клетку вирус гриппа использует еще и разные пути эндоцитоза, что повышает воздействие инфекции и позволяет с большей вероятностью избежать атаки иммунной системой.
Поэтому в ядре зараженной клетки на матрице вирусной (–)РНК сначала образуются две формы с положительной полярностью (+)РНК. Первая – комплементарная вирусная (+)РНК, которая впоследствии служит шаблонном для синтеза дочерней (–)РНК. Вторая – информационная вирусная (+)РНК, которая после сложной цепи превращений с участием клеточных ферментов транспортируется в цитоплазму клетки для будущего синтеза вирусных белков. Разумеется, все эти перемещения также обеспечиваются транспортными системами клетки.
Вот теперь все основные детали для конвейера по производству миллионов вирусных клонов готовы.
Клеточная фабрика
Готовые молекулы мембранных вирусных белков гемагглютинина и нейраминидазы объединяются и в таком виде транспортируются к внешней границе клетки специальными транспортными пузырьками, которые обеспечивают включение вирусных молекул в особые участки плазматической мембраны – липидные рафты (кавеолы).
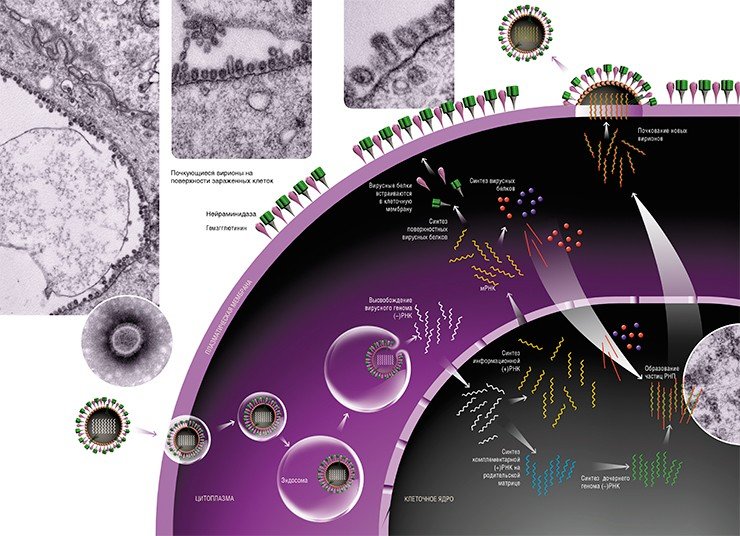
На сборочном конвейере
Наступает финальный этап вирусной репродукции – формирование новых вирионов. Для того чтобы это произошло, необходимо, чтобы вирусный геном – все восемь частиц РНП, а также остальные вирусные белки, встретились в строго определенном месте.
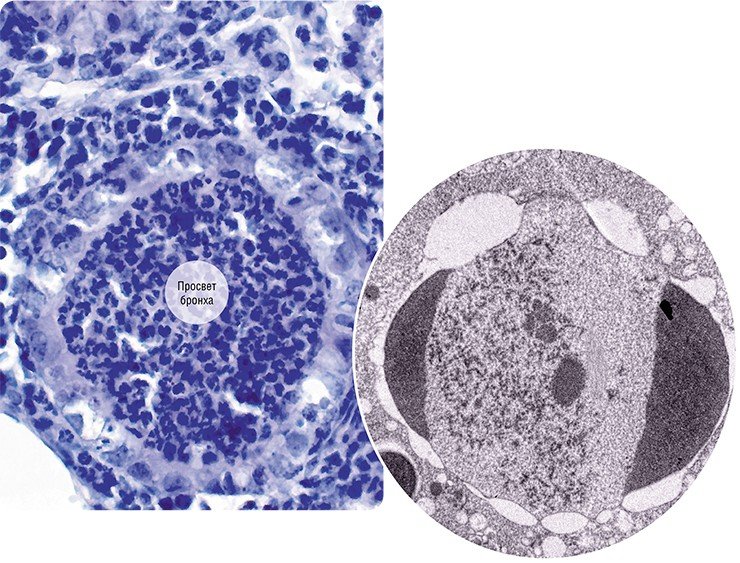
В организме вирусное потомство оказывается в слое слизи, покрывающей внутреннюю поверхность носоглотки, и человек, чихая и кашляя, распространяет вирус с капельками слизи. Клетки, естественно, пытаются защититься от агрессора, включая механизмы интерференции и апоптоза, однако эта защита, как правило, запаздывает, и паразит успевает размножиться и заразить новые клетки. Поэтому так важно применять препараты интерферона в первые сутки (а лучше – в первые часы заболевания), чтобы предотвратить массовое заражение клеток и остановить развитие заболевания.
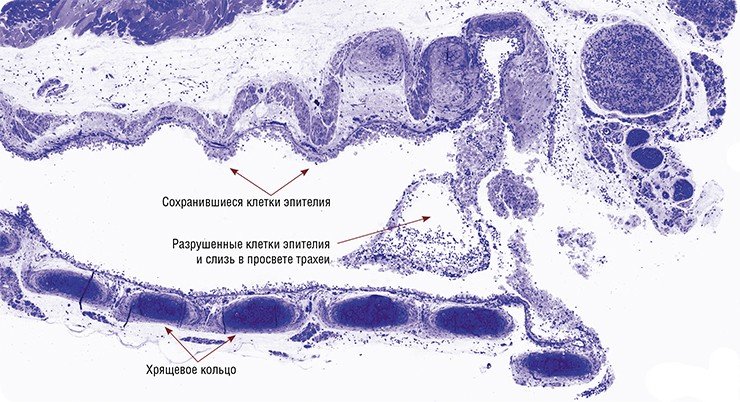
Нужна ли вакцинация против гриппа?
Познакомившись со сложным взаимодействием вируса гриппа с отдельной клеткой, поражаешься той виртуозности, с которой этот паразит эксплуатирует клеточные системы.
Если же перейти на уровень организма, то здесь взаимодействие вируса с хозяином определяется множеством дополнительных факторов, которые могут привести, а могут и не привести к заболеванию. Главный из этих факторов – реакция иммунной системы, и споры о том, надо ли стимулировать эту реакцию вакцинацией, не только не утихают, но становятся со временем все более острыми.
Compans R.W., Dimmock N.J. An electron microscopic study of single-cycle infection of chick embryo fibroblasts by influenza virus// Virology. 1969. V. 39. P. 499—515.
Harris A., Cardone G., Winkler D.C. et al. Influenza virus pleiomorphy characterized by cryoelectron tomography //PNAS. 2006. V. 103. P. 19123—19127.
Kim J.H., Skountzou I, Compans R, Jacob J. Original antigenic sin responses to influenza viruses// J. Immunol. 2009. V. 183. P. 294—301.
Leser G.P., Lamb R.A. Influenza virus assembly and budding in raft-derived microdomains: a quantitative analysis of the surface distribution of HA, NA and M2 proteins// Virology. 2005. V. 342. P. 215—227.
Matrosovich M., Matrosovich T., Uhlendorff J. et al. Avian-virus-like receptor specificity of the hemagglutinin impedes influenza virus replication in cultures of human airway epithelium// Virology. 2007. V. 361. P. 384—390.
Morris S.J., Nightingalea K., Smithb H. et al. Influenza A virus-induced apoptosis is a multifactorial process: Exploiting reverse genetics to elucidate the role of influenza A virus proteins in virus-induced apoptosis// Virology. 2005. V. 335. P. 198—211.
Noda T., Sagara H., Yen A. et al. Architecture of ribonucleoprotein complexes in influenza A virus particles// Nature. 2006. V. 439. P. 490—492.
В публикации использованы фотографии автора.
Автор выражает благодарность Ю. Спицыной и О. Таранову (ИХБФМ СО РАН) за помощь в обработке фотографий